Synthèse de points quantiques de carbone co-dopés en pyridinique N, S en tant qu'imitateurs d'enzymes efficaces
Résumé
Des points quantiques de carbone co-dopés N et S (N, S-CQD) avec des niveaux de dopage N et S élevés ont été synthétisés par pyrolyse micro-ondes en phase solide en 50 s. En raison de l'injection dominante de N pyridinique dans la structure conjuguée, une activité catalytique élevée d'enzyme imite et un rendement quantique de photoluminescence sont atteints simultanément.
Contexte
Les points quantiques de carbone (CQD) qui ont émergé comme un nouveau matériau de carbone de dimension zéro ont reçu une attention considérable en raison de leur stabilité chimique élevée, leur faible cytotoxicité et leur nature électronique et leurs comportements optiques uniques [1,2,3]. Avec des groupes de surfaces actives tels que -OH et -CO2 H, les CQD peuvent être recombinés avec d'autres substances organiques ou inorganiques pour diverses applications fantastiques, notamment la bio-imagerie [4, 5], les dispositifs optoélectroniques et les photocatalyseurs pour la dégradation de colorants organiques ou la production d'hydrogène à partir de la division de l'eau [6,7,8]. Très récemment, des résultats expérimentaux et théoriques ont confirmé que le dopage par hétéroatomes était une méthode efficace pour améliorer les propriétés électroniques et optiques des CQD [9, 10]. Parmi les nouveaux composites, les CQD dopés N ou les CQD co-dopés azote/soufre (N, S-CQD) ont démontré une efficacité quantique de fluorescence ou une activité photocatalytique beaucoup plus élevée que celle d'un composite vierge [11, 12]. De plus, l'amélioration des performances des CQD dopés N a montré une corrélation positive avec la quantité de dopage à l'azote [13, 14]. Bien que ces études certifient de manière convaincante que le dopage N influence de manière frappante les propriétés des CQD, cependant, il existe peu de rapports sur les méthodes efficaces d'hétéro-dopage pour les CQD. Souffrant de la haute solubilité du précurseur inorganique du dopant, les voies de carbonisation hydrothermale conventionnelles conduiraient à une grande quantité de dopants restant dans la solution réactionnelle et donc à une quantité de dopage N assez faible dans les CQD finaux.
Ici, nous avons rapporté la synthèse de points quantiques de carbone co-dopés N, S riches en azote (N, S-CQD) par approche assistée par micro-ondes en seulement 50 s. L'acide citrique (AC) a été choisi comme source de carbone et la thiourée a été utilisée non seulement comme source d'azote et de soufre, mais aussi comme base faible. La concentration d'azote et de soufre des N, S-CQD atteint 12,8 et 7,2 % en poids, respectivement, ce qui est environ cinq et trois fois plus élevé que celui rapporté pour les N-CQD et les CQD co-dopés N, S [11, 14].
Méthodes
Les N, S-CQD ont été obtenus de la manière suivante :le mélange de 0,42 g (2 mmol) d'acide citrique monohydraté et 0,46 g de (6 mmol) de thiourée a été placé dans un creuset en porcelaine et chauffé pendant 50 s dans un réacteur à micro-ondes (445 W). Le produit jaune brunâtre obtenu a été ajouté dans 30 ml d'eau déminéralisée pour former une suspension jaune et centrifugé à 9000 tr/min pendant 20 minutes. Ensuite, le surnageant a été purifié avec une membrane filtrante de 0,22 μm et dialysé avec de l'eau déminéralisée à travers une membrane de dialyse (poids moléculaire retenu, 1000 Da) pendant 24 h. Enfin, le dialysat a été encore lyophilisé sous vide. Les CQD vierges ont été synthétisés à partir d'acide citrique monohydraté pur, et le processus de traitement ultérieur était le même que celui des CQD N, S.
L'activité d'imitation enzymatique des N, S-CQD pour la décomposition de H2 O2 a été mesurée dans une solution tampon de 30 mL d'acide citrique et d'hydrogénophosphate disodique (pH ≈ 3,5, 35 °C) contenant 1 μg mL −1 de N, S-CQD et 8 × 10 −4 M de substrat tétraméthylbenzidine (TMB). Après 160 μL de H2 O2 (30 %) solution a été ajoutée à la solution tampon incolore, la réaction démarre puis prend la solution pour mesurer l'absorbance du produit d'oxydation bleu du TMB à 652 nm toutes les 2 min. Enfin, les vitesses de réaction d'oxydation du TMB ont été calculées. Le test de réutilisabilité des N, S-CQD a été effectué dans le système de réaction contenant 60 ml de solution tampon d'acide citrique-hydrogénophosphate disodique et 2 μg ml −1 de N, S-CQD ainsi que 5 × 10 −3 M de substrat TMB. La réaction a commencé par l'ajout de H2 O2 (0,3 %, 320 μL) dans la solution mélangée et a pris une petite quantité de solution pour mesurer l'absorbance à 652 nm après 1 h et le premier cycle était terminé. Ensuite, 320 μL de H2 frais O2 (0,3 %) de solution a été ajoutée au système réactionnel pour le cycle suivant. D'autres réactions à trois cycles ont été répétées dans les mêmes conditions. L'absorbance correspondante a été calculée en soustrayant la dernière absorbance.
Les images au microscope électronique à transmission (MET) et au microscope électronique à transmission haute résolution (HRTEM) ont été obtenues sur un microscope électronique JEM-2100 à haute tension (200 kV). La diffraction électronique à zone sélectionnée (SAED) a été mesurée par FEITF20 (microscopie électronique à transmission à émission de champ à haute résolution FEI) avec une condition de 200 kV. Les spectres d'absorption UV/vis ont été réalisés avec l'UV-3600 (Shimadzu UV-VIS-NIR Spectrophotometer). Les spectres de fluorescence ont été enregistrés sur F-7000 (Hitachi Fluorescence Spectrometer) avec la condition de 700 V. La durée de vie de fluorescence et FLQY ont été mesurées par le FM-4P-TCSPC (Horiba Jobin Yvon). Les longueurs d'onde d'excitation et d'émission sont respectivement de 358 et 436 nm. Les diffractomètres à rayons X sur poudre (XRD) ont été caractérisés par D8 Advance (Allemagne Bruker AXS Ltd.) en utilisant Cu Kα avec la condition de 40 kV et 40 mA. Les spectres infrarouges à transformée de Fourier (FT-IR) ont été réalisés avec Nicolet iS10 (Thermo Fisher Infrared Spectrometer). Le spectromètre de photoélectrons à rayons X (XPS) a été obtenu sur PHI 5000 Versa (UIVAC-PHI). La TG-MS (spectrométrie de masse thermogravimétrique) est mesurée par Netzsch STA 449C avec une vitesse de chauffe de 10 K min −1 de 35 °C jusqu'à une température finale de 450 °C sous le N2 débit d'air (10 %, air).
Résultats et discussions
On peut voir sur les images MET (Fig. 1a) que les N, S-CQD tels que préparés sont des nanofeuillets minces uniformes et bien dispersés avec une taille moyenne de 2,0 nm de diamètre. L'image HRTEM insérée (Fig. 1a) montre un espacement très net des franges du réseau de 0,24 nm cohérent avec la facette (1120) du graphène, indiquant les noyaux cristallins de N, S-CQD qui pourraient être composés de sp 2 atomes de carbone [15, 16]. L'image SAED insérée (Fig. 1b) montre que les N, S-CQD sont cristallins avec une frange de réseau de 0,312 nm correspondant aux N-CQD graphiques rapportés [13]. Ce d la valeur s'accorde bien avec l'espacement interplanaire des (002) facettes de diffraction des CQD codopants N, S avec une structure graphitique [11]. Le modèle XRD de N, S-CQD illustre un seul large pic centré à 2θ valeur d'environ 25,5° qui a été attribuée au pic de diffraction du graphène (Fig. 1c), correspondant à l'espacement intercouche de 0,33 nm [17]. Cependant, les g-CNQD et β-C3 N4 synthétisés par l'urée avec du citrate de sodium ou de l'acide citrique ont été rapportés [18, 19]. Différent de nos échantillons, les g-CNQD ont deux des pics caractéristiques à 27,4° et 13,1° dans le XRD. Le pic fort à 27,4° représente l'empilement interplanaire caractéristique des systèmes aromatiques, indexé pour le nitrure de carbone graphitique comme pic (002), et le pic de diffraction faible à 13,1° correspond à un motif de tassement structurel interplanaire indexé comme pic (100). Les g-CNQD ont été synthétisés avec un rapport molaire élevé (6:1) de précurseur N/C (urée sur citrate de sodium) [18]. De plus, plus de N injecté dans le noyau pour former des points de nitrure de carbone avec un temps de traitement thermique plus long atteint 60 min. Mais le temps de chauffage pour la pyrolyse micro-ondes en phase solide de notre échantillon N, S-CQD n'est que de 50 s. Différent de nos échantillons, le volume du mélange d'urée et de solution d'acide citrique est bouilli jusqu'à un point de 100 °C et on obtient du nitrure de carbone β nanocristallin. En conclusion, nous supposons qu'un faible rapport molaire du précurseur N/C, un temps de réaction court et une température relativement plus élevée peuvent conduire à une structure carbonée graphitique. Comparé à celui des CQD à dopage libre [20], le pic de diffraction (002) de notre échantillon N, S-CQD passe de 23° à un angle plus élevé de 25,5°, impliquant une diminution de l'espacement intercouche. Fortes interactions d'empilement électronique interplanaire entre les couches de type graphène de N, S-CQD. Possédant une électronégativité plus forte que l'atome de carbone, l'hétéro-dopage d'une grande quantité d'atomes d'azote et de soufre dans le cadre de carbone conjugué entraînerait une augmentation de la densité électronique de l'ensemble du cadre de carbone conjugué, et donc, la distance interplanaire raccourcie [21, 22 ].
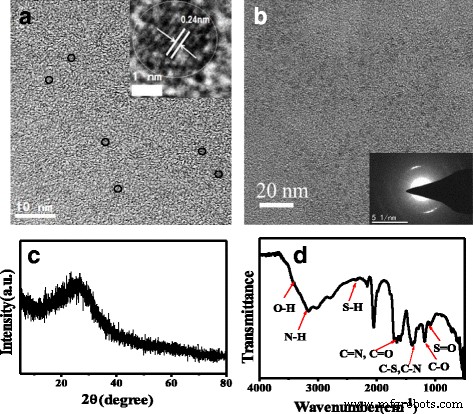
un Image TEM de N, S-CQD (l'insert est une image HRTEM). b Image SAED de N, S-CQD. c XRD et d Spectre FT-IR de N, S-CQD
Le spectre FT-IR (Fig. 1d) confirme divers groupes de surface de N, S-CQD. Les bandes à 3163cm −1 avec une épaule à 3416 cm −1 en 3000-3500 cm −1 représentent les vibrations d'étirement N-H et O-H, respectivement [11]. Ces groupements hydrophiles amino, hydroxyle considérables pourraient permettre aux N, S-CQD une hydrophilie supérieure [23]. Les triples pics qui apparaissent vers 1582, 1656 et 1704 cm −1 peuvent être attribués aux différentes liaisons vibratoires caractéristiques, respectivement. Les pics à environ 1704 cm −1 sont les vibrations d'étirement des groupes carboxyliques C=O et des liaisons C=N [24], et les deux autres pics à 1656 et 1582 cm −1 sont la vibration caractéristique des groupes amide étirant C=O (amide I) et la flexion dans le plan de la liaison N-H (amide II) [24, 25]. Les pics à 1405 et 1345 cm −1 peut être attribué à la vibration de C–S et C–N, respectivement [17], tandis que les bandes à 1177 et 1084 cm −1 confirment en outre l'existence de liaisons C–O et S=O sur les N, S-CQD [17, 23]. Le spectre d'absorption UV/vis des N, S-CQD représente deux bandes d'absorption claires (Fig. 2a). La forte bande d'absorption à 234 nm est attribuée à la transition électronique π-π* du système conjugué aromatique sp 2 domaines [17], tandis que le faible pic d'absorption à 340 nm est attribué à la transition n-π* de la liaison C=O [26]. Il a été remarqué que l'intensité relative du pic d'absorption à 234 nm est beaucoup plus forte que celle des échantillons de N, S-CQD synthétisés par méthode hydrothermale [17, 26], suggérant la formation de sp plus aromatiques 2 domaines avec un dopage N dans le système de noyau conjugué comme N pyridinique. En outre, un large épaulement à environ 430 nm chevauché par le pic à 340 nm provient de nombreux types de transitions d'état de surface [26].
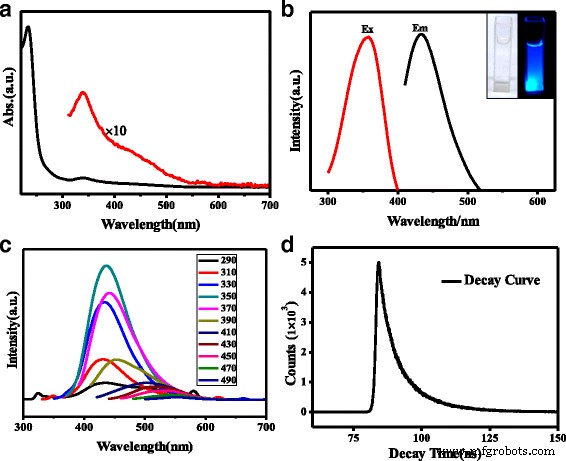
un L'UV/vis de N, S-CQD. b Le PL de N, S-CQD et l'encart est les images de N, S-CQD sous lumière ambiante et irradiation 365 nm. c Les spectres PL de N, S-CQD avec différentes longueurs d'onde d'excitation. d Courbes de décroissance de l'intensité de la photoluminescence à la lumière d'excitation de 358 nm
Les spectres de photoluminescence (PL) (Fig. 2b) illustrent que les N, S-CQD ont une large distribution d'excitations. La longueur d'onde d'excitation maximale est à 358 (longueur d'onde d'émission 436 nm) en raison du pic d'absorption de 340 nm. On peut voir à partir de l'image en médaillon de la figure 2b que la solution aqueuse incolore et transparente de N, S-CQD devient bleu vif sous une irradiation UV de 365 nm. La solution de N, S-CQD est restée limpide pendant 10 mois sans précipitations ; cette grande stabilité des particules de N, S-CQD est attribuée à leur taille très petite et uniforme ainsi qu'aux groupes hydrophiles à la surface.
Le rendement quantique de photoluminescence (PLQY) des N,S-CQD est calculé comme étant de 23,6% sous excitation à 358 nm, ce qui est trois fois supérieur à celui rapporté pour les N,S-CQD ou N,S-CQD [20, 23]. En revanche, le PLQY des CQD vierges n'est que de 1,15 %, ce qui est bien inférieur à celui des N, S-CQD. Il a été rapporté que le PLQY des CQD était lié à la quantité de dopage N dans les CQD [17, 27], et ainsi, de nombreux travaux ont tenté d'augmenter la quantité de dopage N dans les CQD en prolongeant le temps de réaction même jusqu'à 19 h ou en augmentant la température de réaction à 260 °C [11, 23]. Cependant, la quantité de dopage N dans les échantillons solides finaux était encore inférieure à 6 %. Dans notre travail, un niveau de dopage N élevé de 12,5% est atteint sur les N, S-CQD par une voie efficace assistée par micro-ondes en phase solide, dans laquelle les molécules d'acide citrique et de thiourée réagissent rapidement et évitent la sublimation. De plus, la thiourée agit comme une base faible pour accélérer la vitesse de polymérisation. Curieusement, en changeant le rapport de thiourée et CA de 3:1 à 1:3 et 1:1, le PLQY de N, S-CQD a été légèrement réduit à 7 et 2,1 %, respectivement. De plus, l'augmentation du temps de réaction jusqu'à 2 min a simplement obtenu le carbone en vrac. Pour clarifier davantage le mécanisme de réaction, nous avons acquis l'analyseur thermique thermogravimétrique différentiel (TG-DTA) et les courbes de masse TG de CA pur et le mélange de réactifs de CA et de thiourée. Comme le montre la figure 3a, trois pics exothermiques peuvent être observés dans les courbes TG-DTA de l'AC pur ; le premier pic correspond à l'eau absorbante dont l'eau cristalline. Le deuxième pic pointu à 154 °C est attribué au dégagement de chaleur de fusion du cristallin CA, et le large, centré à 214 °C, concerne la déshydratation et la carbonisation intermoléculaires. Alors que pour le mélange de CA et de thiourée, de nombreux changements sur ces deux derniers pics exothermiques peuvent être observés sur le spectre TG-DTA (Fig. 3b), le deuxième pic exothermique apparaît à une basse température de 118 °C, indiquant que l'acide -l'interaction des bases entre le CA et la thiourée entraîne une chute spectaculaire de 36 °C dans l'étape de libération de chaleur de fusion. De plus, le troisième pic exothermique qui correspond à la déshydratation et à la carbonisation dérive deux pics à 214 et 236 °C, et un faible pic à 170 °C peut être observé, ce qui implique que l'ajout de thiourée peut faire avancer le processus de déshydratation et de carbonisation. . En comparant les spectres de masse TG du CA pur et du mélange de CA et de thiourée (Fig. 3c), on peut trouver que la température maximale de H2 Le pic de libération d'O diminue de 215 °C pour le CA pur à 180 °C pour le mélange de CA et de thiourée. De même, le maximum de CO2 le pic de libération est à 227 °C pour le CA, mais il passe à basse température et devient une libération en deux étapes à 179 et 198 °C pour le mélange réactif de CA et de thiourée, respectivement. Cette diminution de température dans la déshydratation et la carbonisation est bien en accord avec les résultats du TG-DTA, impliquant une approche réactionnelle différente pour ces deux systèmes. Pour le CA pur, la déshydratation et la carbonisation intermoléculaires se produisent simultanément à haute température. Alors que pour le mélange de CA et de thiourée, la déshydratation intermoléculaire réagit d'abord entre les groupes carboxyle de CA et les groupes aminés de thiourée, puis, la carbonisation par étapes se produit pour former le noyau carboné des N, S-CQD. Par rapport à la faible interaction de liaison hydrogène entre les molécules CA, une forte interaction acide-base entre les groupes carboxyle et les groupes amino entraîne une diminution significative de la température de déshydratation. Curieusement, comme le montre la figure 3c, la masse résiduelle pour le CA pur et le réactif mixte de CA et de thiourée sont respectivement de 1 et 21% en poids, ce qui indique que la thiourée ajoutée peut jouer un rôle de base faible pour abaisser la température de réaction et éviter la sublimation, améliore ainsi la teneur en dopage N et S des N, S-CQD avec un rendement élevé.
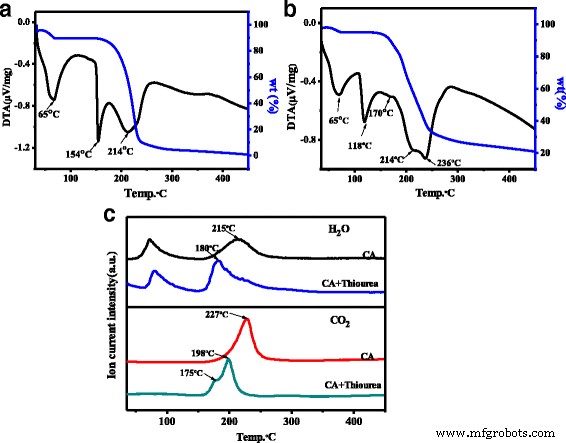
Courbes TG et DTA de a acide citrique pur, b mélange réactif d'acide citrique et de thiourée. c Courbes TG-Mass de CA pur et mélange de réactifs d'acide citrique et de thiourée
La figure 2c illustre les spectres d'émission de N, S-CQD avec différentes longueurs d'onde d'excitation. Lorsque la longueur d'onde d'excitation passe de 290 à 370 nm, les pics d'émission à 440 nm ne présentent pratiquement aucun décalage. Les composants d'émission sont assez constants en énergie et proviennent très probablement de l'absorption de la transition n-π* à 340 nm. La propriété d'émission indépendante de l'excitation des CQD a été étudiée en ajustant les pics d'émission complexes à plusieurs fonctions gaussiennes et en a déduit une conclusion similaire [26]. Alors que lorsque la longueur d'onde d'excitation varie de 390 à 490 nm, le spectre d'émission PL présente un décalage vers le rouge lorsque la longueur d'onde d'excitation augmente, caractérisant une propriété dépendante de la longueur d'onde d'excitation. Cela peut être attribué à divers états de surface de C =O ou au rôle du groupe amide en tant que centres de piégeage d'excitons discrets pour affecter l'énergie d'émission dans le processus PL [11, 19, 28]. La polydispersité et l'hétérogénéité de surface sont à l'origine du comportement PL dépendant de la longueur d'onde d'excitation [28, 29]. Le large pic d'absorption à environ 430 nm est un ensemble de divers états de surface, y compris le carboxyle et l'amide, qui permet un comportement PL dépendant de la longueur d'onde d'excitation des N, S-CQD. La durée de vie de fluorescence des N, S-CQD a été déterminée pour évaluer sa propriété optique (Fig. 2d). Les courbes de décroissance PL de l'échantillon N, S-CQD peuvent être ajustées par une formule double exponentielle, où τ 1 est de 3,48 ns, τ 2 est de 11,05 ns et la durée de vie moyenne est de 6,72 ns. Par rapport à la durée de vie moyenne de 2,42 ns des CQD vierges [30], des durées de vie de fluorescence plus longues des deux τ 1 et τ 2 ont été obtenus sur notre échantillon. Il a été rapporté que le τ 2 la proportion et la durée de vie moyenne s'allongent avec l'augmentation de la quantité de dopage N et ont conclu que plus τ 2 découlent des états de surface [11, 31].
La formation de N, S-CQD a été corroborée par XPS. Comme le montre la figure 4a, cinq pics distincts à 530, 399, 284, 222 et 164 eV présentent O 1s , N 1s , C 1s, S 2s et S 2p des signaux, respectivement, indiquant N et S ont bien été injectés dans le cadre des CQD [17]. C 1s haute résolution Le spectre XPS (Fig. 4b) indique trois caractéristiques de la structure C, y compris le sp aromatique conjugué 2 C (C=C) à 284,4 eV, sp 3 C (C–N, C–O, C–S) à 285,6 eV et C=O/C=N à 288,1 eV [11]. Les N 1s Le spectre XPS (Fig. 4c) des N, S-CQD montre trois pics à 399,5, 400,3 et 401,0 eV, qui représentent respectivement le N pyridinique, le N pyrrolique et le N amidique [17, 24]. Dans le g-CNQD, le rapport atomique Ncore/Ccore, tel que dérivé du rapport d'intensité XPS expérimental, est égal à 1,40, ce qui est proche de la valeur attendue de 1,33 attendue pour un C3 N4 [19]. Nous avons effectué une analyse de données similaire de notre échantillon, en prenant 285,6 eV de C 1s pic en tant que "Ccore" tandis que 400,3 eV (pyrrolique) et 399,6 eV (pyridinique) de N 1s comme "Ncore" (car les valeurs d'énergie de liaison sont similaires avec 399,9 eV de NCore dans le [19]), et le Ncore/Ccore calculé est de 0,43, bien inférieur à 1,33 pour C3 N4 . De plus, le rapport relatif du N pyridinique au N pyrrolique dans nos N, S-CQD s'est avéré très différent de celui des CQD co-dopés N- ou N, S synthétisés par méthode hydrothermale [17, 21]. Le N pyridinique est le dopant dominant dans notre échantillon de N, S-CQD, qui est 1,5 fois supérieur au N pyrrolique, mais il est généralement inférieur à 1,0 pour de nombreux échantillons synthétisés thermiquement. Un N pyridinique aussi élevé peut conférer une propriété supérieure aux N, S-CQD pour une application catalytique ultérieure, car ils peuvent agir comme des sites actifs catalytiques [32]. De plus, le N pyrrolique sur le bord est une composition importante de défauts de surface et peut agir comme centre de photoluminescence [17, 27]. Le S 2p Le spectre XPS (Fig. 4d) affiche deux signaux typiques à 163,3 et 164,4 eV, qui correspondent à S 2p 3/2 et S 2p 1/2 de thiophénique S, respectivement [16]. En combinant le spectre FT-IR, nous supposons que les atomes de soufre se dopent avec succès dans le cadre des N, S-CQD en tant que S thiophénique et existent au bord des N, S-CQD pour améliorer leur PLQY.
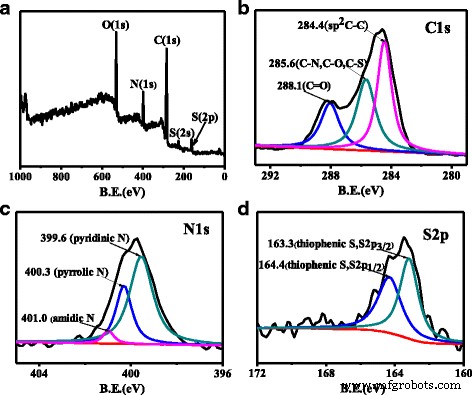
un L'analyse complète XPS de N, S-CQD. Le XPS haute résolution de C 1s b N 1s c et d S 2p spectres de N, S-CQDs
La catalyse enzymatique est attendue en raison de sa spécificité et de son activité élevées. La peroxydase de raifort (HRP) est l'enzyme végétale la plus étudiée qui contient le centre actif du cycle de la porphyrine dans le groupe hème pour catalyser efficacement l'oxydation à un électron, une grande variété de substrats organiques et inorganiques par le peroxyde d'hydrogène [33, 34]. Les propriétés d'imitation des N,S-CQD riches en pyridinique ont été testées pour l'oxydation des substrats de peroxydase de la 3, 3′, 5′, 5′-tétraméthylbenzidine (TMB) en présence de H2 O2 en mesurant l'absorption du produit d'oxydation bleu du TMB à 652 nm. L'absorption UV/vis des N, S-CQD culmine à 234 et 340 nm. La figure 5a illustre les lignes d'ajustement de la concentration de produits d'oxydation dérivés du TMB (μmol/L) en fonction du temps en présence de N, S-CQD et de CQD vierges. La vitesse de réaction (r ) pour la décomposition de H2 O2 sur N, S-CQDs comme imitateurs d'enzymes est de 2,16 × 10 −3 mol −1 L −1 S −1 , qui est deux fois plus élevé que celui des CQD vierges et des CQD non dopés précédemment rapportés dans les mêmes conditions [35, 36]. L'excellente activité des N, S-CQD riches en pyridinique peut être attribuée à la teneur élevée en dopage de N qui possède une grande électronégativité que l'atome de carbone pour augmenter la densité électronique des N, S-CQD et, en particulier, le N pyridinique dominant possédant un seule paire d'électrons qui conduit à l'amélioration de la densité électronique et de la mobilité dans la structure π-conjuguée des N, S-CQD, accélère ainsi la réaction. Il s'agit du premier rapport sur l'amélioration spectaculaire de la propriété d'imitation de la catalase de la dépendance des CQD au dopage dominant du N pyridinique dans la charpente du carbone.
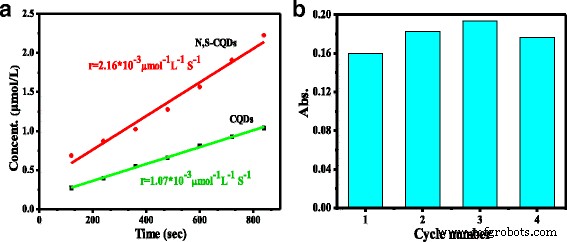
un La vitesse de réaction initiale des N, S-CQD et des CQD dopés libres. b Test de réutilisabilité des N, S-CQD
La réutilisation des N, S-CQD a été étudiée par quatre utilisations consécutives pour une réaction imitant la catalase (Fig. 5b). Sur l'utilisation de quatre cycles, aucune diminution évidente de l'activité de N, S-CQD n'a été observée. La stabilité élevée de l'activité de catalyse intrinsèque des N, S-CQD est attribuée au dopage N pyridinique dominant dans la structure C =C, car le N pyridinique peut jouer un rôle en tant que sites catalytiques efficaces pour imiter les enzymes pour H2 O2 décomposition.
Conclusions
En résumé, nous avons synthétisé un N, S-CQD riche en pyridinique avec un niveau de dopage N et S élevé par une méthode de polymérisation solide par micro-ondes en seulement 50 s. La thiourée joue non seulement le rôle de source de S mais également de base faible pour accélérer la déshydratation intermoléculaire à basse température et la carbonisation en plusieurs étapes, ce qui permet au niveau élevé de dopage N et S des N, S-CQD et N pyridinique dominant d'injecter dans le conjugué car les sites actifs imitent l'enzyme. Notre travail fournit une méthode efficace pour synthétiser des N, S-CQD riches en pyridinique possédant à la fois une activité PLQY élevée et une activité d'imitation d'enzyme.
Nanomatériaux
- Synthèse d'ADN
- Composites de graphène quantique/TiO2 co-dopé S, N pour une génération d'hydrogène photocatalytique efficace
- Points de carbone bleu luminescent à haute efficacité indépendants de l'excitation
- Synthèse de points quantiques de type II/Type-I à suppression de réabsorption ZnSe/CdS/ZnS Core/Shell et leur application pour le dosage immunosorbant
- Points quantiques de bismuth dans des puits quantiques recuits GaAsBi/AlAs
- Synthèse verte de points quantiques InP/ZnS Core/Shell pour une application dans des diodes électroluminescentes sans métaux lourds
- Microsphères de carbone magnétique comme adsorbant réutilisable pour l'élimination des sulfamides de l'eau
- Une approche simple pour la synthèse de points quantiques de carbone fluorescent à partir d'eaux usées de tofu
- Synthèse de points quantiques de sulfure d'antimoine solubles dans l'eau et de leurs propriétés photoélectriques



