Synthèse de points quantiques de type II/Type-I à suppression de réabsorption ZnSe/CdS/ZnS Core/Shell et leur application pour le dosage immunosorbant
Résumé
Nous rapportons une méthode à un seul pot sans phosphine pour synthétiser des points quantiques (QD) core-shell ZnSe/CdS/ZnS avec des structures composites de type II/type I et des propriétés de suppression de réabsorption conséquentes. Les QD tels que synthétisés possèdent une émission rouge hautement efficace (avec un rendement quantique de 82 %) et une stabilité optique élevée. Par rapport aux QD de type I, les QD ZnSe/CdS/ZnS présentent un décalage de Stokes plus important et une réabsorption plus faible, ce qui peut réduire la perte d'émission et améliorer le niveau de sortie de fluorescence. Les QD ZnSe/CdS/ZnS sont utilisés comme marqueurs fluorescents pour exploiter pour la première fois leur application dans le test d'immunoabsorption par fluorescence (FLISA) dans la détection de la protéine C-réactive (CRP) avec une limite de détection (LOD) de 0,85 ng/mL, qui est plus sensible que celle de la FLISA basée sur les QD CdSe/ZnS de type I (1,00 ng/mL). Les résultats indiquent que les QD ZnSe/CdS/ZnS de type II/type I peuvent être de bons candidats pour des applications dans la détection d'informations biomédicales.
Contexte
Les points quantiques (QD) à semi-conducteurs à noyau/coque fluorescents se caractérisent par d'excellentes propriétés optiques telles qu'une plage d'émission plus large, des rendements quantiques de photoluminescence (PL) plus élevés (QY) et une stabilité optique et chimique plus élevée que les colorants organiques traditionnels. Ces avantages ouvrent des opportunités pour des avancées révolutionnaires dans les marqueurs fluorescents pour le diagnostic biomédical, l'imagerie moléculaire et le champ photoélectrique [1,2,3,4,5,6,7]. Selon l'alignement des bandes entre les matériaux du noyau et de l'enveloppe, les QD noyau/enveloppe peuvent être classés en structures de type I, de type I inversé et de type II. QD de type I caractérisés par la structure d'alignement de bande « nichée », qui peut confiner à la fois les électrons et les trous dans la région du noyau pour améliorer la recombinaison radiative et séparer physiquement la surface du noyau actif optique de son milieu environnant, et ainsi améliorer l'intensité PL et stabilité optique [6,7,8,9]. Malgré ces propriétés favorables, un petit décalage de Stokes (seulement une dizaine de nanomètres), appelé différence entre les spectres d'absorption et PL, génère une réabsorption importante, conduisant à une perte globale d'émission et limitant leur application en détermination quantitative [10, 11]. En revanche, les QD de type II avec un alignement de bande interdite en quinconce favorisent la séparation spatiale des électrons et des trous dans différentes régions de la structure noyau/enveloppe. L'énergie de transition de recombinaison e–h de bord de bande subséquente est plus petite que la bande interdite de l'un ou l'autre des composants matériels constitutifs, conduisant à une émission décalée vers le rouge significative, qui n'est pas disponible avec l'un ou l'autre des matériaux monocomposants. La force de l'oscillateur de la première caractéristique d'absorption d'excitons des QD de type II diminue considérablement par rapport à celle des QD de base [12, 13]. L'émission largement décalée vers le rouge et le pic d'absorption du premier exciton aplati réduisent tous deux le chevauchement des spectres d'absorption et d'émission, ce qui supprime la réabsorption, et profite à la détection quantitative biologique. Les QD ZnSe/CdS typiques de type II ont une émission réglable du violet bleuâtre au rouge et une réabsorption supprimée [13]. Cependant, les électrons délocalisés dans la coque CdS sont vulnérables au piégeage des défauts de surface ou du milieu environnant, ce qui entraîne un faible rendement quantique de fluorescence. Une solution réalisable consiste à revêtir les QD de ZnSe/CdS avec la coque la plus externe en ZnS non seulement pour passiver la surface afin d'augmenter le rendement quantique et la stabilité optique, mais également pour restreindre la fuite d'élément Cd toxique, réduisant ainsi la biotoxicité. Jusqu'à présent, la majorité des recherches se sont concentrées sur les QD de type I, et seules quelques-unes ont été menées sur les QD de ZnSe/CdS/ZnS de type II/type I [12,13,14,15]. De plus, toutes les études sur le processus de synthèse des QD de ZnSe/CdS/ZnS ont utilisé une préparation en deux étapes en pré-purifiant les QD de noyau de ZnSe brut et ont utilisé des phosphines toxiques et coûteuses. De plus, aucun d'entre eux n'impliquait l'application de QD ZnSe/CdS/ZnS dans la détection biologique.
Ici, nous rapportons une méthode à un pot sans phosphine pour synthétiser des QDs de haute qualité à émission rouge ZnSe/CdS/ZnS type II/type-I core/shell avec la fonction de réabsorption-suppression et la première utilisation des QD pour fabriquer un test d'immunosorption lié à la fluorescence (FLISA). Nous avons utilisé un précurseur de Se hautement réactif et faiblement toxique (ODE-Se) et de l'oléate de zinc pour synthétiser des QD de noyau de ZnSe de haute qualité, puis nous avons obtenu une croissance multicouche sans purification des points quantiques du noyau. Cela est très prometteur pour la synthèse à grande échelle de points quantiques cœur/coquille. Le rendement quantique des QD ZnSe/CdS/ZnS de type II/type I à émission rouge tels que préparés peut atteindre 82 % avec une teneur en cadmium toxique plus faible, ce qui est particulièrement important pour réduire la biotoxicité dans le domaine biomédical. De plus, les QD ont un grand décalage de Stokes ainsi qu'un premier pic d'absorption aplati, ce qui entraîne un faible chevauchement des spectres PL et d'absorption et un effet de réabsorption supprimé.
La protéine C-réactive (CRP), en tant que protéine de phase aiguë des cellules hépatiques, a été considérée comme un indicateur précoce d'infection et de troubles auto-immuns. Ces maladies commencent souvent à des niveaux de CRP très bas. Par conséquent, l'analyse immunologique quantitative sensible des niveaux de CRP dans des échantillons biologiques est d'une importance critique pour le diagnostic et le suivi de l'évolution des maladies [16]. Comparé au dosage immuno-enzymatique traditionnel (ELISA), le FLISA permet de gagner du temps sans réaction enzymatique et est moins sensible aux conditions environnementales résultant de la qualité optique des QD fluorescents [17]. Par conséquent, FLISA est devenu un nouveau point névralgique de la recherche en immunoessai quantitatif [2, 18,19,20,21]. Ici, nous avons d'abord démontré le dosage immunologique quantitatif FLISA à l'aide de QDs de noyau/coque solubles dans l'eau ZnSe/CdS/ZnS de type II/type I comme sonde fluorescente. La limite de détection (LOD) pour la détection quantitative de la protéine CRP a atteint 0,85 ng/mL, ce qui était 15 % plus sensible que celle de la FLISA basée sur les QD CdSe/ZnS de type I dans les expériences de contrôle. Les QY élevés, l'excellente stabilité optique et le faible effet de réabsorption peuvent favoriser l'application des QD ZnSe/CdS/ZnS de type II/type I en biomédecine et dans le domaine photoélectrique.
Méthodes
Produits chimiques
Oxyde de cadmium (CdO, 99,99 %), oxyde de zinc (ZnO, 99,9 %, poudre), sélénium (Se, 99,9 %, poudre), 1-octadécène (ODE, 90 %), 1-octanethiol (OT, 98 %), acide oléique (OA, 90 %) Le poly(anhydride maléique-alt-1-octadécène) (PMAO) et l'acide 2-(N-morpholino)éthanesulfonique (MES) ont été achetés auprès d'Aldrich. L'huile de paraffine (qualité analytique), l'acétone (qualité analytique), les hexanes (qualité analytique) et le méthanol (qualité analytique) ont été obtenus auprès de Beijing Chemical Reagent Co., Ltd, Chine. NaOH, HCl, Na2 CO3 , NaHCO3 , KH2 Bon de commande4 , Na2 HPO4 , H3 BO3 , Na2 B4 O7 · 10H2 O et Tween-20 ont été achetés auprès de Shanghai Sangon Co., Ltd, Chine. L'albumine de sérum bovin (BSA) et le sérum de veau ont été achetés auprès de Sigma. Le 1-éthyl-3-(3-(diméthylamino) propyl) carbodiimide (EDC), le N-hydroxysulfosuccinimide (sulfo-NHS) et les microplaques ont été achetés auprès de Thermo Fisher Scientific (USA). L'anticorps monoclonal de souris anti-protéine de réaction C et l'antigène CRP ont été obtenus auprès d'Abcam (USA). Tous les produits chimiques et solvants ont été utilisés tels qu'ils ont été reçus sans autre purification.
Solution stock pour le précurseur Se (0,1 M)
Se (6 mmol) et ODE (60 mL) ont été chargés dans un ballon tricol de 100 mL, puis chauffés à 220 °C pendant 180 min sous azote pour obtenir une solution jaune limpide.
Solution stock pour le précurseur Zn (0,4 M) et le précurseur Cd (0,2 M)
Du ZnO (30 mmol), de l'acide oléique (30 mL) et 45 mL d'ODE ont été chargés dans un ballon tricol de 100 mL et chauffés à 310 °C sous azote pour obtenir une solution claire. La solution résultante a été laissée à refroidir à 140 °C pour l'injection. Le processus de préparation du précurseur de Cd était le même que celui du précurseur de Zn, sauf que la concentration a été ajustée à 0,2 M et la température de réaction a été réglée à 240 °C.
Synthèse typique des QD ZnSe/CdS/ZnS Type-II/Type-I
En tant que procédure de synthèse typique, 4 mL de précurseur de Se et d'ODE (15 mL) ont été placés dans une fiole ronde de 100 mL. Le mélange a été chauffé à 310 °C. A cette température, 2 mL de précurseur de Zn ont été rapidement injectés dans le ballon de réaction. Des aliquotes ont été extraites à différents intervalles de temps pour surveiller l'évolution de la position PL qui se coordonne avec la taille des particules de QDs. Lorsque les nanocristaux du noyau ont atteint la dimension souhaitée, la température de réaction a été réduite à 230 °C pour la croissance de la coquille de CdS. Sans aucune étape de purification, car le mélange de précurseur de Cd et de 1-octanethiol (la radio molaire de l'OT et du cation est de 1:1,2) a commencé à être ajouté goutte à goutte avec une pompe à seringue à un débit de 3 mL/h, alors que la température était élevé à 310 °C. Le même processus a été appliqué à la croissance de la coquille de ZnS. Des aliquotes de QD ont été prélevées pendant la réaction pour analyser le développement des QD core/shell de ZnSe/CdS/ZnS. Les QD noyau/enveloppe tels que préparés ont été purifiés en ajoutant de l'acétone, puis redispersés dans du chloroforme.
Synthèse typique des QD CdSe/ZnS Type-I
Les QD CdSe/ZnS ont été synthétisés comme décrit dans nos précédents rapports [7]. Par la suite, le processus de transfert de phase, les sondes de détection d'anticorps QDs et la préparation de FLISA leur étaient identiques des QDs ZnSe/CdS/ZnS, qui seraient décrits ci-dessous.
Transfert de phase de QDs ZnSe/CdS/ZnS pour la bioapplication
Le poly(anhydride maléique-alt-1-octadécène) (PMAO) - un oligomère amphiphile dont les extrémités hydrophobes s'entrelacent avec le revêtement organique sur les QD et les groupes terminaux hydrophiles sont libres d'interagir avec le tampon environnant - a été utilisé pour transférer les QD hydrophobes en pur l'eau. Les QDs ZnSe/CdS/ZnS et PMAO ont été mélangés et dissous dans du chloroforme avec sonication (le rapport molaire de QD/PMAO était de 1:7). Après cela, le chloroforme a ensuite été éliminé par évaporation rotative à 45 °C. Ensuite, un volume égal de 0,1 M de NaHCO3 une solution aqueuse (pH = 8,5) a été ajoutée pour dissoudre le QDs-PMAO. Les QD ZnSe/CdS/ZnS de type II/type I encapsulés dans du PMAO ne présentent aucune perte de fluorescence et présentent une stabilité élevée en solution aqueuse dans une large gamme d'environnements de pH.
Préparation des sondes de détection d'anticorps QDs
La procédure a été largement rapportée dans les littératures précédentes [1,2,3]. Les QDs-PMAO ont d'abord été conjugués avec un anticorps monoclonal CRP par activation de ces groupes -COOH par EDC et sulfo-NHS. Ensuite, une certaine quantité d'anticorps monoclonaux CRP ont été ajoutés dans les QD et dissous dans du tampon BS puis ont été bloqués par BSA. Enfin, le produit a été lavé par du tampon BS 5 mM (pH =8,0) sous centrifugation. Le QDs-mAb a été stocké dans 50 μL de tampon BS (5 mM, pH = 8,0).
Préparation d'une microplaque de fluorescence revêtue d'anticorps
L'anticorps primaire (la concentration d'anticorps monoclonal CRP était de 1,8 mg/mL) a été dilué avec un tampon carbonate-bicarbonate (50 mM pH = 9,6, tampon CB) dans chaque puits de la microplaque. Par la suite, la microplaque a été recouverte d'un film d'étanchéité et incubée à 4 °C pendant 24 h. Afin d'éliminer l'excès d'anticorps de revêtement, la microplaque a été lavée trois fois avec un tampon de lavage (0,05 % de Tween-20 dans 10 mM de PBS, pH =7,4). Ensuite, les sites de liaison en excès ont été bloqués avec 0,5 % (p/v) de BSA dans 10 mM de PBS (pH = 7,4) pour une incubation pendant la nuit à 4 °C. Ce processus a garanti que tous les côtés de liaison disponibles et restants des puits de la microplaque étaient couverts. La microplaque a été séchée dans une chambre à température et humidité constantes pendant 24 h, puis stockée à 4 °C pour une utilisation future.
Détection quantitative de la CRP par dosage immunologique lié à la fluorescence
Dans chaque puits d'une microplaque à 96 puits, l'anticorps de revêtement contenu a été ajouté à 100 μL d'antigène standard et dilué à une série de concentrations avec le tampon d'échantillon. Les plaques ont été incubées à 37 °C pendant 30 min, puis lavées cinq fois avec un tampon de lavage. Ensuite, 100 μL de sondes QDs-mAb ont été dilués avec le tampon de sonde (10 % de sérum de veau (v/v) dans du PBS 0,1 M) dans chaque puits ont été incubés et lavés de la même manière que le processus mentionné ci-dessus.
Caractérisation
L'absorption UV-vis à température ambiante et les spectres PL ont été mesurés avec un spectrophotomètre Ocean Optics (mode PC2000-ISA). Les rendements quantiques PL (QY) ont été déterminés par comparaison de l'intensité de fluorescence intégrée des échantillons QD en solution avec celle du standard des QY connus (solution d'éthanol de Rhodamine 101 (R101) (0.01% HCl, QY = 100%) comme standard) . Des études de microscopie électronique à transmission (MET) ont été réalisées à l'aide d'un microscope électronique JEOL JEM-2010 fonctionnant à 200 kV. La détermination de phase des produits a été réalisée sur un diffractomètre à rayons X (D8-ADVANCE) en utilisant un rayonnement Cu-Ka (longueur d'onde = 1,54 Å). Les tailles des QD et de la sonde d'anticorps QD ont été enregistrées à l'aide de la diffusion dynamique de la lumière (Nano-ZS 90, Malvern Instruments, Royaume-Uni).
Résultats et discussion
Les spectres d'absorption UV-vis et PL du processus de croissance de la coque sont illustrés à la Fig. 1. Le décalage de Stokes du noyau de ZnSe n'est que de 8 nm avec le premier pic d'absorption à 420 nm et le pic d'émission à 428 nm, et l'émission pleine largeur à la moitié maximum (FWHM) de 17 nm. Cependant, lorsqu'une seule monocouche (ML) de coquille de CdS s'est développée sur le noyau de ZnSe, le décalage de Stokes a augmenté de manière significative à 54 nm avec le premier pic d'absorption à 497 nm et le pic d'émission à 551 nm, avec une émission pleine largeur à moitié maximum (FWHM) de 38 nm. En raison de la délocalisation de la fonction d'onde des électrons, l'émission PL des QD de ZnSe/CdS (629 nm) est décalée vers le rouge par rapport aux QD du noyau de ZnSe (428 nm) et la FWHM s'est élargie à 52 nm avec le dépôt d'une couche de CdS. Le PL FWHM élargi provient d'une interaction exciton-phonon de type Frölich améliorée [22, 23]. De plus, la force de l'oscillateur du premier pic d'absorption s'est rapidement affaiblie en raison de la transition spatialement indirecte de type II de la bande de valence du ZnSe à la bande de conduction du CdS. Le phénomène est courant dans les QD de type II [24,25,26]. Alors que l'augmentation spectaculaire de l'absorption dans la région spectrale bleue (<500 nm) a été attribuée à la bande interdite du matériau CdS en vrac (2,42 eV). En conséquence, l'émission rouge, le pic d'absorption du premier exciton aplati et l'absorption robuste dans la région de courte longueur d'onde (<500 nm) des QDs ZnSe/CdS de type II ont entraîné un grand décalage de Stokes et supprimé la réabsorption. Avec la croissance séquentielle de la coque ZnS, le PL a été déplacé vers la courte longueur d'onde et le FWHM a été rétréci de 52 nm à 43 nm. Ce phénomène a été attribué au fait que les atomes de Zn diffusent dans les régions riches en Cd pour former une couche de gradient à haute température, augmentant ainsi le décalage de bande de la coque. Les QY pourraient augmenter de 20 à 82 % au cours du processus de croissance de la coquille de CdS et de ZnS sur les noyaux de ZnSe.
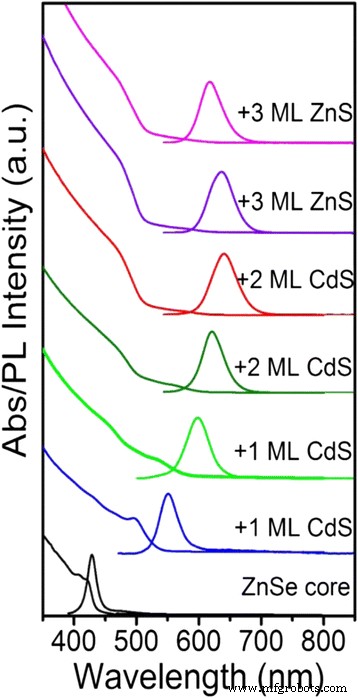
Évolution de l'absorption UV-vis et des spectres PL lors de la croissance consécutive des QD core/shell de ZnSe/CdS/ZnS
Il est à noter que l'excès de précurseur de Zn-OA par rapport au précurseur de Se dans la solution de cœur était nécessaire pour obtenir des QD de cœur de ZnSe monodispersés et de haute qualité. En conséquence, la coque en alliage ZnCdSeS serait inévitablement formée lors de l'ajout de précurseur de coque Cd-OT dans l'étape initiale car la température élevée (>200 °C) favorisait l'échange de cations et la diffusion entre Zn 2+ et Cd 2+ , et l'octanethiol riche en précurseur de Cd-OT pourrait également réagir avec l'excès de Zn-OA [7, 12, 27, 28]. La coque en alliage peut non seulement réduire la tension interfaciale et le défaut pour augmenter les QY, mais également générer une barrière énergétique pour les trous. Le bord de la bande de conduction du matériau de la coque en alliage ZnCdSeS était situé entre celui du ZnSe et du CdS, tandis que le bord de la bande de valence était plus profond que celui du CdS. Cela a formé un creux de potentiel plus grand dans le bord de la bande de valence en tant que couche de blocage supplémentaire pour les trous (Schéma 1) [12]. Cette structure de bande d'énergie peut réduire davantage le chevauchement des électrons et des trous pour diminuer la force du premier pic d'absorption d'excitons et supprimer la réabsorption.
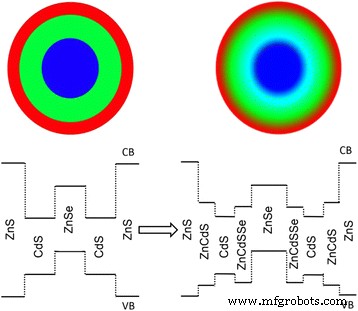
La structure schématique (up ) et l'alignement des bandes (bas ) pour les QD ZnSe/CdS/ZnS type-II/type-I basés sur les interfaces abruptes et alliées correspondantes, respectivement
Les informations sur la structure de la bande cœur/coquille et l'évolution de la PL et de l'absorbance au cours de la croissance de la coquille peuvent être vérifiées davantage par la comparaison de XRD, TEM et HRTEM des nanocristaux cœur et cœur/coquille. Les diagrammes XRD de poudre du noyau ZnSe, du ZnSe/CdS et du noyau/coque ZnSe/CdS/ZnS (l'image de gauche de la Fig. 2) montrent que les pics de diffraction deviennent nets et se déplacent vers des positions correspondant à la wurtzite en vrac (WZ) CdS ou des structures cristallines de ZnS. Ce résultat est cohérent avec les valeurs prédites pour le plus grand volume de coque CdS ou ZnS par rapport au noyau ZnSe dans les QD finaux noyau/coque et témoigne de la croissance des multicoquilles. De plus, une transformation des noyaux en ZnSe de type zinc blende (ZB) en noyau/coque de type WZ s'est produite avec les revêtements CdS et ZnS. Ce phénomène a été rapporté dans les systèmes QD core/shell CdSe/CdS [29, 30]. Les images MET des noyaux QD et de plusieurs noyaux / coques QD sont illustrées à la Fig. 2a − 2 F. Toutes les images MET montrent des QD sphériques presque monodisperses avec des diamètres moyens progressivement croissants du noyau ZnSe d'origine (3,90 nm) au type ZnSe/6CdS- QD II (7,98 nm) et QD ZnSe/6CdS/6ZnS type II/type I (11,92 nm). Comme le montre l'image HRTEM des QD du noyau de ZnSe (encadré de la figure 2a), l'espacement du réseau des plans (111) est de 0,32 nm, et les QD possèdent une bonne cristallinité et monodispersité. Avec la croissance des coquilles, le paramètre de réseau a montré un changement correspondant (0,35 nm pour le CdS et 0,31 nm pour le ZnS) conformément aux données XRD. Les résultats ont clairement suggéré la croissance contrôlable des matériaux de coque CdS et ZnS ultérieurs.
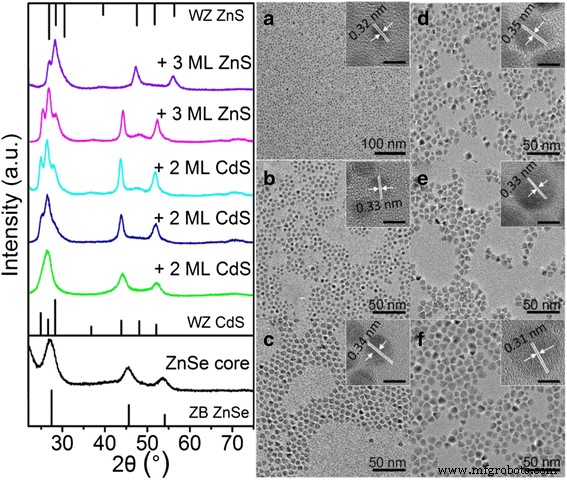
Gauche :Modèles XRD de QDs ZnSe/CdS/ZnS type II/type I avec différents stades de croissance de la coquille. Les raies de diffraction pour le zinc blende (ZB) ZnSe (en bas), WZ CdS (milieu ), et WZ ZnS (haut ) sont indexés. Droit :les TEM et HRTEM correspondants (encart , barre de 5 nm) images du cœur de ZnSe (a ), ZnSe/CdS type-II QDs avec 2 ML (b ), 4 ML (c ) et 6 ML (d ) Shell CdS, respectivement, et QDs ZnSe/CdS/ZnS type-II/type-I avec 3 ML (E) et 6 ML (F), respectivement
Pendant ce temps, pour confirmer l'évolution de la composition au cours de la croissance de la multicouche, l'analyse par spectroscopie à rayons X à dispersion d'énergie (EDS) a été effectuée pour différentes étapes de la croissance noyau/enveloppe, comme indiqué dans le fichier supplémentaire 1 :tableau S1. Les données EDS montrent que les changements correspondants de teneur en Cd, Se, Zn et S sont conformes au stade de croissance de la coquille. Mais il convient de noter que le rapport molaire Cd/(Zn + Cd) dans les QDs ZnSe/CdS résultants est supérieur au rapport d'alimentation Cd/(Zn + Cd) en raison de l'échange de cations entre Zn 2+ et Cd 2+ pendant le processus de revêtement de la coque CdS sur le noyau ZnSe à plus de 200 °C. En comparaison avec la littérature publiée sur les QD typiques de CdSe/CdS/ZnS de type I (rapport molaire Cd ~ 40%) [31], les QDs de type II/type-I ZnSe/CdS/ZnS contenaient beaucoup moins d'éléments Cd (~ 13 %).
Une comparaison visuelle des QD hydrophobes dans le chloroforme et des QDs plafonnés PMAO dans l'eau sous la lumière du soleil et la lumière UV est présentée dans le fichier supplémentaire 1 :Figure S1 (A). Il semble que les deux solutions QD ne soient pas perturbées et sans agrégation de nanoparticules. Les deux QD ont émis la même lumière rouge lorsqu'ils ont été éclairés avec une lampe UV à main (365 nm). Fichier supplémentaire 1 :La figure S1 (B) montre l'absorption UV-visible et les spectres PL des QD avant et après le transfert de phase. Comparé aux QD hydrophobes dans le chloroforme, le spectre PL des QD coiffés de PMAO a un changement négligeable, ce qui n'indique aucun changement évident dans la taille des particules et les propriétés PL. Fichier supplémentaire 1 :Les figures S1 (C) et (D) présentent les images MET des QD avant et après le transfert de phase, qui déterminent en outre la morphologie et l'état des QD coiffés de PMAO. Il semble que les QD plafonnés par PMAO soient bien isolés et rarement observés sous forme d'agrégats.
Afin de confirmer la formation de QD encapsulés dans PMAO pendant le processus de transfert de phase, la spectroscopie FTIR a été utilisée pour caractériser les groupes fonctionnels à la surface des QD (présentés dans le fichier supplémentaire 1 :Figure S2). La diminution du pic à 1777 cm −1 (comparé PMAO avec QDs-PMAO) et l'augmentation du pic à 1715 cm −1 (par rapport aux trois échantillons) ont été attribués à la décomposition de l'anhydride et à la formation de -COOH. Les résultats du FTIR ont indiqué que le polymère amphiphile PMAO a été appliqué avec succès sur la surface des QD ZnSe/CdS/ZnS.
La stabilité des QD tels que préparés est très importante pour le traitement ultérieur. La figure 3a montre que l'évolution de la stabilité relative de la PL des QD hydrophobes de ZnSe/CdS/ZnS lors des étapes de purification. L'intensité PL des QD core/shell de ZnSe/CdS/ZnS pourrait maintenir 85% sur de nombreux cycles de purification dans les hexanes. Comme le montre la figure 3b, la stabilité colloïdale du QDs-PMAO dans le tampon BS (pH = 7,2) a été estimée en fonction du temps à 25 °C. L'intensité PL est restée presque constante et la solution était claire même après 400 h. Cela indique que le QDs-PMAO est stable dans la solution BS sans aucun dommage. La figure 3c montre la variation de l'intensité PL des QDs-PMAO qui ont été immergés dans une solution à pH acide à basique (pH = 1-14, ajusté par HCl ou NaOH) pendant 30 min. L'intensité PL des QD hydrophiles pourrait conserver plus de 85 %, sauf lorsque le PH =14. La figure 3d montre l'effet du paramètre de température sur l'intensité de fluorescence relative des QD-PMAO. L'intensité de la fluorescence a progressivement diminué avec l'augmentation de la température mais s'est maintenue à 76 % à 90 °C, tandis que les pics de PL se sont progressivement déplacés vers une longueur d'onde plus longue en raison de la dilatation thermique et de l'effet de couplage électron-phonon. Toutes les évaluations de stabilité indiquent que les QDs ZnSe/CdS/ZnS type II/type I et QDs-PMAO étaient très stables et donc adaptés aux applications biologiques.
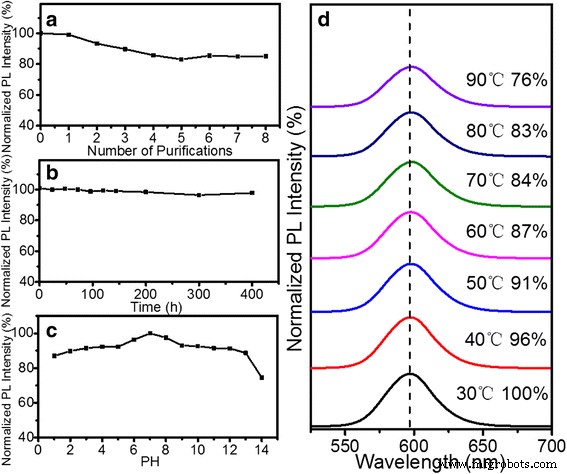
Test de stabilité des QD hydrophobes sur (a ) étapes répétées du processus de purification ; test de stabilité de QDs-PMAO sur (b ) Tampon BS, (c ) PH, et (d ) température
La CRP est une protéine de phase aiguë des cellules hépatiques, et son niveau est considéré comme un indicateur précoce d'infection et de troubles auto-immuns. Ici, les QDs ZnSe/CdS/ZnS coiffés par PMAO tels que synthétisés sont couplés à la CRP pour démontrer la possibilité d'une application dans le dosage immunologique quantitatif. Le diagramme de comparaison des spectres de fluorescence des QDs aqueux de ZnSe/CdS/ZnS et des QDs-mAb est présenté sur la figure 4a. De toute évidence, la forme du pic PL des deux échantillons est approximativement identique, sauf que l'intensité de fluorescence diminue à 60 % après la réaction de couplage en raison de la perte inévitable d'échantillon pendant le processus de séparation par centrifugation. Il prouve l'excellente stabilité optique des QDs ZnSe/CdS/ZnS type-II/type-I même après le processus de couplage anticorps-protéine.
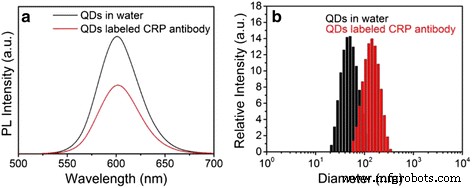
Spectres de fluorescence (a ) et la diffusion dynamique de la lumière (b ) des QDs-PMAO et QDs-mAb en tampon
Pour étudier plus avant l'effet de la conjugaison sur la taille des QD, les QD aqueux et les QD-mAb sont caractérisés par la diffusion dynamique de la lumière (DLS). Les résultats DLS (Fig. 4b) montrent clairement que les deux échantillons ont une distribution de taille étroite avec une bonne monodispersité et conservent une forme discrète sans agrégation, tandis que la taille hydrodynamique augmente de 46 à 120 nm après le processus de couplage. Cela démontre le succès de la conjugaison avec les anticorps CRP.
En outre, nous avons utilisé les points quantiques composites ZnSe/CdS/ZnS type II/type I au lieu des QD CdSe/ZnS type I comme sonde fluorescente pour établir une FLISA pour la détection quantitative de la CRP. Le processus d'assemblage est illustré dans le fichier supplémentaire 1 :schéma S1. La figure 5a montre l'intensité de fluorescence relative du marqueur de fluorescence QDs pour le dosage immunologique dans la détection de diverses concentrations d'antigènes CRP (l'antigène CRP standard est dilué à 0, 1, 5, 10, 50, 100, 200, 400 ng/mL). De toute évidence, l'intensité de PL augmente progressivement avec l'augmentation de la concentration de CRP. La figure 5b montre que la corrélation entre l'intensité de fluorescence et les concentrations cibles de CRP obéit à une équation de courbe de régression quadratique de y = 44230 + 8121,1x-10,3x 2 avec un coefficient de corrélation de 0.9991, qui est le plus proche de 1 mieux c'est. Les concentrations de travail vont de 0 à 400 ng/mL. La LOD est l'un des paramètres clés pour le dosage immunologique pour FLISA. En utilisant les QD composites ZnSe/CdS/ZnS de type II/type I comme sonde fluorescente, la sensibilité de la détection quantitative de la CRP est de 0,85 ng/mL, ce qui est 15 % plus sensible que celle de la FLISA basée sur le type CdSe/ZnS -I QD (1,00 ng/ml) (dans le fichier supplémentaire 1 :Figure S3).
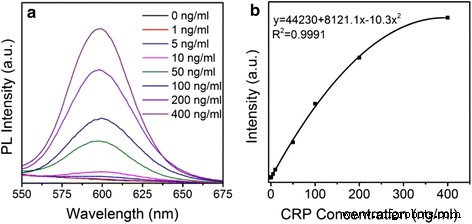
Spectres de photoluminescence de FLISA pour la détermination de différentes concentrations d'antigène CRP (a ) et les courbes étalons (b )
De plus, des expériences de récupération ont été utilisées pour évaluer l'effet de matrice de la FLISA avec une série d'antigènes CRP standard connus pour analyse, et les concentrations finales couvraient les niveaux de risque faible, moyen et élevé. Comme le montre le tableau 1, tous les taux de récupération se situent entre 83,61 et 105,9 %. Ces résultats indiquent que la FLISA basée sur les QD ZnSe/CdS/ZnS type II/type I avec propriété de suppression de la réabsorption a une grande précision et présente de grands avantages dans la détection par immunoessai quantitatif.
Conclusions
Nous rapportons une méthode à un seul pot sans phosphine pour synthétiser des QDs de type noyau/coque de type II/type I de ZnSe/CdS/ZnS supprimés par réabsorption avec un grand décalage de Stokes et un premier pic d'absorption plat. Ces caractéristiques réduisent la réabsorption et améliorent le niveau de sortie de fluorescence. Les QD tels que synthétisés ont un QY élevé (82 %) et une stabilité élevée dans diverses conditions de test. Ensuite, nous utilisons d'abord les QDs ZnSe/CdS/ZnS comme sonde de fluorescence en FLISA pour la détection quantitative de la protéine CRP avec une sensibilité élevée (LOD de 0,85 ng/mL). Cela indique que les QD à noyau/coque ZnSe/CdS/ZnS de type II/type I à réabsorption supprimée ont un potentiel prometteur pour une application dans les domaines biomédicaux et photoélectriques.
Abréviations
- BSA :
-
Sérum albumine bovine
- CRP :
-
Protéine C-réactive
- DLS :
-
Diffusion dynamique de la lumière
- EDC :
-
1-éthyl-3-(3-(diméthylamino) propyl) carbodiimide
- EDS :
-
Spectroscopie à rayons X à dispersion d'énergie
- ELISA :
-
Dosage immuno-enzymatique
- FLISA :
-
Dosage immunosorbant lié à la fluorescence
- FWHM :
-
Pleine largeur à mi-hauteur
- LOD :
-
Limite de détection
- MES :
-
Acide 2-(N-morpholino)éthanesulfonique
- OT :
-
1-octanethiol
- PMAO :
-
Poly(anhydride maléique-alt-1-octadécène)
- QD :
-
Points quantiques
- QY :
-
Rendements quantiques
- sulfo-NHS :
-
N-Hydroxysulfosuccinimide
Nanomatériaux
- Avancées et défis des nanomatériaux fluorescents pour la synthèse et les applications biomédicales
- Synthèse de points quantiques de carbone co-dopés en pyridinique N, S en tant qu'imitateurs d'enzymes efficaces
- Synthèse verte de points quantiques InP/ZnS Core/Shell pour une application dans des diodes électroluminescentes sans métaux lourds
- Synthèse de nanocristaux de ZnO et application dans des cellules solaires polymères inversées
- Synthèse par chauffage à l'état solide du composite poly (3,4-éthylènedioxythiophène)/or/graphène et son application pour la détermination ampérométrique du nitrite et de l'iodate
- Synthèse de points quantiques de sulfure d'antimoine solubles dans l'eau et de leurs propriétés photoélectriques
- Contrôle électrochimique réversible de la luminescence photoexcitée d'un film à points quantiques CdSe/ZnS à noyau/enveloppe
- Synthèse écologique et facile de nanofils de Co3O4 et leur application prometteuse avec du graphène dans les batteries lithium-ion
- Synthèse sonochimique en une étape facile et propriétés photocatalytiques des composites graphène/Ag3PO4 Quantum Dots



