Synthèse par chauffage à l'état solide du composite poly (3,4-éthylènedioxythiophène)/or/graphène et son application pour la détermination ampérométrique du nitrite et de l'iodate
Résumé
Un composite ternaire de poly (3,4-éthylènedioxythiophène)/or/graphène (PEDOT/Au/GO) pour un capteur électrochimique prometteur a été synthétisé par une méthode de chauffage à l'état solide. L'interaction entre le PEDOT, Au et GO a été explorée pour la détection de nitrite et d'iodate. Il a été constaté que le composite PEDOT/Au/GO avait une morphologie de type schiste avec une distribution uniforme de nanoparticules d'or. Des expériences électrochimiques ont montré que l'électrode modifiée composite PEDOT/Au/GO présentait une bonne activité électrocatalytique pour la détermination de l'iodate. Les expériences ampérométriques au PEDOT/Au/GO/GCE ont révélé qu'une bonne relation linéaire existait entre le courant de crête et la concentration dans la plage de 100 à 1000 μM avec la détection de 0,53 et 0,62 μM (S/N = 3) pour le nitrite et iodate, respectivement. De plus, la réponse actuelle de PEDOT/Au/GO/GCE pour le nitrite et l'iodate à 10 μM était respectivement de 9,59 et 11,47 μA.
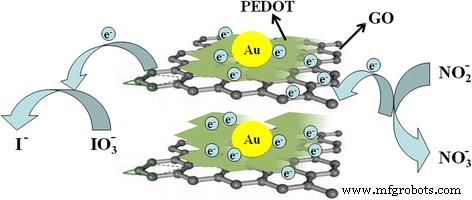
Mécanismes du transfert direct d'électrons entre l'ion (nitrite ou iodate) et le composite PEDOT/Au/GO
Contexte
Nitrite (NO2 − ) est omniprésent dans les produits environnementaux, alimentaires et agricoles, ce qui a été reconnu pour exister dans les systèmes physiologiques lorsque les composés ingérés contiennent du NO2 − [1, 2]. NON2 − peuvent réagir avec les amines pour former des nitrosamines cancérigènes, et l'ingestion continue de ces ions peut être nocive pour la santé animale et humaine [3,4,5]. Aussi avec l'autre presse ionique proche de notre quotidien, l'iodate (IO3 − ), le sel iodé, est reconnu comme la stratégie la plus efficace pour la prévention des troubles dus à une carence en iodure. Cependant, un excès de IO3 − peut produire un goitre et une hypothyroïdie ainsi qu'une hyperthyroïdie [6, 7]. Par conséquent, de nombreuses techniques ont été développées pour le NO2 − et IO3 − détection [8], y compris les méthodes spectroscopiques [9], chromatographiques [10], chimiluminescence [11], électrochimiques [12,13,14,15] et d'électrophorèse capillaire [16]. Parmi eux, la méthode électrochimique a été largement utilisée en raison de sa sensibilité élevée, de sa simplicité, de sa rapidité et de son faible coût. Généralement, les électrodes ont été modifiées avec un métal nanostructuré (tel que Pt, Au), un oxyde métallique (tel que WO3 , RuO2 ) et les nanomatériaux de carbone, et qui ont été largement étudiés pour le développement de capteurs électrochimiques efficaces [17,18,19,20]. Parmi elles, les nanoparticules d'Au ont de larges applications dans le domaine des capteurs électrochimiques avec son activité catalytique idéale, sa sensibilité, sa biocompatibilité, ses propriétés dominées par l'interface, son excellente conductivité et son rapport signal sur bruit élevé. Cependant, le coût élevé, la mauvaise sélectivité et l'instabilité de l'Au le rendent impropre aux applications pratiques [21].
Récemment, les matériaux hybrides polymères conducteurs/or ont été largement étudiés pour obtenir de nouveaux matériaux composites avec des comportements synergiques ou complémentaires [22, 23]. En tant que partie typique et importante des polymères conducteurs, le poly (3,4-éthylènedioxythiophène) (PEDOT) a de larges applications dans le domaine des écrans, des fenêtres intelligentes, des capteurs, des condensateurs, des batteries et des dispositifs photovoltaïques [24,25,26 ]. Généralement, dans les composites PEDOT/Au synthétisés chimiquement, les performances électrocatalytiques du composite pourraient être améliorées grâce aux interactions Au-S (thiophène) et à l'activation de la coordination des ions métalliques [27, 28]. Et de nombreux rapports ont été publiés pour la préparation de composites binaires PEDOT/Au [29, 30].
Ces dernières années, la plupart des recherches se sont concentrées sur la préparation de composites ternaires à base de graphène/polymère conducteur car les matériaux carbonés à base de graphène ont une surface spécifique élevée, une propriété de transport électronique unique, une activité électrocatalytique élevée et une bonne stabilité chimique [31, 32 ]. Ces caractéristiques uniques des matériaux carbonés à base de graphène apportent peut-être des structures chimiques uniques et des performances supérieures aux composites [33].
Yao et al. synthétisé un capteur composite PANI/MWNTs/Au pour la détection de NO2 − , et la réponse actuelle était d'environ 2,8 μA pour 10 μM NO2 − [34]. Xue et al. préparé un nanocomposite ternaire de nanoparticules d'or/polypyrrole/graphène par des voies chimiques humides faciles et a constaté que les composites tels que préparés ont une bonne activité électrocatalytique envers le glucose avec sa haute sensibilité [35]. Dans ce cas, la recherche sur la préparation, la structure et les propriétés des nanocomposites ternaires à base de graphène sera très intéressante et stimulante dans le domaine des capteurs. Cependant, la technique chimique et électrochimique conventionnelle pour le nanocomposite ternaire est généralement compliquée et fastidieuse. Par conséquent, des méthodes synthétiques rentables, claires, écologiques, simples et hautement efficaces sont souhaitables.
Nous rapportons ici la fabrication d'un composite ternaire (PEDOT/Au/GO) de poly (3,4-éthylènedioxythiophène), de nanoparticules d'or et de graphène pour un capteur électrochimique prometteur par la méthode de chauffage à l'état solide. A titre de comparaison, le PEDOT pur et le composite binaire (PEDOT/Au) ont également été synthétisés de la même manière. Les composites PEDOT/Au/GO et PEDOT/Au ont été utilisés pour la détermination électrochimique sensible de l'iodate. Et le composite PEDOT/Au/GO a été sélectionné pour évaluer son application potentielle en tant que capteur électrochimique pour la détection de nitrite et d'iodate sur la base d'études systématiques sur la détermination ampérométrique de nitrite et d'iodate.
Expérimental
Produits chimiques et réactifs
Le 3,4-éthylènedioxythiophène (EDOT) a été obtenu auprès de Shanghai Aladdin Reagent Company (Chine), et il a été purifié par distillation sous pression réduite et stocké dans un réfrigérateur avant utilisation. Acide chloroaurique hydraté (HAuCl4 ·4H2 O) a été acheté auprès de Shanghai Aladdin Reagent Company (Chine). Le graphène (GO) a été acheté auprès de Strem Chemicals Inc. (USA). Tous les autres réactifs étaient de qualité analytique et utilisés tels que fournis sans autre purification. Le 2,5-dibromo-3,4-éthylènedioxythiophène a été synthétisé selon le rapport précédent [36].
Synthèse des composites PEDOT/Au/GO et PEDOT/Au
Avant la synthèse des composites, la solution de sol de nanoparticules d'Au a été préparée à l'avance. La solution de sol de nanoparticules d'Au a été préparée en réduisant HAuCl4 avec NaBH4 comme réducteur. Une préparation typique de solution de sol de nanoparticules d'Au était la suivante :60 mg de HAuCl4 ·3H2 O a été ajouté à 100 mL d'eau pour créer HAuCl4 Solution. Un total de 3,4 mL de solution aqueuse de Na3 C6 H5 O7 (1%) a ensuite été ajouté aux 40 mL de HAuCl4 solution sous agitation vigoureuse pendant 10 min. Le 1,2 mg de NaBH4 a ensuite été rapidement ajouté, et la couleur de la solution a immédiatement viré au violet.
Une synthèse typique de chauffage à l'état solide du composite PEDOT/Au/GO était la suivante (Fig. 1) :un mélange de 0,5 g (2 mmol) de monomère (2,5-dibromo-3,4-thylène dioxythiophène) et 10 mg Les GO dans 30 mL de chloroforme ont été soumis à des ultrasons pendant 30 min pour faciliter l'adsorption du monomère à la surface de GO. On a ensuite laissé le mélange évaporer le chloroforme. Le résidu a été mis dans un mortier suivi d'un broyage constant pendant 5 min. Ensuite, le mélange a été ajouté à la solution de sol de nanoparticules d'Au et agité pendant 10 min. Le mélange a ensuite été filtré et lavé à l'eau distillée, enfin maintenu dans une étuve sous vide à 60 °C pendant 24 h. Le produit obtenu a été désigné comme composite PEDOT/Au/GO.
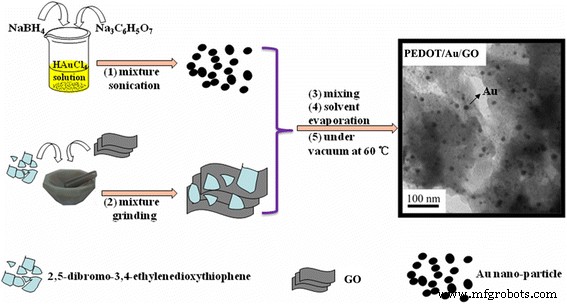
Représentation schématique du processus de formation du PEDOT/Au/GO
À titre de comparaison, le composite binaire (PEDOT/Au) et le PEDOT pur ont également été synthétisés de la même manière.
Caractérisation de la structure
Les spectres infrarouges à transformée de Fourier (FTIR) des échantillons ont été enregistrés sur un spectromètre FTIR BRUKER-QEUINOX-55 en utilisant des pastilles de KBr. Les spectres UV-vis des échantillons ont été enregistrés sur un spectrophotomètre UV-visible (UV4802, Unico, USA). Les échantillons pour les mesures MET ont été préparés en plaçant quelques gouttes de produits en suspension d'éthanol sur des supports en cuivre et réalisés sur un microscope électronique Hitachi 2600. Le contenu élémentaire de l'échantillon a été caractérisé par spectroscopie à rayons X à dispersion d'énergie (EDS), qui a été prise sur un microscope Leo1430VP avec une tension de fonctionnement de 5 kV. Les expériences EDX ont été réalisées avec une pastille qui a été pressée à 200 MPa puis collée sur des plaques de cuivre.
Mesure de l'activité électrocatalytique
Voltamétrie cyclique (CV) et ampérométrie i –t ont été réalisées sur une station de travail électrochimique CHI 660C (ChenHua Instruments Co., Shanghai, Chine). Un système à trois électrodes a été utilisé pour étudier les performances électrochimiques du composite. L'électrode en Pt a été utilisée comme contre-électrode et l'électrode au calomel saturé (SCE) comme électrode de référence. Le composite GCE modifié PEDOT/Au/GO (électrode en carbone vitreux ; diamètre = 3 mm) a été utilisé comme électrode de travail. L'électrode de travail a été fabriquée en plaçant 5 μL de 30 mg/L de suspension composite PEDOT/Au/GO (le composite PEDOT/Au/GO a été dispersé dans de l'eau pour créer une suspension (30 mg/L).) sur une surface nue de GCE et séché à l'air pendant 10 min. Toutes les expériences ont été réalisées à température ambiante et atmosphère d'air.
Résultats et discussion
La figure 2a représente les spectres FTIR de PEDOT, PEDOT/Au et PEDOT/Au/GO. Comme on peut le voir sur la figure 2a, le spectre des composites PEDOT/Au/GO et PEDOT/Au est similaire à celui du PEDOT pur, indiquant une formation réussie de polymère dans le composite. Les deux bandes apparaissant à ~ 1514 et ~ 1324 cm −1 sont affectés respectivement au mode d'étirement asymétrique de C=C et au mode d'étirement inter-anneaux de C–C. Les bandes apparaissant à ~ 1198, ~ 1140 et ~ 1084 cm −1 sont attribuées à la vibration de flexion C–O–C dans l'éthylènedioxy. Ces résultats sont en bon accord avec les précédents spectres FTIR de PEDOT [37]. Bien que les spectres des composites PEDOT/Au/GO et PEDOT/Au soient similaires à celui du PEDOT pur, plusieurs écarts apparaissent entre le PEDOT pur et les composites. Selon le rapport précédent, le degré de polymérisation du polythiophène peut être évalué à partir du rapport d'intégration des bandes infrarouges à 690 et 830 cm −1 [38, 39], et le degré de polymérisation plus élevé peut être le résultat d'une valeur relativement plus faible de ce rapport d'intensité. Par conséquent, on peut déduire de la figure 2a que le degré de polymérisation du PEDOT/Au/GO, PEDOT/Au et PEDOT est de l'ordre de PEDOT/Au/GO> PEDOT/Au> PEDOT, ce qui suggère que le PEDOT /Au/GO a un degré de polymérisation plus élevé que PEDOT/Au et PEDOT. De plus, ce résultat indique que la présence de GO dans le milieu réactionnel peut jouer un rôle positif dans l'augmentation du degré de polymérisation du PEDOT dans la matrice composite.
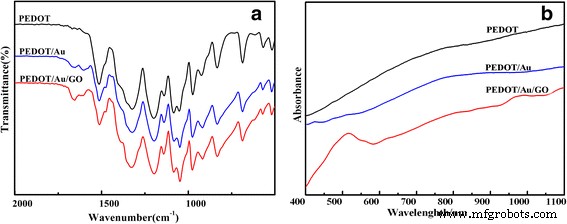
FTIR (a ) et UV-vis (b ) spectres de PEDOT, PEDOT/Au et PEDOT/Au/GO
La figure 2b montre les spectres d'absorption UV-vis de PEDOT, PEDOT/Au et PEDOT/Au/GO. Comme le montre la figure 2b, le PEDOT affiche un large pic d'absorption commençant à ~ 500 nm et s'étendant dans la région du proche infrarouge. Cette caractéristique d'absorption, connue sous le nom de « queue de porteur libre », est en corrélation avec la conductivité des polymères. Il a été démontré que la présence de ce pic d'absorption correspond au polymère ayant une longueur de conjugaison plus longue et un ordre plus important, ce qui permet une plus grande mobilité des porteurs de charge [40, 41]. Dans le cas des composites, le PEDOT/Au présente une caractéristique d'absorption similaire à celle du PEDOT, tandis que le PEDOT/Au/GO présente un pic d'absorption (transition π-π*) à ~ 500 nm avec une queue de porteur libre s'étendant dans la région du proche infrarouge [37, 40, 42]. Ce phénomène implique en outre qu'il existe une forte interaction entre les régions aromatiques du graphène non covalent et les cycles quinoïdes de PEDOT [43, 44].
La figure 3 montre les images de micrographie électronique à transmission (MET) de PEDOT, PEDOT/Au et PEDOT/Au/GO. Comme le montrent les figures 3a, b, le PEDOT pur présente une morphologie de type schiste avec une structure en couches, tandis que le composite PEDOT/Au avait une morphologie de type granulaire se mélangeant à partir de nanoparticules PEDOT et Au avec une taille moyenne de 50 nm. Cependant, dans le cas du composite PEDOT/Au/GO (Fig. 3c), il a été constaté que le composite avait une morphologie de type schiste avec une distribution uniforme de nanoparticules d'or (nanoparticules de couleur foncée). De plus, la morphologie de type schiste du composite PEDOT/Au/GO est construite à partir d'une structure en couches légèrement ombrée et sombre, qui peut être attribuée respectivement au GO et au PEDOT. Ces résultats impliquent que les nanoparticules GO et Au ne sont pas simplement mélangées ou mélangées avec le PEDOT, suggérant que les nanoparticules GO et Au (taille moyenne de 10 à 15 nm) sont intégrées dans une matrice composite. Cette distribution uniforme des nanoparticules GO et Au dans le composite peut être liée à la morphologie de type schiste du PEDOT, qui peut apporter une certaine possibilité de formation de structures lamellaires à partir de l'incorporation de PEDOT et GO, et conduit à une grande surface pour une distribution uniforme des nanoparticules Au .

Images TEM de a PEDOT, b PEDOT/Au, et c PEDOT/Au/GO
La figure 4a indique les profils XRD de PEDOT, PEDOT/Au et PEDOT/Au/GO. De plus, pour étudier le pourcentage d'éléments d'Au, des spectroscopies à rayons X à dispersion d'énergie (EDX) de PEDOT, PEDOT/Au et PEDOT/Au/GO sont également présentées sur la Fig. 4b. Comme le montre la figure 4a, le PEDOT, le PEDOT/Au et le PEDOT/Au/GO affichent de larges pics de diffraction avec une faible intensité à 2θ ~25,9°, qui peut être associé à l'espacement intermoléculaire du squelette polymère ou attribué à la réflexion (020) [45]. De plus, le composite montre un pic de diffraction net à 2θ ~26°, indiquant l'existence de GO dans le composite [46]. Dans le cas du composite PEDOT/Au/GO, le pic de diffraction caractéristique du PEDOT (2θ ~25,9°) se superpose à celui de GO (2θ ~26,6°). Le diagramme XRD du composite indique que la présence de pics de diffraction caractéristiques de Au (quatre pics de faible intensité à 2θ valeurs de 37,9° et 43,7°), qui correspondent aux réflexions de Bragg sur les plans (111) et (200) d'Au [47], suggérant l'incorporation réussie d'Au dans le composite, ce qui est en accord avec le résultat d'EDX ( Fig. 4b) de PEDOT/Au (présence de 1,92 % en poids Au). Cependant, il n'y a pas de pic de diffraction évident pour Au dans PEDOT/Au/GO, ce qui ne correspond pas au résultat de l'EDX (Fig. 4b) de PEDOT/Au/GO (présence de 1,71 % en poids Au). Cela peut être attribué à la petite taille des particules et à la forte dispersion des nanoparticules d'Au dans le composite PEDOT/Au/GO, et ce phénomène est similaire à l'observation dans le nanocomposite Au/Zn, qui n'a montré aucun pic de diffraction pour les nanoparticules d'Au [47] .
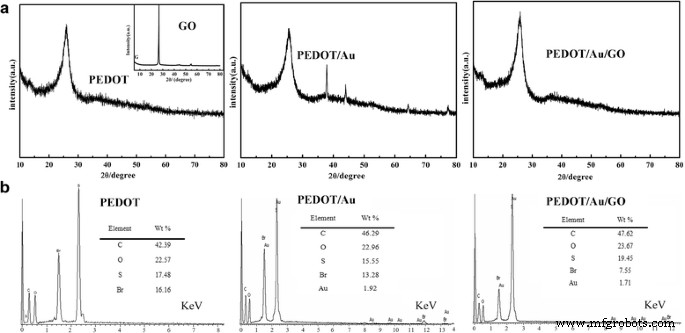
XRD (a ) et EDX (b ) de PEDOT, PEDOT/Au et PEDOT/Au/GO
L'analyse thermogravimétrique de PEDOT, PEDOT/Au et PEDOT/Au/GO est illustrée à la Fig. 5. Il est clair que ces échantillons subissent des comportements de perte de poids en trois étapes. La perte de poids de la première étape à 40-104 °C est due à la perte de trace d'eau ou d'humidité piégée de la chaîne polymère. Les pertes de poids de la deuxième étape se produisent entre 112 et 323 °C avec une perte de poids de 24,78 % (PEDOT), 24,33 % (PEDOT/Au) et 19,17 % (PEDOT/Au/GO), respectivement. Ceci est dû à la perte de polymère de bas poids moléculaire. Dans la troisième étape, le polymère subit une dégradation après 323 °C. Ce résultat indique que le polymère est stable jusqu'à 323 °C. Et présentent des pourcentages massiques résiduels de 20,8 % (PEDOT), 29,1 % (PEDOT/Au) et 36,5 % (PEDOT/Au/GO) après 800 °C. Ces résultats suggèrent que la présence de Au et GO peut améliorer les stabilités thermiques des composites.
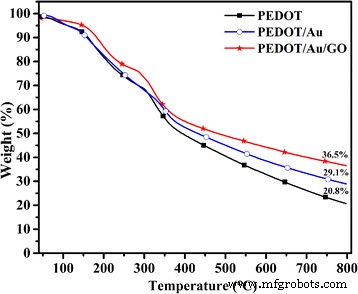
Courbes TGA de PEDOT, PEDOT/Au et PEDOT/Au/GO
Pour évaluer l'application potentielle des composites PEDOT/Au/GO et PEDOT/Au comme capteur électrochimique, l'iodate (IO3 − ) est sélectionné comme espèce d'essai pour l'expérience électrochimique. La figure 6 montre des voltamogrammes cycliques des composites PEDOT/Au/GO et PEDOT/Au dans 0,1 M H2 SO4 solution contenant 5 mM d'iodate. Comme le montre la figure 6, il n'y a pas de pic d'oxydation/réduction dans les deux cas de PEDOT/Au/GO (PEDOT/Au/GO/GCE) et PEDOT/Au modifié électrode de carbone de verre (PEDOT/Au/GCE) sans ajouter OI3 − . Lorsque l'IO3 − est ajouté, les deux composites affichent quelques pics d'oxydation/réduction, et la valeur du courant de pic de réduction est supérieure à celle du pic d'oxydation respectif, qui résulte de la réduction de IO3 − à I − [48]. De plus, l'intensité de courant de réduction la plus élevée se produit dans le cas de PEDOT/Au/GO/GCE, ce qui suggère que PEDOT/Au/GO/GCE a une activité catalytique électrochimique supérieure à PEDOT/Au/GO.
Voltammogrammes cycliques de PEDOT/Au/GO/GCE et PEDOT/Au/GCE dans une solution 0,1 M de H2SO4 contenant 5 mM d'iodate
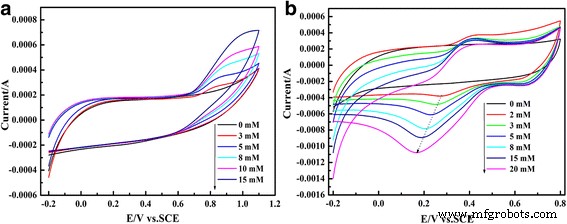
La figure 7 montre des voltamogrammes cycliques de PEDOT/Au/GO/GCE dans une solution de PBS 0,025 M (pH = 6,86) contenant du nitrite (Fig. 7a et 0,1 M H2 SO4 solution contenant de l'iodate (Fig. 7b), respectivement. Le courant de crête augmente avec l'augmentation de la concentration en nitrite (3 à 15 mM) et de la concentration en iodate (2 à 20 mM), respectivement. Comme le montre la figure 7a, il existe un large pic d'oxydation à environ 0,82 V, qui peut être attribué à la conversion de NO2 − à NON3 − par un processus d'oxydation à deux électrons [49]. Dans le cas de l'iodate (Fig. 7b), les courants de crête de réduction augmentent et le potentiel de crête se décale légèrement de 300 à 160 mV, ce qui peut être attribué à la réduction rapide de IO3 − à I − [48].

Voltammogrammes cycliques de PEDOT/Au/GO/GCE dans une solution PBS 0,025 M (pH = 6,86) contenant du nitrite (a ) et 0,1 M H2 SO4 solution contenant de l'iodate (b )
La figure 8 montre la réponse courant-temps catalytique en régime permanent de PEDOT/Au/GO/GCE avec l'ajout successif de 1,0 × 10 −5 , 1,0 × 10 −4 , et 1,0 × 10 −3 Nitrite M (Fig. 8, potentiel contrôlé à 0,78 V) et iodate (Fig. 8b, potentiel contrôlé à − 0,25 V), respectivement. Comme le montre la figure 8, une réponse bien définie est observée sous l'addition successive de 1,0 × 10 −5 , 1,0 × 10 −4 , et 1,0 × 10 −3 M nitrite et iodate, respectivement.
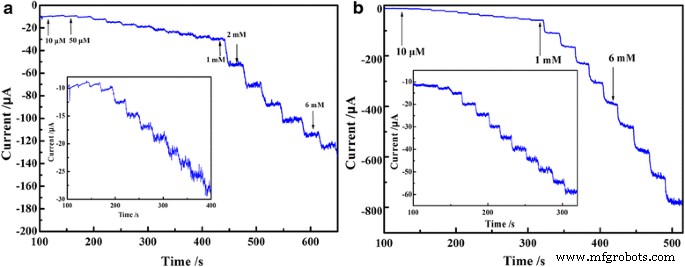
Réponse courant-temps catalytique en régime permanent de PEDOT/Au/GO/GCE avec ajout successif de 1,0 × 10 −5 , 1,0 × 10 −4 , et 1,0 × 10 −3 M nitrite (a ) et iodate (b )
La figure 9 montre la réponse courant-temps catalytique en régime permanent de PEDOT/Au/GO/GCE avec l'ajout successif de 1,0 × 10 −3 M nitrite (Fig. 9a, potentiel contrôlé à 0,78 V) et iodate (Fig. 9b, potentiel contrôlé à − 0,25 V). Les résultats de la figure 9 montrent que la détection du nitrite et de l'iodate a un meilleur courant catalytique à l'état d'équilibre dans la plage de 100 à 1000 μM, et le temps de réponse est d'environ 4 s après chaque ajout de nitrite et d'iodate, respectivement. Les tracés des courants chronoampérométriques en fonction de la concentration en ions (encadrés sur la Fig. 9) indiquent en outre qu'il existe une bonne relation linéaire entre le courant de crête et la concentration dans la plage de 100 à 1 000 μM avec les équations linéaires de I (μA) = 0,0322 C + 26,422 (R 2 = 0.9995) et I (μA) = 0,13757C + 6,80312 (R 2 = 0,999) pour le nitrite et l'iodate, respectivement. Plus important encore, la détection de nitrite et d'iodate par PEDOT/Au/GO/GCE présente une réponse échelonnée et une réponse de courant idéale pour la détection électrochimique de nitrite et d'iodate avec le chargement d'une petite quantité de composite (5 μL à partir de 30 mg/L) sur électrode de carbone vitreux. En outre, la limite de détection basse est estimée à 0,53 μM et 0,62 μM (S/N = 3) pour le nitrite et l'iodate, respectivement.
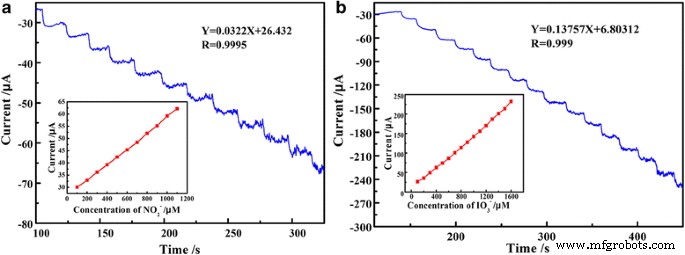
Réponse courant-temps catalytique en régime permanent de PEDOT/Au/GO/GCE avec ajout successif de 1,0 × 10 −3 M nitrite (a ) et iodate (b )
Les comparaisons des paramètres de détection de nitrite et d'iodate par diverses électrodes modifiées chimiquement sont répertoriées dans le tableau 1. Les résultats de comparaison montrent que la réponse de l'électrode modifiée PEDOT/Au/GO/GCE a un courant inférieur (9,59 μA) à celui (17,5 μA) de MWNT-PAMAM-Chit en plus de 10 μM de nitrite. Cependant, la réponse actuelle de PEDOT/Au/GO/GCE pour l'ajout de 10 μM de nitrite est supérieure à celle (0,3 μA) de Nano-Au/P3MT/GCE. De plus, la réponse actuelle du composite PEDOT/Au/GO est de 11,47 μA pour l'ajout de 10 μM d'iodate, ce qui donne également une meilleure preuve que l'électrode modifiée PEDOT/Au/GO/GCE est appropriée [25] pour la détection de iodate.
La figure 10 montre que l'électrode modifiée composite PEDOT/Au/GO/GCE confère une plus grande stabilité aux mesures ampérométriques de l'analyte (1,0 mM de nitrite ou 1,0 mM d'iodate) au cours d'une expérience prolongée de 1000 s. La réponse reste stable tout au long de l'expérience, indiquant l'absence d'effet inhibiteur de l'iodate et de ses produits de réduction pour la surface d'électrode modifiée. Cependant, par rapport à l'iodate, la réponse reste instable dans le cas du nitrite.
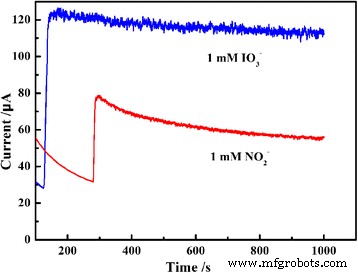
Une ampérométrie enregistrée de PEDOT/Au/GO/GCE dans 1 mM de nitrite (a ) et iodate (b ) pendant une longue période de 1000 s
La figure 11 montre les mécanismes du transfert direct d'électrons entre l'ion (nitrite ou iodate) et le GCE (électrode de carbone vitreux) à travers le composite PEDOT/Au/GO/GCE. Comme le montre la figure 11, le PEDOT de type schiste peut s'incorporer au GO pour former une structure lamellaire, ce qui peut conduire à une grande surface pour une distribution uniforme des nanoparticules d'Au. De plus, les électrons générés conduiront à GCE via le chemin de résistance le plus court à travers un GO hautement conducteur dispersé dans un composite, comme illustré à la Fig. 11. Cependant, sans GO, les électrons devront passer par le milieu PEDOT, qui a une résistance considérable qui provoque des chute de potentiel et taux de transfert d'électrons beaucoup plus faible. Par conséquent, GO joue un rôle important en facilitant l'échange d'électrons entre l'ion (nitrite ou iodate) et le GCE car il forme une matrice conductrice conduisant à des chemins de résistance électrique réduits.
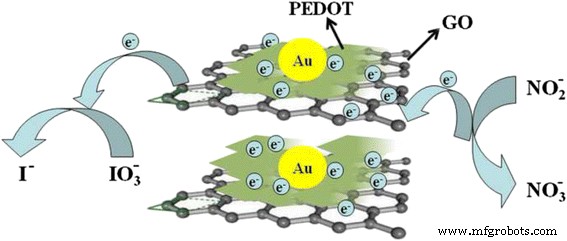
Mécanismes du transfert direct d'électrons entre l'ion (nitrite ou iodate) et le GCE à travers le composite PEDOT/Au/GO
Analyse d'échantillons réels
Afin de valider/tester l'application pratique de l'électrode modifiée, le PEDOT/Au/GO/GCE a été appliqué pour la détection de la concentration de nitrite dans l'eau du robinet avec la méthode d'addition standard. Un certain volume d'échantillons a été ajouté à la cellule électrochimique pour la détermination du nitrite par dosage ampérométrique. Comme le montre le tableau 2, le taux de récupération de l'échantillon variait de 98,4 à 104,3 %. Par conséquent, le PEDOT/Au/GO/GCE pourrait être utilisé pour la détection de nitrite dans l'échantillon d'eau.
Conclusion
Un composite ternaire de PEDOT/Au/GO pour un capteur électrochimique prometteur a été synthétisé par la méthode de chauffage à l'état solide. Les résultats ont révélé que la morphologie de type schiste du PEDOT pourrait apporter une possibilité de formation de structures lamellaires à partir de l'incorporation de PEDOT dans la matrice GO, ce qui pourrait conduire à une grande surface pour une distribution uniforme des nanoparticules d'Au. Par conséquent, l'effet synergique entre les nanoparticules PEDOT, GO et Au ainsi que la grande surface de contact du composite ont conduit le composite PEDOT/Au/GO à afficher une forte activité électrocatalytique vers l'oxydation du nitrite et la réduction de l'iodate. Et les réponses actuelles de la détection de nitrite et d'iodate étaient suffisamment élevées pour obtenir une réponse progressive évidente. De plus, le composite PEDOT/Au/GO avait une réponse de courant idéale pour la détection électrochimique du nitrite et de l'iodate avec le chargement d'une petite quantité de composite (5 μL à partir de 30 mg/L) sur une électrode en carbone vitreux.
Nanomatériaux
- Avancées et défis des nanomatériaux fluorescents pour la synthèse et les applications biomédicales
- Composites de graphène et polymères pour applications de supercondensateurs :une revue
- Composite hybride nanostructuré silice/or-cellulose Amino-POSS par procédé Sol-Gel et ses propriétés
- Synthèse de points quantiques de type II/Type-I à suppression de réabsorption ZnSe/CdS/ZnS Core/Shell et leur application pour le dosage immunosorbant
- Synthèse d'un composite de nanofibres de silice/nanoparticules d'or conductrices d'électricité par impulsions laser et technique de pulvérisation
- Synthèse et propriétés électrochimiques des matériaux cathodiques LiNi0.5Mn1.5O4 avec dopage composite Cr3+ et F− pour batteries lithium-ion
- Synthèse de nanocristaux de ZnO et application dans des cellules solaires polymères inversées
- Évaluation des structures graphène/WO3 et graphène/CeO x en tant qu'électrodes pour les applications de supercondensateurs
- A Resumable Fluorescent Probe BHN-Fe3O4@SiO2 Hybrid Nanostructure for Fe3+ and its Application in Bioimaging



