Électrodes sans liant et leur application pour les batteries Li-Ion
Résumé
Les batteries lithium-ion (LIB) en tant que systèmes d'approvisionnement et de stockage d'énergie ont été largement utilisées dans l'électronique, les véhicules électriques et les réseaux de distribution. Cependant, il existe une demande croissante pour améliorer la densité énergétique du LIB. Par conséquent, le développement de nouveaux matériaux d'électrode à haute densité énergétique devient important. Bien que de nombreux nouveaux matériaux aient été découverts, des problèmes subsistent tels que (1) le problème d'interaction faible et d'interface entre le liant et le matériau actif (oxyde métallique, Si, Li, S, etc.), (2) un grand changement de volume, (3 ) une faible conductivité ion/électron, et (4) l'auto-agrégation des matériaux actifs pendant les processus de charge et de décharge. Actuellement, l'électrode sans liant est un candidat prometteur pour résoudre les problèmes ci-dessus. Tout d'abord, le problème d'interface du liant et des matériaux actifs peut être résolu en fixant le matériau actif directement sur le substrat conducteur. Deuxièmement, la grande expansion volumique des matériaux actifs peut être compensée par la porosité de l'électrode sans liant. Troisièmement, la conductivité ionique et électronique peut être améliorée par le contact étroit entre le substrat conducteur et le matériau actif. Ainsi, l'électrode sans liant présente généralement d'excellentes performances électrochimiques. Le processus de fabrication traditionnel contient des liants électrochimiquement inactifs et des matériaux conducteurs, ce qui réduit la capacité spécifique et la densité énergétique des matériaux actifs. Lorsque le liant et le matériau conducteur sont éliminés, la densité énergétique de la batterie peut être largement améliorée. Cette revue présente la préparation, l'application et les perspectives des électrodes sans liant. Tout d'abord, différents substrats conducteurs sont introduits, qui servent de supports pour les matériaux actifs. Elle est suivie par la méthode de fabrication d'électrodes sans liant du point de vue de la chimie, de la physique et de l'électricité. Par la suite, l'application de l'électrode sans liant dans le domaine de la batterie souple est présentée. Enfin, les perspectives en termes de modes de traitement et d'applications sont fournies.
Introduction
La crise énergétique et les problèmes environnementaux ont conduit au développement des énergies renouvelables et de nouveaux systèmes de stockage d'énergie respectueux de l'environnement. En raison du problème intermittent des sources d'énergie renouvelables telles que l'énergie éolienne, l'énergie hydraulique et l'énergie solaire, les batteries sont considérées comme des systèmes de stockage d'énergie importants [1,2,3]. Il existe une demande croissante pour des dispositifs de stockage d'énergie fiables et efficaces. Les batteries lithium-ion (LIB) ont attiré beaucoup d'attention en raison de leur haute densité d'énergie et de puissance, leur tension de cellule élevée, leur large plage de températures de fonctionnement et leur longue durée de vie [4]. De nos jours, le procédé traditionnel de préparation de la batterie utilise un polyfluorure de vinylidène (PVDF) comme liant pour fixer l'agent conducteur et les matières actives sur le collecteur de courant par une méthode de revêtement [5, 6]. Avec la demande pour les LIB avec une capacité plus élevée et une taille plus petite, le développement de matériaux actifs avec une capacité spécifique élevée et la réduction des matériaux inactifs dans la cellule sont importants. Les méthodes pour réduire les matières inactives sont les suivantes. Premièrement, le liant traditionnel peut être remplacé par le liant conducteur, par exemple un polymère à base de pyrène et un polymère conjugué au polyfluorène. Ces polymères sont naturellement conducteurs et leur chaîne latérale ou squelette est modifié pour augmenter l'adhérence [7,8,9,10]. Le liant conducteur sert d'agent conducteur. Par conséquent, l'utilisation de charbon inactif dans la cellule peut être réduite. Cependant, la faible interaction interfaciale entre ces liants (à la fois le PVDF et les nouveaux liants développés) et les matériaux actifs (oxyde métallique, Si, Sn, Li, S, etc.) entraîne l'auto-agrégation ou/et l'isolement des particules du collecteur de courant. Par conséquent, ces nouveaux matériaux à haute capacité présentent des performances de batterie réduites [11,12,13,14,15]. Deuxièmement, des substrats conducteurs avancés, tels que le tissu de carbone, le graphène et la mousse de Ni, sont étudiés, où les matériaux actifs peuvent être ancrés sur les sites d'adhésion spéciaux des substrats. Les adhérences entre les matériaux actifs et les substrats sont obtenues par une forte liaison chimique et/ou physique, ce qui améliore considérablement l'intégrité des électrodes. De plus, ce processus élimine potentiellement à la fois le liant et les additifs de carbone conducteur. Par conséquent, la densité énergétique peut être largement améliorée [16, 17] (Fig. 1).
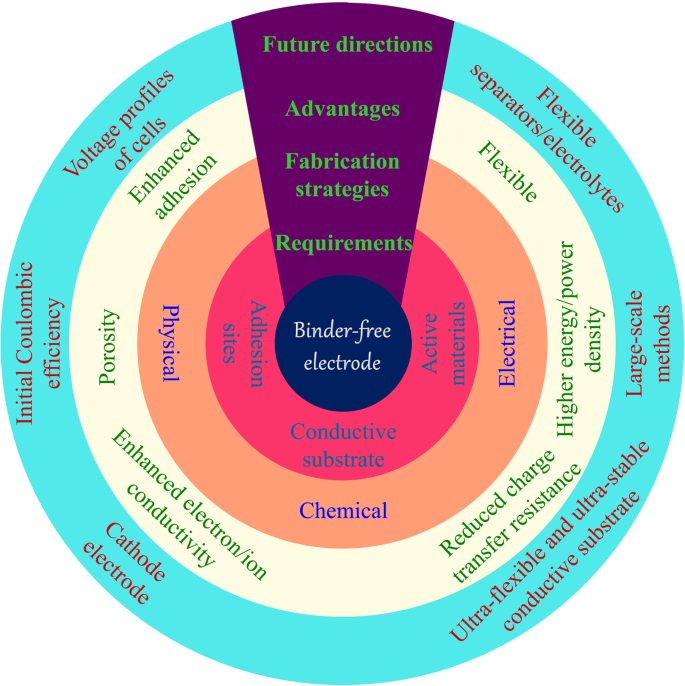
Les exigences, les méthodes de fabrication, les avantages et le développement futur de l'électrode sans liant
De nombreuses recherches ont démontré les nombreux avantages des électrodes sans liant [18,19,20,21]. En immobilisant les matériaux actifs sur le substrat conducteur d'électrons correspondant, le problème interfacial du liant et des matériaux actifs peut être résolu en raison de l'absence de revêtement de liant organique sur la surface des matériaux actifs [22, 23]. Les matériaux actifs adhèrent fermement au substrat conducteur, ce qui améliore fortement la conductivité électronique. Les propriétés des matériaux de support, par exemple les structures poreuses, facilitent la pénétration des électrolytes et la diffusion des ions [24]. En outre, la grande surface présente l'avantage d'une utilisation complète des matériaux actifs et du transport des Li-ions. De plus, le matériau actif est généralement uniformément ancré sur le substrat conducteur, ce qui peut empêcher efficacement l'agglomération des nanoparticules et réduire l'expansion de volume lors du processus de cyclage répété. Les électrodes sans liant présentent généralement un Li + élevé et conductivité électronique, mouillabilité décente de l'électrolyte et espace d'expansion de grand volume, et forte force de liaison. Par conséquent, les électrodes sans liant présentent de meilleures performances de capacité, de cyclage et de débit que le système PVDF/matériaux actifs/noir de carbone. Plus précisément, la durée de vie des nouveaux nanomatériaux est passée de dizaines de cycles à des centaines de cycles, avec une densité de courant élevée de ~ 10 A g −1 .
Le substrat conducteur en tant que support pour le matériau actif est la base de l'électrode sans liant. La matrice conductrice doit disposer de sites adaptés à la croissance des matériaux actifs, et ses propriétés mécaniques jouent un rôle déterminant dans son application. Pour les applications des électrodes dans les dispositifs électroniques portables et flexibles, les substrats conducteurs doivent pouvoir être pliés ou même pliés plusieurs fois. Ceci est difficile à réaliser dans les électrodes conventionnelles fabriquées par le procédé en suspension. La raison principale est que le matériau actif est séparé du collecteur de courant pendant le processus de pliage, ce qui entraîne la désactivation de la batterie. La croissance des matériaux actifs directement sur un réseau flexible fournit une interaction forte et conduit à des électrodes robustes maintenant la densité d'énergie élevée. Ces substrats flexibles comprennent principalement de la mousse métallique, du tissu de carbone et des films autoportants de matériaux de carbone [25].
Cette revue vise à fournir un aperçu de la préparation, de l'application et des perspectives des électrodes sans liant pour les LIB. Notre objectif est de mettre en évidence le développement récent et l'amélioration des électrodes sans liant [26]. Les méthodes de coulée et d'infiltration de la racle, qui sont sans aucun doute importantes dans le domaine des LIB, ne seront pas incluses. Tout d'abord, nous introduisons les différents substrats conducteurs, qui servent principalement de supports pour les matériaux actifs. Nous suivrons avec une présentation sur la méthode de fabrication d'électrodes sans liant du point de vue de la chimie, de la physique et de l'électricité. Par la suite, l'application de l'électrode sans liant dans le domaine de la batterie souple est présentée. Enfin, les enjeux clés concernant ces méthodes de préparation et leurs applications sont prospectés.
Substrat conducteur
Le substrat conducteur est le collecteur de courant avec une bonne conductivité électronique. Par conséquent, le matériau est généralement composé de métal ou de matériau carboné. En raison des limitations de fabrication, les collecteurs de courant métalliques sont généralement fabriqués en films, en treillis [27] et en mousses [28]. Les produits métalliques sont généralement rigides et ne se récupèrent pas facilement après déformation; par conséquent, ils ne conviennent qu'aux batteries à haute densité énergétique de la même configuration que les batteries à base de boue. Le cuivre et l'aluminium sont utilisés comme collecteur de courant négatif et positif, respectivement, en raison de la résistance à l'oxydation différente [29]. La mousse métallique présente les avantages d'un poids léger, d'une grande surface, d'une structure tridimensionnelle, etc., qui est souvent utilisée pour les électrodes sans liant [30].
Les matériaux carbonés proviennent de diverses sources et sont très flexibles dans leur préparation [31]. Ces matériaux peuvent être dérivés d'une grande variété de matériaux biologiques dans la nature, ainsi que de nanotubes de carbone préparés chimiquement, de graphène et de structures de carbone poreuses à partir de matériaux organiques [17, 32]. Par rapport au métal, certains types de matériaux en carbone sont plus légers et ont une grande flexibilité (flexibles, pliables, etc.). Le tissu de carbone est de plus en plus utilisé dans le stockage d'énergie en raison de son excellente conductivité électrique et de sa flexibilité [33].
Méthodes chimiques
Traitement Thermique
Le traitement thermique est l'une des méthodes courantes de préparation d'une électrode sans liant. Cette méthode consiste à modifier les propriétés physiques et chimiques du matériau au moyen d'un processus de chauffage et de refroidissement. Après traitement thermique, le sel inorganique est converti en l'oxyde métallique correspondant et le polymère se déshydrate pour former une structure conductrice de carbone (Fig. 2). Pour la préparation d'électrodes sans liant, un traitement thermique est généralement utilisé pour immobiliser la matière active ou pour construire un squelette autoporteur.
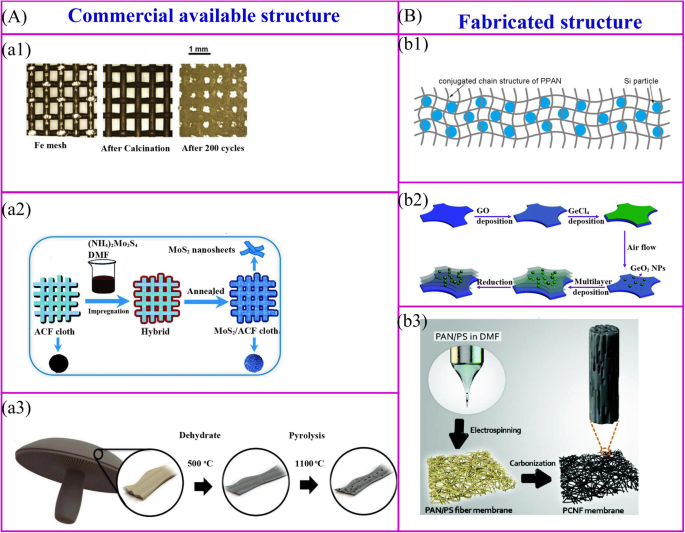
Traitement thermique de la structure disponible dans le commerce (a ) et structure fabriquée (b ). a1 Des nanoparticules d'oxydes métalliques peuvent être obtenues à la surface d'une structure métallique via une simple progression d'oxydation thermique [34]. a2 Les matériaux actifs peuvent être synthétisés à la surface de la structure conductrice par traitement thermique [35]. a3 La biomasse peut être carbonisée pour réaliser l'architecture du carbone [32]. b1 Le mélange de polymère et de matières actives peut être carbonisé pour obtenir l'électrode sans liant [36]. b2 La structure hiérarchique peut être obtenue par de multiples processus [37]. b3 L'électrode sans liant peut être obtenue par traitement thermique de la membrane d'électrofilage [38]
La structure disponible dans le commerce est utilisée comme squelette de support pour immobiliser les matériaux actifs. Ces matériaux sont constitués de treillis métalliques, de fibres de carbone, d'éponges commerciales et de dérivés biologiques et d'éponges commerciales [39], etc. (Fig. 2a). Des nanoparticules d'oxydes métalliques peuvent être synthétisées à la surface de collecteurs de courant métalliques par simple progression d'oxydation thermique [34] (Fig. 2a1). Sans autre traitement, ces collecteurs de courant peuvent être utilisés directement comme matériaux de support pour les LIB sans liant. Fe2 soutenu par un treillis de fer O3 montre une capacité de décharge très élevée de 1050 mAh g −1 après 200 cycles. Le traitement thermique de la membrane conductrice avec une solution de précurseur de matériaux actifs est une méthode largement développée pour la fabrication d'électrodes sans liant (Fig. 2a2). Un exemple représentatif est que le MoS ultramince2 les nanofeuilles revêtues à la surface d'un tissu en fibre de carbone actif (ACF) peuvent être fabriquées par immersion dans le (NH4 )2 MoS4 solution suivie d'un recuit. Les performances électrochimiques sont démontrées que la capacité de décharge de 971 mAh g −1 est atteint à une densité de courant de 100 mA g −1 [35]. Le traitement thermique des matériaux de biomasse est une méthode simple pour la préparation d'électrodes sans liant. Ozkan et ses collègues ont carbonisé le champignon portobello sous forme d'anodes LIB sans liant (Fig. 2a3) [32]. À haute température, la structure des matériaux de biomasse peut être conservée et les hétéroatomes et ions métalliques naturellement présents peuvent se doper dans les matériaux carbonés, ce qui augmente les performances électrochimiques telles que la conductivité et la capacité électroniques.
Le polymère est le matériau principal pour la construction du squelette autoportant de l'électrode sans liant, et la structure du squelette est déterminée par le polymère et sa méthode de préparation (Fig. 2b) [40]. Premièrement, pour les polymères courants, la pyrolyse d'un film composite de matériaux polymères actifs à 550 °C permet de préparer une électrode sans liant (Fig. 2b1) [36]. Le Si/SiOx L'électrode composite /PAN est préparée par cette méthode [41, 42]. Après recuit, le polyacrylonitrile (PAN) peut être converti en structure conductrice dopée N, et le réseau de carbone stabilise non seulement le SEI et s'adapte aux changements de volume, mais offre également une bonne flexibilité et une bonne résistance mécanique à l'électrode. De même, l'électrode Si/rGO peut être obtenue en coulant une suspension de Si, d'oxyde de graphène réduit (rGO) et de polyvinylpyrrolidone (PVP) sur une mousse de nickel suivie d'un processus de recuit [43]. Deuxièmement, le processus couche par couche (LBL) est un moyen attrayant de fabriquer des structures et des nanomatériaux complexes. Une électrode à plusieurs couches peut être fabriquée en immergeant la feuille de Ti dans une solution de poly (chlorure de diallyldiméthylammonium) (PDDA), une suspension d'oxyde de graphène (GO), une solution de PDDA et une solution aqueuse de H3 PMo12 O40 à certains cycles, puis suivi d'un traitement thermique à 500 °C [44]. Une telle méthode LBL peut être appliquée pour préparer une électrode sans liant à grande échelle. Ce type de méthode est adapté à la fabrication d'anatase mésoporeuse TiO2 /mousse de nickel [45], MoS2 nanofeuille/ACF et multicouche GeO2 /rGO (Fig. 2b2) [37, 46]. Enfin, des électrodes sans liant peuvent être fabriquées par encapsulation de matériaux actifs dans des polymères, puis fabrication en une nouvelle nanostructure (Fig. 2b3). Des tapis de nanofibres hiérarchiques flexibles peuvent être synthétisés par électrofilage et traitement thermique ultérieur.
Les structures fabriquées et disponibles dans le commerce présentent de nombreux avantages. Le matériau actif est enduit sur la surface de la structure disponible dans le commerce tandis que la structure fabriquée agit comme un conteneur pour encapsuler le matériau actif. Contrairement à l'encapsulation de matériaux actifs, le revêtement de surface rend le plus de contacts entre les matériaux actifs et l'électrolyte. Par conséquent, il en résulte une meilleure performance de débit mais une efficacité coulombienne initiale inférieure et de mauvaises performances de cyclisme.
Traitement hydrothermal
La méthode hydrothermale est largement utilisée dans différentes disciplines au cours des dernières décennies. Actuellement, cette technique a fait de gros efforts en termes d'interprétation de mécanismes et de fabrication de matériaux. Pour le processus hydrothermal, les ions métalliques sont dissous dans la solution qui forme ensuite une solution sursaturée à haute température et pression. Au cours de ce processus, la croissance cristalline se produit au point de nucléation du substrat. Par rapport aux particules agrégées préparées par traitement thermique, la méthode hydrothermale peut produire des matériaux nanométriques hautement purs, uniformes, monodispersés et contrôlables dans des conditions douces. Le processus hydrothermal de la nanostructure fine a attiré une large attention dans les matériaux de stockage d'énergie.
Un processus synthétique global pour la préparation de l'électrode sans liant utilisant la méthode hydrothermale est similaire à la procédure décrite sur la figure 3a. Les matériaux de support sont d'abord obtenus. Si les matériaux supports sont lisses avec des points de nucléation limités, le dépôt de matériaux actifs à leur surface serait interdit. Généralement, le tissu de carbone a besoin d'un traitement acide ou thermique pour devenir plus hydrophile. Par ailleurs, le pH de la solution doit être ajusté en ajoutant un précipitant approprié pour favoriser la croissance du précurseur à la surface du substrat. Les matériaux obtenus sont traités thermiquement pour obtenir le composite souhaité tout en conservant la nanostructure. Hu, Zhang et leurs collègues ont signalé une méthode évolutive pour la préparation de Znx Co3-x O4 nanocubes/CNF (nano-fibres de carbone, CNF). La taille du cube peut être ajustée par le pH appliqué dans le processus hydrothermal [47].
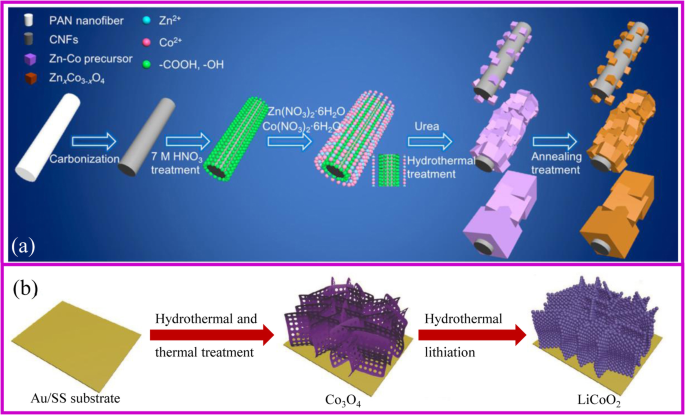
un Le schéma de ZnCoOx /Fabrication composite CNF [47]. b La fabrication d'électrode cathodique par méthode hydrothermale [48]
La méthode hydrothermale permet de fabriquer des composants simples et multiples [49]. De nombreuses morphologies d'électrodes sans liant ont été développées, telles que TiO2 nanotiges sur échafaudage de nanotubes de carbone (CNT) [50], Fe3 O4 nanoparticules, NiO nanocônes, Ni(OH)2 nanofeuillets et Fe3 O4 /Ni/C nanoplaques cultivées sur mousse Ni [51,52,53,54], MnO2 nanoflocons sur mousse de graphène [55], et FeF3 ·0.33H2 O tableaux en forme de fleur sur fibre de carbone [56]. Li et ses collègues ont développé NiCo2 S4 réseaux de nanotubes présentant une structure 3D unique, dans laquelle NiCo2 S4 les nanotubes présentent une longueur de 5 nm et une largeur de 100 nm [57]. NiCo poreux2 O4 les nanoaiguilles cultivées sur un réseau de graphène 3D peuvent être obtenues en utilisant NiCl2 ·6H2 O et CoCl2 ·6H2 O comme précurseurs [58]. Ces nanostructures se répartissent de manière homogène sur le substrat conducteur. Par conséquent, ces composites facilitent non seulement le transfert d'électrons et s'adaptent aux changements de volume des matériaux actifs pendant le processus de décharge/charge, mais améliorent également les propriétés électrochimiques avec une capacité élevée, une capacité de débit élevée et une stabilité de cycle pour les LIB. Plus précisément, Fe3 O4 La mousse nanoparticle@Ni a montré une capacité réversible de 543 mA h g −1 à la densité de courant de 10 C après plus de 2000 cycles [51]. NiO arrays@Ni foam peut fournir une capacité de 969 mAh g −1 à la densité de courant de 0,5 C et restent toujours environ 605,9 mAh g −1 à 10 C [52].
Il convient de noter que la méthode hydrothermale est une bonne stratégie pour réaliser la lithiation des oxydes métalliques pour les matériaux cathodiques. La lithiation classique nécessite un mélange uniforme du précurseur avec le sel de Li, ce qui est tout à fait difficile pour obtenir les électrodes sans liant souhaitées. La lithiation hydrothermale est une méthode de solution qui ne nécessite pas le traitement du précurseur, c'est donc l'une des méthodes intéressantes pour fabriquer l'électrode cathodique sans liant. En 2018, Xia et al. préparé le poreux LiCoO2 cathode sans liant avec de l'acier inoxydable revêtu d'Au comme substrats par la lithiation hydrothermale de Co3 O4 précurseur (Fig. 3b) [48]. Cette électrode présente d'excellentes performances de débit et de cyclage avec une capacité de 104,6 mA h g −1 à un taux de 10 C et la rétention de capacité de 81,8% après 1000 cycles.
Dépôt de bain chimique
Le dépôt en bain chimique (CBD) est un processus de croissance in situ de matériaux actifs sur le substrat par une réaction chimique. Comparée à la méthode hydrothermale, cette méthode de synthèse est facile à étendre et permet aux nanomatériaux de croître à basse température et pression ambiante sans utiliser d'équipement spécial. En outre, le CBD et la méthode hydrothermale font pousser des matériaux à la surface des substrats via un mécanisme similaire, de sorte que les exigences pour les substrats sont très similaires. De la même manière que pour la procédure illustrée sur la figure 4a, le précurseur des matières actives nucléerait et se développerait en ajustant le pH et la température des réactions. Par exemple, graphène 3D/MnO2 les hybrides sont préparés par la présence d'aérogel de graphène 3D dans l'acide KMnO4 solution [59].
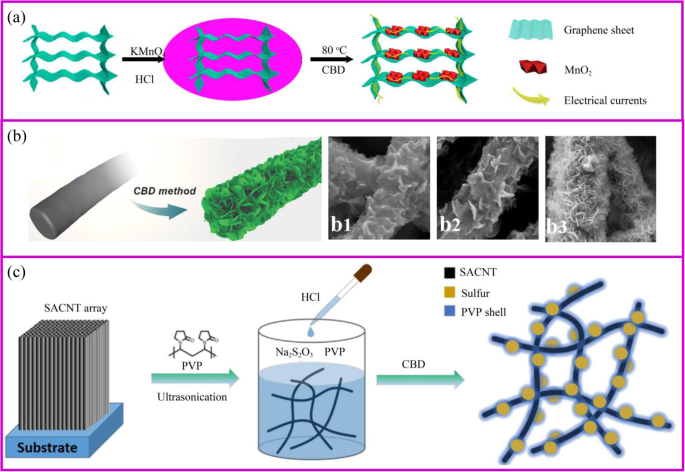
un Illustration schématique de la préparation du graphène 3D/MnO2 hybride, et illustrations de transfert d'électrons sur graphène 3D/MnO2 hybride [59]. b Méthode CBD pour la fabrication de CNF@Ni(OH)2 [60]. b1–3 Différentes membranes hybrides avec augmentation des concentrations de Ni(NO3 )2 Solution. c Schéma de la procédure de synthèse du composite PVP@S-SACNT [61]
La morphologie des matériaux actifs est influencée par les matériaux de support, le temps de réaction et la concentration en précurseurs (Fig. 4b). Le substrat détermine les sites de nucléation initiaux. Par exemple, la morphologie de MnO2 est nanofeuillet et nanoparticule sur le substrat de graphène et de NTC, respectivement [62, 63]. De plus, la morphologie des matériaux actifs sur le matériau support est influencée par la concentration en précurseur. Par exemple, mince Ni(OH)2 les nanofeuillets commencent à se former et à croître perpendiculairement à la surface des nanofibres à faible teneur en Ni(NO3 )2 concentration (Fig. 4b) [60]. Cependant, avec l'augmentation des concentrations de sel de Ni, une couche épaisse de Ni(OH)2 des nanofeuillets se forment progressivement, ce qui peut être attribué à la nucléation rapide et homogène de Ni(OH)2 . Par conséquent, la morphologie des matériaux actifs sur le matériau support peut être variée, comme les particules [64], la gaine, la nanofeuille [65] et les nanofils [66, 67]. Semblable à l'électrode préparée par méthode hydrothermale, l'architecture poreuse et conductrice avec des matériaux à l'échelle nanométrique peut fournir des canaux continus pour une diffusion rapide des ions lithium et un transport efficace des électrons pour une lithiation/délithiation rapide.
Le soufre, un matériau cathodique très prometteur, peut être synthétisé par le CBD dans des conditions douces. Le matériau soufré est basé sur une simple réaction entre Na2 S2 O3 et des acides en solution aqueuse à température ambiante. Le processus est simple et respectueux de l'environnement. Lorsqu'un modèle ou un tensioactif approprié est appliqué, la structure nano-soufre spéciale peut être obtenue [68]. Lorsque les matériaux conducteurs peuvent absorber S2 O3 2- , une grande quantité de soufre est générée aux interphases. Le graphène modifié par des groupes fonctionnels phénylsulfonés permet le dépôt uniforme de soufre via une réaction redox in situ [69]. L'électrode de soufre encapsulée dans du PVP sans liant est préparée en immobilisant in situ les nanoparticules de soufre sur le réseau conducteur (Fig. 4c). Le PVP est un polymère amphiphile avec une chaîne alkyle hydrophobe et des groupes amides hydrophiles qui peuvent être utilisés comme agent dispersant. Lorsque le soufre commence à se former après l'ajout d'acide dans la solution, la nature hydrophobe du PVP le fait enduire préférentiellement sur la surface S formant une couche dense pour protéger la dissolution des polysulfures [61].
Dépôt chimique en phase vapeur
Le dépôt chimique en phase vapeur (CVD) est une réaction chimique au cours de laquelle une substance gazeuse se dépose à la surface d'un substrat chaud. Cette méthode permet de produire le film uniforme sur la structure tridimensionnelle et les nanofils à l'aide de catalyseurs. Le procédé CVD comprend trois étapes :(1) diffusion et absorption des gaz de réaction à la surface du substrat chaud, (2) réactions des gaz sur le site actif pour former un matériau de revêtement, et (3) échappement du gaz généré. En contrôlant la température, la pression, le rapport et le type de gaz, le matériau de revêtement souhaité peut être obtenu.
La méthode CVD permet de cultiver directement des matériaux actifs. Un exemple impressionnant correspondant au processus CVD a été rapporté par Tay et ses collaborateurs [70]. Le composite mousse de nickel 3D/NTC est synthétisé avec de la mousse de nickel comme substrat et de l'éthanol à la fois comme précurseur et source de carbone. Les NTC obtenus servent de substrats pour le dépôt de croissance de nanofeuillets NiO. FeVO amorphe4 les matrices de nanofeuilles peuvent se développer directement sur un substrat flexible en acier inoxydable avec VCl3 comme précurseur. Il peut délivrer des capacités réversibles de 601 mAh g −1 et 453 mAh g −1 à la densité de courant élevée de 8 C et 15 C, respectivement [71].
Les couches superficielles préparées par CVD servent également d'interfaces protectrices entre l'électrode et l'électrolyte. Yang et ses collègues ont utilisé l'éthylène comme précurseur de carbone pour enrober les matériaux actifs par un procédé CVD, qui non seulement améliore la stabilité de la structure mais forme également un excellent réseau conducteur électronique. Les nanofils de Si avec une couche de revêtement de carbone montrent une bonne performance de débit [72, 73]. En 2016, Cui et al. ont montré que les matériaux poreux avec une fine couche de matériaux lithiophiles préparés par la méthode CVD peuvent servir d'échafaudage favorisant le dépôt uniforme de Li-ion [74]. Ce matériau présente des performances de cyclisme stables avec une petite surtension même à une densité de courant élevée de 3 mA/cm 2 pendant les processus de charge et de décharge.
La méthode CVD est l'une des principales stratégies pour la fabrication de matériaux Si avancés. Le silicium est le matériau d'anode le plus prometteur pour les LIB de prochaine génération en raison de la capacité spécifique la plus élevée de 4200 mAh g −1 et une faible tension de fonctionnement [75]. Cependant, le silicium souffre d'énormes changements de volume, ce qui conduit à la formation continue d'une interface d'électrolyte solide (SEI), à la pulvérisation et à la décoloration de la capacité au cours des processus de cyclage [76]. En général, les matériaux de silicium avancés peuvent être préparés par post-traitement de particules de silicium ou par réduction de dioxyde de silicium. Le CVD est un moyen souhaitable de préparer un film mince ou un nanofil de silicium en réduisant ou en pyrolysant des substituts de silane ou de silane de haute pureté. En 2008, Cui et al. utilisé la méthode CVD pour synthétiser des nanofils de silicium (Si NWs) sur l'acier inoxydable avec des nanoparticules d'Au comme catalyseurs et l'a appliquée avec succès comme anode pour les LIBs [77]. Les nanofils de silicium d'un diamètre d'environ 89 nm peuvent s'adapter à un changement de volume de 400 % sans se fissurer. De plus, les nanofils sont directement développés sur le collecteur de courant, et tous les nanofils contribuent activement à la capacité. En raison de la nanostructure, l'ensemble de l'électrode poreuse a une très grande surface spécifique et a donc une excellente conduction ionique. Le matériau de silicium nanofil peut atteindre une capacité théorique de près de 4200 mAh g −1 pour la première fois au taux C/20. Bien que le diamètre des nanofils soit passé de 89 à 141 nm après le processus de cyclage, la structure globale est restée intacte. La croissance de Si est contrôlée par les catalyseurs. L'acier inoxydable peut également agir comme catalyseur pour la formation d'un film de Si. Cependant, la formation de couches de Si sur le collecteur de courant peut provoquer de fortes contraintes entre la couche de Si et le collecteur. La croissance de Si peut être interférée à une certaine étape en contrôlant les germes actifs. Par exemple, la surface de graphène ou de métal Ge chimiquement stable avec des nanoparticules d'Au ou de Sn peut servir de germe pour la croissance de Si NWs [78, 79].
Dépôt de couche atomique
La méthode de dépôt par couche atomique (ALD) est un dépôt en phase vapeur, auto-limitant et couche par couche, qui est similaire au CVD. Cette méthode peut produire des films minces à l'échelle nanométrique et contrôlables dans un dépôt atomique couche par couche. Par conséquent, le processus doit consister en au moins deux gaz précurseurs différents, qui peuvent réagir l'un avec l'autre [80]. Au cours du processus ALD, le premier gaz est introduit dans le four tubulaire et réagit avec le substrat pour former une couche de revêtement avec des groupes actifs. Une fois que le premier gaz est entièrement émis, le deuxième gaz est introduit pour réagir avec la première couche (Fig. 5a) [81]. En répétant ce processus, différentes couches de revêtement peuvent être obtenues. Le film de revêtement d'ALD est principalement influencé par le substrat, les précurseurs de gaz, la température, etc. -libres, denses et uniformes mais aussi conformes même lorsqu'ils sont déposés sur des structures 3D complexes. Ces caractéristiques d'ALD en font un excellent choix pour la nanotechnologie et les matériaux.
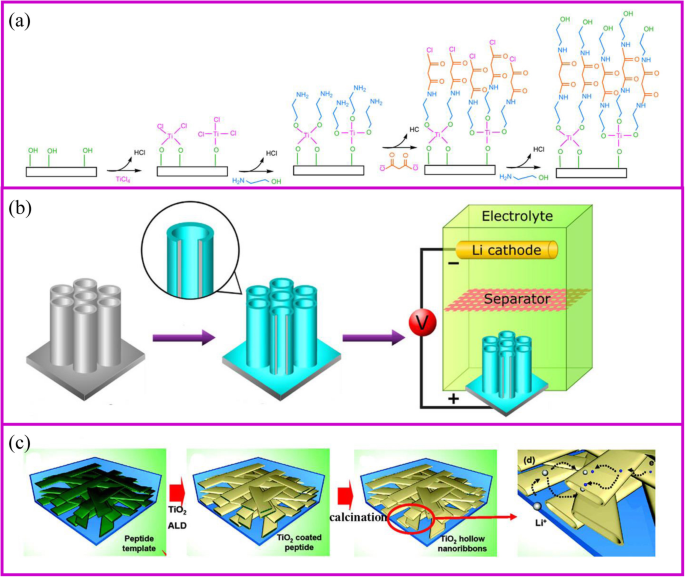
un Le mécanisme de la technique ALD [81], et deux exemples pour b revêtement de surface [82] et c fabrication de matériaux actifs [83]
Les électrodes préparées par ALD ont généralement de bonnes propriétés électrochimiques. TiO2 est le matériau d'électrode le plus étudié (Fig. 5b, c) [84]. Récemment, SnO2 [85], MoS2 [86], etc. sont préparés et utilisés avec succès comme matériau actif pour les LIB (Fig. 5c) [87, 88]. Parce que l'ALD est une méthode de synthèse en phase vapeur, elle peut recouvrir une couche uniforme avec une épaisseur contrôlable sur la surface ou à l'intérieur des pores des matériaux. Kang et ses collaborateurs [83] ont démontré que les nanorubans en tant que matériaux actifs dans les électrodes permettent à l'électrolyte d'être immergé à l'intérieur du matériau, augmentant ainsi considérablement le taux de diffusion des ions lithium. À l'aide d'un modèle, l'espace creux des nanorubans peut être synthétisé par ALD avec une taille de tunnel de près de 100 à 200 nm de largeur et de 20 à 50 nm de hauteur. Il permet à l'électrolyte de mouiller facilement l'espace creux. La performance de taux de TiO2 réseau nanométrique a augmenté au moins cinq fois à 5 C par rapport à celui de 100 nm-TiO2 nano-poudre. Biener et al. électrode poreuse revêtue de TiO2 couches. On constate que le matériau avec une couche de revêtement plus mince montre une meilleure performance de taux. Lorsque le TiO2 layer thickness increased from 2 to 7 and 20 nm, the capacity decreases from 227 to 214 and 157 mAh g −1 , respectively [89].
The most general application of ALD in electrochemical storage is to protect the surface stability of electrodes to enhance the electrochemical performance [90]. The uniform Al2 O3 coating on TiO2 nanotubes for LIBs is the most representative example of surface protection (Fig. 5a) [82]. The coating thickness of the Al2 O3 layer onto the TiO2 nanotube can be controlled by ALD from 0.2, 1 to 10 nm according to the repeated cycles. The 1 nm coating Al2 O3 layer can suppress the SEI formation and undesirable side reactions, which greatly improves the capacity. In addition, Al2 O3 as an artificial layer can participate in the formation of SEI with Li–Al–O groups, which are great ionic conductor. Therefore, the Li-ion conductivity in improved and great rate performance can be achieved. Noked et al. demonstrated the 14 nm Al2 O3 layer can effectively improve the stability of lithium metal interface by avoiding the reactions with electrolyte, cathode shuttles, etc. [91]. Comparing with the bare lithium metal anode, the ALD-protected anode can significantly improve cycling performance.
Electrical Methods
Electroplating
Electroplating is a versatile technique that functions to improve the surface properties of materials or to prepare nanoscale structures. The deposition mechanism is that in the case of an applied electric field, the ions move to the positive electrode and are reduced on the surface of the substrate to form a film. The thickness of film is controlled by the current density and time. Through post-treatment, the metal film can be oxidized to the corresponding metal oxide.
Template synthesis is the most popular method for preparing nanostructures of various materials using electroplating in LIBs. Chen, Xia, and coworkers obtained porous CoO semisphere arrays using the polystyrene as the template [92]. Yan, Tong, and coworkers demonstrated that CoO can coat on the surface of ZnO nanorod arrays by electroplating method. The ZnO template can be removed by treating the obtained electrode at KOH solution [93].
Electroplated surface layers also serves as a protective interfaces between the electrode and the electrolyte. Cu/TiO2 NT/Ti electrode can be prepared via electroplating Cu on TiO2 NT/Ti film. The prepared materials display a much higher discharge capacity, cycle stability, and Li + diffusion coefficient than bare TiO2 NT/Ti electrode [94]. Mulder et al. designed a 3D Ni honeycomb current collector for stable Li metal anode [95]. By controlling the porosity of Ni material with polyethylene glycol as an additive, the Li plating/stripping performance can prolong to 300 and 200 cycles at 0.5 mAh cm −2 and 1.0 mAh cm −2 , respectively, at 1.0 mA cm −2 .
Anodization
Anodization is a well-established technique for modifying a layer on the metal surface. Generally, the metal surface can be thermal treated to form the corresponding oxide protective layer. However, this heating process often carries out at a high temperature, which changes the material structure and properties. Therefore, it is necessary to develop a low temperature method. Anodization refers to a technique in which a metal material is oxidized and precipitated in the electrolyte solution by applying an anode current at room temperature. Anodization is popular because of its controllable structure, economical, and large-area preparation.
Li et al. firstly reported the porous Fe3 O4 thin film as anode material cycled about 100 cycles at the 0.1 C [96]. Subsequently, TiO2 [97], NiO [98], WO3 [99], CuCl nanoparticles [100], etc. were prepared and showed decent cyclic stability, good ion and electron conductivity, and enhanced capacity. The NiO@Ni foam can deliver a reversible capacity up to 705.5 mAh g −1 and 548.1 mAh g −1 at a current density of 1 A g −1 and 2 A g −1 , respectivement.
Electrophoretic Deposition
Electrophoretic deposition (EPD) has been widely used as a surface coating and film preparation method. The deposition mechanism is that during the process, the charged particles with small sizes (need to disperse into the solution) in a suitable suspension migrate towards an electrode under an applied electric field (Fig. 6a, b). The morphology of the achieved film is significantly influenced by the electrolyte solution [104]. EPD has the advantages of low cost, simplicity, green, and controllable operation [105].
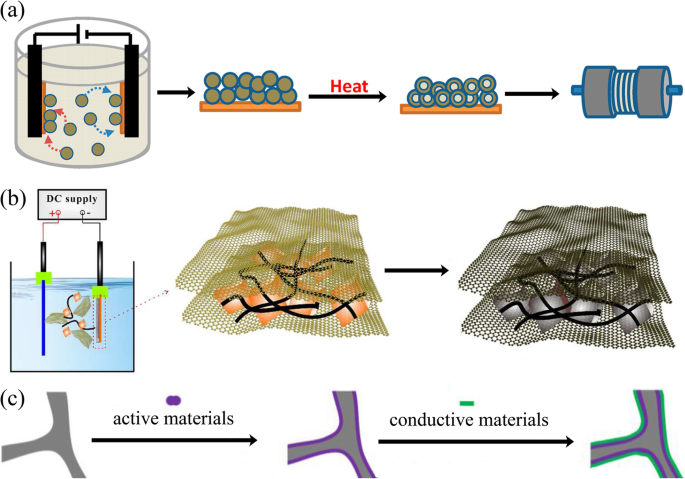
un Schematic of process for fabrication of binder-free, carbon-free film electrodes [101]. b Schematic fabrication process for the Fe3 O4 /CNTs/rGO composite electrode [102]. c Schematic illustration of the synthesis route for rGO/active materials/Ni foam [103]
An electrode made by EPD shows better electrochemical performances than slurry-coated electrode. Robinson and coworkers proved that the Co3 O4 nanoparticle films formed by EPD showed better adhesion and cycle performance than the electrode prepared by conventional methods (Fig. 6a). The EPD can provide a more effective mixed state between active materials and conductive additives [101]. It is worth noting that carbon nanotubes, graphene, and other carbon materials together with active materials can be deposited onto the current collector, which significantly improves the electron conductivity [106, 107]. Besides, the porous structure formed during the EPD process is crucial to accommodate the volume change during lithium-ion insertion and extraction. Zhao and coworkers demonstrated that the Si nanoparticle electrode prepared through EPD shows better electrochemical performance (Fig. 6b) [102, 108].
EPD is able to deposit surface layers composed of either active or inert materials. These layers serve as protective interfaces between the electrode and the electrolyte. For example, the reduced graphene oxide thin film deposited onto the surface of the electrode to improve the electrical conductivity and to buffer the volume changes during charge/discharge processes (Fig. 6c) [103].
Physical Methods
Electrospinning
Electrospinning is a simple and popular technique to synthesize 1D nanostructures with fiber diameters ranged from tens of nanometers up to micrometers [109]. This preparation is difficult to achieve by the approaches mentioned above. This technique can produce polymers, organic, and inorganic composites with dense, hollow, or porous structures [110], from polymer solutions based on electrostatic forces [111]. An electrospinning unit generally consists of a syringe and a needle, a grounded collector, and a high-voltage supply, as shown in Fig. 7a, b [117]. During the electrospinning process, polymer solutions are loaded in the syringe and move into the needle to form a droplet. When a high voltage is applied between the needle and the collector, the electrostatic force at the surface of droplet would drive it to elongate to form a fiber. Finally, the solid polymer fibers would deposit onto the collector.
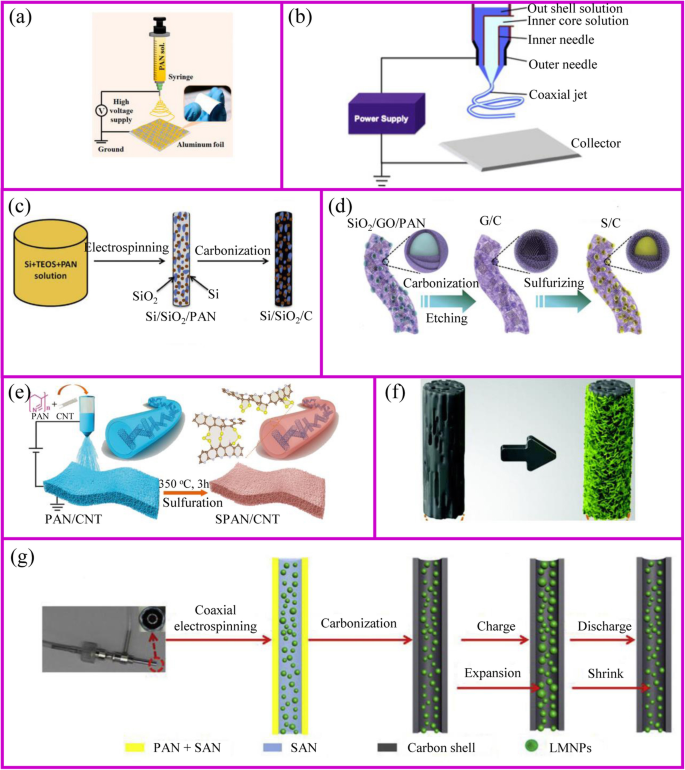
The schemes of a single axial and b coaxial electrospinning [111, 112]. c Inorganic fibers [113]. d Inorganic particles encapsulated carbon fibers [114]. e The modification of carbon fibers [115]. f Carbon fiber membrane with nanoparticles [38]. g Highly flexible carbon fiber membrane [116]
The polymer solutions and needle are the key points for the success of fiber fabrication. Polymer solution should reach the minimum viscosity for the formation of homogeneous fiber structure. The solvent of polymer should have a lower evaporation rate, which allows the polymer solidification after leaving the needle. The needle should be designed with coaxial structure to achieve hollow or core-shell fiber structure (Fig. 7b). For the coaxial electrospinning, the core and shell solutions should be adjusted to be immiscible or non-precipitable. Besides, during the electrospinning process, solution flow rates, voltage, temperature, distance from needle to the collector, and diameter of the needle have a huge influence on the fiber structure.
The obtained electrospun membrane needs further treatment to be a binder-free electrode. Carbon, ceramic, or metal nanofibers can be synthesized from the carbonization of electrospun fibers that contain polymer, metal salts, or metal atoms, respectively. Their composites such as metal/C and ceramic/C can be also obtained from their corresponding mixed precursors followed by a one-step or multi-step heat treatment. A wide range of electrospun materials have been investigated for LIBs including metal oxides (e.g., TiO2 , Fe2 O3 , ZnO, NiO, CuO, LiCoO3 , Li4 Ti5 O12 , and LiMn2 O4 ) [118, 119], hybrids [120] (e.g., SnOx /C, SiOx /C, Co3 O4 /C, SnOx /C, TiO2 /C) [113, 121,122,123,124,125,126,127,128,129,130], and polymers (e.g., polyvinyl alcohol (PVA), PAN and PVP, poly(vinylidene fluoride-co-hexafluoropropylene) (PVDF-HFP), and polyethylene oxide (PEO)) [131].
Conventional electrospinning generally disperses metal salts and nanoparticles inside the fibers. However, the nanoparticles can adhere to the outside of the fibers as well (Fig. 7c). Lan, Yang, and coworker prepared 3D free-standing spider-web-like membranes with high mass loading of bismuth (Bi) nanoparticle clusters followed by carbonization in nitrogen gas [132]. The 3D Bi/C membrane provides good mechanical properties and stabilizes the Bi nanoparticles up to 200 cycles.
The architecture of fibers can be optimized to accommodate large volume changes and instability of the electrode materials during cycling process. The adjustment of the fiber structure can be started from either inside or outside of the fiber. The internal fiber can be regulated by the polymer solution and post-treatment, while the external fiber structure is controlled by post-treatment. When the polymer solution contains etchable materials, a porous fiber structure can be prepared after carbonization and template etching (Fig. 7d). This porous materials is capable of accommodating higher sulfur and suppressing the polysulfides shuttle effects [114]. The polymer can individually form an active material at the expense of flexibility self-standing property. This disadvantage can be addressed by additives. Liu et al. showed the PAN fibers with an appropriate amount of CNTs can still be self-standing after sulfurization [115]. The sulfur only exists in the form of Li2 S2 et Li2 S3 rather than polysulfides in the sulfurized PAN. Therefore, it shows ultra-stable cycling performance up to 1000 cycles (Fig. 7e).
Alternatively, the post-treatment of the surface of electrospun fibers is another way to prepare the high-performance binder-free electrode (Fig. 7f) . After carbonization, the three-dimensional conductive network is formed to provide good electronic conductivity. The fiber surface also provides a large number of sites for the growth of active materials with easy access to electrolyte [38]. Another post-treatment is to coat the nanofibers with a protective surface layer. Generally, the nanoparticles spinning out with the polymer solution is inevitably exposed at the surface of the fiber. This part of the material may fall off from fibers during the cycling process, so the surface coating is equivalent to the protection of the fiber [133].
In addition to polymer solution, the needle is also of importance to the fibers design. The core-shell composite nanofiber can be prepared by a dual nozzle coaxial electrospinning setup (Fig. 7g) [116]. This needle can achieve a great core-shell fiber structure. Besides, hollow fibers can be prepared by designing the inner and outer solutions. When the hollow fiber is filled with the active material, there is sufficient space to allow the volume to expand [112].
Vacuum Filtration
The vacuum filtration method is a rapid manufacturing process to assemble different kinds of nanoscale materials into the macroscopic film for various applications. This process is low-cost, rapid, and efficient, which demonstrates a promising strategy for various functional films. 2D materials can be easily assembled into flexible self-standing paper-like materials, which can be directly used as flexible binder-free electrodes in energy storage devices [134, 135]. In general, the active materials are randomly dispersed between the supporting materials. Therefore, high mechanical strength and flexibility are preserved for the papers (Fig. 8) [136, 137].
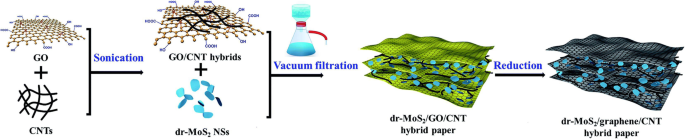
The scheme of vacuum filtration process [136]
The vacuum filtration features as the following strengths. Firstly, active materials can adhere on the conductive substrate, leading to the improvement of electron conductivity. For example, the electron conductivity of MoS2 can be largely improved; therefore, better rate performance can be obtained [138, 139]. Secondly, the large surface area is in favor of the contact between active materials and lithium ions, which facilitates the transportation of Li-ion. When the active material is added into the 2D material, the interlayer spacing becomes large; thus, the electrolyte can be immersed. The lithium ions are more accessible to the material; thereby, the interface impedance of material is reduced [140]. Thirdly, the effective material utilization is also facilitated by hindering the aggregation of 2D materials [141,142,143]. Lastly, the material agglomerations and electrode instabilities result from the huge volume change of active materials during Li insertion/extraction [144, 145]. Supporting sheets can absorb stress induced by volume expansion, similar to the role of elastic buffer [146, 147].
Different types of nanostructures can be assembled into 2D materials. For example, the nanoparticles, nanotubes, nanosheets, nanorods, etc. can fabricate into the graphene sheets [148]. When CNTs as additive are assembled into the nanosheets, the restacking of the nanosheets can be prevented, and the conductivity of ion and electron can be greatly increased [149]. The electrode chemical properties can be enhanced by coating or mixing active materials on other conductive materials and then assembling into 3D functional materials [150,151,152]. It is mainly attributed to the synergistic effects that 3D structure not only serves as a flexible scaffold for strains/stresses release and volume expansion, but also offers a three-dimensional conductive architecture with open channels for electron transfer and Li-ion diffusion. Besides, pre-protection of active materials is a way to improve material stability. The surface modified anode materials in graphene exhibit high capacities, long cycle-life, and excellent rate performance [153]. The Mn2 P2 O7 -carbon in graphene electrode delivers a capacity of 585 mA h g −1 at a current density of 1000 mA g −1 . When increasing the current density to 5000 mA g −1 , a high capacity of 400 mA h g −1 can be remained even after 2000 cycles [153].
Physical Vapor Deposition
At certain temperature and airflow rate, the elemental vapor can be easily deposited onto the porous supporting materials [154,155,156]. Solid sulfur and red P nanoparticles are the typical materials, which can be deposited into porous carbon materials. The commercialization of sulfur as cathode materials is blocked by several intrinsic problems, including low electronic/ionic conductivity, large volumetric expansion, and shuttle effect of intermediate polysulfides (Li2 Sx (4 ≤ x ≤ 8)). Particularly, the shuttle effect of polysulfides results in transport of sulfur from cathode to anode and the reaction with Li metal, which leads to significant capacity loss and safety issues. So far, the design of porous structure is the basic strategy to suppress the polysulfides shuttle effect, and sulfur vapor deposition is an effective way for the fabrication of S/C composite. It is an environmentally friendly, solvent-free method in which the sulfur powder undergoes a physical deposition process with no changes of chemical properties [157]. With proper absorbent in the structure, the shuttle effect of polysulfides can also be fixed. Recently, Yang, Zhang, and coworkers reported Ti3 C2 Tx paper is a good host for sulfur deposition (Fig. 9a). This Ti3 C2 Tx paper shows no cracks after 25 convexly and concavely bending cycles (Fig. 9b, c) [158]. Yu and coworkers [159] demonstrated porous carbon fibers encapsulated with red P shows high capacity of 2030 mAh g −1 at 0.1 C rate after 100 cycles. It is worth noting that physical vapor deposition (PVD) is only one of the procedures of immobilizing S or P onto carbon materials. Therefore, the most important research direction is how to design a porous conductive matrix.
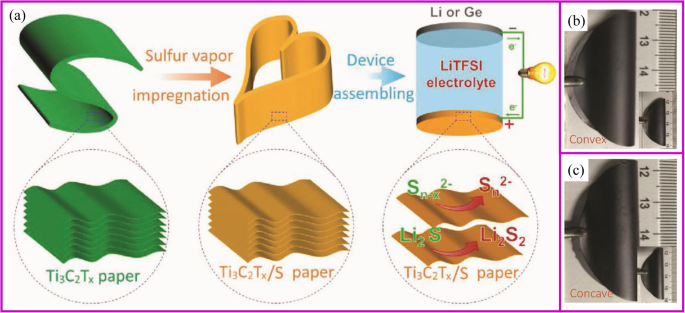
un The scheme of fabrication of robust, freestanding, and conductive Ti3 C2 Tx /S paper. Photographs of freestanding Ti3 C2 Tx /S paper when bending b convexly and c concavely, showing good mechanical flexibility similar to that of the pure Ti3 C2 Tx paper [158]
Application in Flexible Batteries
Flexible devices, such as wearable displays, sensors, sportswear, mobile communication devices, rollup displays, and so on, are one of the important directions for intelligent and smart world [160]. The development of these new devices requires the power of a flexible battery system [161,162,163]. However, current advanced pouch and 18,650 cells cannot be used on flexible devices due to the rigid material properties. Each component of the flexible battery, such as electrodes, separator, and solid electrolyte, must be flexible (Fig. 10a) [164]. The conventional electrode is generally adhered to the metal foil by a coating method to physically bond the active material and the conductive agent. During repeated bending and folding, the active material separates from the current collector, ending up with deactivation. For example, the Li4 Ti5 O12 (LTO)-based electrode folded about 100 cycles would present the detachment of LTO from Al foil. The impedance of the electrode increases from the first fold, and the higher the active material loading, the faster the impedance increases (Fig. 10b). At the same time, the pouch cell bending 30° results in serious capacity fade (Fig. 10c).
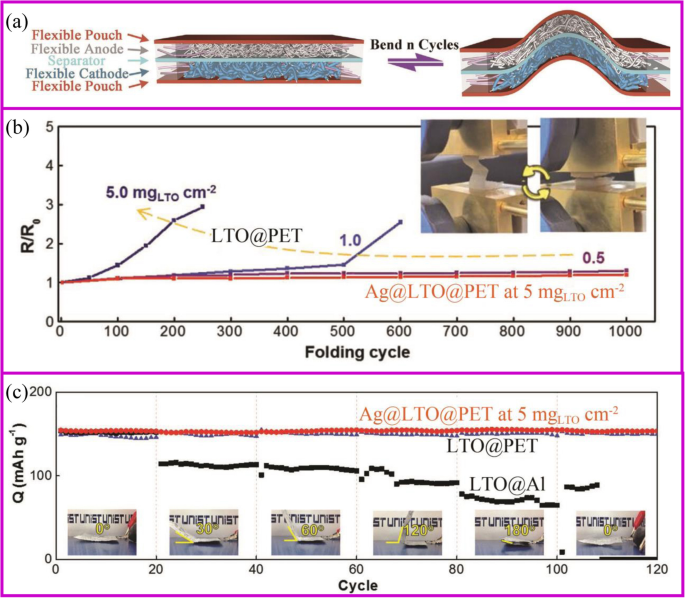
un Assembly and bending tests of flexible batteries with flexible electrodes [164]. b Electrical resistance change with folding cycles [165]. c Capacity retention of folded cells at different angles at 1 C [165]
There are many strategies to fabricate flexible electrodes. Song et al. reported that coating LTO particles and Ag nano wires onto the polyethylene terephthalate (PET) web can greatly improve the electrode flexibility and stability. The electrical resistance of Ag@LTO@PET electrode does not change during 1000 folding cycles (Fig. 10b). Pouch-type Ag@LTO@PET-based half cells showed great cycling performance with little capacity decay when the electrode was bent at any angle (Fig. 11c) [165]. The most mature method is to fix the active material on a flexible substrate. As described in the “Introduction” section, the direct growth of the active material on the conductive substrate can improve battery energy density and rate performance. Herein, we take the carbon cloth and carbon materials as the example to show the application of binder-free electrodes in flexible devices.

un Schematic illustration for the structural features of the flexible SnO2 nanosheets on flexible carbon cloth electrode during the folding (I), the rolling (II), and twisting (III) tests. b Current-time curves of the composite samples at various bending angles of the 1st and 200th cycles, and the inset images show the corresponding bending angles for measurement and photographs [166]
Most carbon materials cannot be used in flexible electronics. For example, a binder-free electrode based on graphite paper can only maintain 25 cycles in a bent state [167]. Comparing with other carbon materials, carbon cloth with excellent flexibility and electrical conductivity is one of the most promising materials for the flexible battery application. Even after the surface modification of inorganic materials, carbon cloth still shows excellent flexibility. As shown in Fig. 11a, there are no apparent changes of the electrode after bending, rolling, twisting, folding, and crumpling tests. After the mechanical test, the active materials on the carbon cloth can maintain structural integrity. Also, after 200 bending cycles, the current value slightly decreases from 17.3 to 16.8 mA, which demonstrates great stability (Fig. 11b) [166].
It is particularly difficult to synthesize flexible carbon materials. For example, the PAN film becomes much more brittle and fracture after carbonization, which is difficult to use in flexible batteries. The ideal carbon material, like the clothes we wear, bending and folding many times can still remain intact. The flexibility of the material can be greatly improved through reasonable design such as the addition of functional additives. Wang et al. reported that the carbonized PAN film with SiO2 filler can fully recover to its original state after repeated rolling or folding process [114]. When assembled into the pouch cell, it can withstand at different bending angles up to 180°. Yu et al. demonstrated that Zn(CH3 COO)2 assists the uniform carbonization of PAN, which relieved the stress concentration [130]. The film obtained by this method can return to the initial state after folding four times (Fig. 12a). When assembled into the pouch cell, it can light the LED at any folding angle. When the pouch cell is disassembled, the binder-free electrode remains intact while the slurry-based electrode is completely destroyed (Fig. 12b–e).

un Digital photographs of Zn(CH3 COO)2 -PAN film, which can be folded four times. LED lighting tests of a full battery when b flat, c folded once, and d folded twice; et e digital photographs of the electrode after the LED lighting test [130]
Conclusions
In conclusion, recent research progress on the preparation of binder-free electrodes for LIBs has been summarized. The fabrication methods focus on the chemical, physical, and electrical treatment, such as thermal treatment, hydrothermal treatment, CBD, ALD, CVD; vacuum filtration, electrospinning; and electrophoretic deposition, anodization, electrodeposition. Thermal treatment is the most commonly used chemical method to carbonize polymer for free-standing structure or decompose of the precursor of metallic oxide. The hydrothermal and CBD methods are very attractive due to accurate control of the size and morphology of nanomaterials. CBD and hydrothermal methods present in situ growth of active materials on the substrate through a chemical reaction. CVD is defined as the deposition of a gas carrier on a heated surface by a chemical reaction, while the ALD technique is a vapor phase chemical deposition process that is capable of producing high-quality nanoscale thin films in an atomic layer-by-layer manner. The vacuum filtration and electrospinning are the representative physical methods. The former is a physical manufacturing process to assemble different materials like nanoplatelets and nanoparticles into the macroscopic film. The latter can produce 1D nanoscale materials with fiber diameters ranged from tens of nanometers up to micrometers. The electrical method is a widely used technique to make coatings and thin films. However, it is not often used to prepare binder-free electrode. Among these methods, CVD and CBD are excellent ways to prepare silicon-based and sulfur-based materials, respectively.
The binder-free electrode shows better electrochemical performances than the traditional slurry system. The binder-free electrode can improve ionic and electronic transportation, cycling performance, and energy density of the electrodes. In addition, nanoscale materials are uniformly anchored on the supporting materials, which can effectively prevent the agglomeration of nanoparticles and mitigate the volumetric expansion during the repeated cycling process.
The conductive matrix plays a crucial role in the electrochemical properties and performances of the binder-free electrode. The ultra-flexible film has great potential to make a big breakthrough in the field of wearable and flexible devices. However, existing substrates are still unable to meet the requirements. The flexible device requires the binder-free electrode to bend and fold for numerous times with no damage and no separation from the substrate. According to current research process, ultra-flexible and ultra-stable carbon materials become the most promising candidate for next-generation flexible binder-free electrode.
Despite the difficulties, the future is expected. The uniform and large-scale growth of the active material on the conductive substrate is one of the necessary conditions for practical application. Fortunately, it is now possible to achieve. Practical applications need to consider the basic properties of the electrode in the battery, such as the initial Coulombic efficiency and voltage profiles. Therefore, the active materials for both anodes and cathodes should be carefully selected. For example, Si, Sn, or carbon materials serve as promising candidates for anode materials while the cathode materials may be selected from S matching with Li metal, or the existing Li metal oxides. In addition, flexible batteries can be achieved with all of flexible components, such as electrodes, separators, and electrolytes. Although these aspects have been studied for a long time, breakthrough is needed to facilitate the research progress.
Disponibilité des données et des matériaux
Toutes les données sont entièrement disponibles sans restriction.
Abréviations
- LIB:
-
Batteries lithium-ion
- PVDF :
-
Fluorure de polyvinylidène
- ACF:
-
Active carbon fiber
- PAN :
-
Polyacrylonitrile
- rGO :
-
Oxyde de graphène réduit
- PVP :
-
Polyvinylpyrrolidone
- LBL:
-
Layer-by-layer
- GO :
-
Oxyde de graphène
- PDDA :
-
Poly (diallyldimethylammonium chloride)
- CNT :
-
Nanotube de carbone
- CBD:
-
Dépôt en bain chimique
- CVD :
-
Dépôt chimique en phase vapeur
- SEI :
-
Interface à électrolyte solide
- Si NW :
-
Nanofils de silicium
- ALD :
-
Dépôt de couche atomique
- EPD:
-
Electrophoretic deposition
- PVA :
-
Alcool polyvinylique
- PVDF-HFP :
-
Poly(vinylidene fluoride-co-hexafluoropropylene)
- PEO :
-
Oxyde de polyéthylène
- Bi:
-
Bismuth
- PVD:
-
Physical vapor deposition
- LTO:
-
Li4 Ti5 O12
- PET :
-
Polyéthylène téréphtalate
Nanomatériaux
- Application du titane dans les matériaux énergétiques
- 13 types de matériaux réfractaires et leurs applications
- Matériaux :PP renforcé de fibre de verre et de carbone pour l'automobile
- Synthèse de points quantiques de type II/Type-I à suppression de réabsorption ZnSe/CdS/ZnS Core/Shell et leur application pour le dosage immunosorbant
- Synthèse facile de nanoparticules SiO2@C ancrées sur MWNT en tant que matériaux anodiques hautes performances pour batteries Li-ion
- Synthèse et propriétés électrochimiques des matériaux cathodiques LiNi0.5Mn1.5O4 avec dopage composite Cr3+ et F− pour batteries lithium-ion
- Matériaux et conception de PCB pour haute tension
- Différents types d'énergie et leurs exemples
- Électrodes de soudage par résistance pour votre application



