Points de carbone bleu luminescent à haute efficacité indépendants de l'excitation
Résumé
Des points de carbone luminescents bleus (CD) ont été synthétisés par la méthode hydrothermale. Des décalages vers le bleu de la longueur d'onde d'émission maximale de 480 à 443 nm ont été observés lorsque la concentration de la solution de CD a diminué. Les spectres de photoluminescence (PL) des CD à faible concentration ont montré un comportement indépendant de l'excitation, ce qui est très différent des rapports précédents. Deux mécanismes d'émission différents pourraient fonctionner :la luminescence intrinsèque de sp 2 -les réseaux de carbone peuvent être responsables de la partie de longueur d'onde plus courte de l'émission (indépendante de l'excitation) à faible concentration et la polarité élevée des clusters nanométriques a conduit au comportement dépendant de l'excitation de la partie de longueur d'onde plus longue à une concentration élevée de solution de CD. La propriété photophysique et le comportement dépendant de la concentration des CD ont offert de nouvelles perspectives sur les CD du point de vue à la fois des expériences et des mécanismes, ce qui favorisera diverses applications potentielles des CD dans un proche avenir.
Contexte
Les points de carbone, en tant que matériau fluorescent de la famille des nanomatériaux de carbone, ont suscité de plus en plus de préoccupations ces dernières années. Typiquement, un CD a un noyau de graphite ou de charpente de carbone amorphe, et dont la surface est recouverte de groupes contenant de l'oxygène, de polymères et d'autres espèces [1]. Pendant ce temps, les CD, qui ne dépassent pas 10 nm, ont des caractéristiques photophysiques uniques, telles qu'une photostabilité élevée, une bonne biocompatibilité, d'excellentes propriétés optiques et de faibles risques environnementaux [2, 3]. Inspirés par ces propriétés, les CD possèdent diverses applications potentielles, telles que l'administration de médicaments [4], l'encre fluorescente [5], les capteurs [6, 7], l'optoélectronique [8], la photocatalyse [9, 10] et les dispositifs électroluminescents. [5, 11,12,13]. Jusqu'à présent, diverses méthodes de synthèse ont été développées pour la préparation des CD, telles que l'oxydation électrochimique du graphite [9], la méthode hydrothermale [5, 10] et la synthèse assistée par micro-ondes [14, 15].
Une propriété particulière des CD est la dépendance du pic d'émission avec la longueur d'onde d'excitation. Sous différentes longueurs d'onde d'excitation, les CD ont des pics de photoluminescence (PL) différents du violet au rouge [10]. De nombreuses raisons possibles ont été rapportées pour expliquer ce phénomène, telles que la taille [9, 11], le dopage des éléments [10, 14], la polarité du solvant [16], les défauts, les états de surface [17], les groupes de surface [18, 19] ou passivation de surface [20]. Cependant, la propriété indépendante de l'excitation des CD est rarement observée.
Fait intéressant, nous avons constaté qu'en diluant la solution de CD avec de l'eau déminéralisée, le décalage vers le bleu du pic d'émission maximal de 480 à 440 nm a été observé. De plus, l'intensité d'émission des CD est devenue plus forte avec la diminution de la concentration. Les spectres PL ont montré un pic d'émission inchangé à 443 nm lorsque la longueur d'onde d'excitation variait, ce qui est très différent des rapports précédents. La haute polarité du cluster nanométrique et le sp 2 -les réseaux carbone peuvent être responsables de ces phénomènes.
Méthodes
Réactifs et produits chimiques
Le monohydrate d'acide critrique (99,5 %) était requis de la SCR (Shanghai, Chine) et l'éthylènediamine a été obtenue à partir du réactif de Tianzheng (Tianjin Chine). L'eau déminéralisée a été obtenue à partir d'un système de purification d'eau purificateur d'eau avec une résistivité de 18,25 m Ω cm (Sichuan, Chine). Tous les produits chimiques ont été utilisés tels qu'ils ont été reçus sans autre purification ni traitement.
Préparation des points de carbone
Les CD ont été préparés comme suit :l'acide citrique (1,0507 g) et l'éthylènediamine (335 μL) ont été ajoutés dans de l'eau déminéralisée (10 mL). Ensuite, la solution bien agitée a été transférée dans un autoclave revêtu de téflon. La solution a été chauffée à 150 °C pendant 5 h. Après la réaction, les réacteurs ont été refroidis à température ambiante naturellement. La couleur de la solution CD préparée était jaunâtre. Avant la caractérisation, la solution CD a été traitée par les méthodes suivantes :a pris 1 ml de solution CD originale, puis diluée par 5 à 400 ml d'eau déminéralisée. La couleur de la solution CD est passée du jaune à l'incolore après la dilution.
Caractérisation
La photoluminescence a été réalisée avec un spectrophotomètre à fluorescence Hitachi F4500 et un microscope confocal Raman avec un laser He-Cd de 325 nm. Les spectres d'absorption ont été collectés par un spectromètre Shi-madzu UV-3101PC. L'infrarouge transformé de Fourier (FTIR) a été enregistré avec un spectromètre Brucker VERTEX; Les images de microscopie électronique à transmission (MET) ont été enregistrées sur un appareil FEI Tecnai G2 20S-twin. L'étude de diffusion dynamique de la lumière (DLS) a été réalisée avec un Malvern Zetasizer Nano ZS. Les diagrammes de diffraction des rayons X (XRD) ont été collectés avec un système Bruker D8. Le profil de décroissance de la fluorescence a été étudié à l'aide d'un spectromètre à fluorescence Edinburgh FLS920. Les spectres Raman ont été réalisés sur LabRAM HR Evolution (Horiba) avec une excitation laser à 532 nm. L'analyse par spectroscopie photoélectronique aux rayons X (XPS) a été mesurée par PHI 5000 Versa Probe (ULVAC-PHI, Japon). Les mesures de microscopie à force atomique (AFM) ont été effectuées avec un microscope à sonde à balayage multimode (MM-SPM).
Résultats et discussion
La formation de CD est confirmée par des mesures de microscopie électronique à transmission, de diffraction des rayons X (XRD) et de spectroscopie Raman. Comme le montre la figure 1a, des nanoparticules de carbone sphériques sont obtenues avec un diamètre moyen d'environ 3,6 nm. L'encart affiche la distribution des tailles de particules entre 2,5 et 5 nm. La figure 1b montre que les CD ont des noyaux internes cristallisés avec un espacement de réseau de 0,295 nm, ce qui correspond au plan (002) du carbone graphitique [4, 9, 14]. Les structures de réseau discernables des CD dans les images MET indiquent que les nanoparticules résultantes ont les noyaux internes de graphite. Le diagramme de diffraction XRD des CD montre un large pic à 20,24° (Fichier supplémentaire 1 :Figure S1), proche de l'espacement intercalaire (002) d'une structure graphitique [5, 21]. La bande G à 1598 cm −1 et bande D à 1350 cm −1 des CD n'étaient pas évidents sur les spectres Raman (Fichier supplémentaire 1 :Figure S2). La caractérisation Raman pourrait être perturbée par la forte fluorescence des CD. De plus, l'absence des deux pics prouve en outre que les CD sont composés d'un noyau de type graphite nanocristallin et de sp 3 désordonnés -carbone [21].
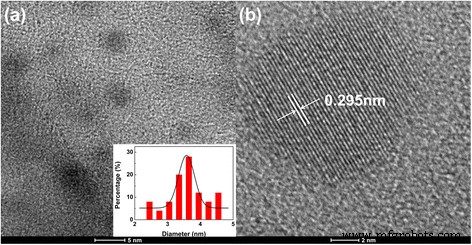
Images TEM et HRTEM de CD tels que préparés. un L'image de microscopie électronique à transmission (MET) de CD tels que préparés (encarts montrant la distribution granulométrique). b L'image MET haute résolution d'un CD représentatif, qui montre son noyau interne en graphite cristallisé
Comme le montre la figure 2a, la couleur de la solution aqueuse de CD telle que préparée est jaunâtre (à gauche), qui présente la luminescence bleu vif sous l'excitation d'une lumière UV à 365 nm (à droite). Dans le spectre d'absorption de la solution CD, le pic d'absorption à 243 nm est attribué à \( \pi \)→\( \pi \) * de C=C, et le pic d'absorption à 345 nm correspond à n→\( \pi \) * transition de la liaison C=O (Fig. 2a) [14]. Le spectre de spectroscopie infrarouge à transformée de Fourier (FTIR) (Fig. 2b) des CD suggère la présence d'abondants groupes contenant de l'oxygène sur leurs surfaces. Comme le montre la figure 2b, les pics à 1120 cm −1 peut être attribuée aux vibrations d'étirement asymétriques et symétriques de C–O–C. Le pic à 1445 et 1464 cm −1 sont affectés aux vibrations de flexion C–H ; les pics à 1488 cm −1 indiquer l'existence de vibrations de flexion N-H ; le pic à 1689 cm −1 est attribué à la vibration d'étirement C=O ; les pics à 2935 cm −1 proviennent des vibrations d'étirement C−H du méthyle/méthylène ; et la large bande centrée sur 3 100-3 500 cm −1 sont attribuées aux vibrations d'étirement O–H et N–H [5, 10, 14]. Les résultats de l'analyse FTIR ont confirmé la présence de groupes contenant de l'oxygène à la surface des CD tels que préparés, tels que C = O et -OH. Les enquêtes XPS ont en outre soutenu les analyses FTIR. Comme le montre le Fichier Additionnel 1 :Figure S3, les CD sont principalement composés d'éléments carbone, oxygène et azote. Le spectre XPS haute résolution des C 1 montre trois pics à 284,56, 285,66 et 287,7 eV, qui indiquent la présence de C=C/C–C, C–O et C=O. Le spectre à haute résolution des N1 a suggéré la présence de N de type pyrrolique (399,7 eV) et de N de type graphitique/aminé (400,7 eV). Les deux pics du spectre haute résolution O 1s à 531,55 et 532,31 eV sont attribués aux liaisons C=O et C–OH/C–O–C [21,22,23,24]. Les résultats de l'analyse XPS sont en bon accord avec le spectre FTIR. En combinant toutes ces données de caractérisation, les CD ont été considérés comme composés d'un noyau de type graphite à l'échelle nanométrique et de groupes contenant de l'oxygène qui se trouvent à la surface du noyau.
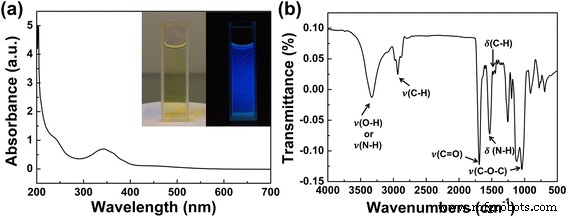
Spectre d'absorption UV-vis et spectre FTIR des CD tels que préparés. un Le spectre d'absorption UV-vis des CD. L'encart les photographies montrent les CD tels que préparés à la lumière naturelle (gauche ) et sous une irradiation de 365 nm (à droite ). b Le spectre FTIR des CD
Les spectres d'émission des CD dilués dans 5 ml d'eau déminéralisée montrent une caractéristique typique dépendant de l'excitation. Le pic PL passe à une longueur d'onde plus longue à mesure que la longueur d'onde d'excitation augmente progressivement (Fig. 3a ; les longueurs d'onde d'excitation passant progressivement de 330 à 480 nm, et l'intensité d'émission de 330 à 390 nm est multipliée par 25), ce qui concorde bien avec d'autres rapports [1, 5, 14]. Les CD ont une intensité d'émission maximale à 481 nm avec une excitation de 420 nm. Utilisation de bisulfate de quinine (QY 0,56 dans 0,1 M H2 SO4 ) comme référence, le rendement quantique des CD est de 74,8%. Le rendement quantique élevé est supposé être l'état moléculaire des CD [5]. De plus, la longueur d'onde d'émission et l'intensité PL des CD obtenus sont sensibles au volume d'eau ajoutée; en d'autres termes, ils sont sensibles à la concentration de la solution CD (Fig. 3b–d). Ce résultat est différent des CD synthétisés par d'autres méthodes, qui n'ont montré qu'un léger décalage du pic d'émission avec la variation de la valeur du pH [25]. En ajoutant plus d'eau déminéralisée (10, 25, 50, 100, 200, 300 et 400 ml) dans 1 ml de solution CD telle que préparée, les décalages vers le bleu des pics d'émission sont observés de 480 à 440 nm (Fichier supplémentaire 1 :Figure S4), tandis que les spectres d'absorption correspondants de la solution CD n'ont pas changé (Fichier supplémentaire 1 :Figure S5). L'intensité des pics d'émission dans la plage de 330 à 400 nm est progressivement augmentée, tandis que les pics d'émission dans la plage de 420 à 480 nm disparaissent progressivement (Fichier supplémentaire 1 :Figure S4). Ce décalage vers le bleu était clairement visible dans les spectres PL normalisés de la figure 3b, lorsque les CD avec des concentrations différentes sont excités par la même longueur d'onde de 330 nm. Sur la figure 3b, c, le changement de longueur d'onde d'émission se produit principalement lorsque le volume d'eau déminéralisée ajoutée est inférieur à 25 ml, qui varie de 505 à 450 nm. Avec une dilution supplémentaire, la longueur d'onde d'émission change assez peu. Sur la figure 3c, l'intensité PL du pic d'émission augmente continuellement avec la diminution de la concentration de CD. Cette amélioration de l'intensité peut bénéficier de la réduction de l'extinction par collision et de l'extinction d'auto-absorption dans les solutions à haute concentration [5, 26].
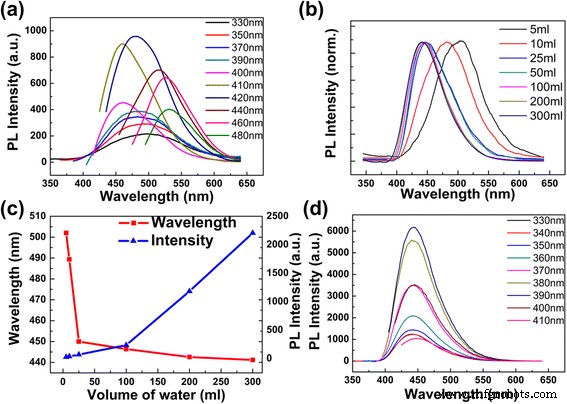
Spectres PL de CD dans différents volumes d'eau déminéralisée. un Spectres PL de 1 ml de CD tels que préparés avec 5 ml d'eau déminéralisée (pH 10,41). b Spectres d'émission de fluorescence normalisés de CD dans différents volumes d'eau avec une longueur d'onde d'excitation de 330 nm. c L'intensité PL maximale et le pic d'émission en fonction des différents volumes d'eau ajoutée. d Spectres d'émission de la dilution de 1 ml de solution de CD tels que préparés avec 300 ml d'eau déminéralisée
Après avoir été dilués avec 300 ml d'eau déminéralisée, les spectres PL montrent un pic d'émission unique à 443 nm, qui est invariable lorsque la longueur d'onde d'excitation varie (Fig. 3d ; les longueurs d'onde d'excitation augmentent progressivement de 330 à 410 nm). L'intensité d'émission la plus élevée est obtenue sous la longueur d'onde d'excitation de 390 nm. Même dilué avec plus de volume d'eau (Fichier supplémentaire 1 :Figure S4), les spectres d'émission ne sont pas décalés.
Lors de l'ajout de différents volumes d'eau déminéralisée dans des solutions CD telles que préparées, la valeur du pH de la solution est modifiée. Les phénomènes que nous avons observés pourraient être causés par les différentes valeurs de pH. Afin de vérifier si la valeur du pH est la cause principale des phénomènes, la solution CD de différentes valeurs de pH a été analysée en détail. Le pH de la solution CD diluée dans 5 ml d'eau déminéralisée est de 10,41. Lors de la dilution de la solution CD telle que préparée avec 300 ml d'eau déminéralisée, la valeur du pH passe à 10,2. Ensuite, nous avons ajusté la valeur du pH de la solution CD diluée de 300 ml de 10,2 à 10,41 en ajoutant du NaOH. La figure 4a montre les spectres PL de la solution CD après ajustement de la valeur du pH à 10,41 (les longueurs d'onde d'excitation augmentant progressivement de 330 à 410 nm). D'après les deux figures (Figs. 3d et 4a), nous avons évidemment pu remarquer que même lorsque la valeur du pH est ajustée de 10,2 à 10,41, la position et l'intensité du pic PL sont presque invariables. Ensuite, nous avons ajusté les valeurs de pH de la solution CD contenant 5 ml d'eau déminéralisée et de la solution contenant 300 ml d'eau déminéralisée à la même valeur de 12,08 en ajoutant du NaOH (sur la Fig. 4b, les longueurs d'onde d'excitation augmentent progressivement de 330 à 480 nm , l'intensité d'émission de 330-380 nm est multipliée par 15, et l'intensité d'émission de 390 nm est multipliée par 6. Sur la figure 4c, les longueurs d'onde d'excitation augmentent progressivement de 330 à 410 nm ); par rapport à la figure 3a,d, les positions et les intensités des émissions de PL n'ont pas non plus changé. Les résultats ci-dessus montrent que le pH n'est pas la raison du pic d'émission immuable dans notre expérience. Ainsi, on peut conclure que la concentration est le point clé pour ajuster la longueur d'onde d'émission et fixer le pic d'émission. À notre connaissance, il s'agit du premier rapport à montrer que la longueur d'onde d'émission et l'intensité PL des CD peuvent être facilement ajustées en ajustant la concentration de la solution CD avec de l'eau déminéralisée.
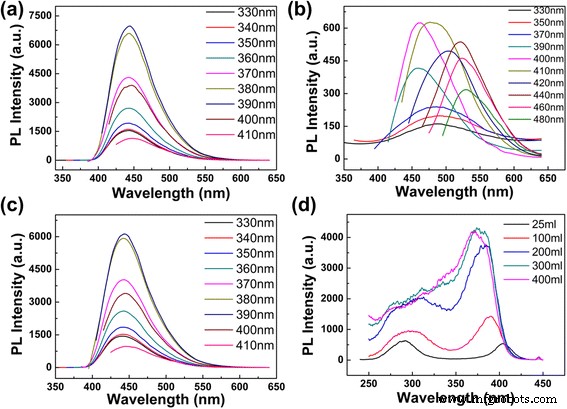
Spectres d'émission et d'excitation des CD dans différents volumes d'eau et pH. un Spectres d'émission de CD avec 300 ml d'eau déminéralisée (pH 10,41). b Spectres d'émission de CD avec 5 ml d'eau déminéralisée (pH 12,08). c Spectres d'émission de CD avec 300 ml d'eau déminéralisée (pH 12,08). d Spectres d'excitation de CD à 445 nm dans différents volumes d'eau
Pour donner un aperçu des caractéristiques indépendantes de l'excitation des CD, nous avons mesuré les spectres d'excitation de différentes longueurs d'onde d'émission et l'avons montré dans le fichier supplémentaire 1 :Figure S6. Pour la solution CD à forte concentration (1 ml de solution telle que préparée diluée avec 25 ml d'eau déminéralisée), il existe deux pics d'excitation puissants situés à 290 et 400 nm, séparément. Avec la diminution de la concentration d'élevée à faible, le pic d'excitation à 290 nm devient faible et le pic à 400 nm est accentué et se déplace vers le bleu jusqu'à 370 nm (Fig. 4d). Les caractéristiques des spectres d'excitation à différentes concentrations révèlent que la luminescence des CD peut avoir plusieurs centres. Pour faire une preuve supplémentaire, la durée de vie de fluorescence des CD (1 ml de solution telle que préparée diluée avec 25 ml d'eau déminéralisée) a été mesurée avec la longueur d'onde d'excitation à 280 nm et les longueurs d'onde d'émission à 447 nm (Fichier supplémentaire 1 :Figure S7). La durée de vie moyenne est de 11,85 ns et la courbe de décroissance peut être ajustée par une fonction double exponentielle avec des durées de vie de 5,11 ns (35,08 %) et 13,28 ns (64,92 %). Les durées de vie multiples de l'échantillon pourraient être dues aux divers fluorophores ou niveaux d'énergie présents sur les surfaces des échantillons [18].
Certaines études de CD ont montré l'existence de petites particules ainsi que d'agrégats de particules même si une solution diluée était utilisée [27]. Un type d'agrégation similaire est également observé par Iijima [28], où de petites particules de carbone s'agrègent en structures de nanocornes de 80 nm. Les petites particules sont attirées les unes vers les autres par les forces de Van der Waals. Nous avons estimé la taille des particules de CD avec différents volumes d'eau déminéralisée par la mesure de diffusion dynamique de la lumière (DLS) (Fichier supplémentaire 1 :Figure S8), et le résultat montre que les diamètres hydrodynamiques des CD sont différents, allant de 34 à 15 nm. Dans une solution de CD telle que préparée (forte concentration), le diamètre moyen est de 34 nm. Après dilution avec 100 ml d'eau déminéralisée, les CD présentent un diamètre moyen de 15 nm. Les tailles moyennes des CD en solution aqueuse ont montré une tendance à la baisse avec la diminution de la concentration (Fichier supplémentaire 1 :Figure S8). En conséquence, on peut conclure qu'à une concentration élevée, un certain nombre de CD simples se sont agrégés pour former des amas de taille nanométrique, ce qui entraîne une augmentation du diamètre moyen. Les CD uniques et les clusters nanométriques coexistent dans la solution. Bien qu'à faible concentration, les grappes de taille nanométrique ont été séparées en CD uniques. Les tailles moyennes des CD testées par mesure DLS sont plus grandes que celles des résultats MET (4 à 6 nm), principalement parce que le DLS considère le diamètre hydrodynamique global qui inclut les particules ainsi que les molécules et les ions absorbés [27]. La microscopie à force atomique (AFM) de CD avec différents volumes d'eau a été mesurée. Comme le montre le fichier supplémentaire 1 :figure S9, lorsque la concentration est élevée, l'image révèle que les CD uniques se sont agrégés pour former des amas nanométriques et que le diamètre moyen est de 40 nm ; à mesure que la concentration diminue d'élevé à faible, les amas nanométriques se sont progressivement séparés en CD uniques, et le diamètre mesuré est d'environ 10 nm, ce qui est inférieur à 40 nm, ce qui est en bonne cohérence avec le résultat du DLS.
La formation de CD à partir de matériaux organiques dans des milieux aqueux a un point de vue commun selon lequel les CD sont composés de noyaux nanocristallins de sp 2 -îlots hybrides bidimensionnels de type graphène [10, 29] perturbés par sp 3 -inclusions hybrides de type diamant [27, 29]. Lors de la formation des nanoparticules, les groupes polaires dérivés des matériaux de départ sont fixés à la surface des CD, ce qui permet aux particules d'être solubles dans l'eau. Ce point de vue a été confirmé par les spectres Raman des CD obtenus à partir de différents matériaux de départ [27, 30], qui ont démontré la présence de sp 2 - et sp 3 -structures hybridées dans des proportions similaires. Pendant ce temps, tous les CD hydrosolubles étudiés obtenus par traitement thermique de matériaux organiques contiennent des éléments oxygène sous forme d'hydroxyles, de carboxyles et de carbonyles [16]. Les groupes polaires à la surface des particules sont particulièrement importants pour l'émission de CD [16, 18, 31].
De l'expérience ci-dessus, nous pouvons conclure qu'il existe deux espèces émissives différentes dans la solution CD. La luminescence intrinsèque de sp 2 -les réseaux de carbone et la forte polarité des clusters nanométriques pourraient contribuer au phénomène d'émission différent (Fig. 5). Le CD unique se comporte comme un dipôle électrique [32] en raison de ses groupes de surface polaires, tels que -CO et -OH [15, 18, 31] (Fig. 2b). Les groupes contenant de l'oxygène à la surface des CD peuvent être responsables de la partie de longueur d'onde plus longue de l'émission de fluorescence [19]. À haute concentration, un certain nombre de CD sont agrégés ensemble par les forces de Van der Waals [28] pour former des nanoclusters, puis un grand nombre de -CO et -OH se réunissent, ce qui conduit à une polarité plus élevée sur les surfaces des nanoclusters [15 ]. La polarité élevée des clusters de taille nanométrique provoque les propriétés d'excitation dépendantes [15, 19, 31]. Pendant ce temps, le degré élevé d'oxydation et la polarité plus élevée des clusters de taille nanométrique conduisent à une relaxation rapide des électrons des états excités aux sous-états, ce qui correspond à une longueur d'onde plus longue. Ensuite, les sous-états contribuent à la photoémission, qui donne finalement lieu à une émission de longueur d'onde plus longue [15]. Ainsi, le phénomène de dépendance à l'excitation s'est produit à une partie de longueur d'onde plus longue lorsqu'à une concentration élevée. Après avoir ajouté de l'eau désionisée dans la solution CD telle que préparée, la concentration de la solution a progressivement diminué. Ensuite, les CD qui ont formé des nanoclusters sont séparés et redispersés en CD uniques, ce qui conduit à l'affaiblissement de la polarité et à la disparition des spectres d'émission à plus grande longueur d'onde. De plus, la séparation des clusters conduit également à la disparition du pic d'excitation à 290 nm (Fig. 4d). Comparée à l'émission des groupes polaires (–CO et –OH) à la surface d'un seul CD, la luminescence intrinsèque de sp 2 -les réseaux de carbone jouent un rôle prépondérant avec la diminution de la concentration en CD. À faible concentration, le spectre de fluorescence du CD unique avec uniquement une luminescence intrinsèque est asymétrique et élargi à la région d'énergie supérieure (courte longueur d'onde), ce qui montre la fluorescence indépendante de l'excitation, comme le montre la figure 4a [15, 33].
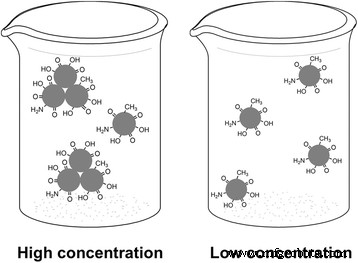
L'esquisse des CD à haute concentration et à faible concentration. Gauche :à haute concentration, un certain nombre de CD simples formaient des amas nanométriques ; à droite :à faible concentration, les clusters de taille nanométrique se séparent en CD uniques
Conclusions
En résumé, nous avons synthétisé les CD par méthode hydrothermale. De manière significative, les CD tels que préparés présentaient une excellente dispersibilité aqueuse et des propriétés PL uniques telles que la sensibilité à la concentration et la longueur d'onde d'émission indépendante de l'excitation. Des décalages vers le bleu de la longueur d'onde d'émission maximale de 480 à 443 nm ont été observés lorsque la concentration de CD diminuait d'élevée à faible. Les spectres PL à faible concentration de CD ont montré un comportement indépendant de l'excitation avec le pic d'émission à 440 nm, ce qui est très différent des rapports précédents. On pourrait conclure qu'il existe deux mécanismes d'émission différents. La luminescence intrinsèque de sp 2 -les réseaux de carbone étaient responsables de l'émission à de courtes longueurs d'onde (indépendant de l'excitation) à faible concentration, et la polarité élevée des clusters nanométriques a conduit à la propriété dépendante de l'excitation de la partie de longueur d'onde plus longue lorsqu'elle est à haute concentration. Les propriétés photophysiques favorables et le comportement dépendant de la concentration des CD fourniront un moyen d'ajuster la longueur d'onde d'émission et offriront de nouvelles perspectives sur les CD du point de vue des expériences et des mécanismes, ce qui favorisera diverses applications potentielles des CD dans un avenir proche.
Abréviations
- AFM :
-
Microscopie à force atomique
- CD :
-
Points de carbone
- DLS :
-
Diffusion dynamique de la lumière
- FTIR :
-
Infrarouge transformée de Fourier
- PL :
-
Photoluminescence
- TEM :
-
Microscopie électronique à transmission
- XPS :
-
Spectroscopie photoélectronique aux rayons X
- XRD :
-
Diffraction des rayons X
Nanomatériaux
- Ambre
- Carbone M2
- Fabrication et imagerie de cyclocarbone
- Synthèse de points quantiques de type II/Type-I à suppression de réabsorption ZnSe/CdS/ZnS Core/Shell et leur application pour le dosage immunosorbant
- Synthèse de points quantiques de carbone co-dopés en pyridinique N, S en tant qu'imitateurs d'enzymes efficaces
- Formation et propriétés luminescentes de nanocomposites Al2O3:SiOC à base de nanoparticules d'alumine modifiées par le phényltriméthoxysilane
- Microsphères de carbone magnétique comme adsorbant réutilisable pour l'élimination des sulfamides de l'eau
- Une approche simple pour la synthèse de points quantiques de carbone fluorescent à partir d'eaux usées de tofu
- ATL Composites contribue au projet de réhabilitation des piliers en béton



