Formation et propriétés luminescentes de nanocomposites Al2O3:SiOC à base de nanoparticules d'alumine modifiées par le phényltriméthoxysilane
Résumé
Al2 O3 :Des nanocomposites SiOC ont été synthétisés par traitement thermique de nanoparticules d'alumine fumée modifiées par du phényltriméthoxysilane. L'effet de la température de recuit dans un environnement inerte sur la structure et la photoluminescence de la poudre d'alumine modifiée a été étudié par spectroscopie IR ainsi que par spectroscopie de photoluminescence avec excitation ultraviolette et rayons X. Il est démontré que l'augmentation de la température de recuit entraîne la formation de précipités de silice à la surface des particules d'alumine qui s'accompagne d'un développement et d'une évolution spectrale de la photoluminescence visible. Ces observations sont discutées en termes de transformation structurale de la surface d'Al2 O3 particules.
Contexte
Récemment, il a été rapporté que des nanoparticules de silice à surface carbonisée par pyrolyse de groupes phénylméthoxy présentent une forte photoluminescence visible (PL) sous excitation ultraviolette [1]. Les matériaux qui démontrent une PL visible à large bande efficace à température ambiante sans activateurs de métaux lourds sont d'un grand intérêt en tant qu'alternative potentielle aux luminophores céramiques dopés aux terres rares pour les sources de lumière blanche artificielle sur la base de lampes à décharge de gaz compactes et de diodes électroluminescentes . Bien que similaire SiO2 Les matériaux :C ont été rapportés précédemment pour démontrer une PL visible à large bande [2,3,4,5], l'origine des centres d'émission de lumière n'est pas claire jusqu'à présent. Une des hypothèses de base associe des centres d'émission dans SiO2 :C avec des nanoclusters de carbone [1, 2, 5]. Dans le cadre de ce modèle, SiO2 La nanopoudre peut être considérée comme un modèle morphologique avec une surface spécifique élevée qui fournit une concentration élevée de centres d'émission liés au carbone situés à la surface de la silice. La vérification de cette hypothèse nécessite évidemment une étude plus approfondie des propriétés luminescentes de la surface carbonisée dans les matériaux nanostructurés associés. L'alumine fumée est un bon candidat comme matrice morphologique avec une surface spécifique relativement élevée. D'excellentes propriétés mécaniques, une bonne inertie chimique et des structures électroniques font des céramiques à base d'alumine largement utilisées comme matériaux fonctionnels à haute température dans les dispositifs électriques et optiques [6,7,8,9,10,11]. PL excité optiquement et aux rayons X dans Al2 superfin O3 poudre avec surface intentionnellement carbonisée de nanoparticules est analysée dans le présent rapport. La procédure de carbonisation de surface était similaire à celle utilisée pour la carbonisation de la silice fumée dans [1], c'est-à-dire une procédure successive de greffage chimique de groupes phénylméthoxy à la surface de nanoparticules suivie de calcinations thermiques dans un environnement chimiquement inerte.
Méthodes
Al 2 pyrogène O3 poudre (89 m 2 /g, granulométrie 30-50 nm) a été traité avec une solution de phényltriméthoxysilane (PhTMS) toluène (1,73 ml de PhTMS pour 10 ml de toluène) à 70 °C pendant 4 h en présence de triéthylamine comme catalyseur. Le but de cette procédure est le greffage de groupements phénylméthoxy à la surface de l'alumine. Le produit de réaction (ci-après « phényl-alumine ») a été séché et soumis à un recuit thermique à des températures de 400, 500, 600 °С, pendant 30 min sous flux d'azote pur à pression atmosphérique.
La liaison interatomique a été étudiée par spectroscopie IR. L'analyse infrarouge à transformée de Fourier (FTIR) a été réalisée en mode transmission à l'aide du vide Bruker Vertex 70 V. Les spectres FTIR ont été enregistrés à température ambiante dans une plage spectrale de 400-5000 cm −1 à l'aide des pastilles échantillons KBr. La photoluminescence a été étudiée sous excitation ultraviolette (290 nm) et rayons X (13-14 keV). La photoluminescence sous excitation ultraviolette a été étudiée en utilisant une excitation par un laser à semi-conducteur de 290 nm (5 mW). Les spectres ont été enregistrés à l'aide du spectromètre LIFESPEC II (Edinburgh Instruments). La luminescence des rayons X était excitée par un rayonnement X avec une énergie de 13 à 14 keV. Le rayonnement des échantillons a été enregistré à l'aide d'un monochromateur MDR-2 et d'un photomultiplicateur FEP-106.
Résultats et discussion
Spectroscopie IR
Les spectres d'étude de transmission FTIR de l'alumine vierge et de la phényl-alumine sont illustrés à la figure 1. La matrice structurelle d'oxyde d'aluminium amorphe dans l'alumine vierge est représentée par de larges bandes d'absorption à 540 et 800 cm −1 (Fig. 1, spectre 1). Il est bien connu que l'oxyde d'aluminium cristallin existe dans une variété de structures métastables (alumines de transition - χ, γ, , , θ) ainsi que dans son -Al2 stable. O3 phase. La structure du polymorphe métastable peut être classée en fonction de la structure du sous-réseau d'anions d'oxygène (cubique à faces centrées ou hexagonal compact) et de la distribution des cations aluminium dans ce sous-réseau en tétraèdre (AlO4 ) et/ou octaédrique (AlO6 ) sites interstitiels [12]. Dans un solide amorphe, il n'y a pas de sens de polymorphisme cristallin, mais les propriétés de vibration des liaisons locales sont également déterminées par la coordination des atomes d'Al. Deux larges bandes à 540 et 800 cm −1 dans le spectre FTIR de l'alumine fumée vierge (Fig. 1, spectre 1) peut être attribué au mélange d'absorption par les vibrations d'étirement Al-O en coordination tétraédrique et octaédrique respectivement [13, 14].
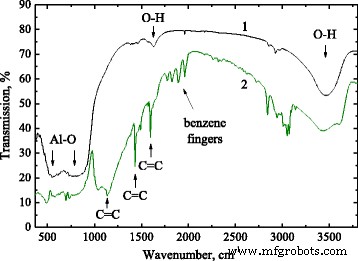
Spectres de transmission FTIR de l'alumine fumée vierge avant (spectre 1) et après traitement chimique (spectre 2). Les spectres sont décalés le long de l'axe des ordonnées pour plus de clarté
La large bande d'absorption comprise entre 3 000 et 3 800 cm −1 et la bande étroite à 1630 cm −1 (Fig. 2) sont attribués aux modes de vibration d'étirement et de flexion des liaisons O-H respectivement dus aux deux groupes hydroxyle de surface dans Al2 O3 et l'eau absorbée par la pastille de prélèvement de KBr [15]. Une faible absorption dans 2800–3000 cm −1 (C(sp 3 )–Hn ) est due à des contaminations organiques absorbées par l'atmosphère ambiante. Il convient de noter qu'après recuit de l'alumine vierge à une température allant jusqu'à 600 °C, le seul changement dans le spectre FTIR a été la disparition de la bande liée à C–H à 2800–3000 cm −1 .
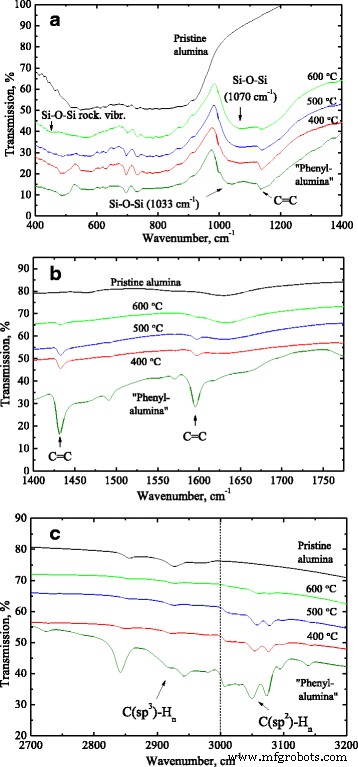
Gammes spectrales sélectionnées des spectres FTIR de l'alumine vierge (spectre 1) et de la phényl-alumine avant et après recuit à 400, 500 et 600 °C dans les gammes spectrales 400–1400 cm −1 (un ), 1400-1775 cm −1 (b ) et 2 700 à 3 200 cm −1 (c ). Les spectres sont décalés le long de l'axe des ordonnées pour plus de clarté
Quelques bandes d'absorption supplémentaires sont apparues après traitement chimique (Fig. 1, spectre 2). Bande d'absorption dans la gamme spectrale 2 800 à 3 000 cm −1 (C(sp 3 )–Hn ) est devenu beaucoup plus fort et s'accompagne maintenant d'une absorption à 3000-3100 cm −1 (C(sp 2 )–Hn ) en raison de l'hydrogène lié aux cycles benzéniques. Les cycles benzène des groupes phényle donnent naissance aux bandes étroites à 1136, 1430 et 1590 cm −1 (vibration C=C dans les anneaux benzéniques) ainsi qu'aux « doigts benzéniques » à 1700-2000 cm −1 due aux vibrations harmoniques/combinées dans les anneaux benzéniques. Une bande d'absorption forte et large dans une plage de 980 à 1 200 cm −1 et centré à 1033 cm −1 est évidemment due aux liaisons siloxanes. Une bande similaire a été observée dans les polymères à base de phényl-siloxane et associée à la réticulation des liaisons siloxane en réseau [16, 17]. Cette bande indique la formation de précipités de siloxane de type polymère à la surface d'Al2 O3 particules pendant la procédure de traitement chimique.
Les plages spectrales les plus informatives des spectres FTIR de la phényl-alumine avant et après le recuit sont illustrées à la Fig. 2. Bandes IR liées aux cycles benzéniques (1136, 1430 et 1590 cm −1 ) fortement réduite après recuit à 400 °С et à température plus élevée (Fig. 2ab). L'augmentation de la température de recuit jusqu'à 600 °C entraîne un décalage à haute fréquence de la bande liée au Si–O de 1033 à 1070 cm −1 indiquant la transition d'une structure de type polymère à une structure céramique. La position et la forme spectrales de cette bande sont devenues typiques de l'oxyde de silicium, indiquant la formation d'un réseau structurel de silice vraisemblablement à la surface de l'oxyde d'aluminium. Il est approuvé par l'apparence de l'épaule à 450-460 cm −1 qui peut être attribué aux vibrations de bascule Si–O–Si.
La figure 2b montre que l'augmentation d'une température de recuit entraîne une diminution de l'intensité des bandes d'absorption étroites à 1430 et 1594 cm −1 et qui est attribué aux vibrations d'étirement C=C dans les cycles phényle. Il est à noter que des traces d'absorption par des groupes phényles sont détectées jusqu'à la température de recuit la plus élevée. La destruction des cycles benzéniques ne provoque pas la formation de carbone pyrolytique amorphe généralement caractérisé par une large bande d'absorption d'environ 1600 cm −1 . L'absence de précipitation de carbone peut s'expliquer par la diffusion de charbon actif thermiquement depuis la surface à l'intérieur d'Al2 O3 particules lors du recuit en milieu inerte. Oxyde d'aluminium dopé au carbone (Al2 O3 :C) est un matériau bien connu largement utilisé en dosimétrie [11] et à taux de diffusion important du carbone dans Al2 O3 est observé même à des températures aussi basses que 400 °C [18].
La figure 2c illustre l'évolution des bandes liées à C–H à 2 800 à 3 100 cm −1 . On voit que les bandes d'absorption à 2800–3000 cm −1 , ce qui correspond à des vibrations d'étirement de (sp 3 )–Hn liaisons dans les groupes méthyle ainsi que groupe de bandes d'absorption à 3000-3100 cm −1 , qui correspond à (sp 2 )–Hn liaisons dans les cycles phényle fortement réduites après recuit, ce qui est bien compatible avec la dégradation thermiquement activée des groupes phényle.
Photoluminescence
La poudre d'alumine fumée vierge présente une photoluminescence à large bande relativement faible dans la plage spectrale de 300 à 600 nm sous une excitation de 290 nm (Fig. 3a, spectre 1). La large bande est composée d'au moins trois constituants avec des maxima à environ 335, 390-400 et 470 nm. La bande avec un pic à 335 nm est probablement due à un manque d'oxygène avec un électron piégé (F + -centres) [9]. Selon [19], la bande avec un maximum de 390 à 400 nm peut être associée à des paires de lacunes anion-cation (P − -centres) ou surface F + -centres (FS + -centres). La bande avec un maximum à 470 nm est éventuellement associée à F2 -centres [20], mais son identification correcte nécessite une analyse plus approfondie.
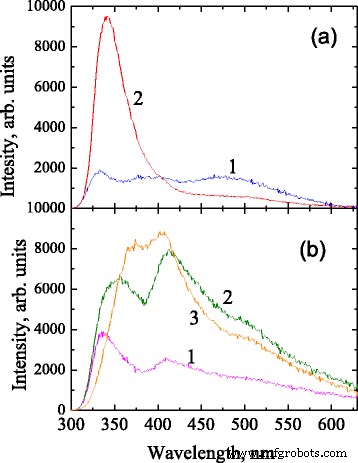
Spectres PL sous excitation de 290 nm. un Alumine fumée vierge (1 ) et de la phényl-alumine avant recuit (2 ). b Phényl-alumine après recuit à 400 °C (1 ), 500 °C (2 ) et 600 °C (3 )
Une bande PL intense avec un maximum à 340 nm apparaît dans Al2 O3 après traitement chimique (Fig. 3a, spectre 2). Cette bande est vraisemblablement associée à des états excimères dans des groupes phényle étroitement localisés greffés à la surface d'alumine [21,22,23]. La décomposition des groupes phényle lors du recuit conduit à la disparition de cette bande (Fig. 3b). La bande d'émission reste évidemment multicomposante après recuit mais l'augmentation de la température de recuit entraîne une évolution compliquée de l'intensité et de la distribution spectrale. L'augmentation de la température de recuit jusqu'à 500 °C entraîne une augmentation de l'intensité PL intégrée. Il convient également de noter que dans le spectre PL de l'échantillon recuit à une température de 500 °C, on observe un faible déplacement d'énergie et un élargissement du pic UV (Fig. 3b, spectre 2). L'augmentation de la température de recuit jusqu'à 600 °C entraîne un nouveau décalage de cette bande à 370 nm. La position spectrale du pic d'émission à 410 nm et de l'épaulement à 500 nm est restée presque inchangée après un recuit à 400-600 °C. Comme cela a été démontré par une étude IR, la structure de ces échantillons peut être représentée sous forme de précipités de silice (vraisemblablement avec des groupes de carbone) à la surface de nanoparticules d'alumine. Ces matériaux peuvent être indiqués comme Al2 O3 /SiOC. On pense que le mécanisme de formation des précipités de surface de SiOC est similaire à la polymérisation et à la réticulation structurelle dans les céramiques SiOC dérivées de polymères obtenues à partir d'un précurseur d'organosilicium contenant du phényle [17]. Il est également important de noter que l'alumine vierge recuite dans les mêmes conditions ne présente aucune photoluminescence notable. Par conséquent, il est raisonnable de s'attendre à une contribution de la silice et/ou du carbone -Centres d'émission liés dans la bande PL visible. Malheureusement, à l'heure actuelle, nous ne sommes pas en mesure d'identifier correctement l'évolution de la bande PL de ces échantillons.
L'utilisation de l'émission UV permet d'exciter des états électroniques avec une énergie d'excitation bien inférieure à la bande interdite de l'alumine et de la silice (généralement, il s'agit d'états électroniques associés à des défauts de volume et de surface). L'alumine et la silice ont une bande interdite très importante (9-10 eV), et l'examen de l'effet de l'excitation bande à bande nécessite des photons de haute énergie, par exemple une excitation par rayons X. Les spectres PL normalisés de l'alumine vierge (spectre 1), de la phényl-alumine (spectre 2) et de la phényl-alumine (spectre 3) recuits à 400 °C et sortis par rayons X à 90 K sont illustrés à la Fig. 4. Spectres PL d'alumine vierge et de phényl-alumine sont assez similaires, représentant une large bande avec une intensité maximale d'environ 470 nm. Aucune PL détectable n'a été observée à température ambiante. La similitude spectrale des bandes dans des échantillons vierges et modifiés chimiquement permet d'attribuer cette bande à l'émission des centres liés à l'alumine. L'excimère PL dans les groupes phényle ne semble pas être excité par un rayonnement de haute énergie. Une bande PL étroite et presque symétrique centrée à environ 550 nm apparaît dans le spectre de l'échantillon de la phényl-alumine après recuit à 400 °C (spectre 3). Une large bande de fond PL faible mais bien prononcée est également observée. L'origine de ce vaste arrière-plan vraisemblablement associé au réseau structurel d'alumine.
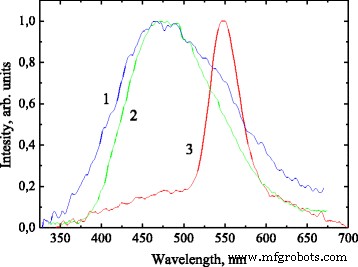
Spectres de luminescence normalisés sous excitation aux rayons X :alumine vierge (spectre 1), phényl-alumine (spectre 2) et phényl-alumine après recuit à 400 °C (spectre 3) à une température de 90 K
Compte tenu du fait que (1) la bande verte étroite PL n'est observée que sous excitation par rayons X (c'est-à-dire, haute énergie du photon d'excitation) et (2) la formation d'un réseau structurel de silice après recuit à 400 °C, il est raisonnable d'attribuer cette émission bande à l'exciton auto-piégé dans la structure de silice. La position spectrale de la bande PL est bien cohérente avec celle rapportée dans [24].
Conclusions
Al2 O3 :Des nanocomposites de SiOC ont été synthétisés en utilisant un traitement thermique de nanopoudre d'alumine fumée modifiée par du phényltriméthoxysilane. Les groupes hydroxyle à la surface des nanoparticules d'alumine ont été remplacés par des groupes phénylsiloxane suivis d'un recuit dans une plage de températures de 400 à 600 °C. Il est démontré que l'augmentation de la température de recuit entraîne la pyrolyse des groupes phényle et la formation de précipités de silice. Aucune précipitation de carbone n'a été détectée après pyrolyse des groupes organosiliciés. Il est suggéré que le développement de la photoluminescence après traitement thermique est dû à la formation de silice carbonisée à la surface des particules d'alumine.
Abréviations
- Al2 O3 :C:
-
Oxyde d'aluminium dopé au carbone
- Al2 O3 :SiOC :
-
Nanocomposite alumine/organosilicium
- F + -centre :
-
Vacance d'oxygène avec électron piégé
- F2 -centre :
-
Deux centres F adjacents
- Centre F :
-
Vacance d'oxygène avec deux électrons piégés
- FS + -centre :
-
Analogue de surface de F + -centre
- FTIR :
-
Transformée de Fourier infrarouge
- IR :
-
Infrarouge
- P − -centre :
-
Paires de vacances anion-cation
- PhTMS :
-
Phényltriméthoxysilane
- SiO2 :C:
-
Matériaux nanocomposites carbonisés à base de silice
Nanomatériaux
- Nanoparticules semi-conductrices
- Préparation et propriétés magnétiques des nanoparticules de spinelle FeMn2O4 dopées au cobalt
- Synthèse facile et propriétés optiques de petits nanocristaux et nanotiges de sélénium
- Détection photo-électrochimique améliorée de l'acide urique sur une électrode de carbone vitreuse modifiée par nanoparticules d'Au
- Influence de l'eau sur la structure et les propriétés diélectriques de la microcristalline et de la nano-cellulose
- Nouveaux nanoparticules Au Nanostars@PEG biocompatibles pour l'imagerie CT in vivo et les propriétés de clairance rénale
- Effets de l'épaisseur de la bicouche sur les propriétés morphologiques, optiques et électriques des nanolaminés Al2O3/ZnO
- Réglage des morphologies de surface et des propriétés des films de ZnO par la conception de la couche interfaciale
- Les effets de couplage des polaritons de plasmon de surface et des résonances dipolaires magnétiques dans les métamatériaux



