Agrégation horizontale d'oxyde de graphène réduit en monocouche sous irradiation UV profonde en solution
Résumé
Le graphène a été largement utilisé dans de nouveaux dispositifs optoélectroniques depuis des décennies. De nos jours, la fabrication de graphène monocouche de grande taille avec une sélectivité spectrale est très demandée. Ici, nous rapportons une méthode simple pour synthétiser du graphène monocouche de grande taille avec des groupes chimiquement fonctionnalisés en solution. Les quelques couches de nano-graphène peuvent être exfoliées en nano-graphène monocouche sous irradiation UV de courte durée dans une solution protique. Le nano-graphène monocouche exfolié pourrait subir une désoxygénation lors d'une exposition prolongée aux UV. Dans le même temps, le bord du nano-graphène pourrait être activé sous une exposition aux UV profonds et des feuilles de nano-graphène de petite taille s'agrègent davantage horizontalement en solution. La taille du rGO agrégé passe de 40 nm à un maximum de 1 μm. Cette approche pourrait être une méthode peu coûteuse et prometteuse pour synthétiser à l'avenir de l'oxyde de graphène réduit en monocouche de grande taille.
Contexte
Le graphène est un matériau potentiel pour les dispositifs optoélectroniques et de photodétection ultrafins en raison de sa mobilité élevée des porteurs et de sa transparence optique élevée [1, 2]. La clé de la photoréponse élevée des dispositifs à base de graphène est le décalage du niveau de fermi induit par l'injonction de porteurs [3]. Avec le développement du dépôt chimique en phase vapeur (CVD), la croissance de graphène de grande taille ainsi que la fabrication de dispositifs à base de graphène deviennent pratiques. Cependant, le dispositif de photoréponse à base de graphène a généralement une faible absorption et une mauvaise sélectivité spectrale. La méthode courante utilisée pour surmonter cet inconvénient consiste à hybrider du graphène avec des points quantiques [4], une nanostructure plasmonique [5] ou d'autres matériaux 2D avec des lacunes énergétiques [6] afin de réaliser une injection de porteurs photo-induite. Bien que la méthode CVD favorise la fabrication de la croissance de graphène de grande taille, le processus de dépôt se produit généralement dans un environnement extrême, tel qu'un vide poussé, un substrat hautement sélectionné, etc. Cela limite la fabrication d'agrandissement pour une fabrication commerciale. Il est urgent de développer des méthodes nouvelles et peu coûteuses. L'exfoliation par solvant pour quelques flocons de couche est l'une des méthodes efficaces et peu coûteuses dans la fabrication de graphène [7,8,9,10,11,12,13,14,15]. La méthode la plus utilisée est la méthode de Hummer modifiée. Le graphite peut être oxydé et exfolié en quelques couches de graphène. Pendant ce temps, le graphène fabriqué par exfoliation chimique oxydée contient généralement divers groupes fonctionnels qui peuvent améliorer l'absorption optique et la sélectivité spectrale. D'autre part, le processus d'exfoliation oxydé endommage généralement la cristallinité de sp 2 domaine [16], qui nécessite une température extrêmement élevée pour la récupération. Bien que le processus de réaction thermique puisse récupérer le sp 2 domaine, presque tous les groupes fonctionnels sont également supprimés, ce qui conduit à nouveau à une faible absorption et à une mauvaise sélectivité spectrale. Nous rapportons ici une nouvelle stratégie pour fabriquer du graphène monocouche fonctionnalisé chimiquement de grande taille par irradiation UV profonde. Le nano-graphène en couches peut être exfolié en monocouche sous une exposition UV de courte durée. Le nouveau sp 2 domaine peut être restauré lors d'une exposition prolongée aux UV. De plus, l'atome de carbone de bord peut être activé pendant l'irradiation UV, conduisant plusieurs feuilles de nano-graphene monocouche à s'agréger horizontalement pour former du graphène monocouche de grande taille.
Méthode expérimentale
Fabrication d'oxyde de graphène
L'oxyde de graphène (GO) a été synthétisé à partir de graphite naturel en modifiant la méthode de Hummer comme indiqué dans nos travaux précédents [17]. Le mélange résultant a été lavé avec une solution de HCl à 5 % et DI des dizaines de fois. Enfin, le solide GO a été obtenu après lyophilisation.
Synthèse de quelques couches de nano-graphène et croissance pour un oxyde de graphène réduit de grande taille
4,4 mg de solide GO ont été transférés dans un autoclave revêtu de téflon et 12 mL d'éthanol (ou N ,N -diméthylformamide (DMF)) a été ajouté. Le mélange a été chauffé à 176 °C pendant 5 h. Le surnageant a été filtré sur membrane microporeuse de 0,22 µm. Enfin, la solution colloïdale était la solution de nano-graphène à quelques couches.
4,4 mg de solide GO ont été transférés dans un autoclave revêtu de téflon et 15 mL de DI ont été ajoutés. Le mélange a été chauffé à 176 °C pendant 5 h. Puis le surnageant a été filtré sur membrane microporeuse de 0,22 µm. La solution colloïdale était la solution de nano-graphène monocouche.
L'exfoliation de quelques couches de nano-graphène et la croissance d'oxyde de graphène réduit de grande taille (rGO) ont été obtenues par irradiation de lumière UV profonde (3 W, 254 nm), comme illustré dans le schéma 1.
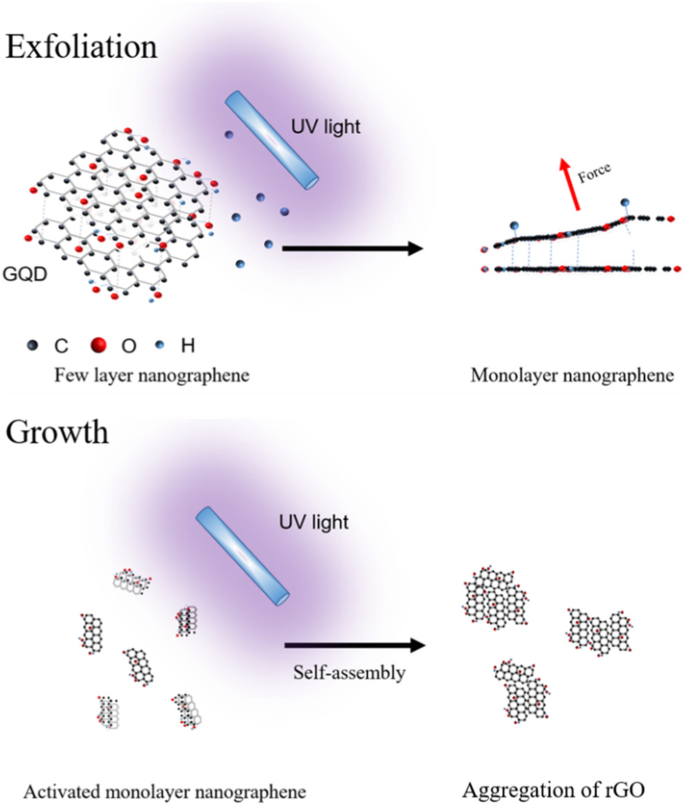
Illustration schématique de l'exfoliation de quelques couches de nano-graphène en monocouche et de l'agrégation de rGO sous irradiation UV
Caractérisation de l'échantillon
La photoluminescence (PL) et l'infrarouge transformé de Fourier (FTIR) ont été mesurées respectivement sur un spectromètre à fluorescence en régime permanent (FluoroMax-4, Horiba, Jobin Yvon) et un spectromètre FTIR (Nicolet 8700, Thermo Scientific). La morphologie et la hauteur ont été caractérisées par microscopie à force atomique (AFM) fonctionnant en mode tapotement à température ambiante sur substrat Si (NT-MDT Prima). La cristallinité de l'échantillon a été réalisée au microscope électronique à transmission à haute résolution (HRTEM) (JEM-2100F, JEOL).
Résultat et discussion
L'AFM a été utilisé pour caractériser la morphologie et la taille du nano-graphène. Les résultats du nano-graphène sous différentes durées d'irradiation UV sont présentés sur la figure 1. Pour le nano-graphene frais, les diamètres sont principalement répartis dans la plage de 30 à 60 nm et la hauteur est> 2,5 nm (Fig. 1a). La hauteur de notre nano-graphène est similaire à celles observées dans le nano-graphène fonctionnalisé par groupe chimique avec une épaisseur de 2 à 3 couches [10, 18, 19]. À partir des données de l'AFM, nous déterminons que plus de 85 % de nano-graphène sont formés en empilant 2 à 3 couches de nano-graphène monomère par la force de Van der Waals (vdW). Ainsi, nous les appelons nano-graphène à quelques couches. Les quelques couches de nano-graphène ont pu être exfoliées en nano-graphène monocouche sous irradiation d'une lampe UV à 254 nm (3 W). La figure 1b–d montre la morphologie de quelques couches de nano-graphène sous une exposition UV de 30 s, 50 s et 240 s, respectivement. Il y a à peine un changement de taille après une courte exposition aux UV. Cependant, la distribution de la hauteur du nano-graphène sous divers temps d'exposition aux UV montre clairement que la hauteur de quelques couches de nano-graphène diminue de> 2,5 nm à < 1,0 nm après plusieurs minutes d'exposition aux UV, indiquant que les quelques couches de nano-graphène ont été exfoliés à monocouches.
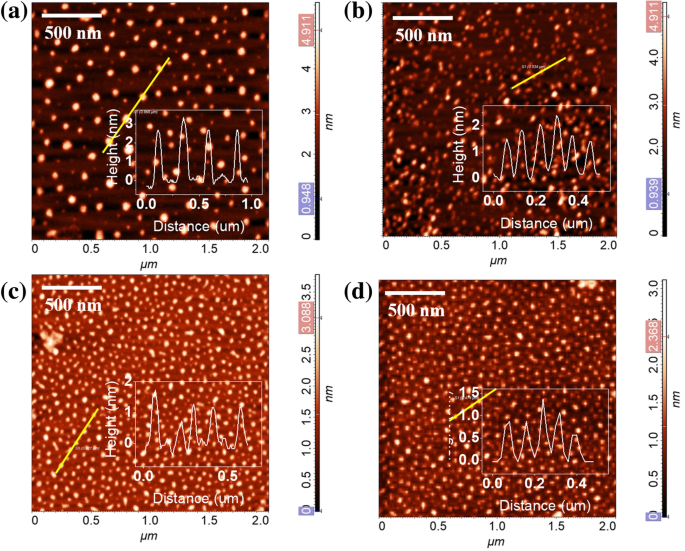
Images AFM de quelques couches de nano-graphène avec divers temps d'exposition aux UV a –d : 0, 30 s, 50 s, 240 s, l'insert est la distribution en hauteur du nano-graphène
La figure 2a est une image au microscope électronique à transmission à haute résolution (HRTEM) d'une couche monocouche de nano-graphène préparée par irradiation UV. Le réseau cristallin du nano-graphène peut être clairement observé. La transformée de Fourier rapide (FFT) de la région sélectionnée est illustrée dans l'encart de la figure 2a, reflétant la structure cristalline hexagonale. L'espacement du réseau dans le plan est de 0,219 nm, ce qui est cohérent avec le réseau du plan [001] [20].
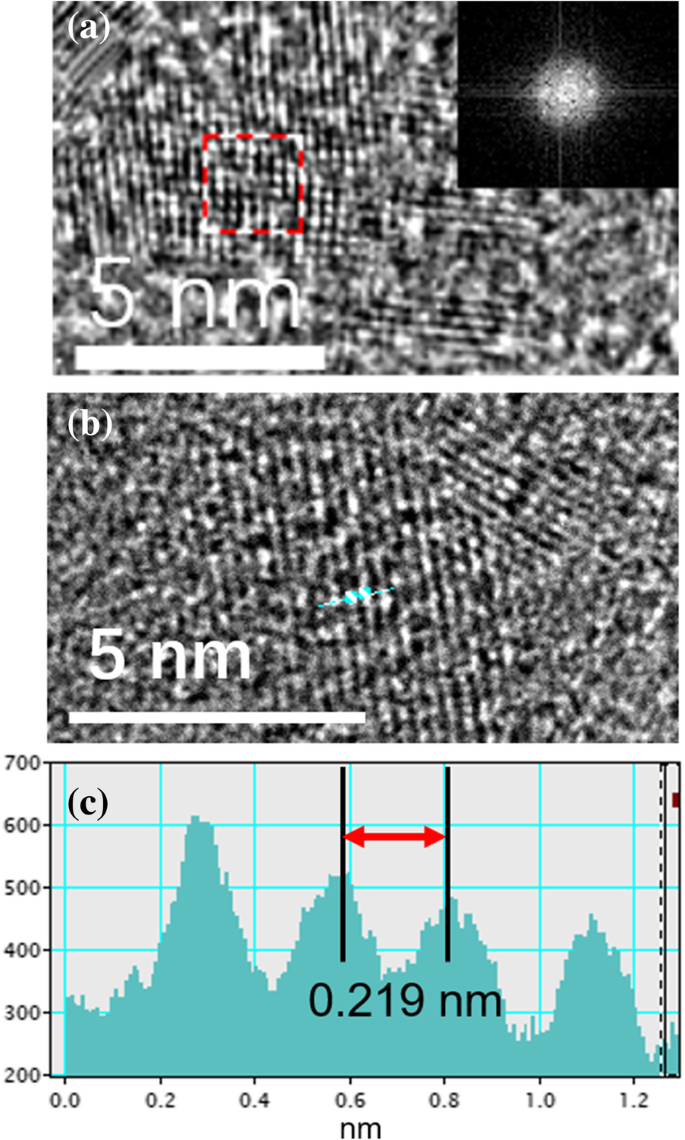
un Images HRTEM de nano-graphène. Encart :image FFT d'une zone sélectionnée. b HRTEM et c profil de ligne du nano-graphène sélectionné
Comme rapporté par Lee et al. [21], les atomes d'hydrogène se lient à la surface du graphène et ils peuvent apporter aux atomes de carbone (C) une force hors du plan. Cette force modifie la configuration des atomes de carbone dans le graphène et peut détruire la force vdW entre les différentes couches de graphène. Par conséquent, sous l'action de la liaison hydrogène, le graphène empilé sera exfolié en une seule couche. Selon la littérature, la spectroscopie Raman du graphène peut fournir des informations importantes pour l'hydrogénation planaire du graphène [21, 22]. Le rapport d'intensité entre D et G (Je D /Je G ) modèle de diffusion Raman peut refléter la façon dont l'atome d'hydrogène est attaché au graphène. Pour étudier le mécanisme d'exfoliation, les spectres Raman de quelques couches de nano-graphène sous divers temps d'exposition aux UV ont été mesurés. Les résultats sont présentés sur la figure 3. Les spectres Raman ont été ajustés par le modèle de Lorenz pour calculer avec précision le rapport d'intensité de pic. Les données montrent que I D /Je G augmente de 1,21 à 1,43, indiquant la présence d'hydrogène de liaison sur la surface de quelques couches de nano-graphène après exposition aux UV. L'atome C se déplace vers la direction hors du plan et conduit à la rupture de la force vdW entre les couches de graphène [21]. Comme illustré dans le schéma 1, l'atome d'hydrogène peut se lier à la surface de quelques couches de nano-graphène et la force hors de la plante induite par le réarrangement de l'atome C peut exfolier les quelques couches de nano-graphène en monocouche de nano-graphène.
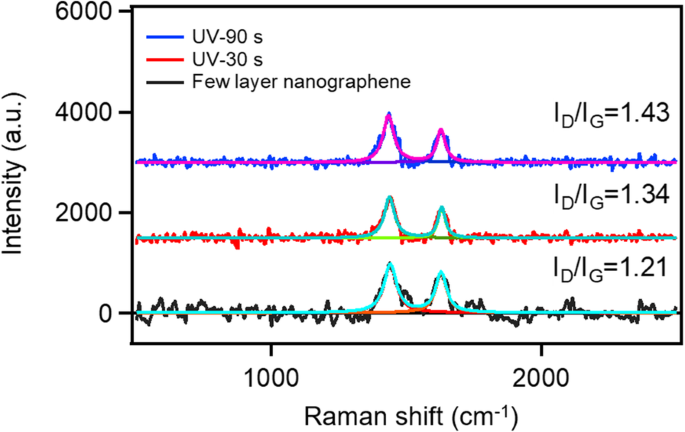
Spectres Raman de quelques couches de nano-graphène sous divers temps d'exposition aux UV
La surface de l'oxyde de graphène est généralement riche en groupes fonctionnels contenant de l'oxygène tels que -COOH, C-OH, C-O-C, etc. Ces groupes fonctionnels contenant de l'oxygène introduisent des états de défaut, qui sont des sources importantes de luminescence d'oxyde de graphène. Par conséquent, il est très important d'étudier les changements du groupe fonctionnel du nano-graphène pendant l'irradiation UV. L'absorption infrarouge est une méthode très efficace pour étudier les changements de groupes fonctionnels chimiques. Le mécanisme d'exfoliation peut être mieux compris en mesurant les changements dans les spectres d'absorption infrarouge du nano-graphène irradié par la lumière ultraviolette. La figure 4 montre les spectres infrarouges à transformée de Fourier (FTIR) de quelques couches de nano-graphène sous différentes durées d'irradiation UV. Pour les quelques couches de nano-graphène, les modes vibrationnels sont indiqués pour les époxydes (C-O-C, 900-1260 cm −1 ). Le pic d'absorption à 1740 cm −1 et 3129 cm −1 correspondent au mode d'étirement du carboxyle lié à un atome de C (-COOH). L'absorption à 2850 cm -1 et 2920 cm −1 révèlent l'existence de C-H. L'absorption à large bande (3 100 à 3 700 cm −1 ) a culminé à 3 450 cm −1 est attribué aux groupes hydroxyle (-C-OH). L'absorption C=C de la sp 2 intrinsèque domaine à 1641 cm −1 est également présenté. Après une courte irradiation UV (240 s), les pics du groupe époxy, du groupe hydroxyle, du groupe carboxyle et C=C n'ont pas changé de manière significative. Cependant, le pic d'absorption de C-H devient plus prononcé. Ceci est cohérent avec le résultat que nous avons obtenu de Raman, indiquant que l'atome H se lie à l'atome C et améliore l'absorption de C-H. Il montre également que l'irradiation UV de courte durée ne conduit pas à la réduction du nano-graphène et que les groupes fonctionnels de l'oxygène dans le nano-graphène ne changent pas pendant le processus d'exfoliation.
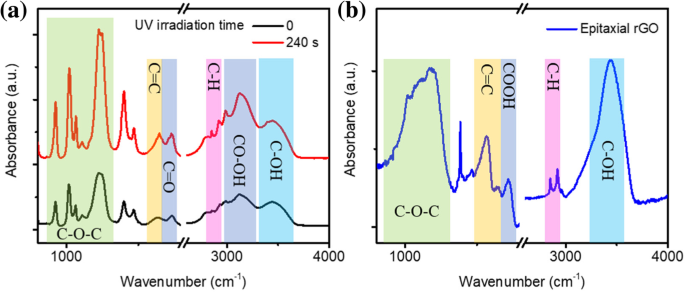
FTIR de (a ) nano-graphène à quelques couches (ligne noire), nano-graphène monocouche (ligne rouge) et (b) nano-graphène épitaxié
D'autre part, les spectres FTIR du nano-graphène changent de manière significative (Fig. 4b) après une longue période d'irradiation UV (2 h). Le premier changement est que l'absorption de -COOH à 3150 cm −1 est considérablement réduit. Dans le même temps, une nouvelle absorption de C-O-C se produit et elle chevauche l'absorption précédente de C-O-C, ce qui entraîne une absorption importante de C-O-C. Deuxièmement, l'absorption de C=O passe de 1740 cm −1 dans la direction du faible nombre d'ondes (1720 cm −1 ). Ceci est dû à l'augmentation du système conjugué. Le troisième changement majeur est l'apparition d'un nouveau pic d'absorption dans le plan C=C à 1562 cm −1 . En effet, ce processus de photo-réduction de GO peut induire une désoxygénation et restaurer la sp 2 domaine [16, 23, 24]. Enfin, une augmentation supplémentaire de l'absorption de C-H est observée puisque davantage d'atomes de H se combinent avec des atomes de C.
Afin d'étudier l'effet des changements de couche sur les propriétés optiques, nous mesurons la fluorescence en régime permanent du nano-graphène sous différents temps d'exposition aux UV. La figure 5a montre les spectres PL du nano-graphène sous une irradiation UV à différents temps. Le nano-graphène à quelques couches tel que préparé émet une lumière UV profonde pure culminant à 307 nm et l'intensité diminue rapidement avec l'augmentation du temps d'irradiation UV. Pendant ce temps, l'intensité PL centrée à 500 nm augmente. Les courbes de la figure 5b présentent la relation entre les durées d'irradiation UV et l'intensité PL à 307 nm et 500 nm. À mesure que la durée d'irradiation UV augmente, l'émission à 307 nm disparaît presque et l'émission de lumière visible à 500 nm domine le spectre PL pendant le processus d'exfoliation.
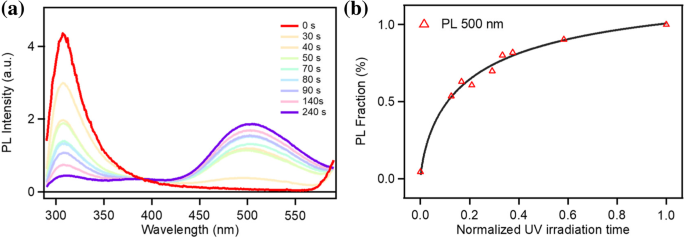
Spectres PL stables de quelques couches de nano-graphène avec divers temps d'exposition aux UV excités à 270 nm
La fluorescence du graphène a été systématiquement étudiée. L'origine de la luminescence est principalement attribuée à la fluorescence induite par l'état propre provoquée par le sp 2 domaine (302 à 380 nm) et sp 3 défaut de luminescence causé par le groupe fonctionnel contenant de l'oxygène [19, 25, 26, 27]. Pour le nano-graphène à quelques couches, l'hétérojonction de Van der Waals (vdW) se forme en raison de l'empilement de quelques couches de nano-graphène. L'hétérojonction vdW effectue une séparation de charge élevée. L'électron excité dans les états de défauts de surface induits par les groupes fonctionnels oxygène serait transféré aux états intrinsèques induits par C=C sp 2 domaine en raison de la flexion de la bande induite par l'empilement. Les quelques couches de nano-graphène émettent une lumière UV pure. Nous attribuons la luminescence avec un pic à 307 nm à la fluorescence de l'état propre du sp 2 domaine. Pendant ce temps, la partie visible (pic à 500 nm) est dérivée de la luminescence des états de défaut comme le rapporte la littérature [19, 25]. Il est clair que la fluorescence de l'état propre de la sp 2 domaine disparaît progressivement à mesure que le nano-graphène est exfolié en monocouche et nous pensons que le changement d'épaisseur du nano-graphène est la principale raison du changement de fluorescence.
Pour une représentation plus claire et intuitive du changement dans les groupes fonctionnels d'oxyde de graphène pendant le processus de réduction, nous avons mesuré la fluorescence à l'état d'équilibre pendant le processus de réduction (Fig. 6). La fluorescence de la partie visible du nano-graphène est dérivée de défauts de surface causés par des groupes fonctionnels contenant de l'oxygène. Différents groupes fonctionnels provoquent différentes profondeurs d'états de défaut, ce qui conduit également à différentes émissions de fluorescence [26, 27]. Konkena et al. étudié en détail la relation entre les groupes fonctionnels et la fluorescence. La fluorescence de notre nano-graphène à 500 nm est dérivée du groupe carboxyle déprotoné. Comme le montre la figure 6, l'augmentation du temps d'exposition aux UV entraîne une diminution progressive de l'intensité PL à 500 nm et le pic d'émission passe de 500 nm à environ 475 nm après 2 h d'exposition aux UV. L'évolution des spectres dans le domaine visible est similaire à celle rapportée dans le processus de réduction chimique du graphène [16, 28]. L'émission caractéristique à 500 nm est le symbole des groupes carboxyliques dans leurs états de déprotonation. L'émission bleue (475 nm) provient des groupes carboxyliques dissociés [28]. Avec l'augmentation du temps d'irradiation UV, les groupes carboxyliques ont été dissociés, ce qui est conforme à la disparition de l'absorption IR de C=O à 1730 cm −1 (Fig. 4). Ainsi, les spectres PL effectuent une diminution et un décalage vers le bleu de l'émission visible.
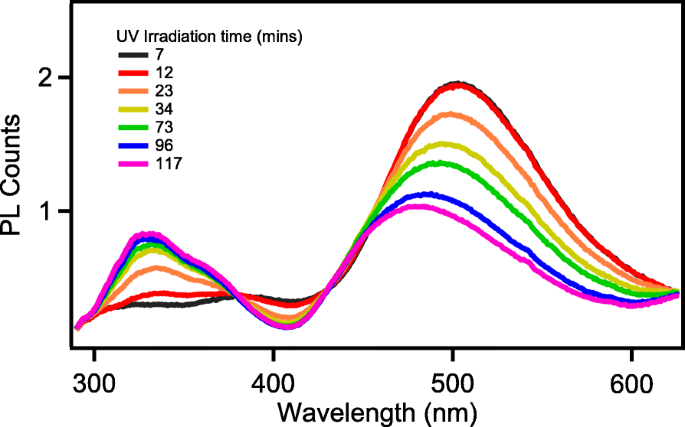
PL stable de nano-graphène monocouche après différentes périodes d'exposition aux UV
Accompagnée du changement d'émission visible, un phénomène surprenant, l'émission UV centrée à 326 nm avec un épaulement à 360 nm est montrée et augmente avec le temps de réduction. La réduction de l'oxyde de graphène s'accompagne généralement de la formation d'un nouveau sp 2 domaine [29]. Nous supposons que cela pourrait être dû à l'agrégation de nano-graphène provoquant une augmentation de la fluorescence ultraviolette.
Pour examiner plus en détail les changements de structure physique du nano-graphène après une irradiation UV de longue durée, nous avons mesuré la morphologie de rGO à l'aide de l'AFM. Comme illustré sur la figure 7, de nombreuses nanofeuillets de grande taille ont été observés après 2 h d'exposition aux UV. La distribution de taille de rGO est beaucoup plus large (300-750 nm) par rapport à celle du nano-graphène tel que préparé. La taille accrue peut être attribuée à l'agrégation horizontale de nano-graphène monocouche. L'agrandissement de l'image AFM montre clairement que les nano-feuilles plus grandes sont entourées de nombreuses feuilles de nano-graphène de petite taille avec une hauteur moyenne de 0,7 nm. Après le processus de désoxygénation, les atomes O au bord du nano-graphène sont actifs et pourraient se lier avec l'atome de bord C d'un autre nano-graphène pour former de nouveaux époxydes. Comme illustré dans le schéma 1, avec une réduction croissante, le nombre de nano-graphène activé augmenterait et la taille continuerait d'augmenter. Considérant qu'à mesure que la durée d'irradiation UV est prolongée, la partie émettant de la lumière ultraviolette est améliorée. Nous pensons que la luminescence UV à 326 nm provient de l'agrégation de nano-graphène. Lorsque le nombre d'agglomérats augmente, l'intensité de la fluorescence ultraviolette augmente également. Le nano-graphène monocouche est stable et aucun précipité n'a été observé même après 2 h d'irradiation UV (Fig. 7).
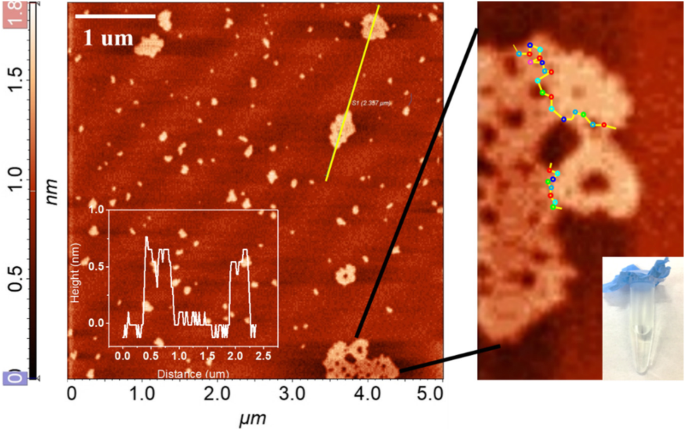
AFM de nano-graphène monocouche sous exposition excessive aux UV, en médaillon :photos numériques de rGO agrégé
Parce que l'intensité est directement liée à l'agrégation, nous étudions la dynamique d'agrégation du nano-graphène en analysant le PL dans la gamme UV. Le temps d'exposition aux UV a été normalisé pour la concentration de nano-graphène liés les uns aux autres. La figure 8 présente la corrélation entre la concentration et l'intensité des UV. Les données expérimentales ont été ajustées par le modèle isotherme d'adsorption de Langmuir. Avec l'augmentation du temps d'exposition aux UV, le nombre de nano-graphène agrégé augmente également ainsi que la taille augmente. Le nombre de nano-graphène adsorbé peut être exprimé en N et l'isotherme d'adsorption de Langmuir peut s'écrire
$$ N=\frac{N_0k{(nx)}^{\left(1-c\right)}}{1+k{(nx)}^{\left(1-c\right)}} $$ (1)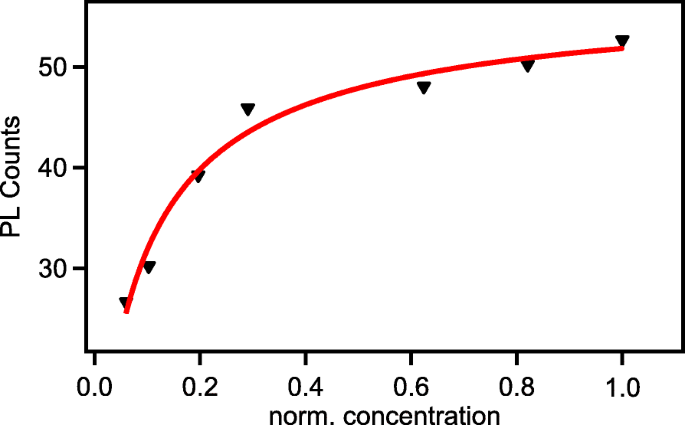
Intensité UV PL par rapport à la concentration normalisée
Ici, N 0 est l'intensité UV initiale. La constante d'équilibre associée k peut être obtenu en ajustant les données expérimentales. Pour un système à l'équilibre chimique, l'énergie libre de Gibbs est donnée
$$ \Delta G=- RT1\mathrm{n}(k) $$ (2)Lorsque nous avons appliqué k à l'éq. 2, nous donnons l'énergie libre de Gibbs ∆G ≈ − 4,43 kJ/mol. Le ∆G < 0 indique que cette réaction est la thermodynamique favorisée à température ambiante [30]. Ainsi, plusieurs nano-graphènes pourraient se lier horizontalement pour former des agglomérats de grande taille. Il convient de souligner que le graphène de grande taille préparé par CVD possède un sp 2 fin. structure mais ne contient pratiquement aucun groupe fonctionnel pour la sélectivité spectrale. Notre agrégation de nano-graphène induite par UV pourrait contenir divers groupes fonctionnels qui ont une propriété optique unique et peuvent être utilisés comme sites d'identification pour une détection sélective.
Afin d'étudier l'effet des solvants sur la structure du nano-graphène, nous avons préparé du nano-graphène dans le solvant aprotique DMF et le solvant protique H2 O. La figure 9 montre le PL et l'AFM du nano-graphène fabriqué en DMF et H2 O. Le PL du nano-graphène dans le DMF effectue une émission UV profonde, qui provient de l'empilement de la couche de nano-graphène. Il n'y a qu'un léger changement même après 115 minutes d'irradiation UV. Cela indique qu'après une longue période d'exposition à la lumière ultraviolette, aucune exfoliation ou agrégation ne se produit. La distribution en hauteur du nano-graphène dans le DMF est illustrée à la figure 9b. La hauteur moyenne est> 15 nm. Le PL du nano-graphène dans H2 O est centré à ~ 475 nm (Fig. 9c). Il y a une émission d'UV et un décalage de pic sous diverses irradiations UV dans le temps. Cette émission visible de nano-graphène est attribuée aux états de défauts induits par l'oxygène fonctionnel. La hauteur du nano-graphène dans H2 O est < 1,0 nm (Fig. 9d) et cela suggère que le nano-graphène est monocouche dans H2 O. Les résultats ci-dessus montrent que l'empilement du nano-graphène peut être contrôlé en utilisant différents solvants.
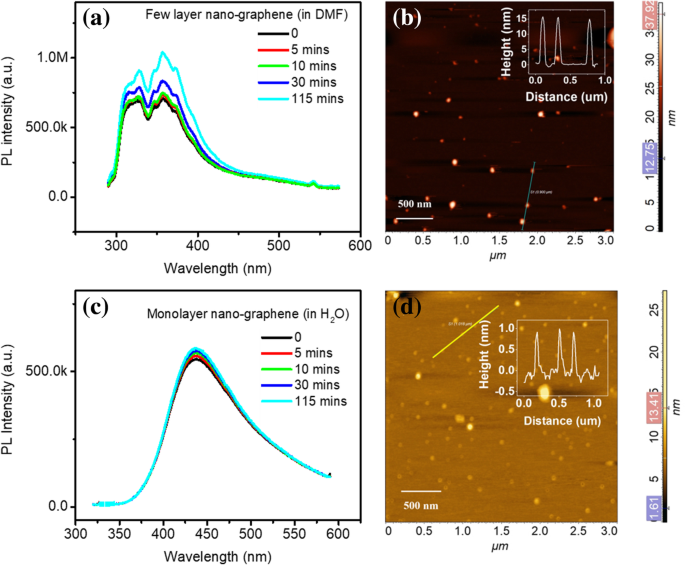
Image PL et AFM du nano-graphène dans le DMF (a , b ) et H2 O (c , d )
Conclusions
En résumé, nous avons découvert que peu de couches de nano-graphène peuvent être exfoliées en monocouche de nano-graphène en raison de l'atome H lié à la surface sous une irradiation UV profonde de courte durée dans une solution protique. Le nano-graphène monocouche pourrait s'agréger en rGO monocouche de grande taille sous une irradiation UV prolongée. Les résultats de l'AFM montrent clairement que le rGO monocouche de grande taille est formé par l'agrégation de plusieurs petites feuilles de nano-graphène. L'agrégation de petits nano-graphènes est en accord avec le modèle d'isotherme d'adsorption de Langmuir, qui indique que le bord du nano-graphène peut être activé et peut se lier avec d'autres nano-graphènes. Cette méthode de croissance induite par les UV pourrait favoriser la fabrication à faible coût et à grande échelle de graphène monocouche à l'avenir.
Abréviations
- AFM :
-
Microscopie à force atomique
- CVD :
-
Dépôt chimique en phase vapeur
- FTIR :
-
Infrarouge à transformée de Fourier
- GO :
-
Oxyde de graphène
- PL :
-
Photoluminescence
- TEM :
-
Microscope électronique à transmission
Nanomatériaux
- Nanotubes de titanate Nanocomposites d'oxyde de graphène décoré :préparation, ignifugation et photodégradation
- Biosécurité et capacité antibactérienne du graphène et de l'oxyde de graphène in vitro et in vivo
- Les échafaudages nHAC/PLGA hybrides à l'oxyde de graphène facilitent la prolifération des cellules MC3T3-E1
- Évaluation des structures graphène/WO3 et graphène/CeO x en tant qu'électrodes pour les applications de supercondensateurs
- Composite Si/Graphène intégré fabriqué par réduction thermique au magnésium comme matériau d'anode pour les batteries lithium-ion
- Préparation par broyage à billes en une étape de l'oxyde de graphène/CL-20 à l'échelle nanométrique pour une taille et une sensibilité des particules considérablement réduites
- Activité photocatalytique du nanocomposite ternaire attapulgite–TiO2–Ag3PO4 pour la dégradation de la Rhodamine B sous irradiation solaire simulée
- Réduction à basse température de l'oxyde de graphène :conductance électrique et microscopie à force de sonde Kelvin à balayage
- L'oxyde de graphène réduit intercalé tensioactif anionique/liquides ioniques pour supercondensateurs hautes performances



