Activité photocatalytique du nanocomposite ternaire attapulgite–TiO2–Ag3PO4 pour la dégradation de la Rhodamine B sous irradiation solaire simulée
Résumé
Un excellent photocatalyseur composite ternaire constitué d'orthophosphate d'argent (Ag3 Bon de commande4 ), l'attapulgite (ATP) et le TiO2 a été synthétisé, dans lequel une hétérojonction s'est formée entre des semi-conducteurs dissemblables pour favoriser la séparation des charges photo-générées. L'ATP/TiO2 /Ag3 Bon de commande4 Le composite a été caractérisé par SEM, XRD et spectroscopie de réflectance diffuse UV-vis. La co-dépôt d'Ag3 Bon de commande4 et TiO2 les nanoparticules à la surface de l'ATP forment une structure de particules de latte. Par rapport aux photocatalyseurs composites constitués de deux phases, ATP/TiO2 /Ag3 Bon de commande4 Le composite ternaire présente une activité photocatalytique grandement améliorée pour la dégradation de la rhodamine B sous une irradiation solaire simulée. Un tel composite ternaire améliore non seulement la stabilité de Ag3 Bon de commande4 , mais réduit également le coût en réduisant la quantité de demande d'Ag3 Bon de commande4 , qui fournit des conseils pour la conception de Ag3 Bon de commande4 - et composites à base d'Ag pour les applications photocatalytiques.
Contexte
La dégradation des polluants organiques a été un processus critique vers la résolution de la pollution de l'environnement. Fujishima et al. rapporté en 1972 que TiO2 a la capacité d'utiliser l'énergie solaire pour la séparation de l'eau et la production d'hydrogène [1]. Depuis lors, la technologie photocatalytique à base de semi-conducteurs est devenue une approche prometteuse et pourtant efficace pour résoudre la pollution de l'environnement. Au cours des dernières décennies, un certain nombre de semi-conducteurs, tels que TiO2 , Ag3 Bon de commande4 , BiVO4 , WO3 , et g-C3 N4 , ont été largement étudiés pour une application photocatalytique [2]. Parmi eux, TiO2 a reçu une grande attention en raison de sa bonne stabilité chimique, de sa non-photocorrosion, de son faible coût et de sa non-toxicité. En raison de sa large bande interdite (3,2 eV) et de l'absence d'absorption de la lumière visible, cependant, TiO2 présente une faible efficacité photocatalytique. L'application du TiO2 -à base de photocatalyseurs a donc été sévèrement entravé.
Les photocatalyseurs, tels que Ag3 Bon de commande4 [3], Bi2MoO6 [4], AD3 [5], et g-C3 N4 [6], peuvent présenter une efficacité élevée sous irradiation de lumière visible, et ont ainsi suscité des efforts de recherche approfondis. Par exemple, Ye et al. ont signalé que l'orthophosphate d'argent (Ag3 Bon de commande4 ) présentait des capacités photooxydantes beaucoup plus fortes et une efficacité plus élevée pour la dégradation photocatalytique [3] que la plupart des autres photocatalyseurs connus tels que WO3 [5] et BiVO4 [sept]. Cependant, la stabilité photocatalytique de Ag3 Bon de commande4 pourrait être détérioré par la photoréduction d'Ag + en Ag métallique. La faible photostabilité et le coût élevé de l'Ag3 Bon de commande4 concernent des problèmes qui limiteront ses applications photocatalytiques. Dans ce contexte, Ag3 Bon de commande4 -des photocatalyseurs composites ont été étudiés dans le but d'améliorer sa photostabilité et sa photocatalyse, tels que TiO2 /Ag3 Bon de commande4 [8], Ag3 Bon de commande4 /graphène [9], et Ag3 Bon de commande4 /Ag/WO3-x [10].
L'attapulgite (ATP) est une sorte de minéral non métallique en silicate de magnésium et d'aluminium hydraté en forme de tige, qui possède des propriétés physiques et chimiques remarquables, telles que des cations échangeables, une absorption d'eau, une décoloration par adsorption et une grande surface spécifique [11]. L'ATP est donc considéré comme un support de catalyseur idéal avec une morphologie de tige, et sa surface spécifique élevée est avantageuse pour l'absorption du catalyseur et des polluants. Bien que Ag3 Bon de commande4 - et TiO2 -base et attapulgite/Ag3 Bon de commande4 des photocatalyseurs composites binaires ont été signalés, les matériaux composites ternaires à base d'attapulgite ont rarement été étudiés.
Dans ce travail, l'ATP/TiO2 /Ag3 Bon de commande4 les composites ternaires ont été synthétisés par une méthode facile en deux étapes pour améliorer la photostabilité et la photocatalyse de Ag3 Bon de commande4 et la suppression de la consommation de métal noble Ag. La structure cristalline et la microstructure de nouveaux composites ternaires ont été caractérisées par XRD et SEM, respectivement, tandis que leurs activités photocatalytiques et leur stabilité ont été mesurées par dégradation du colorant organique rhodamine B (RhB) sous irradiation solaire simulée. Ce composite ternaire présente une efficacité photocatalytique plus élevée que le phosphate d'argent pur et une excellente stabilité photocatalytique.
Section expérimentale
Matériaux
Les nanofibres ATP d'un diamètre moyen inférieur à 100 nm et d'une longueur moyenne inférieure à 1 μm (Fig. 1) ont été recherchées par Jiangsu Qingtao Energy Science and Technology Co., Ltd. RhB (AR), EDTA sel disodique déshydraté (GR, 99 %), tert-butanol (GR, ≥ 99,5 %), chlorure de stéaryl triméthyl ammonium (STAC, 98 %), nitrate d'argent (AR) et dihydrogénophosphate disodique hydraté (Na2 HPO4 ·12H2 O, AR, 99%) ont été achetés chez Macklin. L'oxyde de titane, anatase (nanopoudres, granulométrie 5-10 nm, 99,8 % de base de métaux, hydrophile/lipophile) a été acheté auprès d'Aladdin.
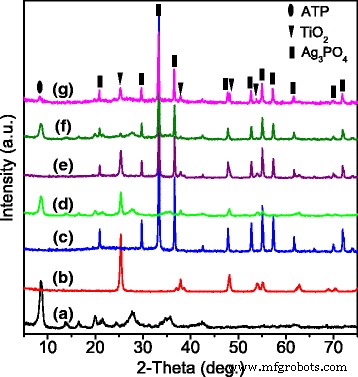
Modèles XRD des échantillons :a ATP, b TiO2 , c Ag3 Bon de commande4 , d ATP/TiO2 , e Ag3 Bon de commande4 /TiO2 , f ATP/Ag3 Bon de commande4 , et g ATP/TiO2 /Ag3 Bon de commande4
Synthèse d'échantillons
L'ATP/TiO2 /Ag3 Bon de commande4 composite ternaire a été synthétisé par une méthode facile en deux étapes. Nanobâtonnets d'ATP bien dispersés et TiO2 des nanoparticules avec un rapport massique de 5:2 ont d'abord été ajoutées dans de l'eau déminéralisée et agitées pendant 4 h. Grâce à l'absorption électronique physique et de surface, le TiO2 des nanoparticules ont été fixées à la surface des nanotiges d'ATP. Après séparation centrifuge, le précipité a été lavé à l'eau déminéralisée puis séché à 60 °C pendant 6 h pour obtenir ATP/TiO2 matériaux composites. Par une méthode de précipitation simple, Ag3 Bon de commande4 des nanoparticules se sont déposées à la surface d'ATP/TiO2 et ATP/TiO2 /Ag3 Bon de commande4 des composites ternaires ont ensuite été préparés. [12] Dans un processus de préparation typique, 20 ml de solution de nitrate d'argent (0,1 mol/L) ont été dissous dans de l'ATP/TiO2 suspension aqueuse avec 0,7 g d'ATP/TiO2 composites et 50 ml d'eau déminéralisée par agitation ultrasonique pendant 30 min. 20 ml de Na2 HPO4 Une solution aqueuse (0,1 mol/L) a ensuite été ajoutée lentement dans la solution ci-dessus sous agitation par ultrasons dans l'obscurité pendant 40 min supplémentaires. Ensuite, le précipité brun jaunâtre clair a été centrifugé, lavé plusieurs fois avec de l'éthanol absolu et séché à 60 °C pendant 12 h, pour obtenir de l'ATP/TiO2 /Ag3 Bon de commande4 composites ternaires. Les échantillons de poudre d'Ag3 Bon de commande4 , Ag3 Bon de commande4 /ATP, Ag3 Bon de commande4 /TiO2 , et ATP/TiO2 ont également été synthétisés en utilisant la méthode similaire.
Caractérisation
La diffraction des rayons X a été collectée à l'aide de XRD Rigaku D/max-RB) pour l'analyse de phase des poudres sous 40 kV et 30 mA. Les microstructures ont été évaluées par microscopie électronique à balayage (SEM, INSPECTF FEI, Pays-Bas). La spectroscopie de réflexion diffuse dans l'ultraviolet visible (UV-vis) du photocatalyseur a été étudiée à l'aide du spectrophotomètre UV-vis U-3010 Hitach utilisant le BaSO4 comme référence.
Expérience photocatalytique
La dégradation photocatalytique de RhB a été testée sous irradiation solaire simulée. 50 mg d'ATP/TiO2 /Ag3 Bon de commande4 a été ajouté à 100 ml de solution de RhB avec une concentration de 5 mg/L et agité à l'obscurité pendant 40 minutes pour assurer l'équilibre adsorption-désorption. La source lumineuse était une lampe Xe de 300 W (Microsolar300, PerfectLight, Pékin, Chine) à environ 150 mW/cm 2 (tel que testé par un radiomètre FZ-A, Usine d'instruments photoélectriques de l'Université normale de Pékin, Chine). Après ouverture de la lampe, 4 ml de solution ont été prélevés à des intervalles de temps connus et séparés par centrifugation (10 000 tr/min, 10 min). Les surnageants ont été analysés en enregistrant les variations du pic d'absorption (554 nm) dans les spectres UV-vis à l'aide d'un spectrophotomètre UV/vis (T6, PERSEE, Pékin, Chine).
Le degré de dégradation du colorant RhB a été déterminé selon l'équation suivante :D % = (c 0 − c )/c 0 × 100% = (A 0 − A )/A 0 × 100 %, où c 0 et c sont respectivement la concentration initiale et la concentration après photocatalyse de la solution; et A 0 et A sont les valeurs d'absorbance de la solution avant et après la réaction photocatalytique, respectivement.
Résultats et discussion
Caractérisation de l'ATP-Ag3 Bon de commande4 -TiO2 composites
Les modèles XRD de l'ATP, TiO2 , Ag3 Bon de commande4 , et les nanocomposites sont présentés sur la figure 1. Les pics de diffraction sur la figure 1a peuvent être indexés en tant que phase ATP avec une structure monoclinique (JCPDS # 21-0958), ce qui implique que l'ATP a été spécialement purifié et qu'aucune phase d'impureté n'existe. La figure 1b présente les pics de diffraction typiques de l'anatase TiO2 sans aucune impureté, tandis que la figure 1c montre les pics de diffraction correspondant à Ag3 pur Bon de commande4 phase, en bon accord avec JCPDS #06-0505. Il n'y a pas de phases d'impuretés ou de déstabilisation de structure pour tous les échantillons nanocomposites d'ATP/TiO2 (Fig. 1d), Ag3 Bon de commande4 /TiO2 (Fig. 1e), ATP/Ag3 Bon de commande4 (Fig. 1f), et ATP/TiO2 /Ag3 Bon de commande4 (Fig. 1g). Dans les modèles XRD d'ATP/TiO2 /Ag3 Bon de commande4 (Fig. 1g), principaux pics caractéristiques associés à la fois à Ag3 Bon de commande4 et TiO2 peuvent être détectés, tandis que les pics de diffraction de la phase ATP sont beaucoup plus faibles. Le phénomène implique que les nanotiges d'ATP sont gainées de TiO2 et Ag3 Bon de commande4 nanoparticules.
La morphologie et la microstructure des photocatalyseurs composites sont illustrées à la Fig. 2. Les nanotiges d'ATP présentaient une longueur moyenne inférieure à 1 μm et un diamètre inférieur à 100 nm (Fig. 2a). En raison de l'adsorption physique et chimique de surface, TiO2 nanoparticules d'un diamètre d'environ 40 nm attachées à la surface des nanotiges d'ATP et formées d'ATP/TiO2 composites, comme le montre la figure 2b. Sur la figure 2c, les nanotiges d'ATP étaient entièrement recouvertes d'Ag3 Bon de commande4 et TiO2 particules en ATP/TiO2 /Ag3 Bon de commande4 composite ternaire, tandis que Ag3 Bon de commande4 apparu à la surface de l'ATP/TiO2 composites sous forme de particules sphéroïdales uniformes d'un diamètre d'environ 50 nm.

Images SEM de a ATP, b ATP/TiO2 , et c ATP/TiO2 /Ag3 Bon de commande4 poudres
Spectres d'absorption
Les spectres d'absorption UV-vis de Ag3 Bon de commande4 , ATP, TiO2 , et ATP/TiO2 /Ag3 Bon de commande4 sont illustrés à la figure 3a. Similaire aux résultats rapportés, [3] Ag3 Bon de commande4 présente une bonne absorption des UV à la région de la lumière visible avec une longueur d'onde jusqu'à environ 500 nm. Par contre, TiO2 présente une excellente absorption UV sans absorption évidente dans la région de la lumière visible. L'ATP montre une absorption UV plus faible et une faible absorption dans la région de la lumière visible. Comme prévu, ATP/TiO2 /Ag3 Bon de commande4 le nanocomposite ternaire présente une forte absorption UV bénéficiant du TiO2 et l'ATP et l'absorption accrue de la lumière visible imposée par Ag3 Bon de commande4 . La bande interdite optique (E g ) peut être estimée à partir du bord d'absorption optique selon l'Eq. (1). [13, 14]
$$ \alpha hv=A{\gauche( hv-{E}_g\right)}^m, $$ (1)où α est le coefficient d'absorption spectrale, "hv ” est l'énergie du photon, A est une constante, et m est égal à 0,5 ou 2 pour les transitions directes et indirectes, respectivement. TiO2 [15] est généralement considéré comme un semi-conducteur à bande interdite indirecte, et son E indirect g est déterminé par l'interception d'une ligne droite passant par le côté à basse énergie de la courbe (αhυ ) 1/2 contre hυ comme le montre la figure 3b, avec une valeur estimée d'environ 3,20 eV. Ag3 Bon de commande4 a été signalé comme un semi-conducteur à bande interdite indirecte, et son écart direct au point Gamma et l'écart indirect sont très proches en termes de résultats calculés. [16] Son écart direct d'environ 2,45 eV était considéré comme la bande interdite d'Ag3 Bon de commande4 dans la plupart des rapports. Ici, le E indirect g et diriger E g sont déterminés par l'interception de la droite passant par le côté à basse énergie de la courbe (αhυ ) 1/m (m = 2 et 0.5) versus hυ , respectivement. Les résultats de Ag3 Bon de commande4 révèlent une bande interdite indirecte de 2,33 eV (Fig. 3b) et une bande interdite directe de 2,49 eV (Fig. 3c). Le E direct g de 2,49 eV correspond mieux à sa limite de bande d'absorption qu'à la bande interdite indirecte de 2,33 eV. Ainsi, le E g de Ag3 Bon de commande4 est déterminé à 2,49 eV. De même, l'ATP montre une bande interdite indirecte de 3,37 eV (Fig. 3b) et une bande interdite directe de 3,75 eV (Fig. 3c), et le E g d'ATP est déterminé comme 3,75 eV. Les valeurs de bande interdite ci-dessus de TiO2 , Ag3 Bon de commande4 et ATP sont assez proches des résultats rapportés. [17] Dans l'ATP/TiO2 /Ag3 Bon de commande4 nanocomposite ternaire, il existe deux bords de bande d'absorption optique différents d'environ 385 et 510 nm dans les spectres d'absorption UV-vis, à partir desquels deux E différents g les valeurs peuvent être estimées. À partir du bord de la bande d'absorption de 385 nm, un E direct g d'environ 3,64 eV est obtenu, ce qui est entre ceux de TiO2 et l'ATP par effet composite. Correspondant au bord d'absorption de 510 nm, un E direct g d'environ 2,49 eV est obtenu, en accord avec le direct E g de Ag3 Bon de commande4 . En conséquence, le composite ternaire a conservé la même absorption exceptionnelle dans la lumière visible que Ag3 Bon de commande4 , ainsi qu'une bonne absorption UV dérivée du TiO2 et ATP. Ce résultat implique l'ATP/TiO2 /Ag3 Bon de commande4 Le composite ternaire a le potentiel d'être un excellent photocatalyseur dans la gamme de longueurs d'onde allant de la lumière UV à la lumière visible.
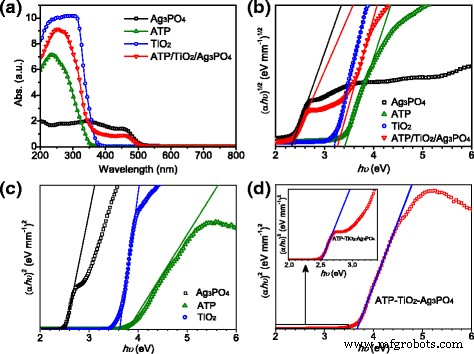
un Spectres d'absorption UV-vis et b parcelles de (αhν ) 1/2 versus (hν ) de Ag3 Bon de commande4 , ATP, TiO2 et ATP/TiO2 /Ag3 Bon de commande4 nanocomposite ternaire; c parcelles de (αhν ) 2 versus (hν ) de Ag3 Bon de commande4 , ATP et TiO2; d parcelles de (αhν ) 2 versus (hν ) d'ATP/TiO2 /Ag3 Bon de commande4 nanocomposite ternaire, et l'encart en d est le détail agrandi partiel des tracés en d
Activités photocatalytiques
L'activité photocatalytique des échantillons résultants a été évaluée par la dégradation de RhB sous irradiation lumineuse Xe, Fig. 4. Après immersion des photocatalyseurs, les solutions de RhB ont été agitées pendant 40 min dans l'obscurité pour établir un équilibre d'adsorption-désorption dans le but d'éliminer les interférences. d'adsorption. La figure 4a montre l'évolution des spectres d'absorption lors de la photodégradation des solutions de RhB par l'ATP/TiO2 /Ag3 Bon de commande4 nanocomposite ternaire sous éclairage Xe en fonction du temps. Les pics d'absorption centrés à 554 nm correspondent au pic d'absorption caractéristique de RhB. En raison de la photodégradation de RhB, la force maximale diminuait à mesure que la concentration de RhB diminuait. Après avoir agité la solution pendant 40 min dans l'obscurité, seule une faible diminution de l'intensité du pic d'absorption est observée pour RhB, ce qui indique une faible adsorption de colorant du nanocomposite. Après irradiation pendant 20 min, le pic d'absorption caractéristique de RhB a presque disparu, ce qui implique une dégradation presque complète du colorant dans la solution. Dans des conditions d'irradiation de lumière Xe similaires, la dégradation photocatalytique de RhB avec différents photocatalyseurs est comparée sur la figure 4b. Les photocatalyseurs de TiO2 monophasé et l'ATP a montré un taux de dégradation inférieur à 50 % sous une irradiation de 60 min, tandis que Ag3 Bon de commande4 affiché une dégradation photocatalytique beaucoup plus forte et plus rapide, en bon accord avec les rapports précédents sur la photocatalyse de TiO2 et Ag3 Bon de commande4 [18]. Ag3 Bon de commande4 a été signalé comme un puissant photocatalyseur, mais sa stabilité de l'activité photocatalytique est faible et son coût est élevé. Les nanocomposites ternaires ont révélé un taux de dégradation rapide d'environ 81,1% seulement après 3 min d'irradiation et une dégradation presque complète après 20 min d'irradiation, ce qui est évidemment supérieur à celui de l'Ag3 monophasique. Bon de commande4 et d'autres photocatalyseurs composites binaires, y compris ATP/Ag3 Bon de commande4 et TiO2 /Ag3 Bon de commande4 comme le montre la figure 4b. L'ATP a peu d'activité photocatalytique, mais il a été rapporté qu'il avait une bonne capacité d'adsorption [19], ce qui facilite l'adhérence des molécules de colorant à sa surface et entraîne un taux de dégradation plus élevé de RhB par l'ATP/TiO2 /Ag3 Bon de commande4 photocatalyseurs nanocomposites ternaires. Fait intéressant, l'ATP/TiO2 /Ag3 Bon de commande4 les photocatalyseurs ont montré une efficacité de dégradation photocatalytique plus élevée que TiO2 /Ag3 Bon de commande4 ou Ag3 Bon de commande4 avec le même poids. En conséquence, le montant de la demande d'Ag3 à coût élevé Bon de commande4 est réduit.
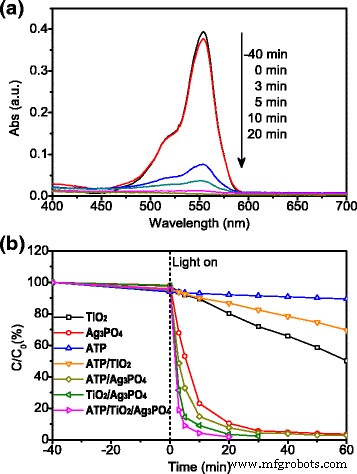
un Spectres d'absorption UV-vis des solutions de RhB dégradées photocatalytiques par l'ATP/TiO2 /Ag3 Bon de commande4 nanocomposite ternaire à différents moments. b Dégradation photocatalytique de RhB avec différents photocatalyseurs sous irradiation solaire simulée
La stabilité des photocatalyseurs pour la photodégradation de RhB sous irradiation lumineuse Xe a été évaluée par des expériences photocatalytiques répétées. Un test similaire a également été effectué sur Ag3 Bon de commande4 en comparaison. Après chaque cycle de dégradation photocatalytique, les photocatalyseurs ont été séparés, lavés, séchés, puis recyclés pour le cycle suivant. La concentration initiale de RhB et le dosage de photocatalyseur ont été maintenus constants pendant chaque cycle de dégradation photocatalytique. Les résultats sont présentés sur la figure 5. Après chaque analyse, l'activité de Ag3 Bon de commande4 significativement diminué comme prévu [20]. Dans le processus photocatalytique, les sites actifs étaient recouverts d'Ag apparaissant à la surface d'Ag3 Bon de commande4 particules. L'activité photocatalytique de l'ATP/TiO2 /Ag3 Bon de commande4 Le nanocomposite ternaire est resté inchangé même après cinq cycles de photodégradation de RhB. Ce résultat indique que la photocatalyse est très stable en ATP/TiO2 /Ag3 Bon de commande4 nanocomposites ternaires.
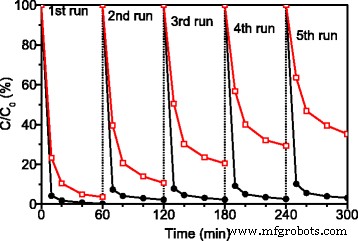
Dégradation photocatalytique répétée de RhB avec Ag3 Bon de commande4 (carrés rouges vides) et ATP/TiO2 /Ag3 Bon de commande4 composites ternaires (cercles pleins noirs) sous irradiation solaire simulée
Mécanisme possible dans le processus photocatalytique
Dans les processus de dégradation photocatalytique, les espèces réactives courantes de l'oxygène comprennent les radicaux •OH, O2 •– radicaux et trous (h + ). [2] Les expériences de piégeage ont été réalisées pour surveiller les espèces réactives de l'oxygène impliquées dans le processus photocatalytique de l'ATP/TiO2 /Ag3 Bon de commande4 composites sur RhB. Trois produits chimiques de tert-butanol (TBA), benzoquinone (BQ) et éthylènediaminetétraacétate disodique (Na2 -EDTA) ont été utilisés comme capteurs de radicaux •OH, O2 •– radicaux et trous, respectivement. [9] Les résultats expérimentaux sous irradiation lumineuse Xe sont présentés sur la Fig. 6. L'introduction de 1 mM de TBA (•OH radical scavenger) n'a pas d'influence évidente sur l'activité photocatalytique du photocatalyseur composite (Fig. 6b). Ce résultat indique que les radicaux OH· ne sont pas les principales espèces actives d'oxygène dans le processus photocatalytique. L'ajout de 1 mM BQ (O2 •– piégeur de radicaux) réduit le degré de dégradation photocatalytique de RhB à 42 % en 60 min (Fig. 6c), ce qui indique que O2 •– les radicaux apportent une contribution importante mais seulement segmentaire aux performances photocatalytiques. Après avoir ajouté le récupérateur de trous Na2 -EDTA (1 mM) dans le système photocatalytique, l'activité de dégradation photocatalytique de l'ATP/TiO2 /Ag3 Bon de commande4 les nanocomposites sont presque complètement supprimés (Fig. 6d) et le degré de dégradation de RhB diminue à moins de 5 % après 60 min. Ce résultat implique que les trous jouent un rôle clé dans la dégradation photocatalytique. En conséquence, les trous et O2 •– les radicaux sont les principaux radicaux réactifs dans l'ATP/TiO2 /Ag3 Bon de commande4 procédé photocatalytique dégradant RhB sous irradiation lumineuse Xe.
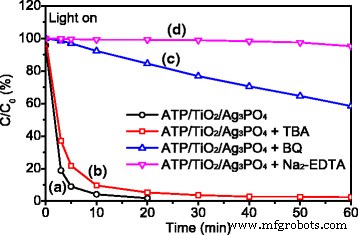
Expériences de piégeage d'espèces réactives d'ATP/TiO2 /Ag3 Bon de commande4 photocatalyseur composite
Sur la base de la discussion mentionnée ci-dessus, un mécanisme photocatalytique possible a été proposé pour expliquer la dégradation photocatalytique de RhB par ATP/TiO2 /Ag3 Bon de commande4 photocatalyseurs composites ternaires, comme le montre la Fig. 7. Les potentiels pour la bande de conduction (CB) et la bande de valence (VB) de TiO2 sont respectivement de − 0,5 eV contre NHE et de + 2,70 eV contre NHE [21, 22]. Ces valeurs sont plus négatives que celles des deux Ag3 Bon de commande4 (CB + 0,45 eV vs NHE, VB + 2,97 eV vs NHE) [3, 16] et ATP (CB − 0,25 eV vs NHE, VB + 3,50 eV vs NHE). Par conséquent, les électrons photo-générés dans le CB de TiO2 peut facilement être transféré à celui d'Ag3 Bon de commande4 , tandis que les trous photo-induits dans le VB de Ag3 Bon de commande4 va migrer vers celui de TiO2 , qui favorise la séparation efficace des paires électron-trou photo-générées et diminue la probabilité de recombinaison des électrons et des trous. En conséquence, l'ATP/TiO2 /Ag3 Bon de commande4 le photocatalyseur composite peut présenter des activités photocatalytiques plus élevées que l'Ag3 à phase unique Bon de commande4 . Pendant ce temps, les trous dans VB de TiO2 , qui a de fortes caractéristiques d'oxydation, non seulement pourrait accélérer considérablement les taux de réaction photocatalytique de dégradation de RhB, mais pourrait également oxyder H2 O pour générer O2 . Le potentiel de réduction de O2 •– est de − 0.28 eV, tandis que les potentiels de CB pour TiO2 et Ag3 Bon de commande4 sont - 0,3 et + 0,45 eV, respectivement. Par conséquent, le résultat O2 à la surface des photocatalyseurs pourraient alors capturer des électrons photogénérés pour produire O2 •– radicaux, et l'Ag + ions dans Ag3 Bon de commande4 pourrait être protégé de la photoréduction en Ag métallique (Ag + + e − → Ag) car les électrons ont été consommés dans la réaction avec O2 . En conséquence, le photocatalyseur composite avec TiO2 et Ag3 Bon de commande4 montre une stabilité beaucoup plus élevée que l'Ag3 monophasé Bon de commande4 photocatalyseur.
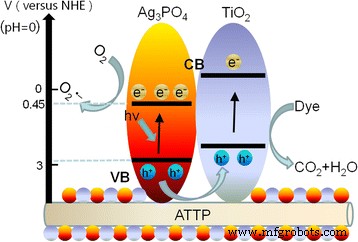
Mécanisme photocatalytique proposé de l'ATP/TiO2 /Ag3 Bon de commande4 composites
Conclusions
En conclusion, nous avons synthétisé ATP/TiO2 /Ag3 Bon de commande4 composite ternaire par une méthode simple :TiO2 des nanoparticules ont été absorbées à la surface de l'ATP pour former une structure binaire, puis Ag3 Bon de commande4 des nanoparticules ont été déposées sur ATP/TiO2 composite par interaction électrostatique. La jonction hétérogène formée dans le composite ternaire améliore l'efficacité et la stabilité photocatalytiques. En comparaison avec Ag3 pur Bon de commande4 phase, ce type de photocatalyseur composite réduit non seulement la consommation du métal précieux argent dans une plus large mesure, mais améliore également l'efficacité des photocatalyseurs. Nos résultats fourniront des conseils pour concevoir des composites à base d'Ag pour une application photocatalytique.
Abréviations
- ATP :
-
Attapulgite
- BQ :
-
Benzoquinone
- CB :
-
Bande de conduction
- Na2 -EDTA :
-
Éthylènediaminetétraacétate disodique
- RhB :
-
Rhodamine B
- À confirmer :
-
Tert-butanol
- VB :
-
Bande de Valence
Nanomatériaux
- Planification de mouvement en temps réel pour une voiture autonome dans plusieurs situations, dans un environnement urbain simulé
- Nano arbres pour cellules solaires à colorant
- Nano-hétérojonctions pour cellules solaires
- Effets synergiques des nanoparticules d'Ag/BiV1-xMoxO4 avec une activité photocatalytique améliorée
- Pérovskite hybride cultivée en vapeur séquentielle pour cellules solaires à hétérojonction planaire
- Synthèse en un seul pot de nanoplaques Cu2ZnSnSe4 et leur activité photocatalytique induite par la lumière visible
- Nanocristal Sb2O3 dopé S :un catalyseur efficace à lumière visible pour la dégradation organique
- Principes de conception des cellules solaires organiques à plasmons de nanoparticules
- Nanotubes de titane préparés par anodisation rapide pour la décoloration photocatalytique de colorants organiques sous UV et lumière solaire naturelle



