Synthèse en un seul pot de nanoplaques Cu2ZnSnSe4 et leur activité photocatalytique induite par la lumière visible
Résumé
Un SeO2 solution d'éthanol comme précurseur facile a été utilisé pour la préparation de Cu2 quaternaire ZnSnSe4 (CZTSe) nanoplaques. Des nanoplaques CZTSe monophasées monodispersées ont été préparées avec succès par une méthode chimique thermique à un seul pot facile. Les nanoplaques de CZTSe telles que préparées présentent une morphologie uniforme avec une bande interdite d'environ 1,4 eV. Comme preuve de concept, les nanoplaques CZTSe ont été utilisées comme photocatalyseur à lumière visible pour la dégradation du colorant Rhodamine B et présentent une activité et une stabilité photocatalytiques élevées. L'excellente élimination des colorants est principalement attribuée à l'utilisation efficace de la lumière des nanoplaques CZTSe.
Contexte
Les polluants chimiques dans l'eau naturelle ont suscité une grande attention en raison de ses graves dommages pour l'environnement, et la technique de dégradation photocatalytique basée sur les semi-conducteurs en utilisant l'énergie solaire a été considérée comme une solution prometteuse à ce problème [1]. Cependant, les photocatalyseurs typiques, tels que TiO2 et ZnO, ne peut absorber que la lumière ultraviolette (UV). En fait, environ 50% de l'énergie solaire est principalement concentrée dans la région de la lumière visible tandis que la lumière UV représente moins de 4% du spectre solaire [2]. Pour utiliser la lumière visible et améliorer l'activité photocatalytique, divers photocatalyseurs efficaces ont été explorés et appliqués dans la dégradation des pigments organiques, le fractionnement de l'eau et les absorbeurs de cellules solaires [3]. Parmi plusieurs photocatalyseurs, les semi-conducteurs chalcogénures ternaires et quaternaires à base de cuivre, tels que Cu2 SnS3 , CuInx Ga1-x Voir2 , et Cu2 ZnSnS4 , ont été d'un grand intérêt en raison de leurs propriétés optoélectroniques exceptionnelles avec un coefficient d'absorption élevé (> 10 4 cm −1 ), une bonne stabilité et une énergie de bande interdite appropriée (1,0 à 1,5 eV) [4,5,6,7,8,9].
Cu2 ZnSnSe4 (CZTSe) les nanocristaux et les films minces avec des éléments constitutifs peu coûteux, non toxiques et abondants en terre ont été largement étudiés ces dernières années [8, 10, 11, 12, 13, 14, 15] ; cependant, il existe quelques rapports liés à l'étude de la morphologie des nanoplaques [16, 17]. L'injection à chaud et la méthode chimique thermique à un pot sont généralement appliquées à la synthèse des nanostructures de CZTSe [18,19,20,21]. Cependant, les précurseurs de Se utilisés dans ces procédés sont coûteux, toxiques ou instables. Ici, un précurseur de Se facile qui dissout SeO2 poudre dans l'éthanol est développé dans cette étude.
Nous rapportons ici une méthode chimique thermique à un pot de synthèse de nanoplaques CZTSe à l'aide d'un précurseur Se facile. L'activité photocatalytique induite par la lumière visible et les performances de recyclage des nanoplaques de CZTSe ont été étudiées. Les nanoplaques CZTSe ont un potentiel dans le traitement des eaux usées.
Méthodes/Expérimental
Synthèse de nanoplaques CZTSe
Tous les produits chimiques utilisés dans ce travail ont été achetés auprès d'Aladdin et utilisés directement. Typiquement, 1,0 mmol Cu(acac)2 , 0,5 mmol Zn(OAc)2 ·2H2 O, 0,5 mmol SnCl2 ·2H2 O et 2,0 mmol de SeO2 dissous dans 4 mL d'éthanol ont été ajoutés à 20 mL d'oléylamine (OLA) dans un ballon à trois cols de 100 mL. Le mélange a été dégazé à 130 °C pendant 1 h, purgé avec de l'Ar pendant 30 min, puis chauffé à 280 °C pendant 1 h. Les nanoplaques ont été lavées avec de l'hexane et de l'éthanol trois fois par centrifugation à 8000 tr/min pendant 5 min. La poudre noire a été recueillie et séchée à 60 °C sous vide. Avant réaction photocatalytique, les nanoplaques ont été traitées hydrophiles avec Na2 S pour éliminer les ligands OLA à longue chaîne [8].
Caractérisations
La diffraction des rayons X sur poudre (XRD, D/max 2200, Rigaku, Japon) utilisant le rayonnement Cu Kα (40 kV, 100 mA) et un spectromètre Raman (Inviareflex, Renishaw, Royaume-Uni) couplé à un laser 514 nm ont été appliqués pour analyser la phase des échantillons. Des mesures de microscopie électronique à transmission (MET, JEM-2100F, JEOL., Japon) et de microscopie électronique à balayage (SEM, Quatan 250FEG, FEI, USA) ont été effectuées pour caractériser les morphologies des échantillons. Les spectres d'absorption UV-vis de la poudre de nanoplaques CZTSe et de la solution aqueuse de Rhodamine B (RhB) ont été enregistrés sur un spectromètre UV/vis en utilisant respectivement la sphère d'intégration et la cuvette (Lambda, Perkin Elmer, USA).
Mesures d'activité photocatalytique
L'activité photocatalytique induite par la lumière visible des nanoplaques de CZTSe a été évaluée par photodégradation de la solution aqueuse de RhB (10 mg/L) à température ambiante. Une lampe Xe de 300 W équipée d'un filtre de coupure de 420 nm a été utilisée comme source de lumière visible. En règle générale, 50 mg de photocatalyseur ont été ajoutés dans 100 mL de solution aqueuse de RhB. La solution a été agitée en continu dans l'obscurité pendant 12 h pour assurer l'équilibre adsorption-désorption avant irradiation. La concentration du RhB résiduel a été surveillée à une séquence d'intervalles de temps par le spectromètre UV-vis à 554 nm pour calculer le taux de dégradation sur la base de la loi de Beer-Lambert.
Résultats et discussion
Sur la figure 1a, tous les pics de diffraction de l'échantillon de CZTSe tel que préparé dans le modèle XRD peuvent être clairement attribués à la structure de kesterite tétragonale de Cu2 ZnSnSe4 (JCPDS n° 70-8930). Les pics de diffraction à 27,1°, 45,1°, 53,5°, 65,8° et 72,5° peuvent être indexés sur (112), (204), (312)/(116), (400)/(008) et (332 ) de CZTSe, respectivement. La diffusion Raman a ensuite été appliquée pour confirmer la phase pure, comme le montre la figure 1b. Trois pics dans le spectre Raman vérifient également la phase pure des nanoplaques CZTSe, et aucune autre phase binaire de Cux Se et ZnSe (principaux pics à 262 et 252 cm −1 , respectivement) et phase ternaire de Cu2 SnSe3 (pic principal à 180 cm −1 ) sont observés. Par conséquent, ni le résultat XRD ni le résultat Raman ne révèlent de phase secondaire, suggérant la phase quaternaire pure des nanoplaques de CZTSe.
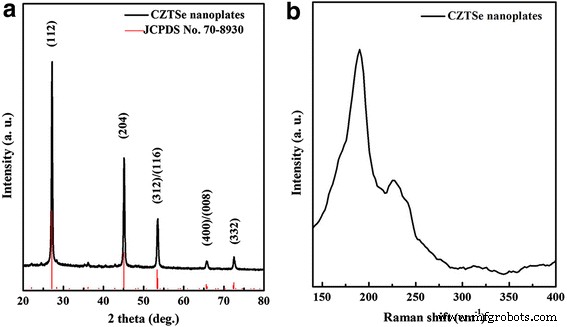
un Modèle XRD et b Spectre Raman des nanoplaques CZTSe
La figure 2 montre les images SEM, TEM et TEM haute résolution (HRTEM) des nanoplaques CZTSe telles que synthétisées. On peut observer sur la figure 2a que les échantillons de CZTSe ont une morphologie en forme de plaque et uniforme. La taille moyenne des nanoplaques de CZTSe calculée à partir de la figure 2b est d'environ 210 nm, ce qui correspond bien à l'observation SEM. Le diagramme de diffraction électronique à aire sélectionnée (SAED) montré dans l'encart de la figure 2b indique une cristallisation élevée des nanoplaques. La figure 2c présente l'image HRTEM d'une nanoplaque, affichant sa structure cristalline principalement ordonnée et un espacement d interplanaire de 0,33 nm indexé sur le (112) du CZTSe.

un Image SEM. b Image TEM (encart :motif SAED). c Image HRTEM de nanoplaques CZTSe
Le spectre d'absorption UV-vis révèle la propriété optique des nanoplaques CZTSe. On peut voir à partir de la figure 3a que les nanoplaques CZTSe ont des performances d'absorption de la totalité de la lumière visible. La bande interdite peut être calculée à partir de l'équation :αhν = A (hν−E g ) 1/2 , où A , α , h , v , et E g sont une constante, le coefficient d'absorption, la constante de planche, la fréquence de la lumière et la bande interdite, respectivement. La bande interdite des nanoplaques de CZTSe obtenue à partir de la figure 3b est d'environ 1,4 eV, ce qui est un peu plus grand que celui du volume de CZTSe en raison de l'effet de confinement quantique [9].
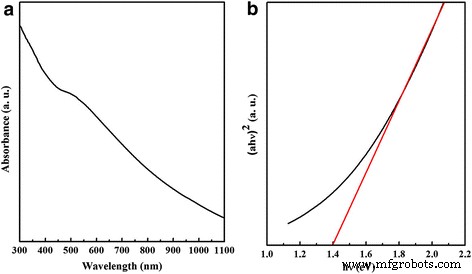
un Spectre d'absorption UV-vis et b bande interdite des nanoplaques CZTSe
L'activité photocatalytique des nanoplaques de CZTSe telles que préparées est évaluée avec la photodégradation de la solution aqueuse de RhB dans la région de la lumière visible. On peut voir sur la figure 4a qu'environ 90 % de RhB sont photodégradés en 120 min. La stabilité et la réutilisation du photocatalyseur jouent un rôle clé dans l'application de polluants écologiques en désintégration. Ainsi, cinq cycles d'expériences ont été réalisés, et les résultats sont présentés sur la figure 4b. Les nanoplaques CZTSe conservent une activité de photodécomposition élevée dans les tests de cycle, ce qui indique leur grande stabilité dans la réaction photocatalytique. Il est bien connu que le processus de photo-oxydation pourrait être principalement lié à plusieurs espèces actives, telles que les radicaux hydroxyles (•OH), les radicaux superoxydes (•O2 − ), et le trou (h + ). Parce que le E CB et E VB de CZTSe sont plus négatifs que les potentiels redox standard de E θ (O2 /•O2 − ) et E θ (H2 O/•OH), le •O2 − plutôt que •OH peut être généré dans le processus photocatalytique. Pour vérifier davantage les principales espèces actives, l'argon (Ar), l'oxalate d'ammonium (AO), le tert-butanol (TBA) et la benzoquinone (BQ) ont été appliqués pour l'élimination de O2 , h + , •OH et •O2 − , respectivement. Le système de réaction avec les extincteurs correspondants (0,1 mmol) a été illuminé pendant 120 min, et les résultats sont présentés sur la figure 4c. On peut confirmer que le O2 est la nécessité dans le processus de photo-oxydation, rarement •OH est produit, et à la fois le •O2 − et h + sont des espèces actives. Le •O2 − joue un rôle plus important que h + car son efficacité de dégradation plus nette diminue après piégeage. La figure 4d montre le mécanisme possible du processus de réaction photocatalytique. Les électrons sont excités de la bande de valence (VB) à la bande de conduction (CB) sous illumination. Les électrons photogénérés sont capturés par O2 dans la solution aqueuse pour former •O2 − , qui est hautement oxydant et peut dégrader RhB en produits inorganiques. Simultanément, les trous fonctionnent directement comme oxydants. Ainsi, l'activité photocatalytique induite par la lumière visible est obtenue grâce à la pleine utilisation de la lumière visible des nanoplaques de CZTSe.
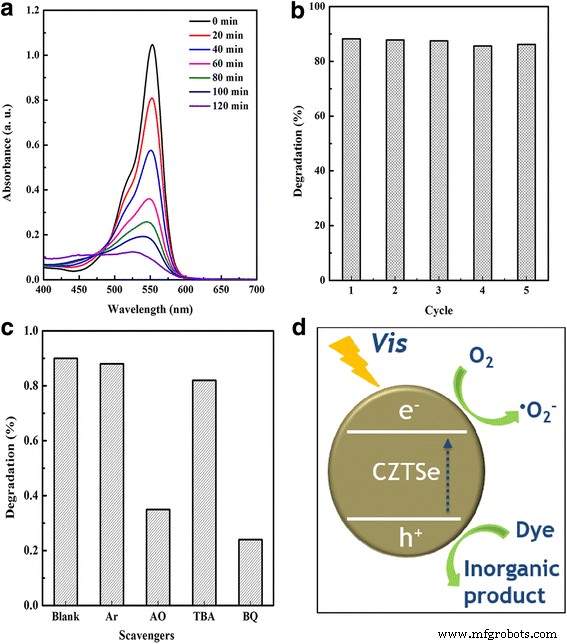
un Dégradation RhB. b Essai de vélo. c Effets de divers quenchers sur l'efficacité de dégradation de RhB. d Schéma du processus de dégradation photocatalytique
Conclusions
Un SeO2 solution d'éthanol comme précurseur facile a été utilisé pour la préparation de nanoplaques CZTSe quaternaires. Des nanoplaques de CZTSe monodispersées ont été préparées avec succès par une méthode chimique thermique simple à pot unique. Comme preuve de concept, les nanoplaques CZTSe ont été utilisées comme photocatalyseur de réponse à la lumière visible pour la dégradation du colorant RhB. L'élimination efficace des colorants est principalement attribuée à l'utilisation efficace de la lumière des nanoplaques CZTSe.
Nanomatériaux
- Synthèse verte à un pot de microsphères de SnO2 décorées d'Ag :un catalyseur efficace et réutilisable pour la réduction du 4-nitrophénol
- Synthèse hydrothermale de nanoparticules d'In2O3 jumelles hybrides disque hexagonal hétérostructures ZnO pour des activités photocatalytiques et une stabilité améliorées
- Activité de synthèse et d'oxydation du CO des catalyseurs d'or pris en charge par l'oxyde binaire mixte 1D CeO2-LaO x
- Synthèse de points quantiques de sulfure d'antimoine solubles dans l'eau et de leurs propriétés photoélectriques
- Synthèse écologique et facile de nanofils de Co3O4 et leur application prometteuse avec du graphène dans les batteries lithium-ion
- Synthèse sonochimique en une étape facile et propriétés photocatalytiques des composites graphène/Ag3PO4 Quantum Dots
- Synthèse et caractérisation de BiOCl modifiés et leur application à l'adsorption de colorants à faible concentration à partir de solutions aqueuses
- Synthèse verte de nanoparticules de métal et d'oxyde métallique et leur effet sur l'algue unicellulaire Chlamydomonas reinhardtii
- Fabrication et propriété photocatalytique de nouveaux nanocomposites SrTiO3/Bi5O7I



