Activités photocatalytiques renforcées par des nanoparticules Au-Plasmonic sur une photoélectrode de nanotube de TiO2 recouverte de MoO3
Résumé
Bien que TiO2 était autrefois un matériau commun pour les réactions de photocatalyse, sa large bande interdite (3,2 eV) permet d'absorber uniquement la lumière ultraviolette, qui ne représente que 4 % de la lumière solaire totale. Modification de TiO2 est devenu un objectif de recherche sur les réactions de photocatalyse, et la combinaison de deux semi-conducteurs à oxyde métallique est la méthode la plus courante dans le processus d'amélioration photocatalytique. Quand MoO3 et TiO2 entrent en contact pour former une interface hétérogène, les trous photogénérés excités à partir de la bande de valence de MoO3 doit être transféré dans la bande de valence de TiO2 réduire efficacement la recombinaison de charge des paires électron-trou photogénérées. Cela peut séparer efficacement les paires et favoriser l'efficacité de la photocatalyse. De plus, l'amélioration du photocourant est attribuée aux puissants effets de champ proche et de diffusion de la lumière des nanoparticules d'Ag plasmoniques. Dans ce travail, nous avons fabriqué MoO3 -enduit TiO2 hétérostructures de nanotubes avec une configuration hiérarchique 3D par oxydation anodique en deux étapes et une méthode hydrothermale facile. Cette structure hiérarchique 3D est constituée d'un TiO2 noyau de nanotube et un MoO3 shell (appelé TNTs@MoO3 ), tel que caractérisé par la microscopie électronique à balayage à émission de champ et la spectroscopie photoélectronique à rayons X.
Contexte
Le développement technologique rapide s'est accompagné d'une demande accrue d'énergie. Par conséquent, la recherche sur les sources d'énergie alternatives est devenue populaire au cours de la dernière décennie, de nombreux scientifiques se concentrant sur les sources d'énergie renouvelables à faible émission de carbone et à impact environnemental minimal. Ceux-ci incluent l'énergie solaire [1, 2], la chaleur géothermique [3, 4], les marées [5] et diverses formes de biomasse [6, 7]. La séparation photocatalytique de l'eau, en tant que méthode la plus directe pour atteindre l'objectif d'énergie propre et renouvelable [8], est également la méthode la plus étudiée pour convertir directement l'énergie solaire en énergie chimique. Certains moyens courants de promouvoir l'efficacité de la conversion d'énergie comprennent l'augmentation de la zone de réaction, le dépôt de catalyseur et la composition avec des matériaux secondaires ; par exemple, synthétiser des microstructures spécifiques [9,10,11], déposer du Pt comme catalyseur [12, 13] et combiner deux oxydes métalliques différents [14,15,16].
TiO2 Les matrices de nanotubes (TNT) ont reçu une attention considérable pour leur grande surface, leur activité photocatalytique robuste et leurs propriétés de transfert de charge vectorielle [17,18,19]. Cependant, l'application pratique de TiO2 est limité par sa large bande interdite (3,2 eV). Cela a pour résultat d'absorber uniquement la lumière UV, qui représente 4% de la lumière solaire totale, limitant considérablement son activité photocatalytique dans la région de la lumière visible. De plus, le taux de recombinaison élevé du TiO2 réduit l'efficacité de l'activité photocatalytique. Pour résoudre ces problèmes, de nombreuses études se sont concentrées sur l'extension du bord d'absorption du TiO2 dans la région de la lumière visible, y compris le dopage avec de l'azote ou d'autres non-métaux [20, 21], la modification de surface avec des métaux nobles [22, 23] et le couplage avec des semi-conducteurs à bande étroite [14, 15, 16].
Trioxyde de molybdène (MoO3 ) est un semi-conducteur à oxyde métallique de type p avec un travail d'extraction élevé et une excellente conductivité des trous ; par conséquent, il est largement utilisé dans les cellules solaires organiques et les diodes électroluminescentes organiques [24, 25]. MoO3 a une bande interdite d'environ 2,8 eV, avec 20 à 30 % de caractère ionique et la capacité d'absorber à la fois les UV et la lumière visible [26]. Les positions des bandes de valence et de conduction de MoO3 sont tous deux inférieurs à ceux de TiO2 . Par conséquent, une hétérojonction entre TiO2 et MoO3 pourrait améliorer l'activité photocatalytique en diminuant la recombinaison de charge et en favorisant le processus de transfert de charge [27]. Sous irradiation de lumière visible, les trous excités à partir de la bande de valence de MoO3 doit être transféré dans la bande de valence de TiO2 , pour réduire la recombinaison de charge des paires électron-trou photogénérées.
La photocatalyse plasmonique a récemment facilité l'amélioration rapide de l'efficacité photocatalytique sous irradiation de lumière visible [28, 29]. Un plasmon de surface est une onde électromagnétique de surface sur l'interface métal-diélectrique, largement utilisée dans la détection optique, chimique et biologique pour la haute sensibilité de ses ondes résonantes. L'effet de résonance plasmonique de surface est confiné à la surface du métal pour former un champ électrique fortement amélioré [30]. Lorsque la fréquence de résonance particulière des nanoparticules métalliques plasmoniques correspond à celle du photon incident, un champ électrique puissant se forme près de la surface du métal. De plus, des interactions réglables entre la lumière visible incidente et les nanoparticules plasmoniques excitées sont obtenues en contrôlant leurs tailles et formes, ainsi que la constante diélectrique de l'environnement environnant [31,32,33].
Dans le présent travail, nous avons d'abord synthétisé MoS2 revêtement sur la surface des TNT par une méthode hydrothermale. MoS2 a ensuite été oxydé en MoO3 par un simple processus de recuit (Schéma 1). Ce processus a permis une couverture élevée de MoO3 particules nanométriques avec une structure très ordonnée. Pour améliorer encore les performances de séparation de l'eau photocatalytique, nous avons introduit un effet de résonance plasmonique de surface (SPR).
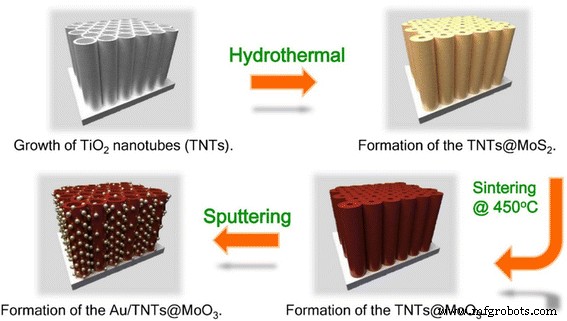
Séparation des charges à l'interface du TiO2 –MoO3 composite
Méthodes
Fabrication du TiO2 Nanotubes
Les TNT ont été fabriqués par une méthode d'oxydation anodique en deux étapes. Avant le processus d'oxydation anodique, la feuille de titane a été coupée à la bonne taille et placée dans de l'acétone, puis de l'éthanol, puis de l'eau déionisée (DI), puis soumise à des vibrations ultrasoniques pendant 5 min. L'oxydation anodique a été réalisée en utilisant un système conventionnel à deux électrodes avec la feuille de Ti comme anode et une tige de carbone comme cathode. Tous les électrolytes étaient constitués de 0,3 % en poids de fluorure d'ammonium (NH4 F) dans l'éthylène glycol (C2 H6 O2 , EG) solution avec 5 % en volume d'eau. Tous les processus ont été effectués à température ambiante.
Dans la première étape de l'oxydation anodique, la feuille de Ti a été anodisée à 60 V pendant 30 min ; les nanotubes tels que cultivés ont ensuite été éliminés dans 1 M HCl par vibration ultrasonique. La même feuille de Ti a ensuite subi un deuxième processus d'oxydation anodique à 60 V pendant 30 min. Une fois les deux étapes terminées, les TNT préparés ont été lavés avec de l'éthanol et de l'eau DI. Les TNT ont été recuits dans l'air à 450 °C pendant 4 h à une vitesse de chauffage de 2 °C/min pour former les TNT anatase.
Synthèse des TNTs@MoO3 Structure noyau-enveloppe
Les TNTs@MoO3 La structure cœur-coquille a été synthétisée avec une méthode hydrothermale et un processus de recuit simple. MoS2 Les nanofeuillets ont été synthétisés par les procédures suivantes :0,12 g de molybdate de sodium (Na2 MoO4 ·2H2 O) et 0,24 g de thioacétamide (TAA) ont été dissous dans 80 ml d'eau DI sous agitation vigoureuse pendant 15 min. Par la suite, la solution transparente et les TNT tels que cultivés ont été transférés dans un autoclave en acier inoxydable revêtu de téflon de 100 ml, qui a été scellé et chauffé à 200 °C à une vitesse de chauffage de 3 °C/min et maintenu pendant 24 h. Une fois l'autoclave refroidi à température ambiante, les TNTs@MoS2 préparés ont été lavés avec de l'eau déminéralisée. Les TNTs@MoS2 ont été recuits sous air à 450 °C pendant 4 h avec une vitesse de chauffe de 2 °C/min pour former les TNTs@MoO3 structure noyau-coque.
Dépôt de nanoparticules Au
Les photoélectrodes cocatalyseurs plasmoniques (Au/TNTs@MoO3 ) ont été fabriqués avec les TNTs@MoO3 préparés structure cocatalytique noyau-enveloppe par la méthode hydrothermale, suivie du dépôt standard par pulvérisation cathodique de nanoparticules d'Au.
Analyse des caractéristiques et mesures du photocourant
Les microstructures et les morphologies des échantillons ont été examinées à l'aide de la microscopie électronique à balayage à émission de champ (FE-SEM) et de la spectroscopie à rayons X à dispersion d'énergie (EDS). Pour confirmer l'énergie de liaison du TiO2 développé , MoS2 , et MoO3 photoélectrodes, la spectroscopie photoélectronique aux rayons X (XPS) a été utilisée. Enfin, la réaction photocatalytique a été mesurée dans une solution de NaOH 1 M en utilisant trois potentiostats terminaux à température ambiante sous une irradiation laser de 532 nm avec une taille de spot de 1 mm de diamètre.
Résultats et discussion
La figure 1 montre les images SEM et la cartographie EDS des échantillons préparés. La figure 1a–c montre les images SEM des TNT, TNTs@MoS2, et TNTs@MoO3 . L'image SEM de TNT obtenue par oxydation anodique en deux étapes d'une feuille de Ti dans 0,3 % en poids de NH4 F contenu dans la solution d'éthylène glycol (Fig. 1a) présentait une taille de pores uniforme (100-120 nm). Après la formation de la structure core-shell avec MoS2 couverte par la méthode hydrothermale, la structure poreuse des TNT n'a pas été bloquée pour réduire les sites de réaction actifs (Fig. 1b). Par la suite, les TNTs@MoO3 La structure noyau-enveloppe a été formée par un simple processus de recuit dans le four tubulaire (Fig. 1c). La figure 1d montre l'image SEM et la cartographie EDS de Au/TNTs@MoO3 , fournissant des informations claires sur le Ti, l'O, le Mo et l'Au. Le dépôt uniforme des nanoparticules d'Au en forme d'île, observable au-dessus des TNTs@MoO3 , a facilité la génération de l'effet SPR.

Images SEM de a TNT, b TNTs@MoS2 , c TNTs@MoO3 , et d Au/TNTs@MoO3 (à gauche), ainsi que la cartographie EDS (à droite)
XPS a été utilisé pour étudier les états chimiques des TNTs@MoO3 après conversion de TNTs@MoS2 par un simple processus de recuit (Fig. 2). Trois pics caractéristiques de Ti et O peuvent être observés sur les Fig. 2a, b. Les énergies de liaison aux pics Ti2p1, Ti2p3 et O1s sont respectivement de 464,6, 458,9 et 530,4 eV. Sur la figure 2c, un pic de Mo3d3 à 231,6 eV et un pic de Mo3d5 à 228,9 eV peuvent être identifiés, indiquant la composition chimique du MoS2 dans le TNTs@MoS2 . De plus, un pic faible apparaissant à environ 226 eV est le pic de signal de S2s. Les pics Mo3d3 et Mo3d5 de la Fig. 2d avec des énergies de liaison de 235,6 et 232,6 eV sont attribués à Mo 6+ dans MoO3 . Par conséquent, les investigations XPS confirment que le décalage vers le rouge du spectre reflète la conversion de la valence de l'élément Mo de tétravalent à hexavalent.
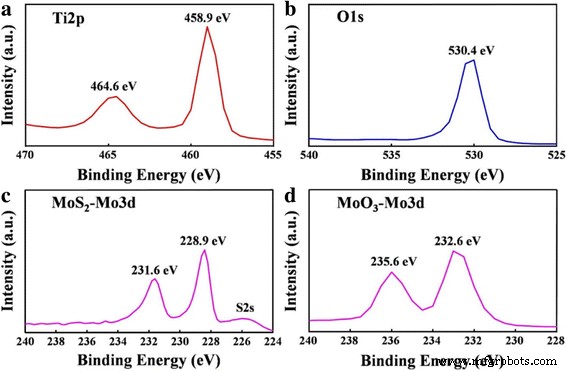
Analyse XPS de a Ti2p, b O1, c Mo3d de MoS2 , et d Mo3d de MoO3
Les performances de séparation d'eau photocatalytique des photoélectrodes préparées ont été mesurées sous irradiation laser à 532 nm. La figure 3a, b montre la réponse photocourante (courbes I-V) de TNTs@MoO3 et Au/TNTs@MoO3 . D'après les résultats, TiO2 @MoO3 présente un photocourant plus élevé en raison du taux de séparation de charge amélioré au TiO2 @MoO3 interface hétérogène (illustrée à la Fig. 3a). De plus, avec l'intégration de nanoparticules d'Au, Au/TNTs@MoO3 a présenté une réponse photocourante environ 1,5 fois plus élevée que TNTs@MoO3 à la tension de polarisation de -1 V. La figure 3c montre les courbes I–T des TNT, TNTs@MoO3 , et Au/TNTs@MoO3 à la tension de polarisation de 0 V. Comme le montre la figure 3c, la réponse du photocourant était à nouveau plus élevée dans Au/TNTs@MoO3 structure par rapport aux TNTs@MoO3 photoélectrode sans application de tension de polarisation. La réponse photocourante de Au/TNTs@MoO3 pourrait être amélioré par le simple effet SPR.
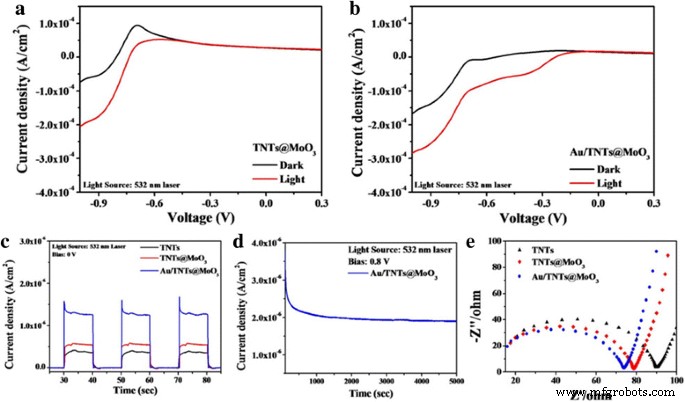
Courbes de balayage linéaire des photoélectrodes a sans et b avec irradiation lumineuse et réponses photocourantes à c 0 V (source lumineuse :laser 532 nm). d Mesures de photocourant prolongées sous irradiation laser à 532 nm. e Diagrammes de Nyquist de diverses photoélectrodes
Pour étudier plus avant l'activité photocatalytique des photoélectrodes préparées, nous avons également examiné les réponses étendues du photocourant et la spectroscopie d'impédance électrochimique pour comprendre la stabilité du photocourant et le transfert de charge aux interfaces photoélectrode-électrolyte (Fig. 3d, e). La stabilité étendue de la photoélectrode avec des performances optimales, Au/TNTs@MoO3 , a été examiné sous irradiation laser à 532 nm pendant environ 1,5 h (Fig. 3d). À la tension appliquée de 0,8 V, le photocourant est resté à 57 % de sa valeur initiale. La figure 3e montre les tracés de Nyquist des trois photoélectrodes testées sous une irradiation laser de 532 nm enregistrées à un potentiel CC de 1,23 V par rapport à RHE et une plage de fréquences de potentiel CA de 10 6 –1 Hz avec une amplitude de 1 V sous irradiation laser à 532 nm. D'après les résultats, des diamètres de demi-cercles plus petits peuvent être observés dans les Au/TNTs@MoO3 échantillon, indiquant une impédance de transport plus faible pour les porteurs de charge. La formation d'une interface hétérogène entre TiO2 et MoO3 est confirmé pour faciliter le transfert de charge et améliorer l'activité photocatalytique grâce aux excellentes propriétés de conduction des porteurs des nanoparticules d'Au.
Conclusions
Informations complémentaires
Dans les informations complémentaires (fichier supplémentaire 1), nous avons effectué l'analyse des spectres Raman de MoS2 couche, l'épaisseur associée et la taille moyenne des pores des images SEM des TNT, et le mécanisme d'amélioration du système.
Dans cette étude, nous avons fabriqué avec succès un TNTs@MoS2 hétérostructure noyau-enveloppe par un processus d'oxydation anodique en deux étapes et une méthode hydrothermale facile pour former un TNTs@MoO3 structure noyau-enveloppe par un simple processus de recuit. D'après les résultats, un MoO3 le revêtement sur une photoélectrode peut améliorer son utilisation des photons dans la région visible. De plus, avec l'intégration de nanoparticules d'Au plasmonique, une amélioration significative du photocourant de séparation de l'eau a été observée par rapport au TiO2 pur. nanotubes sous irradiation de lumière visible. L'ingénierie des bandes d'énergie des TNTs@MoO3 l'hétérostructure favorise le transfert de charge et supprime la recombinaison photogénérée des paires électron-trou entre MoO3 et TiO2 , conduisant à une activité photocatalytique améliorée.
Nanomatériaux
- Synthèse facile de composite CuSCN coloré et conducteur revêtu de nanoparticules CuS
- Synthèse hydrothermale de nanoparticules d'In2O3 jumelles hybrides disque hexagonal hétérostructures ZnO pour des activités photocatalytiques et une stabilité améliorées
- Biocompatibilité améliorée dans les matrices Anodic TaO x Nanotube
- Un nouveau photocatalyseur à hétérojonction Bi4Ti3O12/Ag3PO4 avec des performances photocatalytiques améliorées
- Matrices de nanotubes TiO2 :fabriquées à l'aide d'un modèle Soft-Hard et de la dépendance de la taille des grains des performances d'émission de champ
- Effets synergiques des nanoparticules d'Ag/BiV1-xMoxO4 avec une activité photocatalytique améliorée
- Détermination de l'activité catalytique de nanoparticules de TiO2 dopées par un métal de transition à l'aide d'une analyse spectroscopique de surface
- Effet de l'agent peptisant acide sur le rapport anatase-rutile et les performances photocatalytiques des nanoparticules de TiO2
- Une méthode facile pour charger des nanoparticules de CeO2 sur des matrices de nanotubes de TiO2 anodiques



