Construction d'une hétérojonction ZnTiO3/Bi4NbO8Cl avec des performances photocatalytiques améliorées
Résumé
La construction d'hétérojonctions est une stratégie efficace pour améliorer les performances photocatalytiques des photocatalyseurs. Ici, nous avons fabriqué du ZnTiO3 /Bi4 NbO8 Hétérojonction Cl avec des performances améliorées via une méthode de mélange mécanique typique. Le taux de dégradation de la rhodamine (RhB) sur l'hétérojonction est supérieur à celui du ZnTiO3 individuel ou Bi4 NbO8 Cl sous irradiation lampe à arc au xénon. Combinaison de ZnTiO3 avec Bi4 NbO8 Cl peut inhiber la recombinaison des porteurs photo-excités. L'efficacité quantique améliorée a été démontrée par des réponses de photocourant transitoire (PC), la spectroscopie d'impédance électrochimique (EIS), les spectres de photoluminescence (PL) et les spectres PL résolus en temps (TRPL). Cette recherche peut être précieuse pour les photocatalyseurs dans l'application industrielle.
Introduction
La photocatalyse a suscité un grand intérêt ces dernières années, qui a déjà été appliquée dans les domaines des cellules solaires, de la séparation de l'eau et de la purification de l'eau [1,2,3,4]. Il a été rapporté que les semi-conducteurs à base d'oxyde sont des photocatalyseurs actifs [5], caractérisés par TiO2 [6, 7], ZnO [8], etc. Cependant, le ZnO ou le TiO2 vierges individuels ne montre pas de performances photocatalytiques satisfaisantes. Spécialement, ZnTiO3 montre de meilleures performances dans les oxydes de type pérovskite. ZnTiO3 a été utilisé dans les domaines du capteur de gaz et de la photocatalyse, etc. [9, 10]. Cependant, la large bande interdite de ZnTiO3 (3,1 ~ 3,65 eV) [9,10,11,12,13] limite son utilisation de l'énergie solaire. En revanche, le taux élevé de recombinaison des charges photo-générées est un autre facteur de limitation. Il est nécessaire de prendre des mesures pour améliorer ses performances photocatalytiques. Une voie réalisable et pratique est celle de couplage ZnTiO3 avec un type de semi-conducteur à bande interdite étroite pour former une structure à hétérojonction [14]. Le semi-conducteur à bande interdite étroite pourrait se comporter comme un sensibilisateur pour augmenter la capacité de collecte de lumière et les performances photocatalytiques.
Bi4 NbO8 Cl, un candidat prometteur pour augmenter la récolte de lumière avec plusieurs mérites, notamment une bande interdite étroite (~ 2,38 eV), une structure en couches, un potentiel approprié de bande d'énergie [15,16,17], apparaît aux yeux des chercheurs. En raison de sa faible énergie de bande interdite et de sa structure en couches, ce matériau pourrait absorber la lumière avec une longueur d'onde inférieure à 520 nm et bénéficier du transfert de charge [18]. Quelques hétérojonctions basées sur Bi4 NbO8 Cl ont été préparés, tels que Bi2 S3 /Bi4 NbO8 Cl [17] et g-C3 N4 /Bi4 NbO8 Cl [19]. Par conséquent, en construisant ZnTiO3 /Bi4 NbO8 L'hétérojonction Cl peut être une mesure utile pour améliorer les performances photocatalytiques.
Dans cette étude, nous fabriquons une série de ZnTiO3 /Bi4 NbO8 Cl hétérojonction et évaluer les performances photocatalytiques par dégradation RhB sous irradiation lampe à arc Xénon. Nos résultats indiquent que la performance de l'hétérojonction est meilleure que celle du composant individuel. La formation d'hétérojonction pourrait ralentir la combinaison d'électrons et de trous, ce qui conduit à une activité de dégradation accrue pour RhB. Le mécanisme photocatalytique possible est discuté en détail.
Expérimental
Matériaux
Oxyde de bismuth (Bi2 O3 ), éthanol (C2 H6 O), titanate de tétrabutyle (C16 H36 O4 Ti), acide acétique (CH3 COOH) et le nitrate de zinc (Zn(NO3 )2 • 6H2 O) ont été obtenus auprès de Sinopharm Chemical Reagent Co., Ltd; oxychlorure de bismuth (BiOCl) et pentoxyde de niobium (Nb2 O5 ) ont été obtenus auprès d'Energy Chemical (Shanghai, Chine). Tous les réactifs utilisés dans ce travail sont de qualité analytique et sans autre purification.
Préparation du Bi4 NbO8 Cl
Bi4 NbO8 Le Cl a été synthétisé par des méthodes de mélange par broyeur à boulets et de réaction à l'état solide. Le mélange des matériaux a été réalisé dans un broyeur planétaire à boulets (Grinoer-BM4, Chine), équipé d'un bol de broyage en corindon et de billes de corindon. Bi2 O3 (18 g), BiOCl (12 g) et Nb2 O5 (6 g) ont été pesés et mélangés en utilisant de l'éthanol (30 mL) comme solution de dispersion dans un bol de broyage, et cinquante billes (diamètre 10 mm) ont été ajoutées puis broyées pendant 2 h à 300 tr/min. Après broyage, les réactifs mélangés ont été séchés à 60 °C pendant 12 h et calcinés à 600 °C (vitesse de chauffage de 5 °C/min) à l'air pendant 10 h. Enfin, les poudres jaunes de Bi4 NbO8 Cl ont été obtenus.
Préparation du ZnTiO3
La procédure sol-gel a été utilisée pour préparer le ZnTiO3 poudre. Dans une synthèse typique, 34 mL de titanate de tétrabutyle (0,1 mol) ont été dissous dans 35 mL d'éthanol pour former une solution A. Cinq millilitres d'eau déminéralisée, 15 mL d'acide acétique (CH3 COOH), et une certaine quantité de Zn(NO3 )2 • 6H2 O ont été successivement dissous dans 35 mL d'éthanol pour former une solution B. Ensuite, la solution B a été ajoutée goutte à goutte à la solution A sous agitation magnétique. Un sol transparent a été obtenu après l'ajout d'une agitation pendant 30 min qui a formé un gel sur une période de repos de 24 h. Le gel a été séché à 105 °C pendant 12 h, puis le produit résultant a été calciné à 600 °C pendant 3 h à la vitesse de chauffage de 2 °C/min pour obtenir le ZnTiO3 final. poudres.
Préparation du ZnTiO3 /Bi4 NbO8 Cl hétérojonction
Dans une expérience typique, 400 mg de Bi4 NbO8 Cl et une certaine quantité de ZnTiO3 (rapport massique de ZnTiO3 :Bi4 NbO8 Cl = 10%, 20%, 30%) ont été mélangés et broyés pendant 10 min, puis ils ont été dispersés dans 10 mL d'éthanol, et suivis par ultrasons pendant 30 min. Les mélanges résultants ont été séchés à 60 °C pendant 12 h, puis calcinés à 300 °C pendant 2 h. Les échantillons bruts de fabrication ont été notés 10 % BNZ, 20 % BNZ et 30 % BNZ.
Caractérisation
Les mesures de diffraction des rayons X sur poudre (XRD) ont été enregistrées avec un spectromètre D-max 2500 XRD (Rigaku), et les plages de balayage étaient de 10 à 80° avec 10°/min. Les morphologies des échantillons tels que préparés ont été caractérisées par la microscopie électronique à balayage (SEM, JSM-6700F, JEOL, Japon) et la microscopie électronique à transmission (TEM, JEM-2100, JEOL, Japon). La spectroscopie à dispersion d'énergie et l'analyse de cartographie élémentaire ont été obtenues avec le spectromètre à rayons X équipé du microscope électronique à balayage. Les spectres de réflectance diffuse UV-vis (UV-vis DRS) ont été obtenus à l'aide d'un spectrophotomètre Agilent Technologies Cary 5000 avec une sphère d'intégration dans laquelle BaSO4 la poudre a été utilisée comme référence. Les spectres de photoluminescence (PL) et de décroissance transitoire résolus dans le temps ont été enregistrés sur les spectrophotomètres à fluorescence Hitachi FL-4600 et Edinburgh FLS1000 avec une longueur d'onde d'excitation de 365 nm, respectivement.
Expérimental photocatalytique
La photodégradation RhB a été examinée en tant que réaction modèle pour évaluer les performances photocatalytiques des échantillons. Cinquante milligrammes de photocatalyseur ont été dispersés dans 50 mL de solution de RhB (5 mg/L) dans le récipient du photoréacteur en quartz. Une lampe à arc au xénon de 500 W placée à 15 cm du réacteur a servi de source lumineuse. Initialement, le mélange a été maintenu à l'obscurité pendant 30 minutes sous agitation magnétique pour atteindre l'équilibre adsorption-désorption. Plus tard, des aliquotes de suspension (4 mL) ont été échantillonnées et centrifugées à des intervalles donnés de 30 min. La concentration de colorant a été analysée par un spectrophotomètre Agilent Technologies Cary 5000.
A titre de comparaison, une certaine quantité de Bi4 NbO8 Cl et ZnTiO3 (rapport massique de ZnTiO3 :Bi4 NbO8 Cl = 20%) ont été ajoutés directement dans un récipient de photoréacteur en quartz pour faire une expérience d'évaluation de l'activité photocatalytique. Le résultat de cet échantillon a été nommé 20 % BNZ-C (« C » signifie comparaison).
Le processus de l'expérience de l'agent de capture est le même que celui de l'évaluation de l'activité photocatalytique vient d'ajouter respectivement 40 μL d'isopropanol (IPA) en tant que piégeur de radicaux hydroxyle, 0,005 g de p-benzoquinone (BQ) en tant que piégeur de radicaux superoxyde, 0,0158 g de sel disodique d'acide éthylènediaminetétraacétique (EDTA-2Na) comme agent de piégeage des trous, et 0,078 g de bromate de potassium (KBrO3 ) comme agent de piégeage d'électrons.
Mesures électrochimiques
Les propriétés photoélectrochimiques ont été mesurées sur un système électrochimique CHI760E (Shanghai Chenhua, Chine) dans une électrode standard à trois électrodes avec le verre FTO déposé par catalyseur, la plaque de Pt et l'électrode Ag/AgCl comme photoanode, contre-électrode et électrode de référence, respectivement. Pendant ce temps, 0,5 M Na2 SO4 a été utilisé comme solution électrolytique. Des mesures de photocourants transitoires ont été effectuées en utilisant une lampe Xe de 500 W comme source lumineuse. La mesure de Mott-Schottky a été réalisée à une fréquence de 1000 Hz. Les photoanodes de travail ont été préparées comme suit :un échantillon de 30 mg, 300 μL de solution de mélange de chitosane (1% en poids) et d'acide acétique (1% en poids) ont été mélangés en agitant pendant 20 min pour former une suspension. Ensuite, le mélange ci-dessus a été ajouté goutte à goutte sur un verre FTO (3 × 1 cm) et séché à 40 °C.
Résultats et discussion
La structure cristalline des échantillons a pu être détectée à partir des résultats XRD [20], comme le montre la figure 1a. Les pics de diffraction caractéristiques à 23,7°, 26,0°, 29,6°, 32,6°, 46,7° et 56,3° pourraient être indexés sur (112), (114), (116), (020), (220) et ( 316) plans du Bi4 nu NbO8 Cl (carte JCPDS 84-0843). Les plans cristallins (220), (311), (400), (422), (511) et (440) ont une bonne correspondance avec la pérovskite cubique ZnTiO3 structure (groupe d'espaces R-3 avec constante de cellule a = b = c = 0.841 nm, carte JCPDS 39-0190). Les modèles XRD des échantillons BNZ sont similaires à ceux du Bi4 NbO8 Cl, et l'intensité du pic de diffraction par réflexion à 35,4° pour ZnTiO3 augmenté avec l'ajout de ZnTiO3 contenu. De plus, les signaux associés à Zn, Ti, Bi, Nb, O et Cl sont observés à partir des images de cartographie EDX (Fig. 1d) de ZnTiO3 /Bi4 NbO8 Cl hétérojonction.
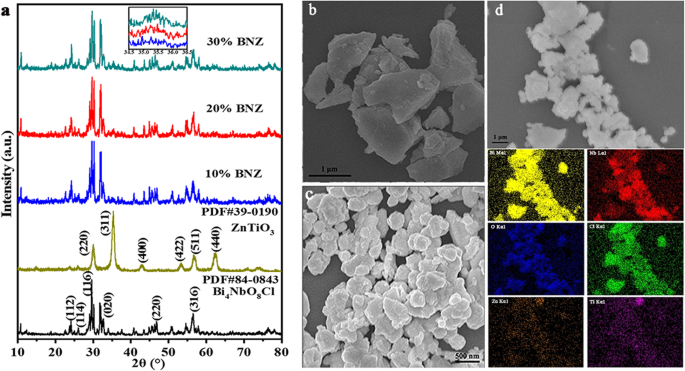
un Modèles XRD de ZnTiO3 , Bi4 NbO8 Échantillons Cl et BNZ ; Images SEM de b Bi4 NbO8 Cl, c ZnTiO3 , d Image SEM et images cartographiques EDX de 20 % BNZ
La morphologie du ZnTiO3 , Bi4 NbO8 Les échantillons Cl et BNZ sont étudiés par SEM. La figure 1b montre que ZnTiO3 l'échantillon est une structure de blocs irréguliers à l'échelle du micron. Bi4 immaculé NbO8 Les produits Cl sont composés de particules ellipsoïdes irrégulières dans lesquelles montre une structure empilée due au regroupement des particules, vue sur la figure 1c. Quant au composé BNZ à 20 % (Fig. 1d), on constate que ZnTiO3 sont écrasés et attachés à la surface du Bi4 NbO8 Cl après broyage, mélange aux ultrasons et traitement de calcination.
La figure 2 affiche les images TEM et HRTEM de l'échantillon de 20 % de BNZ, ainsi que le modèle de transformée de Fourier rapide (FFT) et l'image FFT inverse (IFFT) des zones sélectionnées correspondantes. On peut clairement observer qu'il existe un contact d'interface étroit entre le ZnTiO3 blocs et Bi4 NbO8 Blocs Cl (Fig. 2a). Marquée d'un fil de fer rouge sur la figure 2b, la frange de réseau mesurée de 0,375 nm correspond à Bi4 NbO8 Cl (112) plan cristallin, et ses FFT et IFFT correspondants sont affichés sur la figure 2c. Comme le montre la figure 2b, les franges de réseau mesurées de 0,301 nm et 0,293 nm correspondent bien à Bi4 NbO8 Plan cristallin Cl (116) (zones vertes) et ZnTiO3 (311) plan cristallin (zones oranges), et leurs images FFT et IFFT sont montrées sur les Fig. 2d et 2e, respectivement. L'analyse HRTEM suggère que Bi4 NbO8 Cl et ZnTiO3 sont bien combinés.

un , b Images TEM et HRTEM de 20 % de BNZ ; c Images IFFT et FFT de Bi4 NbO8 plans cristallins Cl (112) ; d Images IFFT et FFT de Bi4 NbO8 plans cristallins Cl (116) ; e Images IFFT et FFT de ZnTiO3 (311) plans de cristal
Les performances photocatalytiques du Bi4 immaculé NbO8 Cl, ZnTiO3 , et les hétérojonctions BNZ ont été évaluées par la dégradation d'une solution aqueuse de colorant RhB sous irradiation par lampe à arc au xénon. Comme le montre la figure 3a, le taux d'adsorption de RhB pour tous les échantillons est de 0 à 11 % dans l'obscurité. Après exposition à la lumière pendant 5 h, le taux de dégradation sur le Bi4 nu NbO8 Cl et ZnTiO3 sont respectivement de 89 % et 61 %. De plus, les composites BNZ présentent une activité photocatalytique améliorée et l'efficacité d'élimination des colorants est augmentée avec l'augmentation de ZnTiO3 contenu dans un premier temps, puis les performances de photodégradation ont une légère diminution lorsque le ZnTiO3 teneur augmentée de 20 % en poids à 30 % en poids. Le composite 20 % BNZ affiche l'activité photocatalytique la plus élevée avec un taux de dégradation de près de 100 %. Quant au BNZ-C à 20 %, le taux d'élimination du RhB est de 81 % après 5 h de réaction. Vingt pour cent de BNZ ont montré des performances photocatalytiques plus élevées en raison d'une séparation efficace des porteurs après la formation d'hétérojonctions.
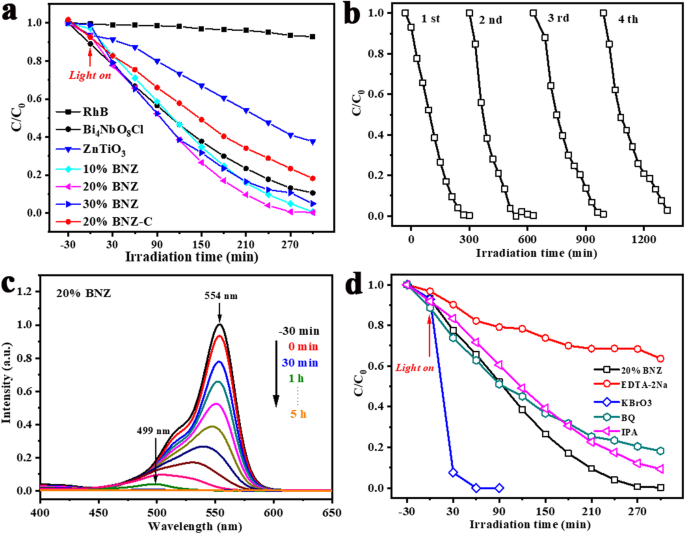
un Efficacité de dégradation photocatalytique de RhB avec ZnTiO3 , Bi4 NbO8 Hétérojonctions Cl et BNZ sous irradiation par lampe à arc au xénon ; b pistes cyclées de 20% BNZ; c changements dans les spectres d'absorption UV-vis de RhB de 20 % de BNZ sous irradiation par lampe à arc au xénon ; d résultats d'expériences de piégeage de 20 % de BNZ avec irradiation par lampe à arc au xénon
La recyclabilité des photocatalyseurs est également un aspect important dans leur application pratique. Les expériences cycliques d'élimination du colorant RhB ont été réalisées dans les mêmes conditions pour étudier la recyclabilité d'échantillons de BNZ à 20 %, comme le montre la figure 3b. Après quatre expériences répétées, l'activité photocatalytique présente juste une légère diminution, indiquant que le BNZ à 20 % est un photocatalyseur stable pour la dégradation de RhB. La figure 3c montre les changements dans les spectres d'absorption UV-vis de RhB de 20 % de BNZ, avec l'augmentation du temps d'irradiation, l'intensité du pic caractéristique est diminuée. De plus, la position du pic d'absorption est passée de 554 à 499 nm au cours de la réaction photocatalytique. Ce décalage vers le bleu du maximum d'absorption est causé par le N -déséthylation de RhB [21,22,23].
Afin de clarifier les principales espèces actives responsables de la dégradation de RhB par 20% de composite BNZ, des expériences de piégeage ont été réalisées. Le sel disodique de l'acide éthylènediaminetétraacétique (EDTA-2Na), le bromate de potassium (KBrO3 ), la benzoquinone (BQ) et l'isopropanol (IPA) agissent comme les charognards du trou (h + ), électron (e − ), le radical superoxyde (•O2 − ) et le radical hydroxyle (•OH), respectivement. Comme le montre la figure 3d, le taux de photodégradation est sérieusement affecté et diminué par l'ajout d'EDTA dans le système de réaction photocatalytique, et l'activité photocatalytique est légèrement inhibée lorsque du BQ ou de l'IPA est ajouté. Par conséquent, le h + était la principale espèce réactive dominante, et le •O2 − ou • OH a participé au processus de dégradation de RhB dans le système BNZ à 20 %.
Comme le montre la figure 4a, les réponses de photocourant transitoire des photocatalyseurs tels que préparés ont été mesurées sous l'irradiation lumineuse avec des cycles intermittents marche-arrêt pour évaluer la production et la migration des porteurs photogénérés. L'intensité plus élevée du photocourant, la capacité de génération plus forte des porteurs photogénérés [24, 25]. La densité de photocourant est plus élevée à la lumière qu'à l'obscurité et affiche un mode de cycle marche-arrêt typique. Les intensités de réponse du photocourant obéissent à l'ordre suivant :20% BNZ > 30% BNZ > 10% BNZ > Bi4 NbO8 Cl > ZnTiO3 . Cela signifie que la capacité de production des supports photogénérés de 20% BNZ est la meilleure. La densité de photocourant manifestement améliorée de l'échantillon de BNZ à 20 % pourrait être attribuée au contact suggéré dans l'hétérojonction, ce qui profite à la génération, à la séparation et au transfert de charge. De plus, la spectroscopie d'impédance électrochimique (EIS) a été utilisée pour étudier la capacité du transfert de charge interfaciale des catalyseurs. Plus le rayon d'arc des tracés EIS de Nyquist devient petit, plus la résistance de transfert de charge est [26]. D'après les résultats (Fig. 4b), on peut observer que les 20 % de BNZ présentaient le plus petit arc semi-circulaire, ce qui indiquait que 20 % de BNZ possédaient une résistance de transfert plus faible et que le processus des porteurs de charge était très rapide par rapport aux autres, car -échantillons préparés. Afin d'étudier les comportements de recombinaison des porteurs photogénérés, les spectres PL (Fig. 4c) avec la longueur d'onde excitée de 365 nm à température ambiante ont été obtenus [27]. Par rapport au Bi4 nu NbO8 Cl, l'intensité PL de la BNZ à 20 % telle que préparée est plus faible, indiquant un taux de recombinaison inférieur des porteurs photogénérés. Ces résultats impliquent que l'introduction de ZnTiO3 pourrait effectivement habiter la recombinaison des électrons photo-générés (e − ) et des trous (h + ). Comme le montre la figure 4d, les spectres PL résolus en temps pourraient fournir des informations sur la durée de vie des porteurs photo-excités. Les courbes de décroissance PL résolues en temps des échantillons ont été ajustées par Eq. (1) :
$$ I(t)={A}_1{e}^{\frac{-t}{\tau_1}}+{A}_2{e}^{\frac{-t}{\tau_2}} $$ (1)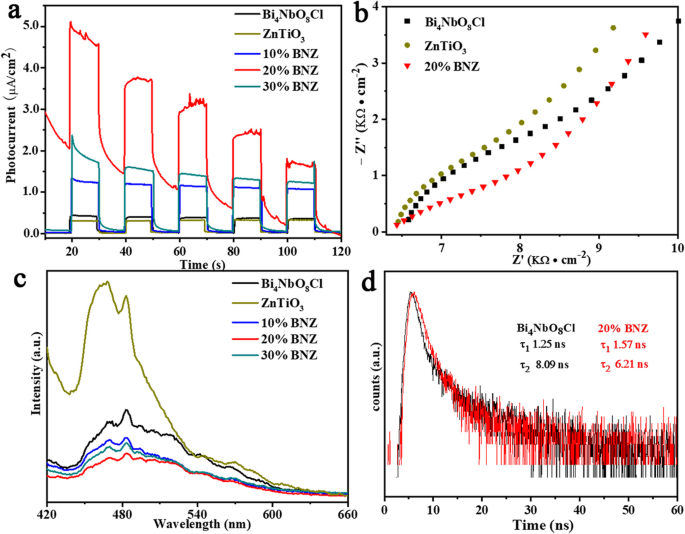
un Réponses transitoires au photocourant de ZnTiO3 , Bi4 NbO8 Échantillons Cl et BNZ. b Spectroscopie d'impédance électrochimique de ZnTiO3 , Bi4 NbO8 Cl et 20% BNZ. c Spectres de photoluminescence de ZnTiO3 , Bi4 NbO8 Échantillons Cl et BNZ. d Spectres PL résolus en temps de Bi4 NbO8 Cl et 20% BNZ
Où τ 1 et τ 2 sont respectivement la constante de décroissance rapide (durée de vie plus courte) et la constante de décroissance plus lente (durée de vie longue). Un 1 et A 2 sont les amplitudes correspondantes. La durée de vie moyenne a été calculée par l'équation. (2) [17] :
$$ \uptau =\frac{A_1{\tau}_1^2+{A}_2{\tau}_2^2}{A_1{\tau}_1+{A}_2{\tau}_2} $$ (2 )La durée de vie moyenne de 20% BNZ est plus courte que celle de Bi4 NbO8 Cl (τBiNb = 3,66 ns et τ20 % BNZ = 2,72 ns). Le τ la valeur est diminuée de 3,66 à 2,72 après modification de ZnTiO3 , indiquant que la formation d'hétérojonctions pourrait améliorer l'efficacité de transfert des porteurs et favoriser la séparation des électrons et des trous photogénérés [28,29,30].
Spectres de réflectance diffuse (DRS) de Bi4 NbO8 Cl, ZnTiO3 , et 20 % de BNZ ont été mesurés dans la plage de 300 à 800 nm pour étudier leur propriété optique. Comme le montre la Fig. 5a, on peut constater que le bord d'absorption de ZnTiO3 est de 375 nm et Bi4 NbO8 Cl a une bande d'absorption intense avec un bord d'absorption abrupt à environ 505 nm. De plus, le bord d'absorption 20% BNZ est d'environ 510 nm. En outre, l'énergie de bande interdite (Eg) des semi-conducteurs peut être calculée par l'équation de Tauc, (αhv) n = A (hv − Eg), où Eg, A , α , h , et v sont respectivement la bande interdite, la constante d'absorption, le coefficient d'absorption, la constante de Planck et la fréquence de la lumière [31]. De plus, n représente un matériau à transition directe (n = 2) ou un matériau à transition indirecte (n = 1/2). Comme nous le savons tous, les deux Bi4 NbO8 Cl et ZnTiO3 sont des semi-conducteurs à transition indirecte, donc n est égal à 4. Comme le montre la figure 5b, les valeurs de bande interdite de Bi4 tel que préparé NbO8 Cl, ZnTiO3 , et 20 % des échantillons BNZ sont respectivement de 2,33 eV, 3,10 eV et 2,31 eV.
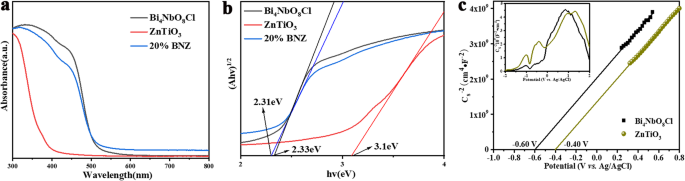
un Spectres DRS de ZnTiO3 , Bi4 NbO8 Cl et échantillon de 20 % BNZ. b Courbes de Tacus de ZnTiO3 , Bi4 NbO8 Cl et échantillon de 20 % BNZ. c Courbes de Mott–Schottky de ZnTiO3 et Bi4 NbO8 Cl
Le potentiel de bande de conduction (CB) et le potentiel de bande de cantonnière (VB) sont les facteurs les plus importants pour comprendre la formation d'hétérojonction et le mécanisme de transfert d'électrons des nanocomposites. On sait que le bas du CB est proche de la position bande plate; ainsi, des tests de Mott-Schottky ont été effectués pour estimer le potentiel de bande plate (Efb ) d'échantillons [32]. Le potentiel de bande plat correspondant de l'électrode a été obtenu à partir des tracés M-S utilisant les équations suivantes. (3) et (4) [31, 33] :
$$ \mathrm{Pour}\ \mathrm{an}\ \mathrm{n}-\mathrm{type}\ \mathrm{semiconducteur}\frac{1}{C^2}=\frac{2}{e\ varepsilon {\varepsilon}_o ND}\left(E-{E}_{fb}-\frac{KT}{e}\right) $$ (3) $$ \mathrm{Pour}\ \mathrm{an} \ \mathrm{p}-\mathrm{type}\ \mathrm{semiconducteur}\frac{1}{C^2}=\frac{2}{e\varepsilon {\varepsilon}_0 NA}\left(E- {E}_{fb}-\frac{KT}{e}\right) $$ (4)où le ε , ε o , e , C , E , E fb , K , T , N D , et N A représentent la constante diélectrique des matériaux, la permittivité de l'espace libre, la charge de l'électron (1,60 × 10 −19 C), capacité de la région de charge d'espace, appliquée au potentiel, au potentiel de bande plate, à la constante de Boltzmann, à la température absolue, à la densité du donneur et de l'accepteur, respectivement. Comme le montre la figure 5c, tous les tracés affichent des pentes positives, ce qui confirme clairement que les échantillons tels que préparés agissent comme un comportement de semi-conducteur de type n [34, 35]. Le potentiel de bande plate peut être mesuré à partir de l'intersection de la courbe de potentiel linéaire jusqu'au X -axe au point 1/C 2 = 0, et peut être converti en échelle d'électrode à hydrogène normalisée (NHE) selon la formule (5) [36] :
$$ E\gauche(\mathrm{NHE}\right)=E\gauche(\mathrm{Ag}/\mathrm{AgCI}\right)+0.197\mathrm{V} $$ (5)Selon les résultats M-S, le potentiel de bande plate pour Bi4 NbO8 Cl et ZnTiO3 est de − 0,60 eV et − 0,40 eV (vs Ag/AgCl), respectivement. En conséquence, ECB de Bi4 NbO8 Cl et ZnTiO3 est de − 0,403 eV et − 0,203 eV, respectivement. Ainsi, le EVB de Bi4 NbO8 Cl est de 1,927 eV et EVB de ZnTiO3 est de 2,897 eV.
Les surfaces spécifiques BET du Bi4 NbO8 Cl, ZnTiO3 , et 20 % BNZ sont indiqués dans le tableau 1. Le SBET de 20 % BNZ correspond à 0,87 m 2 /g plus que SBET de Bi4 NbO8 Cl. Il ressort du tableau 1 que le SBET de ZnTiO3 mesure 5,34 m 2 /g. Le SBET augmenté de 20% BNZ est due à l'introduction de ZnTiO3 . La possibilité d'utiliser la lumière de ZnTiO3 est faible en raison de sa large bande interdite. Par conséquent, l'augmentation du SBET peut ne pas fournir de nombreux sites actifs efficaces. En revanche, ZnTiO3 peut couvrir les sites actifs de Bi4 NbO8 Cl surface ou devient de nouveaux centres de recombinaison d'électrons et de trous. Ainsi, l'augmentation du SBET de 20 % de BNZ peut n'avoir qu'un léger impact pour des performances photocatalytiques améliorées. L'amélioration des performances est principalement due à la formation d'hétérojonction.
Pour expliquer les performances photocatalytiques améliorées, un mécanisme photocatalytique possible est proposé dans le schéma 1. Sous l'irradiation d'une lampe à arc au xénon, les électrons (e − ) sont générés dans Bi4 NbO8 Cl, et ils passent de VB à CB en laissant les trous correspondants (h + ) sur VB. Pendant ce temps, le même processus se déroule dans ZnTiO3 . Par une comparaison du potentiel de bande d'énergie entre Bi4 NbO8 Cl et ZnTiO3 , ECB (Bi4 NbO8 Cl) est plus négatif que ECB (ZnTiO3 ), et EVB (ZnTiO3 ) est plus positif que EVB (Bi4 NbO8 Cl). Par conséquent, ils peuvent former une hétérojonction de type II. En raison du champ électrique interne, e − sur CB de Bi4 NbO8 Cl est transféré au CB de ZnTiO3 , et h + sur VB de ZnTiO3 est transféré au VB de Bi4 NbO8 Cl, réalisant la séparation des e − photo-excités -h + paires, ce qui conduit à l'amélioration des performances. Parce que 20% de BNZ a un potentiel positif élevé de VB, ses trous ont donc une capacité oxydante élevée. Par conséquent, les trous sur VB peuvent oxyder directement les polluants organiques comme RhB. Cependant, rapport excessif de ZnTiO3 dans l'hétérojonction BNZ couvrira les sites actifs de Bi4 NbO8 surface Cl, diminuant sa capacité de récolte de lumière. De plus, rapport excessif de ZnTiO3 peuvent devenir de nouveaux centres de recombinaison d'électrons et de trous. Par conséquent, la quantité de ZnTiO3 a une valeur optimale en hétérojonction.
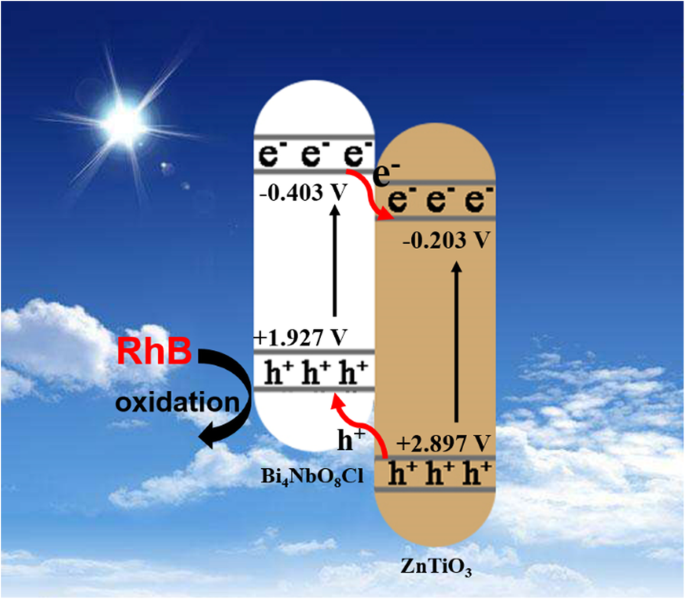
Schéma de principe du mécanisme proposé pour la dégradation de RhB sur le ZnTiO3 /Bi4 NbO8 Photocatalyseurs à hétérojonction Cl sous irradiation par lampe à arc au xénon.
Conclusions
Dans ce travail, le ZnTiO3 /Bi4 NbO8 Le catalyseur à hétérojonction Cl a été préparé avec succès via une méthode de mélange mécanique typique. L'hétérojonction présente des performances photocatalytiques améliorées par rapport au ZnTiO3 individuel ou Bi4 NbO8 Cl sous irradiation lampe à arc au xénon. Spécialement, 20% ZnTiO3 /Bi4 NbO8 L'hétérojonction Cl a les meilleures performances. Ce rapport peut inspirer le développement d'une structure à hétérojonction dans la modification et l'application de catalyseurs.
Disponibilité des données et des matériaux
Les ensembles de données utilisés au cours de la présente étude sont disponibles auprès de l'auteur correspondant sur demande raisonnable.
Abréviations
- BNZ :
-
ZnTiO3 /Bi4 NbO8 Cl
- BNZ-C :
-
ZnTiO3 /Bi4 NbO8 Cl-Comparaison
- SBET :
-
Surfaces spécifiques BET
- PL :
-
Photoluminescence
- CB :
-
Bande de conduction
- VB :
-
Bande de Valence
Nanomatériaux
- Améliorez les performances avec le soudage automatisé
- Blog :Appareils médicaux à haute performance
- Composite mécanique de LiNi0.8Co0.15Al0.05O2/Nanotubes de carbone avec des performances électrochimiques améliorées pour les batteries lithium-ion
- Activités photocatalytiques renforcées par des nanoparticules Au-Plasmonic sur une photoélectrode de nanotube de TiO2 recouverte de MoO3
- Performances photocatalytiques induites par la lumière visible des nanocomposites ZnO/g-C3N4 dopés N
- Préparation et performances photocatalytiques des photocatalyseurs à structure creuse LiNb3O8
- Un nouveau photocatalyseur à hétérojonction Bi4Ti3O12/Ag3PO4 avec des performances photocatalytiques améliorées
- Effets synergiques des nanoparticules d'Ag/BiV1-xMoxO4 avec une activité photocatalytique améliorée
- Comparaison des performances entre les équipements de construction électriques et les moteurs diesel



