Effet des alcalis sur le processus de fabrication du fer dans un haut fourneau
Effet des alcalis sur le processus de fabrication du fer dans un haut fourneau
L'un des principaux objectifs lors de l'exploitation d'un haut-fourneau (BF) est de maximiser la production de métal chaud (HM) de la composition chimique souhaitée au moindre coût. Cela nécessite une base de matière première de haute qualité et un fonctionnement régulier et régulier du haut fourneau. La qualité des matériaux de charge est très importante pour éviter les problèmes dans le processus causés par des éléments indésirables entrant dans le four. Dans ce domaine, il convient également de prêter attention à la teneur en éléments indésirables de la charge d'entrée. Ces éléments indésirables causent un certain nombre de problèmes technologiques dans le BF. De plus, ils affectent considérablement le coût de production du HM. Les principaux éléments indésirables présents dans la charge qui peuvent être gênants pour l'élimination et les performances du BF sont les composés alcalins des métaux potassium (K) et sodium (Na).
Dans le procédé BF, la présence d'alcalis est connue pour avoir des influences négatives sur le procédé. Les alcalis provoquent une plus grande réactivité du coke, un ramollissement prématuré de la charge de minerai, une décomposition de l'aggloméré, un gonflement des pastilles, et sont impliqués dans la formation des dépôts sur le revêtement réfractaire du BF qui accélèrent l'usure du revêtement. Les effets négatifs des alcalis sont dus à l'effet catalytique sur la gazéification du coke, à la destruction de la structure du carbone (C) due à l'insertion d'alcali, à la formation d'échafaudages et à l'attaque réfractaire. Les alcalis sont introduits avec les matières premières et en raison de la circulation des alcalis (Fig 1), les alcalis sont captés sur le chemin vers la zone de température plus élevée dans le BF.
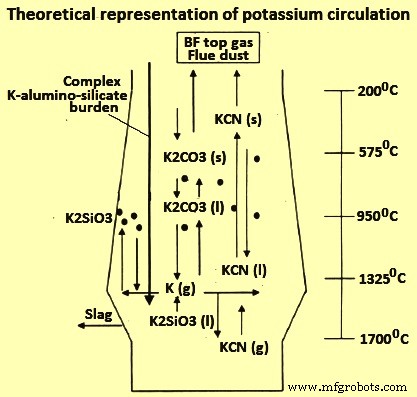
Fig1 Représentation théorique de la circulation du K
La présence d'alcali entraîne une production réduite et une consommation de coke plus élevée dans le BF, environ 4,5 % et 2,3 % respectivement pour chaque kg/tML d'alcali ajouté avec la charge supérieure de matière première. L'alcali diminue la production en raison de l'abaissement du seuil de la réaction réversible de Boudouard, C (s) + CO2 (g) =2CO (g), de l'augmentation du gaz de coke et de la résistance réduite du coke. La perméabilité au gaz est diminuée en raison de la dégradation du coke et des échafaudages sur les murs peuvent se produire, réduisant ainsi le volume du BF.
Réactions alcalines dans le BF
Dans toutes les réactions alcalines données dans cet article, K peut être remplacé par Na. La réduction des silicates alcalins par C peut avoir lieu selon les réactions réversibles K2SiO3 (laitier) + C(s) =2K (g) + SiO2 (laitier) + CO (g), et K2SiO3 (laitier) + 3C(s) =2K (g) + Si (HM) + 3CO (g). L'ampleur de ces réactions dépend de la température et de la pression partielle de CO (monoxyde de carbone). Les oxydes alcalins peuvent être réduits soit par C dans le coke, soit par le CO selon les réactions réversibles K2O + C (s) =2 K (g) + CO (g) et K2O + CO (g) =2 K (g ) + CO2 (g).
Les alcalis sont volatilisés en tant qu'éléments ou réagissent avec C et N2 (azote) dans la région bosh du BF formant des vapeurs de cyanure de potassium (KCN) ou de cyanure de sodium (NaCN) selon la réaction réversible 2K (g) + N2 (g) =2KCN (g). Les vapeurs sont entraînées avec le gaz du four et ne se dissolvent pas dans le HM ni dans le laitier. Le point de fusion et le point d'ébullition pour K sont respectivement de 63,4 degrés C et 759 degrés C, tandis que les températures de fusion et d'ébullition correspondantes pour Na sont respectivement de 97,7 degrés C et 883 degrés C. Les points de fusion de KCN et de NaCN sont respectivement de 622 degrés C et 562 degrés C, et les points d'ébullition sont respectivement de 1625 degrés C et 1530 degrés C. L'état de ces composés est liquide dans le puits inférieur et gazeux dans le chemin de roulement et la zone du foyer, en fonction de la température. Le gaz est transporté par les gaz en mouvement rapide dans le BF.
Dans le puits où le potentiel d'oxygène (O2) augmente (vers 1100 deg C), K et KCN ne sont plus stables et sont oxydés par le dioxyde de carbone (CO2) en carbonates alcalins (K2CO3, Na2CO3) selon les réactions 2K ( g) + 2CO2 (g) =K2CO3 + CO (g), et 2KCN (g) + 4CO2 (g) =K2CO3 (s) + N2 (g) + 5CO (g) respectivement et les oxydes alcalins par le CO selon le réaction réversible 2KCN (g) + CO (g) =K2O + 3C + N2 (g). Les carbonates alcalins générés partent sous forme de fines blanches, qui sont réparties à la surface du matériau de charge ou situées sur le revêtement de brique.
Les composants alcalins adsorbés dans le matériau de charge et le coke forment de nouveaux composés en fonction de leur stabilité relative. Le carbonate de potassium (K2CO3) et le carbonate de sodium (Na2CO3) sont solides à des températures inférieures à 891 degrés C et inférieures à 851 degrés C respectivement. Les composés porteurs alcalins descendent avec les matériaux de charge et sont réduits et vaporisés à nouveau pour atteindre la zone à haute température, selon la réaction réversible K2CO3(l) + 2C =2K (g) =3CO (g).
La majeure partie de l'alcali est évacuée du BF avec le laitier. Cependant, une partie de l'alcali dans le laitier est réduite en générant de la vapeur d'alcali qui monte avec le gaz environnant. La vapeur alcaline se condense dans la partie supérieure du BF d'où une partie sort avec le gaz de tête, tandis que le reste se condense sur les parois internes ou sur le matériau d'alimentation. En raison de la volatilisation et de la condensation de l'alcali dans les différentes zones thermiques, l'alcali a tendance à circuler dans le BF, entraînant une accumulation et des interactions avec d'autres matières premières. Cela peut avoir un impact significatif sur le processus, même lorsque l'alcali est chargé en petites quantités, généralement moins de 5 kilogrammes par tonne de fonte (kg/tML). Une vue simplifiée de la circulation alcaline dans le BF est illustrée à la Fig 2. Des études sur les BF excavées ont montré que le niveau d'alcali est le plus élevé là où la température est supérieure à 1000 ° C, ce qui signifie qu'il y a une concentration accrue d'alcali dans la partie inférieure de le BF.
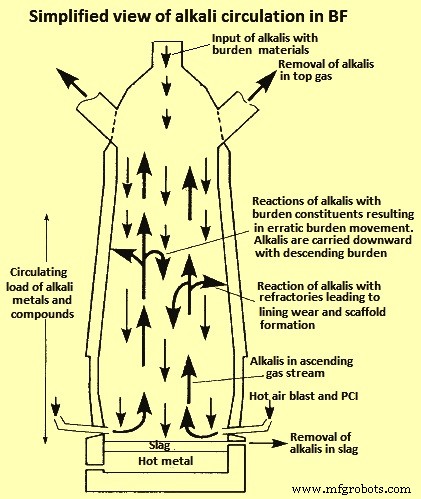
Fig 2 Une vue simplifiée de la circulation alcaline dans le BF
Cycle alcalin dans le BF
Les alcalis entrent normalement dans le BF avec le fer et avec le coke sous forme de silicates. Pour un fonctionnement BF fluide et efficace, il est souhaitable de limiter la quantité d'alcali à environ 1,5 kg/tML à 5 kg/tML, mais elle varie normalement de 2,5 kg/tML à 7,5 kg/tML dans différentes usines. Parmi les deux substances alcalines Na et K, K est normalement le composé principal entrant dans le BF. La plupart des alcalis partent avec le laitier tandis que certains deviennent une partie du gaz de gueulard et quittent le four avec le gaz de gueulard. L'alcali en recirculation peut être éliminé soit par le laitier, soit par le gaz. K va au gaz de tête à un degré plus élevé car il est plus volatil par rapport à Na qui sort plus avec le laitier.
Les alcalis entrent dans le BF sous forme de silicates (K2SiO3). Des études du cycle alcalin ont montré que les silicates descendent avec la charge et le cycle commence avec la réduction du silicate alcalin par le C du coke dans la zone de fusion selon l'équation K2SiO3 + C (s) =2K (g) + SiO2 + CO (g). Les réactions ont lieu à environ 1550 degrés C selon les données thermodynamiques des réactions. Tous les oxydes alcalins qui entrent ou se forment dans le BF réagissent plus haut dans le BF à des températures plus basses selon l'équation K2O + CO (g) =2K (g) + CO2 (g) car ils ne sont pas stables. Le K2O peut également se dissoudre dans le laitier primaire.
De plus les vapeurs de K produites au niveau du foyer dans le BF, réagissent avec le charbon pulvérisé injecté et le N2 du souffle d'air chaud selon l'équation 2K (g) + 2C (s) + N2 (g) =2KCN (g , l). Le point d'ébullition du KCN est de 1625 degrés C, de sorte que lorsque le cyanure de potassium (KCN) s'élève loin du souffle d'air chaud des tuyères, il se transforme en une phase liquide lorsque la température baisse. Le temps dans la zone de la tuyère est très court en raison du débit de gaz élevé, de sorte que les cyanures alcalins ont le temps de remonter le BF avant de se transformer en phase liquide. Plus haut dans le BF, les cyanures alcalins réagissent avec le CO2 (dioxyde de carbone) pour former des carbonates plus stables à des températures inférieures à 1 100 deg C selon l'équation 2KCN (l) + 4CO2 (g) =K2CO3 + N2 (g) + 5CO ( g). Les carbonates suivent le gaz supérieur sous forme de gaz ou se déposent sur la charge lorsqu'ils commencent à se condenser en dessous de 900 deg C.
Par rapport aux silicates alcalins, les cyanures alcalins sont instables, de sorte que tout SiO2 présent dans la partie foyer du BF peut réagir avec les cyanures alcalins pour former à nouveau des silicates alcalins. Le processus de réduction des silicates alcalins en vapeur alcaline, qui monte dans le BF, part avec le gaz de tête ou réagit avec le CO2 pour former des carbonates, est connu sous le nom de cycle alcalin. Il existe des points de vue différents qui résument légèrement le processus en différant sur les réactions exactes qui se produisent. Il y a des doutes quant à la formation réelle de carbonates au sommet du BF puisque les carbonates ne sont pas trouvés lors de l'excavation des BF. Cependant, le processus principal de formation des cyanures alcalins et de circulation de l'alcali dans le BF est convenu dans toutes les vues.
La figure 3 montre la circulation des alcalis dans le BF. Le matériau chargé descend dans la zone à haute température avant que les silicates alcalins ne se décomposent en vapeurs alcalines ou ne soient absorbés par la phase de laitier primaire sous forme de K2O ou de Na2O. Le cycle indique également à peu près quand la vapeur alcaline réagit avec les silicates pour former à nouveau des silicates. La distribution des vapeurs alcalines à travers le BF dépend des voies d'écoulement du gaz et de l'étendue de l'écoulement central du gaz. Les flux de gaz ont un effet important sur la façon dont la chaleur est distribuée dans un BF. Un flux plus central signifie plus de fusion au milieu et moins à la périphérie du BF.
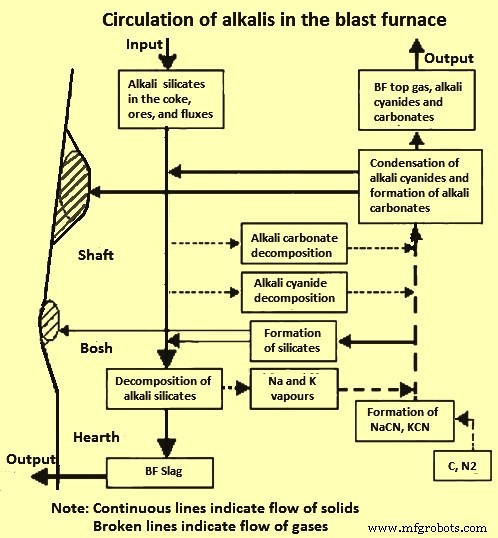
Fig 3 Circulation des alcalins dans le BF
Formation d'ammoniac et de cyanure d'hydrogène dans le BF
On pense que l'ammoniac (NH3) se forme dans le BF. Les réactions de base derrière la formation de NH3 et de cyanure d'hydrogène (HCN) dans le BF sont 2KCN + 3H2O =K2CO3 + 2NH3 + C, et NH3 + CO =HCN + H2O. Le rapport entre ces réactions dépend de plusieurs paramètres tels que (i) la quantité d'humidité disponible, (ii) la quantité de KCN disponible dans le haut, et (ii) la température pendant les réactions. Le seuil de température pour le NH3 est d'environ 600 degrés C et la formation de NH3 diminue continuellement de façon exponentielle jusqu'à 500 degrés C et ensuite elle n'est pas détectée. En outre, le NH3 formé est oxydé par Fe2O3 ou CO2 et la quantité de NH3 formé diminue. L'oxydation de NH3 par Fe2O3 ou MnO2 dépend de la température. À basse température, MnO2 est un oxydant plus fort et à haute température, Fe2O3 est l'oxydant le plus fort.
Comme HCN et NH3 peuvent être trouvés dans le gaz de tête, la cinétique d'oxydation du NH3 n'est pas assez rapide pour l'éliminer complètement. L'eau plus élevée trouvée dans le gaz de tête signifie qu'il y a plus de formation de NH3 qui peut avoir lieu selon la réaction ci-dessus. La formation de NH3 dans le BF est complexe car plusieurs paramètres, comme indiqué ci-dessous, affectent sa formation.
Température maximale du gaz – La température du gaz de gueulard dépend du rapport entre les réactions endothermiques / exothermiques dans le BF. La température affecte la teneur en humidité. Une température plus basse peut également entraîner une solubilité accrue du NH3 dans l'eau et le HCN est miscible dans l'eau, de sorte que la présence d'eau peut diminuer sa présence dans le gaz de tête.
Température de la flamme – La température de la flamme a un effet mineur sur la quantité de vapeur alcaline produite et sur la charge alcaline totale. Une température élevée est nécessaire pour réduire les silicates alcalins en gaz alcalin qui démarre la circulation alcaline. Une température de flamme abaissée conduit donc à plus d'alcali quittant le BF à travers le laitier.
Basicité – Une basicité plus faible entraîne une absorption plus élevée d'alcali dans le laitier, il y a donc moins d'alcali circulant dans le BF et moins de NH3 est produit.
Teneur en humidité - Moins d'humidité introduite avec la charge ou par d'autres moyens dans le BF donne moins d'eau pour que la réaction de formation de NH3 se produise.
Effet de l'alcali et élimination
La concentration d'alcali dans la matière première a augmenté ces dernières années en raison de la disponibilité réduite de charbon à coke de haute qualité. L'alcali est préjudiciable à l'opération BF car il provoque une réactivité accrue du coke en raison de l'effet catalytique sur la réaction de perte de solution (réaction de Boudouard).
L'un des principaux effets négatifs de l'alcali est qu'il catalyse la réaction réversible de Boudouard, abaissant la température de la réaction de 900 ° C à 950 ° C jusqu'à environ 750 ° C à 850 ° C et augmentant la réactivité du coke en fonction de la qualité du coke. Il affecte également négativement la structure du coke. Le seuil abaissé pour la réaction de Boudouard signifie que plus de C est consommé dans le BF dans une réaction fortement endothermique. Ainsi, une augmentation de l'ajout de coke est nécessaire dans le BF pour maintenir un fonctionnement stable avec 2 kg à 10 kg de coke par kg d'alcali ou avec 6 kg à 11 kg de coke selon les sources utilisées.
L'alcali qui est entré dans la structure du coke diminue la résistance du coke dans la partie inférieure du BF en raison de la réactivité accrue du coke et donc de la dégradation accrue. La vitesse de réaction apparente du coke au niveau de la tuyère s'est avérée être dix fois supérieure à la vitesse de réaction du coke d'alimentation, qui est liée à la quantité totale de présence de K. K est connu pour augmenter la réactivité du coke avec le CO2 et peut entraîner en rupture de coke à cause du gonflement des grains de coke par insertion de K. Une réactivité accrue peut être avantageuse puisqu'elle permet de réduire la température de fonctionnement BF, la température dans la zone de réserve thermique et donc d'abaisser la température de réduction de l'oxyde de fer. Cependant, le but du coke est également d'agir comme support de charge dans le four, et par conséquent, la fracture du coke doit être minimisée.
Des études sur la pénétration de la vapeur de K dans le coke ont confirmé que la structure des minéraux du coke peut être brisée en raison de l'expansion volumique des minéraux alcalinisés, en particulier la kalsilite. La surface entre les minéraux et la matrice C augmente du fait de la casse des minéraux dans le coke. Ceci facilite l'interaction de la matière minérale avec les gaz C et BF accélérant la gazéification du coke. Une expansion du coke peut également se produire lorsque des vapeurs alcalines pénètrent dans les couches cristallines du coke pour former des composés intercouches. La résistance du coke et le support de la charge pendant l'opération BF sont essentiels car un effondrement de la charge réduit la perméabilité aux gaz et aux liquides, ce qui réduit l'efficacité à la fois en ce qui concerne la production de HM et l'augmentation des émissions de CO2.
De petites particules de coke de taille différente diminuent les vides dans le lit de coke dans la zone humide et la surface de coke augmente. La rupture du coke favorise également l'inondation, l'étouffement du foyer et l'augmentation de la combustion des tuyères et de l'entaille de laitier, qui limitent tous la puissance du four. La tendance du gaz ascendant à être transporté près des parois augmente lorsque la perméabilité est abaissée, ce qui diminue l'utilisation du gaz et donc augmente le taux de coke.
Un autre effet de l'alcali est le risque accru de formation d'échafaudage dans le puits, car l'alcali se condense sur le revêtement et peut y lier le matériau fin. Les échafaudages sont une accumulation de matériau solide sur la paroi du four et se projettent vers le centre du four. Les échafaudages peuvent se produire à n'importe quel endroit du milieu à la partie supérieure du puits. L'effet de la formation de l'échafaudage est que la descente de la charge est ralentie ou interrompue et, dans les cas extrêmes, entraîne une suspension, un glissement et une charge incontrôlée. Les échafaudages réduisent également le volume de travail du BF. La vitesse du gaz est augmentée dans les parties non affectées de l'arbre, ce qui entraîne une augmentation de la température du gaz supérieur et une diminution de l'utilisation du CO . Lorsque les échafaudages se détachent de la paroi du four, il en résulte souvent un foyer refroidi. Les échafaudages peuvent être retirés en augmentant temporairement la température du four ou lorsqu'un flux de gaz à haute température atteint la zone.
Le matériau de charge peut également être collé par des cyanures et des carbonates liquides condensés, ce qui réduit la perméabilité du lit. De plus, les alcalis peuvent attaquer le matériau réfractaire, en particulier les réfractaires à base de C normalement utilisés dans la partie inférieure du four. Les composés alcalins pénètrent dans les blocs C qui sont consommés en formant une vapeur alcaline. Il en résulte une durée de vie plus courte du revêtement réfractaire et un besoin de regarnissage plus fréquent.
L'élimination de l'alcali se fait principalement avec le laitier et est mieux réalisée à des valeurs de basicité inférieures. Plus de 90 % de l'alcali éliminé est éliminé par le laitier. Ici, la basicité est considérée comme CaO/SiO2. Les résultats de plusieurs études ont montré que la basicité inférieure du laitier augmente la quantité d'alcali dans le laitier. Cependant, le problème avec une basicité trop faible est qu'un niveau plus élevé de soufre (S) reste dans le HM, car le S peut être contrebalancé par le CaO présent dans le laitier BF et le CaO est inférieur lorsque la basicité est inférieure. La limite inférieure de la basicité pour maintenir la qualité de la HM sous contrôle diffère d'une usine à l'autre. La limite dépend des paramètres BF et de la qualité de la matière première utilisée. Une valeur de basicité juste au-dessus ou autour de 1 peut être considérée comme la limite si l'alcali doit être éliminé et la qualité HM doit être maintenue.
Pour empêcher la gazéification des silicates alcalins, la pression partielle de CO doit être maintenue élevée. La température élevée de la réaction à 1550 degrés C signifie qu'une température de flamme inférieure peut également être utilisée pour ralentir la réduction et la gazéification et ainsi réduire la circulation alcaline. L'élimination de l'alcali nécessite une recirculation réduite des matériaux contenant de l'alcali vers le BF, car l'alcali est autrement simplement réintroduit dans le BF.
L'abaissement de l'effet catalyseur de l'alcali sur la gazéification du coke peut être réalisé par des ajouts de cendres de coke qui peuvent lier l'alcali existant sous des formes plus stables. Il a déjà été essayé avec certains ajouts minéraux. Au fur et à mesure que l'alcali se diffuse à travers le coke, un revêtement de l'ajout de minéraux peut stabiliser l'alcali à la surface du coke en l'empêchant de dégrader les parties internes du coke.
Contrôle de la charge alcaline
Pour contrôler la charge alcaline dans le BF, l'entrée d'alcali doit être maintenue aussi faible que possible. S'il y a une variation dans le matériau entrant, le mélange de minerai doit être bien mélangé pour minimiser le risque de sections alcalines élevées dans le BF. Une autre précaution est d'éviter la recirculation des poussières de combustion avec des niveaux élevés d'alcali. Un moyen de minimiser le risque de formation d'échafaudage consiste à augmenter la résistance de la charge ferreuse et du coke pour éviter la formation de fines.
Le BF peut fonctionner avec un débit de gaz central. De ce fait, la température du gaz de tête au centre est augmentée à un niveau tel qu'une partie de l'alcali quitte le four sous forme de vapeur avec le gaz de tête. Cependant, des températures de gaz supérieures plus élevées entraînent une augmentation des pertes de chaleur.
L'alcali recirculé peut être diminué et à la place quitter le BF via le laitier en faisant fonctionner le BF avec un laitier acide. Plus la basicité du laitier est faible, plus le K et le Na basiques sont facilement absorbés dans le laitier car la chaux (CaO) et la magnésie (MgO) occupent les mêmes sites dans le réseau de silice que les oxydes alcalins. Une basicité réduite peut être obtenue en diminuant la basicité dans la charge ferreuse et les ajouts de fondant. Cependant, une basicité plus faible entraîne également une augmentation de la teneur en S (soufre) dans le HM car le S se lie au Ca dans le laitier.
Une autre possibilité de diminuer la charge alcaline consiste à augmenter le volume de laitier, ce qui diminue l'activité des oxydes alcalins dans le laitier et donc augmente l'absorption d'alcali et la sortie à travers le laitier, mais un volume de laitier accru augmente également le taux de coke.
Une température plus basse dans le BF entraîne une diminution de la réduction et de la vaporisation de l'alcali. Le fonctionnement du BF avec une température de flamme plus basse entraîne une diminution de la charge alcaline, mais également une diminution de la productivité et un taux de coke plus élevé. La charge alcaline peut également être diminuée en faisant fonctionner le BF avec une pression partielle élevée de CO car il s'oppose à la réaction de gazéification alcaline. Ceci peut être réalisé par l'enrichissement en O2 du souffle ou par une haute pression supérieure.
Processus de fabrication
- Système d'automatisation, de mesure et de contrôle du processus de haut fourneau
- Utilisation de coke de noix dans un haut fourneau
- Processus de fabrication du fer HIsmelt
- Processus HIsarna pour la fabrication du fer
- Irrégularités du haut fourneau pendant le fonctionnement
- Système de refroidissement de haut fourneau
- Chimie de la fabrication du fer par procédé de haut fourneau
- Revêtement réfractaire de haut fourneau
- Fabrication du fer par haut fourneau et émissions d'oxyde de carbone



