Membrane de nanotubes ultralongues de titanate de sodium autonome avec propriétés de séparation huile-eau, autonettoyantes et photocatalyse
Résumé
Dans ce travail, une membrane de nanotube ultralongue en titanate de sodium autonome pour la purification multifonctionnelle de l'eau a été préparée. Pour obtenir cette membrane autoportante avec une bonne ténacité, des nanotubes ultralongs de titanate de sodium unidimensionnels (1D) d'un diamètre d'environ 48 nm et d'une longueur de centaines de micromètres ont été préparés à partir de TiO2 nanoparticules par une méthode hydrothermale d'agitation, qui peuvent être facilement assemblées en membranes 2D par filtration sous vide facile. Après avoir été modifiée avec du méthyltriméthoxysilane (MTMS), la membrane autoportante à surface hydrophobe possède à la fois des fonctions de séparation huile-eau, d'autonettoyage et photocatalytique, ce qui est favorable à la récupération de la membrane et à la décontamination de divers polluants, notamment les huiles, la poussière , et les colorants organiques de l'eau. De plus, cette membrane présente également une excellente résistance aux sels alcalins, acides et corrosifs. Cette membrane autonome en titanate de sodium multifonction a des applications potentielles dans la purification efficace des eaux usées et l'assainissement de l'environnement.
Introduction
L'eau huileuse, provenant des eaux usées industrielles et des fréquents accidents de marée noire, est nocive pour l'environnement, les animaux, les plantes et même les humains et a suscité une inquiétude généralisée dans le monde entier. L'élimination de l'huile intraitable de l'eau est un travail difficile [1, 2]. À l'heure actuelle, de nombreuses méthodes de traitement des eaux usées huileuses ont été développées. La technologie de séparation par membrane a beaucoup attiré l'attention pour ses avantages de faible consommation d'énergie, de flexibilité, de respect de l'environnement et d'efficacité de séparation élevée en une seule étape [3, 4]. De nombreuses recherches ont été menées sur l'amélioration de la durabilité et de l'efficacité de la technologie de séparation membranaire. Szekely et al. a noté qu'une grande quantité d'eaux usées est générée pendant le processus de fabrication de la membrane polymère, ce qui rend la technologie de séparation par membrane moins écologique qu'on le sait. Pour rendre la technologie membranaire plus verte et plus durable, ils ont proposé un processus de traitement des eaux usées en continu pour éliminer plus de 99% des impuretés organiques par les adsorbants et réutiliser ces eaux purifiées pour la fabrication de la membrane sans effets néfastes sur les performances de la membrane finale [5 ]. Ils ont également révélé les effets directs et indirects de la polarité du solvant de traitement sur les performances de la membrane grâce à des études systématiques, qui ont été appliquées avec succès pour améliorer l'efficacité de la purification pharmaceutique [6]. Plus récemment, de nombreuses techniques de nano-ingénierie ont été développées pour la fabrication précise de membranes poreuses afin de répondre à la séparation spécifique requise. Yang et al. préparé une cristallisation sans solvant de membranes MOF (ZIF-8) par un processus de dépôt couche par couche. La membrane ZIF-8 sans défaut présentait à la fois un H2 plus élevé perméabilité et H2 plus élevé /CO2 sélectivité simultanément que les membranes ZIF-8 jamais rapportées [7]. S'inspirant des moules marines, Szekely et al. pour la première fois fabriqué une membrane nanotechnologique formée par polymérisation in situ de dopamine dans un support PBI pour la séparation de solvants aprotiques polaires. Le revêtement de PDA a éliminé la réticulation covalente du squelette PBI et a atteint la valeur de perméance la plus élevée du DMF [8]. La fabrication de membranes avec des matériaux fonctionnels confère à la membrane une multifonctionnalité en plus de la séparation. Xu et al. ont signalé une membrane composite composée de LiNbO3 couche de revêtement et support en poly(éther sulfone) (PES). La présence de LiNbO3 doté de la fonction de dénitrification photocatalytique membranaire [9]. Les membranes multifonctions sont aspirées pour éliminer efficacement l'huile de diverses eaux usées [10,11,12].
Récemment, de plus en plus de matériaux inorganiques 1D ont été appliqués pour obtenir une membrane autoportante en raison de leur grande surface spécifique, de leur faible densité, de leur conductivité thermique et de leur sensibilité chimique élevées, ainsi que des propriétés accordables des métaux et des semi-conducteurs [13,14,15, 16]. Les matériaux titanate 1D ont non seulement une structure en couches unique, de bonnes propriétés électrochimiques et optiques, mais possèdent également d'excellentes propriétés mécaniques. Ces caractéristiques permettent d'être utilisées dans les domaines de la photocatalyse [17], de l'adsorption [18, 19], de la batterie sodium-ion [20] et du stockage d'énergie [21]. Récemment, Wang et al. ont préparé une membrane pour la séparation d'émulsion huile/eau à haute efficacité en utilisant des nanofibres de titanate de sodium, qui ont été supportées sur une couche de microfibres de cellulose [22]. Dans ce travail, une membrane autoportante a été préparée en utilisant uniquement des nanotubes ultralongs de titanate de sodium d'une longueur de centaines de micromètres. Cette membrane autoportante présentait une excellente flexibilité. Après avoir été modifiée avec du méthyltriméthoxysilane (MTMS), la membrane hydrophobe autoportante possédait des fonctions de séparation huile-eau, d'autonettoyage et de photocatalyse, qui sont favorables au recyclage des membranes de séparation.
Méthodes
Matériaux
TiO2 la poudre (P25) a été achetée auprès de Deguassa Co. Ltd, Allemagne. Méthyltriméthoxysilane (MTMS, ≥ 98%) et éthanol (CH3 CH2 OH, 95 %) ont été achetés auprès d'Aladdin Reagent Company, Chine. L'acide chlorhydrique (HCl, 37%), l'hydroxyde de sodium (NaOH, 96%), et l'acide oxalique (≥ 99,5%) ont été obtenus auprès de Sinopharm Chemical Reagent Co. Ltd. Tous les réactifs chimiques ont été utilisés dans le processus expérimental sans autre purification. . L'eau déminéralisée (DI) a été utilisée tout au long de cette expérience.
Synthèse de Na2 Ti3 O7 Nanotubes ultralongs
La synthèse de Na2 Ti3 O7 nanotubes ultralongs était conforme à la procédure de la littérature [22, 23]. Typiquement, 0,2 g de poudre P25 a été ajouté à 30 mL de solution aqueuse de NaOH 10 M sous agitation continue pendant 5 min. Ensuite, la suspension a été transférée dans un autoclave en acier inoxydable revêtu de téflon de 50 mL avec un agitateur magnétique. L'autoclave a été placé dans un bain d'huile de silicone et la température de réaction a été fixée à 130 °C pendant 24 h. La vitesse d'agitation est de 300 rpm. Après la réaction, l'autoclave a été refroidi naturellement à température ambiante. Le précipité a été récupéré et lavé avec de l'eau distillée plusieurs fois pour éliminer l'excès de NaOH. Le produit obtenu a été encore nettoyé en utilisant une solution de HCl 0,1 M trois fois pour produire du Na2 de haute pureté. Ti3 O7 nanotubes ultralongs et lavés à nouveau avec de l'eau distillée plusieurs fois jusqu'à pH =7.
Synthèse du Na libre2 Ti3 O7 Membrane poreuse et modification de surface
Na2 autonome Ti3 O7 la membrane poreuse a été préparée par simple filtration sous vide sans aucun autre additif. Typiquement, Na2 Ti3 O7 des nanotubes ultralongs se dispersant dans de l'éthanol à différentes concentrations ont été versés dans le flacon filtre et filtrés sous vide pendant 10 min. La membrane obtenue a été séchée à température ambiante. En utilisant différentes quantités de Na2 Ti3 O7 des nanotubes ultralongs, des membranes poreuses avec des poids de 30 mg, 45 mg, 60 mg et 75 mg ont été obtenus, qui sont définis de manière correspondante comme F-30, F-45, F-60 et F-75.
Les membranes obtenues ont été modifiées par trempage dans une solution sol-gel MTMS pendant 30 s et séchées à température ambiante pendant une nuit.
Caractérisation
La morphologie et la taille des échantillons obtenus ont été examinées sur un microscope électronique à transmission Tecnai G2 F30 S-Twin (TEM, FEI, USA) fonctionnant à 200 kV. Les morphologies des membranes ont été caractérisées en utilisant un microscope électronique à balayage à émission de champ (MEB, Hitachi S4800). Les diagrammes de diffraction des rayons X sur poudre (XRD) ont été enregistrés sur un diffractomètre à rayons X sur poudre Bruker D8 Advance à une vitesse de balayage de 4° min -1 , avec rayonnement Cu-Kα (λ =1,5406 Å) dans la plage de 10 à 60°. L'angle de contact (CA) des membranes a été mesuré sur un appareil Krüss DSA 30 (Krüss Company, Ltd., Allemagne).
Résultats et discussion
Na2 Ti3 O7 Nanotubes ultralongs et membrane autoportante
La figure 1a est les modèles XRD du produit synthétisé par agitation méthode hydrothermale. On peut voir qu'il existe des pics caractéristiques à 11,1°, 18,8°, 25,4°, 30,3°, 34,8°, 36,7°, 39,2°, 44,2°, 48,9°, 50,2° et 53,1°, qui peuvent être indexés comme ( 100), (200), (011), (300), (− 303), (− 204), (− 401), (− 214), (020), (120) et (220) plans de Na
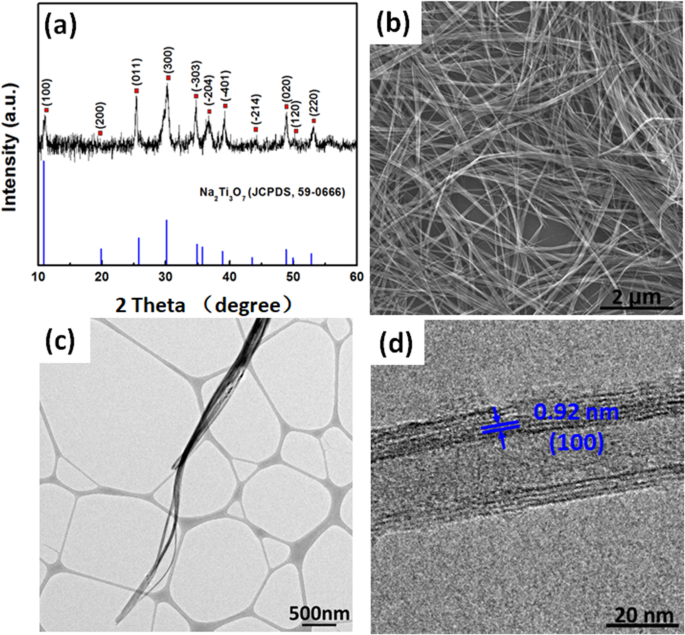
un modèle XRD, b SEM, c TEM, et d HRTEM de Na2 Ti3 O7 nanotubes ultralongs
Dans cette étude, le Na2 Ti3 O7 des nanotubes ultralongs ont été synthétisés par méthode hydrothermale sous agitation. Sun et al. [29] ont systématiquement étudié le mécanisme de formation de Na2 Ti3 O7 nanotubes en procédé hydrothermal sans agitation. Généralement, la longueur de Na2 Ti3 O7 nanotubes synthétisés dans le procédé hydrothermal sans agitation est d'environ 500 nm. Ces nanotubes courts s'agrègent facilement, ce qui n'est pas propice à la formation de membranes (Fig. 2a). Il a été rapporté que la longueur des nanotubes de titanate peut être contrôlée par une vitesse de rotation lors de la réaction hydrothermale [23, 30]. Nous avons trouvé que le Na2 allongé Ti3 O7 les nanotubes sont faciles à poser à plat pour former un film (Fig. 2b). Mais si vous utilisez ces Na2 Ti3 O7 nanotubes pour former une membrane autoportante, des supports polymères tels que la polyéthylèneimine (PEI) doivent être utilisés [31]. Pour obtenir une membrane autoportante sans supports polymères, la quantité de Na2 Ti3 O7 nanotubes ultralongs a été étudié. Les images SEM et MET de la figure 3 indiquent que les membranes sont constituées de nanotubes ultralongs orientés de manière aléatoire et avec l'augmentation du poids de la membrane, Na2 Ti3 O7 les nanotubes ultralongs sont plus denses. La figure 3a–f indique que lorsque la quantité de Na2 Ti3 O7 nanotubes ultralongs est de petite taille (30 mg et 45 mg), l'assemblage de Na2 Ti3 O7 nanotubes ultralongs est lâche et l'adhérence entre les nanotubes est insuffisante. Ainsi, bien que ces membranes aient une certaine ténacité mais elles ont tendance à se diviser en deux lorsqu'elles sont pliées (encadrés fig. 3c et f). Mais lorsque le poids de la membrane atteint jusqu'à 75 mg, cette teneur élevée en nanotubes s'entrelacent fortement, ce qui entraîne moins de liberté d'espacement entre les nanotubes et une irrégularité de la membrane (Fig. 3j–l). Par conséquent, la membrane F-75 avec moins de ténacité se brise facilement en petits morceaux (encadré sur la figure 3l). La membrane F-60 affiche une excellente ténacité en raison de sa teneur modérée en nanotubes, de la liberté relative entre eux et d'une adhérence suffisante (Fig. 3g-i). Ainsi, le F-60 a été utilisé pour d'autres études. Fichier supplémentaire 1 :la figure S2a–d indique que les épaisseurs correspondantes de F-30, F-45, F-60 et F-75 sont respectivement de 44 m, 88 μm, 116 μm et 210 m (tableau 1, fig. 4). Les épaisseurs de ces membranes ont une relation linéaire avec le poids de Na2 Ti3 O7 nanotubes ultralongs (Fig. 4). Ces résultats suggèrent que l'épaisseur et la ténacité des membranes peuvent être ajustées en contrôlant la quantité de Na2 Ti3 O7 nanotubes ultralongs.

Images SEM de Na2 Ti3 O7 nanotubes synthétisés par méthode hydrothermale à 0 rpm (a ) et 300 tr/min (b )

Images SEM d'une coupe transversale de F-30 (a , b ), F-45 (d , e ), F-60 (g , h ), et F-75 (j , k ). Images TEM de la vue de dessus du F-30 (c ), F-45 (f ), F-60 (i ), et F-75 (l ). Les encarts sont les images optiques des membranes correspondantes
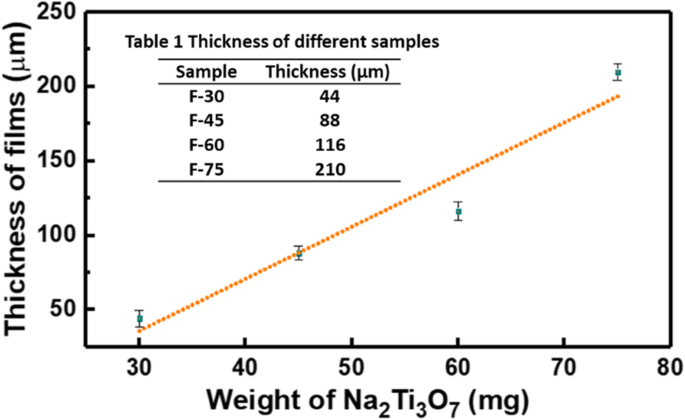
Le tracé de l'épaisseur en fonction du poids de la membrane
Mouillabilité de la membrane F-60
La figure 5a indique que le tétrachlorure de carbone (côté gauche, coloré au rouge de méthyle) et l'eau (côté droit, coloré au bleu de méthylène) peuvent se répandre et s'imprégner de la membrane F-60 obtenue. La tension superficielle du tétrachlorure de carbone et de l'eau est de 26,1 mN m −1 et 72,8 mN m −1 [32], respectivement. Afin d'obtenir une membrane hydrophobe pour séparer le mélange huile-eau, la tension superficielle de la membrane F-60 doit être inférieure à ¼ d'eau pure (environ 18 mN m −1 ) [33]. Ensuite, la membrane F-60 obtenue doit être modifiée. Dans notre étude, la membrane F-60 autoportante est facilement modifiée par trempage dans le sol MTMS en raison de sa faible énergie de surface et de sa structure micro-nano rugueuse [34,35,36]. Le temps de vieillissement du sol MTMS a un effet sur l'angle de contact de la membrane F-60 modifiée. La figure 5b montre qu'avec l'augmentation du temps de vieillissement, l'angle de contact de la membrane F-60 modifiée augmente. Mais lorsque le temps de vieillissement est de 14 h, l'angle de contact diminue. Car avec l'augmentation du temps de vieillissement, un gel MTMS à faible fluidité se forme, ce qui conduit à la surface inégale de la membrane F-60 (Fichier supplémentaire 1 :Figure S3) et à la diminution de l'angle de contact [37]. Les durées de vieillissement comprises entre 10 et 12 h sont adaptées à l'obtention d'une membrane hydrophobe.
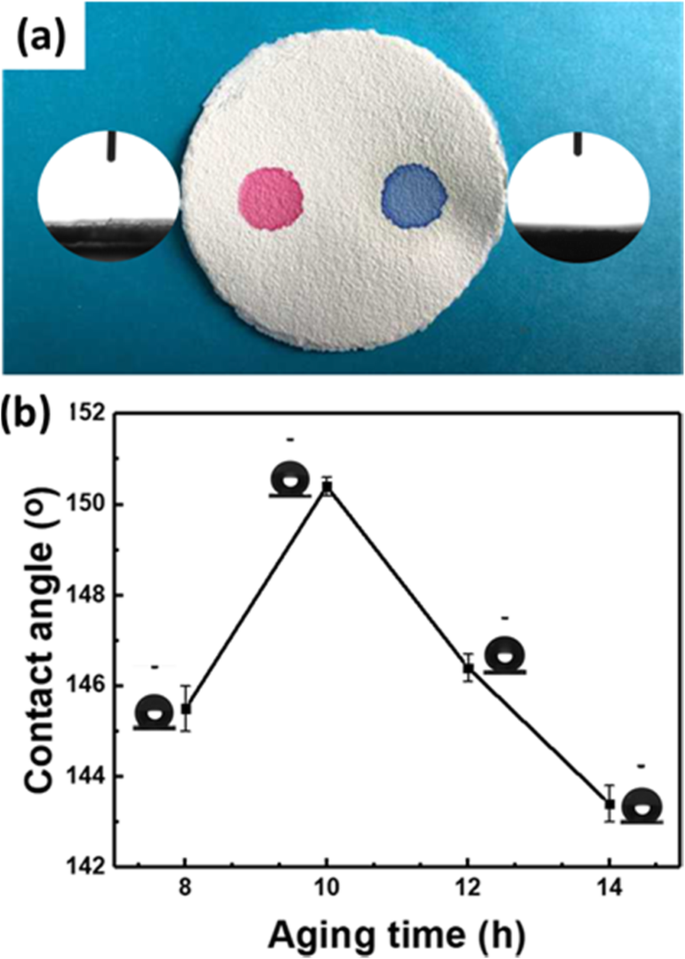
un Photo optique de la membrane F-60 larguée avec du tétrachlorure de carbone (côté gauche, coloré au rouge de méthyle) et de l'eau (côté droit, coloré au bleu de méthylène). b Effet du temps de vieillissement du MTMS sur l'angle de contact de la membrane F-60 modifiée
Multifonction de la membrane F-60 modifiée
La séparation huile/eau par gravité a été réalisée par de nombreuses membranes hydrophobes ou hydrophiles contenant des composants unidimensionnels [37,38,39,40]. Par conséquent, la membrane F-60 modifiée avec hydrophobie a d'abord été utilisée pour la séparation de mélanges huile/eau non miscibles. La phase huileuse est du tétrachlorure de carbone et la phase aqueuse est de l'eau pure, qui sont colorées respectivement par le rouge de méthyle et le bleu de méthylène. Le processus de séparation huile/eau est réalisé dans un simple dispositif de séparation huile/eau comme illustré sur la figure 6a. La membrane F-60 modifiée a été fixée entre deux tubes de verre. Lorsque le mélange huile/eau est versé sur la membrane, du tétrachlorure de carbone a pénétré la membrane tandis que l'eau est conservée dans la partie supérieure. Dix millilitres de tétrachlorure de carbone peuvent traverser la membrane en 240 s. Le flux membranaire calculé est d'environ 849 L m −2 h −1 et l'efficacité de séparation des mélanges huile/eau non miscibles par la membrane F-60 modifiée atteint jusqu'à 99,7 %. Généralement, la phase aqueuse n'est pas neutre notamment pour les eaux usées industrielles huileuses. La figure 6b indique que la membrane F-60 modifiée conserve une efficacité de séparation élevée et que même la phase aqueuse contient de l'acide corrosif, des alcalis ou du sel.

un Dispositif et procédé de séparation huile/eau, b efficacités de séparation pour les mélanges huile/eau non miscibles contenant différentes phases aqueuses par la membrane F-60 modifiée
À l'exception des différents contenus chimiques dans l'eau, il y a toujours de la poussière ou des solides dans les eaux usées industrielles. La figure 7 indique que la poussière restant sur la membrane après la séparation huile/eau peut être facilement éliminée par les gouttelettes d'eau en raison des surfaces hydrophobes de la membrane F-60 modifiée.
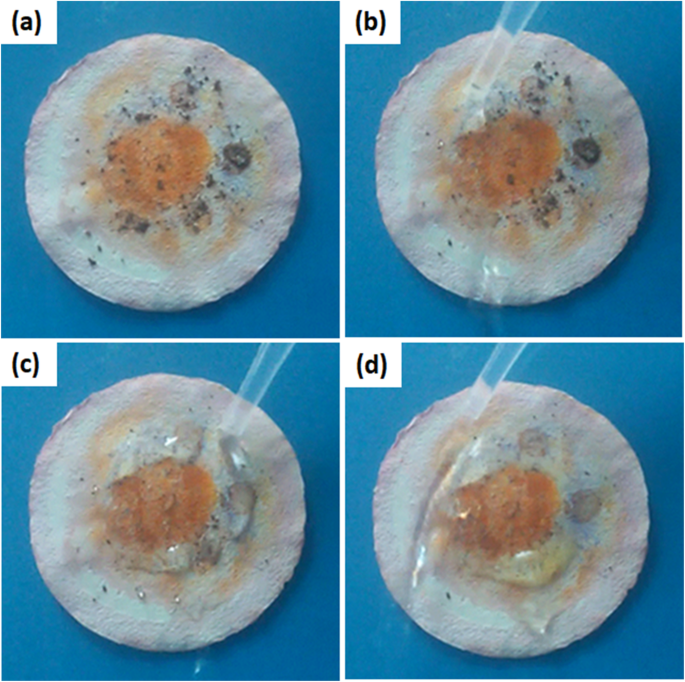
Images numériques du processus d'auto-nettoyage
Les propriétés des matériaux contenus dans la membrane confèrent généralement à la membrane des fonctions spéciales [41,42,43]. La membrane préparée à l'aide d'oxyde de cardanol-graphene réticulé contient non seulement une fonction de séparation huile/eau mais également une activité antibactérienne marquée qui provient du cardanol [44]. Ici, les surfaces spécifiques et le diamètre moyen des pores de la membrane F-60 sont de 240,4 m 2 g −1 et 14,5 nm, respectivement (Fichier supplémentaire 1 :Figure S4). Cette structure poreuse et la surface spécifique élevée de la membrane peuvent avoir une capacité d'adsorption élevée. La figure 7 indique qu'après le processus de séparation huile/eau, le colorant de rouge de méthyle dans la phase huileuse peut être partiellement adsorbé sur la membrane. Le processus d'autonettoyage ne peut pas nettoyer le colorant adsorbé. Profitant de la propriété photocatalytique du titanate de sodium [45,46,47], le colorant adsorbé devrait être éliminé par réaction de photocatalyse. La figure 8a-d montre qu'après une irradiation de 30 min avec de la lumière UV, presque tout le colorant adsorbé est éliminé. Afin de démontrer l'élimination du rouge de méthyle sur la membrane en raison de la réaction de photocatalyse mais pas la décomposition du colorant sous irradiation UV, une solution de rouge de méthyle sans photocatalyseur a été irradiée avec de la lumière UV. On peut voir sur la figure 8e que sans photocatalyseur, le rouge de méthyle ne peut pas être dégradé par la lumière UV, ce qui confirme la fonction photocatalytique de la membrane en titanate de sodium.
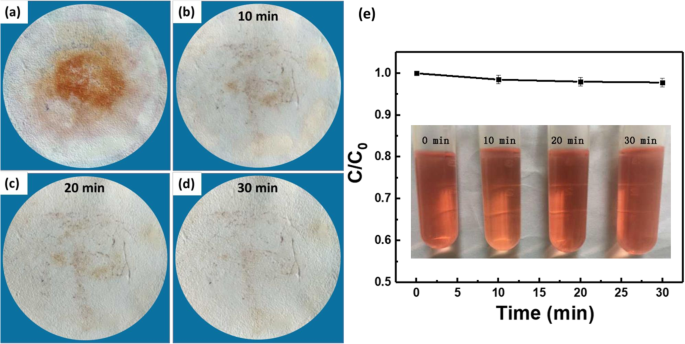
Image optique de la membrane après séparation huile/eau et autonettoyage (a ) et les images optiques de cette membrane irradiée sous lumière UV pendant 10 min (b ), 20 min (c ), et 30 min (d ). e Efficacité de dégradation d'une solution de rouge de méthyle sans photocatalyseur sous irradiation de lumière UV. L'encart est la photo optique d'une solution de rouge de méthyle irradiée à différents moments
La membrane F-60 modifiée par MTMS a une transmittance de la lumière [48], donc le Na2 Ti3 O7 le nanotube peut adsorber la lumière UV et générer des électrons et des trous. Mais la génération de radicaux hydroxyles (Fichier complémentaire 1 :Figure S5) et la dégradation des molécules organiques nécessitent le milieu de l'eau. Pour étudier le mécanisme de dégradation photocatalytique de la molécule organique par une membrane F-60 modifiée par MTMS avec une surface superhydrophobe, une membrane F-60 modifiée par MTMS pure a été irradiée sous lumière UV pendant 30 min. On constate qu'après l'irradiation de lumière UV, l'angle de contact de la membrane diminue fortement de 150,4° à moins de 90° (Fig. 9a). Cela signifie que la propriété de surface de la membrane F-60 modifiée par MTMS change. Le résultat FTIR confirme qu'après irradiation par la lumière UV, les liaisons Si–O–Si dans le MTMS diminuent, indiquant que ces liaisons sont rompues par la lumière UV (Fig. 9b) [49,50,52]. Le Si-O-Si cassé aidera le contact de l'eau et de la lumière avec Na2 Ti3 O7 nanotube et améliorant les performances photocatalytiques. De plus, sous l'action combinée de la lumière UV et de l'oxygène, le MTMS est oxydé et davantage de liaisons Si-OH sont observées sur la figure 9b ; la réaction est montrée dans l'équation. (1) :
$$ \mathrm{Si}-{\mathrm{CH}}_3+{2\mathrm{O}}_2\underrightarrow{\mathrm{UV}}\ \mathrm{Si}-\mathrm{OH}+{\mathrm {CO}}_2+{\mathrm{H}}_2\mathrm{O} $$ (1)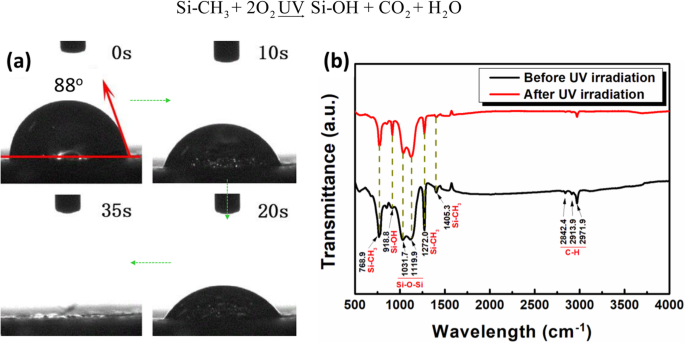
un Angle de contact de la membrane après irradiation aux rayons UV et b Spectres FTIR de membrane pure
La rupture Si–O–Si et l'oxydation de Si–CH3 par la lumière UV rendent possible la génération de radicaux hydroxyles et la dégradation des molécules organiques. Lorsque cette membrane, après irradiation sous lumière UV, a été replongée dans le sol MTMS pendant un temps très court, l'angle de contact de la membrane peut remonter jusqu'à 140° (Fichier complémentaire 1 :Figure S6). La membrane de récupération peut être réutilisée pour la séparation du mélange huile/eau non miscible tout en préservant les fonctions d'autonettoyage et de photocatalyse. Actuellement, la membrane ne peut être recyclée que trois fois car l'augmentation continue de l'épaisseur du MTMS entraîne une diminution spectaculaire de la porosité de la membrane (Fichier supplémentaire 1 :Figure S7). Des études sont toujours en cours pour améliorer encore le taux de récupération de la membrane.
Les résultats ci-dessus indiquent que la membrane en titanate de sodium préserve la multifonctionnalité de la séparation huile/eau, de l'autonettoyage et de la photocatalyse simultanément. Les matériaux inorganiques confèrent aux membranes multifonctionnelles, qui sont nécessaires pour le traitement des eaux usées industrielles (tableau 2).
Conclusions
En résumé, nous avons préparé avec succès une membrane autoportante multifonctionnelle avec Na2 Ti3 O7 nanotubes ultralongs. Le diamètre et la longueur de Na2 Ti3 O7 les nanotubes ultralongs mesurent respectivement environ 48 nm et des centaines de micromètres. Le Na2 allongé Ti3 O7 les nanotubes ultralongs sont faciles à poser à plat pour former une membrane. L'angle de contact de la membrane peut atteindre jusqu'à 150,4° après modification par MTMS. La membrane autonome modifiée par MTMS présente un flux membranaire élevé de 849 L m −2 h −1 et une efficacité de séparation de 99,7 % pour les mélanges huile/eau non miscibles, même dans des conditions fortement alcalines, acides ou salines corrosives. De plus, la poussière résiduelle peut être éliminée par fonction autonettoyante et les colorants adsorbés sur la membrane peuvent être dégradés en 30 min par fonction photocatalytique de la membrane. La membrane autonome en titanate de sodium avec une variété de fonctionnalités de séparation huile/eau, d'autonettoyage et de photocatalyse promettra de larges applications dans l'assainissement de l'environnement et la purification des eaux usées.
Disponibilité des données et des matériaux
Les ensembles de données utilisés et/ou analysés au cours de la présente étude sont disponibles auprès de l'auteur correspondant sur demande raisonnable.
Abréviations
- CA :
-
Angle de contact
- F-30, F-45, F-60 et F-75 :
-
Membranes avec des poids de 30 mg, 45 mg, 60 mg et 75 mg, respectivement
- HRTEM :
-
Microscope électronique à transmission haute résolution
- MTMS :
-
Méthyltriméthoxysilane
- P25 :
-
TiO2 poudre
- SEM :
-
Microscope électronique à balayage
- TEM :
-
Microscope électronique à transmission
- UV :
-
Ultraviolet
- XRD :
-
Diffraction des rayons X
Nanomatériaux
- Fil de nanotubes de carbone, muscle et feuilles transparentes
- Préparation et propriétés magnétiques des nanoparticules de spinelle FeMn2O4 dopées au cobalt
- Vers les nanofluides TiO2—Partie 1 :Préparation et propriétés
- Synthèse et propriétés électrochimiques des matériaux cathodiques LiNi0.5Mn1.5O4 avec dopage composite Cr3+ et F− pour batteries lithium-ion
- Morphologie, structure et propriétés optiques des films semi-conducteurs avec des nano-îlots GeSiSn et des couches tendues
- Amélioration de la conductivité des protons et réduction de la perméabilité du méthanol grâce à la bio-membrane d'oxyde de graphène sulfoné électrolytique d'alginate de sodium
- Élimination des antibiotiques de l'eau avec une membrane de nanofiltration 3D 100 % carbone
- Synthèse hydrothermale et propriétés de conversion ascendante d'environ 19 nm Sc2O3 :nanoparticules Er3+, Yb3+ avec étude détaillée du mécanisme de transfert d'énergie
- Synthèse et caractérisation de zéolites ZSM-5 hiérarchiques avec une mésoporosité exceptionnelle et d'excellentes propriétés catalytiques



