Propriétés matérielles et optiques des points quantiques de carbone fluorescent fabriqués à partir de jus de citron par réaction hydrothermale
Résumé
Les points quantiques de carbone fluorescents solubles dans l'eau (CQD) sont synthétisés en utilisant du jus de citron comme ressource de carbone via une simple réaction hydrothermale. Les CQD obtenus ont une taille moyenne de 3,1 nm. Ils révèlent une morphologie uniforme et bien cristalline et peuvent générer une émission lumineuse bleu-vert sous irradiation UV ou lumière bleue. Nous constatons que la fluorescence de ces CQD est principalement induite par la présence de groupes contenant de l'oxygène sur la surface et le bord des CQD. De plus, nous démontrons que les CQD tels que préparés peuvent être appliqués à l'imagerie des cellules végétales. Cette étude est liée à la fabrication, à l'investigation et à l'application de nanostructures de carbone nouvellement développées.
Contexte
Le point quantique de carbone (CQD) est une nouvelle classe de nanomatériaux à base de carbone normalement avec une taille spatiale inférieure à 20 nm, qui a été découverte par Xu et al. en 2004 [1]. Les nanoparticules de carbone fluorescentes ont été fabriquées par Sun et al. par ablation laser de poudre de graphite en 2006 [2] et ont été nommés « points quantiques de carbone (CQD) » depuis lors. Les CQD fluorescents ont un grand potentiel pour être appliqués dans la photocatalyse, les dispositifs optoélectroniques, la biomédecine, l'affichage à couche mince, l'éclairage sain et d'autres disciplines d'applications pratiques. Par rapport aux points quantiques traditionnels à base de semi-conducteurs, les CQD peuvent être obtenus par des techniques de fabrication à faible coût et présentent des caractéristiques fascinantes et importantes telles qu'une bonne biocompatibilité, une cible biologique précise, une faible toxicité et un effet de taille quantique plus important. Ces dernières années, les CQD fluorescents ont attiré une attention considérable [3, 4] en raison de leurs excellentes propriétés structurelles et optiques [5]. Ils ont été proposés comme matériaux de substitution pour les points quantiques semi-conducteurs conventionnels dans les domaines d'application tels que l'imagerie biologique, le marquage biologique, les LED à points quantiques (QLED), la protection de l'environnement et d'autres domaines connexes [6,7,8,9]. La recherche sur les CQD s'est rapidement développée en physique de la matière condensée, en science des matériaux, en électronique et en optoélectronique. Des études fondamentales et d'application connexes ont été largement entreprises dans le monde [3,4,5,6,7,8,9].
À l'heure actuelle, il existe diverses techniques [10, 11] pour synthétiser les CQD, telles que l'approche hydrothermale [11, 12], la méthode des micro-ondes [13], etc. Les CQD ont été synthétisés à partir de divers précurseurs du carbone tels que le glucose [14], l'acide citrique [15] et l'acide ascorbique [16]. Cependant, la technique de fabrication efficace de CQD fluorescents biocompatibles à grande échelle est toujours nécessaire et est devenue un défi pour les applications pratiques des CQD. Il a été remarqué que la synthèse directe des CQD à partir de produits alimentaires [17,18,19] et/ou de sous-produits [20] est l'une des stratégies prometteuses et significatives. Des points de carbone émetteurs rouges (R-CD) d'un diamètre moyen de 4 nm et d'un rendement quantique élevé (QY) de 28 % dans l'eau ont été synthétisés [21] en chauffant une solution d'éthanol de jus de citron sans pulpe. Un puissant réducteur NaBH4 ajouté dans les R-CD a été utilisé comme moyen d'augmenter l'intensité de l'émission lumineuse des R-CD. Cependant, nous savons que NaBH4 est toxique. Très récemment, nous avons fabriqué les CQD à émission verte et bleue à partir d'eaux usées de tofu sans ajouter de substances toxiques [22]. Les CQD fabriqués à partir de produits alimentaires et/ou de sous-produits sont considérés comme sûrs pour les applications biologiques car il n'y a presque aucune toxicité connue dans ces ressources naturelles de carbone. Récemment, plusieurs études sérieuses ont été menées pour synthétiser des CQD à partir de ressources carbonées non toxiques en utilisant une approche en une étape et des progrès significatifs ont été réalisés dans la synthèse, l'étude et l'application de ces CQD. Par exemple, l'ail a été utilisé comme source verte pour synthétiser les CQD [23]. Des études détaillées de structure et de composition ont démontré [23] que la teneur en N et la formation de C–N et C=N sont des clés pour améliorer la photoluminescence (PL) QY. De plus, les CQD présentent une excellente stabilité dans une large gamme de pH et des concentrations élevées de NaCl, ce qui les rend applicables dans des conditions compliquées et difficiles [23].
La principale motivation du présent travail est de développer une méthode expérimentale simple et efficace pour la fabrication à faible coût de CQD à partir de jus de citron en utilisant un traitement hydrothermal à des températures relativement basses et grâce à un processus moins long. Il est connu que le jus de citron peut être obtenu facilement et à moindre coût et, par conséquent, c'est une bonne source de carbone pour la fabrication d'échantillons et de dispositifs à base de CQD. Par rapport à l'étude précédente [21], les CQD non toxiques obtenus dans notre travail sont plus adaptés à l'imagerie biologique et aux marqueurs cellulaires. Dans cette étude, nous menons également l'examen du matériau de base et des propriétés optiques des CQD réalisés à partir de jus de citron et appliquons les CQD à l'imagerie des cellules végétales.
Méthodes
Matériaux préliminaires
Dans cette étude, les matériaux précurseurs de carbone sont extraits de jus de citron frais. Les principaux ingrédients et leurs pourcentages sont obtenus par mesure de chromatographie liquide à haute performance (HPLC) comme indiqué dans le tableau 1. Pour la préparation des échantillons, le citron frais pris comme source de carbone et l'oignon frais utilisé pour l'imagerie cellulaire ont été achetés au supermarché local. L'éthanol était analytiquement pur et utilisé comme agent dispersant. De l'eau déminéralisée (18,25 MΩ cm) a été utilisée pour les expériences.
Synthèse des CQD
Les CQD ont été synthétisés à partir de jus de citron par un simple traitement hydrothermal à des températures relativement basses et par un processus moins long. Les processus typiques de préparation des échantillons sont illustrés à la figure 1. Quatre-vingts millilitres de jus de citron sans pulpe ont été mélangés avec 60 mL d'éthanol. Le mélange a ensuite été transféré dans un autoclave en acier inoxydable équipé de polytétrafluoroéthylène et est chauffé à une température constante à environ 120 °C pendant 3 h. Après la réaction, le produit brun foncé a été obtenu après refroidissement naturel à température ambiante. La solution brun foncé a été lavée avec un excès de dichlorométhane pour éliminer les fragments organiques n'ayant pas réagi et cette étape peut être répétée 2 à 3 fois. L'eau désionisée a été ajoutée jusqu'à ce que le volume de la solution brune augmente jusqu'à un tiers de la solution et centrifugée à 10 000 tr/min pendant 15 minutes pour séparer les grosses particules. Ainsi, les échantillons CQD peuvent être obtenus par carbonisation de jus de citron, qui contient des glucides et des acides organiques comme le glucose, le fructose, le saccharose, l'acide ascorbique, l'acide citrique, etc. comme précurseurs du carbone. Notre réaction hydrothermale facile est à une température plus basse (120 °C) et prend moins de temps (3 h), par rapport à la méthode rapportée [24].
Préparation de CQD à partir de jus de citron par traitement hydrothermal
Caractérisation
La morphologie et les microstructures des CQD réalisées à partir de jus de citron ont été analysées par le microscope électronique à transmission (JEM 2100, Japon) fonctionnant à 300 KV. La phase cristalline des CQD a été étudiée par diffraction des rayons X (Rigaku TTR-III, Japon) en utilisant le rayonnement Cu-Kα (λ = 0,15418 nm). Le spectre d'absorption UV-Vis a été mesuré par un spectrophotomètre UV-Vis (Specord200). L'émission lumineuse induite par les photons a été examinée par spectrophotomètre à fluorescence (IHR320, HORIBA Jobin Yvon, USA) pour différentes longueurs d'onde d'excitation allant de 330 à 490 nm. Les spectres de spectroscopie photoélectronique aux rayons X (XPS) ont été enregistrés par le spectromètre photoélectronique PHI5000 Versa Probe II avec Al Kα à 1486,6 eV.
Résultats et discussions
Les images au microscope électronique à transmission (MET) des CQD sont illustrées à la Fig. 2. L'image MET à faible grossissement des échantillons tels que préparés indique que les CQD ont une dispersité uniforme. Les CQD sont de forme sphérique avec une distribution de taille étroite allant de 2,0 à 4,5 nm et avec une taille moyenne de 3,1 nm illustrée à la Fig. 2b, c. La figure 2d montre l'espacement de réseau de 0,215 nm qui correspond à la facette [100] du carbone graphitique, et le modèle de transformée de Fourier rapide (FFT) correspondant des CQD montre en outre la structure hautement cristalline, conforme au rapport précédent [25]. Par rapport aux études précédentes [19, 21, 22, 23], comme le montre la Fig. 2, les CQD obtenus dans notre travail sont non seulement de bonne qualité mais présentent également une meilleure morphologie uniforme. Par conséquent, les CQD avec une morphologie arrondie uniforme et bien cristalline peuvent être fabriqués grâce à un processus de traitement hydrothermal facile. Le rendement de production (PY) des CQD peut être calculé selon la définition PY = (m /M ) × 100%, où m est la masse des CQD, et M est la masse de jus de citron frais. Le rendement de production de CQD préparés dans cette étude est d'environ 0,1 % selon les résultats de mesure, à savoir, 100 g de liquide avec 6,30 % d'acide citrique peuvent obtenir environ 0,1 g de CQD (voir Tableau 1).
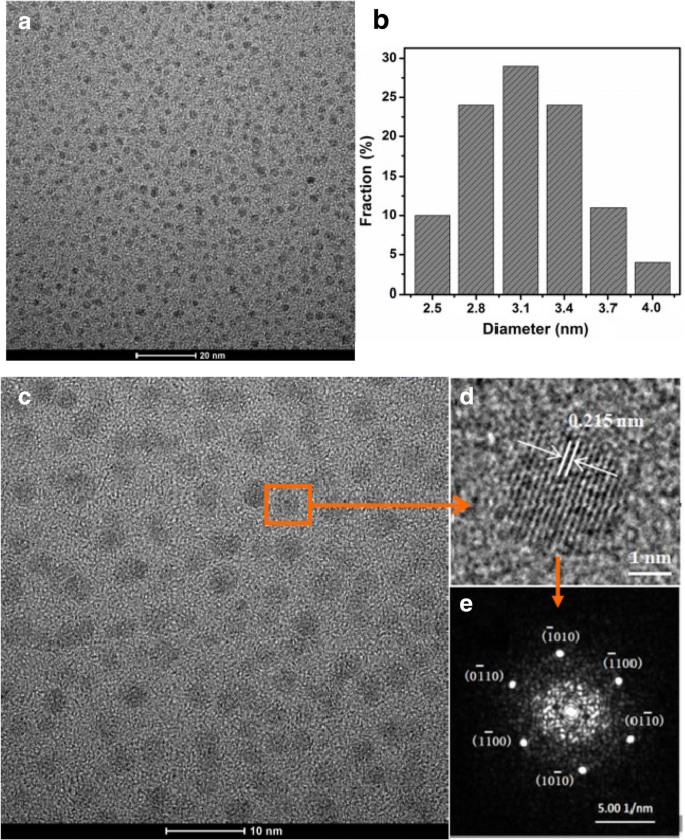
un , c , d image TEM. b Distribution granulométrique des CQD. e Le modèle FFT correspondant des CQD
Le profil typique de diffraction des rayons X (XRD) et XPS des CQD est illustré à la Fig. 3. Il y a un large pic (002) centré à 2θ ~ 21,73°, et l'espacement entre les couches a été calculé à 0,409 nm, correspondant à la structure du graphite, comme le montre la figure 3a, ce qui est similaire aux dévaluations rapportées pour les CQD préparés par d'autres méthodes [15, 26]. La variation de la distance intercouche peut être causée par l'introduction de groupes contenant davantage d'oxygène tels que la présence de -OH et -COOH sur la surface et le bord du CQD pendant la procédure de réaction hydrothermale pour la préparation des CQD. XPS et FTIR ont été utilisés pour détecter la composition des CQD. Comme le montre la Fig. 3b, c, le spectre XPS montre un pic C1s graphitique dominant à 284,5 eV et un pic O1s à 531,4 eV de CQD. Le pic typique à 284,7, 286,5 et 288,9 eV dans une analyse à haute résolution du spectre XPS C1s (Fig. 3c est attribué à C=C/C-C, C-O et C=O/COOH, respectivement. Cela indique clairement que les CQD ont été fonctionnalisés avec des groupes hydroxyle, carbonyle et acide carboxylique, qui sont bénéfiques pour la modification de surface et la fonctionnalisation, et sont également propices à la solubilité dans l'eau.La figure 3d montre le spectre de spectroscopie infrarouge à transformée de Fourier (FTIR) de les CQD. La présence de fonctionnalités oxygène de différents types dans les CQD a été confirmée par des pics à 3 450 cm −1 (vibrations d'étirement O–H), 2927 cm −1 , 1407 cm −1 (vibrations d'étirement C–H), 1726 cm −1 (C=O vibrations d'étirement), 1639 cm −1 (C=C vibrations d'étirement), 1227 cm −1 (vibrations d'étirement C–OH) et 1080 cm −1 (C–O vibrations d'étirement). Il est à noter que l'analyse FTIR est conforme au résultat XPS ci-dessus. Plus important encore, le pic C–O–C (époxy) a complètement disparu à 1290 cm −1 . Ces résultats impliquent le mécanisme de formation des CQD, avec la rupture des groupes époxy et la formation des liaisons C-C sous-jacentes, par la suite le sp 2 domaines a été extrait de précurseurs de petites molécules tels que le glucose, le fructose, l'acide ascorbique et l'acide citrique par une déshydratation ou une carbonisation supplémentaire et finalement pour former des CQD. Par conséquent, la scission de la liaison des groupes oxygène environnants contribue à la formation des CQD [15, 27].
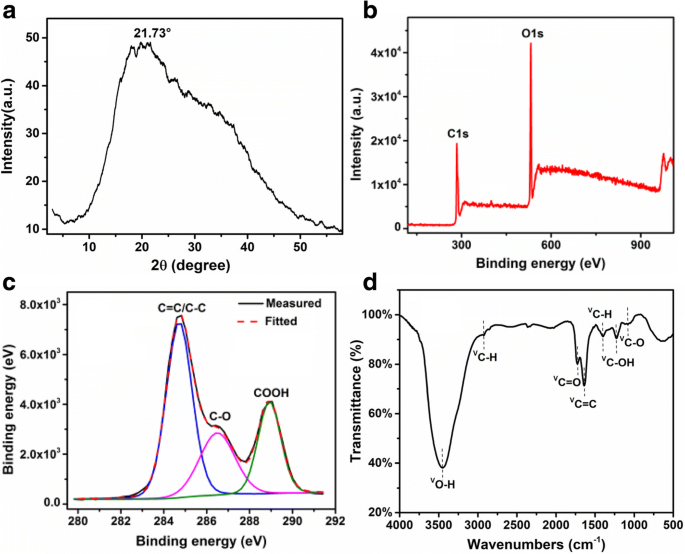
un modèle XRD. b Spectres XPS bas de gamme. c Scan XPS haute résolution de la région C1. d Spectres FTIR des CQD
À l'heure actuelle, les mécanismes possibles pour la formation de CQD à partir de précurseurs de carbone par la méthode hydrothermale ont été proposés et examinés [28]. Sur la base de ces résultats publiés, nous pouvons comprendre le mécanisme de synthèse des CQD à partir du jus de citron. Le jus de citron sans pulpe est chauffé et déshydraté pour former la structure de base de C=C/C–C qui est principalement composée de CQD, et le reste des molécules atteint la surface du noyau pour produire un nouveau C=C/ liaison C-C, puis cultivée en continu sous cette forme. Avec l'allongement du temps de chauffage, la morphologie des CQD se forme progressivement. Dans le même temps, dans le processus de traitement hydrothermal des CQD formés, la surface et le bord des CQD peuvent contenir beaucoup d'hydroxyle (-OH), de carboxyle (-COOH) et de carbonyle (-C=O) ou d'autres oxygènes. contenant des groupes fonctionnels; une partie de l'atome H et O dans ces groupes pourrait être éliminée par déshydratation dans l'environnement hydrothermal.
Pour examiner les propriétés optiques des CQD, les spectres d'absorption ultraviolet-visible (UV-Vis) et de photoluminescence (PL) des CQD ont été mesurés en conséquence. Comme le montre la figure 4a, le pic d'absorption optique des CQD a été observé dans la région ultraviolette avec une absorption maximale à 283 nm, ce qui est dû à n -π * transition de la bande C=O [29]. Le spectre PL de la figure 4b montre que la longueur d'onde d'émission PL des CQD atteint le pic à 482 nm avec une longueur d'onde d'excitation de 410 nm. La longueur d'onde d'émission est passée de 430 à 530 nm lorsque la longueur d'onde d'excitation a été augmentée de 330 à 490 nm. Avec l'augmentation de la longueur d'onde d'excitation, les pics d'émission de fluorescence se transforment en décalage vers le rouge, se référant à l'apparition de la réabsorption des photons. Le résultat révèle que les CQD ont une caractéristique PL dépendante de l'excitation [30]. Les CQD fluorescents verts montrent également un large pic PL qui se déplace avec le changement de longueur d'onde d'excitation, qui est lié à l'effet de confinement quantique et aux défauts de bord. Avec la mesure PL standard [22], le rendement quantique de fluorescence des CQD est de 16,7% avec une longueur d'onde d'excitation de 410 nm, où le sulfate de quinine avait été utilisé comme référence. Cette valeur est significativement meilleure que le QY (8,95 %) des CQD à base de jus de citron dans le rapport précédent [24]. Il est connu que le QY des CQD peut être considérablement amélioré après modification de surface ou passivation [30]. L'ajout d'éthanol au cours du processus de synthèse peut introduire davantage de groupes fonctionnels, ce qui peut entraîner un QY plus élevé des CQD. Cependant, le QY des CQD dans cette étude est nettement inférieur au QY des CQD synthétisés en utilisant l'acide citrique (CA) et l'éthanolamine (EA) comme molécules modèles. Ici, la pyrolyse à 180 °C a donné un précurseur moléculaire avec un PL fortement intense et un QY élevé de 50 %, ce qui est dû au dopage N au cours du processus de synthèse [30].
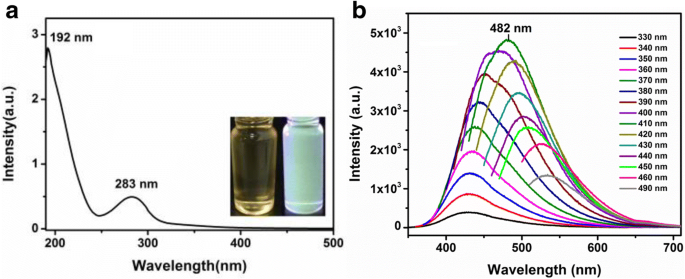
un Spectres d'absorption UV-Vis des CQD, en médaillon :images optiques sous lumière du jour (gauche) et lumière UV (droite). b Spectres PL des CQD à différentes longueurs d'onde d'excitation
Étant non toxiques et respectueux de l'environnement, les CQD sont considérés comme des alternatives aux points quantiques semi-conducteurs à appliquer dans les systèmes biologiques à la fois in vitro et in vivo. Les CQD tels que synthétisés ont été appliqués sur une image optique de cellules épidermiques d'oignon, comme le montre la figure 5. La microscopie à fluorescence révèle que les parois cellulaires et le noyau cellulaire des cellules épidermiques internes de l'oignon peuvent être vus clairement, bien en place et fort au sens tridimensionnel. Les résultats montrent que la coloration et l'imagerie des points quantiques de carbone sont excellentes et n'ont aucun effet néfaste sur les organismes et aucun dommage morphologique des cellules observées, démontrant en outre des CQD avec une faible cytotoxicité. L'image confocale de la figure 5 indique que les CQD synthétisés à partir de jus de citron peuvent être utilisés dans l'imagerie des cellules végétales en tant qu'indicateurs fluorescents, montrant en outre les applications potentielles de l'imagerie biologique des CQD.
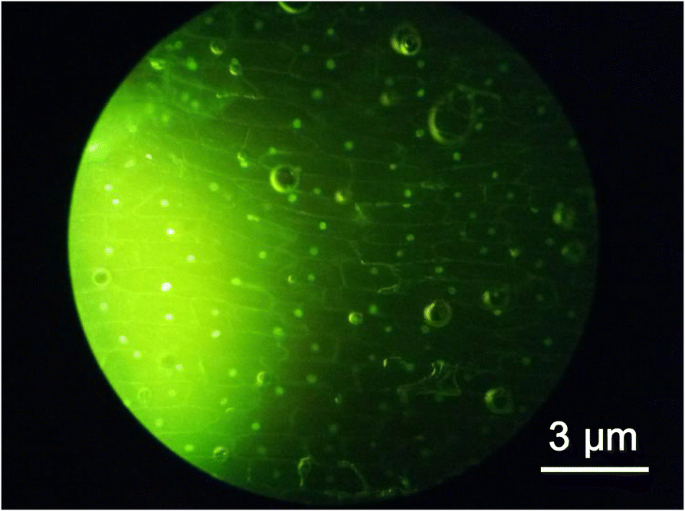
Une image optique de cellules épidermiques d'oignon colorées à l'aide de CQD éclairées par une source de lumière bleue
Conclusions
Dans cette étude, les points quantiques de carbone fluorescents solubles dans l'eau ont été synthétisés en utilisant du jus de citron comme ressource de carbone par une réaction hydrothermale facile. Ces CQD sont dotés de bonnes propriétés matérielles et optiques. Ils peuvent émettre une fluorescence de couleur bleu-vert brillante sous irradiation UV ou lumière bleue. Nous avons démontré que les CQD peuvent être utilisés en imagerie de cellules végétales. Nous espérons que ces découvertes importantes et significatives pourront nous aider à acquérir une compréhension approfondie des CQD et à explorer des applications plus pratiques des nouvelles nanostructures à base de carbone.
Abréviations
- CQD :
-
Points quantiques de carbone
- FFT :
-
Transformée de Fourier rapide
- HPLC :
-
Chromatographie liquide haute performance
- PL :
-
Photoluminescence
- QLED :
-
LED point quantique
- QY :
-
Rendement quantique
- R-CD :
-
Points de carbone émetteurs rouges
- TEM :
-
Microscope électronique à transmission
- UV-Vis :
-
Ultraviolet-visible
- XPS :
-
Spectroscopie photoélectronique aux rayons X
- XRD :
-
Diffraction des rayons X
Nanomatériaux
- Le réarrangement atomique de plusieurs puits quantiques à base de GaN dans du gaz mixte H2/NH3 pour améliorer les propriétés structurelles et optiques
- Modulation des propriétés d'anisotropie électronique et optique du ML-GaS par champ électrique vertical
- Synthèse facile et propriétés optiques de petits nanocristaux et nanotiges de sélénium
- Synthèse de points quantiques de carbone co-dopés en pyridinique N, S en tant qu'imitateurs d'enzymes efficaces
- Caractéristiques optiques et électriques des nanofils de silicium préparés par gravure autocatalytique
- Une approche simple pour la synthèse de points quantiques de carbone fluorescent à partir d'eaux usées de tofu
- Synthèse de points quantiques de sulfure d'antimoine solubles dans l'eau et de leurs propriétés photoélectriques
- Synthèse sonochimique en une étape facile et propriétés photocatalytiques des composites graphène/Ag3PO4 Quantum Dots
- Propriétés microstructurales, magnétiques et optiques des nanoparticules de Perovskite Manganite La0.67Ca0.33MnO3 dopées au Pr synthétisées via un procédé Sol-Gel



