Aptitude verte dans la synthèse et la stabilisation des nanoparticules de cuivre :activités catalytiques, antibactériennes, cytotoxiques et antioxydantes
Résumé
Les nanoparticules de cuivre (CuNP) sont d'un grand intérêt en raison de leurs propriétés extraordinaires telles que le rapport surface/volume élevé, la limite d'élasticité élevée, la ductilité, la dureté, la flexibilité et la rigidité. Les CuNPs présentent des activités catalytiques, antibactériennes, antioxydantes et antifongiques ainsi qu'une cytotoxicité et des propriétés anticancéreuses dans de nombreuses applications différentes. De nombreuses méthodes physiques et chimiques ont été utilisées pour synthétiser des nanoparticules, notamment l'ablation au laser, le processus assisté par micro-ondes, le sol-gel, la co-précipitation, la décharge par fil pulsé, le dépôt en phase vapeur sous vide, l'irradiation à haute énergie, la lithographie, le broyage mécanique, la réduction photochimique, l'électrochimie , synthèse par électropulvérisation, réaction hydrothermale, microémulsion et réduction chimique. La phytosynthèse des nanoparticules a été suggérée comme une alternative précieuse aux méthodes physiques et chimiques en raison de sa faible cytotoxicité, de ses perspectives économiques, de sa biocompatibilité améliorée et respectueuse de l'environnement et de ses activités antioxydantes et antimicrobiennes élevées. La revue explique les techniques de caractérisation, leur rôle principal, leurs limites et la sensibilité utilisées dans la préparation des CuNPs. Un aperçu des techniques utilisées dans la synthèse des CuNPs, la procédure de synthèse, les paramètres de réaction qui affectent les propriétés des CuNPs synthétisés, et une analyse de criblage qui est utilisée pour identifier les composés phytochimiques dans différentes plantes est présenté à partir de la littérature publiée récemment qui a été examinée et résumée . Des mécanismes hypothétiques de réduction de l'ion cuivre par la quercétine, la stabilisation des nanoparticules de cuivre par le santin, l'activité antimicrobienne et la réduction du 4-nitrophénol avec des illustrations schématiques sont donnés. L'objectif principal de cette revue était de résumer les données des plantes utilisées pour la synthèse des CuNPs et d'ouvrir une nouvelle voie aux chercheurs pour étudier les plantes qui n'ont pas été utilisées dans le passé.
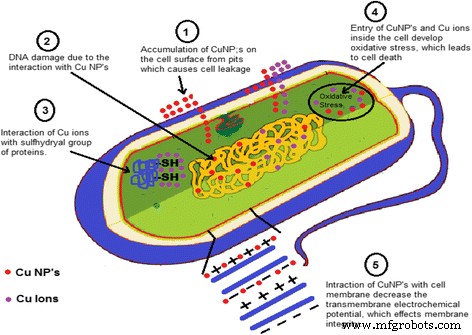
Mécanisme proposé pour l'activité antibactérienne des nanoparticules de cuivre.
Contexte
Les nanoparticules (NP) ont un certain nombre d'applications intéressantes dans le domaine industriel telles que la technologie spatiale, le magnétisme, l'optoélectronique et l'électronique, les cosmétiques et les applications catalytiques, pharmaceutiques, biomédicales, environnementales et énergétiques [1, 2]. Les propriétés extraordinaires des NP telles que la ductilité, la limite d'élasticité élevée, la dureté, la flexibilité, la rigidité, le rapport surface/volume élevé, l'effet tunnel macroquantique et la taille quantique sont attribuables par rapport aux propriétés des matériaux en vrac ayant la même composition chimique [3 ]. En effet, les propriétés des NPs, qui peuvent considérablement différer de celles observées pour les particules fines, sont une surface spécifique plus élevée, des propriétés optiques spécifiques, des points de fusion plus bas, des aimantations spécifiques, une résistance mécanique et de nombreuses applications industrielles [4]. Les nanoparticules de cuivre (CuNP) sont d'un grand intérêt en raison de leur disponibilité facile, de leur faible coût et de leurs propriétés similaires à celles des métaux nobles [5,6,7,8,9]. Les CuNP peuvent également être utilisées dans les capteurs, les systèmes de transfert de chaleur [10,11,12] et l'électronique (pile à combustible et cellule solaire), comme catalyseurs dans de nombreuses réactions et comme agents bactéricides et antimicrobiens utilisés pour revêtir les équipements hospitaliers [13,14, 15,16,17,18,19].
De nombreuses méthodes physiques et chimiques, notamment l'ablation laser [20], le procédé assisté par micro-ondes, le sol-gel [21], la co-précipitation [22], la décharge par fil pulsé [23], le dépôt en phase vapeur sous vide [24], l'irradiation à haute énergie [ 25], lithographie [26], fraisage mécanique [27], réduction photochimique, électrochimie [28,29,30,31,32], synthèse par électrospray [33], réaction hydrothermale [34], microémulsion [35] et réduction chimique sont utilisés pour synthétiser des nanoparticules. Bien que les méthodes physiques et chimiques produisent des nanoparticules pures et bien définies, ces méthodes ne sont ni rentables ni écologiques en raison de l'utilisation de produits chimiques toxiques. L'un des critères les plus importants de la nanotechnologie est le développement de procédures de chimie verte respectueuses de l'environnement, non toxiques et propres [36]. Par conséquent, la biosynthèse des nanoparticules contient une méthode basée sur la chimie verte qui utilise différents corps biologiques tels que les plantes [37, 38], les actinomycètes [39, 40], les champignons [41,42,43,44], les bactéries [45,46, 47,48,49], la levure [50,51,52] et les virus [53, 54]. Les entités biologiques offrent une approche non toxique, propre et respectueuse de l'environnement pour synthétiser les NP avec un large éventail de tailles, de propriétés physico-chimiques, de formes et de compositions [55].
Des nanoparticules de cuivre ont été synthétisées et stabilisées dans la littérature en utilisant différentes plantes telles que Euphorbia esula [56], Punica granatum [57], Ocimum sanctum [58], Ginkgo biloba [59], Calotropis procera [60], Lawsonia inermis [61], Citrus medicalinn [62], Camellia sinensis [63], Datura innoxia [64], Syzygium aromaticum [65], Sesamum indicum [66], Citrus limon , Curcumine de curcuma [67], Gloriosa superba L. [68], Ficus carica [69], Aegle marmelos [70], Caesalpinia pulcherrima [71], Fistule de Cassia [72], Leucas aspera , Leucas chinensis [73], Delonix elata [74], Aloe barbadensis Miller [75], Thymus vulgaris [76], Phyllanthus emblica [77], Magnolia kobus [78], Eucalyptus [79], Artabotrys odoratissimus [80], Capparis zeylanica [81], Vitis vinifera [82], Hibiscus rosa-sinensis [83], Zingiber officinale [84], Datura metel [85], Zea mays [86], Urtique , Matricaria chamomilla , Glycyrrhiza glabra , Schisandra chinensis , Inula helenium , Cinnamomum [87], Dodonaea viscosa [88], Cassia auriculata [89], Azadirachta indica , Appareil photo Lantana , Tridax procumbens [90], Allium sativum [91], Asparagus adscendens , Bacopa monnieri , Ocimum bacilicum , Withania somnifera [92], Smithia sensitiva , Colocasia esculenta [93], Nerium oleander [94], et Psidium guajava [95] ; en utilisant différentes algues/champignons tels que Phaeophyceae [96], Stereum hirsutum [97], et Hypocrea lixii [98] ; et en utilisant certains micro-organismes tels que Pseudomonas fluorescens [99] et Enterococcus faecalis [100] cultures.
Biosynthèse des nanoparticules de cuivre
Parties de plante utilisées pour l'extrait
Différentes parties des plantes sont utilisées pour la préparation d'extraits de plantes tels que les feuilles, les graines, les écorces, les fruits, la peau, la fibre de coco, les racines et la gomme. Les feuilles et les racines sont utilisées de deux manières. Premièrement, des feuilles et racines fraîches sont utilisées pour la préparation d'extraits de plantes, et deuxièmement, des feuilles et racines sèches sous forme de poudre sont utilisées.
Procédure de synthèse des CuNPs
Pour la synthèse des CuNPs, un extrait de plante a été préparé en utilisant différentes parties de différentes plantes. Pour la synthèse de la partie extraite de la plante d'intérêt, les feuilles sont collectées et lavées à l'eau du robinet puis à l'eau distillée pour éliminer les particules de poussière. Les feuilles lavées sont ensuite utilisées de deux manières. Tout d'abord, ces feuilles sont séchées au soleil pendant 1 à 2 h pour éliminer l'humidité résiduelle. Les poids connus de ces feuilles séchées au soleil sont divisés en petites parties et trempés dans de l'eau désionisée ou une solution d'éthanol. Ce mélange est agité pendant 24 h à température ambiante à l'aide d'un agitateur magnétique, puis filtré pour une utilisation ultérieure. Deuxièmement, ces feuilles sont séchées au soleil pendant 4 à 7 jours ou séchées dans un four à 50 °C pendant 1 jour et réduites en poudre à l'aide d'un mélangeur domestique. Le poids connu de la poudre de plante est mélangé dans de l'eau ou une solution d'éthanol, puis agité et filtré.
Pour la synthèse des CuNPs, une solution aqueuse de sels précurseurs tels que le sulfate de cuivre, le chlorure de cuivre, l'acétate de cuivre et le nitrate de cuivre à différentes concentrations est mélangée à un extrait de plante. Une solution aqueuse d'hydroxyde de sodium est également préparée et ajoutée au mélange réactionnel pour contrôler le pH du milieu. Le mélange réactionnel est fortement agité pendant différents intervalles de temps dans un agitateur électrique et chauffé dans un four à différents intervalles de temps et à différentes températures. La formation de CuNPs peut également avoir lieu à température ambiante et est confirmée en changeant la couleur du mélange réactionnel. À la fin, les nanoparticules ont été centrifugées et séchées à différentes températures. Les optimisations de réaction ont lieu en modifiant le pH du mélange, la concentration du sel précurseur, le temps de chauffage et la température du mélange réactionnel. Dans la littérature, différentes plantes ont été utilisées pour la formation de nanoparticules de cuivre en utilisant différents sels précurseurs avec différentes conditions de réaction, comme indiqué dans le tableau 1. À partir du tableau, on peut voir que les différentes conditions de réaction affectent la forme et la taille du cuivre. nanoparticules.
Effet des paramètres de réaction sur les propriétés des NP
La concentration d'extrait de plante joue un rôle principal dans la réduction et la stabilisation des CuNPs. Il a été rapporté qu'en augmentant la concentration d'extrait de plante, le nombre de particules augmentait [88]. En augmentant la concentration d'extrait de plante, la concentration de composés phytochimiques a augmenté et la réduction de sel de cuivre a également augmenté. En raison de la réduction rapide du sel métallique, la taille des nanoparticules a également diminué [101].
La taille et la structure des CuNPs sont fortement affectées par le sel de cuivre. La morphologie des nanoparticules change lorsque le sel (par exemple, le chlorure de cuivre, l'acétate de cuivre, le nitrate de cuivre ou le sulfate de cuivre) est utilisé en présence d'hydroxyde de sodium. Il a été rapporté que la forme était triangulaire et tétraédrique dans le cas du chlorure de cuivre, en forme de tige dans le cas de l'acétate de cuivre et sphérique dans le cas du sulfate de cuivre [102]. En augmentant la concentration du sel précurseur, la taille des CuNPs a également augmenté.
La synthèse des CuNPs donne les meilleurs résultats en faisant varier le pH du milieu réactionnel dans la gamme préférée. La taille des nanoparticules a été contrôlée en modifiant la valeur du pH du mélange réactionnel. À un pH plus élevé, des nanoparticules de plus petite taille ont été obtenues par rapport à celles obtenues à une faible valeur de pH. Cette différence peut être attribuée à la différence de taux de réduction des sels métalliques par extrait végétal. La relation inverse entre la valeur du pH et la taille des nanoparticules a montré qu'une augmentation de la valeur du pH nous permet d'obtenir des nanoparticules sphériques de petite taille tandis qu'une diminution de la valeur du pH donne des nanoparticules de grande taille (en forme de bâtonnet et triangulaire). L'effet sur les spectres d'absorption de différentes valeurs de pH (4, 6, 8, 10 et 12) est représenté sur la figure 1 [36]. Il a été rapporté que l'ajout d'extrait de plante à CuCl2 n'a pas conduit à la formation de CuNPs mais, à la place, les CuNPs ont été obtenus en changeant le pH du mélange réactionnel en milieu basique. Le même comportement a été observé par Wu et Chen, et il a été conclu que le pH joue un rôle important dans la synthèse des CuNPs [103].
Parties de la plante utilisées pour la préparation d'extrait de plante
Mécanisme de phytosynthèse des nanoparticules de cuivre
Dépistage phytochimique :une analyse qualitative
L'analyse de dépistage phytochimique est une analyse chimique effectuée pour la détection de composés phytochimiques dans différentes plantes. L'extrait de plante fraîche avec des produits chimiques ou des réactifs chimiques est utilisé pour cette analyse [77] comme indiqué dans le tableau 2.
Phytochimiques pour la réduction des métaux et la stabilisation des NP
La synthèse verte des CuNPs par l'utilisation de produits phytochimiques offre un contrôle plus flexible sur la forme et la taille des NPs (c'est-à-dire en modifiant la température de réaction, la concentration d'extrait de plante, la concentration de sel métallique, le temps de réaction et le pH du mélange réactionnel). Le changement de couleur du milieu réactionnel indique une réduction de l'ion métallique et la formation de NP. La réduction verte des sels de cuivre commence instantanément et la formation de nanoparticules de cuivre est indiquée par le changement de couleur du mélange réactionnel. Les composés phytochimiques ont un rôle principal dans la réduction des ions métalliques, puis dans la stabilisation des noyaux métalliques sous forme de nanoparticules, comme le montre la figure 2. L'interaction des composés phytochimiques avec les ions métalliques et la concentration de ces composés phytochimiques contrôlent la forme et la taille des CuNP.
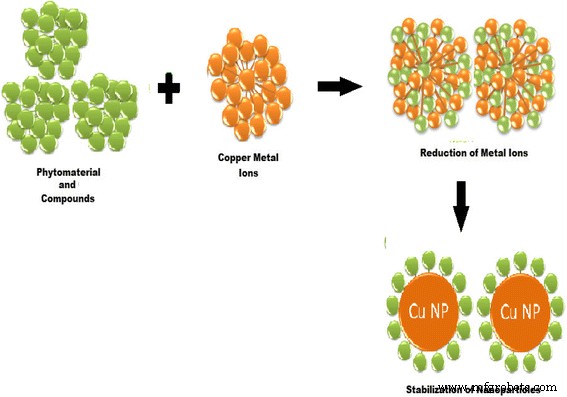
Un protocole pour réduire les ions métalliques puis stabiliser les noyaux métalliques
Les flavonoïdes contiennent des composés polyphénoliques, tels que la quercétine, les catéchines, les flavanones, les isoflavones, le santin, la penduletine, l'alizarine, la pinocembrine, les anthocyanes, les flavones, les tanins et les saponines, qui sont présents dans différentes plantes telles que le Ginkgo biloba [59], Citrus medicalinn [62], Phyllanthus emblica [77], Hibiscus rosa-sinensis [83], et Dodonaea viscosa [93]. Ces composés jouent un rôle principal dans la réduction et la chélation du métal. Divers groupes fonctionnels présents dans les flavonoïdes sont responsables de la réduction de l'ion cuivre. Il a été supposé qu'un atome d'hydrogène réactif dans les flavonoïdes peut être libéré lors des altérations tautomères de la forme énol en forme céto, ce qui peut réduire les ions cuivre pour former des noyaux de cuivre ou des CuNP. Par exemple, on suppose que dans le cas du Ginkgo biloba extraits de plantes, c'est la transformation de la quercétine (flavonoïde) qui joue un rôle principal dans la réduction des ions métalliques de cuivre en noyaux de cuivre ou CuNPs en raison du changement de forme énol en forme céto comme le montre la figure 3.
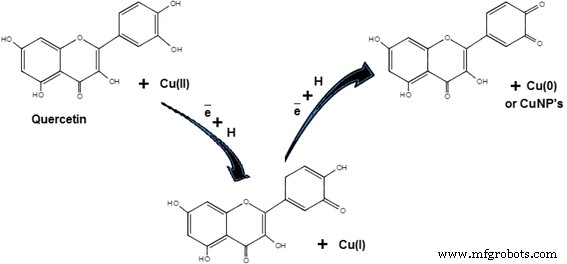
Réduction des ions cuivre par la quercétine
Au cours du processus de synthèse des CuNPs, les ions métalliques avec des états d'oxydation monovalents ou divalents sont convertis en noyaux de cuivre à oxydation nulle et ces noyaux sont fusionnés pour obtenir différentes formes. Pendant la nucléation, les noyaux s'agrègent pour former différentes formes telles que des fils, des sphères, des cubes, des tiges, des triangles, des pentagones et des hexagones. Certains flavonoïdes ont la capacité de chélater les CuNP avec leur π électrons et groupes carbonyle. La quercétine et la santine sont des flavonoïdes à forte activité chélatante en raison de la présence de deux groupes fonctionnels impliquant les hydroxyles et les carbonyles. Ces groupes chélatent avec des nanoparticules de cuivre en suivant le mécanisme précédent et expliquent également la capacité d'adsorption du santin (flavonoïde) à la surface des CuNPs, comme le montre la figure 4.
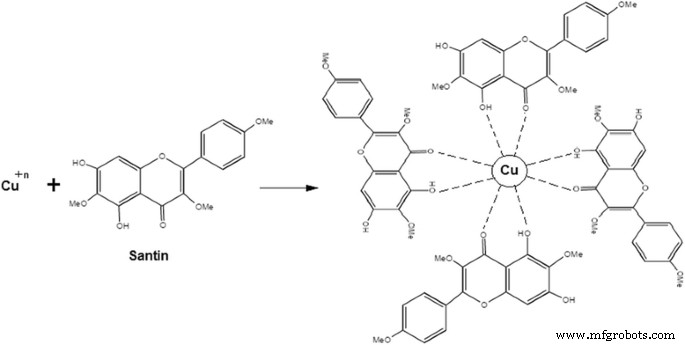
Stabilisation des nanoparticules de cuivre par santin
Il a été supposé que les molécules de protéines (superoxyde dismutase, catalase, glutathion) dans différentes plantes telles que Hibiscus rosa-sinensis [83] et Camellia sinensis [104] présentent une activité réductrice élevée pour la formation de nanoparticules à partir d'ions métalliques mais leur activité chélatante n'est pas excessive. Sucres tels que les monosaccharides (glucose), les disaccharides (maltose et lactose) et les polysaccharides dans Camellia sinensis la plante [63] peut agir comme agents réducteurs ou antioxydants et avoir une série de transformations tautomères de la cétone en aldéhyde.
Autres composés phytochimiques tels que les polyphénols (par exemple, l'acide ellagique et l'acide gallique) qui sont présents dans Hibiscus rosa-sinensis [40], phénylpropanoïdes (phénylalanine, tyrosine) dans Aegle marmelos [70], terpénoïdes dans Ocimum sanctum et Asparagus adscendens [58, 92], protéases à cystéine dans Calotropis procera [60], curcuminanilineazométhine dans Curcumine de curcuma [67], acide ascorbique dans Citrus medicalinn [62], eugénol dans Syzygium aromaticum [65], et les alcaloïdes dans Aegle marmelos [70] jouent le même rôle de réduction des ions cuivre et de stabilisation des nanoparticules de cuivre. Glucides, anthraquinone, quinone et anthocyanoside dans Phyllanthus emblica [77] ; lignines et xanthones dans Hibiscus rosa-sinensis [83] ; et glycoside cardiaque, triterponoïde, glycoside caroténoïde et glycoside d'anthraquinone dans Colocasia esculenta plante [93] sont également des composés phytochimiques qui sont présents dans les extraits de différentes plantes et agissent comme agents réducteurs et stabilisants. Des exemples de certains composés phytochimiques avec des structures sont illustrés à la figure 5.
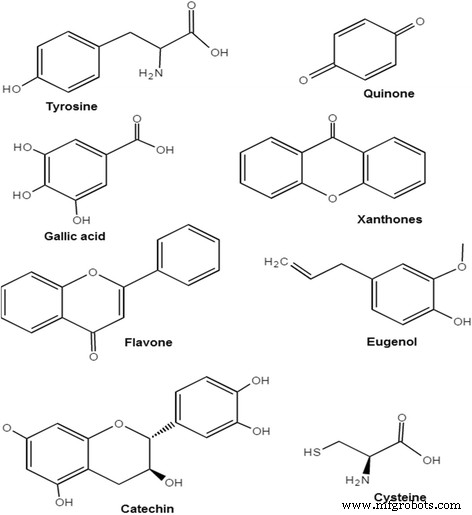
Phytochimiques avec leurs structures
Techniques de caractérisation
Pour la caractérisation des nanoparticules synthétisées, différentes techniques ont été utilisées telles que la spectroscopie ultraviolet-visible (UV-vis), la microscopie électronique à transmission (MET), la diffusion des rayons X aux petits angles (SAXS), la spectroscopie infrarouge à transformée de Fourier (FTIR), X- spectroscopie de fluorescence des rayons (XRF), diffraction des rayons X (XRD), spectroscopie photoélectronique à rayons X (XPS), microscopie électronique à balayage (MEB), microscopie électronique à balayage à émission de champ (FESEM), analyse granulométrique (PSA), Malvern Zetasizer ( MZS), spectroscopie à rayons X à dispersion d'énergie (EDX/EDS), analyse de suivi des nanoparticules (NTA), réflectométrie aux rayons X (XRR), analyse Brunauer-Emmett-Teller (BET), diffraction électronique à zone sélectionnée (SAED) et microscopie à force atomique (AFM) (tableau 3).
Applications des nanoparticules de cuivre
En raison de leurs propriétés chimiques et physiques exceptionnelles, de leur rapport surface/volume élevé, de leur surface constamment renouvelable, de leur faible coût et de leur préparation non toxique, les CuNP ont été d'un grand intérêt pour des applications dans différents domaines. Les nanoparticules de cuivre présentent une activité catalytique, une activité antibactérienne, une cytotoxicité ou une activité anticancéreuse, une activité antioxydante et une activité antifongique dans différentes applications. Dans l'activité catalytique, les nanoparticules de cuivre sont utilisées pour la cycloaddition Huisgen [3 + 2] d'alcynes et d'azides dans de nombreux solvants dans des conditions sans ligand [59], 1-méthyl-3-phénoxy benzène, 3,3-oxybis(méthylbenzène) [94], synthèse de 1H 1-substitué -1,2,3,4-tétrazole [76], adsorption de dioxyde d'azote et adsorption de dioxyde de soufre [66]. Dans la plupart des métaux de transition catalysés, des ligands de réaction de couplage d'Ullmann, tels que les phosphines, sont rapportés dans la littérature et la plupart des ligands sont coûteux, difficiles à préparer et sensibles à l'humidité. Pour ce travail, des nanoparticules de cuivre synthétisées sont utilisées pour le couplage Ullmann sans ligand de l'éther diphénylique. Les différents colorants et composés organiques toxiques et pesticides présents dans les déchets industriels sont très nocifs pour l'environnement et les organismes vivants. Les nanoparticules de cuivre sont utilisées pour la dégradation de différents colorants tels que le bleu de méthylène [73], la dégradation de l'atrazine [86] et la réduction du 4-nitrophénol [76].
Parmi les agents antimicrobiens, les composés du cuivre ont été couramment utilisés dans l'agriculture comme herbicides [105], algicides [106], fongicides [107] et pesticides ainsi que dans l'élevage comme désinfectant [108] (indiqué dans le tableau 4). Les nanoparticules de cuivre biogénique ont montré une puissante activité antibactérienne contre les agents pathogènes à Gram positif et à Gram négatif tels que Pseudomonas aeruginosa (MTCC 424), Micrococcus luteus (MTCC 1809), Enterobacter aerogenes (MTCC 2832) [57], Salmonella enterica (MTCC 1253), Rhizoctonia solani , Xanthomonas axonopodis pv. citri , Xanthomonas axonopodis pv. punicea [58], Escherichia coli (ATCC 14948) [62], Staphylococcus aureus (ATCC 25923), Bacillus subtilis (ATCC 6633), Pediococcus acidilactici [69], et Klebsiella pneumoniae (MTCC 4030). Dans l'activité antifongique, les nanoparticules de cuivre sont utilisées contre Alterneria carthami , Colletotrichum gloeosporioides , Colletotrichum lindemuthianum , Drechslera sorghicola , Fusarium oxysporum f.sp. carthami , Rhizopus stolonifer , Fusarium oxysporum f.sp. cicéris , Macrophomina phaseolina , Fusarium oxysporum f.sp. udum , Rhizoctonia bataticola [58], Candida albicans , Curvulaire , Aspergillus niger , et Trichophyton simii [67]. En cytotoxicité, les nanoparticules de cuivre sont utilisées pour une étude sur les lignées cellulaires HeLa, A549, MCF7, MOLT4 et BHK21 (tumeurs cancéreuses) [60, 104].
Mécanisme hypothétique de l'activité antimicrobienne
Il a été observé que les CuNPs ont une excellente activité antimicrobienne et seuls des rapports limités ont présenté le mécanisme de l'activité antibactérienne des nanoparticules de cuivre dans la littérature, mais ces mécanismes étaient hypothétiques. Il a été observé que les bactéries et les enzymes/protéines étaient détruites en raison de l'interaction des CuNPs avec le groupe -SH (sulfhydryle) [109, 110]. Il a également été rapporté que la structure hélicoïdale des molécules d'ADN est perturbée par l'interaction des CuNPs [111]. L'interaction des CuNPs avec la membrane cellulaire des bactéries a diminué le potentiel électrochimique transmembranaire, et en raison de la diminution du potentiel électrochimique transmembranaire, elle a affecté l'intégrité de la membrane [112]. Il a été supposé que les NP métalliques libèrent leurs ions métalliques respectifs. Les nanoparticules de cuivre et les ions de cuivre s'accumulent à la surface cellulaire des bactéries et forment des creux dans la membrane, provoquant une fuite du composant cellulaire de la cellule et à l'intérieur de la cellule, provoquant un stress oxydatif qui conduit à la mort cellulaire [112,113,114]. Un mécanisme hypothétique d'activité antibactérienne représentant les possibilités ci-dessus est illustré à la figure 6.
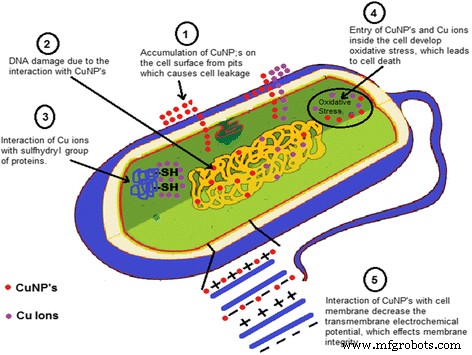
Mécanisme d'activité antibactérienne des nanoparticules de cuivre
Activité catalytique pour la réduction du 4-nitrophénol
Le 4-nitrophénol (4-NP) que l'on trouve généralement dans les eaux usées agricoles et les produits industriels est dangereux et non respectueux de l'environnement. L'hydrogénation ou la réduction du 4-NP, qui est converti en 4-aminophénol (4-AP), a lieu en présence de CuNPs. Les CuNP peuvent catalyser la réaction pour surmonter la barrière cinétique en aidant le transfert d'électrons des ions borohydrates donneurs vers l'accepteur 4-NP.
L'activité catalytique des CuNPs synthétisées a été étudiée dans la réduction du 4-nitrophénol en milieu aqueux à température ambiante en présence d'une solution aqueuse de borohydrure de sodium [56]. La réduction de 4-NP en utilisant des CuNPs est un processus simple et respectueux de l'environnement. L'efficacité catalytique des CuNPs pour la réduction de 4-NP a été examinée à l'aide d'un spectromètre UV-vis. Il a été observé que le pic d'absorption maximum du 4-NP en milieu aqueux était à 317 nm et que le pic d'adsorption s'est déplacé à 403 nm en ajoutant du borohydrure de sodium en raison de la formation d'ions 4-nitrophénolate. Un pic à 403 nm n'est pas affecté même après 2 jours, ce qui indique que la réduction de 4-NP ne peut pas avoir lieu en l'absence d'un catalyseur. Après avoir ajouté les CuNP, le pic d'absorption de la solution s'est déplacé à 300 nm et le pic à 403 nm a complètement disparu, ce qui indiquait la réduction de 4-NP en 4-AP sans aucun produit secondaire. Un mécanisme hypothétique pour la réduction du 4-NP est illustré à la Fig. 7. Dans le mécanisme, le 4-NP et le borohydrure de sodium sont présents dans la solution sous forme d'ions. Les protons de l'ion borohydrure s'adsorbent à la surface des nanoparticules de cuivre et BO2 produit. Les ions 4-nitrophénolate s'adsorbent également à la surface des CuNPs. En raison de l'adsorption des protons et de l'ion 4-nitrophénolate, les CuNP surmontent la barrière cinétique des réactifs et l'ion 4-nitrophénolate est converti en ion 4-aminophénolate. Après conversion, la désorption de l'ion 4-aminophénolate a lieu et il est converti en 4-aminophénol.
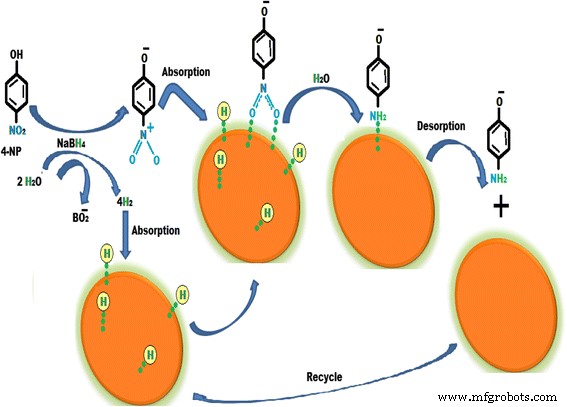
Mécanisme de réduction du 4-nitrophénol
Conclusions
Cet article a passé en revue et résumé des informations récentes sur les méthodes biologiques utilisées pour la synthèse de nanoparticules de cuivre (CuNP) en utilisant différentes plantes. La synthèse verte des CuNPs a été proposée comme une alternative précieuse aux méthodes physiques et chimiques avec une faible cytotoxicité, des perspectives économiques, une biocompatibilité améliorée et respectueuse de l'environnement, une faisabilité et une activité antioxydante élevée et une activité antimicrobienne élevée des CuNPs. Le mécanisme de biosynthèse des nanoparticules est encore inconnu, et davantage de recherches doivent se concentrer sur le mécanisme de formation des nanoparticules et la compréhension du rôle des composés phytochimiques dans la formation des nanoparticules. Cette revue donne des données sur les plantes utilisées dans la synthèse de nanoparticules de cuivre, la procédure de synthèse et les paramètres de réaction qui affectent les propriétés des CuNPs synthétisées. Une analyse de dépistage phytochimique est une analyse chimique utilisée pour identifier les composés phytochimiques tels que la détection des glucides, des tanins, des saponines, des flavonoïdes, des alcaloïdes, des anthraquinones et des anthocyanosides dans différentes plantes. Le mécanisme de réduction de l'ion cuivre par la quercétine et la stabilisation des nanoparticules de cuivre par la santin est décrit dans cet article. Les techniques de caractérisation utilisées dans la littérature pour les nanoparticules de cuivre sont UV-vis, FTIR, XRD, SEM, FESEM, TEM, PSA, MZS, EDX, NTA, SAXS, XRR, XRF, XPS, BET, SAED et AFM. Les nanoparticules de cuivre présentent une activité catalytique, une activité antibactérienne, une cytotoxicité ou une activité anticancéreuse, une activité antioxydante et une activité antifongique dans différentes applications. Les mécanismes hypothétiques de l'activité antimicrobienne et de la réduction du 4-nitrophénol avec des diagrammes sont présentés dans cet article.
Des CuNPs avec différentes propriétés structurelles et effets biologiques efficaces peuvent être fabriqués à l'aide de nouveaux protocoles verts dans les prochains jours. Le contrôle de la taille des particules et, à leur tour, les propriétés dépendantes de la taille des CuNPs ouvriront les nouvelles portes de leurs applications. Cette étude donne un aperçu de la synthèse de CuNP à l'aide d'extraits de plantes, d'extraits microbiens et de biomolécules d'origine naturelle. Bien que tous ces protocoles verts pour la synthèse de CuNP aient leurs propres avantages et limites, l'utilisation d'extrait de plante comme réducteur est plus bénéfique que l'utilisation d'extrait microbien en raison du taux rapide de production de nanoparticules avec l'ancien réducteur vert.
Nanomatériaux
- Synthèse biogénique, caractérisation et évaluation du potentiel antibactérien de nanoparticules d'oxyde de cuivre contre Escherichia coli
- Synthèse facile et propriétés optiques de petits nanocristaux et nanotiges de sélénium
- Activité de préparation et d'hydrogénation catalytique améliorée des nanoparticules de Sb/Palygorskite (PAL)
- Synthèse verte à un pot de microsphères de SnO2 décorées d'Ag :un catalyseur efficace et réutilisable pour la réduction du 4-nitrophénol
- Synthèse facile de composite CuSCN coloré et conducteur revêtu de nanoparticules CuS
- Synthèse hydrothermale de nanoparticules d'In2O3 jumelles hybrides disque hexagonal hétérostructures ZnO pour des activités photocatalytiques et une stabilité améliorées
- Méthode de post-traitement pour la synthèse de nanoparticules binaires monodisperses FePt-Fe3O4
- Saponines de Platycodon de Platycodi Radix (Platycodon grandiflorum) pour la synthèse verte de nanoparticules d'or et d'argent
- Synthèse verte de nanoparticules de métal et d'oxyde métallique et leur effet sur l'algue unicellulaire Chlamydomonas reinhardtii



