Synthèse biogénique, caractérisation et évaluation du potentiel antibactérien de nanoparticules d'oxyde de cuivre contre Escherichia coli
Résumé
Le développement de la résistance aux antibiotiques utilisés pour traiter les infections bactériennes ainsi que la prévalence des résidus de médicaments posent des problèmes de santé publique importants à l'échelle mondiale. Les germes résistants aux antibiotiques entraînent des infections difficiles ou impossibles à traiter. La diminution de l'efficacité des antibiotiques nécessite le développement rapide d'antimicrobiens alternatifs. À cet égard, les nanoparticules (NP) d'oxyde de cuivre (CuO) manifestent une nanostructure inorganique latente et flexible avec un impact antimicrobien notable. La synthèse verte de CuO NPs a été réalisée dans la présente étude, qui a ensuite été dopée avec des quantités variables de gingembre (Zingiber officinale , ZO) et de l'ail (Allium sativum , AS) extraits. À faibles et à fortes doses, le composé synthétisé a été utilisé pour mesurer l'efficacité antimicrobienne contre les Escherichia coli pathogènes. . La présente recherche a démontré avec succès une technique de synthèse renouvelable et respectueuse de l'environnement avec des matériaux naturels qui est également applicable à d'autres NP d'oxydes métalliques verts.
Introduction
Les plantes indigènes à base de plantes et d'épices possèdent de précieuses propriétés antioxydantes et antibactériennes qui sont utilisées dans les traitements humains et vétérinaires [1]. Les plantes médicinales contenant des propriétés antimicrobiennes comprennent l'ail, le gingembre, le neem, le curcuma, le tulsi, etc. et parmi celles-ci, l'ail et le gingembre sont réputés pour leur usage médicinal [2]. Zingiber officinale communément appelé gingembre est une racine de plante indigène appartenant à la famille des Zingibéracées. Il contient du gingérol, du shogaol, de la curcumine et du paradol en tant que composés phytochimiques importants [3]. L'activité antimicrobienne contre un large éventail de microbes s'est manifestée par des extraits aqueux de gingembre, en raison de son contenu phénolique de nature thérapeutique [4]. Allium sativum communément appelé ail contient des composés phénoliques présentant une activité antibactérienne à large spectre même contre les bactéries MDR [5]. Allium sativum a présenté une activité antibactérienne à large spectre contre un certain nombre de bactéries Gram-positives et diverses bactéries Gram-négatives [6].
L'exploitation des connaissances de la nanotechnologie aux niveaux moléculaire et atomique sert de base à l'application d'une approche intégrative pour développer de nouveaux composés dotés de caractéristiques uniques à utiliser dans des applications à large spectre [7]. Les applications médicinales, agricoles, de conservation des aliments et cosmétiques des nanoparticules en raison de leurs propriétés inhérentes inégalées ont conduit à une exploration accrue par les chercheurs [8, 9]. Diverses applications biologiques des nanoparticules d'oxyde de cuivre ont été démontrées avec succès, notamment des antimicrobiens potentiels, des composés thérapeutiques efficaces, des vecteurs d'administration de médicaments, des photocatalyseurs, la détection de gaz, la stabilité photovoltaïque, l'effet de confinement quantique et des sondes biologiques [10,11,12,13,14]. La génération d'espèces réactives de l'oxygène (ROS) est déclenchée par les nanoparticules en raison de leur nature semi-conductrice, entraînant des transformations oxydatives et dégénératives au niveau cellulaire entraînant la destruction des parois cellulaires bactériennes et la libération du contenu cellulaire [15]. De nombreuses méthodes ont été pratiquées pour la synthèse de nanoparticules, c'est-à-dire la synthèse chimique, physique et biologique [16]. La réduction des composés métalliques conduit à la production de nanoparticules à l'aide de tout biochimique ou micro-organisme, de plantes ou de leurs extraits [17].
Escherichia coli (E. coli ), un habitant naturel de l'intestin et une partie de la flore intestinale, a une position particulière dans le monde microbiologique en raison de ses propriétés virulentes potentielles [18]. L'existence de la virulence dépend du nombre de gènes dans E. coli des isolats et, dans certains cas, un transfert horizontal de gènes de résistance ont également été révélés [19, 20], ce qui peut créer un problème de santé chez les êtres humains, les animaux [21] et un défi pour la sécurité sanitaire des aliments [22]. E. coli est l'agent causal de la mammite chez les vaches laitières et les buffles et s'est avéré responsable d'une baisse importante de la production laitière et des pertes économiques qui en résultent [23, 24], qui ont développé des gènes de résistance, c'est-à-dire des β-lactamases à spectre étendu (BLSE) ou céphalosporinases exprimées (AmpCs) [25]. Échec du traitement associé à E. coli les infections sont considérées comme une menace latente conduisant à une multirésistance aux médicaments à la fois en médecine humaine et vétérinaire [26].
Les nanoparticules avec leurs caractéristiques antimicrobiennes caractéristiques ont le potentiel de tuer environ 600 cellules, contrairement à la capacité des antibiotiques à traiter seulement quelques maladies d'origine infectieuse [27]. L'étude actuelle vise à explorer, évaluer et comparer le potentiel antimicrobien possible des nanoparticules de CuO vertes et synthétisées chimiquement et des extraits de racines d'herbes communes d'Allium sativum (AS) et Zingiber officinale (ZO), contre E. coli comme alternatives aux antibiotiques pour surmonter les défis émergents de la résistance.
Méthodes
La présente étude visait à étudier l'action bactéricide des NPs de CuO réduites phytochimiquement contre les racines des herbes d'Allium sativum (AS) et Zingiber officinale (ZO), un isolat de mammite bovine.
Matériaux
Les nanoparticules de CuO fabriquées chimiquement ont été achetées auprès de Sigma-Aldrich, tandis que les racines ZO et AS ont été achetées sur le marché local de fruits et légumes de Lahore, au Pakistan. Les racines de ZO et AS ont été séchées à l'ombre pour atteindre un poids uniforme. Milieu de croissance pour E. coli et des produits chimiques de qualité analytique ont été utilisés sans modification.
Extraction aqueuse des racines ZO et AS
Les racines séchées de ZO et AS ont été broyées ultrafines en poudres fines qui ont ensuite été stockées dans des bocaux hermétiques. Une agitation vigoureuse de 30 min à 70 °C pour le mélange de racines en poudre fine avec de l'eau distillée-DIW a été entreprise à un rapport de 1:10. La filtration des solutions préparées a été effectuée à l'aide du papier filtre Whatman n° 1 après refroidissement des solutions et le stockage du filtrat a été effectué à 4 °C pour l'expérience suivante [28] comme le montre la figure 1a.
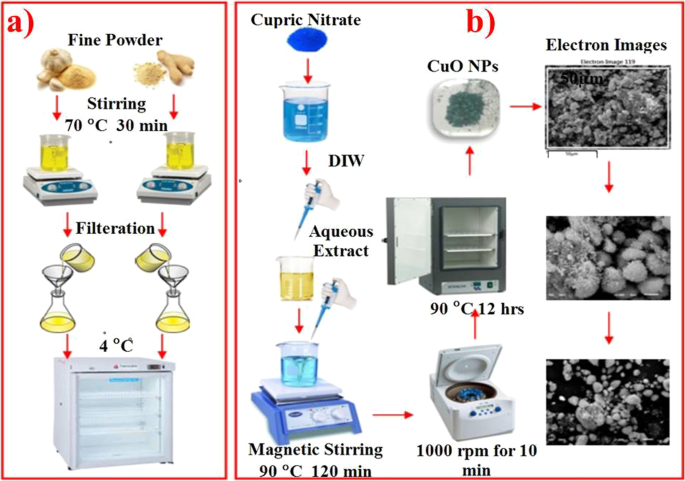
Présentation de a extraction aqueuse de Zingiber officinale et Allium sativum racines, b synthèse verte de CuO NPs
Synthèse verte de CuO
Du nitrate de cuivre tétrahydraté (0,1 M) a été mélangé avec différentes concentrations, c'est-à-dire 3 mL, 6 mL et 12 mL d'extraits de ZO et d'AS sous agitation continue. NaOH (2 M) a été utilisé pour maintenir le pH de 12 de la solution agitée pendant 2 h à 90 °C pour la formation de précipités. La centrifugation des précipités a été effectuée à 10 000 tr/min pendant 20 min, suivie d'un lavage à l'eau déminéralisée et d'un séchage d'une nuit dans un four à air chaud à 90 °C [29] comme le montre la figure 1b.
Caractérisation
Le spectrophotomètre UV-visible GENESYS-10S a été utilisé pour vérifier les spectres d'absorption des nanoparticules de CuO et des extraits aqueux de ZO et AS entre des longueurs d'onde comprises entre 200 et 500 nm [30]. L'analyse structurelle et de phase des CuO NPs a été réalisée à l'aide du Phaser BRUKER D2 par diffraction des rayons X (XRD) avec 2θ = (10°–80°) équipé d'un rayonnement Cu Kα de λ = 1.540 Å [31]. La spectroscopie infrarouge à transformée de Fourier (ATR-FTIR) a été réalisée pour l'analyse des groupes fonctionnels dans les CuO NPs et les extraits aqueux de ZO et AS [31]. La microscopie électronique à balayage (SEM JSM-6610LV) couplée à un détecteur EDS a été entreprise pour l'observation de la constitution élémentaire et morphologique des CuO NPs. Des images MET haute résolution et des modèles SAED ont été pris à l'aide du microscope JEOL JEM-2100F [32].
E. coli Isolement et identification
Collection d'échantillons
Des vaches et des buffles souffrant de mammite clinique ont été retracés et identifiés dans diverses fermes d'élevage pour la collecte d'échantillons de lait.
E. coli Isolement
La gélose MacConkey a été utilisée pour l'étalement et la culture du lait en triple pour l'isolement de colonies purifiées de E. coli [33]. Les diffusions sur disque de colonies distinctes de E. coli ont été évalués pour vérifier la sensibilité à des antibiotiques spécifiques en respectant les directives du National Committee for Clinical Laboratory Standards (NCCLS) pour isoler E. coli .
Identification de E. coli
Identification et confirmation de E. coli les colonies ont été réalisées sur la base de la coloration de Gram; distinguer les caractères morphologiques et les tests biochimiques, c'est-à-dire les tests au rouge de méthyle et à la catalase dans la perspective du Manuel de bactériologie systématique de Bergey. La culture des isolats sur gélose éosine bleu de méthylène (EMB) a été réalisée pour E. coli distinction et ratification des mastitogènes Gram-négatifs apparentés.
Évaluation du potentiel antibactérien in vitro des NP CuO contre E. coli
Un certain nombre d'expériences ont été réalisées pour évaluer in vitro potentiel antibactérien d'extraits dopés CuO NPs contre pathogènes E. coli . In vitro des essais ont été menés en utilisant 10 agents pathogènes représentatifs E. coli isolats pour l'évaluation du potentiel antibactérien des NPs CuO. L'évaluation de la méthode de diffusion sur disque a été utilisée pour évaluer in vitro potentiel antimicrobien. Des boîtes de Pétri ont été tamponnées avec une croissance activée de E. coli 1,5 × 108 UFC/mL (0,5 Mcfarland standard) sur gélose MacConkey [34]. Un perce-bouchon stérile a été utilisé pour préparer des puits de 6 mm de diamètre dans les boîtes de Pétri. Extraits aqueux de ZO et AS, ainsi que des extraits dopés au vert et des nanoparticules d'oxyde de cuivre synthétisées chimiquement à différentes concentrations, ont été appliqués dans des puits. Le potentiel antimicrobien des extraits aqueux de ZO et AS ainsi que des extraits dopés verts et des nanoparticules d'oxyde de cuivre synthétisés chimiquement a été évalué en incubant en aérobie les boîtes de Pétri à 37 °C pendant la nuit en mesurant les zones d'inhibition (mm) à l'aide d'un pied à coulisse. L'analyse statistique des zones d'inhibition (mm) a été réalisée en utilisant une ANOVA à un facteur et en visualisant (p < 0,05).
Résultats et discussion
La spectroscopie UV-Vis des NP de CuO dopées et des extraits aqueux de ZO et d'AS a été réalisée pour étudier le comportement optique, comme le montrent les Fig. 2a, b. Pour la formation ultérieure de NP CuO, un changement de couleur progressif du vin au noir de charbon a été remarqué tandis que l'optimisation des NP synthétisées au moyen d'extraits acoustiques voûtés a été entreprise. Des pics d'absorption des extraits aqueux ZO et AS à 275 et 280 nm ont été observés. Résultats illustrés λ max pour le CuO dopé ZO et AS à 250 nm représentant un rapport de 6 mL : 1 avec des décalages vers le rouge et vers le bleu caractéristiques, respectivement [35]. Les pics larges ont spécifié des amas de particules et la transition des électrons vers les bandes de conduction de la phase de valence avec des extraits concentrés dans CuO tels que divulgués par de fortes bandes d'absorption [36]. Dans les NP CuO synthétisées vertes, une absorption réduite a été observée en augmentant ou en réduisant le volume d'extrait en plus de la valeur optimisée (6 mL : 1).
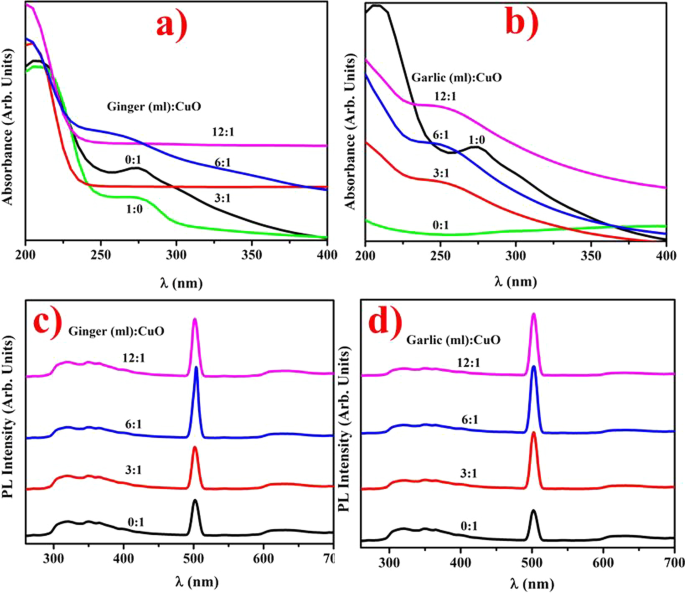
Spectres d'absorption de CuO NPs dopés avec a ZO b Extrait AS et spectres PL CuO NPs avec c ZO et d extraits AS, respectivement
De plus, il était remarquable d'observer que les structures semi-conductrices confirmaient leurs caractéristiques physiques aux effets de taille quantique nanométriques existants. Les spectres PL des NPs CuO dopées ZO et AS avec une longueur d'onde UV d'excitation de 300 nm sont présentés dans les Fig. 2c, d. Les trois pics d'émission à 418, 561 et 664 nm ont été représentés sur chaque graphique PL pur et dopé de CuO (région UV) [37]. Une bande de lumière violet-bleu trouvée à 418 nm est un pic d'émission CuO standard au bord de la bande proche [38, 39]. À 430 nm, le bord de l'épaule peut être dû à des lacunes de CuO, qui est un semi-conducteur de type p. Le bord vert jaunâtre est responsable des défauts de profondeur à basse température à 561 nm. Les pics d'émission rouge à 664 nm sont responsables de différentes conditions de cuivre ou de la présence de lacunes individuelles d'oxygène ionisé [40, 41]. L'existence diverse d'émissions visibles dans le spectre violet-bleu, jaune-vert et rouge indique que les particules de CuO étudiées ont un rapport volume-surface élevé et une multitude de conditions et de défauts surface-volume (lacunes ou interstitiels) qui produisent plages piège-émission [40, 42].
La XRD a été réalisée pour évaluer la structure cristalline, la composition et l'échelle des CuO NPs comme présenté sur la Fig. 3a, d dopé avec ZO et AS, respectivement. L'augmentation de la cristallinité a été démontrée par des pics détectés à 2θ = 38,7°, 48,6°, 53,5°, 58,3°, 61,7° et 66,2° avec les plans cristallins correspondants (111), (−202), (020), (202), (−113) et (022), respectivement. Les pics détectés assuraient la présence de la phase monoclinique CuO synchronisée avec la carte JCPDS n° 00-002-1040 [43]. La taille caractéristique des cristallites mesurée à l'aide de D = 0.9λ /β cosθ s'est avéré être de 24,7 et 47,6 nm pour le CuO dopé au ZO et à l'AS, respectivement, et la taille des cristallites de l'échantillon vierge était de 27,4 nm. Plusieurs produits naturels ont été identifiés comme agents de coiffage et de réduction de la taille moyenne des cristallites dans les extraits AS et ZO [44].
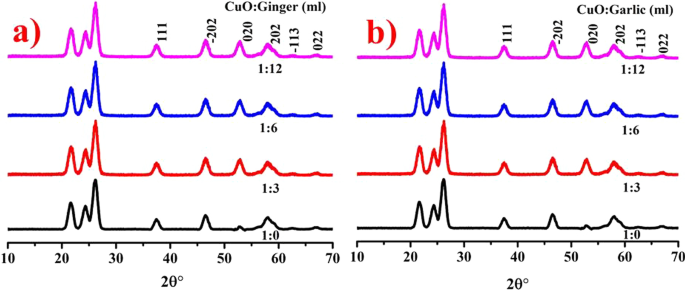
Modèles XRD de CuO NPs sans et avec dopage de a AS b ZO
Des groupes fonctionnels de NPs CuO dopées à l'extrait d'AS et de ZO ont été examinés par FTIR comme illustré sur les Fig. 4a, b, de manière correspondante. Le large pic à 3314 cm −1 a confirmé la présence d'un groupe hydroxyle et l'amplitude du pic représente un C =O direct avec des amines (N-H) [45]. Le pic intense à 1638 cm −1 correspond à CH2 –OCH3 groupe existant dans 6-snogal et 6-gingerol de ZO comme trouvé une réduction substantielle de CuO. Les liaisons simples typiques de Cu–O observées à 478,8 cm −1 en torsion étaient dues à de forts modes de vibration [46]. Tous les pics suggèrent que les groupes alcool, amine et cétone ont entraîné la chélation et le coiffage des flavonoïdes, des substances chimiques végétales et des protéines [47].
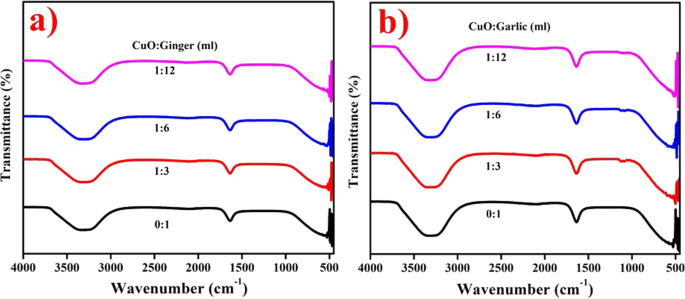
Spectres FTIR de a AS b NPs CuO dopées ZO
Le FE-SEM a été utilisé pour étudier les caractéristiques de surface et l'échelle des NP de CuO dopées avec de l'extrait de ZO et d'AS, comme le montre la figure 5a–d′. Les images FE-SEM montrent que les CuO NPs sont extrêmement agglomérées en morphologie sphérique. Les interférences magnétiques et la conformité des polymères entre les particules peuvent montrer une agglomération entre les particules [48]. Le dopage ZO et AS avec CuO était évident sur les images montrant la formation d'amas et la taille des particules semble < 1 μm, comme illustré sur la Fig. 5b–d′.

Images CuO NPs prises avec FESEM a CuO, b –d CuO dopé ZO et b′ –d′ NPs CuO dopées AS, respectivement
La spectroscopie à rayons X à dispersion d'énergie (EDS) a illustré la composition chimique avec une étude élémentaire d'échantillons vierges et de NPs CuO dopées avec des extraits de racines ZO et AS par des phases CuO invétérées, comme le montre la figure 6a–d′. Trois pics correspondant à la haute pureté du Cu confirmée par EDS des échantillons testés en comparaison avec l'oxygène précurseur entre 1 et 10 keV. La résonance plasmonique de surface (SPR) des CuO NPs a entraîné des pics d'absorption [49]. 83,7%, 15,2% et 0,6% ont été observés pour le poids atomique à travers les spectres de Cu, O et Ca, respectivement, pour l'échantillon de contrôle tandis que 82,8%, 14,8% et 2,4% pour l'échantillon dopé au ZO et optimisé (6 mL :1) observés à travers des spectres pour Cu, O et Zn, respectivement. De même, 65,3, 29,6 et 4,6 pour Cu, O et S avec dopage AS ont été trouvés, respectivement. Les composés atomiques supplémentaires apparaissant dans l'EDS ont répondu au porte-échantillon SEM utilisé lors de l'analyse [50].
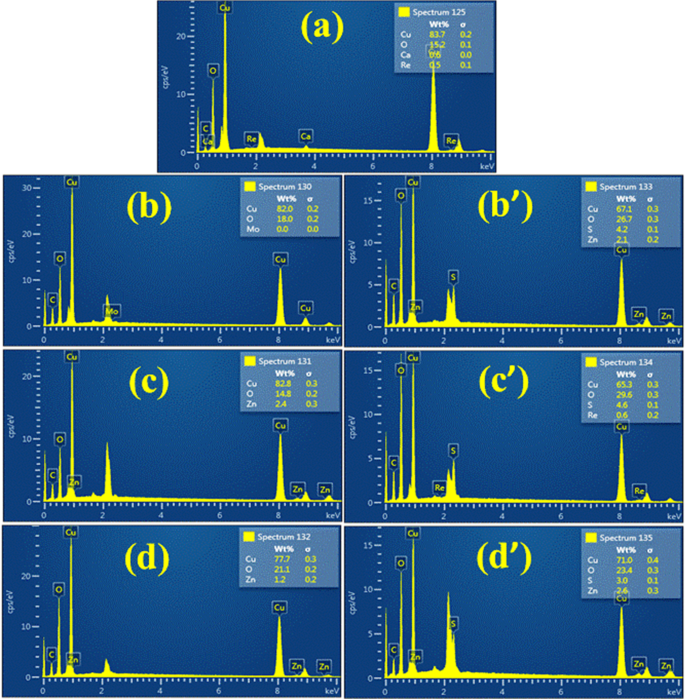
Spectres EDS de CuO NPs a CuO pur b –d CuO dopé ZO et b′ –d′ NPs CuO dopées AS, respectivement
La structure exclusive et caractéristique des CuO NPs a été évaluée en utilisant HR-TEM à 50 nm, comme le montre la figure 7a–l. Les images HR-TEM ont révélé des nanoparticules ornées similaires aux images FE-SEM, ainsi qu'une agglomération plus élevée avec une taille mesurant moins de 50 nm. La présence de composés phytochimiques dans les NP de CuO dopées ZO et AS a également été confirmée par des images HR-TEM [51]. Ni aucune imperfection ni aucune déformation n'a été observée dans la structure en treillis intégral des NPs CuO dopées ZO et AS [52]. Les micrographies filtrées ont été présentées par les résultats HR-TEM avec la transformée de Fourier rapide [FFT] de la zone spécifiée représentée par un carré jaune sur les Fig. 7b, d, f, h, j, l présentant des caractéristiques structurelles et atomiques à haute résolution. Les dimensions particulaires moyennes HR-TEM sont précisément adaptées aux tailles de cristallites observées lors de l'analyse XRD et SEM [53].
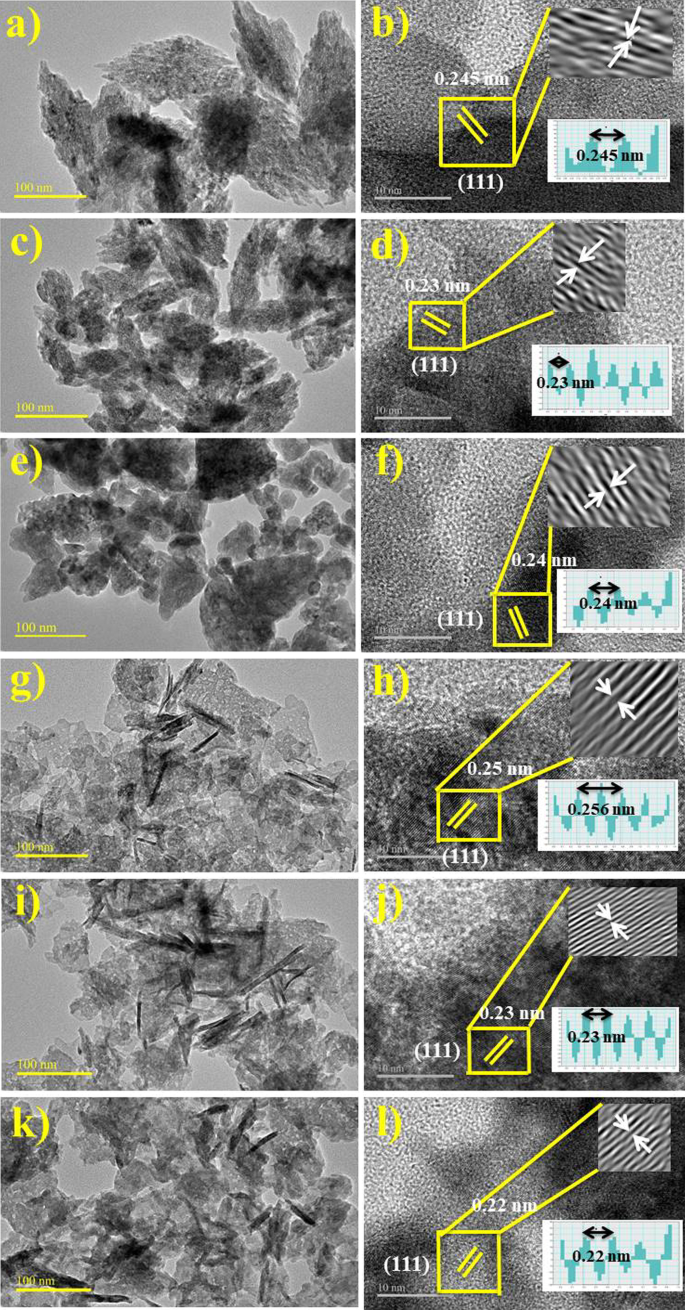
un , b RH-TEM, a –f franges en treillis de 3 mL, 6 mL et 12 mL de CuO dopé ZO g –l franges de réseau de 3 mL, 6 mL et 12 mL de NP CuO dopées AS, respectivement
L'analyse XPS de CuO dopé avec Gi et Ga CAE représentant C 1s et Cu 2p le spectre est illustré à la Fig. 8a, b. Les C1s la plage indique la présence de quatre pics distincts Fig. 8a avec des groupes fonctionnels distinctifs comme C(H,C) (284,39 eV), C(N) (285,6 eV), C(O,=N) (287,0 eV) et C–O –C (288,75 eV) [54,55,56]. Principalement, la figure 8b représente Cu 2p motif de CuO dopé avec des pics à 933,3 et 953,3 eV d'énergies de liaison correspondant à Cu 2p 3/2 et Cu 2p 1/2 l'orbite de rotation indique l'état d'oxydation divalent de l'échantillon préparé. Les pics pertinents à 942,2 et 962 eV se rapportent aux pics satellites de Cu 2p 3/2 et Cu 2p 1/2 qui semblait principalement dû à un 3d partiellement rempli 9 orbitale à l'état d'oxydation divalent [57].
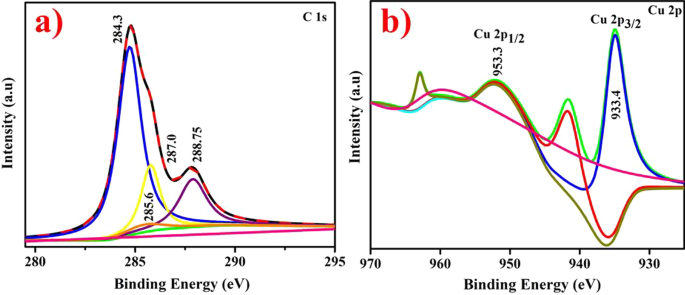
un , b Analyse XPS des NPs CuO dopées a C1s b Cu 2p
La méthode de diffusion par puits a été appliquée pour l'évaluation du potentiel bactéricide des extraits aqueux de ZO et d'AS et des NP de CuO synthétisées en mesurant les zones d'inhibition après incubation des plaques de Pétri pendant 24 h, comme indiqué sur la Fig. 9a–d, Fichier supplémentaire 1 :Fig. S1 et tabulés dans le tableau 1. Les résultats ont révélé que la concentration de NP et les zones d'inhibition répondaient de manière synergique. Les zones d'inhibition significatives trouvées pour l'échantillon 1 (3 mL :1), l'échantillon 2 (6 mL :1) et l'échantillon 3 (12 mL :1) étaient (1,05–1,85 mm) et (1,85–2,30 mm) en utilisant une diminution (↓) et des concentrations accrues (↑), respectivement, pour les nanoparticules de CuO dopées au ZO (p < 0,05), Fig. 9a. De même, les NP dopées à l'AS présentaient des zones d'inhibition (0,65 à 1,00 mm) à la concentration maximale uniquement, Fig. 9b. Les NP dopées AS ont démontré une efficacité nulle contre E. coli à des concentrations minimales. L'extrait de ZO a représenté l'effet à une concentration diminuée (↓) par rapport à une concentration augmentée (↑) montrant une zone de 1,55 mm, de même, aucun effet antibactérien des extraits d'AS n'a été trouvé à la fois à des concentrations diminuées (↓) et augmentées (↑). Le contrôle positif traité avec la ciprofloxacine présentait une zone de 4,25 mm tandis que le contrôle négatif traité avec DIW présentait 0 mm. Le pourcentage d'efficacité bactéricide a été augmenté de 24,7 à 43,5 % et de 43,5 à 54,1 % pour les NP dopées au ZO à des concentrations minimales et maximales, respectivement (Fig. 9c). De même, une efficacité de 15,3 à 23,5 % n'a été obtenue à la concentration maximale que pour les NP dopées AS (Fig. 9d). En résumé, CuO dopé à l'extrait de ZO et optimisé à 6 mL :1 a manifesté un potentiel bactéricide plus élevé contre E pathogène. coli d'origine mammite bovine (p < 0.05) comme indiqué dans la Fig. 9a, b.
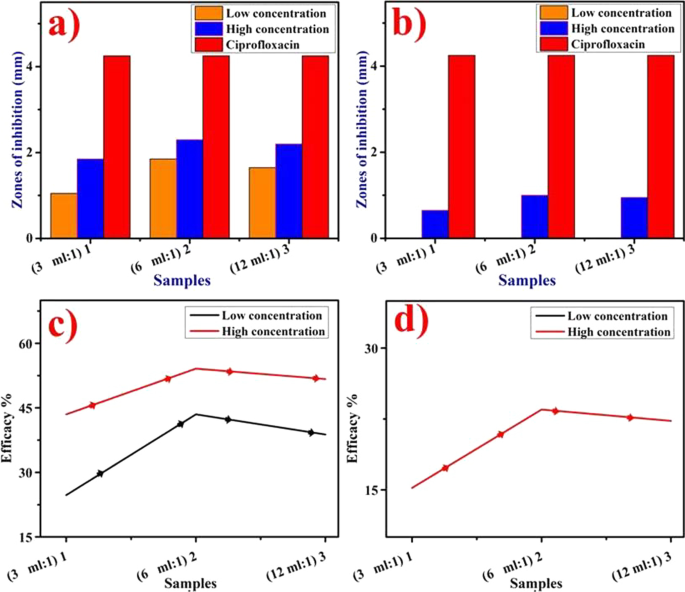
un –d Activité antibactérienne in vitro des CuO NPs a dopé au ZO à ↓ et dose, b dopé avec AS à ↓ et doses, respectivement, c %age d'efficacité dopé au ZO et d % d'efficacité dopé à l'AS
Le potentiel bactéricide des nanoparticules dépend de la taille des NP, de la structure morphologique et du rapport surface-masse. Les espèces réactives de l'oxygène (ROS) seraient responsables de la formation de zones d'inhibition par les nanoparticules de CuO [58, 59]. La dénaturation des protéines cellulaires résulte de la génération d'espèces réactives de l'oxygène (ROS) néfastes [60]. Certaines espèces réactives ont montré des rôles importants dans la photocatalyse tels que les radicaux hydroxyle et superoxyde et les trous [61]. La synthèse d'espèces réactives de l'oxygène (ROS) et la libération d'ions métalliques sont les principales caractéristiques manifestant les changements structurels des enzymes et des protéines, entraînant des dommages irréparables à l'ADN et la mort bactérienne subséquente [62]. De même, le stress oxydatif produit par les espèces réactives de l'oxygène (ROS) est considéré comme le principal contributeur à la photocatalyse [63]. La production de ROS est inversement proportionnelle à la taille des nanoparticules, c'est-à-dire que plus la taille des nanoparticules est petite, plus la production de ROS est élevée, ce qui endommage par conséquent la membrane bactérienne, entraînant l'extrusion du contenu cytoplasmique et la dégradation de l'ADN conduisant à une explosion bactérienne, comme le montre la figure 10. Dans le même temps, le Cu chargé positivement interagit électrostatiquement avec la membrane bactérienne chargée négativement, entraînant la désintégration cellulaire et finalement la destruction bactérienne [58, 64, 65]. Deux réponses ont été proposées comme potentiel pour le mécanisme bactéricide des nanostructures. L'un implique une meilleure liaison entre les cations Cu 2+ et des cellules bactériennes, conduisant à la formation de sections négativées et à un éventuel effondrement. L'autre implique l'excitation électronique de la surface de la bande de cantonnière CuO via l'excitation. De plus, l'O2 électrique la réaction produit O 2− radicaux, conduisant à la formation de H2 O2 . Le O 2− généré espèces sont essentielles à la dégradation des molécules lipidiques ou protéiques sur la membrane cellulaire extérieure des bactéries [58, 66].
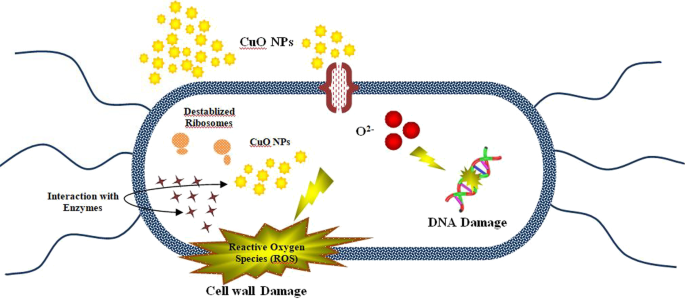
Illustration de l'action bactéricide des CuO NPs
Conclusions
Potentiel bactéricide des NPs CuO dopées au Zingiber officinale et Allium sativum extraits contre E. coli a été évalué dans cette étude, produite dans le but d'antimicrobiens alternatifs, économiques et efficaces. Le rôle important des ingrédients phytochimiques des extraits de ZO et d'AS a été révélé dans la synthèse biogénique des NP de CuO, tandis que les effets synergiques des flavonoïdes avec CuO se sont révélés dépendants de la concentration en exploitant le potentiel bactéricide contre E pathogène. coli . La FTIR a été réalisée pour confirmer le dopage des extraits ZO et AS et les pics XRD ont confirmé la phase monoclinique et la structure sphérique avec des tailles moyennes de 24,7 nm (dopé ZO) et 47,6 nm (dopé AS). La morphologie sphérique a été confirmée avec des images FESEM ainsi qu'un conglomérat exorbitant de CuO NPs. Les nanoparticules embellies ont révélé une agglomération plus élevée dans les images MET avec une taille inférieure à 50 nm. Pour les échantillons dopés avec des extraits de racines, l'espacement intercouche des nanoparticules de CuO mesuré à 0,23 nm s'est avéré compatible avec les modèles XRD. Les résultats de cette étude suggèrent que le potentiel antibactérien des NP CuO synthétisées vertes peut être anticipé en tant qu'agents bactéricides alternatifs pour résoudre les problèmes liés à la résistance et aux résidus d'antibiotiques. On peut conclure que les CuO NP dopées avec des herbes indigènes sont des agents antibactériens économiques, efficaces et respectueux de la nature.
Disponibilité des données et des matériaux
Toutes les données sont entièrement disponibles sans restriction.
Abréviations
- EDS :
-
Spectroscopie à rayons X à dispersion d'énergie
- fcc :
-
Cube à faces centrées
- FTIR :
-
Spectroscopie infrarouge à transformée de Fourier
- G + ve :
-
Gram positif
- G −ve :
-
Gram négatif
- JCPDS :
-
Comité mixte sur les étalons de diffraction des poudres
- CuO :
-
Oxyde de cuivre
- nm :
-
Nanomètre
Nanomatériaux
- Élimination par adsorption des ions cuivre (II) d'une solution aqueuse à l'aide d'un nano-adsorbant de magnétite à partir de déchets de broyage :synthèse, caractérisation, adsorption et modél…
- Synthèse facile et propriétés optiques de petits nanocristaux et nanotiges de sélénium
- Synthèse facile de composite CuSCN coloré et conducteur revêtu de nanoparticules CuS
- Biosécurité et capacité antibactérienne du graphène et de l'oxyde de graphène in vitro et in vivo
- Propriétés de synthèse et de luminescence des nanoparticules hydrosolubles α-NaGdF4/β-NaYF4:Yb,Er Core–Shell
- Activité de synthèse et d'oxydation du CO des catalyseurs d'or pris en charge par l'oxyde binaire mixte 1D CeO2-LaO x
- Aptitude verte dans la synthèse et la stabilisation des nanoparticules de cuivre :activités catalytiques, antibactériennes, cytotoxiques et antioxydantes
- Synthèse et caractérisation de nanostructures de cuivre pur en utilisant l'architecture inhérente au bois comme modèle naturel
- Les nanoparticules d'oxohydroxyde de cuivre dopé au ligand sont des antimicrobiens efficaces



