Vert synthétisé par phytochimie (Zingiber officinale et Allium sativum) Réduction des nanoparticules d'oxyde de nickel à potentiel bactéricide et catalytique confirmé
Résumé
Les nanoparticules phyto-synthétisées (NP) ayant une toxicité chimique réduite ont été focalisées à l'échelle mondiale et sont récemment devenues une composante essentielle de la nanotechnologie. Nous avons préparé des NiO-NPs verts réduits phytochimiquement (gingembre et ail) pour remplacer un agent bactéricide et catalytique synthétique dans l'industrie textile. Les NP ont été caractérisées à l'aide de la spectroscopie visible ultraviolette (UV-Vis), de la diffraction des rayons X (XRD), de la spectroscopie photoélectronique aux rayons X (XPS), de la spectroscopie infrarouge à transformée de Fourier (FTIR), de la spectroscopie à dispersion d'énergie (EDS). ), la microscopie électronique à balayage (MEB) et la microscopie électronique à transmission (MET). La synthèse des NP a été confirmée par XRD et UV-Vis ayant une forte absorption à 350 nm avec une taille comprise entre 16-52 nm pour le gingembre et 11-59 nm pour l'ail. La microscopie électronique à balayage et à transmission a confirmé le pléomorphisme avec des NP de forme cubique et plus sphérique. De plus, les quantités exactes d'extraits d'ail et de gingembre (1:3,6 ml) incorporés pour synthétiser les NiO-NPs ont été confirmées avec succès par FTIR. Les NPs phytochimiquement réduites par l'ail ont présenté une activité bactéricide améliorée contre Staphylococcus aureus multirésistant aux médicaments à des concentrations croissantes (0,5, 1,0 mg/50 μl) et a également dégradé efficacement le colorant bleu de méthylène (MB). En conclusion, les NiO-NP de synthèse verte sont des activistes imminents pour résoudre la résistance aux médicaments ainsi qu'un agent catalytique respectueux de l'environnement qui peut être choisi à l'échelle industrielle.
Introduction
La nanotechnologie influence la matière avec au moins une dimension de 1 à 100 nm qui permet de concevoir des matériaux en contrôlant leur taille [17]. Les NP en raison de leurs propriétés chimiques, physiques et biologiques uniques dans divers domaines, y compris la médecine, ont suscité une grande attention. Leurs propriétés peuvent être facilement modifiées en changeant de taille à l'échelle nanométrique [47].
Les nanoparticules de nickel (Ni) et d'oxyde de nickel (NiO) ont une grande importance en raison de leurs propriétés magnétiques, catalytiques et électroniques particulières dans la technologie énergétique, le magnétisme, la biomédecine et l'électronique [9, 26, 35]. NiO avec une large bande interdite de 3,6 à 4,0 eV et une structure en réseau cubique a un potentiel dû au semi-conducteur de type p. Ces NP ayant une stabilité chimique élevée, des propriétés de supercapacité, une capacité de transfert d'électrons et une électrocatalyse sont utilisées en biomédecine et dans les activités photocatalytiques, anti-inflammatoires et antibactériennes [8, 10, 11, 45]. L'émergence de maladies infectieuses, en particulier résistantes aux antibiotiques (MDR), a dévasté la santé publique dans le monde entier. En règle générale, les souches bactériennes pathogènes à Gram positif (G + ve) et à Gram négatif (G - ve) font partie des principales menaces pour la santé publique.
Dans l'industrie laitière, la mammite bovine est une maladie problématique majeure ayant un grand impact économique caractérisé par des changements chimiques, microbiologiques et physiques dans le lait, tandis que des changements pathologiques dans les tissus glandulaires du pis [6, 19]. L'étiologie de la mammite comprend les agents infectieux, c'est-à-dire les bactéries, les virus et les champignons et les plus importants sont les bactéries, divisés en deux groupes :principaux (Streptocoques, Staphylococcus aureus , Corynebacterium pyogenes , et Coliformes ) et des agents pathogènes mineurs (Corynebacterium bovis et staphylocoques à coagulase négative ) [25]. L'émergence de multiples souches bactériennes Gram-positives et Gram-négatives résistantes aux médicaments constitue une menace importante pour la santé publique [23, 32].
Zingiber officinale (gingembre) est un ingrédient important de l'Ayurvedia et de l'Unani, et la phytothérapie chinoise est traitée pour diverses affections telles que les antinausées, l'aide digestive, les rhumatismes et les troubles de la coagulation en raison de la grande diversité d'huiles volatiles comme le zingibérol, le monoterpène, le sesquiterpène et hydrocarbures sesquiterpéniques [12, 13, 43]. Cependant, Allium sativum (l'ail) contient des composants organo-soufres, c'est-à-dire des groupes sulfure d'allyle, de l'alliine, de l'ajoène, de l'allyl cystéine et de l'allicine, et d'autres tels que des vitamines, des phospholipides, des flavonoïdes, des acides aminés et des acides gras qui orientent ses propriétés médicales [14, 24] . Notre objectif était d'évaluer l'action bactéricide des NP d'oxydes métalliques Ni réduits phytochimiquement contre le MDR (S. aureus ), un isolat de mammite bovine, et ce sera le premier rapport du Pakistan dans le domaine de la recherche vétérinaire sur l'agent mentionné ci-dessus.
Méthodes
La présente étude visait à étudier l'action bactéricide des NiO-NPs phytochimiquement réduits contre MDR (S. aureus ), un isolat de mammite bovine.
Matériaux
Nitrate de nickel [Ni(NO3 )2 ], hydroxyde de sodium (NaOH), bleu de méthylène (MB) et borohydrure de sodium (NaBH4 ) de qualité analytique ont été achetés auprès de Sigma-Aldrich®, et des racines fraîches de gingembre et d'ail ont été collectées sur le marché local. Les racines ont été séchées à l'ombre pour obtenir un poids constant pour un traitement ultérieur. Les disques antibiotiques ont été achetés chez Bioanalyse® (Turquie). Les milieux de croissance bactérienne utilisés étaient de qualité analytique par TM Media (Titan Biotech Ltd, Inde).
Préparation d'extraits aqueux
Les racines de gingembre et d'ail ont été réduites en poussière fine à l'aide d'un broyeur électrique et conservées dans des récipients en plastique. La poudre de racine broyée a été mélangée avec une quantité contrôlée d'eau distillée-DIW (1:10) sous agitation vigoureuse à 70 ° C pendant 30 min. Les extraits ont été refroidis, filtrés par du papier filtre Whatman n°1 et conservés à 4 °C (Fig. 1) jusqu'à une utilisation ultérieure.
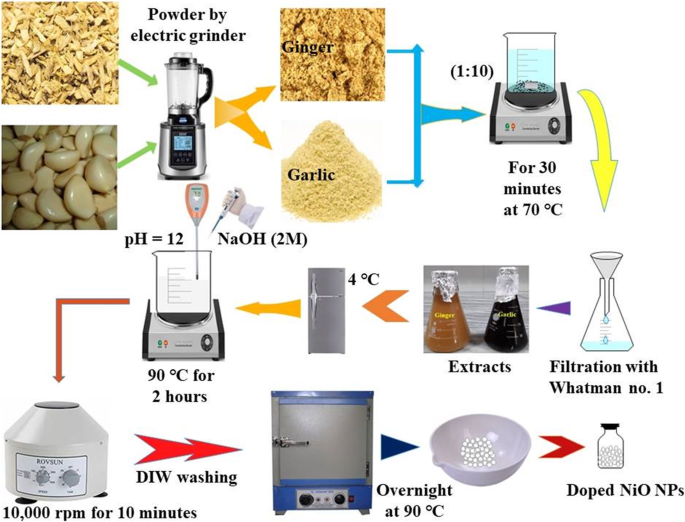
Schéma de synthèse d'extraction du gingembre et de l'ail et des NiO-NPs phytochimiquement réduits
Synthèse verte de NiO-NPs
Des extraits aqueux de gingembre et d'ail de divers rapports (1,2, 1,8, 2,4, 3,0, 3,6 et 4,2 ml) ont été ajoutés à du nitrate de nickel (0,1 M) sous agitation continue. La solution agitée pH 12 a été maintenue en utilisant NaOH (2 M) à 90 °C pendant 2 h. Les précipités formés ont été centrifugés à 10 000 rpm pendant 10 min, lavés avec DIW, et ont été séchés pendant une nuit dans un four à air chaud à 90 °C illustré à la Fig. 1.
Caractérisation
Absorption maximale (ƛ max ) des NPs synthétisées ont été scannées par un spectrophotomètre UV-Visible (Genesys 10 S) à partir de longueurs d'onde de 200 à 800 nm. La composition de phase et les informations structurelles ont été analysées par diffraction des rayons X (XRD) BUNKER D2 phaser ayant une plage de 2θ de (10–80°) équipé de rayonnements Cu Kα1 de λ =1,540 . Les groupes fonctionnels NiO-NP synthétisés en vert ont été enregistrés en utilisant la spectroscopie infrarouge à transformée de Fourier (ATR-FTIR). La taille, la forme et l'analyse élémentaire des NP ont été analysées au microscope électronique à émission de champ (FESEM) et au microscope électronique à transmission Hitachi H7100FA (TEM). La composition de l'échantillon avec les bandes interdites correspondantes a été étudiée par spectroscopie photoélectronique à rayons X (XPS).
Isolement et identification des MDR S. aureus
Isolement de S. aureus
Des échantillons de lait de bovin cliniquement positifs collectés dans des hôpitaux et des fermes vétérinaires des secteurs privé et public du Pendjab, au Pakistan, ont été cultivés sur de la gélose au sang de mouton à 5 % et incubés à 37 °C pendant 24 à 48 h. Les colonies caractéristiques obtenues ont encore été striées sur gélose au sel de mannitol (MSA) TM Media (Titan Biotech Ltd, Inde) en triplets pour isoler du S. aureus .
Identification du MDR S. aureus
L'identification des colonies bactériennes a été effectuée à l'aide de caractéristiques morphologiques, de coloration de Gram et de procédures biochimiques (test de la coagulase et de la catalase) conformément à la description du manuel de bactériologie déterminante de Burgey.
La sensibilité aux antibiotiques des colonies caractéristiques a été évaluée par un test de diffusion sur disque basé sur les directives du Comité national des normes de laboratoire clinique (NCCLS) pour l'isolement de MDR S. aureus . Disques antibiotiques contenant de l'oxytétracycline (30 g), de la tylosine (30 g), de la gentamicine (10 g), de la ciprofloxacine (5 g) et du triméthoprime + sulfaméthoxazole (1,25 g + 23,75 g) appliqués de manière aseptique sur une gélose Mueller-Hinton (MHA) TM (Titan Biotech Ltd, Inde)1 × 10 8 Les UFC/ml ont été maintenues à 37 °C pendant 24 h [7]. La bactérie trouvée résistante à au moins trois antibiotiques a été déclarée MDR [28].
Activité antimicrobienne
Le potentiel d'action antimicrobienne in vitro des NiO-NPs phytochimiquement réduits a été évalué par la méthode de diffusion de puits d'agar sur dix isolats représentatifs de MDR S. aureus collecté à partir de lait mastitique. Les boîtes de Pétri ont été tamponnées avec 1,5 × 10 8 UFC/ml (standard de 0,5 McFarland) MDR S. aureus sur MSA. Des puits de 6 mm de diamètre ont été formés à l'aide d'un perce-bouchon stérile. Diverses concentrations d'extraits aqueux individuels de gingembre, d'ail et de vert synthétisé (phytochimiquement réduit) NiO-NPs ont été appliquées. Des extraits aqueux ont été utilisés à des concentrations de (10 mg/100 μl) et (50 mg/100 μl) et NiO (0,5 mg/50 μl) et (1,0 mg/50 μl). La ciprofloxacine (0,005 mg/50 μl) a été utilisée comme contrôle positif et DIW comme contrôle négatif (50 μl).
Analyse statistique
L'efficacité antimicrobienne a été calculée en termes de taille de la zone d'inhibition (mm) et les diamètres de la zone d'inhibition ont été analysés statistiquement par analyse unidirectionnelle de la variance (ANOVA) à l'aide de SPSS 20.
Catalyse
Pour l'évaluation catalytique de l'extrait synthétisé NiO, du borohydrure de sodium aqueux fraîchement préparé (300 μl) a été mélangé avec 3 ml de bleu de méthylène (0. 03 × 10 −3 M) solution. Par la suite, 300 l d'échantillon colloïdal de concentration souhaitée ont été ajoutés aux solutions. La couleur bleu clair du colorant bleu de méthylène (MB) a disparu, ce qui représente la dégradation du colorant en bleu de leucométhylène, comme le montre la figure 2. L'absorption a été notée entre 200 et 800 nm à l'aide d'un spectrophotomètre UV-Vis.
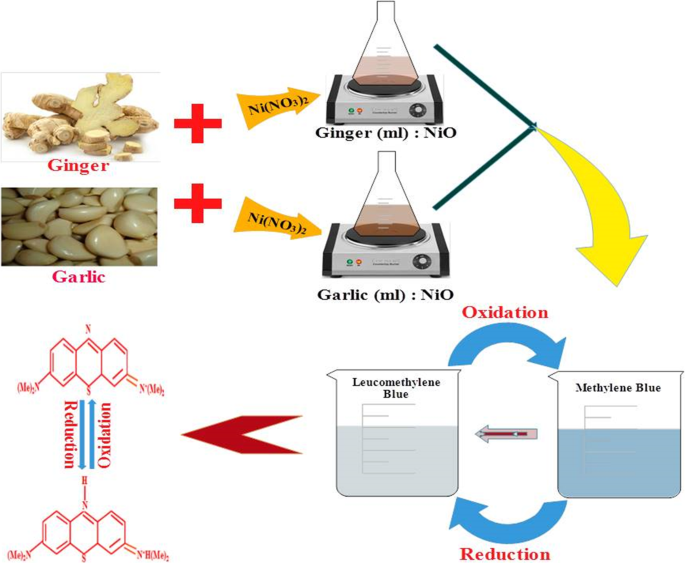
Schéma de principe pour la réduction catalytique de MB en LMB par des NPs synthétisées vertes
Résultats et discussion
Les propriétés optiques du NiO phytochimiquement réduit par les extraits aqueux de gingembre et d'ail entre 200 et 600 nm sont présentées dans les figures 3a, b. L'absorbance maximale (λ max ) dans NiO-NPs a été observée autour de 350 nm (1:3,6 ml) qui augmentait avec la concentration des extraits accompagnée d'un décalage vers le bleu. Les pics d'absorption des extraits de gingembre et d'ail sont apparus respectivement vers 275 et 280 nm. Un changement brusque de couleur dans les mélanges réactionnels a été observé du rouge vin au vert clair après incorporation d'extraits de racines. La largeur du pic indiquait l'agglomération des particules et la transition électronique des bandes de valence aux bandes de conduction avec une concentration d'extrait en NiO révélée par de fortes bandes d'absorption [20]. Par conséquent, sur la figure 3a, les résultats b ont montré une diminution de l'absorption des NP synthétisées avec une augmentation ou une diminution du volume d'extrait au-delà de la valeur optimisée (1 : 3,6 ml). La bande interdite a été calculée en utilisant le tracé de Tauc (Eq. 1).
$$ \left(\alpha hv\right)=B{\left( hv-{E}_g\right)}^{\raisebox{1ex}{$1$}\!\left/ \!\raisebox{-1ex }{$2$}\right.} $$ (1)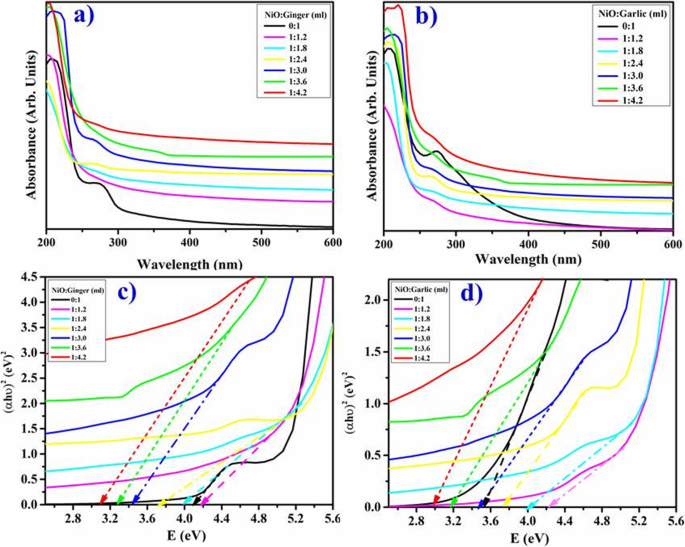
un –d Spectres d'absorption des NiO-NPs synthétisés verts avec du gingembre (a ) et extrait d'ail (b ). Bande interdite de NiO réduit phytochimiquement par le gingembre (c ) et l'ail (d ) respectivement
Où α est le coefficient d'absorption, h est la constante de Planck, B est une constante, υ est connue sous le nom de fréquence photonique, et E g est la bande interdite énergétique. La bande interdite estimée de NiO phytochimiquement réduit par le gingembre et l'ail à partir d'une parcelle de (αhʋ ) 1/2 contre l'énergie photonique (hʋ ). L'interception d'une tangente à x -axe a été enregistré, ce qui fournit les énergies de bande interdite des échantillons comme indiqué sur les Fig. 3c, d. Les variations des énergies de bande interdite ont été déterminées lors du dopage du gingembre dans NiO de 4,15 à 3,1 eV et avec de l'ail de 3,5 à 3,0 eV respectivement (Fig. 3c, d).
La cristallinité, la taille et la composition de phase des NiO-NPs ont été confirmées par XRD, comme le montrent les figures 4 a, b. Les pics aux valeurs 2θ 37,10°, 43,32°, 62,81° et 76,51° correspondent à (111), (200), (220) et (311) (carte JCPDS n° :00-047-1049) (Fig. 4a , b) référencé par [30]. L'intensité maximale indique un NiO cubique hexagonal et centré (fcc) avec une taille moyenne de 32,9 nm calculée par D =0,9λ/βcosθ pour le gingembre et 29,92 nm pour l'ail NiO-NPs phytochimiquement réduits. Les pics larges indiquent la présence d'espaces d'oxygène et d'un trouble local du réseau dans l'échantillon [38]. Divers composés phytochimiques du gingembre (flavonoïdes, alcaloïdes, tanins et saponines) et d'extraits aqueux d'ail (allicine, sulfure d'allyle, alliine, acides gras, glycolipides, phénoliques, acides aminés et flavonoïdes) agissant comme agents de coiffage sont responsables de la taille moyenne des cristallites de oxydes métalliques NPs [14, 46].
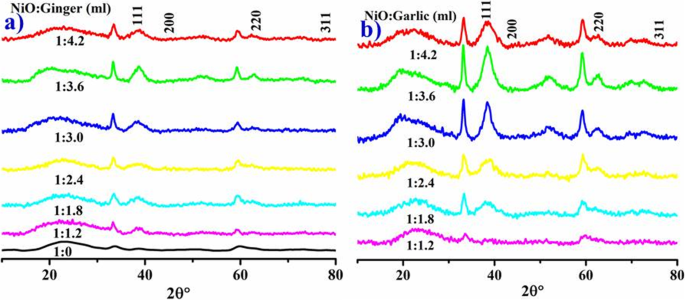
Schéma XRD de différentes concentrations de NiO réduit phytochimiquement par le gingembre (a ) et l'ail (b ) et NiO standard (c )
Les spectres FTIR enregistrés de NiO biosynthétisé à partir de racines de gingembre et d'ail sont illustrés à la figure 5 a, b. Absorption large élaborée à 3380 cm −1 correspondent à OH et la largeur du pic indique un groupe carbonyle avec une fréquence d'étirement de l'amine (N-H) [50]. La forte absorption à 2313 cm −1 indique des vibrations d'étirement de CO2 soit aérienne ou CO2 à l'intérieur des grains NP. Absorption rapide du CO atmosphérique2 indique une plus grande surface de matériau [18]. La large absorption à 1629 cm −1 correspondent à l'étirement du cycle aromatique C=C et à des pics nets à 1392 et 1064 cm −1 correspondent à des vibrations d'étirement des amines aliphatiques C–N [48]. Les pics intenses à 978 cm −1 fréquence confirmée d'étirement de l'oxygène métallique de NiO [44].
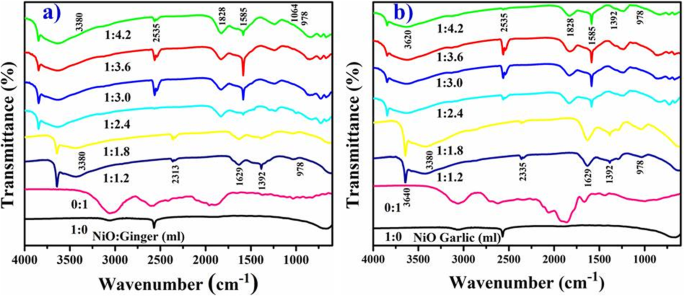
Spectres FTIR avec extrait de gingembre en NiO (a ) et l'ail (b )
Les pics de décalage observés après la bio-réduction de NiO sont de 2535–2313, 1828–1629 et 1585–1392 cm −1 indiquent des composés phytochimiques, des terpénoïdes, des flavonoïdes, des polyols et des protéines ayant des groupes fonctionnels cétones, alcools, acide carboxylique et amines responsables de la chélation et du coiffage dans la bio-réduction [42].
La morphologie de surface et la taille des NiO-NPs réduits phytochimiquement ont été déterminées en utilisant la microscopie électronique à balayage et à transmission, comme le montre la figure 6a–f. Les NiO-NPs ont montré un pléomorphisme avec une forme cubique et plus sphérique (<50 nm) avec une légère agglomération [40]. L'agglomération des NP pourrait être évidente à partir de l'adhérence du polymère et de l'interaction magnétique entre les particules [49].
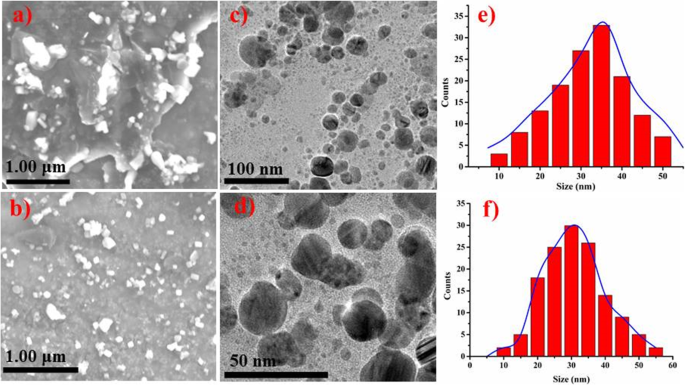
un –f Image SEM de NiO réduit phytochimiquement par le gingembre (a ) et l'ail (b ). Image MET de NiO réduit phytochimiquement avec du gingembre (c ) et l'ail (d ) et la distribution granulométrique du NiO phytochimiquement réduit par le gingembre (e ) et l'ail (f )
L'analyse élémentaire et d'autres caractéristiques des NiO-NPs synthétisés ont été décrites par spectroscopie à rayons X à dispersion d'énergie (EDS) qui a confirmé les phases de NiO pur comme le montrent les figures 7a, b. Les spectres EDS ont confirmé trois pics directement liés à la haute pureté du Ni présent dans les échantillons testés entre 1 et 10 kV. Les pourcentages en poids atomique observés dans les spectres pour Ni, O, C et Zn sont respectivement de 54,69, 27,81, 18,06 et − 0,55.
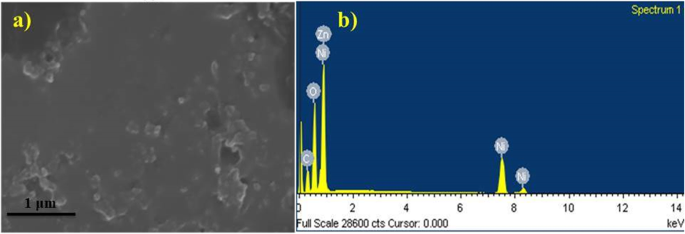
un , b Spectre EDS de NiO-NPs synthétisés verts
XPS affiche les C1s , O1s , et Ni2p spectres de NiO-NPs phytochimiquement réduits sur les figures 8a–d qui suggèrent la nature chimique et les états de liaison des échantillons synthétisés. Les pics les plus intenses à 284,8 et 286,2 eV démontrent des C1s spectre (Fig. 8b) correspondant à C–C et C–OH/C–O–C [21]. Les O1s le pic à 530,8 eV (Fig. 8c) pourrait être attribué aux groupes hydroxyles d'atomes d'oxygène, aux atomes d'oxygène adjacents aux lacunes de nickel ou aux atomes de carbone liés à l'oxygène C =O [1, 15, 37]. La contribution située à 532,2 eV est attribuée aux atomes d'oxygène dans les molécules d'eau absorbées (NiOH) [31, 41]. Le Ni2p spectre contenant Ni2p 3/2 et Ni2p 1/2 pics peuvent être séparés en utilisant la fonction gaussienne-lorentzienne en cinq composants (Fig. 8d). Les pics les plus intenses à 872,72 et 855,82 eV appartiennent au Ni2p 1/2 et Ni2p 3/2 avec les pics satellites correspondants respectivement à 879,36 et 861,57 eV [16]. La division spin-orbite entre le Ni (2p 1/2) et Ni (2p 3/2) et le niveau de base NiO-NP est de 17,28 eV, ce qui correspond bien aux rapports antérieurs [33, 34].
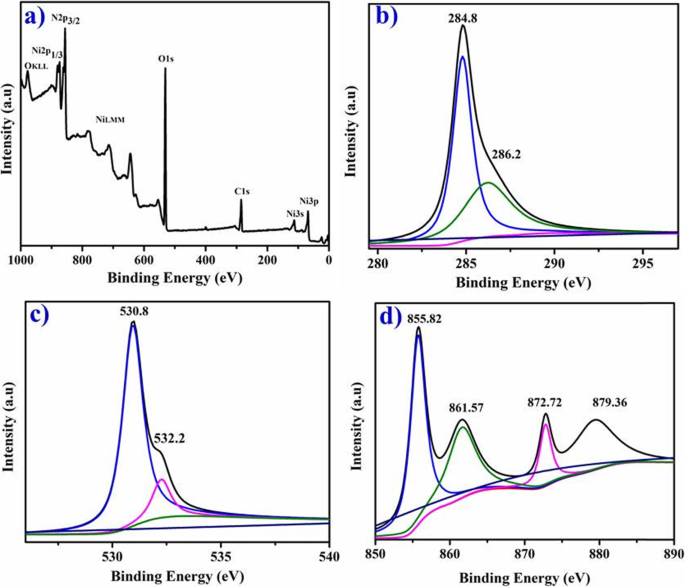
un –d Relevé XPS des particules réduites phytochimiquement (a ), C1s orbitales (b ), O1s spectres de NiO (c ), et Ni2p (d )
L'action antimicrobienne/bactéricide des extraits de racine de gingembre et d'ail et des NiO-NP vertes/phytochimiquement réduites a été évaluée à l'aide d'un essai de diffusion dans les puits d'agar via la mesure de la zone d'inhibition (mm) comme indiqué sur la figure 9a-d et le tableau 1. Les résultats ont montré une forte relation entre la concentration de NP et les zones d'inhibition (mm). Zones d'inhibition significatives (mm) (P <0,05) ont été enregistrés pour l'échantillon 1 (1,2 ml:1), 2 (1,8 ml:1), 3 (2,4 ml:1), 4 (3 ml:1), 5 (3,6 ml:1), et 6 ( 4,2 ml :1) allant de (3–4,9 mm) et (3,05–5,2 mm) à des concentrations faibles et élevées des NiO-NPs phytochimiquement réduits par le gingembre (Fig. 9c, d), tandis que (3,15–5,3 mm) et (3,75– 5.9 mm) NPs phytochimiquement réduites avec de l'ail contre MDR S. aureus (Fig. 9e, f). Les extraits aqueux de racine de gingembre ont montré une efficacité nulle (Fig. 9a), et les racines d'ail ont montré des zones d'inhibition de 2,65 et 5 mm à des concentrations faibles et élevées, respectivement (Fig. 9b). Tous les résultats ont été comparés au contrôle négatif DIW (0 mm) et au contrôle positif à la ciprofloxacine (12,55 mm). Dans l'ensemble, les NiO-NPs phytochimiquement réduits avec l'ail ont montré des valeurs significatives (P <0,05) action bactéricide renforcée contre MDR S. aureus.
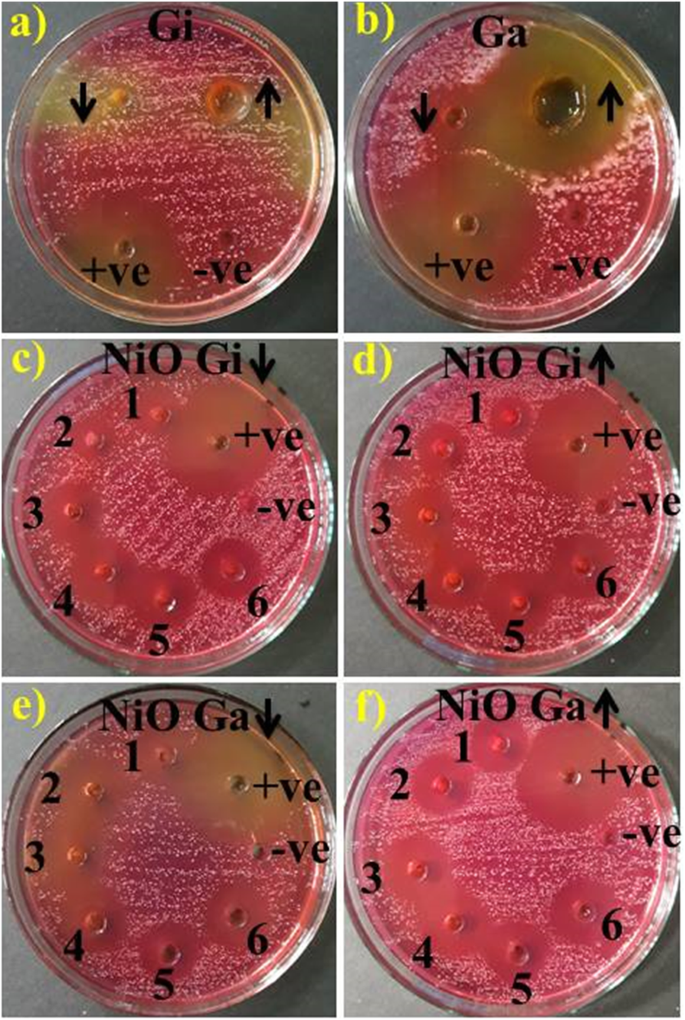
un –f Activité antimicrobienne in vitro de l'extrait aqueux de gingembre (a ), ail (b ), et les NiO-NPs synthétisés phytochimiquement par l'extrait de gingembre à faibles et fortes doses (c , d ) et l'ail (e , f )
La différence de tolérance au stress oxydatif dépend de divers facteurs tels que la surface, la morphologie et la taille des particules du nanomatériau synthétisé jouant un rôle inférentiel dans le potentiel d'action antibactérien [29, 36]. Une interaction électrostatique entre les souches bactériennes et les matériaux à l'échelle nanométrique entraîne la génération d'espèces réactives de l'oxygène responsables de la mort des cellules bactériennes [2,3,4,5, 22]. Deux réactions trouvées possibles pour la réaction des nanomatériaux avec des souches bactériennes, y compris une forte interaction des cations Ni 2+ avec des parties chargées négativement de cellules bactériennes entraînant un effondrement, tandis que la deuxième réaction entraîne une excitation électronique de la cantonnière à la bande de conduction lors de l'irradiation de la surface NiO avec de la lumière. Réaction électronique supplémentaire avec O2 génère O − 2 radicaux résultant en H2 O2 production. La production de ·OH s'est produite lors de la réaction de h + avec de l'eau. Ainsi, résultant O − 2 Les espèces · et ·OH ont joué un rôle important dans la décomposition des molécules lipidiques ou protéiques présentes dans la surface externe des cellules bactériennes [39].
Activité catalytique
Figure 10 a–e démontrant la réduction catalytique du MB en présence d'extraits de racines et de NiO-NPs verts/phytochimiquement réduits à température ambiante. La figure 10a montre le potentiel catalytique des NiO-NPs synthétisés par voie conventionnelle tandis que (Fig. 10b, c) représente le potentiel catalytique des extraits aqueux de racine de gingembre et d'ail. La capacité catalytique des NiO-NPs phytochimiquement réduits est représentée sur la figure 10d, e. Il est évident que NiO et les extraits de racines de plantes ne sont pas un nano-catalyseur efficace car ils consommaient 15, 21 et 38 min pour la réduction du bleu de méthylène (Fig. 10a–c). Les NPs phytochimiquement réduites avec le gingembre ont montré une dégradation rapide (λ max =8 min) avec une conversion efficace du MB en bleu de leucométhylène (Fig. 10d). Les NiO-NPs à médiation par l'ail ont montré un schéma similaire de réduction de 100% de colorant en 5 min (Fig. 10e).
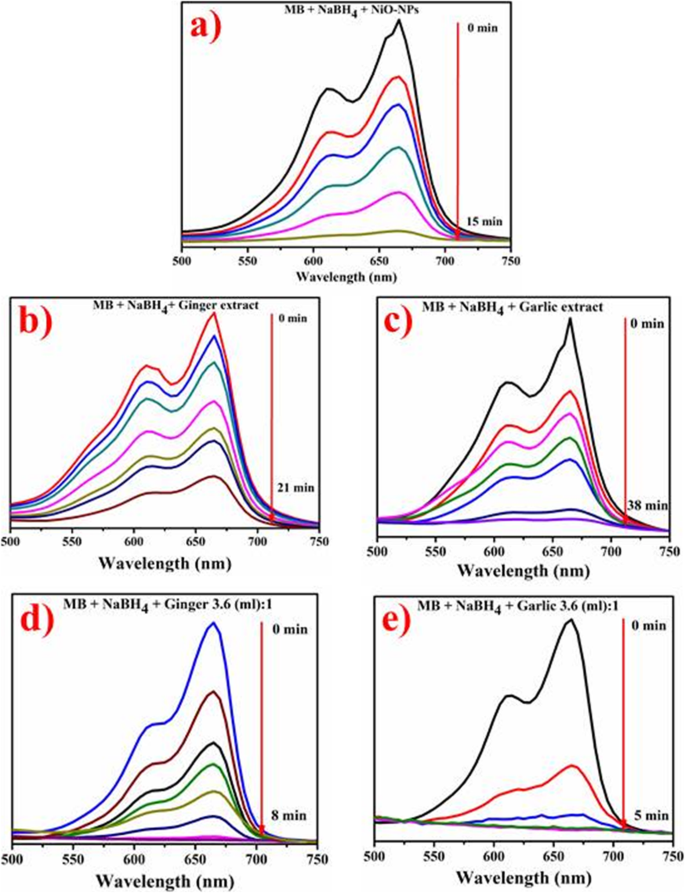
un –e Activité catalytique de NiO (a ), extrait de gingembre (b ), extrait d'ail (c ), NiO phytochimiquement réduit par le gingembre (d ), et les NP réduites à l'ail (e )
Les NP vertes/phytochimiquement réduites effectuent une dégradation significative du colorant catalytique en transférant les électrons des espèces donneuses (BH4 ) à l'accepteur (MB) et stabilise le système en réduisant l'énergie d'activation [27]. Les données ont révélé que les NP vertes étaient des nano-catalyseurs efficaces par rapport aux NP conventionnelles et aux extraits individuels.
Conclusion
Les NiO-NP contenant des extraits de racine de gingembre et d'ail ont été d'excellents agents bactéricides et catalytiques. L'incorporation d'extraits de racines ayant des groupes phytochimiques a abouti à une synthèse réussie de NiO-NP révélée par FTIR. Les pics XRD ont confirmé le réseau NiO hexagonal et cubique à faces centrées (fcc) et le SEM a confirmé le pléomorphisme avec une morphologie cubique et plus sphérique des NP ayant une taille moyenne de 16 à 52 (dopage au gingembre) et de 11 à 59 nm (dopage à l'ail). Cependant, l'analyse élémentaire a révélé la nature chimique et les états de liaison analysés par EDS et XPS et a présenté le pourcentage réel de nickel et d'oxygène, tandis que l'analyse UV a vérifié la différence des pics d'absorption dans la plage 350 nm et a introduit un décalage vers le bleu à une plus grande quantité de dopants. Phytochimiquement, l'ail réduit NiO à haute concentration s'est avéré plus puissant que les NP réduites par le gingembre contre MDR S. aureus ainsi que réduit MB efficacement. Ainsi, le NiO vert/phytochimiquement réduit à partir d'extraits de racine d'ail peut être adopté en médecine avancée comme substitut de la résistance aux antibiotiques et dans les industries textiles comme agent catalytique sans danger pour l'environnement.
Disponibilité des données et des matériaux
Toutes les données sont entièrement disponibles sans restriction.
Abréviations
- EDS :
-
Spectroscopie à rayons X à dispersion d'énergie
- fcc :
-
Cube à faces centrées
- FTIR :
-
Spectroscopie infrarouge à transformée de Fourier
- G +ve :
-
Gram positif
- G –ve :
-
Gram négatif
- JCPDS :
-
Comité mixte sur les étalons de diffraction des poudres
- Mo :
-
Bleu de méthylène
- Non :
-
Nickel
- NiO :
-
Oxyde de nickel
- nm :
-
Nanomètre
- NP :
-
Nanoparticules
- SEM :
-
Microscopie électronique à balayage
- TEM :
-
Microscopie électronique à transmission
- UV-Vis :
-
Spectroscopie visible ultra-violet
- XPS :
-
Spectroscopie photoélectronique aux rayons X
- XRD :
-
Diffraction des rayons X
Nanomatériaux
- Nanoparticules FePO4 biocompatibles :administration de médicaments, stabilisation de l'ARN et activité fonctionnelle
- Synthèse biogénique, caractérisation et évaluation du potentiel antibactérien de nanoparticules d'oxyde de cuivre contre Escherichia coli
- Activité de préparation et d'hydrogénation catalytique améliorée des nanoparticules de Sb/Palygorskite (PAL)
- Des nanoparticules comme pompe à efflux et inhibiteur de biofilm pour rajeunir l'effet bactéricide des antibiotiques conventionnels
- Synthèse verte à un pot de microsphères de SnO2 décorées d'Ag :un catalyseur efficace et réutilisable pour la réduction du 4-nitrophénol
- La toxicité potentielle pour le foie, le cerveau et l'embryon des nanoparticules de dioxyde de titane sur des souris
- Polyglycérol hyperramifié modifié comme dispersant pour le contrôle de la taille et la stabilisation des nanoparticules d'or dans les hydrocarbures
- Détermination de l'activité catalytique de nanoparticules de TiO2 dopées par un métal de transition à l'aide d'une analyse spectroscopique de surface
- Synthèse et performances in vitro de nanoparticules de fer-platine revêtues de polypyrrole pour la thérapie photothermique et l'imagerie photoacoustique



