Le rôle de la voie de l'apoptose dans la cytotoxicité induite par les nanoparticules d'oxyde de zinc fraîches et vieillies
Résumé
Les nanoparticules d'oxyde de zinc (ZnO NP) sont utilisées dans un large éventail d'applications, notamment l'industrie, les produits commerciaux et le domaine médical. De nombreuses études mécanistiques sur la toxicité des NP de ZnO ont été réalisées sur des NP vierges (fraîches). Cependant, la cytotoxicité induite par les NP de ZnO transformées (vieillies) et les mécanismes sous-jacents restent flous. Ici, nous avons observé la transformation physico-chimique des NPs de ZnO au fil du temps, suivie de l'évaluation de la cytotoxicité des NPs fraîches et vieillies. Nous avons constaté que les NPs de ZnO fraîches induisaient un niveau d'apoptose plus élevé que leurs homologues âgés. En conséquence, les données de séquençage d'ARN d'un hybride homme-hamster traité au ZnO NP (A L ) ont montré que les voies de signalisation p53, PI3k–Akt, FoXO, Glutathione, ErbB, HIF-1, Ocytocine et Jak-STAT étaient enrichies mais pas de voie d'apoptose. Les résultats de la PCR quantitative ont révélé le niveau d'ARNm significativement plus élevé de IL1B et CD69 dans les groupes frais traités au NP par rapport à celui des groupes âgés traités au ZnO NP et au chlorure de zinc. Les résultats ci-dessus ont indiqué que la cytotoxicité inférieure des NP de ZnO vieillies est partiellement attribuée à leur puissance réduite à induire l'apoptose. La régulation transcriptionnelle de multiples voies de signalisation activées par les NP âgées peut aider à construire l'homéostasie cellulaire. Ensemble, nos résultats mettent en évidence l'influence du processus de vieillissement (transformation de l'environnement) des NP de ZnO sur leurs toxicités et leurs conséquences biologiques.
Introduction
Avec le développement rapide de la nanotechnologie au cours des dernières décennies, les nanoparticules (NP) ont été appliquées dans divers domaines, notamment l'industrie, la vie quotidienne humaine et la nanomédecine [1, 2]. Le Nanotechnology Consumer Product Inventory (CPI) montre une multiplication par 30 entre 2005 et 2015 du nombre de nano-produits, dont 762 produits de santé (fitness), 72 aliments (boissons) et 23 produits pour bébé [2]. L'application croissante des NP dans les produits de consommation et dans divers domaines a augmenté la possibilité que des NPs pénètrent dans l'environnement, ce qui soulève des problèmes de sécurité en ce qui concerne leurs impacts négatifs potentiels. Les NP d'oxyde de zinc (ZnO) sont parmi les NP les plus couramment utilisées, et sa production annuelle mondiale a atteint près de 3 400 tonnes [3, 4]. Certaines substances auparavant considérées comme biologiquement inertes pourraient devenir toxiques à l'état nanoparticulaire. Un nombre croissant d'études ont élucidé que les NP de ZnO peuvent présenter des risques importants pour les cellules de mammifères et les animaux en induisant une toxicité importante [5,6,7].
Diverses stratégies, notamment le revêtement, la fonctionnalisation de surface et la modification de l'état d'oxydation, ont été utilisées pour atténuer la toxicité potentielle des NP en modifiant leurs propriétés physiques et chimiques (telles que la dissolution, l'agglomération et la perturbation des membranes cellulaires) [8,9,10, 11]. Bien que ces modifications des NP affaiblissent leurs effets toxiques dans une certaine mesure, les utilisations des NP ne sont pas toujours sûres, en particulier dans certaines conditions d'exposition et certains environnements [12,13,14]. En fait, de nombreux types de NP ne sont pas stables et enclins à subir un « vieillissement » ou une « transformation environnementale » après avoir été intentionnellement ou involontairement libérés dans l'environnement naturel [14,15,16,17]. Ces dernières années, de nombreux travaux ont été menés pour explorer le processus de transformation environnementale des NP; cependant, la recherche sur les effets toxiques des NP « transformées (vieillies) » est encore très limitée, sans parler de leurs mécanismes toxiques.
En tant que représentant typique des NP non persistantes, les NP de ZnO ont une réactivité très élevée et sont susceptibles de se transformer en propriétés physiques et chimiques et en état d'occurrence après avoir été libérées dans l'environnement ou ingérées par des animaux, ce qui pourrait affecter de manière significative leurs effets toxicologiques [17 , 18]. Par exemple, des études ont montré que le processus de sulfuration des NP de ZnO modifiait la charge, l'hydrophobie et l'état d'agrégation, entraînant l'adsorption des NP à l'état sulfure dans la salive humaine, la sueur et le liquide de lavage broncho-alvéolaire. De plus, la protéine adsorbée par les NP de ZnO forme une couronne protéique spéciale qui affecte généralement son effet biologique [19]. Les phosphates dans les solutions physiologiques pourraient convertir les NP de ZnO en ZnHPO métastable4 et Zn3 (PO4 )2 dans un délai d'environ 5 à 10 h [20]. Le processus de transformation complète des NP de ZnO (≤ 3 μg/mL) dans le système d'exposition in vitro aux lymphocytes T humains (37 °C, milieu de culture cellulaire RPMI1640 contenant 10 % de FBS pendant 24 h) a été étudié en utilisant le rayonnement synchrotron X- spectroscopie de structure à absorption de rayons (XANES) [21]. Les études ci-dessus suggèrent la sous-estimation des risques environnementaux et sanitaires des NP de ZnO en évaluant uniquement les effets biologiques des NP de ZnO vierges (fraîches). À la lumière de ce problème, il est urgent de comprendre globalement les processus de vieillissement et de transformation environnementale des NP [22].
Notre étude précédente a révélé que les NP de ZnO vieillies pendant 40 à 120 jours dans de l'eau ultrapure subissent une transformation physico-chimique et se transforment en Zn5 (CO3 )2 (OH)6 , Zn (OH)2 , et Zn 2+ [23]. Il est intéressant de noter que les NP de ZnO âgées présentaient une cytotoxicité inférieure à celle de leurs homologues frais [23], mais les mécanismes de toxicité de ce type de variation ne sont pas clairs. Dans la présente étude, nous avons entrepris d'explorer les raisons sous-jacentes des différentes cytotoxicités entre les NP de ZnO fraîches et vieillies. Des NP de ZnO avec deux tailles de particules différentes (20 nm et 90-200 nm) ont été appliquées systématiquement. Les tests de cytotoxicité ont démontré que les NP de ZnO vieillies induisaient des anomalies morphologiques moins prononcées et des viabilités cellulaires relativement plus élevées que leurs homologues frais. Les données de séquençage de l'ARN ont révélé que les gènes apoptotiques étaient enrichis dans les cellules fraîches traitées au ZnO NP, alors que ces gènes étaient beaucoup moins affectés par les traitements au ZnO NP âgés. De plus, les cellules exposées à des NP de ZnO vieillies ont montré un niveau réduit de protéine caspase-3 clivée, indiquant en outre la puissance plus élevée des NP de ZnO fraîches pour provoquer l'apoptose dans les cellules en culture. Combiné avec nos résultats précédents, cette étude a suggéré que la diminution de la cytotoxicité des NP de ZnO âgées est attribuée à leur capacité atténuée à déclencher l'apoptose cellulaire.
Matériaux et méthodes
Nanoparticules et réactifs
Les nanopoudres de ZnO disponibles dans le commerce (ZnO NPs), avec une taille moyenne rapportée par le fabricant de 20 nm (pureté à 99,5 %, presque sphérique) et de 90 à 200 nm (pureté à 99,9 %, morphologie irrégulière), ont été achetées auprès de Nanostructured &Amorphous Materials (Houston, TX ). Sauf indication contraire, tous les réactifs et produits chimiques utilisés dans cette étude ont été achetés auprès de Sigma-Aldrich (Shanghai, Chine).
Dispersion, vieillissement et caractérisation des nanoparticules
Les suspensions mères de ZnO NPs (1 mg/mL) ont été préparées en suspendant des nanopoudres sèches dans Milli-Q H2 O (Millipore, 18 MΩ cm) et stérilisé par autoclavage (120 °C, 30 min) puis conservé à 25°C pour une période de vieillissement naturel allant de 0 à 60 jours. Les NP de ZnO naturellement transformées à 0 et 60 jours ont été désignées respectivement comme NP fraîches et vieillies. Pour assurer une bonne dispersion, les suspensions fraîches et vieillies ont été soniquées (100 W) pendant 30 min dans un bain à ultrasons avant caractérisation ou incubation avec les cellules. La morphologie, la taille des particules et l'agrégation des NPs de ZnO fraîches et vieillies ont été caractérisées en utilisant la microscopie électronique à transmission (TEM, JEOL JEM-2010, Tokyo, Japon). La structure cristalline des NP de ZnO fraîches et vieillies a été déterminée à l'aide de la diffraction des rayons X de puissance (XRD, PANalytical B. V., Shanghai, Chine) en comparant à des normes authentiques. Les détails du processus de vieillissement naturel et de la caractérisation des NP de ZnO ont été décrits précédemment [23].
Culture cellulaire et traitement avec des NP de ZnO
Un L lignée cellulaire, une sorte de cellules hybrides homme-hamster formées par fusion du gly2A mutant d'ovaire de hamster chinois (CHO) et de fibroblastes humains a été utilisé dans cette étude. Ces cellules hybrides contenaient un ensemble standard de chromosomes CHO-K1 et une seule copie du chromosome humain 11 et ont été cultivées dans du milieu F12 de Ham (Hyclone, Grand Island, NY) additionné de sérum bovin fœtal (8 %, Hyclone, Grand Island, NY) ), gentamicine (25 g/mL) et glycine (2 × 10 –4 M) à 37 °C dans un local humidifié à 5% de CO2 incubateur [24]. Les suspensions mères de NP de ZnO fraîches et vieillies ont été dispersées par 30 min d'ultrasons (100 W) pour éviter l'agglomération, puis diluées à des concentrations appropriées avec des milieux de culture cellulaire pour l'exposition des cellules. Les cellules maintenues dans des milieux de culture cellulaire sans NP ont servi de contrôle dans chaque expérience.
Test de détection de la cytotoxicité
Un L les cellules à phase logarithmique de croissance ont été cultivées sur des lames de verre dans des boîtes de Pétri de 35 mm (6 × 10 4 cellules/boîte) pendant 24 h avant la stimulation, suivi d'un traitement avec 2 mL de milieu de culture contenant 1, 5, 10, 12, 15 et 20 µg/mL de ZnO NPs fraîches ou vieillies 72 h. Après la fin du temps de traitement, les images de la morphologie cellulaire ont été obtenues à l'aide d'un microscope Leica DM4B (Leica, Allemagne). ZnCl2 a été inclus comme référence d'ions zinc pour comparer la cytotoxicité avec les NP de ZnO.
Le kit de comptage cellulaire (CCK-8) (APExBIO, Shanghai, Chine) a été utilisé pour détecter la viabilité cellulaire. Dans les détails, A L les cellules ont été ensemencées dans des plaques à 96 puits (4 × 10 3 cellules/puits) avec un milieu de culture cellulaire pendant 24 h et traité avec un milieu contenant différentes concentrations de ZnCl2 , des NP de ZnO fraîches et vieillies pendant 24, 48 et 72 h, respectivement. Pour la solution de travail, le volume de NP ajoutées à partir de la suspension mère était inférieur à 5 % du volume total du milieu de culture dans chaque puits. Après la fin du temps de traitement, le milieu de culture a été aspiré et les cellules ont été incubées avec 100 µL de solution de travail CCK-8 pendant 2 h à 37 °C en suivant les instructions du fabricant. Ensuite, l'absorbance a été enregistrée à 450 nm à l'aide d'un lecteur de fluorescence Spectra Max M2 (Molecular Devices, Wokingham, Berks, Royaume-Uni). La viabilité cellulaire a été calculée en pourcentage d'absorbance dans les puits, chaque concentration de NP étant normalisée par rapport à l'absorbance des cellules témoins (100 %).
Extraction d'ARN, transcription inverse et PCR quantitative
Un L les cellules à une phase logarithmique de croissance ont été ensemencées dans une boîte de Pétri de 35 mm de diamètre (6 × 10 4 cellules/boîte) avec des milieux de culture cellulaire pendant 24 h. Ensuite, le milieu a été remplacé par 2 mL de milieu de culture contenant 12 µg/mL de ZnCl2 , NPs de ZnO frais et vieillis pendant 72 h. Après la fin du temps de traitement, le milieu de culture a été aspiré et les cellules ont été lavées 3 fois avec du PBS. Par la suite, 1 mL de réactif Trizol (Invitrogen, Carlsbad, CA, USA) a été ajouté à chaque boîte pour extraire l'ARN total selon les instructions du fabricant. La concentration et la pureté de l'ARN total obtenu après l'extraction ont été quantifiées à l'aide d'un spectrophotomètre Q5000UV-Vis (Quawell, USA). Après quantification, la transcription inverse a été réalisée à l'aide du kit TransGene RT-PCR (TransGene Biotech, Pékin, Chine) pour obtenir l'ADNc à partir de la matrice d'ARN selon les protocoles du fabricant. Les échantillons d'ADNc résultants ont été quantifiés à l'aide du spectrophotomètre UV-Vis Q5000, puis analysés à l'aide de SYBR-Green comme colorant de fluorescence (TransGene Biotech, Pékin, Chine) sur le système Roche RT-PCR (Applied Biosystems) [25].
Le gène de ménage codant pour la glycéraldéhyde-3-phosphate déshydrogénase (Gapdh ) a été utilisé comme contrôle interne pour évaluerIl-1α , Il-1β , Caspase 3 , CD69 , Juin et MT1 expression de l'ARNm. Les résultats ont été exprimés sous forme de rapport d'expression relatif entre le gène ciblé et Gapdh . Les séquences d'amorces utilisées dans cette étude sont fournies dans le tableau 1.
Analyse des données de séquençage de l'ARN
Les échantillons d'ARN totaux de A L cellules du groupe témoin, groupe vieilli traité au ZnO NP et ZnCl2 groupe traité ont été séquencés par BangFei Bioscience (Beijing, Chine). En bref, l'ARN total de A L les cellules ont été extraites selon les protocoles TRIZOL, jusqu'à la précipitation isoproponale. Ensuite, les échantillons d'ARN ont été remis en suspension dans le tampon d'extraction avant le séquençage. Les données brutes de séquençage de l'ARN ont été analysées à l'aide du package R Deseq2 [Eric1]. Le diagramme de Venn a été généré par le package R VennDiagram [Eric1.2]. Les gènes significativement modifiés ont été utilisés pour une analyse plus poussée de l'enrichissement des voies. Les expériences ont été effectuées en trois répétitions indépendantes. Les gènes d'ARNr, les gènes mitochondriaux et les gènes détectés à moins de 40 pb ont été exclus de l'analyse.
Les données de séquençage d'ARN, séries de référence GSE97852, GSE60159 et GSE39444, ont été obtenues auprès de Gene Expression Omnibus [Eric 2, 3, 4]. Le graphique Gene Set Enrichment Analysis a été généré par R (version 3.6.2) en utilisant le package fgsea [Eric 5]. Les gènes d'apoptose avec un changement significatif 1,5 fois &p value < 0.05 ont été utilisés pour une analyse plus approfondie. La carte thermique avec arbre génétique a été générée par le package R « ComplexHeatmap » [Eric 6]. Le couplage moyen a été utilisé comme méthode de regroupement et Euclidienne a été utilisée comme méthode de mesure de distance. L'analyse d'enrichissement de la voie a été précédée par STRING2.0 [Eric 7].
Western Blot
Un L les cellules à une phase logarithmique de croissance ont été ensemencées dans une boîte de Pétri de 60 mm de diamètre (1,5 × 10 5 cellules/boîte) avec des milieux de culture cellulaire pendant 24 h. Ensuite, le milieu a été remplacé par 4 mL de milieu de culture contenant 12 µg/mL de ZnO NPs fraîches ou vieillies pendant 24 h. A la fin de la période d'exposition, le milieu de culture a été aspiré, puis les cellules ont été lavées 3 fois avec du PBS et lysées sur glace avec du tampon de lyse RIPA (Beyotime, Chine) pour collecter les protéines cellulaires. Des quantités égales de protéines cellulaires ont été séparées sur des gels SDS-PAGE à 12% puis transférées sur une membrane en fluorure de polyvinylidène (PVDF) (Roche, Swiss). Brièvement, après 2 h de blocage avec du lait écrémé à 5 % dans du TBST à 25 °C, les membranes ont ensuite été incubées avec un anticorps primaire à des dilutions appropriées (selon les protocoles du fabricant) à 4 °C pendant la nuit, suivi d'une incubation avec de l'anticorps secondaire conjugué à de la HRP. anticorps (1:5000, Promega, Madison, USA) pendant 2 h à 25 °C. Enfin, l'immunomarquage a été détecté à l'aide d'une solution de chimiluminescence améliorée (ECL) (BOSTER, Chine). Les anticorps primaires de la Caspase-3 anti-pro/clivée et de l'anti-Actine ont été achetés respectivement auprès de Cell Signaling Technology et d'ImmunoWay.
Statistiques
L'analyse statistique a été compilée sur la moyenne des résultats obtenus à partir d'au moins trois expériences indépendantes. Toutes les données ont été présentées sous forme de moyennes ± écart-type (SD) et comparées statistiquement en utilisant une analyse de variance à un facteur (ANOVA). Dans toutes les parcelles p les valeurs < 0,05 ont été présentées comme * et considérées comme statistiquement significatives.
Résultats
Caractérisation des NP de ZnO
Pour déterminer les différences de caractéristiques physico-chimiques détaillées entre les NP de ZnO fraîches et vieillies, nous avons d'abord observé la morphologie des NP à l'aide de la MET (Fig. 1A). Nos résultats ont indiqué que les NP de ZnO frais de 20 nm étaient des cristaux presque sphériques et que les NP de ZnO frais de 90 à 200 nm étaient des cristaux irrégulièrement en forme de bâtonnets/cubiques. La taille de particule unique était conforme à la taille fournie par le fabricant. De toute évidence, les NP de ZnO de 20 nm et 90-200 nm étaient enclines à s'agréger dans l'eau ultrapure. De plus, quelles que soient la forme et la taille des NP d'origine, la microstructure des NP de ZnO à 20 nm et 90 à 200 nm a été considérablement modifiée, passant d'une structure cristalline claire à un état amorphe ou en forme de feuille/aiguille après un vieillissement de 60 jours. De plus, la nature cristalline et la pureté de phase des NPs fraîches et vieillies ont été déterminées en utilisant la diffraction des rayons X (XRD) avec un rayonnement Cu Kα (λ = 0,15418 nm) approche à 25 °C, comme le montre la figure 1B. Le modèle XRD des NPs de ZnO fraîches a indiqué que les échantillons étaient constitués d'une structure cristalline de wurtzite et qu'aucun pic d'impureté caractéristique n'a été identifié, suggérant une haute qualité de NPs fraîches. Pour les NPs âgées, le modèle XRD montrait la néoformation de Zn5 (CO3 )2 (OH)6 (numéro de carte 00-011-0287) et Zn (OH)2 (numéro de fiche 00-003-0888) phases solides, indiquant la transformation chimique des NP de ZnO (20 et 90-200 nm) au cours du processus de vieillissement.
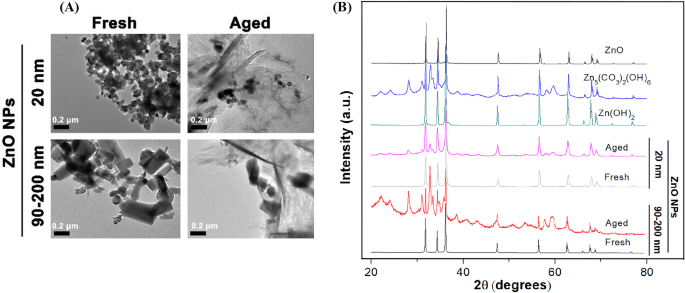
Caractéristiques physico-chimiques des NPs de ZnO fraîches et vieillies. Un Micrographies représentatives de NPs fraîches et vieillies (100 μg/mL, 20 et 90-200 nm) en Milli-Q de l'eau à l'aide d'un TEM basse résolution, B Modèles XRD de NPs fraîches, NPs âgées, ZnO, Zn (OH)2 et Zn5 (CO3 )2 (OH)6 références sous forme séchée
Observation morphologique de A L Cellules exposées à des NP de ZnO fraîches et vieillies
Le traitement des NP entraîne un changement notable de la forme cellulaire, ou de la morphologie, in vitro [26]. Par conséquent, A L les cellules exposées à des NP de ZnO fraîches ou vieillies à 10 et 15 µg/mL pendant 72 h ont été examinées au microscope stéréoscopique. Comme le montre la figure 2, la morphologie cellulaire dans le groupe témoin est restée normale. Les cellules ont bien adhéré, la plupart se fixant en moins de 2 h. La plupart des cellules étaient en forme de fuseau ou polygonales, avec quelques nouvelles cellules en division montrant un cytoplasme plus transparent et une meilleure dispersion pendant le processus d'adhésion. Le traitement avec 12 μg/mL de NP de ZnO fraîches (20 nm et 90-200 nm) pendant 72 h a considérablement modifié la morphologie cellulaire. Bien que la plupart des cellules aient adhéré dans les 3 à 5 heures, elles ne pouvaient pas bien se propager et certaines cellules sont devenues arrondies et ont perdu leur forme polygonale. Lorsque la concentration de ZnO NPs a été augmentée à 15 μg/mL, les cellules traitées se sont atrophiées et n'ont pas pu adhérer, suggérant leur viabilité cellulaire significativement inférieure à celle des cellules traitées avec 10 μg/mL. Ces résultats ont indiqué que la CL100 pour les NPs de ZnO fraîches est probablement inférieure à 15 μg/mL par un traitement de 72 h. En revanche, la morphologie cellulaire dans les groupes traités aux NP âgés de 20 nm et 90-200 nm (15 μg/mL) n'a pas été significativement affectée, et la plupart des cellules survivantes ont pu adhérer et se propager, avec moins de la moitié des cellules mortes observées, révélant que Les NP de ZnO vieillies sont beaucoup moins cytotoxiques que les NP de ZnO fraîches.
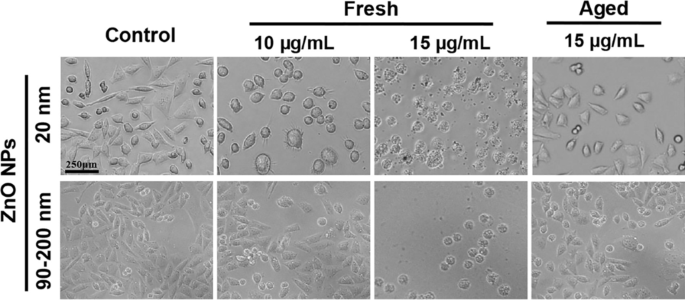
Changements morphologiques dans A L des cellules après exposition à des NP de ZnO fraîches ou vieillies pendant 72 h dans du milieu F12 supplémentaire de Ham, et des cellules non exposées ont été utilisées comme groupes témoins. Un L la morphologie cellulaire a été observée au microscope optique à un grossissement de 10 ×
Les NP de ZnO âgées induisent une cytotoxicité inférieure à celle des NPs fraîches
Pour étudier plus avant la différence de cytotoxicité entre les NP de ZnO fraîches et âgées, nous avons examiné la viabilité cellulaire en utilisant des kits CCK-8. Comme le montre la Fig. 3, incubation A L les cellules avec des doses de gradient de ZnO NPs fraîches et vieillies (allant de 0 à 20 μg/mL, 20 nm et 90-200 nm) pendant 24 h, 48 h ou 72 h ont montré une diminution dose-dépendante de la viabilité cellulaire. Aucune cytotoxicité évidente n'a été observée en traitant les cellules avec ZnO NPs ≤ 10 μg/mL. Lorsque la dose de ZnO NPs fraîches et vieillies s'élevait à 12 et 15 g/mL, la viabilité cellulaire a montré une tendance à la diminution en fonction du temps. De toute évidence, la viabilité cellulaire dans les groupes traités au NP âgés était significativement plus élevée que dans les groupes traités au NP frais. De plus, ZnCl2 -le traitement a également compromis la viabilité cellulaire d'une manière dose-dépendante et temporelle, alors que la cytotoxicité du ZnCl2 était bien inférieur à celui des NP de ZnO frais et vieillis.
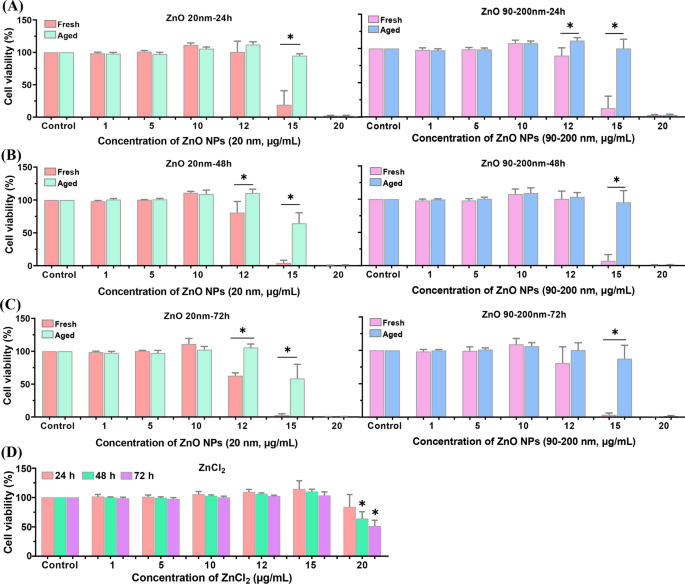
Viabilité cellulaire induite par des NP de ZnO fraîches et vieillies dans A L cellules. Un L les cellules ont été incubées avec diverses concentrations de NP de ZnO fraîches et vieillies (20 et 90-200 nm) pendant 24 h (A ), 48 h (B ) et 72 h (C ). D Un L les cellules ont été exposées à diverses concentrations de ZnCl2 pour des moments différents. Les données étaient basées sur ≥ 3 expériences indépendantes et exprimées en moyenne ± SD, *p < 0,05
Les voies d'apoptose activées par le traitement des NPs fraîches de ZnO et régulent à la hausse l'expression des gènes apoptotiques
Pour dévoiler les mécanismes sous-jacents conduisant à la cytotoxicité inférieure des NPs âgées, nous avons analysé les données de séquençage de l'ARN des NPs ZnO fraîches et âgées. Comme le montre la Fig. 4A, B, après traitement avec des NP de ZnO fraîches, la voie de l'apoptose a été activée dans les cellules Jurkat (p = 0,017) et les cellules HMDM (p = 0,041). Les gènes de l'apoptose :ANXA1 , CYLD , TNFSF10 , IER3 , CDKN1A , JUIN , SAT1 , PMAIP1 , CD38 et ISG20 ont été significativement enrichies en cellules Jurkat fraîches traitées au ZnO NP. Les gènes d'apoptose :CD38 , TNFRSF12A , CCNA1 , BMP2 , PPP2R5B , EREG , IFNGR1 , CD44 , CD14 , GNA15 , GCH1 , TIMP1 , BTG2 , IL1B , IL1A , BTG3 , BCL2L11 , SC5D et SPTAN1 ont été significativement enrichis en cellules HMDM fraîches traitées au ZnO NP (Fig. 4C, D). Étant donné que les cellules de Jurket (cellules lymphocytaires T du sang périphérique) et les cellules HMDM (macrophages dérivés de monocytes humains) sont des types de cellules différents, la façon dont elles déclenchent l'apoptose peut être différente. En résumé, ces résultats ont montré que l'exposition de nouvelles NP de ZnO pouvait activer différentes voies d'apoptose dans divers types de cellules.
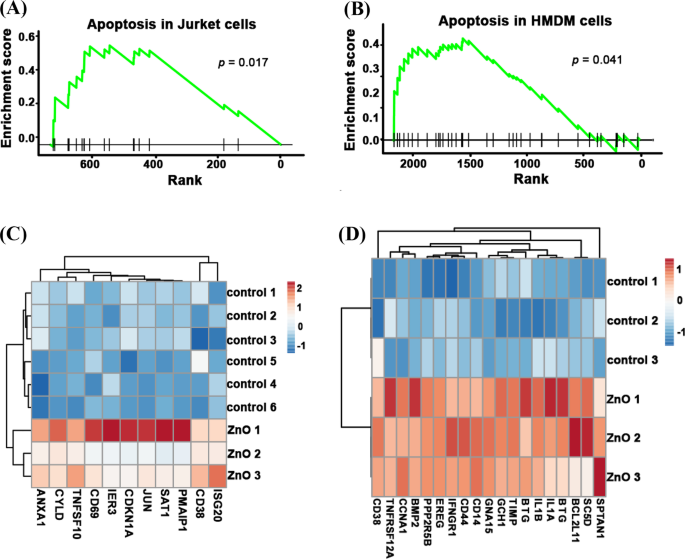
La voie de l'apoptose a été enrichie en données RNA-seq de cellules Jurket et HMDM fraîches traitées au ZnO NP. Le score d'enrichissement des gènes significativement exprimés de la voie de l'apoptose de cellules Jurket fraîches traitées au ZnO NP (A ) et les cellules HMDM (B ). La carte thermique de l'expression des gènes apoptotiques de cellules Jurket fraîches traitées au ZnO NP (C ) et les cellules HMDM (D ) et leurs groupes de contrôle
Les NP de ZnO âgés n'ont pas régulé à la hausse l'expression des gènes apoptotiques en tant que NP de ZnO frais
Nos données de séquençage d'ARN à partir de A âgés traités au ZnO NP L les cellules ont montré que les voies de signalisation p53, PI3k-Akt, FoXO, Glutathione, ErbB, HIF-1, Ocytocine et Jak-STAT étaient enrichies (Fig. 5A). Les gènes d'apoptose enrichis dans les cellules Jurket et HMDM n'étaient pas significativement affectés dans les cellules âgées traitées au ZnO NP (Fig. 5B). Pour confirmer davantage les résultats, nous avons testé l'expression de gènes apparentés par PCR en temps réel. Nous avons découvert que certains des gènes d'apoptose :BMP2 , PMAIP1 , IL1α , CD69 , CCNA1 , CD38 et IL1β étaient indétectables chez les A âgés traités aux ZnO NPs L cellules (données non présentées), probablement parce que la plupart de ces gènes sont exprimés dans les cellules du système immunitaire. Les autres gènes d'apoptose régulés à la hausse (IL1α , IL1β et CD59 ) observés dans les groupes frais traités par ZnO NP n'étaient pas significativement modifiés dans les niveaux d'expression par le traitement des ZnO NP âgés. Alors que le MT1 qui servent de contrôle positif a été significativement augmenté dans un niveau d'expression, l'expression de la Caspase 3 n'a pas été significativement modifié (Fig. 5C). Ces données suggèrent que les NP de ZnO âgées, contrairement à leurs homologues fraîches, sont moins puissantes pour activer les gènes de la voie de l'apoptose dans A L cellules.
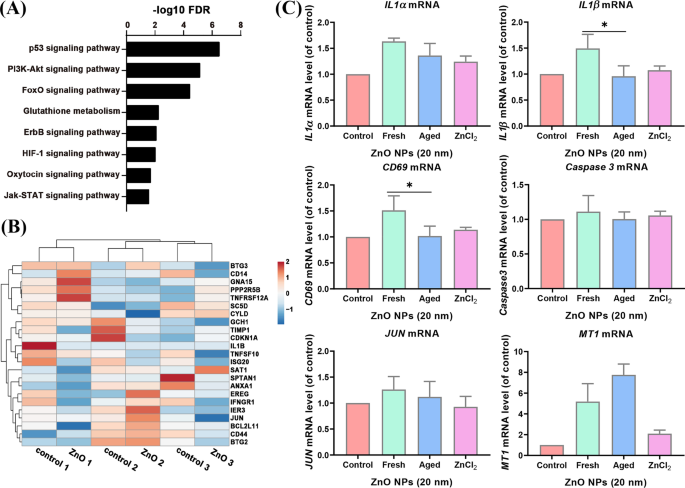
La voie de l'apoptose n'a pas été enrichie dans les données RNA-seq des A âgés traités au ZnO NP L cellules. (Un ) L'analyse de l'ontologie génique des voies enrichies à partir de A âgé traité au ZnO NP L cellules. (B ) La carte thermique de l'expression des gènes apoptotiques des A âgés traités au ZnO NP L cellules et groupe témoin. (C ) L'expression de gènes apoptotiques sélectionnés et de gènes de contrôle (MT1 ) en A frais et vieilli ZnO NP traité L cellules
Les NP de ZnO fraîches mais non vieillies ont augmenté le niveau d'expression de la protéine Caspase 3 activée
Détection de l'expression génique de la Caspase 3 seul ne peut pas indiquer directement l'activation de la voie de l'apoptose. Pour analyser plus en détail si le traitement des ZnO NPs pouvait modifier le niveau des protéines apoptotiques, l'expression de la protéine caspase 3 clivée, un biomarqueur couramment utilisé pour indiquer l'activation de l'apoptose cellulaire [27], a été examinée par Western blot analyse. Comme le montre la figure 6, par rapport au groupe témoin, le traitement avec des NP de ZnO fraîches (20 nm) a augmenté le niveau cellulaire de la protéine caspase 3 clivée de 1,31 ± 0,023 fois, ce qui était significativement plus élevé que celui des NP de ZnO de 20 nm - groupe traité (1,12 ± ± 0,039 fois). Lorsque la taille des particules des NPs de ZnO fraîches a été augmentée à 90-200 nm, l'expression de la protéine caspase 3 clivée induite par les NPs fraîches a été augmentée de 1,46 ± 0,078 fois, significativement plus élevée que celle des NPs âgées (1,07 ± 0,075 fois) . Ces données ont illustré davantage la puissance plus élevée des NPs de ZnO fraîches dans l'induction de l'apoptose cellulaire, par rapport à leurs homologues plus âgées.
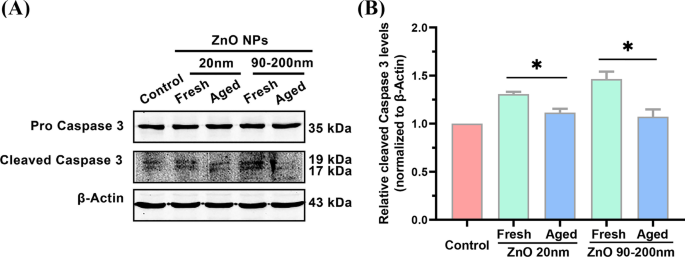
Niveaux d'apoptose dans A L cellules incubées avec des NP de ZnO fraîches et vieillies (20 et 90-200 nm). Analyse Western Blot (A ) et quantification (B ) des niveaux de protéine caspase 3 clivée lorsque les cellules ont été incubées avec 12 μg/mL de NP de ZnO fraîches et vieillies (20 et 90-200 nm) pendant 72 h. Les données étaient basées sur ≥ 3 expériences indépendantes et exprimées en moyenne ± SD, *p < 0,05
Discussion
Il a été rapporté que les NP de ZnO subissent une transformation physico-chimique en Zn5 (CO3 )2 (OH)6 avec la sortie de Zn 2+ au cours du processus naturel de vieillissement [23, 28]. Cependant, la cytotoxicité induite par les NP de ZnO transformées (vieillies) et les mécanismes sous-jacents restent flous. Ici, pour dévoiler le mécanisme de la cytotoxicité diversifiée entre les NP de ZnO fraîches et âgées, une analyse de séquençage d'ARN et un test RT-PCR ont été effectués. En outre, le transfert de Western a été appliqué pour examiner le niveau de protéine de la caspase 3, l'exécuteur clé de l'apoptose cellulaire.
Nos données ont montré que les NPs de ZnO vieillies induisaient beaucoup moins de cytotoxicité que les NPs de ZnO fraîches dans A L cellules. Le LC100 des deux NPs de ZnO fraîches (90-200 nm et 20 nm) dans notre étude actuelle était inférieure à 15 μg/mL (Fig. 3), ce qui est cohérent avec les conclusions précédentes selon lesquelles la LC100 de ZnO NPs avec 19-36 nm à NIH-3T3 ou cellule MSTO est d'environ 15 μg/mL [29]. Nous avons confirmé que les transformations environnementales des propriétés physico-chimiques des NP peuvent considérablement modifier leur toxicité. Il a été rapporté que le processus de sulfuration des NP de ZnO modifie leur charge, leur hydrophobie et leur état d'agrégation, entraînant l'adsorption des NP à l'état de sulfure dans la salive humaine, la sueur et le liquide de lavage broncho-alvéolaire. Et la protéine adsorbée par les NP de ZnO a formé une couronne protéique spéciale, qui a affecté son effet biologique [19]. Les phosphates largement présents dans les solutions physiologiques (comme la salive) pourraient convertir les NP de ZnO en ZnHPO4 métastable et Zn3 (PO4 )2 dans les 5 à 10 heures environ et a montré une cytotoxicité pour les cellules épithéliales du tube digestif [20]. Ivask et al. a prouvé l'occurrence d'une transformation complète des NPs de ZnO (≤ 3 μg/mL) dans le système d'exposition in vitro aux lymphocytes T humains (37 °C, milieu de culture cellulaire RPMI1640 contenant 10 % de FBS pendant 24 h) en utilisant l'absorption des rayons X par rayonnement synchrotron spectroscopie de structure proche du bord (XANES). Le spectre et la cytotoxicité des produits de transformation étaient cohérents avec ceux du ZnSO4 [21]. Nos résultats ont révélé la toxicité dose-dépendante et temporelle du ZnCl2 à A L cellules, où sa cytotoxicité est beaucoup plus faible que les NPs ZnO fraîches et vieillies (Fig. 3). L'observation explique en outre la découverte selon laquelle la cytotoxicité du ZnO NP frais n'est pas entièrement attribuée à son Zn 2+ libéré. [30].
Notre étude précédente a également montré que les NP de ZnO âgées présentent une puissance plus élevée pour déclencher des ROS (espèces réactives de l'oxygène), ainsi qu'une capacité atténuée à tuer les cellules par rapport aux NP de ZnO fraîches [23]. Nous pensons que la cytotoxicité inférieure induite par les NP de ZnO âgées pourrait être plus tolérable dans les cellules de mammifères. La présente étude des données de séquençage de l'ARN a illustré que les gènes apoptotiques ont été régulés à la hausse dans les cellules fraîches traitées au ZnO NP, où ils étaient beaucoup moins affectés dans les groupes âgés traités au NP. IL1α et IL1β sont membres de la famille des cytokines de l'interleukine 1. La libération d'IL1α et d'IL1β active l'apoptose partiellement dépendante de la caspase 8 [31]. CD69 code pour un membre de la superfamille des lectines dépendantes du calcium des récepteurs transmembranaires de type II. Une expression accrue de CD69 était associée à une expression accrue du marqueur annexine V d'apoptose et CD95 (Fas) [32]. JUN est une sous-unité du facteur de transcription AP-1. L'augmentation de l'activité JUN clive de manière protéolytique l'alpha-fodrine, un substrat de l'enzyme de conversion de l'interleukine 1beta (ICE) et la famille CED-3 de protéases à cystéine, ce qui provoque en outre la mort cellulaire programmée [33]. L'expression accrue de ces gènes apoptotiques a révélé que les NP fraîches déclenchent l'apoptose de plusieurs manières différentes. Après l'élévation de ces expressions géniques apoptotiques, les processus d'apoptose sont finalement exécutés par des protéines apoptotiques (Fig. 7). La caspase 3 est la protéase de base pour divers scénarios d'apoptose ; cleavage of this protein is necessary to activate both extrinsic and intrinsic apoptotic pathways [34, 35]. Therefore, detection of cleaved caspase 3 is a common method for identifying apoptosis induced by a wide variety of apoptotic signals [36]. Our Western blotting data revealed that, for both 20 nm and 90–200 nm ZnO NPs, sublethal exposure did not alter the level of Pro caspase 3 in all treatment groups. In contrast, cleaved Caspase 3 was significantly elevated by fresh NPs treatment, where aged NPs showed few (if any) effects on the level of cleaved caspase 3 (Fig. 6). Combined with RNA expression analysis, our results clearly elucidated the higher potency of fresh ZnO NPs in inducing cell apoptosis.
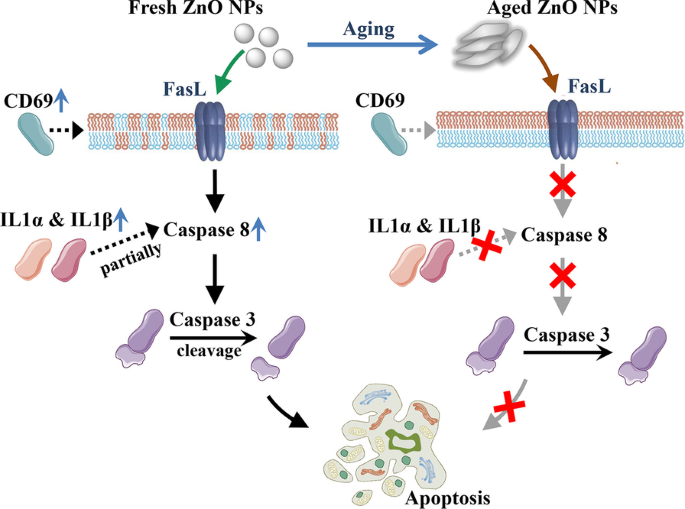
Model for Fresh ZnO NPs but not aged ZnO NPs induces Caspase 8- and Caspase 3-dependent apoptosis. The increased expression of apoptotic gene CD69 activates Fas and apoptosis annexin V expression in fresh ZnO NP-exposed mammalian cells. The increased expression of apoptotic gene IL1α and IL1β partially activates Caspase 8-dependent apoptosis. It further causes activation of Caspase 3 and induces apoptosis. All these changes in mRNA and protein level were not detectable in aged ZnO NPs-exposed mammalian cells
Conclusions
In the present study, the natural physicochemical transformation of ZnO NPs in ultrapure water was confirmed, and variations in cytotoxicity induced by fresh &aged NPs were investigated. We focused on RNA sequencing data from our aged ZnO NP-treated A L cells and that of fresh NPs from database. We compared those signaling pathway specifically enriched in aged NP-treated group, which are different from that of fresh NP- or ZnCl2 -treated groups. Our data indicated that the lower cytotoxicity of aged ZnO NPs is closely related to its attenuated ability in inducing apoptosis, while the transcriptional regulation of the multiple pathways activated by NPs promotes the establishment of cellular homeostasis in mammalian cells.
Disponibilité des données et des matériaux
Non applicable.
Abréviations
- NP :
-
Nanopowders
- ZnO :
-
Oxyde de zinc
- Zn5 (CO3 )2 (OH)6 :
-
Hydrozincite
- Zn (OH)2 :
-
Zinc hydroxide
- ZnCl2 :
-
Zinc chloride
- ZnSO4 :
-
Zinc sulfide
- ZnHPO4 :
-
Zinc hydrogen phosphate
- Zn3 (PO4 )2 :
-
Zinc phosphate
- A L cells:
-
Human–hamster hybrid cells
- CHO cells:
-
Chinese hamster ovary cells
- Jurket cells:
-
Peripheral blood T lymphocyte cells
- HMDM cells:
-
Human monocyte-derived macrophages
- NIH-3T3cells:
-
Mouse embryonic cells
- MSTO cells:
-
Human lung cancer cells
- RPMI1640:
-
Roswell Park Memorial Institute 1640
- ICE:
-
Interleukin 1beta-converting enzyme
- CED-3:
-
Caenorhabditis elegans death gene
- IL1α:
-
Interleukin 1alpha
- IL1β:
-
Interleukin 1beta
- mRNA:
-
Messenger ribonucleic acid
- cDNA:
-
Complementary deoxyribonucleic acid
- FBS :
-
Sérum fœtal bovin
- TEM :
-
Microscopie électronique à transmission
- XRD :
-
Diffraction des rayons X
- RT-PCR:
-
Real-time polymerase chain reaction
- CPI:
-
The Nanotechnology Consumer Product Inventory
- XANES:
-
Synchrotron radiation X-ray absorption near-edge structure spectroscopy
- RIPA:
-
Radio immunoprecipitation assay
- SDS-PAGE :
-
Polyacrylamide gel electrophoresis
- PVDF :
-
Fluorure de polyvinylidène
- ECL:
-
Enhanced chemiluminescence
- CCK-8 :
-
Kit de comptage cellulaire-8
Nanomatériaux
- Nanoparticules FePO4 biocompatibles :administration de médicaments, stabilisation de l'ARN et activité fonctionnelle
- Effets de l'épaisseur de la bicouche sur les propriétés morphologiques, optiques et électriques des nanolaminés Al2O3/ZnO
- Réglage des morphologies de surface et des propriétés des films de ZnO par la conception de la couche interfaciale
- Aptitude verte dans la synthèse et la stabilisation des nanoparticules de cuivre :activités catalytiques, antibactériennes, cytotoxiques et antioxydantes
- Fabrication et caractérisation de nano-clips de ZnO par le procédé à médiation par polyol
- Un examen comparatif in vivo des nanoparticules d'oxyde de cuivre et de zinc biosynthétisées par des voies d'administration intrapéritonéale et intraveineuse chez le rat
- Synthèse verte de nanoparticules de métal et d'oxyde métallique et leur effet sur l'algue unicellulaire Chlamydomonas reinhardtii
- Propriétés des nanoparticules d'oxyde de zinc et leur activité contre les microbes
- Le rôle de la robotique et de l'automatisation dans l'industrie 4.0



