Penta-graphène conçu par défaut et dopage pour la catalyse de la réaction d'évolution de l'hydrogène
Résumé
L'électrolyse de l'eau est une méthode durable et propre pour produire de l'hydrogène combustible via la réaction de dégagement d'hydrogène (HER). L'utilisation d'électrocatalyseurs stables, efficaces et peu coûteux pour HER pour remplacer les métaux nobles coûteux est fortement souhaitée. Dans cet article, en utilisant le calcul des premiers principes, nous avons conçu un défaut et du penta-graphene (PG) dopé N-, S-, P comme électrocatalyseur bidimensionnel (2D) pour HER, et sa stabilité, ses propriétés électroniques et les performances catalytiques ont été étudiées. L'énergie libre de Gibbs (ΔG H ), qui est le meilleur descripteur du HER, est calculé et optimisé, les résultats du calcul montrent que le ΔG H peut être de 0 eV avec des lacunes C2 et un dopage P sur les sites actifs C1, ce qui devrait être la performance optimale pour un catalyseur HER. De plus, nous révélons que plus le transfert de charge de PG vers H est important, plus ΔG est proche H est à zéro selon le calcul des différences de densité de charge électronique et l'analyse des charges de Bader. Ultérieurement, nous avons démontré que la performance HER préfère le mécanisme Volmer-Heyrovsky dans cette étude.
Contexte
En raison du changement climatique et de la pollution environnementale causée par l'utilisation de combustibles fossiles, l'exploitation et l'utilisation d'énergies propres et renouvelables sont la voie à suivre après aujourd'hui [1,2,3,4]. En tant que source d'énergie propre, renouvelable et respectueuse de l'environnement, l'hydrogène (H2 ) a attiré une attention considérable pour répondre aux futurs besoins énergétiques humains [5, 6]. L'électrolyse de l'eau est une méthode durable et propre pour produire H2 , et les électrocatalyseurs peuvent améliorer l'efficacité de la séparation de l'eau de manière observable [7, 8]. Pour la réaction de dégagement d'hydrogène (HER), les nanomatériaux à base de platine sont considérés comme les meilleurs électrocatalyseurs en raison d'une faible pente de Tafel, d'un faible surpotentiel, d'une énergie libre de Gibbs légèrement négative (ΔG H ) et une densité de courant d'échange élevée [9, 10], mais la rareté et le coût élevé entravent leurs applications à l'échelle industrielle [11]. Par conséquent, le développement d'électrocatalyseurs efficaces, riches en terre et à faible coût est essentiel pour HER [12,13,14].
En fait, une large gamme d'électrocatalyseurs abondants en terre a été étudiée et conçue pour HER [15,16,17]. Parmi ces matériaux, les nanomatériaux bidimensionnels (2D) offrent de nouvelles opportunités pour HER en raison de leurs propriétés structurelles et électroniques convaincantes. À ce jour, les dichalcogénures de métaux de transition (TMD) et les matériaux à base de graphène sont les groupes d'électrocatalyseurs 2D les plus importants et les plus étudiés pour HER [18,19,20,21,22,23]. Les catalyseurs TMD HER ont une faible surtension et une faible pente de Tafel, des propriétés électroniques inhabituelles et une stabilité élevée dans l'air, présentent des performances HER élevées, et différentes méthodes ont été utilisées pour améliorer leurs performances catalytiques [24, 25]. Les catalyseurs HER à base de graphène ont attiré une attention considérable et des études persistantes en raison de leurs mérites structurels distinctifs, tels qu'une conductivité électrique élevée, une grande surface et une bonne stabilité chimique [26, 27]. De nombreuses méthodes ont été utilisées pour améliorer l'activité catalytique, telles que le dopage par hétéroatome et l'ingénierie de défection [28, 29]. Parallèlement, des recherches intensives sur d'autres nouveaux allotropes de carbone 2D ont également été développées, telles que graphdiyne [30] et penta-graphène (PG) [31]. En tant qu'allotrope de carbone 2D, le PG est composé uniquement de pentagones de carbone et hérite de nombreuses propriétés exceptionnelles des matériaux 2D, telles qu'une bande interdite électronique finie, des sites actifs abondants et une grande surface. applications comme d'autres matériaux à base de graphène 2D [32,33,34,35]. Puisqu'il n'y a que des applications dans l'adsorption de gaz [36,37,38], H2 stockage [39, 40], matériaux d'anode à l'heure actuelle [41, 42], aucun rapport n'a jamais été trouvé sur l'application dans HER. Par conséquent, la recherche sur HER par PG est d'une grande importance et peut non seulement combler une telle lacune, mais aussi élargir la portée des catalyseurs HER à base de graphène. Cependant, le PG vierge s'avère inerte pour le HER avec un ΔG relativement grand H , ce qui signifie que l'adsorption d'hydrogène est difficile et inhibe le HER. Ceci est similaire aux problèmes rencontrés par le graphène vierge (ΔG H = 1,85 eV [43]). Le dopage d'hétéroatomes dans des matériaux à base de graphène pourrait ajuster leurs propriétés électroniques et catalytiques, ce qui en fait des catalyseurs potentiels pour les applications pratiques [3]. Par conséquent, nous avons réussi à adapter l'activité catalytique du PG par dopage d'hétéroatomes [44,45,46] et ingénierie de défection [47, 48].
Dans cet article, en utilisant le calcul des premiers principes, nous avons conçu et démontré un défaut et un PG dopé N, S, P et étudié leur stabilité et leurs propriétés électroniques et évalué leurs performances en tant qu'électrocatalyseurs HER. Nos résultats révèlent que le PG défectueux et dopé peut évidemment augmenter l'activité catalytique vers HER, par rapport au PG vierge. Il est également montré que le ΔG H peut être de 0 eV avec des lacunes C2 et un dopage P sur les sites actifs C1, ce qui devrait être la performance optimale pour un catalyseur HER, de sorte que le PG dopé P a le ΔG optimal H et une barrière d'énergie d'activation pour l'étape de détermination de la vitesse parmi les trois contreparties, et elle présente des performances plus favorables. Nous montrons en outre que l'activité catalytique provient des atomes de dopage incorporés, qui peuvent fournir une voie efficace pour le transport de charge pendant l'électrolyse, entraînant la réduction de ΔG H . Nous démontrons également que le mécanisme Volmer-Heyrovsky est plus préféré pour HER sur défaut et PG dopé. Nous avons comparé nos résultats avec ceux d'autres chercheurs sur le graphène, et on peut constater que la défection et l'ingénierie du dopage sont plus efficaces pour le PG dans la catalyse de l'HER. Ainsi, nos efforts sur le PG défectueux et dopé en font un électrocatalyseur très prometteur pour HER, et nos résultats fournissent une compréhension approfondie de la conception d'électrocatalyseurs efficaces et durables. Cette méthode peut également être appliquée à d'autres matériaux à base de graphène.
Méthodes de calcul
Nos calculs de premiers principes ont été effectués à l'aide du Vienna Ab initio Simulation Package (VASP) [49]. Les potentiels d'onde augmentée projetée (PAW) ont été utilisés pour analyser les interactions entre les électrons du noyau et les électrons de valence [50,51,52]. Les interactions d'échange d'électrons-corrélation ont été décrites en utilisant la fonctionnelle de Perdew-Burke-Ernzerhof (PBE) dans l'approximation de gradient généralisé (GGA) [53]. La fonction d'échange-corrélation DFT-D3 a été introduite dans l'optimisation structurelle pour prendre en compte l'interaction de van der Waals. L'espace vide le long du z -direction a été fixée à 20 Å afin d'éliminer les interactions entre PG et ses images périodiques.
La coupure d'énergie des ondes planes a été fixée à 500 eV. Le critère de convergence a été fixé à 10 −5 eV pour une énergie totale. Toutes les positions atomiques et les structures du réseau étaient complètement relâchées avec le seuil d'une force maximale de 0,02 eV Å −1 . Afin d'assurer la précision et l'efficacité du calcul, un maillage de points k centré Gamma avec une méthode de Monkhorst–Pack 5 × 5 × 1 a été utilisé pour toutes les structures considérées après test de convergence [54]. La quantité de transfert de charge entre les atomes C et les atomes H a été calculée en utilisant le code Bader [55]. Nous avons également calculé les barrières énergétiques d'adsorption H* à l'aide de la méthode de bande élastique d'escalade (CI-NEB) [56, 57]. Le CI-NEB est une méthode efficace pour déterminer le chemin d'énergie minimum et les points de selle entre une position initiale et finale donnée [58,59,60], et dans nos calculs CI-NEB, les structures initiale et finale ont été entièrement optimisées.
L'énergie d'adsorption (ΔE H ) est défini comme
$$\Delta E_{{\text{H}}} =E(*{\text{H}}) - E(*) - \frac{1}{2}E({\text{H}}_ {2} )$$où E (*H) et E (*) sont l'énergie totale des structures avec et sans adsorption d'hydrogène, respectivement, et E (H2 ) est l'énergie totale d'un H2 molécule.
L'énergie libre de Gibbs (ΔG H ) est défini comme :
$$\Delta G_{{\text{H}}} =\Delta E_{{\text{H}}} + \Delta E_{{{\text{ZPE}}}} - T\Delta S_{{\ texte{H}}}$$où ΔE H est l'énergie d'adsorption, ΔE ZPE est la différence d'énergie au point zéro, T est la température (298,15 K) et ΔS H est la différence d'entropie entre H adsorbé et H en phase gazeuse. Nous avons approximé l'entropie de l'adsorption d'hydrogène comme \(\Delta S_{{\text{H}}} \approx \frac{1}{2}(S_{{{\text{H}}_{2} }}^ { \circ } )\), où \(S_{{{\text{H}}_{2} }}^{ \circ }\) est l'entropie de la phase gazeuse H2 aux conditions standard, T ΔS H a été fixée à − 0,202 eV après calcul dans cette étude.
Résultats et discussion
Structure et activité catalytique du défaut et du PG dopé
La structure optimisée de PG est illustrée à la Fig. 1. Pour faciliter la discussion, nous regroupons ci-après les sp 3− et sp 2− les atomes C hybrides en tant que C1 et C2, respectivement. La distance entre C1 et C2 est de 1,55 Å, et la longueur de liaison C2-C2 est de 1,34 Å, ce qui est cohérent avec le résultat expérimental [31].
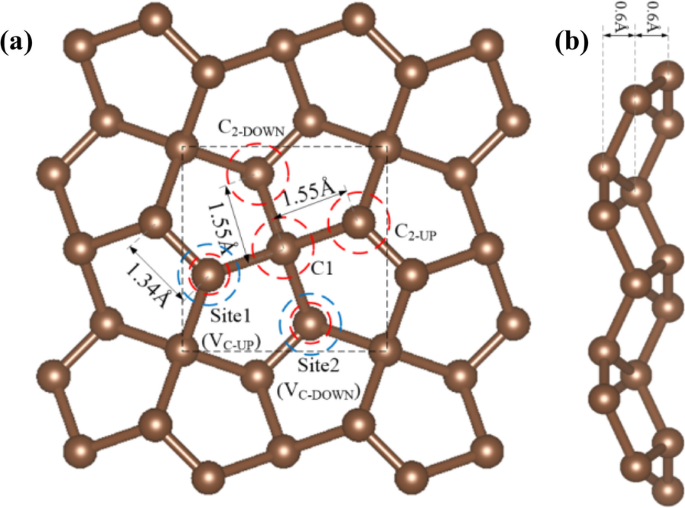
un Haut et b vues latérales de la structure optimisée de PG. Le rectangle en pointillés noirs indique la cellule unitaire, les cercles en pointillés bleus indiquent deux sites vacants C, les cercles en pointillés rouges indiquent les sites de dopage utilisés dans cet article
Au début, nous avons d'abord étudié les sites C1 et C2 dans le plan basal du PG vierge pour HER, le ΔG calculé H les valeurs sont respectivement de 2,43 eV et 2,72 eV. Ainsi, nos calculs montrent que le PG vierge s'avère inerte pour le HER avec un ΔG relativement grand H de H, ce qui signifie que l'adsorption d'hydrogène est difficile et HER est inhibée. Par conséquent, nous avons réussi à utiliser certaines méthodes pour adapter l'activité catalytique du PG. Nous avons recherché les sites actifs possibles pour le dopage et nous avons également étudié les sites actifs pour C1 et C2 avec un dopage N, S, P, respectivement. Les résultats des calculs montrent qu'aucune amélioration évidente de HER ne peut être obtenue si seule l'ingénierie du dopage a été introduite. Dans le cas de la structure dopée P, le ΔG calculé H les valeurs des sites C1 et C2 sont respectivement de 1,24 eV et 1,40 eV. Ultérieurement, nous avons étudié le défaut PG avec des sites de vacance C. Les résultats des calculs révèlent que la structure de vacance C1 ne peut pas améliorer les performances HER mais la structure de vacance C2 peut diminuer ΔG H évidemment, nous utilisons donc la structure des postes vacants C2 dans cette étude. Les structures optimisées avec VC-UP et VC-DOWN Les sites vacants C2 sont illustrés à la Fig. 2, les défauts d'inoccupation sont construits en supprimant les atomes C2 de C2-UP ou C2-DOWN site dans une supercellule de 24 atomes. Le ΔG calculé H les valeurs sont indiquées dans le tableau 1, où C1 et C2 sont les sites actifs pour l'adsorption d'hydrogène.
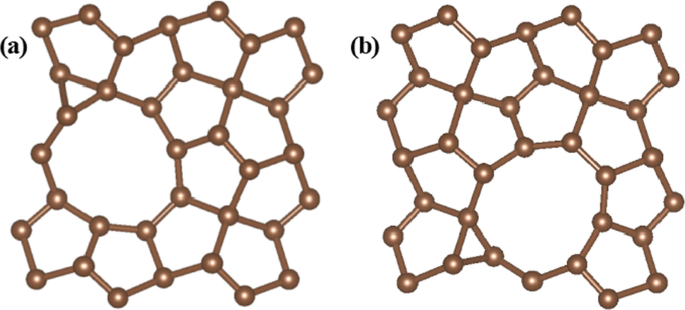
Les structures optimisées de PG avec deux sites de vacance C2 différents. un VC-UP Site de vacance C2, b VC-DOWN Site de vacance C2
Bien qu'il soit confirmé par nos calculs que les lacunes C2 sont efficaces pour améliorer l'activité HER, le PG avec la structure des lacunes C2 n'est pas encore optimal pour un catalyseur HER. Ainsi, nous avons enquêté plus avant sur le défaut et le PG dopé pour HER. Nous avons utilisé le PG avec la vacance C2 comme structure initiale, qui est illustrée à la Fig. 2, puis nous avons étudié tous les différents sites actifs possibles avec un dopage N, S, P, y compris C1, C2-UP et C2-DOWN des sites. En conséquence, nous avons constaté que de meilleures performances HER pouvaient être obtenues avec une combinaison de vacance C2 et de dopage hétéroatome. Nous avons étudié toutes les structures possibles, et les résultats ont montré qu'il existe deux structures qui peuvent atteindre de meilleures performances HER, une structure est une combinaison du C2-UP vacance et dopage hétéroatome dans le C2-DOWN site, et l'autre est une combinaison du C2-DOWN vacance et dopage hétéroatome dans le C2-UP site. Nous nous sommes donc concentrés sur ces deux structures et avons découvert qu'elles peuvent déplacer le ΔG H valeurs proches de zéro. Les structures optimisées sont illustrées à la figure 3 et les longueurs de liaison calculées sont résumées dans le tableau 2.
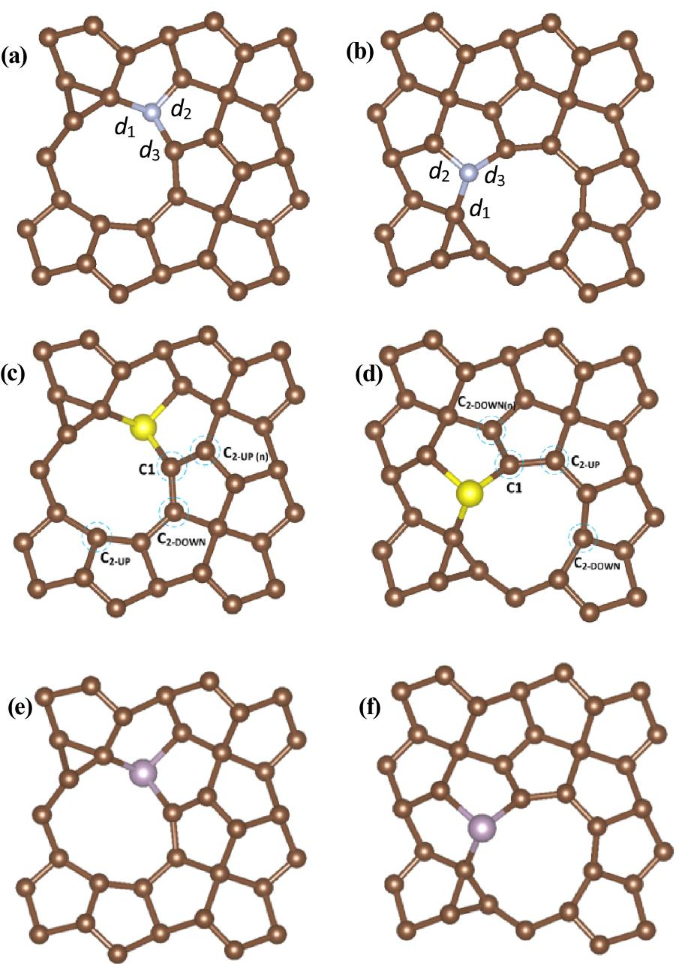
Les structures optimisées pour le défaut et le PG dopé avec les deux sites de vacance C2 différents, a VC-UP N-dopé, b VC-DOWN N-dopé, c VC-UP dopé S, d VC-DOWN dopé S, e VC-UP dopé P, f VC-DOWN Dopé P, les cercles bleus en pointillés indiquent des sites actifs possibles pour le dégagement d'hydrogène
Nous pouvons voir qu'il existe une légère différence entre les longueurs de liaison correspondantes du PG dopé N et celle du PG vierge. En raison du grand rayon des atomes S et P, ces deux structures subissent beaucoup plus de distorsion, mais elles peuvent toutes les deux conserver la structure de PG.
Pour étudier la stabilité du PG avec la lacune C2 et le dopage hétéroatome, nous avons calculé l'énergie de formation, qui est définie comme
$$E_{{\text{f}}} =\left( {E_{{\text{t}}} - E_{{\text{V}}} + E_{{\text{C}}} - E_{{\text{d}}} - \frac{1}{2}\mu_{{\text{H}}} } \right)$$où E t est l'énergie totale du défaut et du système dopé, et E V est l'énergie de la vacance C2 PG, E C est l'énergie moyenne par atome de C du PG vierge, E d est l'énergie des atomes dopants,\(\mu_{{\text{H}}}\) est tiré de l'énergie totale du H2 molécule, respectivement. L'un de nos résultats de calcul sur les énergies de formation des deux structures précédentes avec des sites actifs C1 pour HER est illustré à la Fig. 4. Nous pouvons voir que les énergies de formation négatives indiquent un défaut énergétiquement favorable et réalisable et un PG dopé S-, P. De même, E f les valeurs des structures dopées N avec des sites actifs pour HER sont toutes positives. Nous avons étudié tous les sites actifs possibles et avons obtenu des résultats similaires à ceux indiqués sur la figure 4, nous n'étudierons donc que les PG dopés S et P. Selon la définition, un E plus négatif f La valeur indique une stabilité plus élevée de la structure, de sorte que le PG dopé au P a une excellente stabilité, ainsi que de bonnes performances HER.
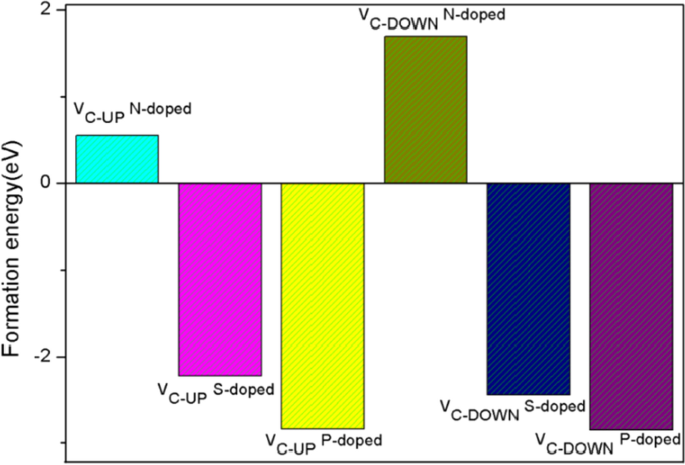
Énergie de formation de deux structures PG à défaut initial et dopées avec des sites actifs C1 pour HER, une valeur plus négative indique une stabilité plus élevée de la structure
Origine de l'activité catalytique HER
DOS et structures de bande
Pour parvenir à une compréhension approfondie de la nature de la lacune C2 et de l'ingénierie du dopage dans l'activité HER, nous avons étudié le DOS total et projeté, la structure de bande électronique du défaut et le PG dopé S-, P. La figure 5 est l'un de nos résultats de calcul sur les structures de bandes électroniques, le DOS total et projeté de PG vierge, VC-UP , VC-UP dopé S et VC-UP PG dopé P.
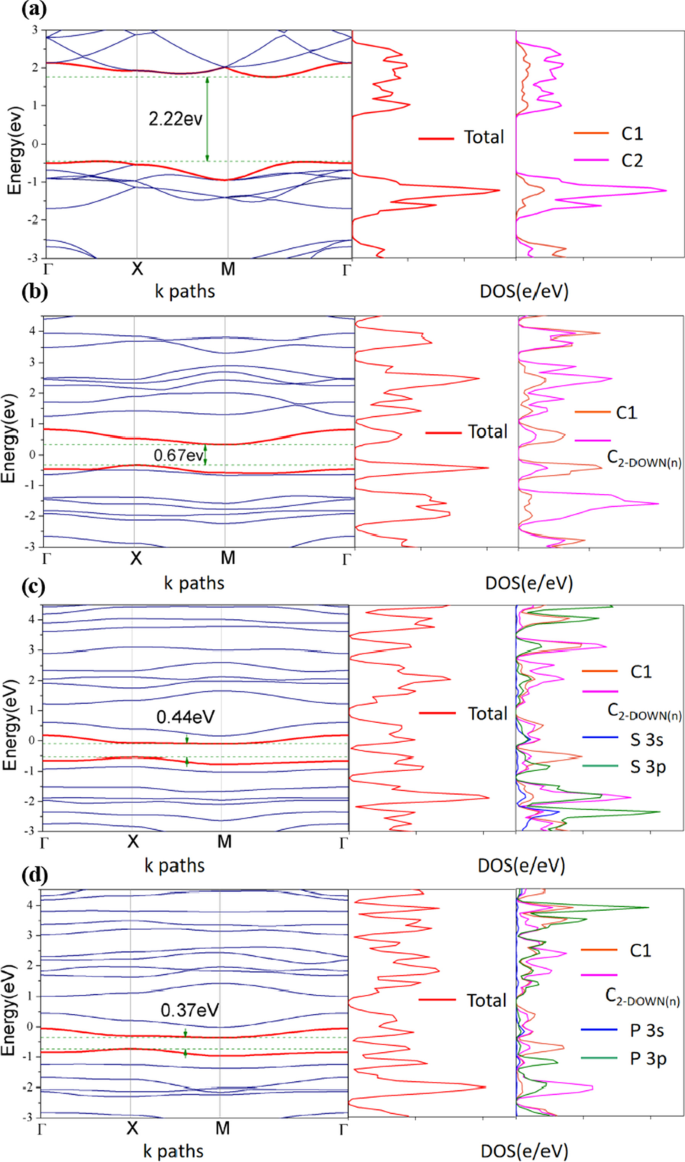
Structure de bande électronique, DOS total et projeté du défaut et PG dopé. un PG impeccable, b VC-UP Site vacant C2, c VC-UP dopé S et d VC-UP Dopé au P, respectivement. Les structures de c et d comme le montre la Fig. 3. Ils sont calculés en utilisant la fonction PBE, le niveau de Fermi est décalé à 0,00 eV
D'après la figure, nous pouvons voir que lorsque la vacance C2 est introduite, de nouveaux états de défaut mis en évidence par des courbes rouges apparaissent dans la bande interdite près du niveau de Fermi. Évidemment, ces nouveaux états découlent de la vacance de C2. De plus, lorsque le dopage des hétéroatomes S, P est introduit, la bande interdite se rétrécit (de 2,22 eV [31] à 0,37 eV) et le nombre de nouveaux états de défauts à proximité du niveau de Fermi augmente, ce qui peut éventuellement améliorer la force d'adsorption de H*.
Cependant, nous avons constaté que le DOS de VC-UP près du niveau de Fermi est beaucoup plus grand que celui du PG vierge. De plus, la densité électronique près du niveau de Fermi de la lacune C2 et du PG dopé S, P est encore augmentée par rapport au PG vierge. Nous avons également constaté que les orbitales S 3p et P 3p subissent une hybridation significative avec les états C1 et C2, conduisant à de fortes interactions entre les hétéroatomes et C, et la formation de liaisons S–C et P–C. Ces résultats démontrent que la combinaison de la lacune C2 et du dopage des hétéroatomes S, P peut être une meilleure ingénierie pour améliorer l'activité HER.
Différence de densité électronique et transfert de charge
De plus, pour étudier l'interaction de liaison entre l'atome H et le PG, nous avons calculé les différences de densité de charge électronique pour le défaut et le PG dopé S, P avec différents sites actifs pour le dégagement d'hydrogène. L'un de nos résultats de calcul sur la différence de densité de charge électronique et l'analyse des charges de Bader pour un C2-DOWN La lacune et le PG dopé au P avec H* adsorbé sur les différents sites actifs pour l'adsorption d'hydrogène sont illustrés à la Fig. 6. Les couleurs jaune et bleu représentent respectivement l'accumulation et la réduction de charge. Il est montré que les électrons s'accumulent autour des atomes H et diminuent autour des atomes C qui sont liés aux atomes H, indiquant un transfert de charge de PG vers H*. Le transfert de charges est également confirmé par l'analyse des charges Bader. Les résultats du calcul montrent qu'il y a 0,18, 0,04, 0,02 et 0,01 électrons transférés vers H* à C1, C2-DOWN , C2-DOWN(n) et C2-UP sites, respectivement. Nous montrons en outre que plus le transfert de charge de PG vers H* est important, plus ΔG est proche H est à zéro, ce qui signifie les performances optimales pour un catalyseur HER, comme le montre la Fig. 7. On peut voir sur la Fig. 6 que les électrons sont transférés de PG à H*, ce qui entraîne une augmentation de la densité de charge des liaisons, ce qui signifie que la stabilisation des espèces H* dans les performances HER peut provenir de la densité de charge améliorée des atomes C dopés P, indiquant que les atomes P sont intrinsèquement plus avantageux pour interagir avec les atomes H que les atomes C. Nous avons également remarqué que H* est absorbé sur C au lieu de P, indiquant que la densité de charge accrue peut contribuer à l'électrocatalyseur sur l'atome H. Ainsi, nos calculs montrent que le dopage P dans le PG peut conduire à une adsorption accrue de H* sur les atomes de C. Comme mentionné ci-dessus, les calculs DFT ont également suggéré que le dopage P dans PG pourrait améliorer beaucoup plus efficacement l'activité HER que celle du dopage S.
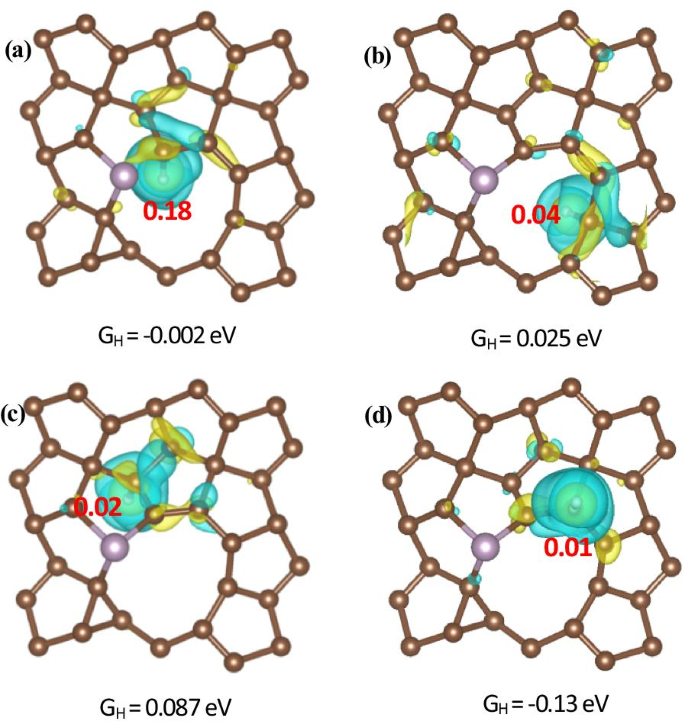
Vues de dessus de la différence de densité de charge électronique et de l'analyse des charges de Bader pour un C2-DOWN vacance et PG dopé P avec H adsorbé au a C1, b C2-DOWN , c C2-DOWNn et d C2-UP des sites. Le niveau d'isosurface est de 0,004 e/Bohr 3 . Les couleurs jaune et bleu représentent respectivement l'accumulation et la réduction des charges
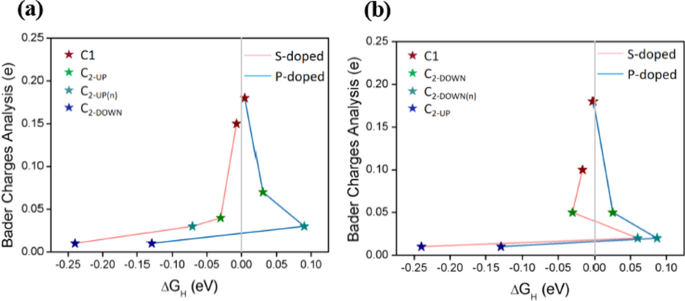
Relation entre ΔG H et l'analyse des frais Bader pour a VC-UP dopé S, VC-UP dopé P et b VC-DOWN dopé S, VC-DOWN Structures dopées P. Le ΔG H les valeurs et les sites actifs sont indiqués dans le tableau 3
Activité du défaut et du PG dopé vers ELLE
Gibbs Free Energies of HER
Le ΔG H est le descripteur vital du HER pour une variété d'électrocatalyseurs, le ΔG optimal H la valeur pour un électrocatalyseur est nulle, donc l'adsorption et la désorption de H* peuvent se produire spontanément sans barrière d'énergie d'activation [61, 62]. Pour évaluer l'activité HER du PG et étudier l'ingénierie de défection et de dopage, nous avons calculé le ΔG H d'ELLE. Un de nos résultats de calcul sur ΔG H par rapport à la coordonnée de réaction du HER pour le PG est illustré à la Fig. 8, où C1 et C2 à l'intérieur des crochets sont des sites actifs pour l'adsorption d'hydrogène.
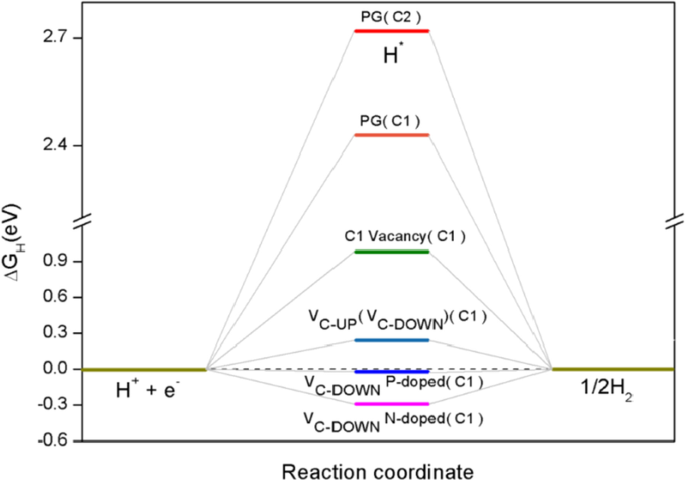
Énergie libre de Gibbs par rapport aux coordonnées de réaction du HER pour PG, où C1 et C2 à l'intérieur des crochets sont des sites actifs pour l'adsorption d'hydrogène
Nos calculs montrent que le PG vierge s'avère inerte pour le HER avec une énergie libre Gibbs relativement grande de H* (ΔG H = 2,72 eV(C2), ΔG H = 2,43 eV(C1)). Lorsque des postes vacants sont introduits, il existe deux sites de vacance C différents, le site de vacance C1 et le site de vacance C2. Nous avons calculé le ΔG H sur les deux sites et a constaté que la vacance C2 peut notamment diminuer ΔG H (ΔG H = 0,24 eV), ce qui indique que H* s'adsorbe préférentiellement sur les structures de lacune C2. Les structures optimisées avec des sites vacants C2 (VC-UP et VC-DOWN ) sont illustrés à la Fig. 2. Bien que les lacunes C2 montrent une amélioration significative par rapport au PG vierge, elles ne sont toujours pas optimales pour l'adsorption d'hydrogène, donc l'ingénierie du dopage est explorée pour améliorer les performances HER. Nous montrons nos effets des lacunes C2 et du dopage hétéroatome S, P sur l'activité HER et optimisons les performances HER. Le ΔG H les valeurs sont résumées dans le tableau 3 et les sites actifs pour le dégagement d'hydrogène sont indiqués sur la figure 3.
Les résultats du calcul révèlent que ΔG H diminue de manière significative, démontrant que la défection et l'ingénierie du dopage sont très efficaces pour réduire ΔG H . Remarquablement, nous avons constaté que le ΔG H valeurs des sites actifs C1, C2-UP et C2-UP(n) pour VC-UP , sites actifs C1, C2-DOWN et C2-DOWN(n) pour VC-DOWN sont très proches de zéro, en particulier pour deux sites C1, ce qui signifie que les conditions optimales peuvent être atteintes, qui sont nettement supérieures au PG vierge. Et nous avons comparé nos résultats avec des travaux antérieurs d'autres chercheurs sur le graphène, par exemple, le graphène avec vacance C (ΔG H = − 2.108 eV) [28], graphène avec N-dopé (ΔG H = − 0.693 eV) [28], graphène à lacune C et dopé N (ΔG H = − 0,595 eV) [28], graphène dopé S (ΔG H = − 0,30 eV) [29] et du graphène avec N/S co-dopé (ΔG H = − 0,12 eV) [29]. Nous pouvons constater que la défection et l'ingénierie du dopage sont plus efficaces pour PG. Ainsi, nos résultats suggèrent clairement que le ΔG H de PG peut être manipulé en appliquant une technique de défection et de dopage pour atteindre l'activité HER optimale.
Les voies de réaction du défaut et du PG dopé
Le HER procède d'un processus électrochimique en plusieurs étapes, via l'une des deux voies connues sous le nom de mécanismes Volmer-Tafel et Volmer-Heyrovsky. La première étape de HER est l'adsorption de H* sur la surface de l'électrocatalyseur (c'est-à-dire la réaction de Volmer), qui est décrite par H + + e − → H*. Ensuite, H* se combine avec H + et un électron (e − ) pour former un H2 molécule, connue sous le nom d'étape de Heyrovsky, qui est décrite par H* + H + + e − → H2 . Alternativement, H2 molécule peut être formée via l'étape de Tafel, c'est-à-dire la combinaison de deux H* sur la surface de l'électrocatalyseur, qui est décrite par 2H* → H2 [63].
Pour étudier les effets d'ingénierie de défection et de dopage sur PG et mieux comprendre le mécanisme de l'activité supérieure de HER, les barrières énergétiques des réactions de Tafel et Heyrovsky avec C2-UP et C2-DOWN postes vacants, S-, P-dopé PG pour le site C1 ont été calculés. L'état initial (IS), l'état final (FS) et l'état de transition (TS) sont affichés sur la figure 9 avec les barrières énergétiques correspondantes. Pour la réaction de Tafel, la recombinaison de 2H* montre des barrières énergétiques de 1,51 eV (dopé S), 1,32 eV (dopé P), respectivement. Considérant que la sortie d'un H2 molécule dans la réaction de Heyrovsky impliquée dans un proton réagissant avec un H* adsorbé doit surmonter les barrières énergétiques de 1,01 eV (dopé S), 0,99 eV (dopé P), respectivement. Les résultats révèlent que les barrières énergétiques de la réaction de Tafel sont significativement plus élevées que celles de la réaction de Heyrovsky. Ainsi, le HER sur défaut et PG dopé préfère le mécanisme Volmer-Heyrovsky.
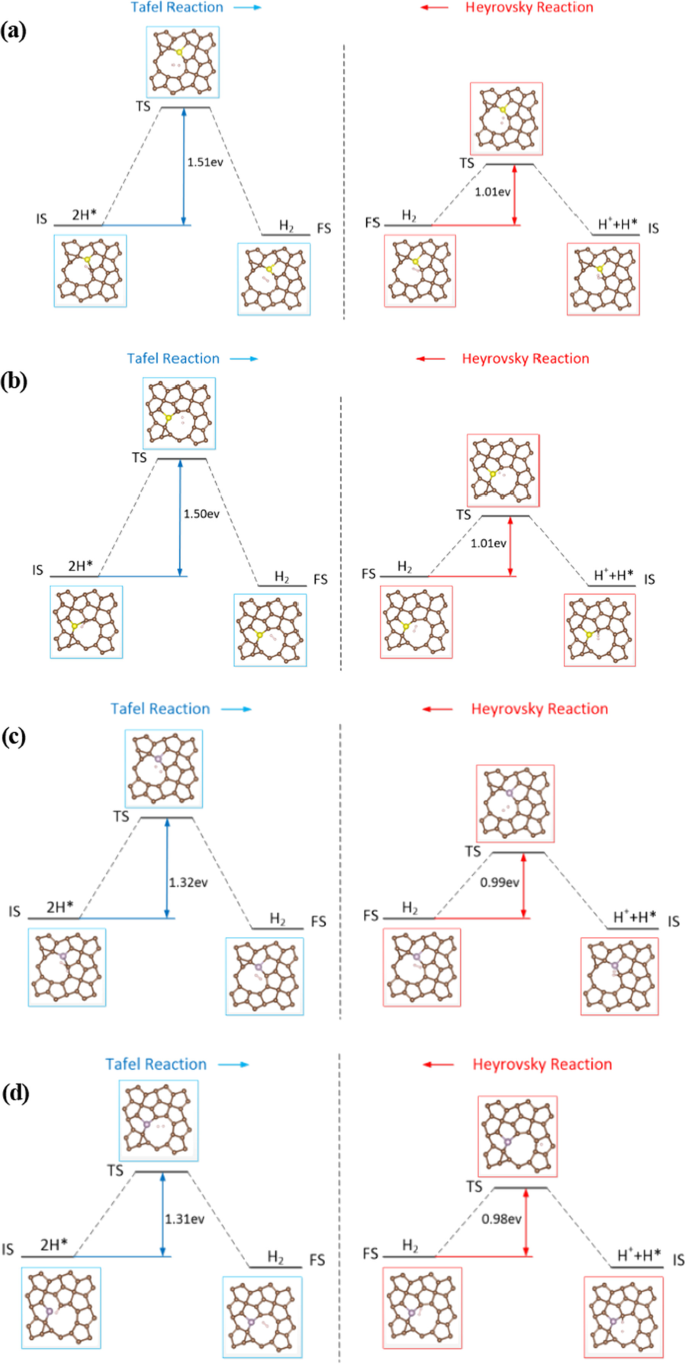
Cheminements schématiques pour l'HER. Profils énergétiques pour les réactions de Tafel et Heyrovsky avec a C2-UP poste vacant et PG dopé S, b C2-DOWN poste vacant et PG dopé S, c C2-UP poste vacant et PG dopé P, d C2-DOWN vacance et PG dopé P. L'état initial (IS), l'état de transition (TS) et l'état final (FS) sont indiqués dans le schéma avec les barrières énergétiques correspondantes
Conclusions
Nous avons théoriquement conçu une lacune C et un PG dopé N, S, P et étudié systématiquement leur stabilité et leur rôle unique d'électrocatalyseur envers HER. Nous constatons que l'ingénierie de défection et de dopage possède une performance HER supérieure à celle du PG vierge. Il est important de noter que l'activité HER optimale peut être obtenue avec des lacunes C2 et un dopage d'hétéroatomes S, P, ce qui indique que les propriétés catalytiques du défaut et du PG dopé peuvent être ajustées facilement et efficacement. Nos calculs révèlent que ΔG H diminue significativement avec les lacunes C2 et le dopage S, P hétéroatome, et les conditions optimales peuvent être atteintes avec le dopage P sur les sites actifs C1, pour lesquels la défection ou l'ingénierie du dopage ne peuvent à eux seuls atteindre les conditions optimales. L'analyse de la structure électronique montre que lorsque la lacune C2 et le dopage des hétéroatomes S, P sont introduits, plusieurs nouveaux états de défection se rapprochent du niveau de Fermi, conduisant à une bande interdite plus étroite et à une amélioration de la force d'adsorption d'hydrogène. On retrouve également le transfert de charge de PG vers H* en calculant les différences de densité de charge électronique, plus le transfert de charge vers H* est important, plus ΔG est proche H valeurs à zéro en utilisant l'analyse des charges de Bader, qui indique les performances optimales pour un catalyseur HER. Et nous démontrons en outre que le HER sur défaut et PG dopé préfère le mécanisme Volmer-Heyrovsky. Ainsi, notre étude montre que le défaut conçu et le PG dopé sont hautement activés vis-à-vis de l'électrocatalyseur HER, l'activité HER optimale peut être atteinte et des sites d'activité catalytique abondants sont fournis. On s'attend à ce que les stratégies développées dans cet article puissent être appliquées à la conception d'électrocatalyseurs 2D à base de graphène pour des applications HER à faible coût et hautes performances.
Disponibilité des données et des matériaux
Les ensembles de données soutenant les conclusions de cet article sont inclus dans l'article, et de plus amples informations sur les données et les matériaux pourraient être mises à la disposition de la partie intéressée sur demande motivée adressée à l'auteur correspondant.
Abréviations
- ELLE :
-
Réaction de dégagement d'hydrogène
- PG :
-
Penta-graphene
- 2D :
-
Deux dimensions
- ΔG H :
-
L'énergie libre de Gibbs
- TMD :
-
Les dichalcogénures de métaux de transition
- VASP :
-
Package de simulation ab initio de Vienne
- PAW :
-
Onde augmentée projetée
- PBE :
-
Le Perdew–Burke–Ernzerhof
- GGA :
-
L'approximation du gradient généralisé
- CI-NEB :
-
L'élastique d'escalade image-nudge
- EST :
-
État initial
- FS :
-
L'état final
- TS :
-
L'état de transition
Nanomatériaux
- Nanofibres et filaments pour une administration améliorée des médicaments
- Nanoparticules pour le traitement du cancer :progrès actuels et défis
- MoS2 avec épaisseur contrôlée pour l'évolution électrocatalytique de l'hydrogène
- Dopage de substitution pour les minéraux d'aluminosilicate et performances supérieures de fractionnement de l'eau
- Synthèse et propriétés électrochimiques des matériaux cathodiques LiNi0.5Mn1.5O4 avec dopage composite Cr3+ et F− pour batteries lithium-ion
- Hétérostructure hiérarchique des sphères creuses ZnO@TiO2 pour une évolution photocatalytique hautement efficace de l'hydrogène
- Modification du cocatalyseur en alliage PtNi de l'hybride g-C3N4/GO sensibilisé à l'éosine Y pour une évolution efficace de l'hydrogène photocatalytique en lumière visible
- Saponines de Platycodon de Platycodi Radix (Platycodon grandiflorum) pour la synthèse verte de nanoparticules d'or et d'argent
- Relations mathématiques magiques pour les nanoclusters :errata et addendum



