Dopage de substitution pour les minéraux d'aluminosilicate et performances supérieures de fractionnement de l'eau
Résumé
Le dopage de substitution est une stratégie dans laquelle des impuretés atomiques sont éventuellement ajoutées à un matériau hôte pour promouvoir ses propriétés, tandis que l'évolution de la structure géométrique et électronique du minéral nanoargile naturel lors du dopage de métal de substitution est encore ambiguë. Cet article a d'abord conçu une stratégie de dopage efficace au lanthane (La) pour l'argile nanotubulaire (nanotube d'halloysite, HNT) via l'équilibre dynamique d'un atome de substitution en présence d'AlCl3 saturé. solution et une caractérisation systématique des échantillons a été effectuée. D'autres calculs de la théorie de la fonctionnelle de la densité (DFT) ont été effectués pour révéler l'évolution de la structure géométrique et électronique lors du dopage du métal, ainsi que pour vérifier l'effet au niveau atomique du dopage La. La charge de CdS et ses performances de fractionnement de l'eau correspondantes pourraient démontrer l'effet du dopage La. Des nanoparticules de CdS (11 % en poids) ont été uniformément déposées à la surface d'un nanotube d'halloysite dopé au La (La-HNT) avec une taille moyenne de 5 nm, et le taux de dégagement d'hydrogène photocatalytique notable de CdS/La-HNT a atteint jusqu'à 47,5 mol/h. Les résultats pourraient fournir une nouvelle stratégie pour le dopage par ions métalliques et un aperçu constructif du mécanisme de dopage substitutionnel.
Contexte
Les minéraux aluminosilicatés (par exemple, la kaolinite [1,2,3], la zéolite [4, 5] la montmorillonite [6, 7] et l'halloysite [8,9,10,11,12,13]) ont été largement étudiés comme support de catalyseur car ils sont non toxiques pour l'environnement et disponibles en abondance à peu de frais à partir de gisements naturels. Un certain nombre de techniques ont été utilisées pour améliorer les fonctionnalités des matériaux de support, telles que le revêtement polymère [14, 15], le revêtement carbone [8] et le dopage atomique [16,17,18,19]. Des minéraux d'aluminosilicate dopés peuvent se former dans la nature, mais leur synthèse en laboratoire permet diverses propriétés avec les dopants spécifiés [20,21,22,23]. L'incorporation d'ions métalliques dans la structure de la couche d'aluminosilicate rend le nanomatériau correspondant attrayant pour diverses applications, notamment la catalyse [24, 25, 26], la libération contrôlée de produits pharmaceutiques [27, 28] ainsi que les batteries lithium-ion [29, 30]. Récemment, sur la base de calculs de la théorie fonctionnelle de la densité (DFT), la stabilité, les propriétés électroniques et mécaniques des aluminosilicates nanostructurés, comme l'imogolite, l'halloysite et le chrysotile, ont été révélées [31]. Cependant, le mécanisme de dopage substitutionnel et l'évolution de la structure électronique d'un métal en aluminosilicates sont encore ambigus [32, 33].
Dans le but d'améliorer notre compréhension de ce mécanisme, nous avons conçu une stratégie de dopage efficace pour l'un des minéraux d'aluminosilicate représentatifs (nanotube d'halloysite [34,35,36], HNT) à travers l'équilibre dynamique d'un atome de substitution en présence de AlCl3 solution contenant du sel de lanthane. Ensuite, une stratégie de dopage atomique de substitution basée sur le dopage La dans la structure HNT et la partie remplacée de l'atome Al de la feuille Al-O est présentée. Halloysite (HNTs, Al2 Si2 O5 (OH)4 nH2 O), en tant que minéral argileux naturel, contient de la gibbsite octaédrique Al(OH)3 et tétraédrique SiO4 feuilles, et il se compose également de cylindres creux formés par plusieurs couches laminées. Le CdS est un matériau semi-conducteur attrayant qui peut convertir l'énergie solaire en énergie chimique sous irradiation de lumière visible. L'incorporation de nanoparticules de CdS dans les La-HNT et ses performances de séparation de l'eau correspondantes pourraient démontrer les effets du dopage au La. Le processus de diffusion d'Al 3+ solution saturée et les feuilles d'alumine de l'halloysite, le changement des formes cristallines et des structures de surface, et la possibilité d'une activité catalytique accrue ont été étudiés en détail. Les microstructures et les morphologies des échantillons ont été caractérisées et la structure interfaciale entre CdS et La-HNT a été étudiée. L'activité photocatalytique de l'hydrogène a été évaluée et le rôle du La-HNT dans l'amélioration de l'activité catalytique du CdS/La-HNT a également été étudié.
Méthodes
Section expérimentale
Préparation du matériel
Les nanotubes d'halloysite (HNT) ont été obtenus auprès de Hunan, en Chine. Tous les produits chimiques étaient de qualité analytique et utilisés sans autre purification. Les HNT ont été prétraités par dispersion d'émulsion, filtration, lavage à l'eau distillée et séchage pendant 8 h à 313 K. Les La-HNT ont été synthétisés par une voie hydrothermale modifiée. Une quantité de 34,3 g d'AlCl3 a été dissous dans 60 mL d'eau déminéralisée pour former AlCl3 solution sursaturée, tandis que 3 mmol HNT et 6 mmol La(NO3 )3 ·6H2 O ont été dissous dans de l'eau déminéralisée (5 mL), respectivement. Puis La(NON3 )3 ·6H2 La solution O et la suspension HNT ont été ajoutées à AlCl3 solution sursaturée pour former une suspension. La suspension résultante a été agitée pendant 10 minutes dans un bécher en polypropylène et soniquée pendant 10 minutes pour briser les agrégats de matière de départ. Le volume était limité à 70 mL (L/S = 70–80). Le mélange a été transféré dans une bouteille en téflon (100 mL) et traité sous une pression autogénérée sans agitation à 373 K pendant 48 h. L'autoclave a été naturellement refroidi à température ambiante, et les précipités obtenus ont été filtrés et lavés plusieurs fois avec de l'eau déminéralisée, et enfin séchés à 353 K sous vide (noté La-HNT). À titre de comparaison, des HNT traités à l'acide synthétisés par 1,00 g de HNT ont été dissous dans 250 mL d'une solution de HCl 6 M à 373 K dans un bain-marie. La réaction a été effectuée dans un erlenmeyer pendant 4 h sous agitation constante. La fiole conique a été naturellement refroidie à température ambiante, et les précipités obtenus ont été filtrés et lavés plusieurs fois avec de l'eau déminéralisée, et enfin séchés à 353 K sous vide (appelé HNT traité à l'acide).
Les CdS/La-HNT ont été synthétisés en utilisant la méthode d'adsorption et de réaction par couche ionique successive (SILAR), 3 mmol de La-HNT ont été dissous dans 50 mL 0,5 M de Cd(NO3 )2 solution d'éthanol pendant 5 min, rincée à l'éthanol, puis dissoute pendant 5 min supplémentaires dans 50 mL 0,5 M Na2 S solution de méthanol, et rincé à nouveau avec du méthanol. Un tel cycle d'immersion a été répété plusieurs fois jusqu'à ce que le dépôt souhaité de nanoparticules de CdS soit atteint. Ensuite, les précipités obtenus ont été filtrés et lavés plusieurs fois avec de l'eau déminéralisée, et enfin séchés à 353 K sous vide (noté CdS/D-Lax-HNT).
Caractérisation
L'analyse par spectroscopie photoélectronique à rayons X (XPS) a été effectuée à l'aide d'un spectromètre Thermo Fisher Scientific K-Alpha 1063 équipé d'une source de rayons X monochromatique Al Ka. La pression de la chambre d'essai a été maintenue en dessous de 10 −9 mbar lors de l'acquisition spectrale. L'énergie de liaison XPS (BE) a été référencée en interne au C 1s pic (BE = 284,1 eV). Les phases cristallines ont été identifiées par analyse XRD à l'aide d'un diffractomètre à poudre RIGAKU D/max-2550VB1 18 kW avec rayonnement Cu Ka (λ = 1,5418 Å). Les données ont été collectées dans la plage de balayage 2θ = 10–80°, avec une vitesse de balayage de 2°/min. Les spectres FTIR ont été enregistrés à l'aide d'un spectrophotomètre Nicolet 5700. La surface spécifique a été calculée à partir des isothermes d'adsorption d'azote en utilisant l'équation de Brunauer-Emmet-Teller (BET). Des images de microscopie électronique à transmission (MET) ont été obtenues à l'aide d'un instrument JEOL JEM-200CX équipé d'une spectroscopie à rayons X à dispersion d'énergie (EDS) à une tension d'accélération de 200 kV. Le spectre (PL) de l'échantillon a été détecté sur un spectromètre à fluorescence Hitachi H-4500 en utilisant une lampe Xe comme source lumineuse. Les spectres UV-vis d'échantillons en solution aqueuse ont été obtenus à l'aide d'un spectromètre UV-2400 (Shimadzu Corp., Japon). État solide 29 Si et 27 Les spectres RMN Al MAS ont été enregistrés à l'aide d'un spectromètre Bruker AMX400 dans un champ magnétique statique de 9,4 T à une fréquence de résonance de 79,49 MHz. L'analyse électrochimique a été réalisée dans une cellule conventionnelle à trois électrodes en utilisant un fil noir de platine et une électrode au calomel saturé (SCE) comme contre-électrode et électrode de référence, respectivement. L'électrode de travail a été préparée sur verre conducteur FTO (oxyde d'étain fluor). En détail, 20 mg d'échantillon ont été ajoutés dans 10 mL d'éthanol et ont formé une suspension uniforme. Comme dans un procédé standard de spin-coating, la suspension d'éthanol a été étalée sur du verre FTO, dont la partie latérale a été préalablement protégée à l'aide de scotch. Le filage était à une vitesse élevée de 150 rps, puis séché dans un four à 70 °C pendant 1 h. Les réponses au photocourant transitoire de différents échantillons ont été mesurées dans 0,1 M Na2 S + 0,02 M Na2 SO3 solution aqueuse sous irradiation à la lumière visible (≥420 nm) à 0 V vs SCE. La zone éclairée de l'électrode de travail est de 2 cm 2 . L'expérience photoélectrochimique a été réalisée en utilisant un poste de travail électrochimique CHI-660A (ChenHua Instruments Co. Ltd., Shanghai, Chine). La spectroscopie d'impédance électrochimique (EIS) a été mesurée avec un poste de travail électrochimique CHI-660A (ChenHua Instruments Co. Ltd., Shanghai, Chine), et l'électrolyte était composé de 0,01 mol/L d'hexacyanoferrate de potassium (III), 0,01 mol/L d'hexacyanoferrate de potassium (II) et 0,5 mol/L de KCl. Le potentiel appliqué était un potentiel de circuit ouvert (OCP).
Réaction photocatalytique
Les réactions de fractionnement de l'eau ont été effectuées dans une circulation fermée de gaz sous vide. Un échantillon de 100 mg de poudre de photocatalyseur a été dispersé dans une solution aqueuse de 300 mL de 0,1 M de Na2 S et 0,1 M Na2 SO3 . La source lumineuse était une lampe Xe de 300 W et l'intensité lumineuse atteignant la surface de la solution réactionnelle était de 135 mW/cm 2 . Le montant de H2 l'évolution a été déterminée à l'aide d'un chromatographe en phase gazeuse (Agilent Technologies :6890 N).
Détails de calcul
Tous les calculs ont été effectués avec le code CASTEP, basé sur la théorie fonctionnelle de la densité du premier principe (DFT). Le potentiel d'approximation de la densité locale (LDA) a été utilisé pour les calculs. Le formalisme d'onde plane pseudo-potentiel ultradoux et une coupure d'énergie de 400 eV ont été utilisés. La grille Monkhorst-Pack avec 3 × 3 × 1 k -Le maillage des points a été utilisé pour le calcul précis des résultats DOS, tandis que le point Gamma a été utilisé pendant la relaxation de la géométrie. L'énergie totale auto-cohérente dans l'état fondamental a été effectivement obtenue par le schéma de mélange de densité. Pour les optimisations géométriques, le seuil de convergence pour la tolérance de champ auto-cohérent (SCF) a été défini sur 1,0 × 10 −6 eV/atome, toutes les forces sur les atomes ont convergé à moins de 0,03 eV/Å, le tenseur de contrainte total a été réduit à l'ordre de 0,05 GPa et le déplacement ionique maximal était de 0,001 Å. Les paramètres cellulaires et la coordination atomique des structures ont été optimisés à l'aide d'un algorithme de minimisation Broyden-Fletcher-Goldfarb-Shanno (BFGS).
Résultats et discussion
L'intégrité de la morphologie est importante pour assurer le succès du dopage car l'acide peut endommager la structure de l'halloysite alors qu'il est saturé en AlCl3 la solution ne le fera pas. Les images MET du HNT et du La-HNT sont présentées sur la figure 1. Le HNT montre une structure tubulaire multicouche de 0,7 à 1,5 μm de longueur, avec un diamètre extérieur de 50 à 75 nm et un diamètre intérieur de 10 à 30 nm (Fig. 1a). Après dopage en La, la morphologie tubulaire typique s'est conservée avec une teneur en La de 4,2 % (Fig. 1b). Pour le HNT traité à l'acide, la morphologie tubulaire typique a également été conservée (Fichier complémentaire 1 :Figure S1a), mais amorphe.
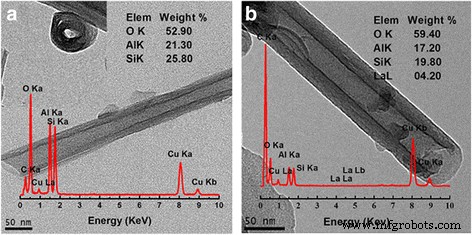
Images TEM de a HNT et b Échantillons La-HNT
La structure de HNT peut être influencée par le dopage en raison de la plus grande taille de l'atome de La utilisé pour remplacer l'atome d'Al. Pour le La-HNT, les données caractéristiques de l'halloysite (fiche JCPDS n° 29-1487) peuvent être observées sur la Fig. 2a et le Fichier complémentaire 1 :Tableau S1, qui indiquent que la phase cristalline du La-HNT est restée. Le léger décalage du premier pic dans les La-HNT est attribué au remplacement des atomes d'Al par des atomes de La de plus grande taille, ce qui entraîne l'élargissement de l'espacement interlamellaire (001). Cependant, il n'y a qu'un pic large centré à 22° pour les HNT traités à l'acide (Fichier supplémentaire 1 :Figure S1b), ce qui indique qu'il y a de la silice amorphe. Les spectres FTIR de HNT et La-HNT sont illustrés à la Fig. 2b, et l'affectation relative de chaque pic vibrationnel est répertoriée dans le fichier supplémentaire 1 :Tableau S2. Pour HNT, ces affectations sont basées sur les littératures précédentes [37,38,39,40]. Pour La-HNT, la vibration de déformation O–H des groupes Al–OH internes à 909 cm −1 et la vibration de déformation Al-OSi des feuilles tétraédriques Al-O à 553 cm −1 passer à 915 et 544 cm −1 , respectivement. Cependant, la feuille octaédrique de gibbsite de l'halloysite est complètement détruite et les bandes d'étirement Al-O disparaissent pour le HNT traité à l'acide (Fichier supplémentaire 1 :Figure S1c). Toutes ces observations prouvent le succès du dopage La dans la structure du HNT et le changement de la structure du HNT influencé par le dopage La. Les 27 Les spectres RMN Al CP/MAS des échantillons HNT et La-HNT sont présentés sur la figure 2c. Le signal de résonance à -3 ppm est attribué à Al à 6 coordonnées. Le signal de résonance à 64 ppm est attribué au déplacement de l'Al à 4 coordonnées à 58 ppm après le dopage La, indiquant que l'environnement de l'atome d'Al a été influencé par le dopage La. Cependant, il y a trois pics à -111,32, -101,70 et -91,71 ppm dans le HNT traité à l'acide, identifié comme Si(OSi)4 , Si(OSi)3 OH et Si(OSi)2 (OH)2 (Fichier supplémentaire 1 :Figure S1d), respectivement. Les isothermes de sorption d'azote du HNT et du La-HNT sont illustrés à la figure 2d, et les données relatives sont résumées dans le fichier supplémentaire 1 :tableau S3. Le SBET , le volume des pores et le diamètre moyen des pores du La-HNT sont de 59 m 2 /g, 0,37 cm 3 /g et 25 nm, respectivement. Le SBET et les valeurs de volume poreux du La-HNT sont inférieures à celles du HNT (82 m 2 /g, 0,41 cm 3 /g), tandis que son diamètre moyen de pores (25 nm) est supérieur à celui du HNT (20 nm). Cependant, le SBET la valeur et le volume poreux du HNT traité à l'acide sont trois fois supérieurs à celui du HNT (Fichier complémentaire 1 :Figure S1e). Tous ces résultats démontrent que le dopage La influence la structure des HNT, étant donné que le SBET pour La-HNT est inférieur à celui de HNT, et il y a une diminution du volume poreux total. Le SBET diminué et le volume des pores pourrait être attribué à la partie des couches d'halloysite effondrées, et l'augmentation de la taille des pores pourrait être associée au remplacement de l'atome d'Al par l'atome de La, conformément aux analyses XRD et FTIR [18]. Par conséquent, il est supposé que La-HNT peut servir d'excellent support en modifiant les performances chimiques et structurelles de l'halloysite, et pourrait ainsi contribuer à l'amélioration de l'activité de catalyse pour les matériaux nanocomposites catalytiques à base de HNT.
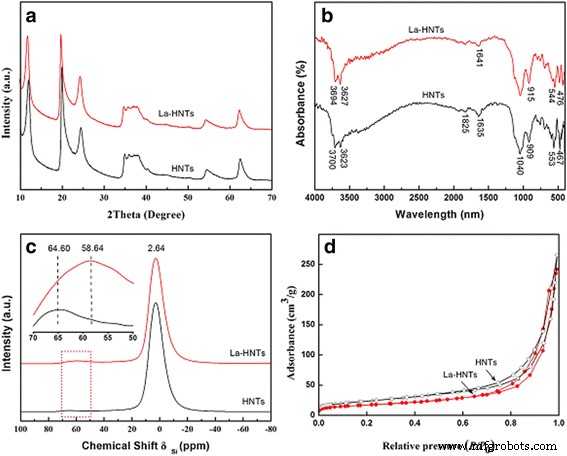
un Modèles XRD, b Spectres FTIR, c 27 spectres Al RMN, et d isothermes d'adsorption-désorption d'azote des échantillons de HNT et de La-HNT
Pour confirmer les effets du dopage au La, des nanoparticules de CdS ont été déposées à la surface du La-HNT et du HNT. La figure 3a–c, e montre clairement que la surface du HNT et du La-HNT est bien recouverte d'une couche de nanoparticules de CdS continue, dense et uniforme d'une épaisseur d'environ 5 nm. Cependant, l'élément La n'a pas été détecté dans l'échantillon CdS/La-HNT (encadré sur la figure 3e). La disparition de l'élément La dans les CdS/La-HNT peut être attribuée à l'abri de la couche de nanoparticules de CdS, plus l'élément La faible correspondant. Le rapport de CdS dans CdS/HNT à CdS/La-HNT est de 11 % en poids. La figure 3d, f montre une image HRTEM typique de la couche de revêtement de nanoparticules de CdS sur la surface de l'hôte avec un diamètre de 5 nm, correspondant à la taille des particules de 5 nm calculée par l'équation de Scherrer (Fichier supplémentaire 1 :Figure S2).
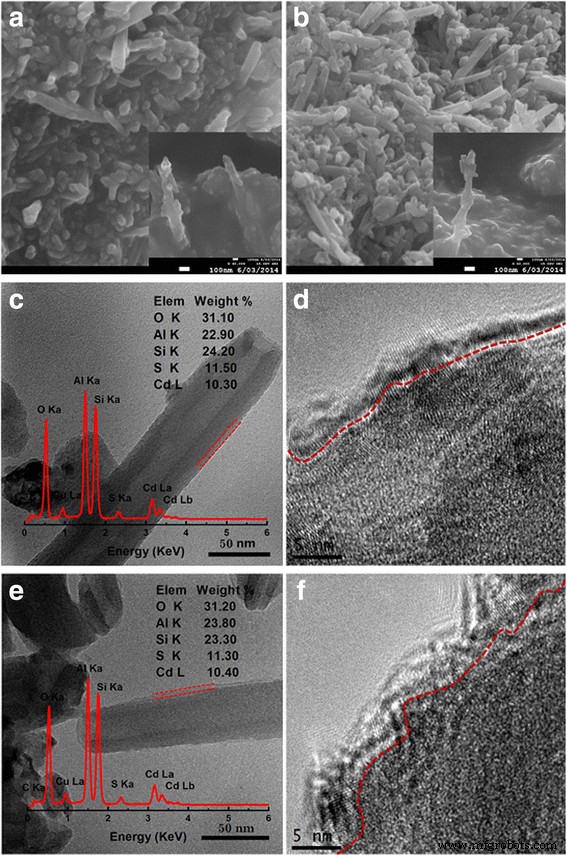
Images SEM et TEM de a , c , d CdS/HNT et b , e , f Échantillons CdS/La-HNT
Les propriétés optiques des composites HNT, La-HNT, CdS/HNT et CdS/La-HNT sont caractérisées par spectroscopie de réflectance diffuse UV-vis (Fig. 4a). Les bords d'absorption de CdS/HNT et CdS/La-HNT sont à 554 et 562 nm, respectivement, et CdS/La-HNT montre une intensité d'absorption plus forte que CdS/HNT dans la région de la lumière visible. Les composites La-HNT ne présentent aucune absorption dans la région UV, et les caractéristiques d'absorption sont similaires à celles du HNT sous l'aspect d'une large absorption dans la région de la lumière visible. Le E tel qu'obtenu g les valeurs sont de 2,31 et 2,25 eV pour CdS/HNT et CdS/La-HNT, respectivement. La performance catalytique du La-HNT pour la séparation de l'eau a été évaluée pour révéler comment le processus de dopage et le changement de microstructure correspondant affectent les propriétés macroscopiques. Photocatalytique H2 l'évolution des CdS/HNT et CdS/La-HNT (Fig. 4b) a été réalisée dans une solution aqueuse contenant du SO3 2− et S 2− ions comme réactifs sacrificiels sous irradiation solaire simulée [41,42,43]. Les résultats montrent que le photocatalytique H2 le taux de CdS/La-HNT (47,5 μmol/h) est supérieur à celui de CdS/HNT (26,0 μmol/h) dans les mêmes conditions de réaction (Fichier supplémentaire 1 :Tableau S4), et CdS/La-HNT et CdS/ Les HNT présentent un taux d'hydrogénation plus élevé que la plupart des photocatalyseurs à base de CdS précédemment rapportés dans la littérature [43-45]. Pour savoir si le photocatalytique supérieur H2 dérivé du dopage La, les réponses photocourantes transitoires de CdS/HNT et CdS/La-HNT ont été mesurées sur la figure 4c. On peut clairement voir que le photocourant augmente rapidement à une valeur élevée sous éclairage, et le photocourant diminue jusqu'à presque zéro lorsque la lumière est éteinte. Les résultats montrent que l'intensité du photocourant de CdS/La-HNT est plus élevée que celle de CdS/HNT, indiquant qu'une séparation plus efficace des porteurs de charge a été influencée par le dopage La.
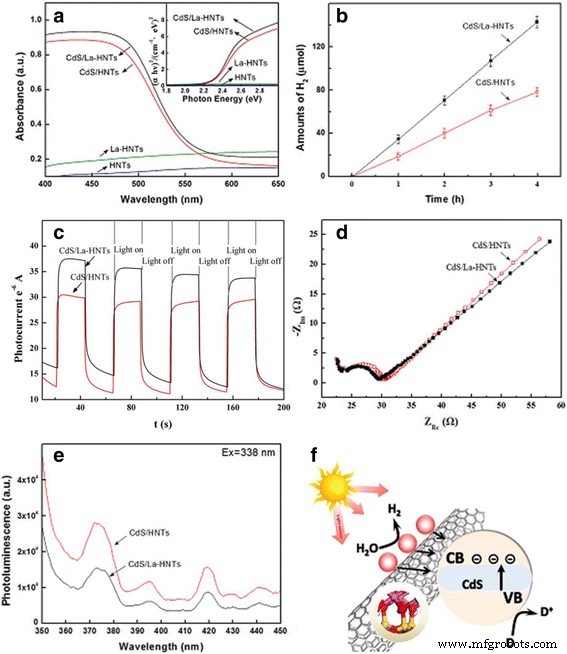
un Spectres UV-vis, b courbe d'hydrogène photocatalytique, c les réponses photocourantes transitoires, d Tracés d'impédance de Nyquist, e spectres PL, et f schéma catalytique correspondant des échantillons CdS/HNT et CdS/La-HNT
Afin d'examiner le transfert de charge et le transport d'ions, la spectroscopie d'impédance électrochimique (EIS) a été utilisée [2], et le comportement d'impédance de CdS/HNT et CdS/La-HNT a été mesuré sur la figure 4d. Les tracés de Nyquist ont montré un demi-cercle, qui s'est produit en raison du processus électrochimique à un niveau de fréquence élevée, suivi d'une ligne qui indique la résistance de diffusion de l'électrolyte et des matériaux actifs. La résistance de transfert de charge confinée en demi-cercle, qui est étroitement liée à la réversibilité des réactions électrochimiques. CdS/La-HNT montre un arc plus petit que celui de CdS/HNT, indiquant que le dopage La a conduit à un transfert de charge plus efficace sur CdS/La-HNT.
Le rayon de demi-cercle plus petit des CdS/La-HNT par rapport aux CdS/HNT a révélé que le nanocomposite CdS/La-HNT a une plus petite résistance au transfert de charge et une bonne résistance électrochimique. Les effets du dopage La sont également confirmés par les spectres d'émission de photoluminescence (PL) (Fig. 4e), plus l'intensité PL est faible, plus l'efficacité de la séparation électron-trou photogénérée est élevée.
Ici, nous étudions la structure de surface de HNT pour confirmer davantage l'environnement de l'atome d'Al influencé par le dopage La. La gamme complète des spectres XPS de HNT et La-HNT est présentée sur la figure 5a, et la concentration atomique relative est indiquée dans le fichier supplémentaire 1 :tableau S5. Les éléments Si et Al sont détectés dans les HNT et les La-HNT, tandis que l'élément La n'est détecté que dans les La-HNT. Le rapport de concentration Al/Si est de 0,62 dans La-HNT, inférieur à celui de HNT (0,88), ce qui peut être dû au remplacement de l'atome Al par l'atome La. Pour le HNT traité à l'acide, seul Si 2p et O 1s sont détectées du fait de l'enlèvement de la feuille d'alumine (Fichier complémentaire 1 :Figure S1f). La figure 5b montre le La 3d spectres, et leurs positions de pic sont observées à 835,7 eV (La 3d 5/2 ), 839,0 eV (La 3d 5/2 ), 852,3 eV (La 3d 3/2 ) et 855,9 eV (La 3d 3/2 ), respectivement. La figure 5c, d montre l'Al 2p et Si 2p spectres, et leurs positions maximales sont observées à 74,8 eV (Al-OH), 74,3 eV (Al-O), 103,3 eV (Si-OH) et 102,7 eV (Si-O), respectivement. Remarquablement, les valeurs d'énergie de liaison (BE) de l'atome d'Al dans Al-OH et Al-OSi sont passées à 75,1 et 74,6 eV, respectivement, tandis que la position de la valeur BE des atomes de Si n'a pas changé. Ainsi, tous les résultats ci-dessus confirment que l'atome de La a remplacé une partie de l'atome d'Al de la feuille Al-O et que l'environnement des atomes d'Al a été influencé.
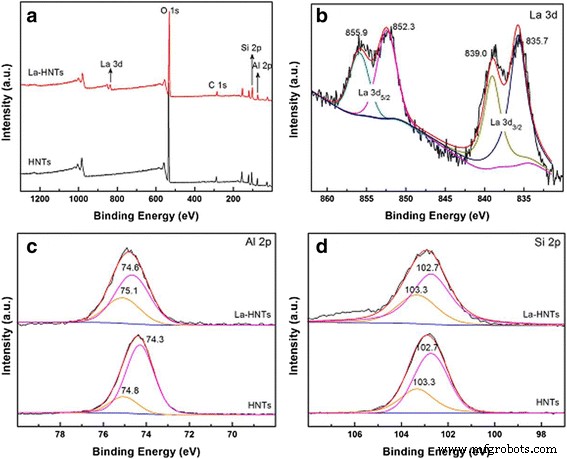
un gamme complète, b La3d, c Al2p et d Spectres XPS Si2p des échantillons HNT et La-HNT
Sur la base de la caractérisation du dopage La dans la structure HNT et de la partie remplacée de l'atome Al de la feuille Al-O, un modèle de dopage atomique substitutionnel a été proposé comme suit (Fig. 6). Chaque couche de HNT se compose d'une feuille tétraédrique de Si et d'une feuille octaédrique d'Al. La distance entre les cellules unitaires est difficile à modifier en raison de la forte force de couplage, de sorte que les molécules d'eau ne peuvent pas entrer. Ainsi, l'halloysite a été identifiée comme le minéral d'aluminosilicate de faible activité. Dans la phase initiale, l'AlCl saturé typique3 solution a été choisie car l'AlCl3 anhydre est un acide de Lewis fort, capable de former des adduits à base d'acide de Lewis avec l'eau, tels que AlO2 2− , HCl et H3 O + . La gravure commence par les adduits à base d'acide de Lewis interagissant avec l'alumine dans la structure de l'halloysite, et l'étendue de la réaction augmente avec la concentration d'Al 3+ en augmentant. Comme la concentration d'Al 3+ est déjà sursaturée, une couche d'inhibition se formera, près de la surface de l'halloysite. Dans cette situation, une substitution de cations pourrait se produire dans la couche d'inhibition. Le La 3+ ions suivant Al 3+ solution saturée sont substitués par les atomes d'aluminium solubles de l'halloysite dans la couche d'inhibition selon le principe de la conservation de la concentration en ions de la solution saturée. Ensuite, l'équilibre dynamique du dopage atomique de substitution formé et des composites d'halloysite dopé La est atteint. L'utilisation d'un autoclave dans le processus était de forcer le processus de dopage car le rayon de La 3+ ion est plus grand que celui de Al 3+ . Les formes cristallines et les structures de surface peuvent évidemment être modifiées par dopage, et les performances chimiques et structurelles du support seraient améliorées, ce qui apporte une uniformité continue au chargement des nanoparticules et améliore l'activité de catalyse pour les matériaux nanocomposites catalytiques.
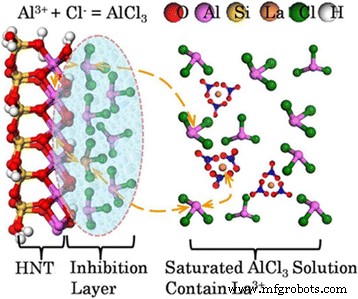
Mécanisme proposé de dopage La dans HNT
Les calculs de la théorie fonctionnelle de la densité (DFT) du premier principe ont été effectués pour étudier plus avant la rationalité du mécanisme de dopage et l'effet du dopage La. Le modèle de structure de HNT est simulé en utilisant des approximations cristallines, et le La-HNT est construit en remplaçant l'atome d'Al de l'halloysite par l'atome de La. La structure du HNT en utilisant la structure de la kaolinite est simulée (Fig. 7a, b), et les structures de surface sont construites en clivant une structure de couche 2 × 1 de deux épaisseurs de couche Al–O–Si hors de l'halloysite en vrac. Un espace de vide de 15 Å est utilisé. Le La-HNT est construit en remplaçant un Al dans la feuille d'Al de l'halloysite par un atome de La ou en ajoutant La(OH)3 à la surface de l'halloysite (Fig. 7c, d). Il a été constaté que les liaisons Al-O (Als –O) et les liaisons Si–O perpendiculaires à la couche plane (Sips –O) sur la surface du HNT sont légèrement augmentées par rapport à celle de la structure en vrac du HNT (Fichier supplémentaire 1 :Figure S3), c'est-à-dire 0,05–0,10 et 0,02–0,03 Å, respectivement. Dans le même temps, les liaisons Si–O dans la couche plane (Siest –O) a diminué. De plus, la distribution de la liaison O-H sur la surface HNT est élargie en raison de l'effet de surface. Pour le cas dopé au La, contraction des Als –O et Sips –O liaisons, ainsi qu'une expansion du Siis La liaison –O se produit plutôt après la relaxation de la structure atomique de la surface La-HNT (Fichier supplémentaire 1 :Figure S3). La structure locale autour de La montre que les six liaisons La–O possèdent une longueur de liaison (environ 2,3–2,5 Å) beaucoup plus longue que les liaisons Al–O, ce qui augmente l'espace autour du site de dopage La (Fichier supplémentaire 1 :Figure S4a). Notamment, l'allongement de trois liaisons OH de surface avec H se dirigeant directement vers les atomes O de La(OH)3 (HLa ) induit trois groupes OH de surface réactifs autour de l'atome La à la surface La-HNT.
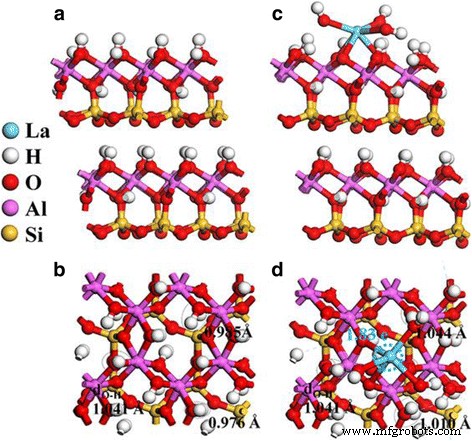
Structure géométrique de a vue de côté et b vue de dessus de HNT, et c vue de côté et d vue de dessus de La-HNT
La charge de Mulliken calculée pour l'atome La dans La-HNT est de 1,83 e (Fig. 7d), ce qui correspond aux états de cantonnière +3. Le résultat PDOS montre une bande interdite de 5,2 eV pour le HNT vierge, et la bande de cantonnière près du niveau de fermi est principalement composée de O 2p état tandis que le minimum de bande de conduction (CBM) est mélangé principalement par H 1s , Si 3s 3p , et partiellement O 2p , Al 3s États 3p (Fichier supplémentaire 1 :Figure S4b). L'appui de La sur la surface HNT introduit La 5d états dans le CBM (Fig. 8a, violet) et le dopant réactif La avec 5d z 2 orbitals est confirmé comme une impureté de type donneur. Pendant ce temps, les trois groupes OH autour de La ont fourni des électrons à paires isolées (Fig. 8a, jaune et vert) au maximum de la bande de cantonnière (VBM), ce qui améliorera la capacité d'absorption de la surface. La différence de densité de charge autour de l'interface La-HNT montre qu'il y a un transfert de charge des atomes Al environnants de la surface HNT aux dopants La après le dopage La (Fig. 8b). Il est supposé que les dopants La pourraient servir de pont de transfert de charge entre la surface du HNT et des nanoparticules fonctionnelles comme le CdS, et ainsi le taux de dégagement d'hydrogène photocatalytique serait amélioré. Ainsi, la conformité de l'expérimentation et de la simulation a permis de vérifier la rationalité du modèle de simulation et du modèle de dopage atomique substitutionnel.
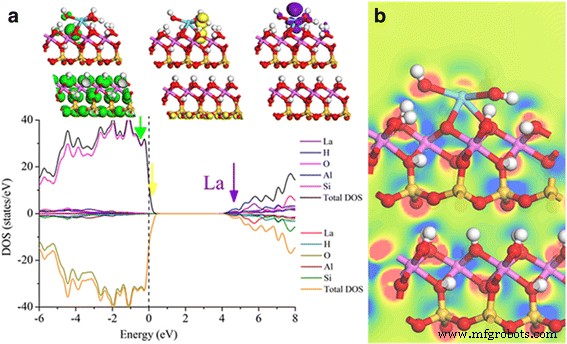
un Les résultats PDOS de la surface La-HNT. b Différence de densité de charge de l'interface La-HNT tracée le long du plan désigné par les lignes en pointillés montré dans le panneau inférieur de la Fig. 7c. Bleu correspond à l'épuisement de la charge et au rouge pour charger le gain. Les isosurfaces sont affichées dans la plage [−0,08, 0,08] (e/Å 3 ). Les contours de densité de charge constante sont séparés de 0,005 eV/Å 3
Conclusions
En résumé, les nanotubes naturels d'halloysite ont été dopés avec succès par l'atome de La. Le dopage La dans la structure du HNT conduit à des formes cristallines et à des changements évidents de structure de surface, ce qui apporte une uniformité continue pour le chargement de CdS et modifie l'activité de catalyse pour les matériaux composites nanocatalytiques, entraînant ainsi un taux d'évolution d'hydrogène photocatalytique amélioré. Le contraste du dégagement d'hydrogène photocatalytique de CdS/La-HNT et CdS/HNT confirme la haute efficacité du dopage La. Ce résultat est très encourageant et devrait être hautement applicable pour étendre la technique de dopage à d'autres minéraux aluminosilicatés et la conception correspondante de matériaux fonctionnels.
Nanomatériaux
- Surveillance des performances qui fonctionne à la fois pour les opérations informatiques et les propriétaires d'applications
- Améliorer les performances des applications pour les utilisateurs et les clients de CyrusOne
- Exigences pour de bonnes performances de liaison de communication :modulation et démodulation IQ
- Nanofibres et filaments pour une administration améliorée des médicaments
- Le HDPE représente un changement radical dans les performances des bouteilles et conteneurs moulés par soufflage
- Nanoparticules pour le traitement du cancer :progrès actuels et défis
- Ingénierie des procédés de revêtement par immersion et optimisation des performances pour les appareils électrochromes à trois états
- Synthèse et propriétés électrochimiques des matériaux cathodiques LiNi0.5Mn1.5O4 avec dopage composite Cr3+ et F− pour batteries lithium-ion
- Les arguments en faveur du fractionnement des stocks, par grandes et petites marques



