Hétérostructure hiérarchique des sphères creuses ZnO@TiO2 pour une évolution photocatalytique hautement efficace de l'hydrogène
Résumé
La conception rationnelle et la préparation de nanoarchitectures hiérarchiques sont essentielles pour une réaction photocatalytique améliorée d'évolution d'hydrogène (HER). Ici, creux bien intégré ZnO@TiO2 les hétérojonctions ont été obtenues par une simple méthode hydrothermale. Cette hétérostructure hiérarchique unique a non seulement provoqué des réflexions multiples qui améliorent l'absorption de la lumière, mais a également amélioré la durée de vie et le transfert des porteurs de charge photogénérés en raison de la différence de potentiel générée sur le ZnO-TiO2 interface. Par conséquent, par rapport au ZnO nu et au TiO2 , le ZnO@TiO2 photocatalyseur composite présentait une production d'hydrogène plus élevée évaluée jusqu'à 0,152 mmol h −1 g −1 sous la lumière solaire simulée. De plus, une photostabilité très répétée a également été observée sur le ZnO@TiO2 photocatalyseur composite même après un test continu de 30 h. On s'attend à ce que ce ZnO@TiO2 à faible coût, non toxique et facilement disponible le catalyseur pourrait présenter un potentiel prometteur en photocatalytique H2 pour répondre aux futurs besoins en carburant.
Contexte
Hydrogène (H2 ), l'une des énergies propres et durables les plus importantes, a été considérée comme une énergie alternative prometteuse pour répondre aux futurs besoins en carburant [1,2,3,4,5]. Depuis la découverte du système photoélectrochimique (PEC) de séparation d'eau par Fujishima et Honda dans les années 1970 [6], la production de H2 basé sur TiO2 photocatalyseurs semi-conducteurs utilisant la lumière du soleil a attiré une attention croissante. Cependant, l'application pratique du TiO seul nu2 dans l'industrie est toujours un défi en raison de la recombinaison à haut débit des électrons photogénérés et des trous à la surface du TiO2 entraîne une faible efficacité quantique. A ce jour, de nombreux efforts ont été faits pour concevoir TiO2 photocatalyseurs composites pour résoudre les problèmes ci-dessus, tels que le couplage avec un autre semi-conducteur, le dopage d'ions de métaux de transition ou d'atomes non métalliques, etc. [7,8,9]. En particulier, la formation d'hétérojonctions semi-conducteur-semi-conducteur avec des potentiels de bande correspondants est un moyen efficace d'empêcher la recombinaison de charge et d'augmenter la durée de vie des porteurs de charge [10,11,12].
Parmi les différents semi-conducteurs, le ZnO est également largement étudié en raison de ses propriétés identiques de TiO2 avec non-toxicité, bon marché, haute efficacité et stabilité chimique [13, 14]. Puisque la bande de conduction (CB) et la bande de valence (VB) de ZnO sont supérieures à celles de TiO2 , les électrons photogénérés dans le ZnO seront transférés au TiO2 une fois qu'une hétérojonction s'est formée entre TiO2 et ZnO. Ce genre de ZnO@TiO2 l'hétérojonction composite bénéficiera à la séparation des paires électron-trou photogénérées, entraînant ainsi plus d'électrons accumulés sur le TiO2 qui réagira avec H2 O pour générer H2 [15,16,17].
En plus de ce que nous avons discuté ci-dessus, les formes géométriques et les morphologies des photocatalyseurs influencent également fortement les performances de la réaction de dégagement d'hydrogène (HER) [18,19,20]. Il a été rapporté que les diffractions sur les sphères creuses et les réflexions multiples dues à la structure de la coque augmenteraient l'efficacité de l'utilisation de la lumière [21]. Par exemple, le groupe de Li a préparé des sphères creuses d'oxyde de titane en forme de cage hydrogénée présentant des activités HER beaucoup plus élevées que la structure solide [22]. Au-delà de cela, les structures creuses sphériques présentent les avantages d'une grande surface spécifique, de longueurs de transport réduites pour les porteurs de charge et d'une bonne stabilité chimique et thermique, qui contribuent toutes à l'excellente capacité photocatalytique [23]. Cependant, la plupart des recherches se sont concentrées sur la préparation de sphères creuses composites par dopage d'éléments de transition, tels que Ce-ZnO [24], Ni-ZnO [25], Ag-TiO2 [26], Au–TiO2 [27], et ainsi de suite. À notre connaissance, peu d'études ont rendu compte de la synthèse de sphères creuses fermées, complètes et intactes composées de particules poreuses d'oxydes métalliques mixtes. Même ainsi, la plupart de ces composites sont appliqués dans la dégradation photocatalytique de polluants organiques mais pas dans la production photocatalytique d'hydrogène.
Dans cet article, nous avons rapporté une méthode facile pour synthétiser hiérarchiquement le ZnO@TiO2 poreux microsphères creuses composites et appliqués dans le photocatalytique H2 . Les sphères creuses ont amélioré l'absorption de la lumière par de multiples réflexions, en même temps, la durée de vie et le taux de transfert des porteurs de charge photogénérés ont également été améliorés en raison de la différence de potentiel générée sur le ZnO-TiO2 interface. Le résultat a montré que le ZnO@TiO2 le photocatalyseur composite présentait un H2 amélioré taux d'évolution, par rapport au ZnO et TiO2 nus . De plus, le mécanisme du photocatalytique H2 sur le ZnO@TiO2 sphères creuses composites a été discuté en détail.
Méthodes
Synthèse de la Hiérarchique ZnO@TiO2 Sphères creuses
La préparation de ZnO@TiO2 composites était basée sur une méthode hydrothermale sans modèle en une étape très facile dans des conditions ambiantes. Dans une procédure typique, 0,015 mol de Ti(SO4 )2 , 0,015 mol de Zn(NO3 )2 ·6H2 O, 0,015 mol de NH4 F, et 0,06 mol de CO(NH2 )2 ont été ajoutés à un bécher avec 50 mL d'eau déminéralisée. Après agitation pendant 60 min, la solution de mélange a été transférée dans un autoclave en acier inoxydable revêtu de Téflon et chauffée dans un four électrique à 180 °C pendant 12 h. Après cela, le précipité blanc a été soigneusement lavé avec de l'éthanol quatre fois, puis séché à 60 °C pendant 12 h pour obtenir ZnO@TiO2 hétérostructures. A titre de comparaison, TiO2 nu et ZnO ont été préparés dans les mêmes conditions.
Synthèse de Pt–ZnO@TiO2 Échantillons
Dans un processus de synthèse typique de Pt–ZnO@TiO2 échantillons, le ZnO@TiO2 les sphères creuses ont été placées dans un récipient contenant 10 % en volume de triéthanolamine et H2 PtCl6 Solution. Ensuite, le système a été barboté avec de l'azote pendant 30 minutes pour éliminer l'air. Enfin, le Pt a été photodéposé in situ sur le ZnO@TiO2 sphères creuses sous une irradiation lumineuse à arc complet (λ> 300 nm) pendant 2 h. La teneur en Pt peut être ajustée par la concentration de H2 PtCl6 et le temps de réaction, qui a été déterminé par plasma à couplage inductif (ICP, PE5300DV).
Caractérisation
La morphologie de ZnO@TiO2 Les hétérostructures ont été caractérisées par microscope électronique à balayage à émission de champ (FESEM, Hitachi, Japon), microscopie électronique à transmission (TEM, Tecnai F20), TEM annulaire à champ sombre à angle élevé (STEM, Tecnai F20) et TEM haute résolution (HRTEM, Tecnai F20). Les images cartographiques de la spectroscopie à rayons X à dispersion d'énergie (EDS) ont été capturées sur un microscope analytique à résolution atomique Tecnai G2 F20 S-TWIN. Les propriétés de la phase cristalline des échantillons ont été caractérisées à l'aide d'un diffractomètre à rayons X avec rayonnement Cu-K (XRD, M21X, MAC Science Ltd., Japon). Les surfaces spécifiques BET ont été mesurées sur l'analyseur Belsorp-mini II (Japon).
Mesures photoélectrochimiques
Des études de photocourant ont été réalisées sur un poste de travail électrochimique CHI 660D, en utilisant une configuration à trois électrodes où des électrodes d'oxyde d'étain dopé au fluor (FTO) ont été déposées avec les échantillons comme électrode de travail, Pt comme contre-électrode et une électrode au calomel saturé (SCE) comme référence . L'électrolyte était 0,35 M/0,25 M Na2 S–Na2 SO3 solution aqueuse. Pour la fabrication de l'électrode de travail, 0,25 g de l'échantillon a été broyé avec 0,06 g de polyéthylène glycol (PEG, poids moléculaire 20 000) et 0,5 mL d'éthanol pour former une suspension. Ensuite, la suspension a été étalée sur un verre FTO de 1 × 4 cm par la technique de la racle, puis laissée à sécher à l'air. Une lampe à arc au xénon de 300 W a servi de source d'irradiation solaire simulée (Perfectlight, PLS-SXE 300C, Pékin, Chine). L'intensité lumineuse incidente a été réglée sur 100 mW/cm 2 mesuré par NOVA Oriel 70260 avec un thermodétecteur.
Tests photocatalytiques de production d'hydrogène
Des expériences de production d'hydrogène photocatalytique ont été réalisées dans un flacon de quartz scellé à température ambiante et sous pression atmosphérique. Une lampe à arc au xénon de 300 W (Perfect light, PLS-SXE 300C, Pékin, Chine) a été utilisée comme source lumineuse pour déclencher la réaction photocatalytique. Le H2 évolué ont été collectées et analysées en ligne par un H2 -système solaire (Beijing Trusttech Technology Co., Ltd.) avec un chromatogramme en phase gazeuse équipé d'un détecteur de conductivité thermique (TCD), une colonne de tamis moléculaire 5A et de l'azote comme gaz vecteur. Toutes les expériences photocatalytiques sur 100 mg de photocatalyseur ont été réalisées dans une solution aqueuse contenant H2 O (80 mL) et alcool (20 mL). Avant l'irradiation, le système a été désaéré par barbotage d'azote pendant 15 min. Au cours de la réaction photocatalytique, le réacteur a été hermétiquement fermé pour éviter les échanges gazeux.
Résultats et discussion
La taille et la morphologie du ZnO@TiO2 tel que préparé des sphères creuses ont été affichées sur la figure 1. La figure 1a montre que l'échantillon a une morphologie sphérique uniforme avec un diamètre moyen d'environ 1,45 μm selon la distribution de la taille des nanoparticules (encadré de la figure 1a). La figure 1b révèle une seule sphère brisée, indiquant que l'échantillon préparé est une structure creuse composée de petites particules. L'image TEM a ensuite été utilisée pour confirmer la structure du ZnO@TiO2 sphères creuses. Le changement de couleur du ZnO@TiO2 les sphères au centre et à l'extérieur étaient respectivement sombres et lumineuses, confirmant le ZnO@TiO2 les sphères étaient une structure creuse (Fig. 2a). Une vue à fort grossissement de la Fig. 2b montre également que la surface des sphères creuses était rugueuse qui ont été construites par des sous-unités de nanoparticules, à la suite de la formation de l'hétérostructure hiérarchique de ZnO@TiO2 sphères creuses. Les cartes élémentaires de la Fig. 2(d–f) ont été utilisées pour confirmer la distribution élémentaire dans le ZnO@TiO2 sphères creuses. On peut voir que le Zn, Ti et O étaient uniformément distribués dans ZnO@TiO2 sphères creuses.

un Une image SEM à faible grossissement de ZnO@TiO2 sphères creuses; l'encart montre l'analyse statistique de la distribution des diamètres des échantillons. b Une image SEM à fort grossissement d'un seul ZnO@TiO2 cassé sphère
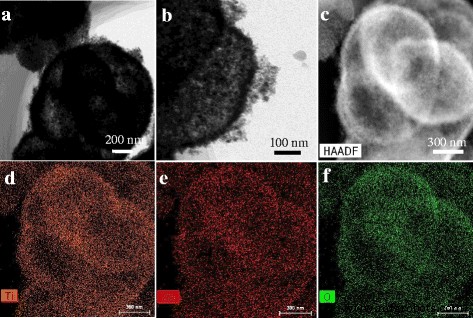
un TEM, b TEM agrandie, et c Images STEM de ZnO@TiO2 sphères creuses; Mappages élémentaires EDS correspondants de c indiquant la distribution uniforme de d Ti, e Zn, et f O, respectivement
Les images HRTEM de la Fig. 3 ont vérifié la structure d'hétérojonction de ZnO@TiO2 sphères creuses. Les zones sélectionnées sur la figure 3a marquées par un carré blanc ont été agrandies sur la figure 3b–d, correspondant à ZnO, TiO2 , et ZnO@TiO2 hétérojonction. Les distances d'espacement du réseau de 0,28 et 0,35 nm correspondaient aux plans (100) de la wurtzite ZnO et (101) plans de l'anatase TiO2 , respectivement, comme le montre la Fig. 3b, c. La figure 3d montre une transition claire de la phase wurtzite ZnO à l'anatase TiO2 phase, qui a confirmé que l'hétérojonction s'est formée à l'interface entre ZnO et TiO2 . Une telle structure d'hétérojonction peut grandement favoriser le transfert d'électrons photoexcité pour une activité photocatalytique améliorée.

un Images HRTEM de ZnO@TiO2 sphères creuses. b , c , et d sont des images HRTEM amplifiées de la partie carrée désignée dans a , indiquant ZnO, TiO2 , et ZnO@TiO2 hétérojonctions, respectivement
Les propriétés de structure des pores de ZnO, TiO2 , et ZnO@TiO2 les échantillons ont en outre été déterminés par le N2 isothermes d'adsorption-désorption et diagrammes correspondants de distribution de la taille des pores de Barrett-Joyner-Halenda (BJH) (Fig. 4). Tous les échantillons présentaient une isotherme de type IV avec une boucle d'hystérésis à haute pression relative (P /P 0> 0.7), démontrant l'existence de structures mésoporeuses selon la classification de l'Union internationale de chimie pure et appliquée (IUPAC). L'encart de la figure 4 est constitué de diagrammes de distribution de la taille des pores BJH, qui indiquent en outre que tous les échantillons ont les structures mésoporeuses. Pendant ce temps, les surfaces BET calculées du ZnO@TiO2 microsphère mesurait environ 102 m 2 g −1 , qui était bien plus grande que celle du ZnO (23 m 2 g −1 ) et TiO2 (35 m 2 g −1 ). On peut conclure l'introduction de ZnO dans TiO2 pour former le ZnO@TiO2 les sphères creuses pourraient augmenter considérablement les surfaces, bien que tous les échantillons aient les structures mésoporeuses. Les surfaces supérieures de ZnO@TiO2 les sphères creuses fourniraient plus de sites pour le H2 catalytique amélioré performances.
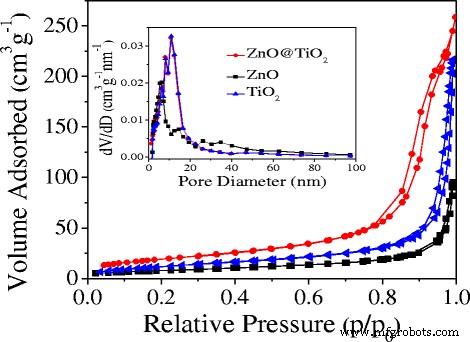
N2 les isothermes d'adsorption-désorption et l'encart montrent les courbes de distribution de taille de pores correspondantes
La capacité photocatalytique des échantillons tels que préparés a été évaluée par photocourant et photocatalytique H2 essais. Comme le montre la Fig. 5a, le ZnO@TiO2 les sphères creuses ont donné la densité de photocourant la plus élevée de 3,38 mA/cm 2 , qui était plus de 2,61, 2,17 fois supérieur à celui de ZnO et TiO2 , respectivement. Ces résultats signifient une plus grande capacité de production de porteurs de charge et une efficacité de séparation améliorée de ZnO@TiO2 sphères creuses. Sauf exception, le taux de production d'hydrogène de ZnO@TiO2 sphères creuses atteintes à 0,152 mmol h −1 g −1 , supérieur à 0,039 mmol h −1 g −1 de ZnO et 0,085 mmol h −1 g −1 de TiO2 (Fig. 5b). Le Pt, en tant que cocatalyseur de métal noble à très haute efficacité, a été largement utilisé pour H2 réaction d'évolution dans la littérature rapportée [8, 11]. Une série de Pt–ZnO@TiO2 avec différentes teneurs en Pt ont été préparés et comparés sur la Fig. 5c. Il a été montré que le chargement de Pt sur ZnO@TiO2 les sphères creuses pourraient améliorer considérablement le H2 l'activité d'évolution et l'échantillon avec 1,5 à % de Pt présentant le H2 le plus élevé taux d'évolution. La figure 5d montre que le ZnO@TiO2 les sphères creuses ont conservé leur activité photocatalytique d'origine sans dégradation notable au cours des cinq cycles de réaction pendant 30 h, ce qui démontre la stabilité photocatalytique exceptionnelle.
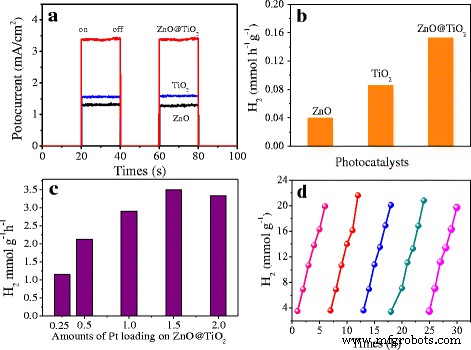
un Réponses photoactuelles et b photocatalytique H2 évolution du ZnO nu, TiO nu2 , et ZnO@TiO2 hétérojonctions. c Photocatalytique H2 évolution sur Pt–ZnO@TiO2 composites d'hétérojonctions avec différents rapports pondéraux de Pt. d Stabilité photocatalytique de ZnO@TiO2 sphères creuses. Toutes les mesures ont été effectuées sous une source d'irradiation de lumière solaire simulée avec une intensité de 100 mW/cm 2
Un mécanisme photocatalytique a été proposé pour l'amélioration de l'activité HER du ZnO@TiO2 sphères creuses, comme le montre la figure 6. Sous une irradiation solaire simulée, les électrons de ZnO et de TiO2 ont été excités de leurs bandes de valence (VB) à leurs bandes de conduction (CB). Puisque la bande de conduction (CB) et la bande de valence (VB) du ZnO étaient plus positives que celles du TiO2 , les électrons photogénérés transférés de ZnO à TiO2 par les contacts interfaciaux intimes [16]. Ensuite, les électrons les plus accumulés sur le TiO2 a réagi avec H2 O pour générer H2 pour le photocatalytique supérieur H2 taux (comme indiqué sur la droite de la Fig. 6). Dans le même temps, les trous photogénérés dans le VB de TiO2 ont migré vers ZnO, qui ont été piégés par l'agent sacrificiel pour maintenir l'équilibre thermodynamique. De plus, les sphères creuses hiérarchiques bénéficient de la diffusion de la lumière et des réflexions multiples entre ZnO@TiO2 photocatalyseur composite, ce qui améliorerait l'efficacité de l'utilisation de la lumière [10, 21, 22]. Ainsi, plus d'électrons libres et de trous seraient générés en raison de l'augmentation de la longueur effective du chemin des photons [21, 22], conduisant à une efficacité HER plus élevée (comme indiqué sur la gauche de la figure 6).
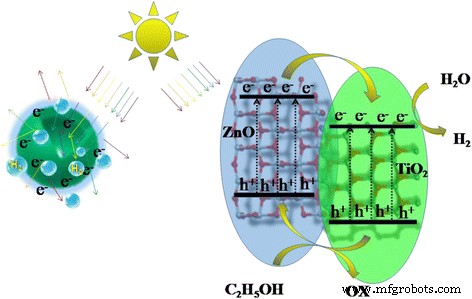
Illustration schématique du mécanisme HER proposé de ZnO@TiO2 sphères creuses
Conclusions
En résumé, l'hétérostructure hiérarchique de ZnO@TiO2 sphères creuses a été préparée avec succès via une méthode hydrothermale simple. Par rapport au ZnO et TiO2 nus , le ZnO@TiO2 photocatalyseur composite présentait une production élevée d'hydrogène évaluée jusqu'à 0,152 mmol h −1 g −1 sous la lumière solaire simulée. On pense que l'hétérostructure hiérarchique a augmenté la surface qui prouve des sites plus actifs pour un HER efficace et a simultanément amélioré la durée de vie et le transfert des porteurs de charge photogénérés en raison de la différence de potentiel générée sur le ZnO-TiO2 interface. De plus, le ZnO@TiO2 photocatalyseur composite présentait une bonne durabilité même après avoir été réutilisé cinq fois. Ce travail a démontré une bonne perspective pour photocatalytique H2 évolution à partir de l'eau basée sur l'utilisation rationnelle et la préparation d'une activité élevée, peu coûteuse et d'une stabilité chimique de ZnO et TiO2 .
Nanomatériaux
- Agent de purge hautement efficace pour les polyoléfines de moulage par soufflage
- Optimisation des couches minces hautement réfléchissantes pour les micro-LED plein angle
- MoS2 avec épaisseur contrôlée pour l'évolution électrocatalytique de l'hydrogène
- Composites de graphène quantique/TiO2 co-dopé S, N pour une génération d'hydrogène photocatalytique efficace
- Exploration du cadre organique Zr-Metal-Organic comme photocatalyseur efficace pour la production d'hydrogène
- Modification du cocatalyseur en alliage PtNi de l'hybride g-C3N4/GO sensibilisé à l'éosine Y pour une évolution efficace de l'hydrogène photocatalytique en lumière visible
- Évolution de l'hydrogène photocatalytique améliorée en chargeant des QD Cd0.5Zn0.5S sur des nanofeuilles poreuses Ni2P
- Fabrication d'hétérostructures Hiérarchiques ZnO@NiO Core–Shell pour de meilleures performances photocatalytiques
- Incorporation de matériaux composites de carbone nanostructurés dans des contre-électrodes pour des cellules solaires à colorant hautement efficaces



