Optimisation et évaluation de la méthode de prétraitement pour sp-ICP-MS pour révéler la distribution des nanoparticules d'argent dans le corps
Résumé
L'utilisation répandue de nanoparticules manufacturées (ENP) a augmenté notre exposition à ces particules. Les techniques analytiques actuellement disponibles ne parviennent pas à quantifier et à analyser simultanément les propriétés physiques des ENP dans les tissus biologiques. Par conséquent, de nouvelles méthodes sont nécessaires pour évaluer les conditions d'exposition aux ENP. La spectrométrie de masse à plasma à couplage inductif à particule unique (sp-ICP-MS) est une approche attrayante qui peut effectuer des analyses quantitatives et qualitatives des ENP. Cependant, l'application de cette approche pour les échantillons biologiques est limitée en raison du manque de méthodes de prétraitement pour récupérer efficacement les ENP des tissus biologiques. Dans cette étude, nous avons évalué diverses méthodes de prétraitement et identifié les conditions de prétraitement optimales pour les analyses sp-ICP-MS des ENP dans les tissus biologiques en utilisant des nanoparticules d'argent (nAg) comme modèle. Nous avons sélectionné cinq réactifs comme solvants de prétraitement (hydroxyde de sodium, hydroxyde de tétraméthylammonium, acide nitrique, acide chlorhydrique et protéinase K). Nos résultats ont montré que le traitement à l'hydroxyde de sodium était optimal pour détecter le nAg dans le foie de souris. De plus, cette méthode de prétraitement peut être appliquée à d'autres organes, tels que le cœur, les poumons, la rate et les reins. Enfin, nous avons évalué l'applicabilité de cette méthode en analysant la quantité et les propriétés physiques de l'argent dans le sang et le foie de souris, après administration intraveineuse de nAg ou d'ions argent. Notre méthode sp-ICP-MS a révélé que le nAg administré dans le sang était partiellement ionisé et avait tendance à être distribué sous forme de particules (environ 80 %) dans le foie et sous forme ionique (environ 95 %) dans le sang. En conclusion, nous avons optimisé les stratégies de prétraitement pour l'évaluation sp-ICP-MS des ENP dans les tissus biologiques et démontré son applicabilité en évaluant les changements dans les propriétés physiques du nAg dans le foie et le sang. Nous avons également montré que des changements partiels de la forme particulaire à la forme ionique du nAg influencent leur cinétique et leur distribution lorsqu'ils sont administrés à des souris.
Introduction
Les progrès récents de la nanotechnologie ont accéléré le développement de nanoparticules artificielles (ENP) inférieures à 100 nm. En raison de leurs propriétés bénéfiques telles qu'une perméabilité tissulaire et une réaction de surface améliorées par rapport à d'autres matériaux de taille micro ou supérieure, les ENP sont largement utilisées dans divers produits, notamment les cosmétiques, les aliments et les médicaments [1, 2]. Par exemple, les nanoparticules d'argent (nAg), l'une des ENP les plus courantes, sont utilisées dans les antibiotiques en raison de leur libération constante d'Ag + . De plus, ils sont utilisés comme matériaux conducteurs dans la technologie de l'électronique imprimée [3]. En revanche, les propriétés physico-chimiques uniques associées à la petite taille des particules de nAg peuvent être dangereuses. Il est connu que ces particules peuvent perturber la barrière hémato-encéphalique et induire une inflammation [4]. L'utilisation accrue des ENP dans les produits d'usage quotidien a exposé les humains à divers types d'ENP. Leur utilisation continue doit être évaluée pour déterminer leur sécurité [2, 3].
Afin d'assurer la sécurité, il est indispensable de comprendre le « risque » des ENP, qui est le concept intégratif de « danger » (toxicité potentielle) et de « condition d'exposition ». Alors que les dangers des ENP ont été analysés dans le monde entier, peu d'études ont examiné les situations d'exposition aux ENP [5]. De plus, il a été récemment rapporté que la distribution intracellulaire du nAg incorporé dans les cellules en culture diffère de celle de l'Ag + [6] et que Ag + particules dans les tissus de souris [7]. Par conséquent, il est nécessaire d'évaluer leurs propriétés physiques, telles que la taille des particules et de faire la distinction entre les particules et les ions dans le corps [3, 6,7,8].
En utilisant la technologie analytique actuellement disponible, il est difficile d'analyser quantitativement les propriétés physiques des ENP dans le corps. La spectrométrie de masse à plasma à couplage inductif (ICP-MS) convient aux analyses quantitatives mais pas aux analyses de propriétés physiques, car toutes les cibles telles que les ions et les particules ne peuvent pas être distinguées lors de la quantification. En revanche, la microscopie électronique à transmission (MET) est adaptée pour analyser les propriétés physiques mais pas pour quantifier les ENP, car seule une partie du tissu est observée. Par conséquent, une nouvelle méthode est nécessaire pour les analyses simultanées des propriétés physiques et les analyses quantitatives des ENP afin d'étudier leur biotransformation.
L'ICP-MS à particule unique (sp-ICP-MS), basé sur l'ICP-MS, introduit une ou aucune particule dans l'analyseur par temps de séjour et constitue une méthode attrayante pour déterminer la taille des particules en analysant l'intensité maximale et les concentrations de particules en analysant taux de pointe. Les particules et les ions peuvent être distingués en analysant les signaux de crête et les signaux de fond [9]. Quelques études précédentes ont rapporté l'utilisation de la sp-ICP-MS pour la quantification et les analyses des propriétés physiques des ENP [10, 11].
Cependant, la plupart de ces études ont utilisé la sp-ICP-MS pour analyser l'eau environnementale ou des produits commerciaux contenant des ENP [10, 11] et quelques études ont adopté la sp-ICP-MS pour les tissus biologiques. De plus, ces études ont prétraité les tissus par digestion à la protéinase K ou avec de l'hydroxyde de tétraméthylammonium (TMAH) pour solubiliser les matrices protéiques et lipidiques. Comme différents réactifs ont des propriétés de solubilisation différentes, des variations dans les méthodes de prétraitement peuvent influencer le taux de récupération des ENP distribués dans les tissus. De plus, il est important que la méthode de prétraitement n'affecte pas la taille ou les propriétés ioniques des ENP et récupère efficacement les ENP distribuées dans les tissus.
Dans cette étude, nous avons évalué et optimisé différentes méthodes de prétraitement pour la sp-ICP-MS dans des échantillons biologiques afin de déterminer la quantité et les propriétés physiques des ENP dans le corps en utilisant nAg comme ENP modèles.
Matériaux et méthodes
ENP
Les nAg « Biopure » de 30, 70 et 100 nm (nAg30, nAg70 et nAg100) ont été obtenus auprès de nanoComposix (San Diego, CA, USA). Le RM8013 a été utilisé comme norme pour calculer l'efficacité des transports et a été obtenu auprès du National Institute of Standards and Technology (Gaithersburg, MD, États-Unis). Chaque type d'ENP a été soniqué pendant 10 min avant utilisation.
Réactifs
Des solutions de 0,1 µmol/L d'hydroxyde de sodium (NaOH), 25 % de TMAH, 30 % d'acide chlorhydrique (HCl) et de protéinase K ont été obtenues auprès de Wako (Osaka, Japon). Une solution d'acide nitrique à 70 % (HNO3 ) a été obtenu de Kanto Kagaku (Tokyo, Japon).
Animaux
Des souris BALB/c (femelles, 6 semaines) ont été achetées auprès de Japan SLC (Shizuoka, Japon). Les souris ont été logées dans une pièce avec un cycle lumière/obscurité de 12 h (lumières allumées à 8h00 et lumières éteintes à 20h00). La nourriture et l'eau étaient fournies ad libitum. Les protocoles expérimentaux ont adhéré aux directives éthiques de l'Université d'Osaka, au Japon.
Mesure des distributions granulométriques par diffusion dynamique de la lumière
Le nAg a été dilué dans de l'eau milliQ jusqu'à une concentration finale en argent (Ag) de 10 g/mL. Ensuite, la taille et la cellule capillaire zêta (Malvern Instruments, Malvern, Royaume-Uni) ont été remplies avec 1 mL de la solution pour mesurer la distribution des particules et le diamètre moyen avec un Zetasizer Nano-ZS (Malvern Instruments).
Mesure de la masse brute d'Ag
Pour mesurer la concentration totale d'Ag dans les échantillons, un Agilent 7700x (Agilent Technologies, Santa Clara, CA, USA) a été utilisé. Les conditions d'analyse étaient une puissance RF de 1550 W, un gaz porteur de 1,05 L/min d'Ar et un temps de séjour de 100 ms. Les mesures ont été répétées trois fois en mode MS. Une méthode d'étalon interne a été utilisée et le rhodium a été utilisé comme étalon interne pour Ag. Les éléments cibles des analyses ICP-MS étaient 103 Rh et 107 Ag. Des solutions étalons d'Ag et de rhodium ont été obtenues auprès de Wako (Osaka, Japon).
Analyse de sp-ICP-MS et de son calcul
Pour l'analyse sp-ICP-MS, nous avons utilisé un Agilent 7700x (Agilent Technologies; Santa Clara, CA, USA) similaire à l'analyse de l'Ag total. Les conditions d'analyse étaient les suivantes :puissance RF 1550 W, gaz porteur 1,05 L/min Ar, temps de séjour 10 ms et temps d'analyse 30 s. Afin de calculer la taille des particules, des outils de calcul de particules uniques publiés par RIKILT ont été utilisés [12].
Concentration de particules critiques pour sp-ICP-MS
La concentration de la solution mère de nAg était de 1,0 mg/mL, qui a été utilisée pour préparer des solutions de 2000, 800, 700 et 600 pg/mL. Chacune de ces solutions a ensuite été diluée 10 fois en série pour obtenir 40 solutions de nAg différentes. Nous avons déterminé les concentrations de particules de ces 40 échantillons par sp-ICP-MS.
Optimisation des méthodes de prétraitement pour le foie de souris
Les foies prélevés sur les souris ont été mélangés avec une solution saline tamponnée au phosphate (PBS) (w /v rapport de 1:10) puis homogénéisé. L'homogénat a été mélangé avec 100 ng/mL de solution de nAg. Le mélange a ensuite été traité avec l'un des réactifs suivants à un v /v rapport de 1:1—0,1 mol/L de solution de NaOH, 25 % de TMAH, 30 % de HCl ou une solution de protéinase K (10 U/mL de protéinase K, 0,01 M de Tris-HCl, 0,01 M d'EDTA et 0,5 % de SDS). Les échantillons ont été incubés pendant 3h à 37°C et les résidus ont été collectés et pesés. Les surnageants ont été dilués 500 fois et analysés par sp-ICP-MS.
Évaluation de la polyvalence du prétraitement NaOH dans divers organes
Les cœurs, poumons, rate et reins prélevés sur les souris ont été mélangés avec du PBS (w /v rapport de 1:10), homogénéisé et mélangé avec 100 nm/mL de nAg. Ensuite, 1 mol/L de solution de NaOH à un v /v un rapport de 1:1 a été ajouté et incubé pendant 3 h à 37 °C. Après incubation, les résidus ont été collectés et pesés. Les surnageants ont été dilués 500 fois et analysés par sp-ICP-MS.
Évaluation de la quantité et des propriétés physiques de nAg100 et Ag + chez la souris après administration intraveineuse unique
Pour administration intraveineuse, nAg100 et AgNO3 ont été dilués à 0,25 mg/mL (comme Ag + ) avec une solution de glucose à 5%. Des souris BALB/c ont reçu par voie intraveineuse du nAg100 (1,5 ou 0,75 mg/kg), AgNO3 (1,5 ou 0,75 mg/kg en Ag + ) ou une solution de glucose à 5 % (contrôle). Après 24h, le sang et les foies des souris sacrifiées ont été collectés. Les foies ont été mélangés avec du PBS (w /v rapport de 1:10) et homogénéisé. Les homogénats de sang et de foie ont été mélangés avec une solution de TMAH (v /v rapport de 1:1) et avec une solution de NaOH (v /v rapport de 1:1), respectivement. Ces échantillons ont été analysés par ICP-MS pour mesurer les concentrations d'Ag et par sp-ICP-MS pour évaluer les propriétés physiques, telles que la taille des particules et la distinction entre les particules et les ions.
Résultats et discussions
Optimisation de la détection de particules par sp-ICP-MS
Dans l'analyse sp-ICP-MS, il est important d'introduire une ou aucune particule dans le détecteur par temps de séjour. Si plusieurs particules sont introduites dans le détecteur au cours du temps de séjour, la masse brute de plusieurs particules est considérée comme la masse d'une seule particule [13]. Par conséquent, les échantillons doivent être suffisamment dilués pour l'analyse sp-ICP-MS. En revanche, l'analyse sp-ICP-MS d'un échantillon avec une très faible concentration d'ENP conduit à des données de distribution et de taille des particules inexactes.
Pour déterminer les relations entre la concentration de nAg100 et le nombre de particules détectées, nous avons dilué en série les solutions mères de nAg100 pour évaluation par sp-ICP-MS. Le résultat a montré que le nombre de particules détectées augmentait théoriquement et linéairement dans la région de concentration d'Ag relativement plus faible. En revanche, à des concentrations d'Ag relativement plus élevées, le nombre de particules détectées était inférieur à la valeur théorique (Fig. 1a). Ces données ont indiqué qu'à des concentrations d'Ag plus élevées, plusieurs particules ont tendance à être introduites dans le détecteur pendant chaque temps de séjour, ce qui entraîne une surestimation de la taille des particules. Ainsi, il est nécessaire de déterminer le plus grand nombre de particules détectées qui ne diffèrent pas de la valeur théorique pour évaluer avec précision les tailles de particules. Ensuite, nous avons soustrait le nombre de particules détectées de la valeur théorique et tracé la différence sur l'axe vertical. Les résultats ont indiqué que des écarts dans l'estimation de la taille se produisaient lorsque le nombre de particules détectées était> 500. Cela suggère qu'il est nécessaire de détecter ≤ 500 particules pendant le temps d'analyse (Fig. 1b). Bien que ces données aient été obtenues dans un seul essai, la répétition de l'expérience a montré les mêmes résultats (données non présentées).
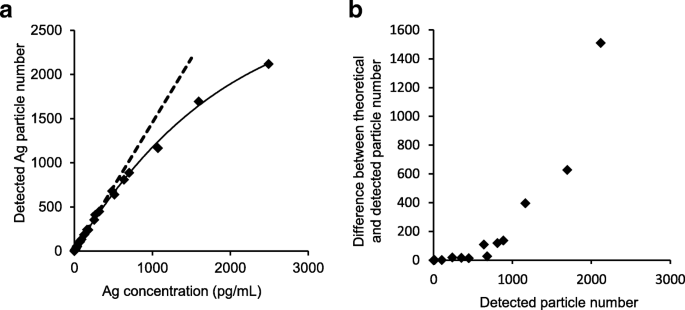
Détermination du nombre optimal de particules par temps de séjour pour une analyse sp-ICP-MS précise. Une série de solutions de nAg (600 fg/mL à 2 500 pg/mL) ont été analysées par sp-ICP-MS. un Pour déterminer la relation entre la concentration de nAg100 et le nombre de particules détectées, une courbe pour les particules détectées (trait plein) les valeurs théoriques (trait pointillé) ont été tracées. b Le nombre de particules détectées soustrait de la valeur théorique a été tracé sur l'axe vertical pour déterminer le nombre optimal de particules. Chaque point est le résultat d'un seul essai (n = 1)
Afin de valider les conditions d'analyse, nous avons dilué du nAg avec différents diamètres (nAg30, nAg70, nAg100) pour détecter < 500 particules par temps d'analyse et évalué leurs diamètres. L'analyse sp-ICP-MS a indiqué que les diamètres primaires de nAg30, nAg70 et nAg100 étaient respectivement de 30,0 ± 1,2, 65,1 ± 0,6 et 97,4 ± 0,6. De plus, les diamètres hydrodynamiques déterminés par diffusion dynamique de la lumière (DLS) étaient respectivement de 36,4 ± 1,6, 70,6 ± 1,7 et 101 ± 1,0, ces valeurs sont similaires à celles estimées par sp-ICP-MS. Ces résultats suggèrent que les conditions sp-ICP-MS étaient appropriées pour mesurer les diamètres de nanoparticules de différentes tailles.
Optimisation des méthodes de prétraitement pour la détection de nAg dans les tissus hépatiques de souris
Pour quantifier et déterminer les propriétés physiques des ENP dans le corps, il est nécessaire de lyser complètement les tissus. De plus, il est essentiel de récupérer efficacement les particules et les ions distribués dans l'organisme sans induire de modifications physiques ou chimiques des particules. Nous avons testé cinq réactifs solubilisants, NaOH, TMAH, HNO3 , HCl ou protéinase K, et analysé la quantité et les propriétés physiques par sp-ICP-MS pour optimiser les stratégies de prétraitement en utilisant le foie comme modèle [14,15,16,17,18].
L'homogénat de foie a été mélangé avec nAg100 pour obtenir une concentration finale en Ag de 100 ng/mL suivi d'un traitement avec chaque réactif solubilisant à 37°C. Tout d'abord, nous avons évalué la quantité de résidus tissulaires en tant qu'indicateur de la solubilité des tissus. Plus de 90 % des tissus ont été dissous par traitement avec NaOH, TMAH et protéinase K, tandis que seulement 75 % des tissus ont été dissous par HNO3 et les traitements au HCl (Fig. 2a). Considérant que près de 80% du tissu est composé d'eau [19], HNO3 Les traitements par , HCl et PBS étaient inefficaces pour dissoudre la matrice tissulaire insoluble. En revanche, le traitement avec NaOH, TMAH et la protéinase K a dissous efficacement la matrice insoluble des tissus, indiquant leur aptitude à quantifier avec précision le nAg dans le tissu. Ensuite, nous avons analysé le taux de récupération de chaque particule et ion pour évaluer le changement des propriétés physiques avec chaque traitement. L'analyse Sp-ICP-MS a montré que nAg100 était presque complètement ionisé par traitement avec des réactifs acides (HNO3 et HCl) et partiellement ionisé lorsqu'il est traité avec la protéinase K. Cela suggère que les réactifs acides et la protéinase K ont dissous les particules et les ont converties en ions. En revanche, 100 ng/mL Ag, correspondant à la quantité initialement ajoutée, ont été détectés sous forme de particules lorsque le tissu a été traité avec des réactifs alcalins (NaOH et TMAH). Presque aucun ion n'a été détecté après les traitements alcalins (Fig. 2b), indiquant que NaOH et TMAH maintenaient les propriétés physiques du nAg. Enfin, nous avons évalué la distribution des diamètres de particules dans les tissus traités avec les différents réactifs, afin d'analyser les propriétés physiques en détail. Le diamètre moyen des particules est passé de 100 nm à 120 après traitement TMAH (Fig. 2c). De plus, les particules étaient plus larges après le traitement au TMAH (Fig. 2d), indiquant une agrégation des particules. En revanche, lorsque les tissus ont été traités avec du NaOH, le diamètre moyen des particules était proche de 100 µnm, correspondant à la granulométrie initiale. Cela suggère que le prétraitement avec NaOH est la condition optimale pour détecter nAg100 dans les tissus hépatiques de souris.
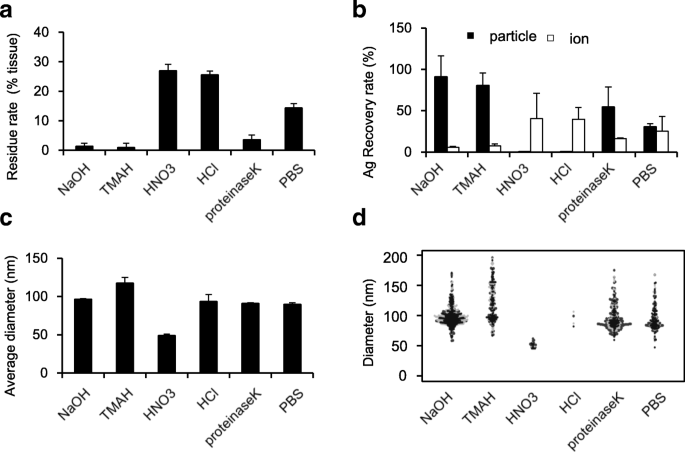
Le prétraitement au NaOH est la méthode optimale pour détecter nAg100 dans le foie de souris. Cinq réactifs solubilisants ont été criblés comme solvants de prétraitement pour lyser les tissus (NaOH, TMAH, HNO3 , HCl et protéinase K). L'homogénat de foie a été mélangé avec une solution de nAg100 pour obtenir une concentration finale en Ag de 100 ng/mL et traité avec chaque réactif solubilisant à 37°C. Après 3 h, a taux de résidus dans chaque groupe en tant qu'indicateur de solubilité tissulaire, b taux de récupération (les barres noires et blanches représentent le taux d'argent détecté sous forme de particules et d'ions, respectivement), c diamètres moyens des particules indiqués dans un graphique à barres, et d la distribution granulométrique montrée dans un diagramme d'abeille a été analysée par analyse sp-ICP-MS. Les résultats sont exprimés en moyenne ± SD (n = 3)
Le prétraitement TMAH a été largement utilisé pour l'analyse sp-ICP-MS dans diverses études. Le TMAH peut induire l'agrégation de nAg100 en fonction de diverses propriétés physiques telles que la viscosité et le pH. De plus, la constante diélectrique peut être liée à l'agrégation. Un traitement au TMAH pendant 3 h peut augmenter la constante diélectrique causée par la décomposition du TMAH en triméthylamine (TMA) et en méthanol [20]. Une augmentation de la constante diélectrique amène le potentiel zêta de nAg100 qui est inversement proportionnel à la constante diélectrique, à presque zéro, entraînant la perte de répulsion électrostatique entre nAg et l'induction d'agrégation. Le traitement de nAg100 avec du TMAH pendant une courte période (1 min) a donné une taille de particule moyenne d'environ 100 nm (données non présentées).
Évaluation de la polyvalence du prétraitement NaOH dans divers organes
Pour évaluer la polyvalence du prétraitement NaOH pour détecter le nAg, nous avons traité divers organes de souris (cœur, poumon, rein et rate) avec du NaOH et effectué une sp-ICP-MS pour la détection de particules. Tout d'abord, nous avons évalué la quantité de résidus tissulaires en tant qu'indicateur de la solubilité des tissus. Plus de 95 % de solubilisation des tissus a été obtenue par traitement au NaOH (Fig. 3a). De plus, l'Ag correspondant aux quantités d'additifs a été détecté sous forme de particules (Fig. 3b). Bien que certains taux de récupération aient dépassé 100 %, les critères de la Food and Drug Administration des États-Unis indiquent qu'un taux de récupération de 80 à 120 % est suffisamment fiable [21]. Notre analyse est donc fiable. De plus, le diamètre moyen des particules de nAg détecté dans n'importe quel organe était proche de 100 nm, correspondant à la taille des particules du nAg ajouté (Fig. 3c, d). Ces études suggèrent que le prétraitement au NaOH est idéal pour détecter le nAg non seulement dans le foie de souris, mais également dans le cœur, les poumons, les reins et la rate de souris.
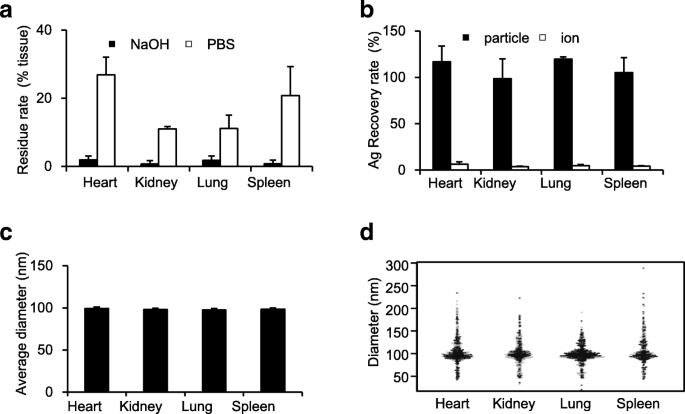
Le prétraitement au NaOH est la méthode optimale pour détecter nAg100 dans divers organes. Comme sur la figure 2, les homogénats de cœur, de rein, de poumon et de rate ont été mélangés avec du nAg100 et incubés avec une solution de NaOH. Après 3 h, a taux de résidus (les barres noires et blanches représentent les taux de résidus dans le traitement NaOH ou PBS, respectivement), b taux de récupération (les barres noires et blanches représentent le taux d'Ag détecté sous forme de particules et d'ions, respectivement), c diamètres moyens des particules indiqués dans un diagramme d'abeilles chaudes, et d la distribution de la taille des particules montrée dans un diagramme d'abeille a été analysée par analyse sp-ICP-MS dans chaque échantillon de tissu. Les résultats sont exprimés en moyenne ± SD (n = 3)
Pris ensemble, nos résultats démontrent que le prétraitement NaOH est la stratégie de prétraitement optimale pour la quantification et les analyses des propriétés physiques du nAg dans les tissus animaux par sp-ICP-MS.
Évaluation de sp-ICP-MS pour les analyses quantitatives et physiques des propriétés de nAg et Ag + dans les tissus biologiques
nAg s'ionise dans le corps ou cet Ag + particules dans les tissus de souris, bien que les détails de ce processus ne soient pas clairs. Par conséquent, nous avons évalué l'application pratique de la sp-ICP-MS en analysant à la fois la quantité et les propriétés physiques de l'Ag dans le sang et le foie de souris après une seule administration intraveineuse de nAg100 ou Ag + . L'analyse ICP-MS a montré que l'Ag a été détecté dans le sang des deux Ag + - et des souris traitées au nAg100 (Fig. 4a). De plus, Ag a été détecté dans le foie des deux groupes (Fig. 4b). Ensuite, nous avons analysé les propriétés physiques de l'Ag dans chaque échantillon. Parce que de petites quantités de nAg ont été détectées dans le sang des deux Ag + - et chez les souris traitées au nAg100, la plupart des Ag détectés étaient sous forme ionique (Fig. 4c). Dans les échantillons de foie, environ 80 % d'Ag ont été détectés sous forme de particules chez les souris traitées avec nAg100, tandis qu'une petite quantité de nAg a été détectée dans Ag + -souris traitées (Fig. 4d). Enfin, nous avons évalué la taille des particules dans le foie de souris traitées avec nAg100 par sp-ICP-MS, qui a montré que la taille des particules était d'environ 80 nm (Fig. 4e). Ces données suggèrent que Ag + administré dans le sang à peine changé en particules, et les propriétés physiques de l'Ag + dans le sang et le foie n'ont pas été modifiés. En revanche, nAg100 administré dans le sang était partiellement ionisé; 20 % de l'Ag dans le foie et la plupart des Ag dans le sang étaient sous forme ionique. En raison de l'ionisation partielle, le diamètre moyen du nAg dans les tissus hépatiques était inférieur à celui des particules initialement administrées (80 vs 100 nm). Par conséquent, notre stratégie sp-ICP-MS applicable aux échantillons biologiques a révélé que le nAg100 administré dans le sang était distribué sous forme de particules (environ 80 %) dans le foie et sous forme d'ions (environ 95 %) dans le sang, tandis que la méthode ICP-MS pouvait évaluer uniquement les quantités d'Ag et non les changements physiques ou chimiques dans les particules.
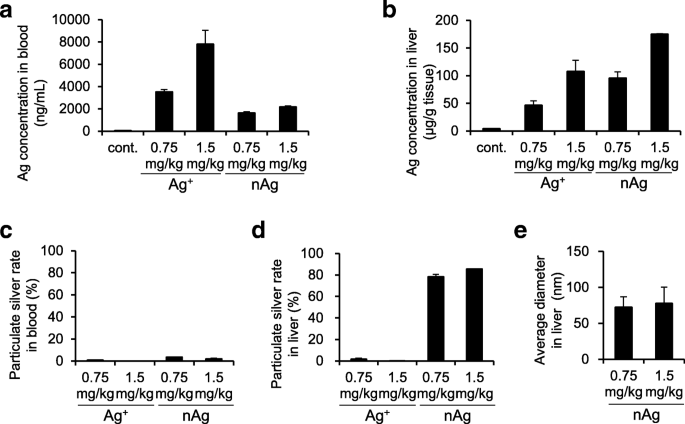
Quantification simultanée et analyses des propriétés physiques du nAg100 et de l'Ag + administrés par voie intraveineuse . nAg100 et Ag + ont été administrés par voie intraveineuse à des souris (0,75 ou 1,5 µmg/kg). Après 24h, leurs foies et leur sang ont été prélevés. Tous les échantillons ont été prétraités avec une solution de NaOH. Concentration d'Ag dans a sang et b foie ont été mesurés par ICP-MS. nAg dans c sang et d foie ont été mesurés par sp-ICP-MS. Le diamètre moyen des particules détectées dans le foie est indiqué en e . Les résultats sont exprimés en moyenne ± SE (n = 3)
Conclusions
Nous avons identifié les conditions optimales de prétraitement pour l'analyse sp-ICP-MS du nAg dans les tissus biologiques, permettant une quantification simultanée et des analyses des propriétés physiques des ENP dans les tissus animaux. Nous avons également développé une méthode sp-ICP-MS adaptée à l'évaluation d'échantillons biologiques et démontré son applicabilité en évaluant le changement des propriétés physiques de nAg100 dans le foie et le sang. Nous avons également montré que le changement partiel de la forme particulaire à la forme ionique de nAg100 administré aux souris influençait leur cinétique et leur distribution. Cette technique peut être appliquée dans l'analyse des risques des ENP en évaluant les conditions d'exposition aux ENP, en élucidant les réponses biologiques aux ENP et en identifiant les mécanismes sous-jacents aux réponses.
Disponibilité des données et des matériaux
Le partage de données n'est pas applicable à cet article car aucun ensemble de données n'a été généré ou analysé au cours de l'étude en cours.
Abréviations
- Ag :
-
Argent
- Ag + :
-
Ion d'argent
- DLS :
-
Diffusion dynamique de la lumière
- ENP :
-
Nanoparticules d'ingénierie
- HCl :
-
Acide chlorhydrique
- HNO3 :
-
Acide nitrique
- ICP-MS :
-
Spectrométrie de masse à plasma à couplage inductif
- nAg :
-
Nanoparticules d'argent
- nAg100 :
-
100 nm nAg
- nAg30 :
-
30 nm nAg
- nAg70 :
-
70 nm nAg
- NaOH :
-
Hydroxyde de sodium
- PBS :
-
Solution saline tamponnée au phosphate
- sp-ICP-MS :
-
ICP-MS à particule unique
- TEM :
-
Microscope électronique à transmission
- TMAH :
-
Hydroxyde de tétraméthylammonium
Nanomatériaux
- Stylo et papier vs logiciel de maintenance :la meilleure méthode pour réduire les temps d'arrêt
- Nanoparticules pour le traitement du cancer :progrès actuels et défis
- Ingénierie des procédés de revêtement par immersion et optimisation des performances pour les appareils électrochromes à trois états
- Nouveaux nanoparticules Au Nanostars@PEG biocompatibles pour l'imagerie CT in vivo et les propriétés de clairance rénale
- Méthode de post-traitement pour la synthèse de nanoparticules binaires monodisperses FePt-Fe3O4
- La préparation de la nanostructure jaune-enveloppe Au@TiO2 et ses applications pour la dégradation et la détection du bleu de méthylène
- Progrès récents dans les méthodes de synthèse et les applications des nanostructures d'argent
- Le meilleur niveau d'optimisation et d'organisation dans l'usine intelligente
- Le défi de la méthode 5S pour l'industrie 4.0



