Progrès récents dans les méthodes de synthèse et les applications des nanostructures d'argent
Résumé
En tant que matériaux fonctionnels avancés, les nanoparticules d'argent sont potentiellement utiles dans divers domaines tels que la photoélectrique, la biodétection, la catalyse, l'antibactérien et d'autres domaines, qui sont principalement basés sur leurs diverses propriétés. Cependant, les propriétés des nanoparticules d'argent sont généralement déterminées par leur taille, leur forme et le milieu environnant, qui peuvent être modulés par diverses méthodes de synthèse. Dans cette revue, les méthodes de fabrication pour synthétiser des nanoparticules d'argent de différentes formes et tailles spécifiques sont illustrées en détail. En outre, les propriétés et applications correspondantes des nanoparticules d'argent sont également discutées dans cet article.
Contexte
Les nanoparticules métalliques aux propriétés optiques et électriques uniques ont été largement étudiées au cours des dernières décennies. Les nanoparticules d'Ag (AgNPs) sont les nanoparticules métalliques les plus étudiées en raison de leurs propriétés et applications uniques [1,2,3,4,5]. Les propriétés des AgNPs dépendent grandement de la morphologie des particules, y compris les formes, les tailles et le milieu environnant. De gros efforts ont été consacrés aux méthodes de synthèse et à la régulation morphologique des nanoparticules d'argent.
Récemment, des chercheurs ont mené une étude approfondie sur l'excellente fonction des nanoparticules d'argent telles que la photo-électricité [6], la catalyse [7], les antibactériens [8, 9], les biocapteurs [10] et la diffusion Raman améliorée en surface (SERS ) [11]. Jusqu'à présent, les AgNPs ont été préparés avec succès par réduction chimique [12,13,14,15,16], photo-réduction [17, 18] et synthèse laser [19], etc. Cependant, ces méthodes sont généralement consommatrices de temps et d'énergie. Dans le même temps, ils présentent également les inconvénients de conditions de préparation strictes et les AgNPs étaient de taille inhomogène. Par conséquent, des méthodes simples et économiques, par lesquelles la taille, la forme et la distribution de la taille des AgNPs peuvent être finement contrôlées, doivent être développées de toute urgence. L'utilisation d'agents protecteurs est un moyen efficace de fabriquer les AgNPs avec une bonne stabilité et dispersibilité. Pendant ce temps, l'agglomération entre les particules peut être empêchée par un agent protecteur. Il est donc important d'utiliser des agents protecteurs pour la synthèse des AgNP [20].
Dans ce travail, la préparation de nanoparticules d'argent de différentes formes telles que des nanocubes, des nanofils et des nanosphères a été examinée en détail. Les travaux représentatifs sur la préparation de nanoparticules d'argent avec différentes formes et tailles d'AgNPs 1-10 nm, AgNPs 10-100 nm ont été examinés auparavant. En tant qu'excellentes caractéristiques de protection de l'environnement et opération simple, les nouvelles méthodes de biosynthèse pour obtenir des nanoparticules d'argent qui peuvent servir d'alternative aux procédures de synthèse chimique complexes ont été mises en évidence. Pendant ce temps, les propriétés et les applications des AgNPs telles que l'antibactérien, la fluorescence, la catalyse et la résonance plasmonique de surface ont été examinées en détail comme suit. L'application importante des nanoparticules d'argent qui peuvent être utilisées dans les nanocapteurs a été soulignée dans cette revue.
Cette étude fournit une approche globale qui est importante pour l'étude des AgNPs. Cependant, il convient de noter que les méthodes de préparation innovantes et les percées d'application doivent encore être explorées.
Méthodes synthétiques
Les nanoparticules d'argent ont été synthétisées par diverses méthodes, telles que la méthode de croissance des graines [21] et la méthode de réduction par étapes [22]. Chaque méthode présente des avantages et des limites. Ainsi, développer une méthode de préparation efficace reste un défi. En raison des propriétés uniques et des applications étendues, la méthode de synthèse des nanoparticules d'argent mérite d'être optimisée. Nous avons résumé six types de méthodes de préparation, y compris de nouvelles méthodes de biosynthèse dans ce travail. Nous espérons apporter un peu d'aide aux travailleurs qui s'engagent dans ce domaine.
Préparation de différents types d'AgNPs
Récemment, les chercheurs se sont concentrés sur le contrôle de la forme des AgNPs en raison de leurs propriétés dépendantes de la morphologie [23, 24]. Parallèlement, afin d'étendre leurs applications actuelles, la préparation de nanoparticules d'argent de différentes formes (telles que la forme de corail [25], la cage [26] et les nanocristaux triangulaires [27]) a suscité un large éventail de recherches scientifiques. Le mécanisme de formation et les différentes méthodes de préparation des nanoparticules d'argent ont été longtemps explorés.
Synthèse d'Ag Nanocubes
Xia et al. [28,29,30] ont préparé massivement des échantillons monodispersés de nanocubes d'argent en réduisant le nitrate d'argent avec de l'éthylène glycol en présence de poly vinyl pyrrolidone (PVP). Dans le processus de synthèse, le PVP a été utilisé comme agents protecteurs qui peuvent stabiliser les nanoparticules d'argent dispersives et empêcher l'agglomération. Dans le même temps, la quantité d'ajout de PVP peut également affecter la morphologie des AgNPs. Par conséquent, il est essentiel d'utiliser PVP lors de la synthèse. Il est bien connu que le chauffage peut fournir plus d'énergie de réaction, ce qui est bénéfique pour augmenter la réductibilité de l'éthylène glycol. En présence d'ions hydroxyles, Ag + a été réduit pour former des nanocubes d'argent. L'avantage de cette recherche est qu'elle peut être utilisée pour préparer des nanocubes monocristallins homogènes. À l'échelle du nanomètre, les métaux dont la plupart sont cubiques à faces centrées (fcc) ont tendance à nucléer et à se développer en particules jumelées et multi-jumelées (MTP) en raison de leurs surfaces délimitées par les facettes les plus énergétiques à l'échelle nanométrique [31] . De plus, cette structure est avantageuse pour être appliquée dans le domaine de la photonique, de la catalyse et de la détection basée sur SERS. L'image (Fig. 1) montre les images SEM, TEM et XRD de nanocubes d'argent. Ces nanocubes d'argent avaient une longueur de bord moyenne de 175 nm, avec un écart type de 13 nm. Leurs surfaces étaient lisses et tous les coins et bords de ces particules étaient légèrement tronqués. Cette structure peut être utilisée pour les systèmes d'administration de médicaments en injectant du médicament dans les coins tronqués.
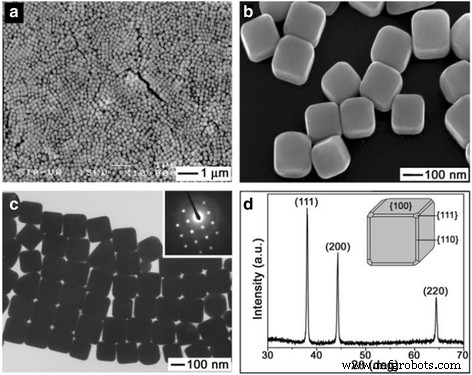
un Faible et b images SEM à fort grossissement de nanocubes d'argent légèrement tronqués. c Une image MET du même lot de nanocubes d'argent. d Un modèle XRD du même lot d'échantillon, confirmant la formation d'argent fcc pur [28]
Une nouvelle nanoparticule d'argent a été publiée par Yam et al. [32] qui utilisait le bromure de cétyltriméthylammonium (CTAB) comme tensioactif en solution aqueuse. L'ion brome peut réagir avec le complexe argent ammoniac ([Ag (NH3 ) 2 ] + ) pour produire une précipitation d'AgBr, et les ions argent seront libérés lentement dans la réaction suivante. Dans le même temps, les ions d'argent résiduels ont été réduits par le glucose et une taille d'environ 55 nm de cube de nano-argent a été formée avec le tensioactif enrobé. Le tensioactif CTAB peut être adsorbé à la surface des AgNPs par adsorption physique. Pour cette raison, l'agglomération et la croissance d'échelle des AgNPs peuvent être efficacement contrôlées par inhibition. En raison de l'existence de CTAB, il est possible d'obtenir des AgNPs avec une dispersion uniforme et une taille appropriée.
Il faut beaucoup de temps pour préparer des cubes de nanoargent rapportés par la méthode synthétique de Xia et Yam. Mais les nanoparticules d'argent peuvent être rapidement produites par la méthode des micro-ondes. Saraf et al. [33] ont préparé des nanocubes d'argent en utilisant une grande quantité de graines d'or en présence de polyélectrolyte et de chauffage par micro-ondes pendant 60 à 120 s. L'expérience indique que le polyélectrolyte guide la croissance de la particule dans une direction cristallographique spécifiée, ce qui donne la particule à facettes, c'est-à-dire un nanocube. A l'heure actuelle, la préparation de nanoparticules d'argent par la méthode polyol est plus aboutie.
Synthèse de nanofils et nanotiges d'Ag
Murphy et al. [34] ont rapporté que les nanotiges et les nanofils peuvent être préparés avec succès en utilisant de l'acide ascorbique pour réduire l'AgNO3 en présence de germe Ag, de la matrice micellaire CTAB, et de NaOH. Le diamètre moyen des graines d'Ag est de 4 nm. Dans ce travail, la concentration de graine et la concentration relative de base d'Ag + jouer un rôle clé dans la fabrication de nanomatériaux à rapport d'aspect plus important. Le CTAB est également nécessaire pour préparer un haut rendement de crayons. L'image du MET (Fig. 2) montre la forme des nanotiges et des nanofils.

un Nanotiges d'argent séparées par la forme d'une préparation avec 0,06 ml de graine. b Nanofils d'argent séparés par des formes [34]
Des nanotiges d'argent ont été préparées par Lee et al. [35]. Dans la méthode de croissance médiée par les graines, de petites particules métalliques sont d'abord préparées et ensuite utilisées comme graines pour la préparation de nanotiges. Les graines d'argent ont été préparées par réduction d'ions argent avec du borohydrure de sodium en présence de citrate de sodium dihydraté comme stabilisant. Ces graines d'argent ont été ajoutées à la solution contenant plus de sel d'argent, un acide ascorbique (agent réducteur faible) et un CTAB. Dans cette étude, la température de réaction et le pH ont contrôlé le rapport d'aspect et l'uniformité des tiges résultantes. L'augmentation de la température de réaction a entraîné une diminution du rapport d'aspect des nanotiges d'argent et une augmentation de la taille des particules monodispersées. De plus, l'augmentation du pH a montré des résultats similaires. Lorsque la température de réaction et le pH ont été augmentés, le taux de réduction de l'argent a été encore augmenté. Dans l'expérience, des nanotiges d'argent avec un rapport d'aspect élevé et une monodispersité ont été synthétisées dans des conditions de 30 °C et de pH 10,56. Des nanotiges d'argent ont été synthétisées par des méthodes électrochimiques à partir d'une solution aqueuse d'AgNO3 en présence de polyéthylène glycol (PEG) par Zhu et al. [36]. Il a été constaté que la concentration d'AgNO3 et le PEG ont affecté la formation des nanotiges.
Murphy et al. a fourni une meilleure méthode pour préparer des nanofils d'argent, mais la méthode synthétique de Sun [37, 38] est plus raffinée. Ils ont synthétisé des nanofils d'argent en réduisant AgNO3 avec de l'éthylène glycol en présence de graines et de PVP. Le mécanisme de réaction est le suivant :
$$ {2\mathrm{H}\mathrm{OCH}}_2\hbox{--} {\mathrm{CH}}_2\mathrm{O}\mathrm{H}\à {2\mathrm{CH}} _3\mathrm{CHO}+{2\mathrm{H}}_2\mathrm{O} $$ (1) $$ {2\mathrm{CH}}_3\mathrm{CHO}+{2\mathrm{Ag} \mathrm{NO}}_3\à {\mathrm{CH}}_3\mathrm{CO}\hbox{--} {\mathrm{COCH}}_3+2\mathrm{Ag}+{2\mathrm{HNO }}_3 $$ (2)Ensuite, AgNO3 et du PVP ont été ajoutés au guttatim dans le système de réaction, permettant la nucléation et la croissance de l'argent et formant une forme et une taille uniformes de nanofils. Des nanofils d'argent d'un diamètre de 30 à 40 nm et d'une longueur allant jusqu'à ∼ 50 m ont ainsi été produits. Les effets de diverses conditions de réaction (température, temps de réaction et conditions d'ensemencement) sur la morphologie et la taille ont été discutés dans cette revue. La figure 3 montre les formes et les tailles des nanofils purifiés.
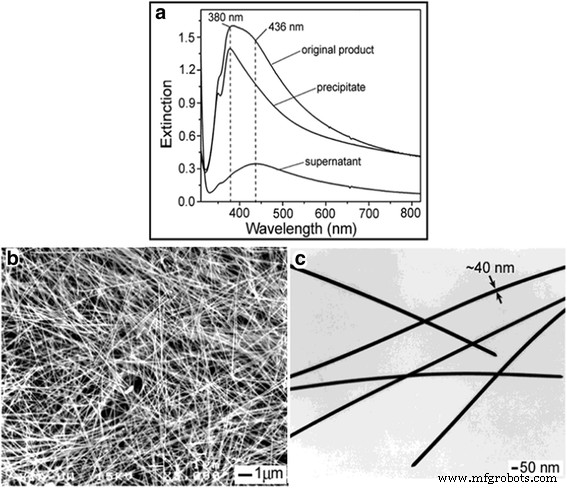
un Spectres d'extinction UV-visible du produit final avant et après 3 cycles de centrifugation et de séparation. b SEM et c Images MET d'un échantillon purifié de nanofils d'argent [37]
Dans le spectre UV-vis (Fig. 3a), on peut voir que les nanofils d'argent montrent un décalage vers le bleu évident dans l'absorption UV-vis par rapport à l'échantillon d'origine après purification. Le pic d'absorption UV-vis apparaît à 380 nm. La figure 3c montre que la largeur de ces nanofils est de 40 nm. On peut obtenir des nanofils de même largeur, ce qui est le meilleur atout de ce travail. Ces nanofils peuvent être utilisés pour préparer des films conducteurs [39] et des cellules solaires organiques efficaces [40], etc.
En étudiant plus avant la réaction de la PVP avec les nanofils d'argent, Xie et al. [41,42,43] ont conclu que la monocouche de PVP réagit avec les nanofils d'Ag via des liaisons Ag–O. Sur cette base, Xie et al. [44, 45] ont observé l'existence de jumeaux multiples dans des expériences qui ont prouvé que Xia sur le jumelage multiple est l'un des facteurs clés dans la formation de nanofils d'Ag. Le contrôle de la quantité initiale de nitrate d'argent ou la réduction du taux initial de réduction du nitrate d'argent est propice à la formation de nanofils d'argent dans la solution [46, 47]. La méthode spécifique qu'ils ont utilisée consiste à contrôler la réaction du sel métallique et du nitrate d'argent en ajoutant des ions chlore à la solution de réaction ou en réduisant le taux de libération des ions argent.
Tang et al. [48] ont synthétisé des nanofils d'argent à taille contrôlée en ajoutant un treillis en acier inoxydable au système qui a une concentration en ions plus élevée. C'est principalement que la maille en acier inoxydable peut réagir avec l'acide nitrique, ce qui peut être utile pour empêcher la corrosion des multiples grains de cristal. En présence d'ions chlorure, ils ont préparé des nanofils d'argent uniformes en utilisant la méthode hydrothermale, la méthode des micro-ondes et d'autres méthodes expérimentales [49, 50]. La nanoparticule de sulfure d'argent est un nouveau type de semi-conducteur qui est facilement synthétisé par la réaction d'ions de soufre avec des ions d'argent. Les nanoparticules de sulfure d'argent peuvent fournir des électrons et faire adsorber les ions d'argent à sa surface et agir comme un noyau et un agent réducteur. Dans le même temps, des atomes d'argent peuvent également être déposés à la surface d'Ag2 S pour former Ag2 Les graines S@Ag jouent ainsi un rôle d'auto-réduction catalytique, propice à la formation de nanofils d'argent [51].
Synthèse de nanosphères d'Ag
Les nanoparticules d'argent quasi-sphériques, qui sont couramment synthétisées par une méthode de réduction chimique, sont rapportées par de nombreux travaux car les atomes d'argent ont facilement tendance à former une structure sphérique pendant le processus de synthèse des nanoparticules d'argent. Dans le processus de réduction chimique, les agents de réduction couramment utilisés comprennent le borohydrure de sodium [52], le citrate de sodium [53], l'hydrate d'hydrazine [54], l'acide ascorbique [55] et l'hydrogène [56]. De toutes les équipes de recherche, l'équipe de Xia est la plus détaillée et la plus complète en matière d'étude. Afin d'obtenir la haute qualité des nanosphères monocristallines d'Ag [57], ils utilisent une nouvelle méthode basée sur la gravure humide qui est différente de la réduction chimique. En mélangeant rapidement la suspension de nanocubes d'Ag uniformes avec une petite quantité de solution de gravure à base de nitrate ferrique ou de ferricyanure, ils pourraient soit tronquer les coins et les bords pointus pour former des nanocubes arrondis, soit obtenir des nanosphères sans caractéristiques tranchantes qui ont le même diamètre que l'original cubes. Parce que les méthodes de synthèse précédentes sont incapables de préparer des sphères uniformes supérieures à ∼ 35 nm. Notamment, cette méthode pourrait être utilisée pour produire des nanosphères d'Ag uniformes avec une large gamme de tailles et ouvrir de nouvelles possibilités pour des études fondamentales sur SERS. Dans ce travail, les sphères d'Ag peuvent être préparées avec la plus petite taille de 25 nm et la plus grande taille de 142 nm. La figure 4 montre que les nanocubes d'argent ont été gravés en quasi-nanosphères.
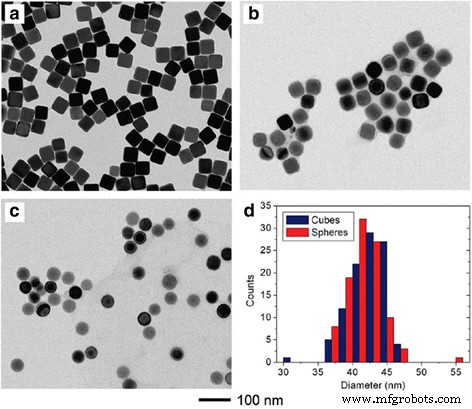
Images TEM (a–c ) de cubes d'Ag 42 nm coiffés de PVP lorsqu'ils sont gravés avec différents volumes de nitrate ferrique 0,5 mM. un 0 L. b 10 L. c 100 L. d Distributions de tailles calculées à partir de 100 particules dans les parties a et c [57]
Les AgNP préparés avec cette méthode ont une forme régulière et une taille uniforme. Ces nanosphères d'argent de forme régulière et de taille uniforme peuvent être utilisées pour préparer une nanocage d'or uniforme qui peut être utilisée pour l'administration de médicaments biologiques ciblés [58].
Liang et al. [59] ont rapporté une nouvelle technique de fabrication de nanoparticules d'argent monodispersées. Le PEG est utilisé à la fois comme solvant et réactif réducteur et le PVP est utilisé comme agent de coiffage pour la synthèse de nanoparticules d'argent monodispersées. Pour obtenir des nanosphères uniformes d'un diamètre moyen de 54 nm, Liang a utilisé le PVP/AgNO3 molaire dans un rapport de 8 à 260 °C. La figure 5 montre les images TEM, HRTEM et XRD de nanosphères d'argent.

un TEM et b Images HRTEM des nanosphères d'argent préparées à 260 °C pendant 24 h avec un rapport molaire de PVP à AgNO3 de 8, et le modèle SAED (en médaillon) d'une nanosphère d'argent individuelle d'un diamètre d'environ 50 nm. c Modèle de poudre XRD prélevé sur le même lot d'échantillons [59]
On peut voir que la taille des nanosphères d'Ag est uniforme à partir de l'image MET. De plus, la méthode de synthèse est simple et elle peut être appliquée à la production de masse. Bien sûr, il existe de nombreux autres articles sur l'étude du nanoargent sphérique qui méritent également d'être appris. Mais dans ce travail, nous ne les répéterons pas. Dans la section suivante, nous décrirons trois types de méthodes de préparation par lesquelles différentes tailles de nanoparticules d'argent sont fabriquées. Nous espérons apporter un peu d'aide aux travailleurs qui étudient l'effet de la taille et des performances.
Préparation de différentes tailles d'AgNPs
Il est universellement reconnu que les nanoparticules d'argent de différentes tailles ont une influence significative sur les performances des matériaux. Néanmoins, nous constatons que peu d'articles décrivent systématiquement les méthodes de préparation de nanoparticules d'argent de différentes tailles. Nous avons donc introduit quelques méthodes synthétiques dans la section suivante dans l'espoir que cela puisse aider quelqu'un qui souhaite obtenir une taille définie.
Fabrication d'AgNPs de 1 à 10 nm
Les nanoparticules d'argent de petite taille étaient généralement produites par le processus de réduction rapide dans lequel le borohydrure de sodium était utilisé comme agents de réduction, et la taille et la forme des particules produites n'étaient pas uniformes. Shekhar et al. [60] ont préparé des nanoparticules d'argent de 5 à 10 nm en mélangeant différentes proportions de borohydrure de sodium et de citrate de sodium qui sont utilisés comme réducteur (en utilisant du borohydrure de sodium pour réduire préférentiellement la nucléation rapide et la réduction du citrate de sodium à nouveau pour maintenir une croissance régulière). Par cette méthode, la taille et la forme uniformes des AgNPs ont été obtenues. Le tableau 1 suivant montre les conditions conçues pour la synthèse de nanoparticules d'argent de différentes tailles.
Lin et al. [61] ont préparé des particules d'argent de 7 à 10 nm de forme et de taille uniformes en 2003. Une méthode synthétique simple a été décrite selon laquelle ils préfèrent préparer directement des nanoparticules d'argent étroitement dispersées plutôt que d'utiliser des processus de sélection de taille par réduction thermique du trifluoroacétate d'argent dans éther isoamylique en présence d'acide oléique. Cette synthèse directe est synthétiquement facile à contrôler et capable d'obtenir des AgNPs avec des diamètres compris entre 7 et 10 nm et une distribution de taille étroite. Au lieu d'utiliser l'approche traditionnelle qui implique le précurseur de sels d'argent et d'agent réducteur dans un solvant, un précurseur à source unique dans un solvant organique a été utilisé dans l'expérience. Pour cette raison, ils ont choisi le trifluoroacétate d'argent comme précurseur à source unique car il est facilement disponible et peut être thermiquement réduit en argent métallique à différentes températures. Enfin, ils ont transformé le diamètre des AgNPs en ajustant le rapport molaire de l'acide oléique au trifluoroacétate d'argent. La figure 6 ci-dessous montre les images MET en champ clair et l'analyse de la distribution granulométrique correspondante des AgNPs qui ont été obtenues à un rapport molaire acide oléique/trifluoroacétate d'argent de 10:1 pour des durées de (A, B) 30, (C, D ) 90, et (A, F) 150 min.
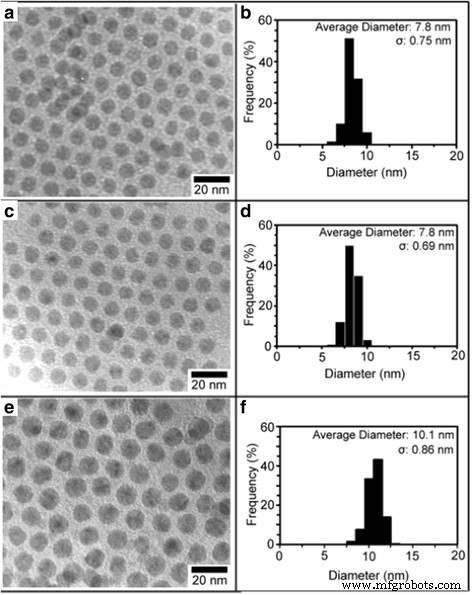
Images MET en fond clair et analyses de distribution granulométrique correspondantes des AgNPs obtenues à un rapport molaire acide oléique/trifluoroacétate d'argent de 10:1 pour des durées de (a , b ) 30, (c , d ) 90, et (e , f ) 150 min [61]
Yang et al. [62]. Ils ont été les pionniers d'une méthode selon laquelle l'aniline était utilisée comme agent réducteur et l'acide dodécylbenzène sulfonique (DBSA) comme stabilisant. Lors de l'ajout de NaOH en excès à l'aniline DBSA AgNO3 système, la formation de nanoparticules d'argent était presque terminée en seulement 2 minutes à 90 °C (avec un rendement de 94%). De plus, la taille moyenne de ces nanoparticules d'argent résultantes est de 8,9 ± 1,1 nm et le colloïde peut être stocké pendant plus d'un an à température ambiante. La Fig. 7 est les images TEM, DLS et XRD des AgNPs.
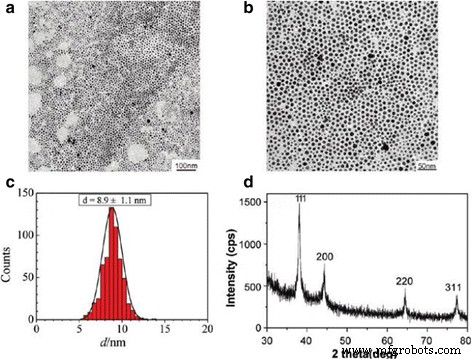
un , b Images MET à deux grossissements de nanoparticules d'argent recueillies à partir du système de réaction après avoir ajouté NaOH à 90 C pendant 1 h. c Histogramme correspondant de la distribution granulométrique des nanoparticules d'argent. d Modèle XRD de nanoparticules d'argent [62]
Les procédés de synthèse de nanoparticules d'argent de petite taille décrits ci-dessus sont tous dans le système en phase liquide. Cependant, Zheng et al. [63] ont synthétisé des nanoparticules d'argent d'un diamètre de 2 à 4 nm dans le système en phase solide. Ils ont synthétisé des nanoparticules d'argent luminescentes et actives Raman en tirant parti de la méthode de réduction thermique. La figure 8 montre la distribution de taille, la structure et l'émission de luminescence de nanoparticules d'argent de 3 nm qui sont créées par thermolyse en phase solide.
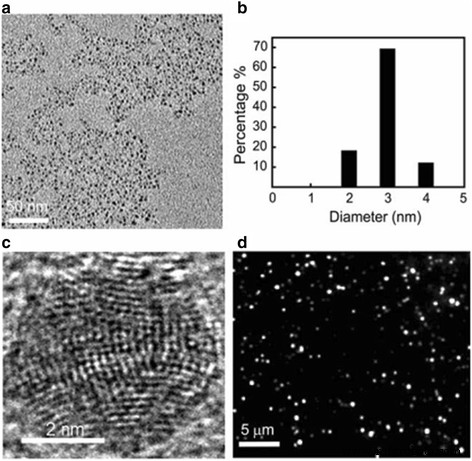
Distribution de taille, structure et émission de luminescence des nanoparticules d'argent de 3 nm créées par thermolyse en phase solide. un Image MET basse résolution de ces nanoparticules. b Distribution de taille des nanoparticules déterminée à partir de MET. c L'image MET haute résolution d'une si petite nanoparticules d'argent montre une structure hautement multi-domaine. d Image de luminescence de ces petites nanoparticules d'argent prise sous excitation laser de 488 nm à ~ 10 W/cm 2 [63]
Fabrication de 10-100 nm AgNPs
Par irradiation avec des électrons de 6 MeV, des AgNP d'un diamètre de 10 à 60 nm ont été synthétisés par Bogle et al. [64] dans le mélange de nitrate d'argent et de PVP. Cette méthode présente de nombreux avantages tels que l'efficacité de la préparation, une productivité élevée et peu de sous-produits. Abid et al. [65] ont préparé des nanoparticules d'argent en utilisant l'irradiation laser similaire au travail ci-dessus. La différence est qu'ils ont utilisé du dodécyl sulfate de sodium (SDS) comme agent de coiffage à mélanger avec du nitrate d'argent et que des nanoparticules d'argent d'une taille de 13 à 16 nm peuvent être préparées. La taille des particules est contrôlée par l'intensité du laser et la concentration initiale de tensioactif SDS. Avec l'utilisation de la réduction de l'acide ascorbique, des particules d'argent sphériques d'une taille de 30 à 72 nm ont été synthétisées par Qin et al. [66]. Pendant ce temps, la taille des nanoparticules d'argent diminuait à mesure que le pH du système réactionnel passait de 6,0 à 10,5. Ajitha et al. [67] ont utilisé une réduction chimique en ajustant le pH pour obtenir des AgNPs de 14 à 31 nm. Ils ont utilisé l'éthanol comme solvant, le borohydrure de sodium comme agent réducteur et l'alcool polyvinylique (PVA) comme agent de coiffage. La figure 9 montre le mécanisme de formation de ces nanoparticules d'argent.
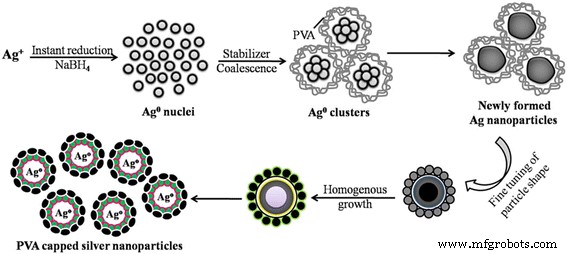
Représentation schématique de la synthèse d'AgNPs à taille contrôlée utilisant la méthode de réduction chimique [67]
De même, des particules d'Ag d'un diamètre de 15 à 21 nm ont été synthétisées par Silvert, P. Y. et al. [68] qui ont utilisé une solution d'éthylène glycol-PVP pour réduire le nitrate d'argent dans des conditions de température spécifiques. Les quasi-nanosphères uniformes ont été synthétisées par cette méthode. Afin de détecter la solubilité des nanoparticules d'argent de différentes tailles, des particules d'Ag de 10 à 80 nm ont été préparées par Rui Ma et al. [69]. Ils ont préparé de l'argent colloïdal dispersif par le procédé au polyol qui est une méthode de préparation mature [70]. Leurs méthodes de préparation sont basées sur Silvert, P. Y, en changeant le type d'agent protecteur. Récemment, l'étude de synthèse verte est très ardente et les chercheurs utilisent généralement des acides aminés ou une réduction de la peau Ag + pour synthétiser des nanoparticules d'argent. Parce qu'une méthode de synthèse respectueuse de l'environnement peut surmonter le problème de la production de substances toxiques dans les méthodes de préparation physiques et chimiques. Parmi eux, Maddinedi et al. [71] ont utilisé la tyrosine comme agents réducteurs et coiffants pour préparer des particules d'argent de 13 à 33 nm en ajustant le pH de 12 à 10. Mandal et al. [72] ont obtenu les mêmes résultats. Ils ont utilisé l'extrait de feuille de Cinnamomum tsoi comme agents réducteurs et coiffants pour préparer des particules d'argent de 11 à 31 nm en ajustant le volume intrant d'extrait de feuille de Cinnamomum tsoi. La figure 10 montre les modèles TEM et SAED des AgNPs.
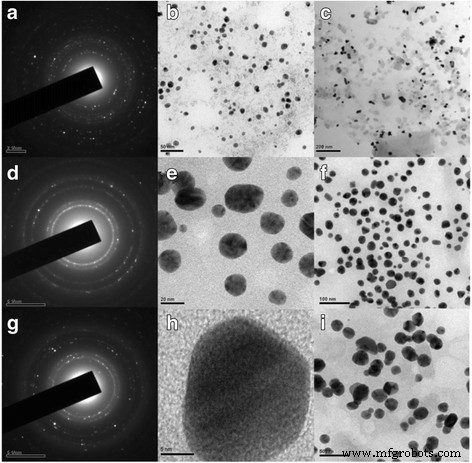
Images MET et patrons SAED de colloïdes le volume d'extrait de feuille 4 ml (Ct4) (a –c ), Ct3 (d –f ), et Ct1 (g –je ) nanoparticules [72]
La figure 11 montre la diffusion dynamique de la lumière (DLS) des AgNPs que le volume d'extrait de feuille a varié comme 1, 3 et 4 ml.
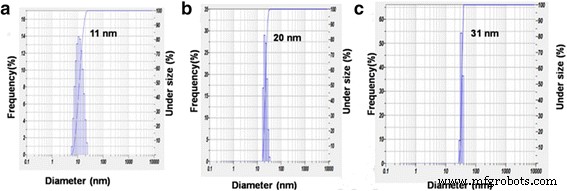
Tailles moyennes des particules obtenues pour les AgNPs Ct1 (a ), Ct3 (b ), et Ct4 (c ) [72]
Bien sûr, il existe de nombreuses autres méthodes pour préparer des particules d'argent de 1 à 100 nm. Les documents ci-dessus ne sont que typiques. Nous faisons ce travail parce que nous espérons aider quelqu'un qui veut synthétiser une taille définie. En conclusion, la préparation des nanoparticules d'argent doit être orientée vers une synthèse conviviale et une taille contrôlable.
Préparation des AgNPs par des méthodes biosynthétiques
La biosynthèse de nanoparticules métalliques à l'aide de systèmes biologiques a évolué pour devenir un domaine important de la nanobiotechnologie. Les méthodes de biosynthèse sont de meilleurs candidats pour la préparation des AsNP en raison des techniques respectueuses de l'environnement qui sont adoptées dans leur processus de fabrication et les produits sont adaptés aux bioapplications. Ici, les méthodes de biosynthèse ont une perspective de développement et de recherche. Nous avons donc une discussion détaillée pour certains cas synthétiques. En 1999, Klaus et al. [73] a d'abord utilisé Pseudomonas stutzeri pour synthétiser des nanocristaux d'argent de la taille de 200 nm. Par la suite, l'utilisation d'autres souches pour préparer des nanoparticules d'argent s'est beaucoup développée, comme l'aspergillus flavus et le trichoderma. Et Kazemi et al. [74] ont réussi à synthétiser des nanoparticules d'Ag en utilisant Geotricum sp. Geotricum sp. a été cultivé dans du milieu Sabro Dextrose Agar (SDA) à 25 ± ± 1 °C pendant 96 h. Le mycélium est utilisé pour convertir une solution de nitrate d'argent en nanoargent. Des nanoparticules d'argent ont été synthétisées de manière extracellulaire à l'aide de ces champignons (Geotricum sp.). Cette méthode synthétique efficace, écologique et simple peut être utilisée pour synthétiser des nanoparticules d'Ag de 30 à 50 nm. En raison de l'utilisation des conditions de température ambiante et de l'absence d'agents réducteurs nocifs, nous pouvons considérer cette méthode comme respectueuse de l'environnement et peu coûteuse. Récemment, Laryssa et al. [75] ont préparé des nanoparticules d'argent en utilisant le filtrat acellulaire du champignon nématophage Duddingtonia flagrans. Dans cette étude, ils ont rapporté un processus biologique simple pour la synthèse d'AgNPs en utilisant le champignon nématophage D. flagrans. Comparée à la biosynthèse qui est un processus bon marché, respectueux de l'environnement et à haut rendement, la synthèse extracellulaire qui ne nécessite pas de traitement supplémentaire pour séparer les particules des cellules vivantes est un processus plus simple. Les AgNPs biosynthétisés et fonctionnalisés ont une bonne stabilité et un rendement élevé, et les excellentes propriétés antibactériennes, antifongiques, antivirales et anticancéreuses leur confèrent un avenir prometteur dans les applications thérapeutiques, ce qui potentialise de nouvelles conceptions expérimentales sur l'utilisation du champignon D. flagrans.
On peut voir que le type de micro-organisme biologique sera la dernière direction de recherche dans l'étude du nanoargent.
Propriétés et applications des AgNPs
Propriétés et applications des AgNPs sur les antibactériens
Ces dernières années, les propriétés antibactériennes des nanomatériaux Ag ont progressivement suscité l'inquiétude des gens et de nombreuses applications antibactériennes ont été rapportées [76, 77]. Les AgNPs antibactériens avec différentes formes ont été recherchés par Helmlinger et al. [78]. By studying the cytotoxicity and antibacterial effect of four types silver nanometals, it can be seen that silver nanoparticles with different shapes own equal cytotoxicity, but it has different antibacterial effect. Meanwhile, particles with a higher specific surface area are more toxic for bacteria than particles with smaller specific surface areas. The dissolution kinetics is correlated to the estimated specific surface area of the particles where particles with a higher specific surface area dissolve faster than particles with a smaller one. The difference in the dissolution rate may be exploited to synthesize silver nanoparticles with a relative higher antibacterial effect and a lower cytotoxic effect towards tissue. However, Helmlinger et al. did not give a further detail study on the antibacterial effect of different sizes of AgNPs.
The antibacterial properties of silver particles with different sizes were studied by Agnihotri et al. [60]. It can be seen that 5 nm nanoparticles have the best antibacterial properties. It was found that the smaller particles exhibited the better antibacterial properties. The Fig. 12 shows the antibacterial properties of the different-sized silver nanoparticles.
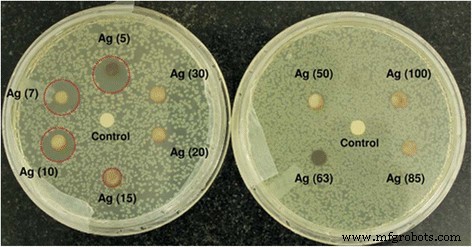
Disk diffusion tests for different-sized silver nanoparticles against the E. coli MTCC 443 strain. The zone of inhibition is highlighted with a dashed circle indicating a noticeable antibacterial effect [60]
Silver extends its antibacterial properties by combining with other materials. Research about combining with other materials included SiO2 @Ag [79], PLLA microcapsules combined with silver nanoparticles [80], electrodeposited chrome/silver nanoparticles (Cr/AgNPs) [81], graphene quantum dot/silver nanoparticles [82], Ag-decorated polymeric micelles with curcumin [83] and so on.
All the above studies are about the antibacterial properties of AgNPs. Next, we introduced the silver nanoparticles for antimicrobial application. It was found that the silver nanoparticles can be directly utilized as antibacterial agents which have been also testified by Kujda et al. [84]. It is shown that silver particles attach to the bacteria surface inducing disintegration, which enables their penetration inside the bacteria. In the future, the antibacterial properties of silver nanoparticles should be applied in industry by combining with other materials. For example, Meng et al. [85] made silver nanoparticles adhered to multilayered film-coated silk fibers with the aim to get antibacterial application. The as-prepared silk could effectively kill the existing bacteria and inhibit the bacterial growth, demonstrating the antimicrobial activity. Moreover, the release of Ag + for the modified silk can last for 120 h, rendering the modified silk sustainable antimicrobial activity. This work may provide a novel method to prepare AgNPs-functionalized antimicrobial silk for potential applications in textile industry. Figure 13 shows the surface morphologies of pristine silk fiber and coated morphologies of silk. By the EDS analysis, we can make sure that nanosilver was coated with silk.

Surface morphologies of pristine silk fiber (a ), (PAA/PDDA)8 film-coated silk fiber (b ), and AgNPs-(PAA/PDDA)8 film-coated silk fiber (c ). Inset:SEM image with higher magnification. (d ) EDS spectrum of AgNPs-(PAA/PDDA)8 film-coated silk. The arrow indicates the point randomly selected for the EDS analysis [85]
Other people like Zulfiqar Ali Raza et al. [86] investigated single-bath fabrication and impregnation of silver nanoparticles on enzymatic pretreated cotton fabric by using starch both as reducing as well as stabilizing agent under the autoclave conditions of 103.42 kPa, 121 °C for 15 min. The silver nanoparticles impregnated cotton fabrics showed good durable antibacterial activity against Escherichia coli and Staphylococcus aureus souches. Figure 14 shows the formation mechanism of impregnation of silver nanoparticles on cotton fabric.
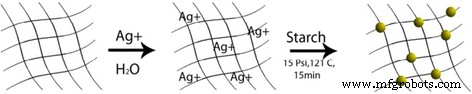
Schematic diagram of impregnation of silver nanoparticles on cotton fabric [86]
Recently, silver nanoparticles were coated with zirconia by Yamada et al. [87] for antibacterial prosthesis. In view of the pronounced antimicrobial properties and small toxicity of AgNPs, the biocompatible AgNPs-coated yttria-stabilized zirconia can be potentially utilized to control dental caries and periodontal disease. Maybe the inspiration about wound repair will be obtained by this study. The excellent antibacterial properties of silver nanoparticles can be revealed by the above studies. Moreover, this work will help someone who wants to do further research on antibacterial.
Properties and Applications of AgNPs on Fluorescence
Because nanomaterials with fluorescent property have a great application prospect. Many efforts have been devoted to study the fluorescent property [88, 89]. Research on fluorescent nanoparticles mainly concentrates on semiconductor particles, which are usually referred to as quantum dots. Among these, CdSe particles and ZnS particles have stronger fluorescent intensity. In spite of their broaden applications, quantum dots frequently still have some problems which are related to the intrinsic blinking of their luminescence and to toxicity issues that limit their applications in the health sciences [90]. Silver is expected to have lower toxicity and can be readily prepared reproducibly and with excellent solution stability. At the same time, Ag is readily detectable in the visible spectral region [91]. Because silver has the abovementioned advantages, the preparation of highly fluorescent silver nanoparticles is needed. Highly fluorescent silver nanoparticles were prepared by Maretti et al. [92] with a facile photochemical method, which can yield these materials with excellent long-term stability in just a few minutes. The method is used photogenerated ketyl radicals which can reduce Ag + from silver trifluoroacetate in the presence of amines. The conclusion they obtained is that the luminescence arises from particle-supported small metal clusters (predominantly Ag2 ). Typically, silver nanoparticles show a distinct plasma band which has been between 390 and 420 nm in their past work. Due to the presence of small silver clusters, the study of the absorption band obtained was closer to 450 nm. Figure 15 shows the UV-vis absorption spectra of silver nanoparticles. Figure 16 shows the absorption (red), emission (green), and excitation (blue) spectra of Ag particles after 4 min of irradiation in tetrahydrofuran (THF) under the conditions of Fig. 15 and resuspension in toluene. From Fig. 16, we can draw the conclusion that the silver nanoparticles can emit green light. This property can be used for fluorescence diagnosis in biomedical field [93].
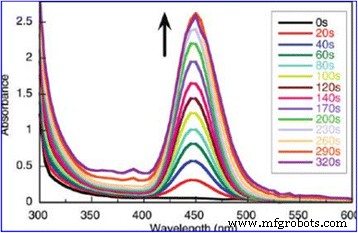
UV-vis absorption spectra following irradiation (350 nm, four lamps) of a toluene solution containing 2 mM silver trifluoroacetate, 2 mM I-2959, 2 mM cyclohexylamine. Reaction performed and monitored directly in a 0.7 × 0.3 cm quartz cuvette [92]
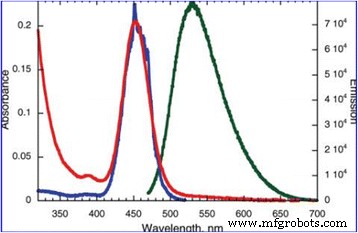
Absorption (red), emission (green), and excitation (blue) spectra of Ag particles after 4 min of irradiation in THF under the conditions of Fig. 15 and resuspension in toluene [92]
In order to distinguish these ultra-small particles, these nanoparticles which are smaller than 2 nm are usually called nanoclusters. In this size regime, metal nanoclusters become molecular species and size-dependent strong fluorescent emission can often be observed upon photoexcitation in the UV-visible range [94]. In particular, Ag nanoclusters, which show higher fluorescent intensity than Au nanoclusters in solutions, received considerable attention in the past few years owing to their great promise in a wide range of applications [95]. Fluorescent Ag nanoclusters were found to have wide applications in bio-imaging [96], chemical sensing [97, 98], fluorescence labeling [99], and single-molecule microscopy [100].
Properties and Applications of AgNPs on Catalysis
Since the addition of silver nanoparticles into reaction, the catalytic performance of the reaction has been significantly improved. Thus, nanocatalysis of silver nanoparticles has been a rapid growing research area which involves the use of nanoparticles as catalysts. As we all know, metals such as Ag, Au, Pt, and other metal ions can catalyze the decomposition of H2 O2 to oxygen [101]. Guo et al. found that when the AgNP colloid was added into the solution of luminol-H2 O2 , the chemiluminescence (CL) emission from the luminol–H2 O2 system could be greatly enhanced. AgNPs exhibited a better catalytic performance of CL than gold and platinum nanoparticles. The AgNPs-enhanced CL was ascribed to that AgNPs could catalyze the decomposition of H2 O2 to produce some reactive intermediates such as hydroxyl radical and superoxide anion. Figure 17 shows the effect of Ag colloid, Au colloid, Pt colloid, and filtrated solution of precipitated Ag colloid on luminol–H2 O2 CL [102].
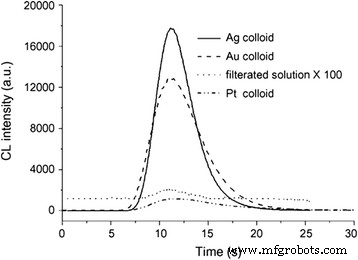
Effect of Ag colloid (solid line), 38 nm Au colloid (dashed line), Pt colloid (dash-dot-dot line), and filtrated solution of precipitated Ag colloid (dotted line) on luminol–H2 O2 CL. The blank (filtrated solution of precipitated Ag colloid) signal was amplified by 100 times. Conditions:luminol, 1 × 10–4 mol/L; H2 O2 , 0.15 mol/L; pH 9.32 carbonate buffer for Ag, pH 12.0 NaOH for Au, pH 10.3 carbonate buffer for Pt [102]
Silver is the most popular catalyst when it has interaction with oxygen, water, carbon dioxide, ethylene, and methanol [103]. From the study that the catalytic properties of silver nanoparticles have accordingly changed can be realized. Jiang et al. [104] enhanced the catalytic properties of Ag by combining silver nanoparticles with silica spheres, and they also applied it to the detection of dye reduction. The technique to support silver particles on silica spheres effectively avoids flocculation of nano-sized colloidal metal particles during a catalytic process in the solution, which allows one to carry out the successful catalytic reduction of dyes. Figure 18 shows how the absorbance spectrum of the dyes decreases when the dyes are reduced.
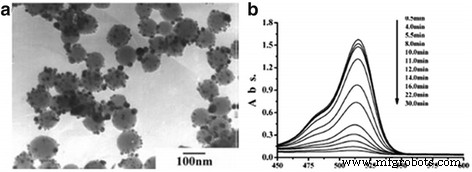
un Silver nanoparticles immobilized on silica spheres are illustrated. b The absorbance spectrum of the dyes decreases as the dyes are reduced by sodium borohydride. This process is catalyzed by silver nanoparticles. The arrow marks the increase of reaction time [104]
In addition, the catalytic properties of silver also have important applications in other areas, for example, wet-spun fibers [105].
Properties and Applications of AgNPs on Surface Plasmon Resonance
In 1902, Wood found the SPR phenomenon for the first time in an optical experiment and made a brief record about that, but until in 1941, a scientist named Fano explained the phenomenon of SPR. Over the next 30 years, the theory about SPR has not been further explored nor has it been put into practical application. In 1971, Kretschmann put forward prism coupling structure that settled the foundation for the structure of SPR sensor, and SPR theory started to be widely achieved for experiments. On this basis, the surface plasma resonance effect of silver nanoparticles was explored deeply. The most successful part of the applications of plasmonic structures was in the detection of molecules. This technique has been commercialized for propagating surface plasmons (PSPs) on continuous metal films. The films are chemically functionalized to selective bind target molecules like DNA strands or proteins. Upon binding the target molecule, the dielectric environment is altered around the surface of the metal film. Consequently, binding can be monitored by measuring the change in coupling geometry (i.e., the angle) between the metal film and the excitation source needed to generate PSPs [106, 107]. This technique plays a key role, and a number of commercially available instruments are widely used today in the biological sciences [108].
Recently, the combination of silver nanoparticles with other materials to improve their surface plasmon resonance performance is another way of development. The nanosilver particles were bonded with starch by Vasileva et al. [109], and the materials were applied as a surface plasmon resonance-based sensor of hydrogen peroxide. Figure 19 shows the change of hydrogen peroxide decomposition.
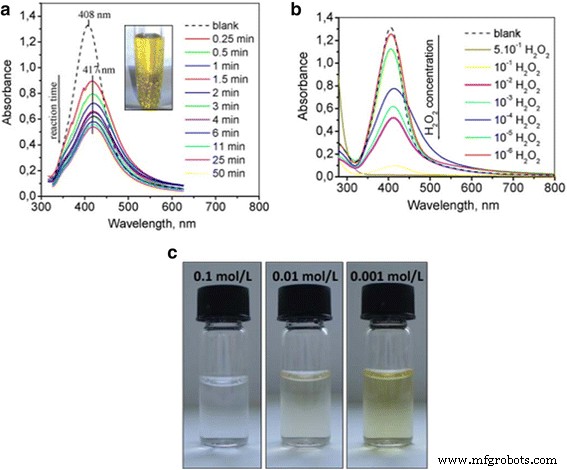
un Change of the LSPR absorbance strength with time due to the introduction of 10–3 mol/L H2 O2 solution in the as-synthesized Ag-NPs solution at a volume ratio 1:1.5; the inset shows the bubbles from H2 O2 decomposition generated by the catalytic reaction between hydrogen peroxide and starch-stabilized Ag-NPs. b UV-vis absorption spectra recorded 15 min after the introduction of hydrogen peroxide solution with different concentrations in the solution of Ag-NPs at a volume ratio 1:1.5. c relevant photographs of Ag-NPs dispersions 60 min after the introduction of hydrogen peroxide with different concentrations [109]
SPR has a wide range of applications in other fields such as life science, medical testing, drug screening, food testing, environmental monitoring, and forensic identification.
The SPR technology becomes an indispensable part in the field of biological chemistry, food, and drug monitoring. The applications of SPR biosensors will be more diversified. And especially its emerging application in small molecule detection and lipid field will make it play an increasingly important role in the film and biology. In recent years, its development is particularly rapid. With the continuous improvement of SPR instruments and the continuous enhancement of biological membrane construction capability, SPR biosensor has a bright future.
Applications of AgNPs on Nanosensors
Due to the great research prospect of silver nanoparticles in nanosensors, many researchers have devoted to study it [110, 111]. So, we pick three representative examples to write in detail. Among them Zhu et al. [110] fabricated rhombic silver nanoparticles for biosensing. The rhombic silver nanoparticles were prepared by follow method. The mixed solution (polystyrene nanospheres and glass nanospheres with fluorocarbon surfactant) was coated onto the glass substrate to form a deposition mask, and then followed by hydrofluoric acid etching to remove the glass nanospheres. After that, the Ag metal thin film was deposited through the nanosphere masks using thermal evaporation or electron beam evaporation. After removal of the polystyrene nanospheres by sonication in absolute ethanol for 3 min, well-ordered rhombic AgNPs array was finally obtained on the substrates. The rhombic AgNPs array was single particle dimension of 140 nm in-plane width and 47 nm out-of-plane height. To prepare the biosensing, the Ag nanorhombuses are firstly functionalized using the self-assembly monolayer technique. Then assisting with 1-ethyl-3-[3-dimethylaminopropyl] carbodiimide hydrochloride, we covalently attached biotin to the carboxylate groups. The advantage of this biosensor is that the rhombic AgNPs array-based sensor with more hot spots has higher sensitivity than that of the traditional Ag triangular nanoparticles-based sensor. A detection of high sensitivity of the bio-molecule in lower concentration has been realized by means of the LSPR-based nanobiosensor. This type of biosensor will have potential applications in many fields such as medical science and biological technology. Meanwhile, M. Ghiaci et al. [111] utilized silver nanoparticles compounds as new electrochemical sensors for glucose detection. These electrochemical sensors were prepared based on synthesizing of two amine compounds bounded to silica support. The size of used AgNPs is 10 nm. The electrochemical sensor prepared by this method has a lower limit of glucose detection than other electrochemical sensors. This type of nanosensors will be more conducive to diabetes detection and treatment. Silver nanoscale sensors can also be used for environmental detection such as Li et al. [112] synthesized aza-crown ether (ACE)-modified silver nanoparticles as colorimetric sensors for Ba 2+ . What is more, colorimetric sensors merely need minimal instrumentation, achieve high sensitivity, and thus can make on-site detection even easier. The colorimetric sensors were synthesized by silver nanoparticles efficiently conjugated with CS2 –ACE. ACE-modified AgNPs have good recognition of Ba 2+ , with the detection limit of 10 − 8 mol/L.
In addition to the abovementioned, silver nanosensors also have other different applications that are worth us to explore.
Other Applications
Ag nanomaterials also have many other applications in various fields, such as nanoscale detection [113] and solar cells.
Silver nanoparticle and its complex can be used for solar cells to enhance photoelectric conversion efficiency and photovoltaic performances [114,115,116].
Shen et al. [114] enhanced photovoltaic performances of polymer solar cells by incorporating Ag–SiO2 core–shell nanoparticles in the active layer. They creatively incorporated Ag–SiO2 core–shell nanoparticles (Ag–SiO2 -NPs) into photo−/electro-active layers consisting of poly(3-hexylthiophene) (P3HT) and phenyl-C61 -butyric acid methyl ester (PCBM) in polymer solar cells (PSCs). By this way, the photovoltaic performance of PSCs have largely been enhanced. The results demonstrate a 13.50% enhancement of short-circuit photocurrent density and a 15.11% enhancement of power conversion efficiency as the weight percent of doped Ag–SiO2 -NPs is 1.5 wt% in the active layer of corresponding PSCs. In the later research, bare silver nanoplate (Ag-nPl) were spin-coated on indium tin oxide and silica capsulated Ag-NPs were incorporated to a PBDTTT-C-T:PC71BM active layer by Shen et al. [115]. As a result, the devices incorporated with Ag-nPl and Ag@SiO2 -NPs showed great enhancements. With the dual effects of Ag-nPl and Ag@SiO2 -NPs in devices, all wavelength sensitization in the visible range was realized; therefore, the power conversion efficiency of PSCs showed a great enhancement of 14.0 to 8.46%, with an increased short-circuit current density of 17.23 mA cm − 2 . Importantly, the methodology of multiple shape combination of metallic nanoadditives improves the photovoltaic performance of PSCs very effectively compared to the single-shape method.
Thus, Ag is a promising material for the conversion of solar energy into electricity and good detection. In addition to the abovementioned, Ag also has many other applications, but it still needs people to further explore it.
Conclusions
This work reviewed the development progress of Ag nanomaterials on synthesis methods and applications. Different shapes of Ag nanostructures had been synthesized such as cubic, rod-shaped, and sphere-shaped, Ag nanostructure obtained by chemical synthesis and microwave methods were successfully prepared. In addition, different size of AgNPs have been synthesized such as 1–10 nm, 10–100 nm, AgNPs obtained by chemical synthesis, laser ablation, and green synthesis. Meanwhile, it has been successfully applied to many fields, such as antibacterial, fluorescence, catalysis, SPR, and nanosensors, and it is expected to use in other fields. In fact, there are still limitations for their practical applications in photoelectric and medical fields because it often requires complex preparation process, and the yield is very low. In most cases, AgNPs are easy to agglomerate, which will greatly reduce its optical properties. Therefore, it is necessary to utilize surface active agent to achieve a good effect. Although, there are so many challenges, the advances in nanoscience and nanotechnology of silver still promise a better future for many kinds of industries. In conclusion, the future research of silver nanoparticles should be directed towards biosynthetic, size controllable, and uniform shape preparation. And the future application of AgNPs-based will be utilized in new energy battery or wearable intelligent equipment by its excellent localized surface plasmon resonance effect and antibacterial activity. In addition, AgNPs-based materials can be further utilized for applications in nanodevices by self-assembly and molecular molding technology.
Abréviations
- ACE:
-
Aza-crown ether
- Ag-nPl:
-
Silver nanoplate
- AgNPs:
-
Ag nanoparticles
- CL:
-
Chemiluminescence
- CTAB :
-
Cetyltrimethyl ammonium bromide
- DBSA:
-
Dodecyl benzene sulfonic acid
- DLS :
-
Diffusion dynamique de la lumière
- EDS :
-
Energy dispersive spectroscopy
- fcc:
-
Face-centered cubic
- HRTEM :
-
Microscopie électronique à transmission haute résolution
- LSPR :
-
Résonance plasmonique de surface localisée
- MTCC:
-
The name of bacteria
- MTPs:
-
Multiply twinned particles
- P3HT :
-
Poly(3-hexylthiophène)
- PAA:
-
Poly(acrylic) acid
- PBDTTT-C-T:
-
Poly[4,8-bis((2-ethylhexyl)thiophen-5-yl)-benzo[1,2-b:4,5-b’]dithiophene-2,6-diyl]-alt-[2-(20-ethylhexanoyl)-thieno[3,4-b]thiophene-4,6-diyl]}
- PC71BM:
-
Fullerene derivatives acceptor material C71-butyric acid methyl ester
- PCBM :
-
Phenyl-C61 -butyric acid methyl ester
- PDDA:
-
Poly(dimethyldiallylammonium chloride)
- PEG:
-
Polyethylene glycol
- PLLA:
-
Poly(L-lactide)
- PSCs:
-
Polymer solar cells
- PSPs:
-
Propagating surface plasmons
- PVA :
-
Poly-vinyl alcohol
- PVP:
-
Poly-vinyl pyrrolidone
- SDA:
-
Sabro dextrose agar
- SDS:
-
Sodium dodecyl sulfate
- SEM :
-
Microscope électronique à balayage
- SERS :
-
Diffusion Raman améliorée en surface
- SPR :
-
Résonance plasmonique de surface
- TEM :
-
Microscope électronique à transmission
- THF:
-
Tetrahydrofuran
- UV-vis:
-
Ultraviolet-visible
- XRD :
-
Diffraction des rayons X
Nanomatériaux
- Applications du molybdène et des alliages de molybdène
- Nanoparticules d'or multifonctionnelles pour des applications diagnostiques et thérapeutiques améliorées :une revue
- Avancées et défis des nanomatériaux fluorescents pour la synthèse et les applications biomédicales
- La préparation de la nanostructure jaune-enveloppe Au@TiO2 et ses applications pour la dégradation et la détection du bleu de méthylène
- Fabrication, caractérisation et cytotoxicité de nanoparticules de carbonate de calcium dérivées de coquilles d'or conjuguées de forme sphérique pour des applications biomédicales
- Saponines de Platycodon de Platycodi Radix (Platycodon grandiflorum) pour la synthèse verte de nanoparticules d'or et d'argent
- Surrefroidissement de l'eau contrôlé par nanoparticules et ultrasons
- Dernières avancées et applications de la technologie IoT
- Techniques de programmation CNC :guide de l'initié sur les méthodes et applications efficaces



