Caractérisations structurelles et propriétés diélectriques de poudres de PbTiO3 de type sphère et tige synthétisées par synthèse de sel fondu
Résumé
Par réaction de PbC2 O4 et TiO2 dans les sels eutectiques NaCl-KCl, PbTiO3 en forme de sphère et de tige Les poudres (PTO) ont été synthétisées via des méthodes de synthèse de sel fondu (MSS) et de matrice MSS, respectivement. Les diagrammes de diffraction des rayons X révèlent que toutes les poudres PTO cristallisent dans une structure de phase tétragonale. Augmenter le rapport molaire de PbC2 O4 :TiO2 :NaCl:KCl de 1:1:10:10 à 1:1:60:60 dans le procédé MSS a peu d'effet sur la morphologie sphérique des poudres PTO synthétisées à 950 °C pendant 5 h. Des poudres de PTO polycristallines à grande échelle en forme de tige avec des diamètres de 480 nm à 1,50 μm et des longueurs allant jusqu'à 10 μm ont été synthétisées à 800 °C pendant 5 h par la méthode MSS modèle, où l'anatase en forme de tige TiO2 précurseurs ont été utilisés comme modèles et le rapport molaire de PbC2 O4 :TiO2 :NaCl:KCl était égal à 1:1:60:60. Les spectres de spectroscopie à dispersion d'énergie des rayons X révèlent que toutes les poudres PTO sont composées d'éléments Pb, Ti et O, et que les rapports atomiques Pb:Ti mesurés sont proches de 1:1. Dans le processus MSS modèle, la teneur en sel fondu joue un rôle important dans la formation des poudres PTO en forme de tige. Sous une faible teneur en sel fondu, les poudres de PTO en forme de tige ne peuvent pas être synthétisées même si le TiO2 en forme de tige des modèles sont utilisés. De plus, l'allongement du temps de réaction a supprimé la formation de poudres de PTO en forme de tige, mais a favorisé la formation de nanoparticules de PTO en forme de sphère. Les propriétés diélectriques des poudres PTO en forme de sphère et de tige ont été étudiées comparativement. A température ambiante, la constante diélectrique et la perte diélectrique des poudres sphériques PTO synthétisées par la méthode MSS avec le rapport molaire de PbC2 O4 :TiO2 :NaCl:KCl égal à 1:1:30:30 étaient ~ 340 et 0,06 (mesuré à 10 6 Hz), respectivement. Les valeurs correspondantes pour les poudres PTO en forme de tige synthétisées par la méthode MSS modèle avec le rapport molaire de PbC2 O4 :TiO2 :NaCl:KCl égal à 1:1:60:60 étaient respectivement de 140 et 0,08. Les présents résultats démontrent que les poudres PTO en forme de sphère ont de meilleures propriétés diélectriques, qui ont des applications prometteuses dans les domaines des condensateurs multicouches et des résonateurs.
Introduction
Oxydes pérovskites de formule générale ABO3 sont l'une des classes de matériaux les plus importantes en chimie du solide, qui ont été largement utilisées dans les domaines de la ferroélectricité, du magnétisme, de l'optoélectronique et de la conversion d'énergie [1,2,3]. Parmi tous les membres de la famille des oxydes pérovskites, PbTiO3 (PTO) a la distorsion tétragonale la plus élevée (c /un ~ 1.064), ce qui le rend remarquable par rapport aux autres. Cette grande distorsion tétragonale correspond à la polarisation spontanée la plus élevée parmi tous les oxydes de pérovskite ferroélectrique. En tant que paradigme des oxydes ferroélectriques pérovskites, le PTO possède d'excellentes propriétés diélectriques, piézoélectriques et pyroélectriques [4, 5]. Cependant, les céramiques PTO pures sont difficiles à préparer en tant que céramiques haute densité et monolithiques en raison de problèmes tels que le décalage de dilatation thermique, la force d'étirement mécanique et les microfissures dans les céramiques PTO. Au cours de la dernière décennie, de nombreux travaux ont été consacrés à la synthèse de poudres PTO par diverses voies, telles que la réaction à l'état solide [6], le procédé sol-gel [7, 8], la méthode hydrothermale [9, 10], la méthode de Pechini [11], la co-précipitation [12], etc. Cependant, dans toutes ces méthodes, une calcination à plus ou moins haute température est nécessaire pour obtenir une PTO ferroélectrique cristallisée pure. Malheureusement, la calcination à haute température produit généralement des poudres agglomérées avec une grosseur de particules qui nécessite un processus de broyage supplémentaire. La contamination et d'autres caractéristiques indésirables pendant le processus de broyage peuvent créer des défauts dans les produits fabriqués, endommageant les propriétés électriques de la céramique PTO.
La méthode de synthèse de sel fondu (MSS) est un moyen efficace de préparer des poudres céramiques électroniques d'oxyde de pérovskite, qui implique le sel fondu utilisé comme milieu pour synthétiser des oxydes de pérovskite purs à partir de leurs matériaux constitutifs (oxydes et carbonates) à une température relativement basse et dans un délai plus court. temps de réaction par rapport aux réactions conventionnelles à l'état solide [13]. Récemment, des poudres de pérovskite PTO sont synthétisées par réaction de flux fondu en utilisant NaCl et NaCl-KCl comme milieu de réaction [14,15,16]. La formation de poudres de PTO sphériques a été obtenue par la diffusion de PbO dissous sur le TiO2 surface dans les sels fondus et réagir in-situ pour former des nanoparticules PTO, puis suite à la nucléation et la croissance des nanoparticules PTO. Par rapport aux poudres PTO, la synthèse de nanomatériaux PTO 1D (par exemple, nanotiges, nanofils et nanotubes) par la méthode MSS est restée loin derrière. La principale raison est due aux défis de la synthèse de nanomatériaux PTO 1D de haute qualité, car la symétrie élevée de la structure de la pérovskite peut facilement conduire à la croissance de la PTO en un bloc cubique. A ce jour, seuls quelques travaux sur la synthèse de nanomatériaux PTO 1D par la méthode MSS sont disponibles dans la littérature. Deng et al. [17] ont synthétisé des nanotiges PTO avec des diamètres de 50-80 nm et des longueurs de quelques micromètres à 700 °C en utilisant une approche assistée par un tensioactif (polyoxyéthylène (9) nonylphényl éther, NP-9) dans un milieu de sel fondu NaCl. La croissance des nanotiges PTO a été attribuée à la dispersion de fines nanoparticules PTO et à leur redéposition sur des particules plus grosses, conduisant à la formation de nanotiges le long de la direction axiale sous les effets combinés du tensioactif NP-9 et du flux de NaCl. Cai et al. [15] ont rapporté la synthèse de nanotiges PTO monocristallines avec des diamètres de 0,1 à 1,0 m et des longueurs allant jusqu'à quelques micromètres par la méthode MSS modèle, où le NP-9 a été utilisé comme tensioactif et le TiO en forme de tige2 précurseurs ont été utilisés comme modèles pour les sources de titane. La taille et la morphologie du TiO2 en forme de bâtonnet modèles ont été conservés dans les particules PTO synthétisées. De même, des poudres de PTO en forme d'aiguille ont également été synthétisées via la méthode MSS modèle, où TiO pur en forme d'aiguille2 les particules ont été utilisées comme modèles [18]. Les particules PTO en forme d'aiguille synthétisées par la méthode MSS modèle à 800 °C avaient une longueur de 30 à 100 μm et des diamètres de 500 nm à 2,0 μm.
Malgré les rapports ci-dessus sur la synthèse de nanomatériaux PTO par la méthode MSS et la méthode MSS modèle, il existe peu de données sur les propriétés diélectriques des poudres PTO. De plus, le mécanisme de formation des nanotiges PTO par la méthode MSS modèle n'est pas bien compris. Dans ce travail, nous rapportons la synthèse de poudres de PTO en forme de sphère et de tige via des méthodes MSS (modèles) par réaction de PbC2 O4 et TiO2 dans les sels eutectiques NaCl-KCl sans utiliser le tensioactif NP-9. L'influence des paramètres de traitement de la méthode MSS modèle tels que le temps de réaction et la teneur en sel fondu sur la formation de poudres PTO en forme de tige a été étudiée en détail. Les résultats démontrent que la teneur en sel fondu joue un rôle critique dans la formation de l'ABO en forme de tige3 composés à structure cristalline cubique ou pseudo-cubique dans le procédé MSS modèle. À faible teneur en sel fondu, les nanotiges PTO ne peuvent pas être synthétisées même si le TiO2 en forme de tige les modèles sont utilisés dans le processus de modèle MSS. Les propriétés diélectriques des poudres PTO en forme de sphère et de tige synthétisées par la méthode MSS et la méthode MSS modèle ont également été étudiées de manière comparative, et les résultats ont démontré que les poudres PTO en forme de sphère présentaient de meilleures propriétés diélectriques.
Méthodes
Matériaux
Réactifs de qualité analytique de PbC2 O4 et TiO2 (avec une morphologie sphérique et une structure en phase mixte d'anatase et de rutile) ont été achetés auprès de Sigma-Aldrich (Shanghai) Trading Co., Ltd. Réactifs de qualité analytique des sels NaCl et KCl, K2 CO3 , AgNO3, et les solutions de HCl ont été obtenues auprès de Shanghai Chemical Reagent Co., Ltd.
Synthèse de poudres PTO de type sphère par la méthode MSS
Des poudres de PTO de type sphère ont été synthétisées via la méthode MSS par réaction de PbC2 O4 et TiO2 dans les sels eutectiques NaCl-KCl. Les rapports molaires de PbC2 O4 :TiO2 :NaCl:KCl ont été sélectionnés comme 1:1:10:10, 1:1:20:20, 1:1:30:30, 1:1:40:40 et 1:1:60:60. Les mélanges de PbC2 O4 , TiO2 , NaCl et KCl ont été broyés dans un mortier et un pilon pendant 30 min puis chauffés dans les creusets en alumine à 950°C pendant 5 h. Enfin, les produits ont été refroidis naturellement dans le four à température ambiante, et ils ont été lavés plusieurs fois avec de l'eau déminéralisée jusqu'à ce qu'aucun ion chlorure libre ne soit détecté par AgNO3 solution pour assurer l'élimination complète des sels. Après lavage, les produits ont été séchés à 120°C pendant 4 h pour des caractérisations structurales.
Synthèse de poudres PTO de type tige par la méthode MSS de modèle
Des poudres de PTO en forme de tige ont été synthétisées via la méthode MSS de modèle, où l'anatase en forme de tige TiO2 des particules ont été utilisées comme source de titane. Le TiO2 en forme de tige les modèles ont été préparés à partir du K2 en forme de tige Ti4 O9 , suivant une procédure rapportée précédemment par Hayashi et al. [19]. Tout d'abord, K2 CO3 l'oxyde a été mélangé avec TiO2 oxyde avec un rapport molaire de 1:3, puis le mélange a été chauffé à 1000°C et maintenu pendant 18h. Enfin, le produit a été refroidi naturellement dans le four à température ambiante et lavé plusieurs fois avec de l'eau déminéralisée pour éliminer le K2 résiduel. CO3 . Le produit principal obtenu de K2 Ti4 O9 a été lavé dans une solution HCl 70 °C (concentration de 1 M) pendant 2 h pour extraire K2 O, et la phase résultante était TiO2 ·nH2 O, qui a été recuit pendant 1 h à 600 °C, 700 °C et 800 °C, respectivement, pour obtenir le TiO2 en forme de tige composés. Et puis, PbC2 O4 a été mélangé avec du TiO2 en forme de tige modèles et sel fondu NaCl-KCl avec des rapports molaires de PbC2 O4 :TiO2 (modèles):NaCl:KCl égal à 1:1:20:20 et 1:1:60:60, respectivement. Les deux mélanges ont été recuits à 800°C pendant différentes heures (par exemple, 1 h, 5 h et 10 h). Les produits finaux ont été lavés et séchés selon les mêmes étapes ci-dessus.
Caractérisation microstructurale
Les structures de phase des poudres PTO telles que préparées ont été caractérisées par diffraction des rayons X sur poudre (Rigaku D/Max-RA, rayonnement Cu Kα). Une taille de pas était de 0,01° par seconde et la plage de 2θ était de 15 à 70°. Les morphologies de surface des produits PTO ont été examinées par microscopie électronique à balayage (SEM, Hitachi S-3400 N II, 30 kV) équipée d'une spectroscopie à dispersion d'énergie (EDS) à rayons X (spectroscopie EX-250, HORIBA Corporation) pour l'élément détection. Les échantillons SEM ont été préparés en saupoudrant de poudre sur du ruban de carbone et ensuite recouverts d'or si nécessaire.
Mesures diélectriques
Pour les mesures des propriétés diélectriques, les poudres séchées de PTO en forme de sphère et de tige ont été pressées en pastilles de 12 mm de diamètre et 1,0 mm d'épaisseur sous une pression de 7 MPa, qui ont été recuites à 1150 °C pendant 2 h dans l'air. Par la suite, les surfaces des pastilles recuites ont été meulées et polies, suivies d'une peinture à la pâte d'argent sur les deux surfaces. Les pâtes d'argent ont ensuite été cuites à 550 °C pendant 60 min. Les constantes diélectriques et les pertes diélectriques des poudres PTO recuites ont été mesurées à température ambiante de 10 Hz à 1 MHz en utilisant un analyseur d'impédance Agilent 4192 A.
Résultats et discussion
Structure de phase et morphologie des poudres PTO synthétisées par la méthode MSS
Les diagrammes XRD des poudres PTO synthétisées par la méthode MSS à 950°C pendant 5 h sous différentes teneurs en sels fondus sont montrés sur la Fig. 1. On observe que tous les pics de diffraction XRD peuvent être parfaitement indexés sur le PTO tétragonal (JCPDS No. 06-0452, P 4mm groupe d'espace, constante de réseau a = 0.390 nm et c = 0.415 nm), et aucune autre phase d'impureté n'est détectée. Normalement, le motif XRD dans la région 2θ = 45° est caractéristique de la présence d'une structure pérovskite cubique ou tétragonale. Dans ce cas, la division des réflexions cubiques (200) en réflexions tétragonales (200) et (002) à environ 2θ = 45 ° est clairement observée, indiquant la formation d'une phase ferroélectrique tétragonale pure. Les paramètres de maille (a et c ) des poudres PTO tétragonales peut être calculé par l'équation suivante :
$$ \frac{1}{d^2}=\frac{h^2+{k}^2}{a^2}+\frac{l^2}{c^2} $$ (1)où d est l'espacement interplanaire entre les voisins (hkl ) avions, et a et c sont les paramètres de réseau dans la structure de phase tétragonale. Les paramètres de maille a des poudres PTO calculées à partir des modèles XRD étaient dans la plage de 0,3905 à 0,3911 nm, et c dans la plage de 0,4077 à 0,4089 nm. Les détails sont présentés dans le tableau 1. Le c /un Le rapport était compris entre 1,043 et 1,047 avec une valeur moyenne de 1,045, inférieure à 1,064 pour le monocristal PTO. D'après les diagrammes XRD illustrés sur la figure 1, on peut observer que la structure de phase des poudres PTO n'est pas influencée par la teneur en sel fondu. Toutes les poudres PTO ont cristallisé dans une structure de phase tétragonale avec un groupe spatial de P 4mm . Récemment, les études théoriques sur l'évolution structurelle de la pérovskite PTO d'un cluster 0D à un cristal 3D par la méthode de recherche de structure CALYPSO (Crystal structure AnaLYsis by Particle Swarm Optimization) en conjonction avec les calculs de la théorie fonctionnelle de la densité révèlent que la structure de l'état fondamental de la PTO à pression ambiante est le P 4mm phase et la structure quasi-planaire du cluster PTO et de la double couche PTO 2D sont également stables à pression ambiante [20]. Les examens SEM-EDS des poudres PTO sont illustrés à la Fig. 2. Les images SEM illustrées aux Fig. 2a–e révèlent que les poudres PTO sont principalement constituées de nombreuses nanoparticules sphériques, à l'exception de quelques particules en forme de tige. Avec l'augmentation du rapport molaire de PbC2 O4 :TiO2 :NaCl:KCl de 1:1:10:10 à 1:1:60:60, la morphologie des poudres PTO n'a apparemment pas changé, comme le montre la figure 2a–e. Cela signifie que différentes quantités des mêmes sels fondus n'agissent que comme milieu réactionnel, elles ont juste une influence sur la vitesse de diffusion des ions réactionnels. Les sels fondus eutectiques NaCl-KCl (point de fusion eutectique 650°C) fournissent un environnement de réaction en phase liquide à relativement basse température, ce qui facilite le transport des ions réactifs pendant le processus MSS. Il est rapporté que la solubilité des réactifs dans le sel fondu joue un rôle important dans le processus MSS, qui affecte de manière critique la vitesse de réaction et la morphologie des produits tels que synthétisés [13]. Dans le présent travail, PbO est décomposé de PbC2 O4 via la réaction chimique à des températures de 400–500 °C [14]
$$ {\mathrm{PbC}}_2{\mathrm{O}}_4\à \mathrm{PbO}+\mathrm{CO}\uparrow +{\mathrm{CO}}_2\uparrow $$ (2)qui a une solubilité plus élevée dans le sel fondu de NaCl-KCl (la solubilité dans les sels de NaCl-KCl est de 30 μmol/g de chlorures à 900 °C [21]) que TiO2 (qui a une très faible solubilité dans les chlorures alcalins [22]). Par conséquent, le réactif le plus soluble PbO dans le sel fondu peut diffuser à la surface du TiO2 en forme de sphère. précurseur et réagir avec lui in situ pour former des poudres de PTO en forme de sphère par le processus de précipitation en solution. Un spectre EDS typique illustré à la figure 2f démontre que l'échantillon est composé d'éléments Pb, Ti et O, et l'analyse EDS confirme que la composition chimique est presque similaire à celle nominale.
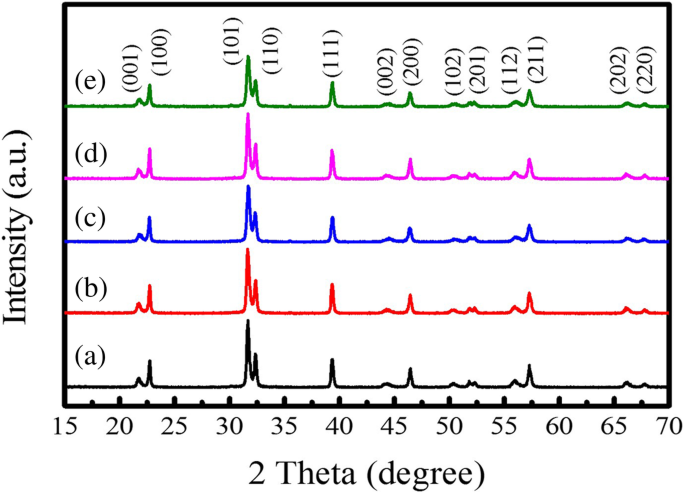
Schémas XRD des produits PTO en forme de sphère synthétisés par la méthode MSS à 950°C pendant 5 h avec les rapports molaires de PbC2 O4 :TiO2 :NaCl:KCl égal à (a) 1:1:10:10, (b) 1:1:20:20, (c) 1:1:30:30, (d) 1:1:40:40, et (e) 1:1:60:60, respectivement

Images SEM des produits PTO en forme de sphère synthétisés par la méthode MSS à 950°C pendant 5 h avec les rapports molaires de PbC2 O4 :TiO2 :NaCl:KCl égal à a 1:1:10:10, b 1:1:20:20, c 1:1:30:30, d 1:1:40:40, et e 1:1:60:60, respectivement. f Spectre EDS typique acquis à partir des produits PTO en forme de sphère synthétisés à 950°C pendant 5 h avec le rapport molaire de PbC2 O4 :TiO2 :NaCl:KCl égal à 1:1:10:10
Structure de phase et morphologie des poudres PTO en forme de tige synthétisées par la méthode MSS de modèle
Avant de synthétiser les poudres PTO en forme de tige par la méthode MSS modèle, la structure de phase et la morphologie du TiO2 les modèles ont d'abord été étudiés. La figure 3 illustre les modèles XRD du TiO2 gabarits recuits à différentes températures pendant 1 h. On observe que la phase anatase prédominante de TiO2 s'est formé dans les produits après recuit à 600°C (Fig. 3a) et 700°C (Fig. 3b). Cependant, une certaine quantité de K2 Ti4 O9 encore retenu dans les produits. Les pics de diffraction XRD indiqués par des étoiles proviennent du K2 Ti4 O9 phase (ICDD n° 32-0861). En augmentant la température de recuit jusqu'à 800°C (Fig. 3c), le K2 impur Ti4 O9 phase a presque disparu. Tous les pics de diffraction XRD montrés sur la figure 3c peuvent être bien indexés sur l'anatase TiO2 (JCPDS n° 021-1272), indiquant la formation de phase anatase pure TiO2 . Il a également été remarqué que la qualité cristalline du TiO2 Le modèle s'est beaucoup amélioré car l'intensité du pic de diffraction principal (101) a considérablement augmenté. La figure 4 montre les images SEM du TiO2 modèles recuits à différentes températures. Tous les TiO2 les modèles présentaient une morphologie en forme de tige et leurs diamètres moyens variaient de 490 nm à 570 nm, puis 500 nm lorsque les températures de recuit augmentaient tandis que leurs longueurs moyennes étaient maintenues à environ 12,0 m. Les proportions du TiO2 les matrices recuites à 600°C, 700°C et 800°C étaient respectivement d'environ 25, 23 et 24. La morphologie en bâtonnet du TiO2 recuit matrices est attribuée à la croissance anisotrope de la structure de la phase anatase dans le processus de recuit. Sur la base des résultats expérimentaux ci-dessus, on peut conclure que le TiO2 les modèles avec une phase anatase recuite à 800 °C pendant 1 h ont une cristallinité élevée et une morphologie en forme de tige, qui sont aptes à synthétiser les poudres de PTO en forme de tige via la méthode MSS de modèle.
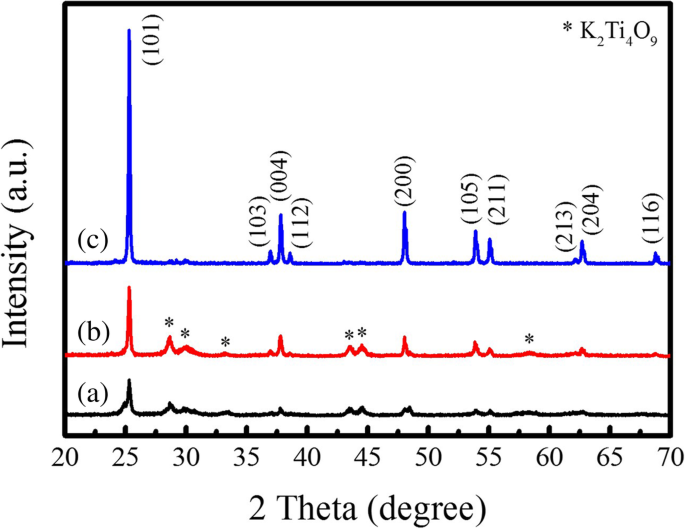
Modèles XRD du TiO2 gabarits recuits à (a) 600 °C, (b) 700 °C, et (c) 800 °C pendant 1 h

Images SEM du TiO2 modèles recuits à a , b 600 °C ; c , d 700°C ; et e , f 800 °C pendant 1 h
La figure 5 montre les modèles XRD des poudres PTO synthétisées par la méthode MSS modèle à 800 °C pour différents temps de réaction, où le TiO en forme de tige2 des matrices (phase anatase recuite à 800 °C pendant 1 h) ont été utilisées comme source de titane et le rapport molaire de PbC2 O4 :TiO2 (modèle):NaCl:KCl était égal à 1:1:20:20. Les diagrammes de diffraction XRD révèlent que toutes les poudres PTO cristallisent dans une structure de phase tétragonale (JCPDS n° 06-0452), et aucune autre phase d'impureté n'est détectée, illustrant la formation d'une structure de phase tétragonale pure. Les paramètres de réseau des poudres PTO ont été déduits des modèles XRD, les détails sont présentés dans le tableau 2. Les images SEM correspondantes des poudres PTO sont présentées sur la figure 6. Comme le montre la figure 6a, la morphologie des poudres PTO recuites à 800°C pendant 1 h est une combinaison de quelques particules en forme de tige et d'une grande quantité de particules PTO en forme de sphère. La fraction volumique qualitative des particules de PTO en forme de tige n'était que d'environ 3 %, et les particules de PTO en forme de tige avaient un diamètre moyen d'environ 860 nm et une longueur de 4,50 m. Cependant, avec l'augmentation du temps de réaction de 1 h à 5 h, la fraction volumique des particules de PTO en forme de tige a été réduite à ~ 2,4% (Fig. 6c), et les particules de PTO en forme de tige avaient un diamètre moyen d'environ 930 nm et longueur de 6,0 m. En augmentant encore le temps de réaction jusqu'à 10 h (Fig. 6e), les particules PTO en forme de tige ont été à peine observées dans les produits PTO, alors qu'une grande quantité de particules PTO en forme de sphère se sont formées (voir Fig. 6e-f). Cela signifie que l'allongement du temps de réaction favorise la formation de particules PTO sphériques tandis que la formation de particules PTO en forme de tige est supprimée. La taille moyenne des particules des particules sphériques PTO recuites à 800 °C pendant 10 h était d'environ 550 nm (Fig. 6e), légèrement plus grande que le diamètre du TiO2 en forme de tige. modèle (480 nm) (Fig. 4e). La formation d'une grande quantité de particules PTO sphériques dans les produits recuits à 800 °C pendant 10 h peut être attribuée au TiO2 en forme de tige les modèles sont brisés en petites particules sphériques pendant le processus de modèle MSS, qui réagissent avec le PbO dissous (décomposé à partir de PbC2 O4 ) dans le sel fondu NaCl-KCl, formant des poudres de PTO sphériques via un mécanisme de précipitation en solution. La trace brisée du TiO2 modèle a été observé sur les figures 6b et d, où certaines particules sphériques de prise de force ont été liées ensemble pour former la forme d'une ficelle de gourde à sucre. Il semble que les poudres de PTO en forme de tige ne soient pas synthétisées avec succès par la méthode MSS modèle sous une faible teneur en sel fondu.
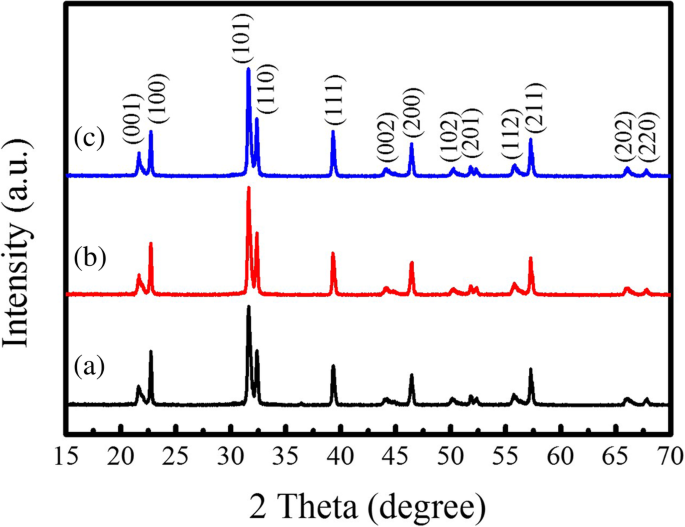
Modèles XRD des poudres PTO synthétisés via la méthode modèle MSS avec le rapport molaire de PbC2 O4 :TiO2 (modèle):NaCl:KCl égal à 1:1:20:20 et à 800 °C pour (a) 1 h, (b) 5 h, et (c) 10 h

Images SEM des produits PTO synthétisés via la méthode modèle MSS avec le rapport molaire de PbC2 O4 :TiO2 (gabarit):NaCl:KCl égal à 1:1:20:20 et recuit à 800 °C pour a , b 1 h ; c , d 5 h ; et e , f 10h
Il est connu que dans le procédé MSS, le grain croît à travers les flux de sel fondu à haute température, la teneur en sel fondu contrôle la vitesse de croissance du grain et la morphologie des produits finaux [23]. Avec l'augmentation de la teneur en sel fondu, de plus grandes quantités de sel fondu liquide se forment à haute température. Ainsi, les ions de réaction dissous (par exemple, les ions plomb) sont séparés efficacement dans le liquide de sel fondu, et leurs concentrations nécessitent un temps plus long pour atteindre la concentration de saturation. Par conséquent, le taux de nucléation des nanocristallites PTO à la surface de TiO2 insoluble les particules modèles doivent être réduites. Les nanocristallites de PTO formées ont suffisamment de temps pour se réunir en particules de PTO en forme de tige dans l'environnement à forte teneur en sels fondus. Cela signifie qu'un environnement à forte teneur en sels fondus est utile pour synthétiser les particules de PTO en forme de tige dans le processus MSS modèle. Par conséquent, nous avons augmenté le rapport molaire de PbC2 O4 :TiO2 (modèle):NaCl:KCl jusqu'à 1:1:60:60, et leurs mélanges ont été recuits à 800°C pendant différentes heures. La figure 7 montre les profils XRD des poudres PTO synthétisées à 800 °C par la méthode MSS modèle sous une teneur élevée en sels fondus. Il a été constaté que les poudres PTO recuites à 800°C pendant 5 h (Fig. 7b) et 10 h (Fig. 7c) avaient une phase tétragonale pure ; cependant, les poudres PTO recuites à 800 °C pendant 1 h (Fig. 7a) avaient une phase tétragonale prédominante à l'exception des petites phases impures de Ti3 O5 et TiO2 . Les constantes de réseau a et c des poudres PTO recuites à 800 °C pendant différentes heures ont été calculées et présentées dans le tableau 2. Le c /un rapport était d'environ 1,050. Les morphologies de surface des poudres PTO correspondantes sont illustrées sur la figure 8. On observe sur la figure 8a que les poudres PTO recuites à 800 °C pendant 1 h sont composées de particules en forme de tige et de sphère. La fraction volumique qualitative des particules en forme de tige estimée à partir de l'image SEM était d'environ 70 %. Les diamètres des particules en forme de tige variaient de 480 nm à 1,50 m tandis que leurs longueurs étaient comprises entre 3,0 et 7,0 m. L'image SEM agrandie locale montrée sur la figure 8b révèle que les poudres de PTO en forme de tige sont composées de très petits nanocristallites de PTO, indiquant la trace brisée du TiO2 en forme de tige. modèles pendant le processus de modèle MSS. Avec l'augmentation du temps de réaction de 1 h à 5 h, la fraction volumique des poudres de PTO en forme de tige dans le produit final a augmenté jusqu'à ~ ~ 97 % (Fig. 8c). La longueur des poudres de prise de force en forme de tige était de l'ordre de 7,0 à 10,0 m. Cependant, en augmentant encore le temps de réaction jusqu'à 10 h (Fig. 8e), la fraction volumique des particules de PTO en forme de tige dans le produit final était d'environ 85 % et la longueur des tiges de PTO était comprise entre 3,5 et 6,5 μm. Le diamètre des poudres de prise de force en forme de tige était compris entre 970 nm et 1,50 μm.
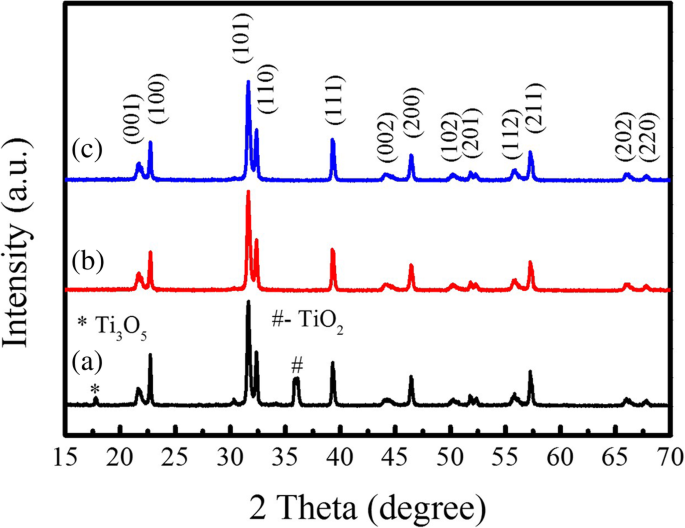
Modèles XRD des poudres PTO synthétisés via la méthode modèle MSS avec le rapport molaire de PbC2 O4 :TiO2 (gabarit):NaCl:KCl égal à 1:1:60:60 et recuit à 800 °C pendant (a) 1 h, (b) 5 h, et (c) 10 h

Images SEM des poudres PTO synthétisées via la méthode modèle MSS avec le rapport molaire de PbC2 O4 :TiO2 (modèle):NaCl:KCl égal à 1:1:60:60 et à 800 °C pour a , b 1 h ; c , d 5 h ; et e , f 10h
La formation de poudres de PTO en forme de tige sous une teneur élevée en sels fondus par la méthode MSS modèle peut être comprise par le processus suivant. Dans le processus MSS modèle, PbC2 O4 est d'abord décomposé en PbO, CO et CO2 dans la plage de température de 400 à 500 °C, et le PbO est dissous dans le sel fondu liquide à 800 °C (sa solubilité dans les sels NaCl-KCl est de 14 mol/g de chlorures à 800 °C [21]). Le PbO dissous diffuse à la surface du TiO2 en forme de tige modèle et réagit avec TiO2 in situ pour former des nanocristallites PTO via la réaction chimique à 800 °C
$$ \mathrm{PbO}+{\mathrm{TiO}}_2\à {\mathrm{PbTiO}}_3 $$ (3)Étant donné que la teneur en sel fondu est très élevée (le rapport molaire de PbC2 O4 :TiO2 (modèle):NaCl:KCl égal à 1:1:60:60), de sorte que les ions plomb dissous sont séparés efficacement dans le liquide de sel fondu, sa concentration nécessite plus de temps pour atteindre la concentration de saturation. Le TiO2 en forme de tige les modèles ont une très faible solubilité dans les sels de NaCl-KCl, qui sont décomposés en petits TiO2 particules sphériques à haute température dans un environnement à haute teneur en sels fondus. Par conséquent, le PbO dissous réagit avec le TiO2 brisé particules à leur surface pour former des nanocristallites PTO. Ces nanocristallites PTO ont suffisamment de temps pour se réunir dans les particules PTO en forme de tige dans un environnement à forte teneur en sels fondus. Comme le montre la figure 8c, des poudres PTO polycristallines à grande échelle en forme de tige avec des diamètres compris entre 480 nm et 1,50 μm et une longueur allant jusqu'à 10 μm ont été synthétisées. Ils sont composés de petits nanocristallites comme observé sur la figure 8d. Les diagrammes schématiques illustrant la formation de particules PTO dans le processus MSS et de poudres PTO en forme de tige dans le processus MSS modèle sont présentés à la Fig. 9. Notre travail actuel démontre que la teneur en sel fondu joue un rôle essentiel dans la formation de la forme en tige. ABO3 composés à structure cristalline cubique ou pseudo-cubique dans le procédé MSS modèle. Cela est dit sous une faible teneur en sel fondu, les poudres de PTO en forme de tige ne peuvent pas être synthétisées même si le TiO2 en forme de tige les modèles sont utilisés dans le processus de modèle MSS. La formation de poudres de PTO polycristallines en forme de tige sous la forme d'une ficelle de gourde à sucre plutôt que de tiges de PTO monocristallines doit encore être étudiée.
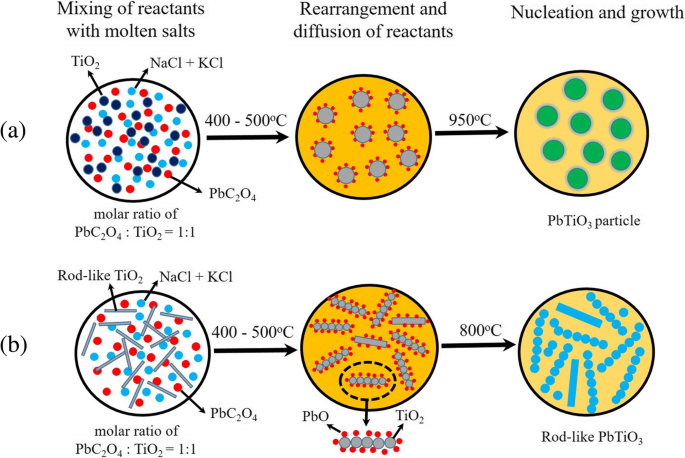
Diagrammes schématiques illustrant la formation (a) de particules PTO dans le processus MSS et (b) de poudres PTO en forme de tige dans le processus MSS modèle
Propriétés diélectriques des poudres PTO sphériques et en forme de tige
The dielectric constants (εr ) and dielectric losses (tanδ ) of the spherical and rod-like PTO powders synthesized by MSS and template MSS methods are shown in Fig. 10, which are measured at room temperature as a function of the frequency. Similar frequency-dependent dielectric behaviors are observed in the spherical and rod-like PTO powders. As shown in Fig. 10a, the sphere-like PTO powders (a) and (b) synthesized by MSS method at 950 °C for 5 h with the molar ratios of PbC2 O4 :TiO2 :NaCl:KCl equal to (a) 1:1:30:30 and (b) 1:1:60:60, respectively, have much higher dielectric constants than the rod-like PTO powders (c) and (d) synthesized by template MSS method at 800 °C for (c) 5 h and (d) 10 h with the molar ratio of PbC2 O4 :TiO2 (template):NaCl:KCl equal to 1:1:60:60. It is noticed that the dielectric constants of the sphere-like PTO powders (a) and (b) have decreased fast (from ~ 3000 to ~ 700) in the frequency range below 10 3 Hz, then reduced slowly with further increasing the frequency over 10 3 Hz, and finally become a constant value of ~ 340 at a higher frequency over 10 5 Hz. The fast decrease of the dielectric constant at lower frequencies is ascribed to the space charge polarization effect, which is correlated to the non-uniform charge accumulation at grain boundaries within the sphere-like PTO powders. The slow reduction of the dielectric constant is due to that the dipoles present in the PTO powders could not reorient themselves as fast as the frequency of an alternating electric field, resulting in a decrease of the dielectric constants [24]. In contrast, the rod-like PTO powders (c) and (d) synthesized by template MSS method exhibit a slight frequency-dependent dielectric behavior, their dielectric constants are slightly reduced with increasing frequency below 10 3 Hz, and then become a constant value of ~ 140. It is observed in Fig. 10b that all the dielectric losses of the spherical and rod-like PTO powders are decreased with increasing frequency due to the existence of the space charge polarization in all the PTO powders. The dielectric loss of the PTO powder (b) has the highest value, which has reduced fast with increasing frequency below 10 5 Hz, and then it becomes constant. The dielectric losses of the PTO powder (a) are reduced slowly with increasing frequency, which has the lowest value as compared with the other three PTO samples. The dielectric losses of the spherical PTO powders (c) and (d) synthesized by template MSS method exhibit very similar dielectric behavior, their dielectric losses are reduced slowly as the frequency increases. At room temperature, the dielectric constant and dielectric loss of the spherical PTO powders (a) measured at 10 6 Hz were ~ 340 and 0.06, respectively. The corresponding values for the spherical PTO powders (b) were 155 and 0.12, 140 and 0.08 for the rod-like PTO powders (c), and 130 and 0.07 for the rod-like PTO powders (d). Therefore, the sphere-like PTO powders (a) have high dielectric constant and low dielectric loss, and these dielectric data are better than that reported previously for the PTO nanoparticles synthesized via sol-gel process and annealed at 600 °C for 6 h (the dielectric constant and dielectric loss at 10 6 Hz were about 15 and 0.40) [25], and for the PTO nanoparticles synthesized by stearic acid gel method and annealed at 400 °C for 1 h (the dielectric constant and dielectric loss at 10 6 Hz were about 50 and 0.002) [26]. Normally, to measure the dielectric properties of PbTiO3 ceramics prepared from the nanopowders synthesized by chemical methods such as the sol-gel method [27], hydrothermal method [28, 29], or by physical method such as high-energy ball milling technique [30], PbTiO3 powder samples are usually pressed into pellets under a hydraulic press (using 1 cm diameter die). For making dense PbTiO3 ceramics, the samples are needed to be sintered at high temperatures (e.g., 900 °C or 1000 °C for 2 h in air) followed by furnace cooling. Leonarska et al. [28] synthesized the PTO nanopowders at 490 K for 2 h by hydrothermal method and then prepared the PTO ceramics from the as-synthesized PTO nanopowders and sintered it at 1240 K for 1.5 h. They checked the impact of high-temperature process on the morphology or crystallization degree of the PTO ceramics by SEM observations and found that the PTO ceramics had slightly larger and rounded ceramic grains in comparison with the nanoparticles obtained directly from hydrothermal method. Similarly, Hu et al. [29] also reported the preparation of PTO nanoceramics (with grain sizes of ~ 200 nm) under sintering process (at 950 °C for 2 h in air) using the hydrothermal PTO nanopowders (with average grain size of ~ 100 nm) as the raw materials. This result indicates the sintering process of the hydrothermal PTO nanopowders can increase the grain size. Kong et al. [30] prepared the PTO nanopowders (with average grain size of ~ 10 nm) by high-energy ball milling technique, and pressed them directly into green pellets and sintered at 1100 °C for 1 h. Crack-free PTO ceramics with 95% of the theoretical density were successfully obtained. SEM images revealed that the average grain size of the sintered samples were < 1.5 μm. In the present work, we have prepared dense PbTiO3 ceramic samples under a sintering process (at 1150 °C for 2 h) by using the as-synthesized sphere-like PTO powders via MSS method and the as-synthesized rod-like PTO powders via template MSS method. The high-temperature process has improved the crystallized quality and the grain sizes of the PTO powders but has few effects on the morphology. The best dielectric properties of the PTO ceramics prepared the as-synthesized spherical PTO powders by MSS method are attributed to their larger average particle size (~ 2.0 μm).
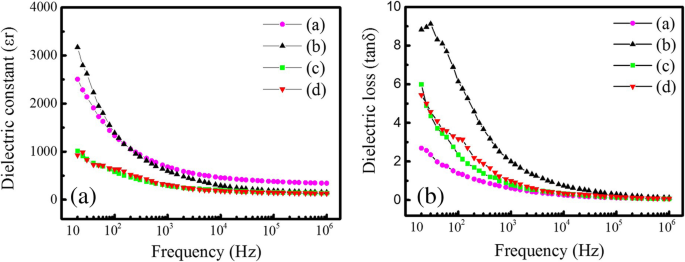
un Dielectric constants (εr ) and b dielectric losses (tanδ ) of the PTO powders synthesized by MSS method and template MSS method. Samples (a) and (b) were synthesized by MSS method at 950 °C for 5 h with the molar ratios of PbC2 O4 :TiO2 :NaCl:KCl equal to 1:1:30:30 and 1:1:60:60, respectively. Samples (c) and (d) were synthesized by template MSS method with the molar ratio of PbC2 O4 :TiO2 (rod-like template):NaCl:KCl equal to 1:1:60:60 and annealed 800 °C for 5 h and 10 h, respectively
Conclusions
Both sphere- and rod-like PTO powders were synthesized by MSS and template MSS methods, respectively. XRD patterns reveal that all the PTO powders are crystallized in a tetragonal phase structure. SEM images demonstrated that increasing the molar ratio of PbC2 O4 :TiO2 :NaCl:KCl from 1:1:10:10 to 1:1:60:60 in the MSS process had little effect on the sphere-like morphology of the PTO powders synthesized by MSS method. Large-scale polycrystalline rod-like PTO powders with length up to 10 μm and diameters in the range of 480 nm–1.50 μm were successfully synthesized by template MSS method at 800 °C for 5 h, where the rod-like anatase TiO2 precursors were used as a titanium source and the molar ratio of PbC2 O4 :TiO2 :NaCl:KCl was equal to 1:1:60:60. It is found that under low molten salt content, extending the reaction time promoted the formation of sphere-like PTO particles whereas the formation of rod-like PTO particles was suppressed. In addition, the rod-like PTO powders cannot be synthesized even if the rod-like TiO2 templates are used. Dielectric measurements demonstrated that the dielectric constants of the sphere-like PTO powders synthesized by MSS method decreased fast from ~ 3000 to ~ 700 at low frequencies below 10 3 Hz, and at high frequencies over 10 5 Hz they became a constant value of ~ 340. The fast decrease of the dielectric constant at low frequencies is ascribed to the space charge polarization due to the non-uniform charges accumulated within the PTO powders. The rod-like PTO powders synthesized by template MSS method exhibited slight frequency-dependent dielectric behavior, their dielectric constants decreased slowly at the frequencies below 10 3 Hz and then remained a constant value of ~ 140 as the frequency increased up to 10 6 Hz. At room temperature, dielectric constant and dielectric loss (measured at 10 6 Hz) of the sphere-like PTO powders synthesized by MSS method at 950 °C for 5 h with low molten salt content (the molar ratio of PbC2 O4 :TiO2 :NaCl:KCl equal to 1:1:30:30) were 340 and 0.06, respectively, and the corresponding values were 155 and 0.12 for the sphere-like PTO powders synthesized by MSS method with high molten salt content (the molar ratio of PbC2 O4 :TiO2 :NaCl:KCl equal to 1:1:60:60). The dielectric constant and dielectric loss for the rod-like PTO powders synthesized by template MSS method at 800 °C for 5 h and 10 h under high molten salt content (the molar ratio of PbC2 O4 :TiO2 (rod-like template):NaCl:KCl equal to 1:1:60:60) were 140 and 0.08, and 130 and 0.07, respectively. The higher dielectric constant and lower dielectric loss of the sphere-like PTO powders synthesized at 950 °C for 5 h by MSS method with the molar ratio of PbC2 O4 :TiO2 :NaCl:KCl equal to 1:1:30:30 are ascribed to their large average particle size (~ 2.0 μm), which have promising applications in multilayer capacitors and resonators.
Abréviations
- CALYPSO:
-
Crystal Structure AnaLYsis by Particle Swarm Optimization
- EDS :
-
Energy Dispersive Spectroscopy
- MSS:
-
Molten Salt Synthesis
- NP-9:
-
Polyoxyethylene (9) Nonylphenyl Ether
- PTO:
-
PbTiO3
- SEM :
-
Scanning Electron Microscopy
- XRD :
-
X-ray Diffraction
Nanomatériaux
- Synthèse facile et propriétés optiques de petits nanocristaux et nanotiges de sélénium
- Composite hybride nanostructuré silice/or-cellulose Amino-POSS par procédé Sol-Gel et ses propriétés
- Caractéristiques structurelles des composites polymères organiques-inorganiques conducteurs d'ions à base de résine époxy aliphatique et de sel de perchlorate de lithium
- L'effet du plasma de contact hors équilibre sur les propriétés structurelles et magnétiques des spinelles Mn Х Fe3 − X О4
- Influence de l'eau sur la structure et les propriétés diélectriques de la microcristalline et de la nano-cellulose
- Propriétés de synthèse et de luminescence des nanoparticules hydrosolubles α-NaGdF4/β-NaYF4:Yb,Er Core–Shell
- Propriétés structurelles et optiques dans le proche infrarouge du TiO2 dopé au Cr pour les pigments froids colorés
- Synthèse de points quantiques de sulfure d'antimoine solubles dans l'eau et de leurs propriétés photoélectriques
- Synthèse facile d'oxyde d'étain mésoporeux semblable à un trou de ver via l'auto-assemblage induit par l'évaporation et les propriétés de détection de gaz améliorées



