Utilisation de différents ions pour ajuster les structures de pile de graphène de feuille à oignon pendant l'exfoliation au plasma, avec des applications de supercondensateur
Résumé
Dans cet article, nous rapportons une approche facile et simple pour régler les structures de nanofeuillet de graphène (GNS) avec différents ions dans les électrolytes par le biais d'un processus d'exfoliation par plasma cathodique dans les réactions électrochimiques. Nous avons obtenu un GNS en forme de feuille et d'oignon lorsque l'électrolyte aqueux NaOH et H2 SO4 , respectivement, étaient présents pendant l'exfoliation au plasma dans les réactions électrochimiques, comme en témoignent les images de microscopie électronique à balayage et de microscopie électronique à transmission. De plus, le GNS en forme d'oignon présentait une surface spécifique de 464 m 2 g −1 et une performance supercapacitive de 67,1 F g −1 , mesuré à une vitesse de balayage de 5 mV s −1 dans 1µM NaCl; ces valeurs étaient bien supérieures à celles (72 m 2 g −1 et 21,6 F g −1 , respectivement) du GNS en forme de feuille. Cette nouvelle approche pour générer efficacement des structures de graphène empilées accordables avec différents ions, dans le processus d'exfoliation par plasma cathodique, a des potentiels prometteurs pour une utilisation dans des dispositifs de stockage d'énergie.
Introduction
Avec l'épuisement rapide des combustibles fossiles et la controverse croissante sur leur utilisation, le développement de dispositifs de stockage et de conversion d'énergie - y compris les batteries [1, 2] et les supercondensateurs [3, 4] - devient de plus en plus nécessaire pour la communauté mondiale. Les supercondensateurs ont été largement étudiés en raison de leurs excellentes densités de puissance et durées de vie en cyclage. Ils peuvent être divisés en deux types - les pseudocondensateurs et les condensateurs électriques à double couche (EDLC) - en fonction de leurs mécanismes de stockage de charge. Dans les pseudocondensateurs, le stockage de charges dépend de réactions de Faraday réversibles, dont les électrodes sont souvent constituées d'oxydes de métaux de transition et de polymères conducteurs. Pour les EDLC, l'énergie électrique est stockée par des processus d'adsorption et de désorption d'ions, en utilisant des matériaux d'électrode typiques (par exemple, des matériaux de carbone poreux). Ces dernières années, les matériaux bidimensionnels (2D), y compris le graphène et les dichalcogénures de métaux de transition (TMDC), ont attiré une attention considérable pour leurs excellentes propriétés physiques et chimiques. TMDC de type MX2 , où M est un atome de métal de transition (par exemple, Mo, W) et X est un atome de chalcogène (S, Se ou Te), possède une structure en sandwich et possède une capacité théorique et une activité catalytique adéquates [5,6,7]. Le graphène, un matériau carboné monocouche 2D ayant des réseaux en nid d'abeilles, a également attiré beaucoup d'attention pour ses extraordinaires conductivités électrique [8, 9] et thermique [10], son élasticité [11, 12], sa transparence [13, 14, 15 ], et la surface spécifique [16].
Deux formes de graphène sont courantes :les films minces et les poudres. L'exfoliation mécanique [17] et l'épitaxie [18, 19] et le dépôt chimique en phase vapeur [20,21,22,23] peuvent être utilisés pour produire des films minces de graphène de haute qualité—affichant une flexibilité et une transparence élevée—qui peuvent être appliqués dans des appareils électriques , mais des coûts élevés et un contrôle minutieux sont nécessaires, en raison des équipements de production et des précurseurs nécessaires. Le graphène en poudre est plus largement utilisé en raison de sa plus grande production de masse, de sa stabilité supérieure, de sa grande surface spécifique et de sa grande applicabilité aux applications de stockage de charge (par exemple, les condensateurs [24], les batteries lithium-ion [25, 26]). De nombreuses méthodes, notamment le broyage à billes, la décharge à l'arc, le plasma en solution et l'exfoliation électrochimique, ont été décrites pour la production de matériaux de graphène en poudre. Les méthodes de broyage à billes et de décharge à l'arc impliquent une exfoliation physique et peuvent être utilisées pour une production à l'échelle industrielle [27, 28] ; néanmoins, des équipements coûteux et des conditions de vide sont essentiels, ce qui entraîne des coûts plus élevés. Les méthodes d'exfoliation par plasma en solution et électrochimique peuvent toutes deux générer des feuilles de graphène à partir d'électrodes en graphite en utilisant des configurations simples et des électrolytes facilement accessibles [29, 30]. Bien que l'exfoliation au plasma en solution nécessite des tensions élevées (> 1000 V) entre des anodes et des cathodes très proches et, par conséquent, une attention particulière, l'exfoliation électrochimique peut être effectuée à des tensions appliquées relativement inférieures (< 20 V), mais des niveaux d'oxydation plus élevés sont introduits dans les produits , en raison de l'exfoliation anodique lors de l'électrolyse. De plus, la réagrégation immédiate du graphène en couche, via de fortes interactions d'empilement π, peut affaiblir ses performances.
Plusieurs méthodes ont été développées pour améliorer les performances des matériaux actifs, notamment les méthodes composites pour les dispositifs de stockage d'énergie [31,32,33], les matériaux 2D confinés à un seul atome et la régulation de surface pour la catalyse [34, 35], les hétérostructures en photovoltaïque [ 36], et l'ingénierie structurelle pour d'autres applications technologiques [37]. Ces méthodes entraînent toutes des effets synergiques des matériaux hétérogènes, avec des sites actifs plus accessibles fournis par les hétérojonctions et les plus grandes surfaces des matériaux modifiés. Pour les matériaux de graphène, les méthodes de modèle sacrificiel et la fabrication d'aérogels sont les processus les plus couramment utilisés pour surmonter les problèmes de réagrégation en couches. Les méthodes de modèle sacrificiel utilisent normalement des solutions aqueuses d'oxyde de graphène et de microsphères de polymère qui sont soumises à une réduction à haute température, produisant souvent des matériaux de graphène de surfaces spécifiques élevées [38, 39] ; néanmoins, l'uniformité du mélange doit être bien contrôlée en termes de nature de la charge de surface, et de telles méthodes prennent du temps. Les aérogels de graphène peuvent être synthétisés à basse température [40,41,42] ou dans des conditions ambiantes [43] pour donner des surfaces spécifiques exceptionnelles ; La congélation et la sublimation par solvant sont cependant chronophages et nécessitent des solvants toxiques pour préserver les architectures poreuses des aérogels. Par conséquent, il reste l'opportunité de développer une méthode facile à installer, peu coûteuse, en une seule étape et très efficace pour la production de graphène en poudre de surface spécifique élevée dans des conditions ambiantes sans utiliser de produits chimiques dangereux.
Nous rapportons ici une méthode facile pour réguler les morphologies des structures de nanofeuillet de graphène tel que produit (GNS) grâce à l'utilisation de divers électrolytes lors de l'exfoliation électrochimique par plasma cathodique dans des conditions ambiantes. En peu de temps, nous pourrions produire des GNS ayant des surfaces spécifiques élevées. Nous proposons un mécanisme pour l'exfoliation par plasma cathodique et discutons des morphologies, des structures et des performances supercapacitives du GNS lorsqu'il est utilisé comme matériau d'électrode.
Méthodes
Matériaux
L'hydroxyde de sodium et l'acide sulfurique ont été achetés auprès de Sigma-Aldrich. Tiges de graphite (φ 7 mm ; longueur 70 mm) et du graphite (99,5%) ont été obtenus auprès de Toyo Tanso (Taiwan). Des plaques de platine (longueur 200 um; largeur 30 um; épaisseur 0,7 um) ont été achetées auprès de Guang Yi Eleciron Chemical Equipment (Taiwan). Les échantillons GNS ont été préparés par les procédures suivantes :une tige de graphite et une plaque de platine ont été utilisées comme cathode et anode, respectivement, pendant le processus d'exfoliation; ils ont été immergés à des profondeurs de 10-20 et 60-120 mm, respectivement, sous l'électrolyte. Aqueux 2 M H2 SO4 et 4 µM de NaOH ont été utilisés comme électrolytes. Une fois qu'un potentiel de 60 V a été appliqué par l'alimentation (LinVac Tech, Taiwan), l'électrode de graphite a été recouverte par le plasma cathodique et les GNS ont été immédiatement exfoliés dans l'électrolyte. Après filtration sous vide à l'aide d'un filtre en nylon (Millipore; taille des pores 0,2 µm), les échantillons tels que produits ont été lavés et séchés à 70°C pendant 3 µh. Après dispersion du GNS dans de l'éthanol à une concentration de 0,3 mg mL −1 , la dispersion a été soumise à une centrifugation (2000 rpm, 30 min) pour éliminer tous les flocons de graphite non exfoliés. Le surnageant a été soumis à d'autres caractérisations. Le GNS obtenu en utilisant H2 SO4 et NaOH sont désignés ici par GNS_H + et GNS_Na + , respectivement.
Caractérisation
Les microstructures des échantillons GNS ont été étudiées en utilisant la microscopie électronique à balayage à émission de champ froid (SU-8010, Hitachi). Un microscope électronique à transmission à balayage corrigé pour les aberrations sphériques (ARM200F, JEOL) a été utilisé pour obtenir des images de microscopie électronique à transmission (MET), de MET haute résolution (HRTEM) et de transformée de Fourier rapide (FFT). HRTEM a en outre été utilisé pour déterminer la distribution d'épaisseur des échantillons GNS. Les spectres Raman permettant de déterminer les défauts dans les échantillons GNS ont été obtenus à l'aide d'un spectromètre Raman (HORIBA, LabRAM HR) avec une source laser He/Ne (longueur d'onde d'excitation laser 632,8 nm); N2 les isothermes d'adsorption/désorption de gaz ont été enregistrées à l'aide de la méthode Brunauer-Emmett-Teller (BET) (ASAP 2020, Micromeritics). Les distributions de la taille des pores ont été déterminées à l'aide du modèle Barret–Joyer–Halenda (BJH) et des branches de désorption des isothermes. La spectroscopie photoélectronique à rayons X (XPS; ULVAC, PHI Quantera SXM) et une source de rayons X en Al (1200 eV) ont été utilisées pour analyser les compositions de surface du GNS tel que produit. Un diffractomètre à rayons X D2 (Bruker), équipé d'un tube Cu Kα et d'un filtre Ni (λ =0,1542 nm), a été utilisé pour l'analyse structurelle du graphite et du GNS tel que produit.
Mesures électrochimiques
Les performances électrochimiques du graphite, GNS_H + , et GNS_Na + ont été déterminés dans 1 M de NaCl, en utilisant une station de travail électrochimique Zahner Zennium en mode à trois électrodes, comprenant une électrode au calomel standard comme électrode de référence et une feuille de platine comme contre-électrode. Le test a été effectué dans la plage de potentiel de − 0,4 à + 0,6 V. Chaque électrode a été préparée en mélangeant 90 % en poids de l'échantillon et 10 % en poids de poly (fluorure de vinylidène) avec du N -méthylpyrrolidone (NMP) puis enduction de la suspension sur des papiers graphite et séchage à 80°C pendant une nuit. La capacité spécifique (C , F g −1 ) peut être calculé à partir des courbes de voltamétrie cyclique (CV) à l'aide de l'équation :
$$ C=\frac{\int \mathrm{Idv}}{2\times v\times \Delta m\times \Delta V\ } $$où v est la vitesse de balayage (mV s −1 ), ∆m est la masse de la matière active, ∆V représente la fenêtre potentielle et Idv est l'aire sous la courbe CV (Q). La spectroscopie d'impédance électrochimique (SIE) a également été réalisée en utilisant une amplitude de la tension alternative de 5 µmV; les données ont été collectées dans la plage de fréquences de 100 mHz à 100 kHz.
Résultats et discussion
La figure 1 présente des images schématiques et numériques de la configuration d'exfoliation au plasma cathodique et des images schématiques du processus d'exfoliation et des matériaux tels que produits obtenus à l'aide de NaOH aqueux et de H2 SO4 électrolytes. Une tige de graphite a été utilisée comme cathode, tandis qu'une plaque de platine a été utilisée comme anode. Contrairement à l'exfoliation électrochimique traditionnelle [44, 45], ici le rapport de la surface en contact avec les électrolytes entre la cathode et l'anode était plutôt faible (1:10), de sorte qu'une densité de courant plus élevée pouvait être créée au niveau de la zone submergée. partie de la cathode [46, 47]. Avec une accumulation rapide de chaleur due à la densité de courant plus élevée, la vaporisation de l'eau à la cathode dominait initialement sur le H2 gaz produit par l'électrolyse normale. Lorsque la différence de tension a atteint 60 V, la partie immergée du graphite a été rapidement recouverte d'une gaine de gaz stable et mince, accompagnée d'un plasma, entraînant une exfoliation immédiate des feuilles de graphène [47, 48]. En raison des cations et de l'eau dans les électrolytes, des plasmas orange et blanc se sont formés lors de l'utilisation de NaOH aqueux et de H2 SO4 électrolytes, respectivement. Dans des études précédentes [49, 50], nous avons découvert que des nanofeuillets de graphène en forme de feuille pouvaient être générés par exfoliation plasma cathodique lors de l'utilisation de NaOH ou de KOH comme électrolyte. Dans cette étude, cependant, nous avons obtenu une morphologie de type oignon lorsque l'électrolyte était H2 SO4 , vraisemblablement à cause d'un type différent de bombardement cationique lors de l'exfoliation plasmatique cathodique [51]. Nous discutons des mécanismes affectant les morphologies telles que produites ainsi que la caractérisation de leurs matériaux ci-dessous.
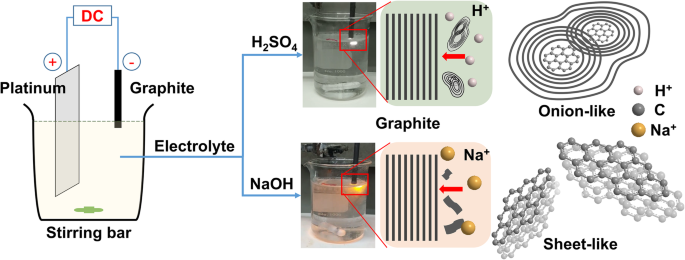
Représentations schématiques du dispositif expérimental et des processus d'exfoliation plasma cathodique utilisant NaOH et H2 SO4 comme électrolytes, ainsi que des images numériques des expériences
La figure 2a présente les images FESEM de GNS_Na + à un grossissement de 20 k; la morphologie en forme de feuille indique l'exfoliation réussie des feuilles de graphène typiques du processus plasma cathodique, en raison du stress thermique et du bombardement ionique entraîné par le potentiel. Fait intéressant, la figure 2b montre une morphologie de type brocoli avec des grappes sur les surfaces de GNS_H + Matériel. Nous soupçonnons que cette différence morphologique était liée à différents effets de bombardement ionique lors de l'exfoliation plasma cathodique :le plus petit H + Les ions ont non seulement exfolié les feuilles de graphène de l'électrode en graphite, mais ont également décoré les surfaces pour créer des nanostructures, tandis que le plus grand Na + les ions n'avaient qu'un effet exfoliant [50, 52]. Les figures 2c et d affichent des images MET de GNS_Na + et GNS_H + , respectivement. GNS_Na + avait une morphologie typique du graphène avec une surface lisse en forme de couche et des bords fracturés ; en revanche, GNS_H + en vedette plusieurs nanostructures empilées. HRTEM a révélé que le GNS_Na + tel que produit (Fig. 2e) comprenait quatre couches de feuilles de graphène ; une morphologie semblable à l'oignon existait pour GNS_H + (Fig. 2f), avec des diamètres de 4 à 10 nm. Fait intéressant, les anneaux comprenaient quatre à six couches de feuilles de graphène. La structure sphérique en forme d'oignon résulte vraisemblablement de l'effet de H + ions pendant le bombardement, en accord avec les données de la FESEM. Par rapport au plus grand Na + ions, le plus petit H + Les ions ont facilité une rupture de liaison et une dissociation plus poussées des radicaux de graphène produits lors de l'exfoliation plasmatique [53, 54]. Dès que ces espèces radicalaires ont été pulvérisées vers l'extérieur de la zone de plasma vers l'électrolyte, elles ont été trempées en raison du gradient de température [55] ; en même temps, en raison de la perte d'énergie des radicaux hautement énergisés, ils se sont recombinés pour former la structure sphérique en forme d'oignon afin de minimiser l'énergie de surface. Les encarts des Fig. 2e et f présentent des images FFT de GNS_Na + et GNS_H + , respectivement; les deux révèlent des motifs de diffraction hexagonaux typiques, suggérant que les réseaux de graphène sont restés après l'exfoliation par plasma cathodique. En raison des nombreux points de diffraction résultant des multiples orientations cristallines du graphène de type oignon, des motifs annulaires supplémentaires étaient évidents dans l'image de GNS_H + . Nous n'avons pu contrôler que grossièrement l'épaisseur du graphène tel que produit lors de la variation des ions dans les électrolytes, en raison de la nature hétérogène de l'intercalation et du bombardement des ions [50, 56, 57]. Fichier supplémentaire 1 :La figure S1a révèle les distributions d'épaisseur de plus de 30 échantillons GNS, telles que déterminées à partir de leurs images HRTEM. Notamment, GNS_H + et GNS_Na + les échantillons ayant moins de six couches de graphène représentaient respectivement environ 87 et 74% de toutes les nanofeuillets de graphène, tandis que le pourcentage de nanofeuillets de graphène comprenant trois à six couches de graphène était plus élevé pour GNS_H + que ce ne l'était pour GNS_Na + , suggérant que l'uniformité du GNS tel que produit était associée au type d'ions :le plus petit H + les ions pourraient induire plus de rupture de liaison et d'exfoliation que le Na + ions au cours du processus électrochimique plasma. Nous avons effectué deux séries d'expériences supplémentaires pour examiner la reproductibilité du GNS en forme d'oignon produit par H + ions. Fichier complémentaire 1 :Les figures S1b et S1c révèlent les histogrammes de GNS_H + des deuxième et troisième lots ; les distributions d'épaisseur étaient similaires à celles du premier lot, avec les images HRTEM des morphologies en forme d'oignon décrites dans les encarts du fichier supplémentaire 1 :figures S1b et S1c, suggérant la reproductibilité cohérente de GNS_H + .

un , b Images FESEM de a GNS_Na + et b GNS_H + ; c , d images TEM à fond clair et e , f Images HRTEM avec les images FFT correspondantes de c , e GNS_Na + et d , f GNS_H +
Nous avons utilisé XPS pour étudier la composition chimique de surface du GNS tel que produit. Fichier supplémentaire 1 :La figure S2a affiche les spectres de relevé des deux échantillons, révélant la présence d'espèces carbonées et oxygénées. L'oxydation du GNS peut être attribuée à l'exfoliation plasmatique cathodique, qui a radicalisé le graphène et les électrolytes avec des molécules d'eau. Après des réactions radicalaires, une trempe et un réarrangement atomique, des groupes fonctionnels contenant de l'oxygène ont été créés à la surface des matériaux tels que produits. Les figures 3a et b présentent les spectres C 1s déconvolués de GNS_Na + et GNS_H + , respectivement. Dans les deux spectres, nous attribuons les pics situés à 284,5 et 285,1 eV à la liaison de sp 2 - et sp 3 -atomes de carbone hybridés, à savoir respectivement C=C et C–C [58, 59]. Les pics avec des énergies de liaison plus élevées de 285,7 et 287,1 eV sont référencés aux unités C–O et C=O. Les pourcentages atomiques de carbone et d'oxygène pour GNS_Na + étaient respectivement de 97,9 et 2,1 % en pourcentage; GNS_H + avait un pourcentage d'oxygène plus élevé (jusqu'à 6,1 at.%). Le degré d'oxydation le plus élevé pour GNS_H + vraisemblablement résulté des nanostructures supplémentaires et des défauts introduits par le H + relativement plus petit ions—une conséquence de l'apparition de sites plus radicalisés sur le graphène lors de l'exfoliation.
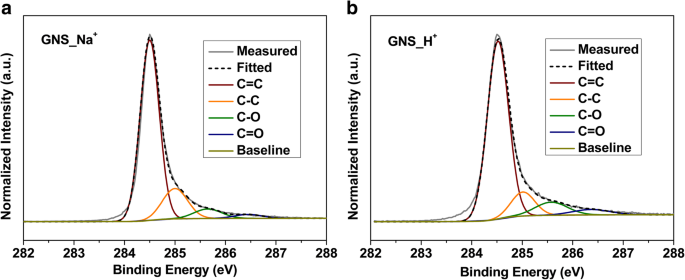
Spectres XPS C 1s haute résolution de a GNS_Na + et b GNS_H +
Nous avons obtenu des informations structurelles supplémentaires en utilisant la spectroscopie Raman. Sur la figure 4a, les trois pics distinctifs à 1325, 1571 et 2648 cm −1 représentent respectivement les bandes D, G et 2D [60,61,62,63]. La bande D représente le A1g mode, lié aux défauts et au désordre structurel; la bande G est associée à la liaison dans le plan d'une paire d'étirement formée de sp 2 -atomes de carbone hybridés, tout comme le E2g mode; liée à la séparation des bandes de phonons ou des bandes d'électrons, la bande 2D est l'ordre secondaire de la bande D. Les rapports des intensités de crête I D /Je G pour le graphite, GNS_Na + , et GNS_H + étaient de 0,08, 0,46 et 0,79, respectivement. Parce que le processus plasma cathodique a augmenté le nombre de groupes fonctionnels et de bords et a augmenté le désordre structurel du réseau de carbone, les intensités de défaut de GNS_Na + et GNS_H + étaient supérieurs à celui du graphite. De plus, nous attribuons la valeur la plus élevée de I D /Je G pour GNS_H + aux niveaux plus élevés d'oxydation et de formation de nanostructures, comme en témoignent XPS, FESEM et TEM. Le D′ relativement distinctif (1610 cm –1 ) et D + G (2909 cm –1 ) les bandes ont confirmé le plus grand désordre de GNS_H + . En raison des forces de van der Waals, une certaine agglomération s'est produite dans les échantillons pulvérulents du GNS, comme en témoignent les images FESEM ; à partir de nos spectres Raman sur la figure 4a, les bandes 2D symétriques et décalées de GNS_Na + et GNS_H + , par rapport à celui du graphite, suggèrent que les structures de graphène à quelques couches ont été principalement conservées sans grands degrés de réempilement pour former du graphite. La figure 4b fournit également des diagrammes en boîte des rapports d'intensité des bandes D et G pour GNS_Na + et GNS_H + , chacun collecté à partir de 15 échantillons. GNS_H + présentait des niveaux de défauts plus élevés en moyenne, suggérant que la plupart des domaines de cristallinité dans la morphologie de type oignon étaient plus petits que ceux du GNS_Na + en forme de feuille . Fait intéressant, la plage statistique des valeurs de I D /Je G pour GNS_H + était plus étroit que celui de GNS_Na + , indiquant que GNS_H + avait une uniformité supérieure, associée au plus petit H + ions induisant une rupture de liaison et une dissociation plus poussées des radicaux de graphène. Les motifs XRD du graphite, GNS_Na + , et GNS_H + révéler (Fichier supplémentaire 1 :Figure S2b) des informations structurelles supplémentaires. Le motif pour le graphite présentait un pic de diffraction net à 26,7°, que nous avons attribué à la diffraction (002), indiquant un degré élevé de graphitisation et une distance intercouche de 0,334 nm; ce pic pour les deux GNS a été abaissé de 0,1°, ce qui correspond à une augmentation de leurs distances intercouches. Les pleines largeurs à mi-hauteur (FWHMs) des pics de diffraction des rayons X près de 26,7° pour le graphite, GNS_Na + , et GNS_H + étaient respectivement de 0,11, 0,40 et 2,7°, suggérant que la taille des cristaux diminuait dans cet ordre et, par conséquent, que la nature amorphe des échantillons GNS augmentait après l'exfoliation plasmatique cathodique. Nous avons effectué N2 expériences d'adsorption pour déterminer les surfaces BET et les tailles de pores BJH, avec les distributions, des échantillons. La figure 5a révèle que le N2 les isothermes d'adsorption/désorption avaient des boucles d'hystérésis H3 typiques, selon la classification de l'Union internationale de chimie pure et appliquée (IUPAC). Les boucles d'hystérésis sont apparues à une pression relativement basse (0,4 à 0,8), indiquant la présence de mésopores dans les matériaux tels que produits [50]. Les surfaces spécifiques du graphite, GNS_Na + , et GNS_H + avaient 9, 72 et 464 m 2 g −1 , respectivement. La surface spécifique plus élevée de GNS_H + est cohérent avec ses nanostructures en forme d'oignon, confirmant la participation de H + ions lors de l'exfoliation cathodique. Théoriquement, une surface spécifique plus élevée pour le graphène en tant que matériau d'électrode fournirait plus de sites d'absorption pour les ions lors des mesures électrochimiques. Les distributions de taille de pores BJH des échantillons (Fig. 5b) ont révélé que les tailles de pores dominantes comprises entre 2 et 20 nm pour le graphite, GNS_Na + , et GNS_H + étaient respectivement de 2,5, 14,9 et 9,2 nm. Ainsi, la taille dominante des pores du GNS tel que produit était plus petite lorsqu'elle était fabriquée à l'aide de H + ions. Néanmoins, le volume poreux de GNS_H + (0,928 cm 3 g −1 ) était plus grand que ceux de GNS_Na + (0,289 cm 3 g −1 ) et graphite (0.058 cm 3 g −1 ), suggérant que les structures poreuses entre les nano-paquets de GNS_H + fourni des espaces supplémentaires pour l'accès de l'électrolyte et pour le transport des ions pendant la charge et la décharge électrochimique.
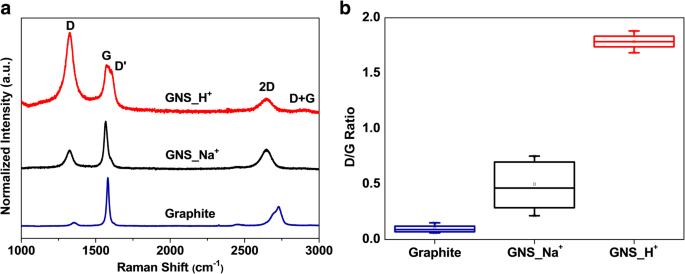
un Spectres Raman et b diagrammes en boîte des rapports d'intensité des bandes D et G du graphite, GNS_Na + , et GNS_H +
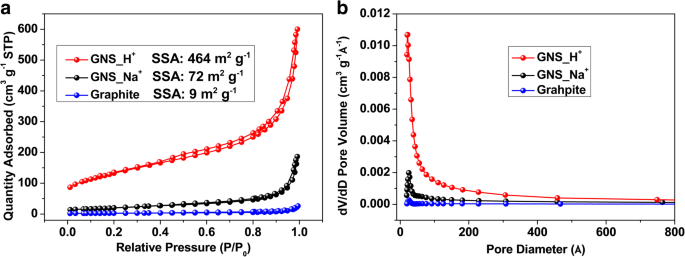
un N2 typique isothermes d'adsorption/désorption et b Distribution de la taille des pores BJH du graphite, GNS_Na + , et GNS_H +
Nous avons utilisé un système à trois électrodes pour déterminer les propriétés électrochimiques du graphite, GNS_Na + , et GNS_H + dans 1 M NaCl à des potentiels de - 0,4 à + 0,6 V. La figure 6a présente les voltamogrammes cycliques du graphite, GNS_Na + , et GNS_H + enregistré à une vitesse de balayage de 5 mV s −1 . Nous observons des formes quasi-rectangulaires des courbes mesurées sans réaction faradique évidente, suggérant que les matériaux d'électrode avaient une excellente capacité électrique à double couche en raison d'ions hautement accessibles [64]. Le tableau 1 compare les surfaces spécifiques, les volumes de pores, les capacités spécifiques et les résistances de transfert de charge du graphite, GNS_Na + , et GNS_H + . Les capacités spécifiques, déterminées à une vitesse de balayage de 5 mV s −1 , pour graphite, GNS_Na + , et GNS_H + étaient de 11,4, 21,6 et 67,1 F g −1 , respectivement. Étant donné que des structures de graphène de quelques couches seulement ont été produites lors de l'exfoliation par plasma cathodique, les performances supercapacitives des deux GNS étaient supérieures à celles du graphite ; en outre, le GNS_H + en forme d'oignon structuré en 3D avait une capacité spécifique encore plus élevée car sa surface spécifique et son volume de pores plus grands pouvaient accueillir des ions supplémentaires pendant la charge et la décharge. Fichier supplémentaire 1 :Le tableau S1 compare les méthodes de synthèse, les temps et les températures; les surfaces spécifiques; et les performances électrochimiques (dans des solutions de NaCl à différentes vitesses de balayage) de divers matériaux de graphène qui ont été rapportés dans la littérature. Bien que les capacités spécifiques de cette étude soient inférieures à certaines de celles rapportées précédemment, la plupart des autres méthodes de synthèse ont nécessité des temps de traitement plus longs et des températures plus élevées pour produire des matériaux de graphène avec des surfaces spécifiques élevées. Par conséquent, nous pensons que notre processus d'exfoliation au plasma cathodique facile, en une seule étape et vert est très compétitif pour produire un GNS de bonne qualité. Fiche complémentaire 1 :Les figures S3a–c présentent les voltamogrammes cycliques du graphite, GNS_Na + , et GNS_H + enregistrées à différentes vitesses de balayage. Lors de l'augmentation de la vitesse de balayage, les courbes mesurées de chaque échantillon ont conservé leurs formes quasi-rectangulaires, suggérant que les matériaux des électrodes avaient une excellente capacité électrique à double couche sans réaction faradique évidente. Notamment, les deux GNS ont présenté une excellente stabilité électrochimique sur une large gamme de vitesses de balayage; les améliorations distinctes de la densité de courant lors de l'augmentation de la vitesse de balayage suggèrent des capacités de vitesse supérieures pour ces deux matériaux d'électrode. La figure 6b révèle que les capacités spécifiques de GNS_H + étaient relativement plus élevés que ceux de GNS_Na + à toutes les vitesses de balayage de 5 à 500 mV s −1 , probablement en raison de la surface spécifique plus élevée résultant des nanostructures en forme d'oignon de GNS_H + . La figure 6c affiche les courbes de charge/décharge galvanostatiques typiques des matériaux de graphène GNS_Na + et GNS_H + à une densité de courant de 0,1 A g −1 . Leurs courbes triangulaires hautement symétriques impliquent que les deux échantillons n'ont subi aucune chute de potentiel (iR) évidente, indiquant de faibles résistances internes dans ces matériaux d'électrode. Fichier supplémentaire 1 :Les figures S3d–f présentent les courbes de charge/décharge galvanostatique des échantillons à différentes densités de courant. Les courbes mesurées conservent les formes triangulaires notables dans leur symétrie lors de l'augmentation de la densité de courant, indiquant les capacités de débit exceptionnelles de ces GNS tels que produits avec différentes morphologies. Nous avons mesuré les capacités de cyclisme de GNS_Na + et GNS_H + plus de 1000 cycles à une vitesse de balayage de 100 mV s −1 (Fichier supplémentaire 1 :Figure S4). Chaque matériau a affiché une rétention de capacité exceptionnelle :93, 91 et 88 % pour le graphite, GNS_Na + , et GNS_H + , respectivement. Le pourcentage de rétention de capacité légèrement inférieur de GNS_H + est probablement due au piégeage d'ions non réversible dans les pores plus petits de ses nanostructures pendant les processus de charge et de décharge. L'EIS est une méthode puissante pour mesurer les conductivités électriques des électrodes de carbone. La figure 6d affiche les tracés de Nyquist du graphite, GNS_Na + , et GNS_H + mesurée dans la gamme de fréquences de 100 mHz à 100 kHz. En général, la première interception par rapport à l'axe réel des courbes mesurées dans la région des hautes fréquences, connue sous le nom de résistance série électrochimique (R s ), peut être liée à la conductivité ionique de l'électrolyte dans les matériaux d'électrode, à la résistance intrinsèque des matériaux d'électrode et à la résistance de contact des matériaux au collecteur de courant. Petites valeurs de R s étaient évidents pour nos deux échantillons dans leurs courbes mesurées, indiquant la conductivité supérieure de ces matériaux de graphène tels que produits. Le tracé d'impédance comportait également des demi-cercles dans les régions des hautes et moyennes fréquences, liés aux processus de transfert de charge aux interfaces entre les matériaux actifs sur l'électrode et l'électrolyte ; une ligne inclinée à 45° dans la région des basses fréquences suggérait une impédance de Warburg corrélée au transport de masse [65, 66]. Les résistances de transfert de charge (R ct ) de graphite, GNS_Na + , et GNS_H + étaient respectivement de 3,5, 3,9 et 4,6 Ω, révélant des matériaux de graphite et de graphène hautement conducteurs qui facilitaient la diffusion ionique pendant la charge et la décharge. La valeur légèrement supérieure de R ct pour GNS_H + peut être corrélé à sa zone de cristallinité plus petite et à son niveau d'oxydation plus élevé, par rapport à ceux du graphite et du GNS_Na + . Ainsi, bien que différentes morphologies se soient formées en présence de Na + et H + ions, les conductivités du GNS produit par exfoliation plasma cathodique n'ont pas été compromises, en raison de la préservation de la cristallinité du réseau de graphène. En raison de la courbure des structures en forme d'oignon, GNS_H + pourrait avoir présenté plus de luxations structurelles et, par conséquent, des sites plus actifs dans les réseaux hexagonaux de graphène dans le plan basal incurvé [67,68,69]. Par conséquent, l'absorption d'ions pour le GNS_H + semblable à l'oignon aurait pu se produire sur plus d'arêtes et de plan basal, plutôt que seulement sur le plan basal comme dans le cas du GNS_Na + en forme de feuille . De plus, l'état oxydant plus élevé de GNS_H + could provide a more hydrophilic surface for interaction with the aqueous electrolyte and, thus, allow more efficient transport and accessible micro-tunnels for ions during charging and discharging, resulting in higher supercapacitive performances.
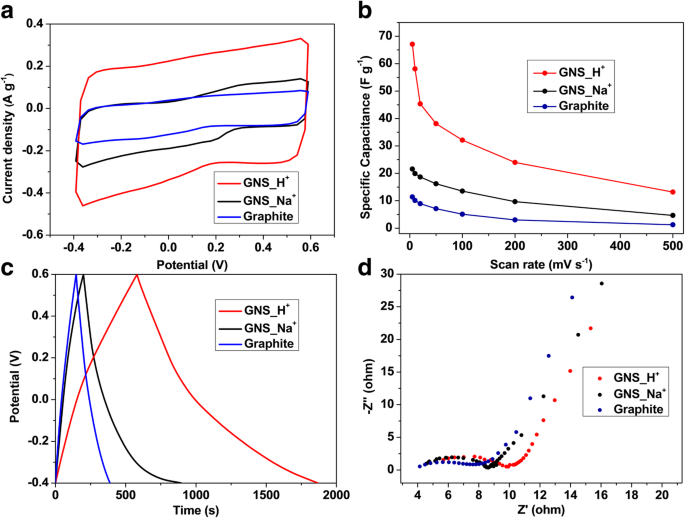
un Cyclic voltammograms of the various samples, recorded at 5 mV s −1 . b Specific capacitances of the samples, determined at scan rates from 5 to 500 mV s −1 . c Galvanostatic charge/discharge curves recorded at 0.1 A g −1 . d Nyquist plots of the samples measured from 100 mHz to 100 kHz; inset:corresponding expanded high-frequency region of the plots
Conclusion
We have produced typical sheet-like GNS when using aqueous NaOH as the electrolyte in a cathodic plasma exfoliation process performed within a short period of time under ambient conditions. When the electrolyte was replaced by aqueous H2 SO4 , an onion-like morphology was introduced to the as-produced GNS, which featured a superior specific surface area (464 m 2 g −1 ) and pore volume (0.928 cm 3 g −1 ). We suspect that the involvement of H + ions facilitated more thorough bond breaking and dissociation of radical species than did the Na + ions during the cathodic plasma exfoliation. Measurements of supercapacitive performance at a scan rate of 5 mV s −1 in 1 M NaCl indicated that the GNS featuring the onion-like nanostructures had a specific capacitance (67.1 F g −1 ) higher than that of the GNS having the sheet-like morphology (21.6 F g −1 ). Thus, it is possible to produce GNS with different morphologies and supercapacitive performances when using readily accessible electrolytes in a facile cathodic plasma exfoliation process; furthermore, the unique onion-like GNS structure, with some retained crystallinity and curvature, created by the H + ions, exhibited extraordinary conductivity and a high specific surface area, suggesting greater potential (relative to that of the corresponding sheet-like GNS) for use in energy storage devices.
Abréviations
- BET:
-
Brunauer–Emmett–Teller
- CV :
-
Cyclic voltammogram
- EDLC:
-
Condensateurs électriques double couche
- FESEM:
-
Field-emission scanning electron microscopy
- FFT:
-
Fast Fourier transform
- FWHM:
-
Full width at half maximum
- GNS:
-
Graphene nanosheets
- GNS_H + :
-
Graphene nanosheets produced using H2 SO4
- GNS_Na + :
-
Graphene nanosheets produced using NaOH
- H2 SO4 :
-
Sulfuric acid
- KOH:
-
Potassium hydroxide
- NaCl:
-
Sodium chloride
- NaOH:
-
Sodium hydroxide
- NMP :
-
N-Methyl-2-pyrrolidone
- TEM :
-
Microscopie électronique à transmission
- XPS :
-
X-ray photoelectron spectroscopy
- XRD :
-
Diffraction des rayons X
Nanomatériaux
- En accord avec le cœur d'un atome de cuivre
- LPWA :les opérateurs Challenger pourraient bénéficier d'une technologie différente de celle du leader du marché
- Élimination par adsorption des ions cuivre (II) d'une solution aqueuse à l'aide d'un nano-adsorbant de magnétite à partir de déchets de broyage :synthèse, caractérisation, adsorption et modél…
- Composites de graphène et polymères pour applications de supercondensateurs :une revue
- Fabrication de structures périodiques 3D basées sur des nanoshells par processus de modélisation à l'aide de ZnO dérivé de la solution
- Fabrication de nanomotifs ordonnés à l'aide d'un copolymère tribloc ABC avec du sel dans du toluène
- Nanosphères de carbone monodispersées à structure poreuse hiérarchique comme matériau d'électrode pour supercondensateur
- Évaluation des structures graphène/WO3 et graphène/CeO x en tant qu'électrodes pour les applications de supercondensateurs
- Aérogel de graphène/polyaniline avec superélasticité et haute capacité en tant qu'électrode de supercondensateur hautement tolérante à la compression



