Hydroxydes de nickel-cobalt avec nanofeuillets accordables en couche mince pour électrode de supercondensateur hautes performances
Résumé
Les hydroxydes doubles en couches en tant que matériaux d'électrode de supercondensateur typiques peuvent présenter des performances de stockage d'énergie supérieures si leurs structures sont bien régulées. Dans ce travail, une méthode hydrothermale simple en une étape est utilisée pour préparer divers hydroxydes doubles couches nickel-cobalt (NiCo-LDH), dans lesquels les différentes teneurs en urée sont utilisées pour réguler les différentes nanostructures des NiCo-LDH. Les résultats montrent que la diminution de la teneur en urée peut améliorer efficacement la dispersibilité, ajuster l'épaisseur et optimiser les structures de pores internes des NiCo-LDH, améliorant ainsi leurs performances de capacité. Lorsque la teneur en urée est réduite de 0,03 à 0,0075 g sous un rapport massique de matériaux précurseurs fixe de nickel (0,06 g) à cobalt (0,02 g) de 3:1, l'échantillon préparé NiCo-LDH-1 présente une épaisseur de 1,62 nm , et les structures de nanofeuilles transparentes en couche mince et un grand nombre de pores de surface sont formés, ce qui est bénéfique pour la transmission des ions dans le matériau de l'électrode. Après avoir été préparé comme une électrode de supercondensateur, le NiCo-LDH-1 affiche une capacité spécifique ultra-élevée de 3982,5 F g −1 sous la densité de courant de 1 A g −1 et une rétention de capacité élevée supérieure à 93,6 % après 1 000 cycles de charge et de décharge à une densité de courant élevée de 10 A g −1 . L'excellente performance électrochimique du NiCo-LDH-1 est prouvée par l'assemblage d'un supercondensateur asymétrique à deux électrodes avec des sphères de carbone, affichant la capacité spécifique de 95 F g −1 à 1 A g −1 avec la rétention de capacité de 78% sur 1000 cycles. Le travail actuel offre un moyen facile de contrôler la nanostructure des NiCo-LDH, confirme l'affection importante de l'urée sur l'amélioration des performances capacitives pour l'électrode de supercondensateur et offre une grande possibilité de développement de supercondensateurs haute performance.
Introduction
En tant que dispositif de stockage d'énergie respectueux de l'environnement, le supercondensateur attire beaucoup d'attention en raison de ses avantages uniques, notamment une longue durée de vie, une réversibilité supérieure, une densité de puissance élevée et une grande fiabilité [1,2,3]. Ces dernières années, il a été potentiellement appliqué dans de nombreuses applications potentielles telles que les voitures électriques, les appareils portables intelligents et les ordinateurs portables, ce qui est d'une grande importance pour l'utilisation et le stockage futurs de l'énergie. Cependant, la densité d'énergie plus faible des supercondensateurs a toujours été une raison importante pour limiter leur développement ultérieur. Il est bien connu que le facteur crucial pour déterminer la capacité du supercondensateur est la propriété électrochimique du matériau de l'électrode. Ainsi, la principale solution à l'heure actuelle est de développer des matériaux d'électrode avec d'excellentes propriétés électrochimiques [4,5,6,7,8,9]. Les matériaux carbonés [10,11,12,13], les oxydes de métaux de transition [14], les hydroxydes de métaux de transition (TMH) [15,16,17] et les polymères conducteurs [18] sont les principaux matériaux utilisés comme électrodes de supercondensateurs. Parmi eux, les nanomatériaux multihybrides de TMH sont devenus une forte tendance d'exploration en raison de l'existence d'un effet synergique, d'une meilleure contrôlabilité de la composition chimique, d'une activité redox exceptionnelle et d'excellentes performances d'échange d'anions. En tant que TMH typique, l'hydroxyde de nickel-cobalt est préféré en raison de son faible prix, de son processus de préparation simple et de sa capacité théorique élevée. Cependant, obtenir des matériaux d'électrodes hautes performances d'hydroxydes de nickel-cobalt par une méthode simple reste un défi de taille.
Les propriétés électrochimiques des hydroxydes de nickel-cobalt dépendent en grande partie des nanostructures morphologiques spéciales [19,20,21,22,23] et des compositions des ions métalliques [24, 25]. Dans des études antérieures, Wu et al. [26] ont synthétisé des matrices de nanofeuillets hiérarchiques poreux de nickel-cobalt à double couche d'hydroxyde de vanadium dopé au vanadium qui ont fourni une capacité spécifique élevée de 2960 F g −1 à une densité de courant de 1 A g −1 . Yan et al. [27] ont conçu les microsphères creuses à double couche d'hydroxyde nickel-cobalt avec une morphologie de type hortensia, présentant une capacité spécifique de 2158.7 F g −1 sous une densité de courant de 1 A g −1 . D'autres efforts ont été faits pour diminuer la résistance, augmenter la conductivité électrique des matériaux d'électrode et obtenir d'autres morphologies spéciales avec une surface spécifique élevée. Lorsque le matériau actif était cultivé à la surface du substrat, il formerait une structure tridimensionnelle en couches qui pourrait assurer le contact complet entre l'ion électrolyte et le matériau actif et améliorer l'efficacité de la réaction. Sur cette base, Ouyang et al. [28] ont obtenu une capacité spécifique élevée de 2047 F g −1 à une densité de courant de 1 A g −1 en fabriquant des particules d'hydroxydes doubles couches sphériques de nickel-cobalt structurées hiérarchiquement cultivées sur du carbone poreux de la biomasse. Zha et al. [29] ont conçu et fabriqué avec succès des nanofeuillets de sulfure de nickel-cobalt hautement ouverts sur de la mousse de Ni, qui présentaient une faible résistance et une capacité spécifique élevée de 2553,9 F g −1 sous une densité de courant de 0,5 A g −1 . Malheureusement, bien que de grands progrès aient été réalisés dans les études précédentes sur les hydroxydes en couches de nickel-cobalt, la capacité spécifique de la plupart d'entre eux en tant que matériaux d'électrode reste encore inférieure à 3000 F g −1 .
Dans ce travail, nous proposons une stratégie simple et efficace pour faire croître des NiCo-LDH sur la mousse de nickel et ajuster les nanostructures des matériaux d'électrode pour améliorer la capacité de stockage de charge. Les NiCo-LDH sont préparés par un procédé hydrothermal en une étape, avec la structure comprenant la dispersité, l'épaisseur et les porosités facilement ajustées en diminuant la teneur en urée sous un rapport massique Ni/Co fixe de 3:1. Le NiCo-LDH-1 optimal affiche des nanofeuillets en couche mince d'une épaisseur d'environ 1,62 nm et des structures poreuses évidentes. La structure poreuse en couche mince peut fournir des sites actifs abondants pour la réaction d'oxydoréduction, augmenter l'affinité des matériaux d'électrolyte et d'électrode et réduire la résistance à la diffusion et la distance de migration des ions électrolytiques. En conséquence, NiCo-LDH-1 présente une capacité spécifique ultra-élevée de 3982,5 F g −1 sous la densité de courant de 1 A g −1 , et une rétention de capacité élevée supérieure à 93,6 % après 1 000 cycles de charge et de décharge à une densité de courant élevée de 10 A g −1 . L'excellente performance électrochimique du NiCo-LDH-1 est encore prouvée par l'assemblage d'un supercondensateur asymétrique à deux électrodes avec des sphères de carbone, affichant la capacité spécifique de 95 F g −1 à 1 A g −1 et la rétention de capacité avec 78% sur 1000 cycles.
Méthodes
La mousse de nickel (NF, 1 cm 2 ) utilisé dans l'expérience a été fourni par Canrd Co., Ltd., Chine. Avant utilisation, il a été soumis aux ultrasons dans 2 M HCl pendant 15 min pour éliminer l'oxyde attaché à la surface, puis lavé par de grandes quantités d'eau désionisée et d'éthanol pour éliminer les ions de la surface. Après cela, il a été séché à 60 °C pendant 3,5 h sous vide. Tous les autres produits chimiques étaient de qualité analytique, achetés auprès de Sinopharm Chemical Reagent Co., Ltd., en Chine et utilisés sans autre purification.
Dans une procédure typique, d'abord 0,06 g NiCl2 ·6H2 O et 0,02 g de CoCl2 ·6H2 O ont été dissous dans 80 ml d'eau déminéralisée sous ultrasons pendant 15 min. Deuxièmement, l'urée a été mise dans la solution mélangée et maintenue aux ultrasons pendant 10 minutes jusqu'à ce que le solide soit complètement dispersé. Ensuite, des NF avec du ruban résistant à la chaleur sur un côté ont été fixés en diagonale au fond de l'autoclave en acier inoxydable revêtu de téflon après avoir mesuré sa masse. Enfin, la solution homogène a été transférée dans l'autoclave puis a été maintenue à 100 °C pendant 8 h. Après la réaction, les NF refroidis déposés avec des NiCo-LDH ont été récupérés et lavés avec de l'eau déminéralisée pour éliminer les impuretés collées à la surface, puis séchés à 60 °C pendant 4 h sous vide. Les teneurs totales en urée étaient de 0,0075, 0,015 et 0,03 g, respectivement, correspondant aux échantillons de NiCo-LDH-1, NiCo-LDH-2 et NiCo-LDH-3. L'échantillon, préparé de la même manière que ceux mentionnés ci-dessus sauf sans ajout d'urée, a été nommé NiCo-LDH-0.
Le diffractomètre automatique à rayons X (XRD, D8 Advance) a été utilisé pour mesurer la structure cristalline des matériaux. Un spectromètre de photoélectrons à rayons X (XPS, ESCALAB 250Xi) a été utilisé pour mesurer la valence des éléments et le contenu des matériaux. Un microscope électronique à balayage à vide poussé et à vide (SEM, JSM-6360LV) a été utilisé pour observer la morphologie et la composition de la microstructure de la surface des échantillons. Un microscope électronique à transmission (MET, TF20 Jeol 2100F) a été utilisé pour observer l'ultrastructure du matériau. Un microscope à force atomique (AFM, Dimension Icon) a été utilisé pour obtenir les informations sur la structure de la topographie de la surface et les informations sur la rugosité de la surface avec une résolution nanométrique. La cartographie des éléments de spectroscopie à rayons X à dispersion d'énergie (cartographie EDS) a été utilisée pour mesurer la distribution des éléments.
Un système typique à trois électrodes dans une solution de KOH 1 M a été utilisé pour tester les performances électrochimiques. La mousse de nickel préparée développée avec le matériau de l'électrode était l'électrode de travail, et la plaque de platine et l'électrode au calomel saturé ont été utilisées comme contre-électrode et électrode de référence, respectivement, par lesquelles les voltamogrammes cycliques (CV), les courbes de charge-décharge galvanostatique (GCD ), des tests d'impédance électrochimique (EIS) et de stabilité de cycle ont été mesurés. La capacité spécifique C c (F g −1 ) et capacité spécifique Q (C g −1 ) des échantillons peut être calculé en fonction des paramètres obtenus par les courbes de décharge galvanostatique, et les expressions sont les suivantes :
$$\begin{array}{c}{ C}_{c}=\frac{I\times \Delta t}{\Delta V\times m}\end{array}$$ (1) $$\begin {array}{c}Q=\frac{I\times \Delta t}{m}\end{array}$$ (2)où je (A) représente le courant de décharge ; t (s) désigne le temps de déchargement; ΔV (V) donne la fenêtre de potentiel de décharge; et m (g) correspond à la masse de la matière active, environ 0,0012 g.
Un supercondensateur asymétrique (ASC) est fabriqué dans un système à deux électrodes après avoir équilibré les charges par Qs+ ms+ = Qs- ms- . Le NiCo-LDH-1/NF est utilisé comme électrode positive, et l'électrode négative est obtenue en mélangeant des sphères de carbone, du noir de carbone et du PTFE au rapport de 8:1:1 sur le NF. L'électrolyte est le même que celui du système à trois électrodes, et la plage de fenêtres potentielles pour l'ASC est de 0 ~ 1,4 V. Pour examiner les performances électrochimiques pratiques, la densité d'énergie spécifique E c (W h kg −1 ) et densité de puissance spécifique P c (W kg −1 ) pour la configuration asymétrique sont calculés comme suit :
$$\begin{array}{c}{E}_{c}=\frac{{C}_{c}{\left(\Delta V\right)}^{2}}{2\times 3.6} \end{array}$$ (3) $$\begin{array}{c}{P}_{c}=\frac{{E}_{c}\times 3600}{\Delta t}\end{ tableau}$$ (4)où je (A) représente le courant de décharge ; t (s) donne le temps de décharge; ΔV (V) correspond aux fenêtres potentielles; m (g) signifie la masse active totale des électrodes positive et négative, environ 0,0065 g.
Résultats et discussion
La figure 1 illustre les microstructures et les morphologies des NiCo-LDH cultivées sur le NF préparé avec différentes teneurs en urée. La figure 1a–l montre les images SEM, les images AFM et l'épaisseur des échantillons, respectivement. Comme le montre la figure 1a, le NiCo-LDH-3 synthétisé affiche des structures en forme de feuille empilées et entrelacées dans la direction horizontale parallèle à la NF. Les structures en forme de feuille sont inégales et ont une forte adhérence. Lorsque la teneur en urée diminue progressivement, les NiCo-LDH croissent progressivement dans le sens vertical et sont perpendiculaires au NF. Comme le montre la figure 1c, lorsque la teneur en urée est réduite à 0,0075 g, les nanofeuillets de NiCo-LDH-1 sont entrelacés et distribués à la surface du NF, ce qui forme une structure tridimensionnelle évidente et des structures de pores riches entre les couches. Les morphologies de ces nanofeuillets sont bénéfiques pour augmenter la surface spécifique de l'électrode pour fournir des sites réactifs abondants pour la réaction [30]. Par conséquent, il peut augmenter considérablement la surface de contact avec l'électrolyte pour favoriser la réaction électrochimique en contribuant à une grande capacité spécifique dans la réaction électrochimique [31]. La figure 1e–l représente les images AFM permettant de détecter les épaisseurs de nanofeuillets de NiCo-LDH. Pour les échantillons de NiCo-LDH-3, NiCo-LDH-2 et NiCo-LDH-1, les épaisseurs correspondantes sont respectivement de 3,29, 2,52 et 1,62 nm. Il est montré que l'épaisseur des nanofeuillets du matériau diminue progressivement avec la diminution de la teneur en urée. La structure ultra-mince de NiCo-LDH-1 offre de bonnes conditions pour la formation de la structure des pores et raccourcit la distance jusqu'au transfert d'ions. Cependant, l'image SEM de NiCo-LDH-0 (Fig. 1d) montre que l'échantillon préparé sans ajout d'urée présente également des structures en forme de feuille, mais l'épaisseur est de 3,31 nm (Fig. 1h, l), ce qui est plus épais que ceux d'autres échantillons préparés avec de l'urée. Cela implique que les microstructures et les morphologies des NiCo-LDH peuvent être affectées par la teneur en urée. Dans le processus d'obtention des échantillons contenant de l'urée, l'urée se décompose lentement en NH3 et CO2 à haute température et produit en outre du CO3 2− , NH4 + et OH − ions par réaction avec l'eau. Sous condition de teneur plus faible en urée, Co 2+ et Ni 2+ les ions ont peu de sites de contact avec OH − , qui formeront les structures de nanofeuillets en couche plus mince [32]. Néanmoins, la gravure ne se produit pas pendant le processus de l'échantillon préparé sans urée. En conséquence, par rapport aux échantillons obtenus avec de l'urée, l'épaisseur de l'échantillon sans ajout d'urée devient plus épaisse.
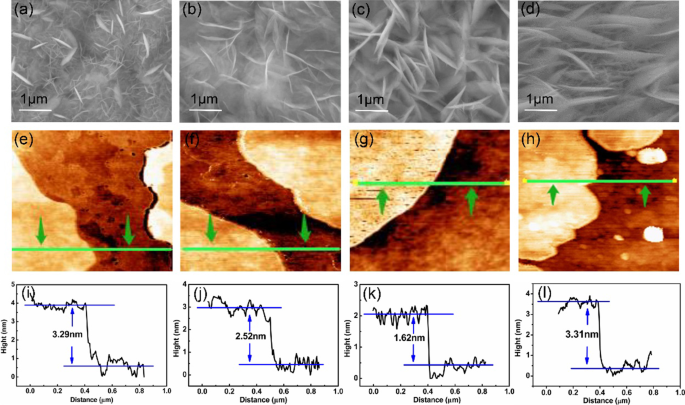
un –d Images SEM des échantillons :a NiCo-LDH-3, b NiCo-LDH-2, c NiCo-LDH-1, d NiCo-LDH-0; e –h Images AFM de l'échantillon :e NiCo-LDH-3, f NiCo-LDH-2, g NiCo-LDH-1, h NiCo-LDH-0; je –l les épaisseurs des échantillons :i NiCo-LDH-3, j NiCo-LDH-2, k NiCo-LDH-1, l NiCo-LDH-0
Les spectres XRD des NiCo-LDH sont présentés sur la figure 2a. Après comparaison avec la carte PDF standard, tous les matériaux peuvent être affectés à Ni0.75 Co0.25 (CO3 )0.125 (OH)2 0,215 ·0.38H2 O (PDF#40–0216). Les pics de diffraction à 2θ de 11,59°, 23,14°, 34,95°, 39,40°, 62,44° et 65,96° correspondent aux hydroxydes nickel-cobalt (003), (006), (012), (015), (113) et ( 116) plans cristallins, respectivement. La micro-morphologie détaillée de NiCo-LDH-1 est en outre caractérisée par MET. Comme le montre la figure 2b–d, NiCo-LDH-1 apparaît sous forme de couches poreuses minces et il y a très peu d'empilement entre les couches. En effet, la teneur réduite en urée améliore la dispersibilité du matériau et réduit l'empilement latéral entre les couches. La structure de croissance tridimensionnelle rend la structure en feuille du matériau plus mince et présente des pores évidents. L'existence de la structure poreuse en couche mince peut augmenter considérablement l'immersion de l'électrolyte dans le matériau de l'électrode, réduire la résistance de diffusion et la distance de migration des ions électrolytiques [33].
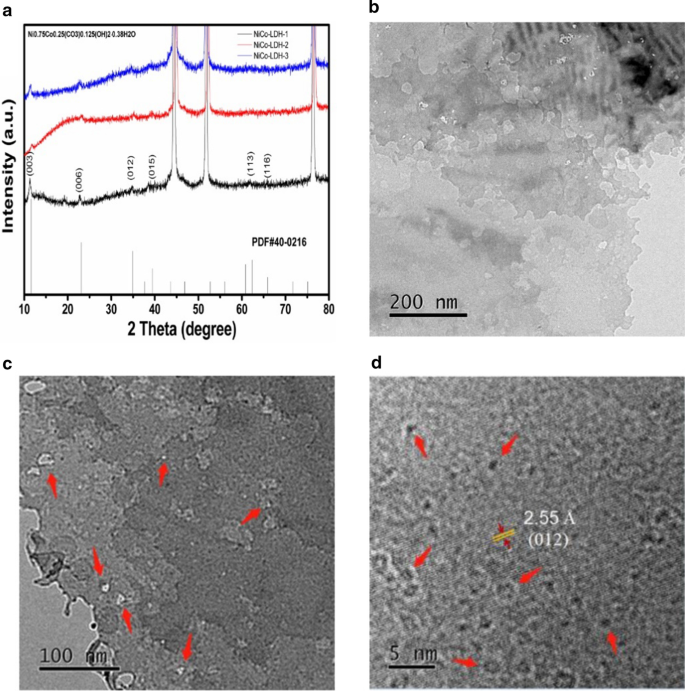
un Diagrammes de diffraction des rayons X des échantillons ; b –d Images MET de NiCo-LDH-1
La figure 3 montre l'analyse XPS du NiCo-LDH-1. Pour le spectre Ni 2p XPS de la Fig. 3a, deux pics principaux sont observés autour de 873,1 et 855,5 eV correspondant à Ni 2p1/2 et Ni 2p3/2 , respectivement. Les pics avec une énergie de liaison à 874,4 et 856,5 eV sont attribués au Ni 3+ , tandis que les pics d'ajustement à 873,1 et 855,3 eV correspondent à Ni 2+ [34, 35]. Pendant ce temps, les pics à 872,1 et 854,2 eV impliquent la présence de Ni 0 qui sont attribués à NF et deux autres pics à 878,8 et 861,2 eV peuvent être attribués aux pics satellites. De même, la figure 3b représente le spectre XPS ajusté de Co 2p, et deux pics principaux situés à 796,1 et 780,8 eV sont indexés sur Co 2p1/2 et Co 2p3/2 , respectivement. Les doublets à 796,9 et 781,5 eV sont en accord avec Co 2+ , tandis que les autres doublets à 795,5 et 780,1 eV sont cohérents avec Co 3+ [35, 36]. Les pics satellites correspondants sont à 784,9 et 803,7 eV. Le spectre O 1 s est illustré à la Fig. 3c, dans laquelle les pics centrés à 529,6, 531 et 532,5 eV doivent être attribués à l'oxygène lié au métal (O1), à l'oxygène défectueux (O2) avec une faible coordination et à l'oxygène dans l'eau (O3) qui est liée physiquement et chimiquement sur et dans la surface, respectivement [35]. Ces résultats montrent que le NiCo-LDH-1 a une distribution riche d'états de valence, ce qui est bénéfique pour l'amélioration des performances électrochimiques.
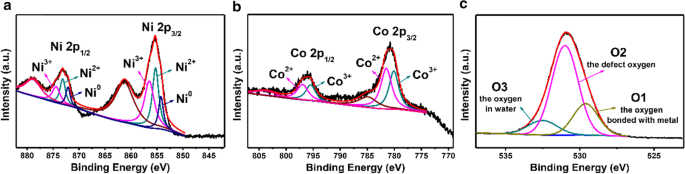
Spectres de photoélectrons aux rayons X de a Ni 2p, b Co 2p et c O 1 s de NiCo-LDH-1
Les diagrammes de cartographie EDS de NiCo-LDH-1 sont illustrés à la Fig. 4a–d. On peut voir sur les figures que les éléments Ni, Co et O sont uniformément répartis sur le matériau, ce qui est conforme aux résultats de XPS.

un SEM de NiCo-LDH-1; Diagrammes de mappage des éléments EDS de b Ni, c Co et d O dans NiCo-LDH-1
Afin de tester les performances électrochimiques des NiCo-LDH, les tests CV, GCD EIS et de stabilité de cycle sont effectués dans un système de test typique à trois électrodes. La figure 5a montre les courbes de voltamétrie cyclique de NiCo-LDH-1 à différentes vitesses de balayage. On peut voir qu'il y a des pics d'oxydation et des pics de réduction évidents observés pour tous les échantillons, et les zones pour les pics anodiques et cathodiques à une vitesse de balayage fixe sont fondamentalement les mêmes, ce qui indique que le matériau de l'électrode a une excellente réversibilité. Les réactions redox peuvent être exprimées sous la forme :
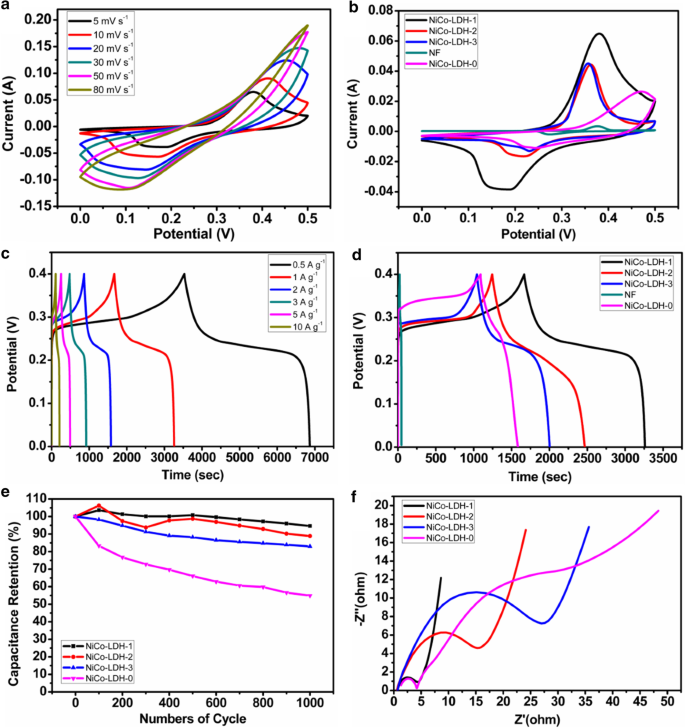
un Courbes CV de NiCo-LDH-1 à différentes vitesses de balayage ; b Courbes CV des échantillons à une vitesse de balayage de 5 mV s −1 ; c Courbes GCD de NiCo-LDH-1 à différentes densités de courant ; d Courbes GCD des échantillons à 1 A g −1 ; e diagramme de stabilité cyclique de NiCo-LDH-1, NiCo-LDH-2, NiCo-LDH-3 et NiCo-LDH-0 à 10 A g −1 ; f Diagrammes de Nyquist de NiCo-LDH-1, NiCo-LDH-2, NiCo-LDH-3 et NiCo-LDH-0
$$\begin{array}{c}{Ni\left(OH\right)}_{2}+{OH}^{-}\leftrightarrow NiOOH+{H}_{2}O+{e}^{-} \end{array}$$ (5) $$\begin{array}{c}{Co\left(OH\right)}_{2}+{OH}^{-}\leftrightarrow CoOOH+{H}_{ 2}O+{e}^{-}\end{array}$$ (6) $$\begin{array}{c}CoOOH+{OH}^{-}\leftrightarrow Co{O}_{2}+{ H}_{2}O+{e}^{-}\end{array}$$ (7)La figure 5b présente les courbes de voltamétrie cyclique des NiCo-LDH à la vitesse de balayage de 5 mV s −1 . On peut voir que les courants de pointe d'oxydation et de réduction du NiCo-LDH-1 sont significativement plus élevés que ceux du NiCo-LDH-2, du NiCo-LDH-3 et du NiCo-LDH-0, et la zone délimitée par la largeur de crête et les intensités de courant de crête des NiCo-LDH augmentent séquentiellement. Selon la littérature précédente [37], l'aire délimitée par la courbe peut refléter la contribution du matériau à la capacité. Plus la zone intégrale enfermée sous la même fréquence de balayage et fenêtre de tension est grande, meilleures sont les performances de capacité du matériau, de sorte que le NiCo-LDH-1 régulé en diminuant la teneur en urée améliore les performances de capacité. De plus, il peut être observé à partir des courbes CV de NF à 5 mV s −1 que l'aire des courbes CV pour NF est négligeable par rapport à d'autres échantillons, ce qui indique que la contribution de capacité de NF est insignifiante.
Les courbes de charge et de décharge galvanostatiques du NiCo-LDH-1 à différentes densités de courant sont illustrées à la Fig. 5c. De toute évidence, NiCo-LDH-1 a une capacité spécifique ultra-élevée de 4166 (1667 C g −1 ) et 3982,5 F g −1 (1593 C g −1 ) à une densité de courant de 0,5 et 1 A g −1 , respectivement. A la forte densité de courant de 10 A g −1 , la capacité spécifique de 2550 F g −1 (1020 C g −1 ) peut toujours être conservé. En comparant avec les résultats de la littérature comme indiqué dans le tableau 1, notre travail est plus avantageux.
La figure 5d représente les courbes de charge et de décharge galvanostatiques des NiCo-LDH sous la même densité de courant et la même fenêtre de tension. On peut observer que lorsque la teneur en urée diminue, les temps de charge et de décharge des NiCo-LDH s'allongent à leur tour. La capacité spécifique passe de 2405 F g −1 (962 C g −1 ) pour le NiCo-LDH-3 à 3052,5 F g −1 (1221 C g −1 ) pour le NiCo-LDH-2 et passe finalement à 3982,5 F g −1 (1593 C g −1 ) pour le NiCo-LDH-1. Il illustre que le changement de teneur en urée a une influence importante sur la réaction redox des matériaux. La raison en est qu'avec une teneur élevée en urée, les NiCo-LDH se développent principalement dans la direction parallèle à la surface NF latéralement, et les couches sont empilées, ce qui augmente l'épaisseur globale des couches, de sorte que l'électrolyte ne peut pas bien pénétrer et redox les réactions résultant de la pseudocapacité ne peuvent s'effectuer que sur ou près de la surface. La diminution de la teneur en urée améliore la dispersibilité du matériau. Les NiCo-LDH se débarrassent progressivement de l'état empilé entre les couches. La structure de croissance tridimensionnelle rend les structures de couches du matériau plus minces et les pores évidents. Cela fournit des sites plus actifs pour la réaction et réduit la résistance à la diffusion et la distance de migration des ions électrolytes, ce qui favorise la transmission et la diffusion des ions, améliorant ainsi considérablement les performances de pseudocapacitance du matériau [36, 44]. Selon la courbe GCD de NiCo-LDH-0, la capacité spécifique de l'échantillon est de 1232,5 F g −1 (493 C g −1 ) à une densité de courant de 1 A g −1 qui est inférieur à ceux des échantillons obtenus avec l'urée. Cela confirme en outre que la structure modifiée, y compris la morphologie et l'épaisseur, causée par l'introduction d'urée a un effet de promotion positif sur les propriétés électrochimiques des NiCo-LDH.
La figure 5e montre la stabilité du cycle des NiCo-LDH. Sous la densité de courant de 10 A g −1 , le taux de rétention de capacité du NiCo-LDH-1 est supérieur à 93,6% après 1000 cycles, supérieur à 88,9% et 83% pour le NiCo-LDH-2 et le NiCo-LDH-3, respectivement. Cependant, le taux de rétention de capacité du NiCo-LDH-0 n'est que de 54,9%. Cela indique que la teneur en urée appropriée peut améliorer efficacement la stabilité des matériaux d'électrode. De plus, pendant les 100 à 500 cycles, la rétention de capacité du NiCo-LDH-1 est supérieure à 100 %, ce qui suggère que la structure de couche verticale plus mince au cours de ce processus de cycle peut suffisamment diffuser l'électrolyte vers la surface proche de la substance active. pour soutenir le processus de réaction redox. La figure 5f est le résultat du test EIS pour les NiCo-LDH. Les tracés de Nyquist sont composés de deux parties :une région à haute fréquence et une région à basse fréquence, correspondant respectivement à un demi-cercle et à une section de ligne. Le diamètre du demi-cercle dans la région haute fréquence reflète la résistance de transfert d'électrons. Plus le diamètre du demi-cercle est petit, plus la résistance de transfert d'électrons sera petite. La pente de la ligne représente la capacité de diffusion des ions électrolytes à la surface du matériau. Plus la pente est élevée, plus la capacité de diffusion sera forte [45]. Pour les échantillons de NiCo-LDH-1, NiCo-LDH-2 et NiCo-LDH-3, lorsque la teneur en urée diminue progressivement, la résistance de transfert et la distance de migration des électrons diminuent pour les électrodes correspondantes, le taux de transmission des ions vers le la surface de l'électrode augmente et la conductivité du matériau s'améliore progressivement. Cependant, pour l'échantillon de NiCo-LDH-0, bien que la résistance au transfert d'électrons soit relativement faible, le taux de transmission des ions est trop lent pour correspondre à la capacité de transmission électronique, ce qui conduit à de mauvaises performances électrochimiques.
L'excellente performance électrochimique du NiCo-LDH-1 comme électrode positive est encore confirmée par la fabrication d'un supercondensateur asymétrique à deux électrodes avec les sphères de carbone comme électrode négative. La figure 6a représente les courbes CV de la sphère de carbone et des électrodes NiCo-LDH-1 à 10 mV s −1 . La sphère de carbone et les électrodes NiCo-LDH-1 avec une fenêtre de potentiel de -1 ~ 0 et 0 ~ 0,5 V peuvent être assemblées dans un dispositif de stabilisation avec une tension étendue de 1,5 V de manière efficace, comme le montrent les courbes CV à 10 mV s −1 de l'appareil sur la Fig. 6b.
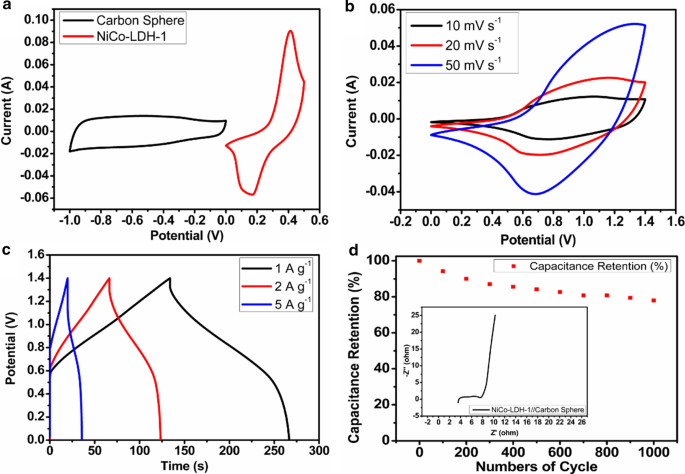
Performances électrochimiques du supercondensateur asymétrique NiCo-LDH-1/carbone :a Courbes CV à une vitesse de balayage de 10 mV s −1 ; b courbes CV sous différentes vitesses de balayage ; c courbes GCD à différentes densités de courant ; et d stabilité cyclique sous la densité de courant de 10 A g −1
Après avoir comparé les Fig. 6a, b, il y a deux distinctions principales observées entre elles dans la fenêtre de potentiel et la forme de la courbe CV. Les causes de ces différences résident dans les aspects suivants :1) Par rapport à l'électrode de référence au calomel saturé, la fenêtre de tension de l'électrode unique NiCo-LDH-1 et sphères de carbone est 0 ~ 0.4 et -1 ~ 0 V dans un trois- système d'électrodes, respectivement. Cependant, après avoir utilisé NiCo-LDH-1 comme électrode positive pour fabriquer un supercondensateur asymétrique à deux électrodes avec les sphères de carbone comme électrode négative, la fenêtre de tension de l'appareil est relative à l'électrode négative (à savoir les sphères de carbone avec la plage de potentiel de -1 ~ 0 V). Ainsi, après avoir équilibré les charges, le dispositif assemblé par deux électrodes avec des processus opposés pourrait fonctionner sous la fenêtre de potentiel de 0 ~ 1.4 V [46]. 2) Comme le montre la figure 6b, les courbes CV du supercondensateur asymétrique montrent une paire de pics distincts sous les différentes vitesses de balayage, ce qui confirme les caractéristiques de pseudocapacitance faradiques typiques apportées par NiCo-LDH-1 [47]. De plus, une courbe CV quasi-rectangulaire plus claire ainsi qu'un processus de charge et de décharge approximativement linéaire sur la Fig. 6b, c pour le supercondensateur asymétrique par rapport à celui de NiCo-LDH-1 confirme en outre l'amélioration de la réactivité de la capacité en raison de l'électricité effet de capacité double couche généré par les sphères de carbone. Ainsi, le supercondensateur asymétrique fabriqué présente une variation de l'apparence de la courbe CV par rapport à l'électrode unique de NiCo-LDH-1 et de sphères de carbone. Ceci résulte de l'unification des supériorités de deux matériaux d'électrode avec divers mécanismes de stockage de charges. Avec cet avantage, la tension de l'appareil peut être améliorée, contribuant ainsi à la promotion des densités de puissance et d'énergie [48].
Les courbes GCD à différentes densités de courant sont présentées sur la Fig. 6c avec la plage de tension de 0 ~ 1,4 V. Selon les calculs, les capacités spécifiques du supercondensateur asymétrique sont de 95 (132,9) et 57 F g −1 (79,75 C g −1 ) sous les densités de courant de 1 et 5 A g −1 , respectivement. La densité énergétique maximale est de 25,9 W h kg −1 à la densité de puissance de 701,6 W kg −1 . Pendant ce temps, la courbe basse fréquence de l'EIS montrée dans l'encadré de la figure 6d est presque verticale, ce qui indique que les ions électrolytes ont une excellente capacité de navette entre les électrodes positives et négatives [49]. La stabilité en cyclage de l'appareil est également évaluée par des tests de charge et de décharge répétés à 10 A g −1 . Comme le montre la figure 6d, la rétention de capacité est supérieure à 78 % après 1 000 cycles.
Conclusions
Une méthode hydrothermale simple et efficace en une étape est utilisée pour synthétiser divers NiCo-LDH. Les nanostructures des NiCo-LDH peuvent être ajustées en optimisant la teneur en urée, améliorant ainsi ses performances électrochimiques en tant que matériaux d'électrode. Les conséquences des caractéristiques structurelles montrent qu'avec la diminution de la teneur en urée, les nanofeuillets NiCo-LDH-1 présentent une dispersité bien améliorée et forment une structure poreuse mince avec une épaisseur de seulement 1,62 nm, ce qui crée des sites plus actifs pour la réaction redox, améliore la l'affinité entre l'électrolyte et le matériau de l'électrode, raccourcit le chemin de diffusion des ions et améliore la capacité de transfert d'électrons. Le NiCo-LDH-1 affiche une excellente capacité spécifique de 3982,5 F g −1 à une densité de courant de 1 A g −1 et au-dessus de 93,6 % de taux de rétention de capacité sur 1 000 cycles sous la densité de courant élevée de 10 A g −1 . L'excellente performance électrochimique du NiCo-LDH-1 est en outre attestée par la fabrication d'un supercondensateur asymétrique à deux électrodes avec des sphères de carbone. La capacité spécifique est de 95 F g −1 à 1 A g −1 , et la rétention de capacité est supérieure à 78% sur 1000 cycles. Ces résultats indiquent que les NiCo-LDH sont le matériau de stockage d'énergie de nouvelle génération avec de grandes perspectives d'application et offrent une grande possibilité pour le développement de supercondensateurs à haute énergie.
Disponibilité des données et des matériaux
Les ensembles de données utilisés et/ou analysés au cours de la présente étude sont disponibles auprès de l'auteur correspondant sur demande raisonnable.
Abréviations
- NiCo-LDH :
-
Hydroxydes doubles couches nickel-cobalt
- TMH :
-
Hydroxydes de métaux de transition
- Non :
-
Nickel
- Co :
-
Cobalt
- NF:
-
Nickel foam
- XRD :
-
X-ray automatic diffractometer
- XPS :
-
Spectromètre photoélectronique à rayons X
- SEM :
-
Microscope électronique à balayage
- TEM :
-
Microscope électronique à transmission
- AFM :
-
Microscope à force atomique
- EDS mapping:
-
Energy-dispersive X-ray spectroscopy element mapping
- CV :
-
Voltammogrammes cycliques
- GCD :
-
Galvanostatic charge–discharge curves;
- EIS :
-
Electrochemical impedance
- ASC:
-
Asymmetric supercapacitor
Nanomatériaux
- Installations d'impression 3D avec des matériaux hautes performances
- Nexam fournira à Diab le Nexamite améliorant les propriétés pour une mousse PET haute performance
- MoS2 avec épaisseur contrôlée pour l'évolution électrocatalytique de l'hydrogène
- Composites de graphène et polymères pour applications de supercondensateurs :une revue
- Fibres de carbone activées avec nanostructure hiérarchique dérivées de déchets de gants de coton en tant qu'électrodes hautes performances pour supercondensateurs
- Nanosphères de carbone monodispersées à structure poreuse hiérarchique comme matériau d'électrode pour supercondensateur
- Aérogel de graphène/polyaniline avec superélasticité et haute capacité en tant qu'électrode de supercondensateur hautement tolérante à la compression
- Nanofeuilles V6O13 interconnectées 3D cultivées sur du textile carbonisé via un processus hydrothermique assisté par des semences en tant que cathodes flexibles hautes performances pour les batter…
- Synthèse hydrothermale de microsphères CoMoO4 comme excellent matériau d'électrode pour supercondensateur



