Le dopage de Mg sur des nanotiges de ZnO a démontré une amélioration de la dégradation photocatalytique et du potentiel antimicrobien grâce à l'analyse d'amarrage moléculaire
Résumé
Diverses concentrations de nanotiges de ZnO dopé au Mg (NR) ont été préparées en utilisant la technique de co-précipitation. L'objectif de cette étude était d'améliorer les propriétés photocatalytiques du ZnO. L'effet du dopage au Mg sur la structure, la constitution de phase, la présence de groupes fonctionnels, les propriétés optiques, la composition élémentaire, la morphologie de surface et la microstructure du ZnO a été évalué avec XRD, FTIR, spectrophotomètre UV-Vis, EDS et HR-TEM, respectivement. Les spectres d'absorption optique obtenus à partir des échantillons préparés ont montré des signes de décalage vers le bleu lors du dopage. Les résultats XRD ont révélé une phase wurtzite hexagonale de nanocomposite avec une diminution progressive de la taille des cristallites avec l'ajout de Mg. La spectroscopie PL a montré l'efficacité de piégeage et la migration des porteurs de charge avec un comportement de recombinaison électron-trou, tandis que le HR-TEM a estimé l'espacement d intercouche. La présence de liaisons chimiques, de modes de vibration et de groupes fonctionnels à l'interface de ZnO a été révélée par les spectres FTIR et Raman. Dans cette étude, les performances photocatalytiques, sonocatalytiques et sonophotocatalytiques des NR préparés ont été systématiquement étudiées en dégradant un mélange de bleu de méthylène et de ciprofloxacine (MBCF). Les résultats expérimentaux suggèrent qu'une amélioration des performances de dégradation a été montrée par les ZnO NR dopés au Mg. Nous pensons que le produit synthétisé dans cette étude s'avérera être un photocatalyseur bénéfique et prometteur pour le traitement des eaux usées. En conclusion, le ZnO dopé au Mg présentait des (p < 0,05) efficacité contre les bactéries gram-négatives (G-ve) par rapport aux bactéries gram-positives (G+ve). Des études d'amarrage moléculaire in silico des NR de ZnO dopés au Mg contre DHFR (score de liaison :-7,518 kcal/mol), DHPS (score de liaison :- 6,973 kcal/mol) et FabH (- 6,548 kcal/mol) de E. coli inhibition prédite d'enzymes données comme mécanisme possible derrière leur activité bactéricide.
Introduction
Les effluents de polluants organiques dans l'eau et les contaminants bactériens infectieux dans les aliments deviennent des défis majeurs qui doivent être surmontés afin de maintenir un environnement sain dans notre environnement [1, 2]. À titre d'exemple, les infections causées par Shigellaflexneri les bactéries causent environ 1,5 million de décès par an en raison de la contamination des aliments et des boissons [3]. Les agents toxiques et cancérigènes présents dans les colorants rejetés dans le milieu aquatique présentent des risques graves pour l'environnement et la santé publique [4]. Ces colorants affectent également l'activité photosynthétique des formes de vie aquatique telles que les cyanobactéries et les algues qui servent à diminuer la transparence de l'eau douce [5].
D'innombrables études expérimentales ont été menées pour développer des méthodes physiques, biologiques et chimiques ainsi que de nouvelles technologies pour l'élimination des colorants des eaux usées. Jusqu'à présent, les méthodes physiques incluant l'ultrafiltration membranaire, l'adsorption et la précipitation [6] et les approches biologiques étaient étudiées. De plus, des procédures de biodégradation ont été utilisées pour la dégradation de la matière organique soluble afin d'éradiquer les bactéries présentes dans les rejets, tandis que les méthodes chimiques comprennent la décoloration photochimique, la chloration et l'ozonation [7]. Les méthodes conventionnelles de traitement des eaux usées, y compris la précipitation chimique, l'adsorption, la coagulation et la séparation, ne sont pas des techniques adaptées car elles nécessitent le transfert de colorants d'un point à un autre et provoquent une contamination secondaire [8]. Par conséquent, les chercheurs recherchent des technologies de traitement respectueuses de l'environnement qui impliquent la dégradation directe des polluants organiques en composés inoffensifs [9].
Récemment, les processus d'oxydation avancée photocatalytique et sonocatalytique (AOP), en présence de nanoparticules semi-conductrices (NP), ont suscité beaucoup d'intérêt en raison de leur stabilité chimique, leur rentabilité et leur non-toxicité [10,11,12]. La photocatalyse est une méthode d'oxydation améliorée, qui implique la génération de porteurs de charge dans un photocatalyseur semi-conducteur lors d'une irradiation lumineuse. Les porteurs de charge photo-générés participent aux réactions d'oxydoréduction et éliminent les polluants de l'eau [13, 14]. Plusieurs études ont montré que OH · les espèces radicalaires s'accumulent sur la surface du photocatalyseur au cours des réactions photochimiques et conduisent à la dégradation de divers colorants organiques. De nos jours, suite à une augmentation de la production d'OH · ions, la synergie de l'irradiation photocatalytique (PCA) et ultrasonore, appelée sonophotocatalyse (SPCA), semble augmenter l'efficacité de dégradation des nanocatalyseurs. En effet, le SPCA a montré un impact bénéfique sur la vitesse de dégradation des composés chimiques dans l'eau qui sont toxiques, dangereux et vénéneux [15]. Actuellement, l'utilisation des NP d'oxydes métalliques pour le traitement des eaux polluées, en raison de leurs avantages en termes de coûts, de respect de l'environnement, de stabilité et de recyclabilité, a suscité l'intérêt des chercheurs [16, 17]. En outre, les semi-conducteurs inorganiques à large bande interdite tels que TiO2 , WO3, ZrO2 et ZnO se sont avérés efficaces dans les processus d'oxydoréduction catalytique induits par la lumière pour dégrader le colorant [18, 19]. Le ZnO, un semi-conducteur à large bande interdite bien connu (Eg =3,37 eV), présente un potentiel extraordinaire en raison de sites de défauts de surface actifs dans les applications PCA, d'une stabilité physicochimique exceptionnelle, d'un potentiel d'oxydoréduction élevé, d'une grande énergie de liaison des excitons (∼60 meV), en plus d'être peu coûteux et non toxique [20,21,22,23]. Parmi divers métaux, le magnésium (Mg) est le dopant le plus fascinant pour synthétiser des nanomatériaux optiques de ZnO fabriqués par Eg. La substitution de Mg dans ZnO est favorisée en raison des facteurs suivants ; (i) constantes de réseau invariantes, (ii) les rayons ioniques sont très proches (Mg +2 =0,72 Å et Zn +2 =0,74 Å), (iii) une solubilité élevée du Mg dans le ZnO, (iv) le ZnO dopé fournit une augmentation de l'intensité de luminescence Eg et UV-Vis, ce qui est utile pour les applications optoélectroniques. De plus, le ZnO dopé au Mg peut servir de photocatalyseur efficace pour la dégradation des colorants et encourager l'agent antibactérien en raison de sa large bande interdite optique [23].
Dans ce travail de recherche, la voie de co-précipitation a été adoptée pour synthétiser des nanocomposites de ZnO dopés au Mg efficaces pour des activités catalytiques et bactéricides. Les échantillons préparés ont été caractérisés par spectroscopie XRD, HR-TEM, EDS, FTIR, UV-Vis et Raman pour une analyse détaillée. L'activité catalytique des échantillons préparés a été étudiée pour la dégradation d'un mélange de bleu de méthylène et de ciprofloxacine (MBCF), tandis que l'activité antibactérienne a été testée contre les bactéries G + ve et G - ve. En outre, des études d'amarrage moléculaire ont été réalisées contre la dihydrofolate réductase (DHFR) et la dihydroptéroate synthase (DHPS) de la voie de biosynthèse du folate et β -cétoacyl-acyl transporteur protéine synthase III (FabH) de la voie de biosynthèse des acides gras.
Méthodes
L'étude actuelle visait à améliorer la dégradation photocatalytique et le potentiel antimicrobien avec une analyse d'amarrage moléculaire de nanotiges de ZnO dopé au Mg.
Matériaux
Nitrate de zinc tétrahydraté (Zn(NO3 ).4H2 O, 99,0%, chlorure de magnésium hexahydraté (MgCl2. 6H2 O, 99,0 % et l'hydroxyde de sodium (NaOH, 99,0 %) ont été reçus de Sigma-Aldrich.
Synthèse d'oxyde de zinc dopé au magnésium (ZnO)
Diverses concentrations de Mg dopé dans une quantité fixe de nanomatériaux de ZnO ont été synthétisées avec la méthode de co-précipitation. 0,5 M de Zn(NO3 ).4H2 Une solution d'O a été utilisée comme précurseur de Zn, et la quantité souhaitée (2, 4, 6 et 8 % en poids) de dopant a été ajoutée en versant du MgCl2 dans la solution. Les solutions préparées ont été agitées dans de l'eau déminéralisée (eau DI) pendant 90 min à 80 °C, tandis que le pH a été maintenu autour de 12 en ajoutant lentement du NaOH (0,1 M) dans la solution agitée. Les précipités obtenus ont été centrifugés à 4000 rpm (20 min), séchés à 100°C pendant 24 heures, puis broyés pour obtenir une poudre fine (Fig. 1).
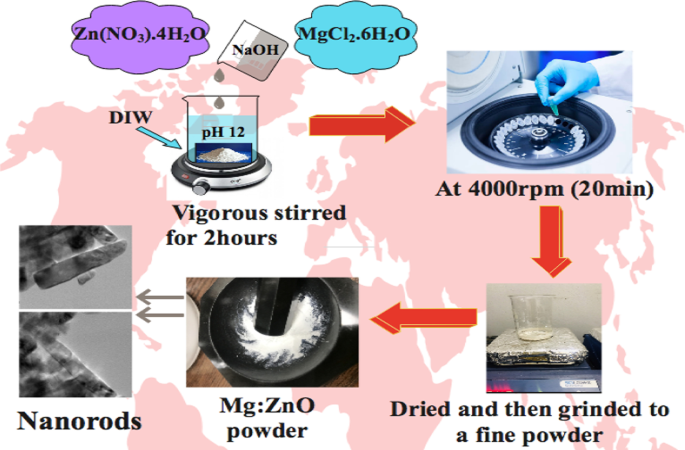
Illustration schématique du stratagème de synthèse de nanotiges de ZnO dopé Mg
Caractérisation des matériaux
Afin d'identifier la constitution de phase et la structure des produits, le diffractomètre à rayons X-XRD PANanalytical X-pert PRO équipé d'un rayonnement CuK alpha (λ = 1.541874 Å) a été utilisé dans la gamme 2θ° (20°–80°) . L'existence de groupes fonctionnels à l'aide du spectromètre PerkinElmer a été vérifiée par FTIR. Avec le spectrophotomètre UV-Vis, des propriétés optiques ont été observées (spectrophotomètre Genesys 10S). Pour acquérir des spectres d'émission de photoluminescence (PL) dans la bande 300-500 nm, le spectrofluoromètre JASCO FP-8200 a été utilisé. Avec la spectroscopie à rayons X à dispersion d'énergie (EDS) utilisant le logiciel INCA EDS, la composition élémentaire a été estimée. Le microscope électronique à balayage (modèle SEM JEOL JSM 6460LV) et le microscope électronique à transmission haute résolution (modèle HR-TEM JEOL JEM 2100F) ont été utilisés pour déterminer la morphologie et la microstructure des échantillons synthétisés.
Activité photocatalytique, sonocatalytique et sonophotocatalytique
L'activité sonocatalytique (SCA) et sonophotocatalytique (SPCA) de la dégradation du MBCF a été testée dans des bains à ultrasons pour les catalyseurs ZnO et Mg:ZnO fonctionnant à une fréquence fixe ~ 35 kHz. De même, sous irradiation de lumière visible, la dégradation photocatalytique a été testée pour les nanocatalyseurs ZnO et Mg:ZnO contre MBCF. Dans chaque expérience, dans 50 ml de colorant modèle, le photocatalyseur (10 mg) a été suspendu et la solution a été placée dans l'obscurité pendant 10 à 15 minutes pour atteindre l'équilibre adsorption-désorption. La lumière visible (photocatalyse—PCA), l'ultra-sonicateur (sonocatalyse—SCA) et l'irradiation combinée à la lumière visible avec ultrasons (sonophotocatalyse—SPCA) ont été méthodiquement placés sous des solutions en suspension. La suspension de 3 ml a été collectée pendant l'exposition pour une analyse d'absorption à intervalles de temps réguliers. Le constituant colorant résultant a été observé en déterminant la différence dans le Àmax = 670 nm de MBCF. La solution de couleur bleue s'est estompée avec le temps en raison de la dégradation du MBCF en présence de nanocatalyseurs. Enfin, le degré de dégradation (Ct/Co), où Ct est la concentration temporelle de colorant et Co est la concentration initiale de colorant, a été évalué. Le pourcentage de dégradation pour chaque échantillon a également été calculé à l'aide de l'équation % Degradation = \(\frac{{\left( {Co - Ct} \right)}}{Co}\) × 100.
Isolement et identification de S. aureus et E. coli
Des échantillons de lait de vache (bovin) testés avec la mammite des champs de surf ont été collectés dans différentes fermes. Les échantillons incubés (cultivés sur 5% de gélose au sang de mouton) ont été striés avec du MSA (Gélose au sel de Mannitol) et du MA (Gélose MacConkey) pour G+ve S. aureus et G-ve E. coli , respectivement (pH ~ 7). Des colonies caractéristiques ont été identifiées par analyse biochimique (test de catalase et de coagulase) et morphologique (coloration de Gram).
Activité antibactérienne
Les performances bactéricides des NR synthétisés ont été examinées sur des souches bactériennes G-ve et G+ve en utilisant une approche de diffusion par puits d'agar en tamponnant 1,5 × 108 CFU/mL de S. aureus et E. coli isolats avec MSA et MA, respectivement. Des puits d'un diamètre de 6 mm ont été formés à l'aide d'un perce-bouchon stérile sur des boîtes de Pétri MSA et MA écouvillonnées. En comparaison avec le contrôle négatif (eau DI) et le contrôle positif (ciprofloxacine), différentes concentrations de Mg:ZnO NR (0,5 mg/50 l) et (1,0 mg/50 l) ont été utilisées. Les boîtes de Pétri contenant la dose ont été incubées (37 ° C) pendant la nuit et les performances antibactériennes des NR ont été enregistrées en mesurant le diamètre des zones d'inhibition avec un pied à coulisse. Au moyen d'une analyse de variance à un facteur (ANOVA) utilisant SPSS 20, l'efficacité statistiquement mesurée en termes de zones d'inhibition a été considérée comme significative.
Études d'amarrage moléculaire
Les études d'amarrage moléculaire in silico étant une approche efficace pour l'identification de la caractéristique structurelle clé derrière l'activité antibactérienne des ZnO NR dopés ont été utilisées pour la prédiction de leur mécanisme possible. Les enzymes clés de la voie de biosynthèse du folate, à savoir la dihydrofolate réductase (DHFR) et la dihydroptéroate synthase (DHPS) aux côtés de β -cétoacyl-acyl transporteur protéine synthase III (FabH) enzyme de la voie de biosynthèse des acides gras, ont été signalés comme une cible attrayante pour la découverte d'antibiotiques. Les caractéristiques structurelles 3D des enzymes sélectionnées ont été extraites de la banque de données de protéines et préparées à l'aide d'un outil de préparation de protéines pour l'amarrage des ZnO NR dopés au Mg à l'intérieur du site actif.
Le code d'accession pour les cibles sélectionnées était le suivant :2ANQ (DHFRE.coli ) [24], 5U0V (DHPSE.coli ) [25] et 4Z8D (FabHE.coli ) [26]. Des études d'amarrage moléculaire ont été réalisées à l'aide du logiciel ICM Molsoft (Molsoft L.L.C., La Jolla, CA) [27] où les structures des protéines ont été optimisées grâce à un outil de minimisation d'énergie. Les molécules d'eau de la structure cristalline aux côtés du ligand co-cristallisé ont été retirées, suivies de l'ajout d'atomes H polaires pour la préparation de la structure des protéines, et une grille a été utilisée pour identifier la poche active. Enfin, les meilleurs complexes amarrés ont été sélectionnés pour l'analyse des interactions de liaison afin d'observer les acides aminés clés impliqués dans la liaison du ligand. Le visualiseur Discovery Studio et Pymol ont été utilisés pour l'analyse des complexes ancrés.
Résultats et discussion
Les propriétés structurelles et la constitution de phase de ZnO sans dopant et dopé ont été évaluées en utilisant la diffraction des rayons X (Fig. 2a). Les pics observés à 31,7°, 34,5°, 36,3°, 47,5°, 56,6°, 62,9° et 68,0° peuvent être attribués aux plans de diffractions (100), (002), (101), (102), (110), ( 103) et (112) qui ont confirmé que le ZnO a une structure hexagonale (JCPDS n° 361451) avec le groupe spatial P63mc. Deux pics reflètent les impuretés des composés comprenant du zinc-carboxyle (marqués par des flèches noires). Ces traces zinc-carboxyle pourraient être apparues en raison de la réaction du précurseur de Zn avec d'autres réactifs au cours de la synthèse [28]. La taille des cristallites de ZnO était de 26 nm estimée à l'aide de la formule de Scherrer, qui diminuait progressivement jusqu'à 23 nm avec une quantité croissante de dopant (à 8 % en poids). Pour garantir l'ajout réussi de « Mg » dans le réseau de l'hôte, trois plans de positions de pics proéminents (100), (002) et (101) ont été suivis [23]. On pense que les pics de ZnO se déplacent vers 2θ élevés lors du dopage au Mg, tandis que plusieurs études rapportent une réduction progressive de la taille des cristallites avec l'ajout de dopants tels que Mg, Fe et Al au ZnO [29, 30]. Plusieurs facteurs, y compris la contrainte de compression causée par la différence entre les rayons ioniques du Zn et l'ion dopant, l'obstruction de la croissance cristalline et/ou la génération de défauts dans les cristaux lors du dopage pourraient supprimer la croissance du ZnO. Le décalage des pics observé pour les NR de ZnO dopé pourrait être attribué aux ions Mg qui ont remplacé les ions Zn en raison de la différence de rayons ioniques entre Mg 2+ (0,57 ) et Zn 2+ (0,60 ) [23, 29].

un Modèle XRD de ZnO dopé au Mg, b–d Modèle SAED de ZnO, 4%, 8% de ZnO dopé Mg et e Spectres FTIR, respectivement
Les motifs SAED de ZnO dopé affichaient des points brillants dus à la diffraction des électrons. Chaque tache provenait d'un ensemble de plans parallèles trouvés dans la structure cristalline du produit synthétisé qui affectait la condition de diffraction de Bragg. Les indices de Miller ont été attribués en conséquence, comme le montre la figure 2b–d. Les motifs ont été indexés avec des plans (002), (100), (101) et (102) connectés à la structure hexagonale de ZnO avec un faisceau d'électrons se projetant le long de l'axe de la zone [101] [31]. En général, la direction de croissance anisotrope du ZnO est déterminée à la fois par l'énergie libre interfaciale et le potentiel de dissolution de l'eau. La vitesse relative de la croissance des différents plans contrôle également la croissance. La croissance est également contrôlée par la vitesse de croissance relative des différents plans [32].
Une analyse FTIR a été réalisée pour étudier la présence de groupes fonctionnels, la chimie de surface et les modes de vibrations pour les liaisons chimiques existant dans les échantillons (Fig. 2e). Bandes de 400 à 560 cm -1 sont désignés pour l'étirement des modes vibrationnels Zn–O–Zn qui ont confirmé la formation de ZnO. Les bandes de la région des basses fréquences/empreintes digitales ont été attribuées aux vibrations translationnelles M–O (590, 670 cm −1 ) et O–M–O (430 cm −1 ) [33]. Avec une concentration croissante de Mg, aucun changement significatif n'a été observé dans la bande d'absorption de Zn-O et l'intensité. Bande à 1651 cm -1 correspond au mode d'étirement symétrique C=O qui est fortement intensifié avec l'augmentation du pourcentage de charge de nitrate de magnésium, tandis que ~ 1362 cm -1 La bande correspond au mode d'étirement asymétrique C–O. Le carbone des matières premières pourrait avoir été incorporé dans les NR par inadvertance, alors qu'apparition d'une large bande de transmission à 3456 cm -1 correspond à l'étirement O–H des molécules d'eau adsorbées en surface [34].
Afin de vérifier le changement de comportement d'absorption lors du dopage, la spectrométrie UV-Vis a été déployée pour les échantillons dopés et non dopés. Les spectres d'absorption UV-Vis des NR synthétisés ont été enregistrés dans la plage de 250 à 600 nm en fonction de la longueur d'onde (Fig. 3a). Les échantillons ont montré une absorption maximale autour de 370-395 nm, avec un décalage du bord d'absorption vers une longueur d'onde inférieure à différentes concentrations de dopage. Cette augmentation de l'absorption et du déplacement lors du dopage se manifeste par un manque d'oxygène, un effet granulométrique et des défauts de structure des grains [35]. Les valeurs extraites de la figure 3a ont été utilisées pour calculer la bande interdite optique (Eg) de ZnO (en utilisant le tracé de Tauc), qui est passée de 3,32 à 3,72 eV lors du dopage au Mg (Fig. 3b) [36, 37]. Ce décalage vers le bleu dans Eg peut être confirmé par le phénomène d'effet Burstein-Moss. Dans la méthode des oxydes métalliques, il est rapporté que la réduction de la taille des particules entraîne un décalage vers le bleu de la bande interdite en raison de l'effet de confinement quantique (QCE). Cependant, QCE n'est pas la seule raison; le dopage peut également affecter la symétrie locale et générer des centres de défauts du réseau qui modifient la structure de la bande et induisent des changements significatifs dans les propriétés optiques [38]. Comme décrit précédemment dans l'analyse XRD, le Mg dopé dans le ZnO génère des lacunes d'oxygène dans le cristal hôte, qui agissent comme des donneurs dans le système et se comportent comme des ions chargés positivement en libérant des électrons vers le CB. Comme la concentration des porteurs d'électrons dépasse la densité d'états dans le CB, le niveau d'énergie de Fermi est poussé dans le CB. Zn 2+ remplacer par Mg 2+ conduit à l'augmentation de la concentration d'électrons et de la lacune d'oxygène en raison des rayons ioniques et de la différence d'électronégativité des deux matériaux, et ainsi, l'augmentation de la densité de porteurs ouvre la voie à l'élévation du niveau de Fermi au semi-conducteur dégénéré CB car ZnO est l'un des semi-conducteurs les plus dégénérés . En raison de cette action, le niveau de Fermi ainsi que sa position dépendent de la concentration d'électrons libres et de l'excitation des électrons du niveau VB au niveau de Fermi, entraînant l'augmentation de la densité d'électrons libres et l'élargissement de la bande interdite [39]. Ce décalage Burstein-Moss contribue à l'élargissement observé par Eg des NR de ZnO dopé Mg.
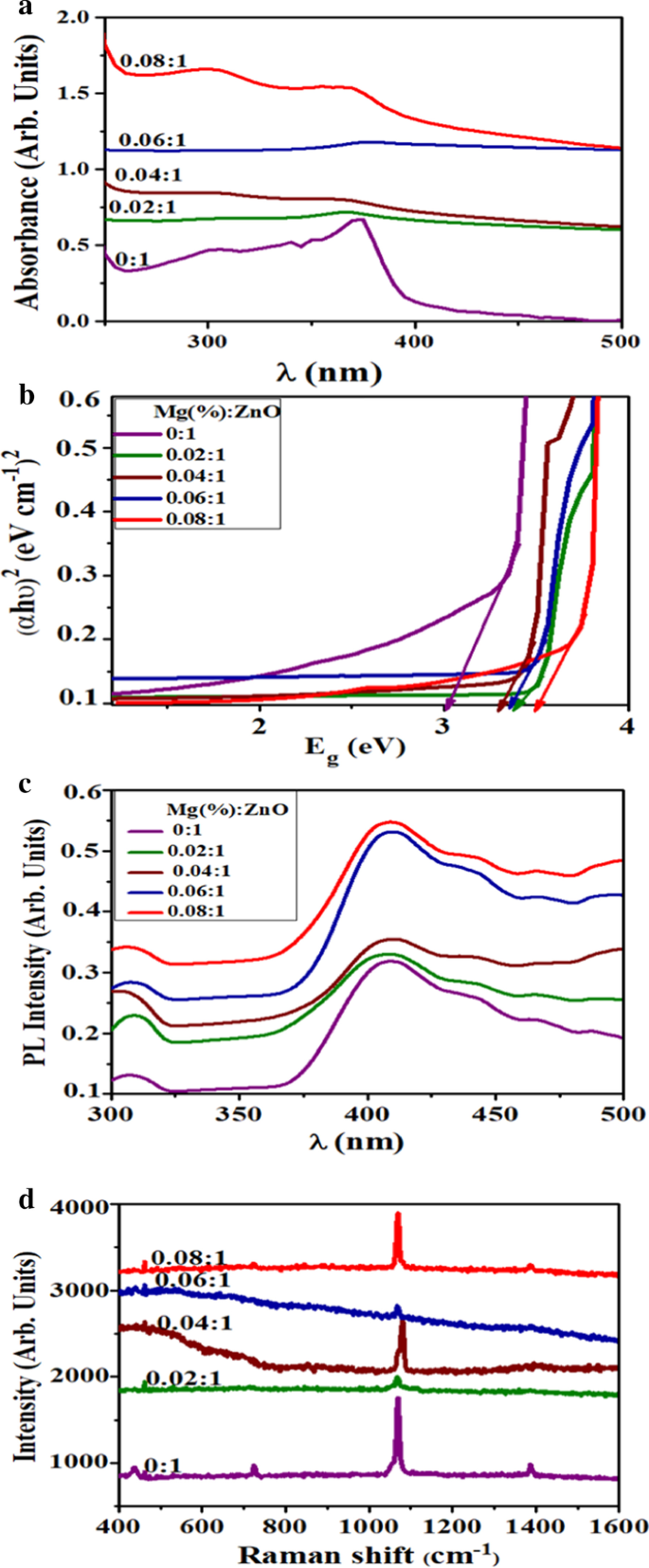
un Spectres d'absorption d'échantillons de ZnO dopé Mg, b Parcelle du Tauc, c Spectres PL et d Spectres Raman de nanotiges de ZnO dopé Mg
L'analyse PL est un outil précieux pour obtenir de meilleures informations sur les impuretés, les transitions et les dopants en étudiant les spectres d'émission. Les effets de taille quantique affectent les propriétés physiques des matériaux semi-conducteurs à l'échelle nanométrique, comme le ZnO a modifié son comportement optique par l'augmentation du confinement quantique observé à partir de PL [40]. Les spectres PL de diverses concentrations de Mg incorporé dans ZnO ont été mesurés avec une excitation ~ 325 nm à température ambiante (Fig. 3c). Pour le ZnO non dopé et dopé, un large niveau profond et des émissions proches de la bande ont été détectés. Tous les échantillons ont montré un pic d'émission dans la région UV, qui est attribué à la recombinaison des excitons. Les pics observés dans la région visible apparaissent en raison d'états défectueux (donneur), tels que O2 postes vacants-Vo , Zn interstitiels-Zni , états de défaut (accepteur) à partir des lacunes de zinc-Vz et interstitiels d'oxygène-Oi [39]. Le rapport d'intensité des pics dans les régions UV et visible est principalement affecté par la qualité cristalline des matériaux dopés, car la densité des défauts diminue avec l'amplification de la cristallinité. Les échantillons ont montré des pics d'émission autour de 408 nm, attribués à la transition NBE-NBE proche de la bande de ZnO [39]. Les pics trouvés à 408, 442, 467, 488 nm conduisent à une émission bleue et attribuables aux interstitiels Zn ont une émission violette majeure à 408 nm. Les faibles émissions observées à 442, 467 et 488 nm sont associées à une recombinaison de paire donneur-accepteur (D/A) qui implique différents niveaux de défauts dans les échantillons. L'émission à 488 nm est due aux électrons dans O2 ionisé simple vacance avec trous photo-excités dans le VB [41]. L'intensité de l'émission de large niveau profond a augmenté lors du dopage, tandis que les pics d'émission de NBE ont été transférés vers une région d'énergie plus élevée. Ce décalage vers le bleu de l'émission de NBE pourrait être interprété sur la base de l'effet Burstein-Moss. Le ZnO est un matériau de type n, et lors d'un dopage important, son niveau de Fermi se déplace à l'intérieur de la bande de conduction. Ainsi, l'absorption doit afficher un décalage vers le bleu comme proposé par Burstein; les régions remplies bloqueraient les excitations optiques ou thermiques [42]. Une augmentation de l'intensité PL a été observée pour les échantillons dopés, ce qui implique une efficacité de transfert d'électrons réduite.
La diffusion Raman est une technique sensible et non destructive pour étudier la microstructure et analyser les propriétés liées aux états vibrationnels des nanomatériaux. L'oxyde de zinc wurtzite avec une cellule primitive contenant deux unités de formule est placé dans le groupe d'espace C6ν. Les phonons optiques présents au niveau de la cellule primitive dans l'espace réciproque sont justifiés par une relation irréductible :Гopt =1A1 +2B1 + E1 +2E2 où B1 représente les modes silencieux Raman, tandis que A1 et E1 sont des modes polaires (forces de Coulomb à longue portée), qui sont divisés en phonons optiques longitudinaux (LO) et optiques transverses (TO). De plus, un mode phonon double fréquence E2 (non polaire), ayant E2 (faible) et E2 (élevé), correspond au sous-réseau Zn et O2 atomes [43]. Dans les spectres Raman, les pics qui se déplacent vers des nombres d'ondes plus élevés et plus bas dépendent des longueurs de liaison variables entre les molécules. L'augmentation de la longueur de liaison régit le passage vers un faible nombre d'ondes et vice versa. Aucun autre pic d'ordre élevé n'a été observé au-dessus de 1 300 cm -1 (Fig. 3d). Pic dominant observé à ~ 1069 cm -1 représente E2 Mode H (caractéristique) du ZnO hexagonal [44]. De plus, trois pics mineurs ont également été observés vers 436, 723 et 1386 cm −1 qui provient d'un fond fluorescent élevé. De plus, le spectre Raman de 8 % en poids de ZnO dopé était décalé vers le bleu, ce qui est attribué à la substitution de Mg 2+ avec Zn 2+ dans le réseau ZnO qui jouerait un rôle dans la dynamique du réseau [45]. Habituellement, les décalages de pic Raman se produisent pour trois raisons :les effets de confinement des phonons, la déformation du réseau et les lacunes en oxygène. Les spectres acquis à partir de la spectroscopie XRD et Raman ont confirmé que la structure wurtzite-ZnO n'est pas affectée par l'incorporation de Mg ; cependant, la qualité du cristal est considérablement réduite.
Pour la confirmation morphologique du ZnO non dopé et dopé, une HR-MET a été réalisée (Fig. 4a-e) pour délimiter la morphologie en forme de tige hexagonale du ZnO:Mg. Il semble que Mg ait montré le rôle de la nucléation lors de sa croissance avec le dopage [39]. Les valeurs d'espacement d intercouches pour le ZnO non dopé et dopé ont été calculées ~ 0,464, 0,183, 0,333, 0,27 et 0,232 nm d'images HR-TEM (Fig. 4a′–e′). Les valeurs d'espacement d sont bien en accord avec les plans obtenus avec l'analyse XRD. Aucune présence d'impuretés/phases secondaires ne suggère une incorporation adéquate d'atomes de dopant dans les nanotiges de ZnO sans agrégation [46]. De plus, la modification de l'espacement d a été attribuée à l'incorporation de Mg dans les réseaux de ZnO.
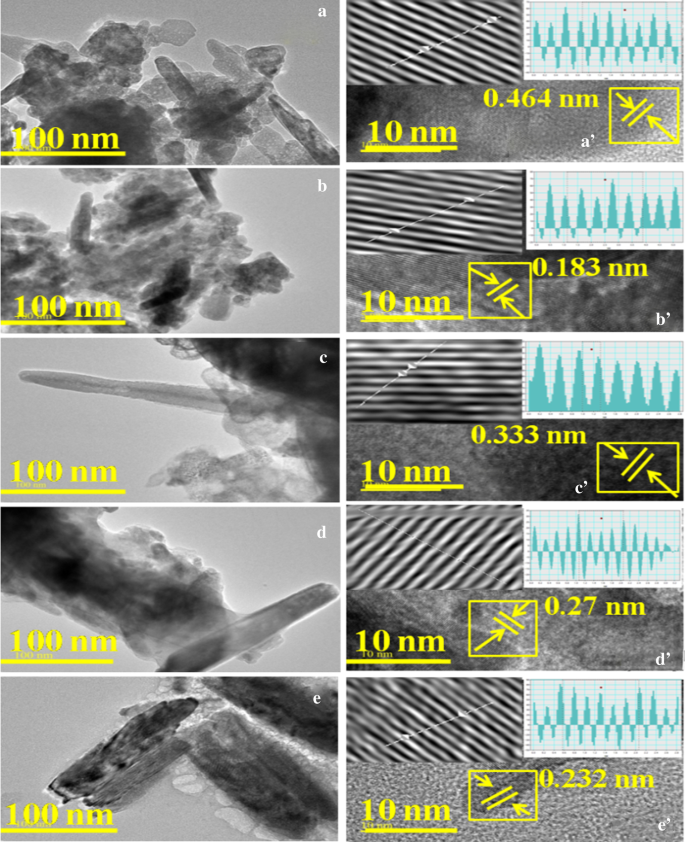
a–e Images HR-TEM de diverses concentrations de ZnO dopé au Mg et espacement d calculés à l'aide d'images HR-TEM de Mg-ZnO a ′–e ′ avec teneur en Mg (2, 4, 6 et 8 % en poids)
L'analyse élémentaire a été réalisée à l'aide d'EDS pour confirmer la présence de zinc et d'oxygène dans les nanopoudres de ZnO (Fig. 5a–e). Le rapport atomique moyen (67,6:23,6) a confirmé quantitativement la formation de ZnO avec le dopant. Des pics d'or (Au) apparaissent dans les spectres en raison du revêtement d'or pulvérisé sur l'échantillon pour réduire l'effet de charge. Les pics de Cu peuvent provenir de la bande de Cu utilisée avec le porte-échantillon. Certains pics supplémentaires (Cl, Si) peuvent indiquer une contamination. Le pic de Na peut provenir de NaOH qui a été utilisé pour maintenir le pH basique pendant la synthèse. Cependant, le pic Na chevauche le Zn, de sorte que sa présence dans l'échantillon ne peut pas être vérifiée.
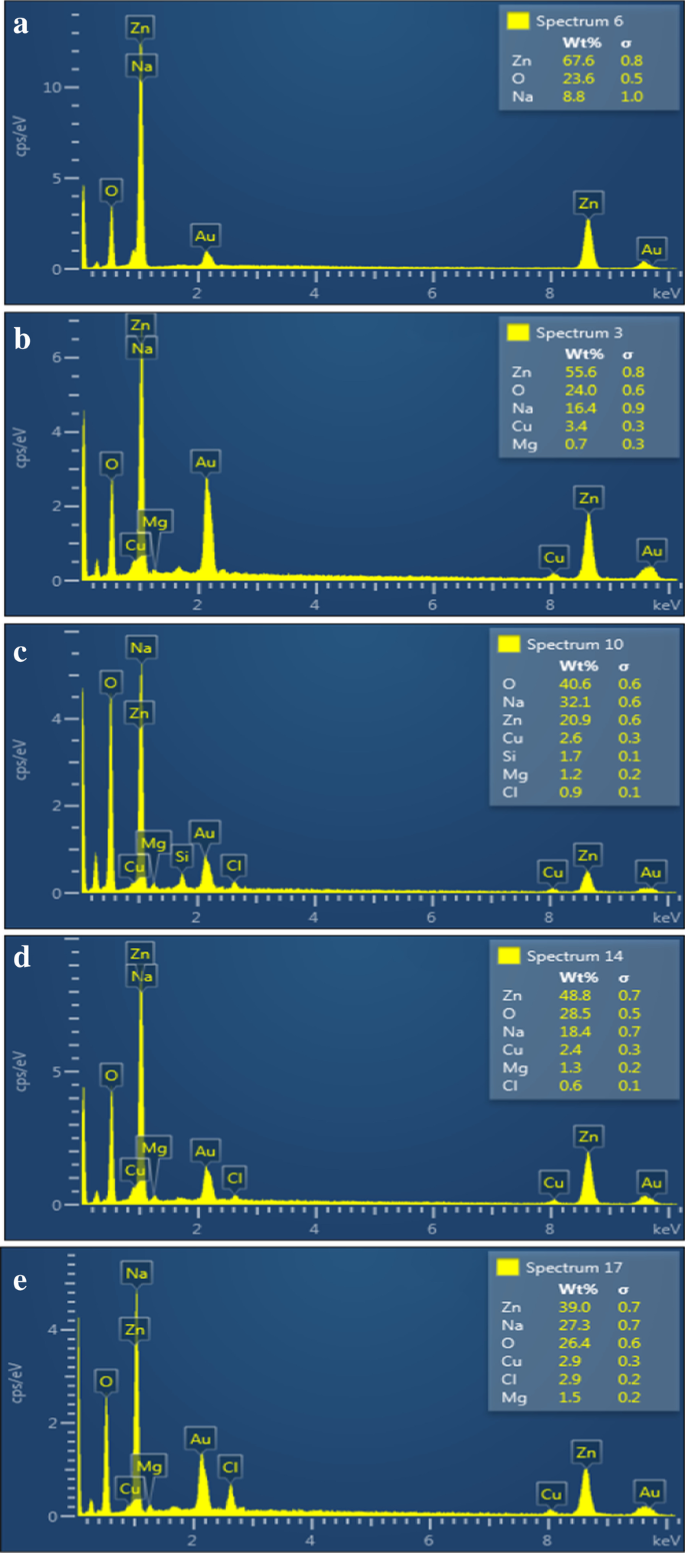
un Analyse EDS de ZnO et de diverses concentrations (2, 4, 6 et 8% en poids) de ZnO dopé Mg (b–e ), respectivement
Le processus photocatalytique implique la génération de paires électron-trou (e-, h +) avec séparation et recombinaison successives des électrons et des trous (Fig. 6), démontrant la réaction redox suivante [35].
$$\begin{aligned} &{\text{ZnO}} + h\nu \to {\text{ZnO}}\,({\text{e}}_{{{\text{CB}}}} + {\text{h}}_{{{\text{VB}}}} ) \\ &{\text{e}}_{{{\text{CB}}}} + {\text{O} }_{2} \to {\text{O}}_{2}^{\cdot - } \\ &{\text{O}}_{2}^{\cdot - \,} + {\text {colorant}}\,{\text{degraded}}\,{\text{products}} + {\text{CO}}_{2} + {\text{H}}_{2} {\text{ O}} \\ &{\text{OH}}^{\cdot} + {\text{colorant}}\,{\text{degraded}}\,{\text{products}} + {\text{CO }}_{2} + {\text{H}}_{2} {\text{O}} \\ \end{aligned}$$
Illustration schématique du mécanisme de photocatalyse de nanotiges de ZnO dopé Mg
Tous les échantillons préparés ont été évalués pour leurs activités photocatalytique, sonocatalytique et sonophotocatalytique contre MBCF en tant que contaminant ciblé. Les profils de dégradation du colorant MBCF photocatalysé sous irradiation de lumière UV par des nanocatalyseurs synthétisés sont affichés sur les figures 7a–c.
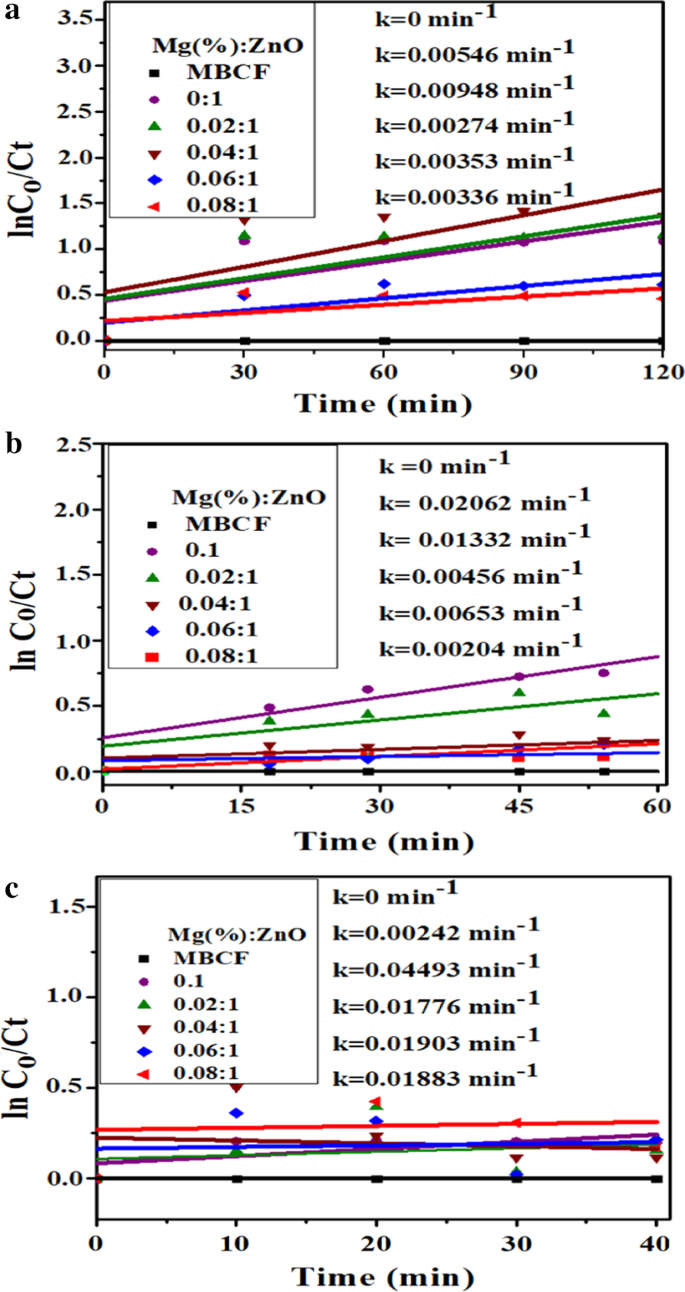
un Photocatalyse, b sonocatalyse et c cinétique de réaction de sonophotocatalyse de la dégradation du colorant MBCF pour les nanotiges de ZnO dopé Mg
La k (constante de vitesse) basée sur la cinétique de pseudo-premier ordre a été déterminée en traçant des courbes linéaires de ln(Ct/Co), en fonction du temps d'exposition t. La constante de vitesse de dégradation k pour le ZnO non dopé et dopé (2, 4, 6 et 8 % en poids) a été calculée comme étant de 0,00546, 0,00948, 0,00274, 0,00353 et 0,00336 min −1 , respectivement (Fig. 7a). Le ZnO dopé s'est avéré avoir une meilleure efficacité photocatalytique que le ZnO pur avec une dégradation maximale de 26 % pour le ZnO dopé (8 % en poids) (Fig. 8a–c). En raison de la présence de lacunes en oxygène à la surface, l'augmentation de la surface était l'explication de l'augmentation de l'activité photocatalytique du ZnO dopé [35]. Le transfert photo-induit d'électrons dans le CB d'un semi-conducteur avec des trous positifs laissés dans VB est le mécanisme fondamental de la photocatalyse [15]. Jusqu'à ce que les excitons soient annihilés, ils participent à des réactions d'oxydoréduction avec les molécules de colorant environnantes à la surface des catalyseurs, ce qui entraîne des produits dégradés. Les électrons photo-induits agissent comme un agent réducteur puissant, qui interagit avec l'O2 environnant molécules pour générer du O2 réactif ·− espèce. D'autre part, les trous photo-induits agissent comme un puissant agent oxydant qui génère des OH · hautement réactifs. espèces de groupes hydroxyle. L'espèce radicale résultante (O2 ·− et OH · ) interagissent avec les molécules de colorant environnantes pour les dégrader en produits ou minéraux non toxiques.
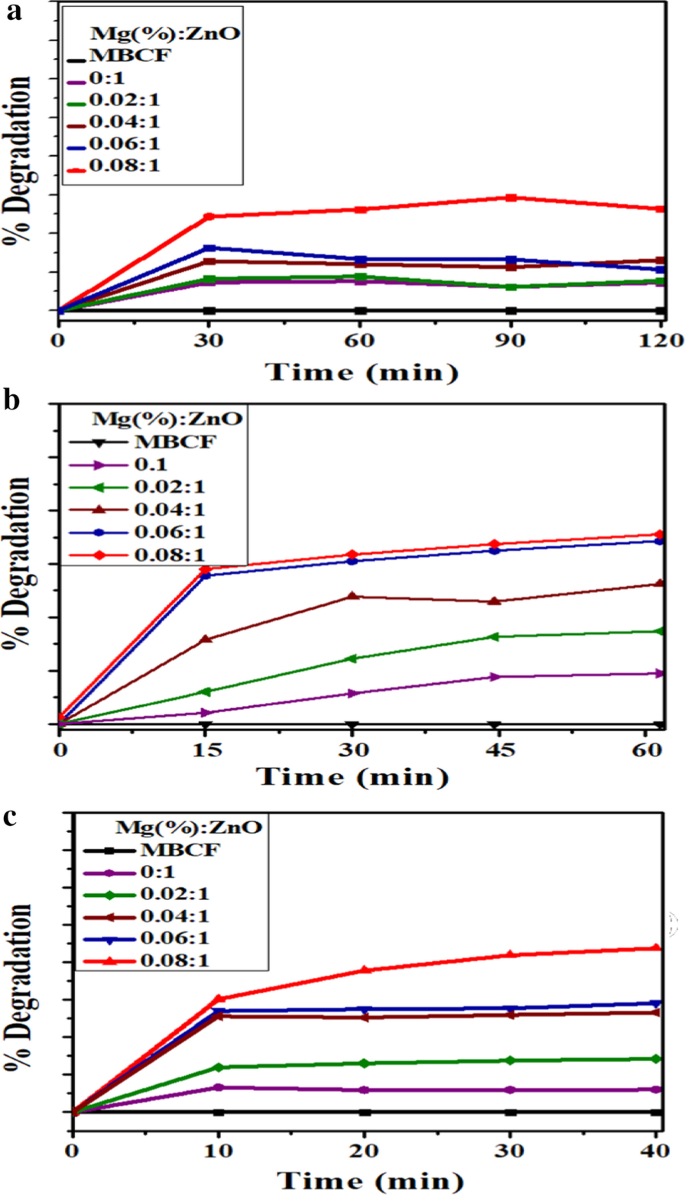
un Photocatalyse, b sonocatalyse et c photodégradation par sonophotocatalyse du MBCF pour nanotiges de ZnO dopé Mg
Une autre approche pour une dégradation efficace des déchets organiques dans l'eau est la sonocatalyse (SC) [15]. L'influence des ondes ultrasonores sur la dégradation du MBCF a été étudiée avec du ZnO non dopé et dopé. (Fig. 7b). En termes de concentration de colorant MBCF, la dégradation SC du MBCF par le ZnO dopé a suivi une cinétique de pseudo-premier ordre. Les constantes de vitesse de dégradation du ZnO non dopé et dopé (2, 4, 6 et 8 % en poids) étaient de 0,02062, 0,01332, 0,00456, 0,00653 et 0,00204 min −1 , respectivement. Plusieurs études ont été récemment rapportées sur la dégradation des colorants SC, basée sur le mécanisme des points chauds et la sonoluminescence, en présence de divers catalyseurs. La formation de bulles de cavitation en solution peut être stimulée en créant des points chauds par nucléation asymétrique des bulles. Ces points chauds peuvent déclencher la formation de OH par H2 O molécules à pyrolyser. Le mécanisme sonochimique nécessite généralement une sonolyse de l'eau, qui est le solvant sous haute pression et température dans les bulles de cavitation qui s'effondrent. In MBCF and nanocatalyst solution, ultrasonic waves not only cause water sonolysis, but also catalyst couple to create charge carriers. OH radicals and superoxide anions · O 2− can be generated by electron–hole pairs, which decompose dyes into non-toxic species [15, 47]. Sonophotocatalysis (SPC) also appears to follow pseudo-first-order kinetics, similar to photocatalysis and sonocatalysis. Degradation rate constants for undoped and doped ZnO (2, 4, 6 and 8 wt %) were 0.00242, 0.04493, 0.1776, 0.01903 and 0.01883 min −1 , respectively (Fig. 7c). Degradation performance of doped ZnO was 12, 29, 53, 58 and 87%, respectively (Fig. 8c).
These results suggest that doping plays a crucial role in the efficiency of ZnO photocatalytic. At identical operating conditions, SPC has a higher degradation rate than the corresponding individual mechanisms. The combined process reaction rate constant is greater than the sum of individual processes' rate constants, i.e., photo of Ksono > Kphoto + Ksono, which can be attributed to (i) increase in OH production in mixture, (ii) raised transfer of mass between solution and catalyst surface, and (iii) enhanced activity related to ultrasound disaggregation, consequently enhancing the area of surface [15, 48]. In order to estimate the reusability as well as sample steadiness, Fig. 9a indicates that photocatalytic switches off MBCF colorant degradation under similar conditions after back to back (four cycling experiments). In this way, sample’s degradation efficiency reduced from to 82 to 75%. Herein (Fig. 9b), there is some depletion of nanomaterial by centrifugation or washing while doing recycling experiment. Following the recycling results, it was concluded that the product lasts stable and possesses remarkable ability and acceptance for dangerous wastewater treatment. Anyhow, Table 2 shows the comparison of photocatalytic degradation efficiency of present work with other reported materials.
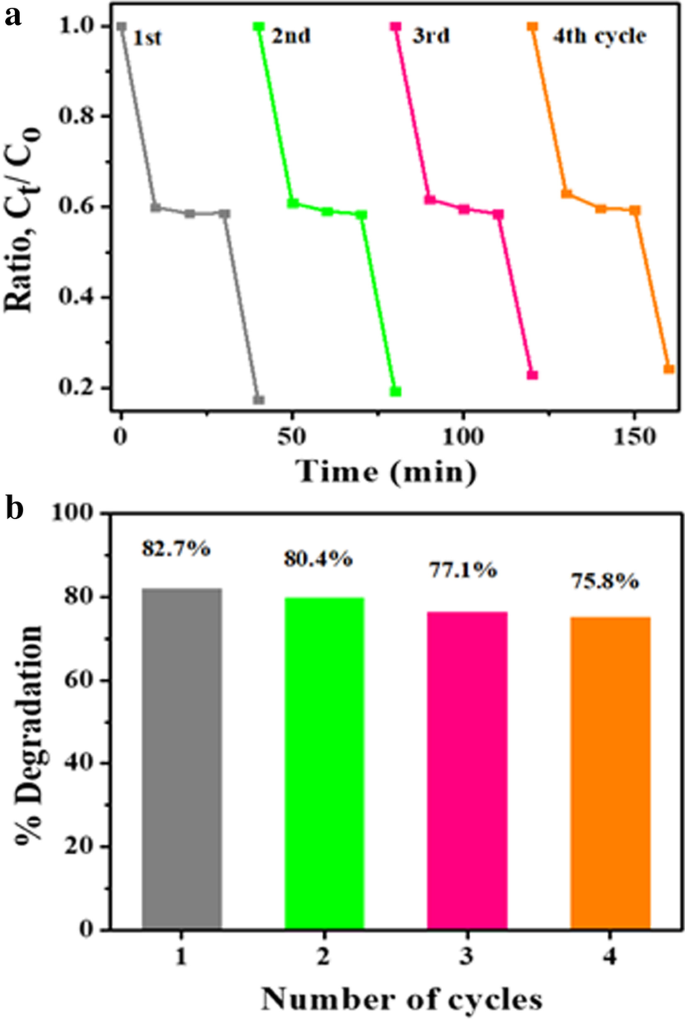
un Photocatalysis reusability performance of Mg-doped ZnO and b %degradation bar graph
In vitro bactericidal action of undoped and doped ZnO NRs for G-ve and G+ve bacteria is given in Table 1. Results depict improved bactericidal synergism and action of doped ZnO against E. coli in contrast to S. aureus . Inhibition zones were recorded as (1.05–2.05 mm) and (2.10–4.15 mm) for S. aureus and (0–6.15 mm) to (0–8.65 mm) for E. coli , respectively, while ZnO showed negligible efficacy for E. coli as compared to S. aureus . Moreover, control + ve depicted inhibition zone (9.00 mm) against E. coli et S. aureus parallel to control -ve (0 mm). Overall, Mg-doped ZnO exhibited substantial (P < 0.05) efficacy against G-ve as compared to G+ve bacteria.
Oxidative stress induced by prepared doped ZnO depends upon concentration, shape and size of NRs, while increment in NRs size reduces antibacterial activity. Nanosized rods generate oxygen species (ROS) to produce bacterial cell membrane as a result of extrusion of cytoplasmic content, which cause bacteria death as shown in Fig. 10. Another possible phenomenon involves strong interaction between negatively charged cell membrane and cations (Mg 2+ et Zn 2+ ) that results in crumbling of micro-pathogens [49].
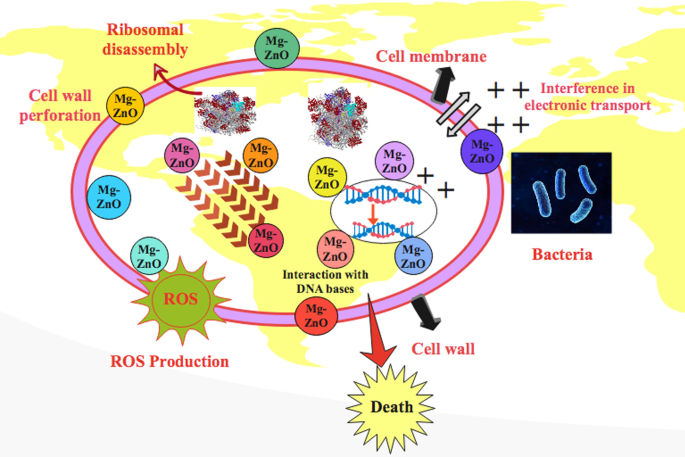
Schematic illustration of bactericidal mechanism of Mg-doped ZnO nanorods
Drug resistance has been considered as major threat to mankind, and there is continuous need for discovery of more compatible antibiotics. Bactericidal activity of metal NRs is well documented, and their role as possible candidate for new antibiotic discovery has been suggested previously [50]. In silico molecular docking studies facilitate to get insight into mechanism behind their antibacterial activity. Dihydrofolate reductase (DHFR) and dihydropteroate synthase (DHPS) enzyme belonging to folate biosynthetic pathway have been reported as well-known target for trimethoprim and sulfonamide drugs, respectively [51, 52]. Here, we evaluated binding tendency of Mg-doped ZnO NRs against DHFR, DHPS and FabH enzymes from E. coli . Docked complexes revealed their binding pattern inside active site and suggested them as possible inhibitor against selected enzyme targets.
For DHFRE.coli , the best docked complex revealed H-bonding interaction with Ile94 (3.1 Å), Tyr100 (3.1 Å) and metal–contact interaction with Met20 and Ala7 with overall binding score -7.518 kcal/mol. Binding interactions with key amino acids of active pocket and orientation of Mg-doped ZnO NP are depicted in Fig. 11a.

Binding interaction pattern of Mg-doped ZnO NRs inside active pocket a Dihydrofolate reductase (DHFR), b Dihydropteroate synthase (DHPS) from E. coli
For DHPSE.coli , docking complexes showed H-bonding with Leu21 (3.1 Å), Asp56 (3.4 Å), Gly59 (2.9 Å), Thr62 (2.8 Å) and Arg255 (2.8 Å). In addition, the Asn22 and Ile20 interacted with NRs through metal contact inside active site as shown in Fig. 11b. These Mg-doped ZnO NPs blocked active site (binding score:-6.973 kcal/mol) and are suggested to be possible inhibitors against DHPS enzyme.
Similarly, docking of Mg-doped ZnO NRs against the β -ketoacyl-acyl carrier protein synthase III (FabH) enzyme of fatty acid biosynthetic pathway showed H-bonding interaction with Glu302 (3.3 Å), Leu220 (2.9 Å), Thr254 (3.2 Å), and Gln245 (2.7 Å) having binding score -6.548 kcal/mol (Fig. 12). Furthermore, Mg-doped ZnO NPs involved metal contact interaction with Ile250 and His241.
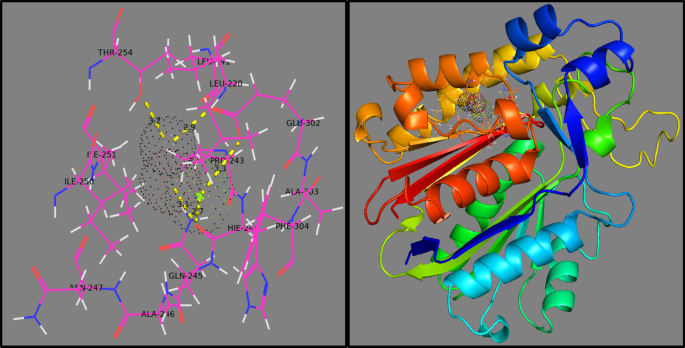
Binding interaction pattern of Mg-doped ZnO NRs inside active pocket β -ketoacyl-acyl carrier protein synthase III (FabH) from E. coli
Blockage of active site through binding of ligands prevents entry of substrate and thus leads to loss of enzyme activity. Owing to better antibacterial activity of Mg-doped ZnO NRs against E. coli as compared to S. aureus , in silico predictions against selected enzyme targets revealed their possible binding patterns inside active pocket and suggested them potential inhibitors of given enzymes.
A comparison of present sonophotocatalytic study with the literature is shown in Table 2.
Conclusion
Using co-precipitation technique, Mg-doped ZnO NRs were successfully synthesized, and the influence of Mg doping on the phase constitution, elemental composition, morphology and optical properties of ZnO was investigated. Using XRD analysis, the ZnO has hexagonal wurtzite phase, while the estimated crystallite size was less than 100 nm. Crystalline structure of ZnO was also improved by Mg doping, which in turn led to increased luminescence and an increase in the band gap. UV–Vis absorption spectra revealed blueshift indicating band gap widening, while ZnO rod formation was confirmed by EDS study, where an average atomic ratio of 67.6:23.6 was observed. Raman spectrum was blueshifted for higher values of doping (8 wt%) caused by substitution of Mg 2+ for Zn 2+ in ZnO lattice. PL results indicated increased visible emissions with Mg, leading to an increase in electron hole pair delocalization. Dye degradation performance of synthesized NRs was evaluated against MBCF, and best results were obtained via sonophotocatalysis with maximum degradation efficiency of 87% for Mg-doped ZnO. Inhibition zones were recorded as (1.05–2.05 mm) and (2.10–4.15 mm) for S. aureus and (0–6.15 mm) to (0–8.65 mm) for E. coli , respectivement. Therefore, doped nanorods may be imposed as a control material to minimize antibiotic resistance. Furthermore, in silico molecular docking studies predicted Mg-doped ZnO NRs as potential inhibitor of DHFR, DHPS and FabH enzyme. The inhibition of given enzymes is suggested as possible mechanism behind bactericidal activity of Mg-doped ZnO NRs against E. coli .
Disponibilité des données et des matériaux
Toutes les données sont entièrement disponibles sans restriction.
Abréviations
- DHFR:
-
Dihydrofolate reductase
- DHPS:
-
Dihydropteroate synthase
- EDS :
-
Spectroscopie à rayons X à dispersion d'énergie
- FTIR :
-
Spectroscopie infrarouge à transformée de Fourier
- FESEM :
-
Microscopie électronique à balayage à émission de champ
- G+ve:
-
Gram-positive
- G-ve:
-
Gram-negative
- HR-TEM :
-
Microscopie électronique à transmission haute résolution
- JCPDS :
-
Comité mixte sur les normes de diffraction des poudres
- Mg:
-
Magnesium
- UV–Vis:
-
Ultraviolet–visible spectroscopy
- XRD :
-
Diffraction des rayons X
- ZnO :
-
Oxyde de zinc
Nanomatériaux
- Composés à base de polycétone pour concurrencer les nylons 6, 66 et POM
- Synthèse biogénique, caractérisation et évaluation du potentiel antibactérien de nanoparticules d'oxyde de cuivre contre Escherichia coli
- Mécanisme de conduction et endurance améliorée dans la RRAM à base de HfO2 avec traitement de nitruration
- Fabrication d'hétérostructures Hiérarchiques ZnO@NiO Core–Shell pour de meilleures performances photocatalytiques
- Synthèse facile et amélioration de l'activité photocatalytique en lumière visible de nouveaux composites à hétérojonction p-Ag3PO4/n-BiFeO3 pour la dégradation des colorants
- Résistance de contact réduite entre le métal et le n-Ge par insertion de ZnO avec traitement au plasma d'argon
- Influence du dopage au magnésium sur les nanoparticules de ZnO pour une évaluation photocatalytique améliorée et une analyse antibactérienne
- Microstructure et photoluminescence dépendante du dopage/de la température d'un réseau de nanolances de ZnO préparé par méthode hydrothermale
- Effet des hétérostructures bicouche CeO2−x/ZnO et ZnO/CeO2−x et polarité d'électroformage sur les propriétés de commutation de la mémoire non volatile



