Synthèse facile et amélioration de l'activité photocatalytique en lumière visible de nouveaux composites à hétérojonction p-Ag3PO4/n-BiFeO3 pour la dégradation des colorants
Résumé
Dans ce travail, Ag3 Bon de commande4 des microparticules ont été décorées sur la surface de BiFeO3 microcuboïdes par une méthode de précipitation pour obtenir p-Ag3 Bon de commande4 /n-BiFeO3 composites à hétérojonction. Les composites ont été utilisés pour la dégradation de l'orange acide 7 (AO7) sous irradiation à la lumière visible. On constate que les composites présentent une efficacité photocatalytique beaucoup plus élevée que le BiFeO3 nu. . Pendant ce temps, l'activité photocatalytique intrinsèque à la lumière visible de Ag3 Bon de commande4 /BiFeO3 composites a été confirmée par la dégradation du phénol. De plus, la propriété de catalyse de type photo-Fenton du composite a également été évaluée. L'analyse du photocourant indique que la combinaison de BiFeO3 avec Ag3 Bon de commande4 conduit à l'inhibition de la recombinaison des électrons et des trous photo-induits. L'amélioration évidente de l'activité photocatalytique du composite est principalement attribuée à la séparation efficace des charges photogénérées et à la migration des charges interfaciales causées par la formation d'Ag3 Bon de commande4 /BiFeO3 p-n hétérojonctions.
FormalPara PACS81.05.Hd82.65.+r82.50.–m
Contexte
Récemment, la photocatalyse à semi-conducteur a reçu une attention considérable en tant que technologie prometteuse pour la conversion d'énergie et le traitement de la pollution [1,2,3]. Comme nous le savons, le photocatalyseur largement étudié TiO2 est simplement actif sous irradiation de lumière ultraviolette (UV) qui ne constitue qu'environ 5% de la lumière solaire et limite ainsi fortement ses applications photocatalytiques sous la lumière du soleil. Par conséquent, il est nécessaire de développer les photocatalyseurs à lumière visible [4,5,6,7,8].
Les oxydes semi-conducteurs à base de bismuth ou de fer possèdent généralement une énergie de bande interdite modérée (~ 2,0 eV) et sont considérés comme une classe importante de photocatalyseurs sensibles à la lumière visible [9,10,11,12,13,14,15,16, 17,18,19]. Parmi eux, BiFeO3 avec une structure de type pérovskite s'avère présenter des performances photocatalytiques intéressantes pour la dégradation du colorant et la séparation de l'eau sous irradiation de lumière visible [20,21,22,23,24,25]. Cependant, son activité photocatalytique n'est pas impressionnante en raison du taux de recombinaison élevé des électrons photogénérés (e − ) et des trous (h + ). Heureusement, il est démontré que le couplage de BiFeO3 avec un semi-conducteur à bande interdite étroite de potentiels de bord de bande appariés pour former une hétérojonction est l'une des stratégies les plus prometteuses pour favoriser la séparation des charges photogénérées, conduisant ainsi à une meilleure activité photocatalytique de BiFeO3 [26,27,28,29,30,31]. Par exemple, Chaiwichian et al. a signalé que BiFeO3 -Bi2 WO6 les nanocomposites ont montré une activité accrue dans la dégradation des colorants [29]. Wang et al. ont observé que AgCl/Ag/BiFeO3 a montré une activité photocatalytique en lumière visible beaucoup plus élevée que le BiFeO3 nu [30]. Le fan et ses collègues ont découvert que la combinaison de g-C3 N4 avec BiFeO3 peut évidemment améliorer l'activité catalytique par rapport au BiFeO3 pur [31].
Orthophosphate d'argent (Ag3 Bon de commande4 ), en tant qu'excellent photocatalyseur entraîné par la lumière visible, a attiré une attention considérable dans le domaine photocatalytique [32,33,34,35,36,37]. Il a été démontré que Ag3 Bon de commande4 peut atteindre un rendement quantique extrêmement élevé (~ 90%) pour la génération d'oxygène à partir de la division de l'eau [32, 33]. De plus, il possède une capacité de photooxydation supérieure pour la dégradation de la pollution organique en raison de sa position de bande de valence hautement positive [34]. Dans la plupart des cas, en raison de sa position de bande d'énergie appropriée et de sa bande interdite étroite, Ag3 Bon de commande4 est largement utilisé comme cocatalyseur à combiner avec d'autres photocatalyseurs pour former des composites, conduisant à une amélioration évidente du comportement photocatalytique, tel que Ag3 Bon de commande4 /Bi2 WO6 , Ag3 Bon de commande4 /BiPO4 , Ag3 Bon de commande4 /Bi2 O2 CO3 , Ag3 Bon de commande4 /g-C3 N4 , Ag3 Bon de commande4 /BiVO4 , Bi4 Ti3 O12 /Ag3 Bon de commande4 , Ag3 Bon de commande4 /ZnFe2 O4 , Ag3 Bon de commande4 /WO3 , Ag3 Bon de commande4 /ZnO et Bi2 MoO6 /Ag3 Bon de commande4 [38,39,40,41,42,43,44,45,46,47]. Il est rapporté que BiFeO3 est un semi-conducteur de type n et Ag3 Bon de commande4 est connu comme un semi-conducteur de type p [43, 48]. La construction de Ag3 Bon de commande4 /BiFeO3 Les composites à hétérojonction p-n peuvent être une méthode réalisable pour obtenir un photocatalyseur efficace. Cependant, à notre connaissance, peu de travaux ont été consacrés à l'étude des performances photocatalytiques de Ag3 Bon de commande4 /BiFeO3 composites.
Dans ce travail, Ag3 Bon de commande4 /BiFeO3 Les composites à hétérojonction p-n ont été facilement préparés via la précipitation d'Ag3 Bon de commande4 microparticules sur le BiFeO3 microcuboïdes. L'orange acide 7 (AO7) et le phénol ont été choisis comme polluant modèle pour évaluer l'activité photocatalytique des composites sous irradiation en lumière visible. De plus, l'activité de catalyse de type photo-Fenton du composite a également été étudiée. Le mécanisme sous-jacent des composites pour la dégradation des polluants organiques a été discuté.
Méthodes
Préparation de l'Ag3 Bon de commande4 /BiFeO3 Composites
BiFeO3 les microcuboïdes ont été synthétisés par voie hydrothermale. 0,005 mol de Bi(NO3 )3 • 5H2 O et 0,005 mol de Fe(NO3 )3 • 9H2 O ont été dissous dans 20 mL de solution d'acide nitrique diluée (5 mL de HNO3 + 15 mL d'eau déminéralisée). Soixante millilitres de solution de KOH avec une concentration de 4,5 mol/L ont été ajoutés goutte à goutte à la solution ci-dessus sous agitation magnétique. Après 8 min de traitement aux ultrasons et 30 min supplémentaires d'agitation magnétique vigoureuse, la solution de mélange a été scellée dans un autoclave en acier inoxydable revêtu de téflon d'une capacité de 100 mL et soumise à une réaction hydrothermale à 200 °C pendant 6 h. Une fois l'autoclave refroidi naturellement à température ambiante, le précipité a été récupéré par centrifugation, lavé avec de l'eau déminéralisée (deux fois) et de l'éthanol absolu (trois fois), puis séché à 80 °C pendant 12 h pour obtenir le BiFeO final. 3 produit. Ag3 Bon de commande4 les microparticules ont été préparées par une méthode de précipitation. Trois millimoles d'AgNO3 a été dissous dans 30 mL d'eau déminéralisée et 1 mmol de Na3 Bon de commande4 ·12H2 O a été ajouté dans 30 ml d'eau déminéralisée à l'aide d'une agitation magnétique. Une fois la solution homogène, cette dernière solution a été ajoutée goutte à goutte dans la première sous agitation magnétique vigoureuse pendant 7 h. Au cours de la réaction, la couleur de la solution a viré au jaune. Enfin, le mélange a été centrifugé pour récupérer le précipité. Le précipité obtenu a été lavé plusieurs fois avec de l'eau déminéralisée puis séché dans une étuve sous vide à 60 °C pendant 8 h.
Ag3 Bon de commande4 /BiFeO3 les composites ont été synthétisés comme suit :0,1 g de BiFeO3 les microcuboïdes ont été dispersés dans 30 mL d'eau déminéralisée, puis soumis aux ultrasons pendant 2 h. Après cela, une certaine quantité d'AgNO3 a été dissous dans la suspension ci-dessus. A ce mélange a été ajoutée goutte à goutte une certaine concentration de Na3 Bon de commande4 solution (30 mL) sous agitation magnétique vigoureuse pendant 7 h. Les composites obtenus ont été séparés par centrifugation, lavés à plusieurs reprises avec de l'eau désionisée et séchés dans une étuve à vide à 60 °C pendant 8 h. Pour étudier l'effet de Ag3 Bon de commande4 contenu sur la propriété photocatalytique des composites obtenus, une série d'échantillons a été fabriquée avec différents Ag3 Bon de commande4 des rapports de masse de 5 %, 10 %, 20 % et 40 % et les échantillons correspondants ont été appelés 5 % en poids d'Ag3 Bon de commande4 /BiFeO3 , 10wt%Ag3 Bon de commande4 /BiFeO3 , 20wt%Ag3 Bon de commande4 /BiFeO3 , et 40wt%Ag3 Bon de commande4 /BiFeO3 , respectivement. A titre de comparaison, le composite appelé 20wt%Ag3 Bon de commande4 /BiFeO3 -M a également été préparé par mélange mécanique direct de BiFeO3 microcuboïdes et Ag3 Bon de commande4 microparticules, où Ag3 Bon de commande4 occupe une fraction massique de 20% dans le composite.
Mesures photoélectrochimiques
Le test de photocourant a été réalisé sur le poste de travail électrochimique (CST 350) avec une cellule à trois électrodes comme décrit dans la littérature [49]. Dans ce système à trois électrodes, une feuille de platine et une électrode au calomel standard ont été utilisées comme contre-électrode et électrode de référence, respectivement. L'électrode de travail a été fabriquée comme suit :15 mg de photocatalyseurs, 0,75 mg de noir de carbone et 0,75 mg de fluorure de polyvinylidène (PVDF) ont été ajoutés à de la 1-méthyl-2-pyrrolidone (NMP) pour produire une suspension, qui a ensuite été uniformément enduite sur un 1,0 × 1,0 cm 2 électrode en verre d'oxyde d'étain dopé au fluorure. Après cela, l'électrode a été séchée à 60 °C pendant 5 h. Une lampe Xe de 300 W avec un filtre de coupure de 420 nm a été utilisée comme source de lumière visible. La mesure photoélectrochimique a été réalisée dans le Na2 0,1-M SO4 solution d'électrolyte, et sa valeur de pH a été mesurée à ~ 5,3. Les courbes photocourant-temps (It) ont été mesurées à un potentiel de polarisation fixe de 0,2 V. Le test de spectroscopie d'impédance électrochimique (EIS) a été réalisé en utilisant l'impulsion de tension sinusoïdale avec amplitude de 5 mV et dans la plage de fréquences de 10 −2 à 10 5 Hz.
Test d'activité photocatalytique
L'activité photocatalytique des échantillons a été évaluée vis-à-vis de la dégradation de l'AO7 et du phénol sous irradiation à la lumière visible. Typiquement, la concentration initiale en AO7 ou en phénol était de 5 mg/L avec une charge de catalyseur de 0,5 g/L. Les valeurs de pH de l'AO7 et de la solution de phénol ont été mesurées à ~ 6,8 et ~ 6,2, respectivement. Avant l'éclairage, le mélange a été agité dans l'obscurité pendant 0,5 h pour atteindre l'équilibre d'adsorption-désorption de la molécule organique à la surface des catalyseurs. Cette solution réactionnelle a ensuite été exposée à une lampe au xénon de 300 W avec un filtre de coupure de 420 nm, et l'intensité lumineuse correspondante a été mesurée à ~ 50 mW cm −2 . Au cours de l'expérience photocatalytique, une petite quantité de solution réactionnelle a été collectée à des intervalles de temps donnés, puis centrifugée pour séparer les catalyseurs. La concentration d'AO7 ou de phénol a été déterminée en détectant l'absorbance du surnageant à une longueur d'onde donnée (λ AO7 = 484 nm et λ phénol = 270 nm) à l'aide d'un spectrophotomètre UV-visible. Pour évaluer la réutilisabilité photocatalytique des photocatalyseurs, l'expérience de recyclage pour la dégradation de l'AO7 a été réalisée. Une fois le premier test photocatalytique terminé, les photocatalyseurs ont été collectés par centrifugation, lavés avec de l'eau distillée et séchés. Les photocatalyseurs collectés ont été ajoutés à la solution de colorant frais pour le cycle suivant de l'expérience photocatalytique. Pour étudier la capacité de catalyse de type photo-Fenton des photocatalyseurs, H2 O2 (5 mmol/L) a été ajouté à la solution réactionnelle. La procédure d'expérience de type photo-Fenton était similaire au processus photocatalytique ci-dessus.
Caractérisation
La pureté de phase des échantillons a été étudiée par diffractomètre à rayons X (XRD, Bruker D8 Advanced) en utilisant le rayonnement Cu Kα. La morphologie des échantillons a été observée au microscope électronique à balayage à émission de champ (SEM, JEOL JSM-6701F) et au microscope électronique à transmission à émission de champ (TEM, JEOL JEM-2010). La composition des échantillons a été mesurée par spectroscopie à rayons X à dispersion d'énergie. L'état chimique de l'élément a été testé à l'aide de la spectroscopie photoélectronique à rayons X (XPS, PHI-5702), où l'échelle d'énergie de liaison des données XPS a été calibrée par rapport au pic accidentel C 1s à l'énergie de liaison de 284,8 eV. Les spectres de réflectance diffuse ultraviolet-visible (UV-vis) des produits ont été obtenus à l'aide d'un spectrophotomètre UV-vis (PERSEE TU-1901) avec BaSO4 pour référence. Les spectres PL des échantillons ont été enregistrés sur un spectrophotomètre à fluorescence (SHIMADZU RF-6000) avec une longueur d'onde d'excitation de ~ 350 nm.
Résultats et discussion
Analyse XRD
La figure 1 présente les modèles XRD de BiFeO3 , Ag3 Bon de commande4 , et Ag3 Bon de commande4 /BiFeO3 composites avec différents Ag3 Bon de commande4 Contenu. Pour BiFeO nu3 échantillon, tous les pics de diffraction correspondent bien à la structure rhomboédrique de BiFeO3 (fiche PDF n°74-2016), et pour Ag3 nu Bon de commande4 échantillon, les pics de diffraction peuvent être parfaitement indexés sur Ag3 cubique Bon de commande4 phase (fiche PDF n° 06-0505); cela indique que BiFeO3 de haute pureté et Ag3 Bon de commande4 ont été préparés avec succès. Dans le cas des composites, les diagrammes XRD peuvent être attribués aux pics de diffraction caractéristiques de BiFeO3 et Ag3 Bon de commande4 , et aucun pic de diffraction d'impureté n'apparaît dans les motifs. De plus, on voit qu'en augmentant la teneur en Ag3 Bon de commande4 , l'intensité des pics caractéristiques de Ag3 Bon de commande4 augmente progressivement. Les résultats suggèrent que les composites sont constitués de BiFeO3 rhomboédrique et Ag cubique3 Bon de commande4 , et aucune autre phase n'est générée lors de la préparation des composites.
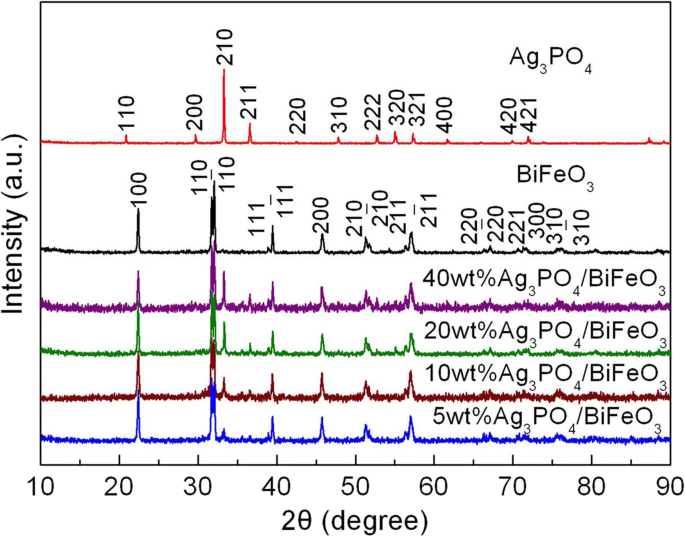
Modèles XRD de BiFeO3 , Ag3 Bon de commande4 , et Ag3 Bon de commande4 /BiFeO3 composites
Observation de la morphologie
La morphologie des échantillons a été observée par SEM et MET. La figure 2a, b montre l'image SEM et l'image TEM de BiFeO3 nu , révélant que le BiFeO3 préparé les particules présentent une forme cuboïde avec une taille de 200 à 500 nm et ont une surface lisse. L'encart de la figure 2a affiche la distribution du rapport longueur/largeur de BiFeO3 particules, ce qui révèle que le rapport longueur/largeur varie de 1,1/1 à 2,5/1. Comme on peut le voir sur l'image TEM de la Fig. 2c, Ag3 nu Bon de commande4 se compose de particules sphériques irrégulières. La distribution de taille d'Ag3 Bon de commande4 Les particules sont montrées dans l'encart de la figure 2c, indiquant une large distribution de la taille des particules allant de 110 à 180 nm. À partir de l'image TEM du 20wt%Ag3 Bon de commande4 /BiFeO3 composite (Fig. 2d), on peut voir que les microsphères irrégulières sont attachées à la particule en forme de cuboïde. Les images MET haute résolution (HRTEM) obtenues à partir des différentes particules indiquent deux ensembles distincts de franges de réseau (encarts sur la figure 2d). L'espacement interplanaire de ~ 0.288 nm correspond au BiFeO3 (110) plans, alors que la distance interplanaire de ~ 0,267 nm correspond à l'Ag3 Bon de commande4 (210) avions. De plus, l'analyse EDX suggère que le composite inclut tous les éléments de Ag3 Bon de commande4 et BiFeO3 phases (Fig. 2e). Les signaux C et Cu observés dans le spectre EDX de la figure 2e pourraient provenir du micro-réseau utilisé pour supporter l'échantillon [50]. Ces résultats révèlent que Ag3 Bon de commande4 les particules sont décorées à la surface de BiFeO3 microcuboïdes, entraînant la formation d'Ag3 Bon de commande4 /BiFeO3 p-n hétérostructures.

un SEM (l'encart est la distribution du rapport longueur-largeur de BiFeO3 microcuboïdes) et b Image MET de BiFeO3 microcuboïdes. Image TEM de c Ag3 Bon de commande4 microparticules (l'encart est la distribution de taille d'Ag3 Bon de commande4 microparticules) et d 20wt%Ag3 Bon de commande4 /BiFeO3 goûter; l'encart montre son image HRTEM. e Spectre EDX de 20wt%Ag3 Bon de commande4 /BiFeO3 échantillon
Analyse XPS
L'analyse XPS a été réalisée pour révéler les états chimiques de BiFeO3 et 20 % en poids d'Ag3 Bon de commande4 /BiFeO3 , comme le montre la figure 3. La figure 3a montre le spectre XPS haute résolution de Ag 3d dans le composite. Les deux pics évidents à 373,8 et 367,7 eV sont attribués à l'Ag 3d3/2 et Ag 3d5/2 énergies de liaison de l'Ag + . La figure 3b présente le spectre XPS haute résolution P 2p du composite. Le pic à environ 133,2 eV correspond à l'énergie de liaison caractéristique de P 5+ état d'oxydation dans Ag3 Bon de commande4 [51]. La figure 3c, d, montre respectivement les spectres XPS haute résolution Bi 4f et Fe 2p. Pour BiFeO nu3 , le spectre Bi 4f montre deux pics forts à des énergies de liaison de 164,1 eV et 158,8 eV, appartenant au Bi 4f5/2 et Bi 4f7/2 , respectivement, ce qui indique que l'ion Bi possède l'état d'oxydation de + 3. Pour le spectre Fe 2p, le pic situé à 723,7 eV est attribué au Fe 2p1/2 de Fe 3+ . Un autre signal XPS puissant à ~ 711,6 eV peut être intégré à deux pics à 711,7 et 709,9 eV. Le pic à 709,9 eV correspond à l'énergie de liaison de Fe 2p3/2 de Fe 2+ . L'énergie de liaison à 711,7 eV appartient au Fe 2p3/2 de Fe 3+ . De plus, un pic satellite se trouve à environ 718,2 eV, ce qui est attribué aux états d'oxydation mixtes de Fe. D'après l'analyse XPS de l'élément Fe, on peut voir que Fe existe sous la forme de Fe 3+ et Fe 2+ en nu BiFeO3 . Il est à noter que les énergies de liaison Bi 4f et Fe 2p dans 20wt%Ag3 Bon de commande4 /BiFeO3 présentent un léger décalage par rapport au BiFeO nu3 , qui est principalement attribuée à l'interaction entre BiFeO3 et Ag3 Bon de commande4 . La figure 3e affiche les spectres XPS haute résolution O 1s de BiFeO3 et 20 % en poids d'Ag3 Bon de commande4 /BiFeO3 . Pour BiFeO nu3 , le signal O 1s peut être divisé en deux pics à 529,8 et 531,0 eV. L'énergie de liaison de 529,8 eV correspond à l'oxygène du réseau tandis que le petit pic à une énergie de liaison plus élevée de 531,0 eV est causé par des défauts de surface et des espèces d'oxygène chimisorbées. Par rapport au BiFeO nu3 , le pic O 1s dans le composite subit un décalage, qui est également dû à l'interaction entre Ag3 Bon de commande4 et BiFeO3 .
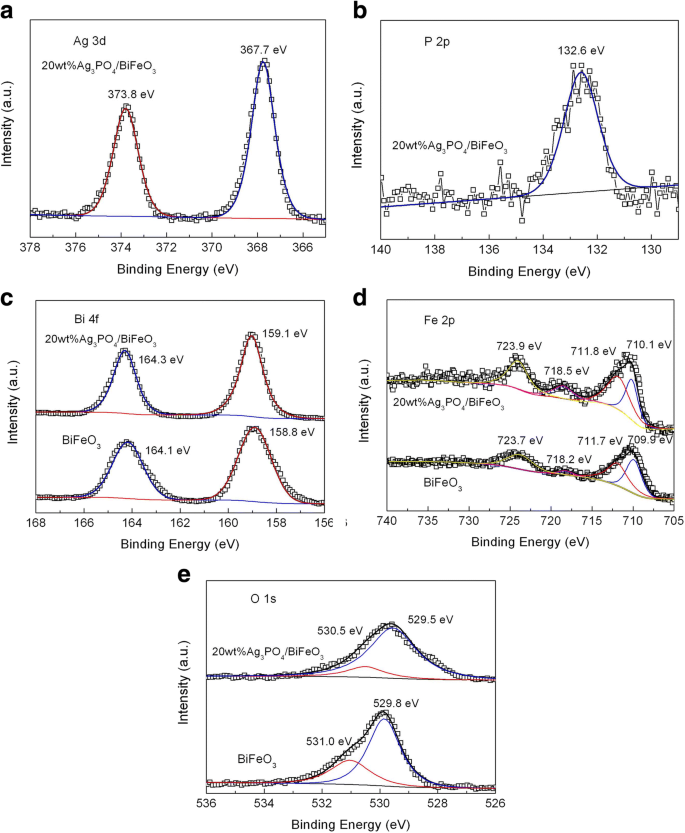
Spectres XPS haute résolution de BiFeO3 et 20 % en poids d'Ag3 Bon de commande4 /BiFeO3 goûter. un Ag 3d et b P 2p de 20wt%Ag3 Bon de commande4 /BiFeO3 goûter. c Bi 4f, d Fe 2p, et e O1s de BiFeO3 et 20 % en poids d'Ag3 Bon de commande4 /BiFeO3 échantillon
Propriété d'absorption optique
Le comportement d'absorption optique des échantillons a été étudié en mesurant leurs spectres de réflectance diffuse UV-vis, comme le montre la figure 4a. Les spectres d'absorption correspondants transformés à partir des spectres de réflectance diffuse selon la théorie de Kubelka-Munk (K-M) sont présentés sur la figure 4b [52]. On constate que tous les échantillons présentent une absorption lumineuse importante à λ < 600 nm. Afin d'obtenir le bord d'absorption des échantillons, la dérivée première de la réflectance (R) par rapport à la longueur d'onde (c'est-à-dire dR/dλ) a été réalisée, comme le montre la figure 4c. Le bord d'absorption peut être déterminé à partir de la longueur d'onde maximale dans les spectres dérivés [53]. On peut voir que le bord d'absorption lumineuse de l'Ag3 nu Bon de commande4 est situé à ~ 527 nm, correspondant à l'énergie de la bande interdite (E g ) de ~ 2,35 eV. Nu BiFeO3 présente un bord d'absorption à environ 567 nm, correspondant au E g de ~ 2.18 eV. En plus du bord d'absorption, un pic faible à ~ 700 nm est observé, ce qui est probablement attribué à l'existence d'états de surface au milieu de la bande interdite de BiFeO3 . Lorsqu'il est couplé avec Ag3 Bon de commande4 , le bord d'absorption de BiFeO3 ne subit pas de changement évident, ce qui indique que l'introduction d'Ag3 Bon de commande4 n'a aucun effet apparent sur la structure de bande interdite de BiFeO3 .
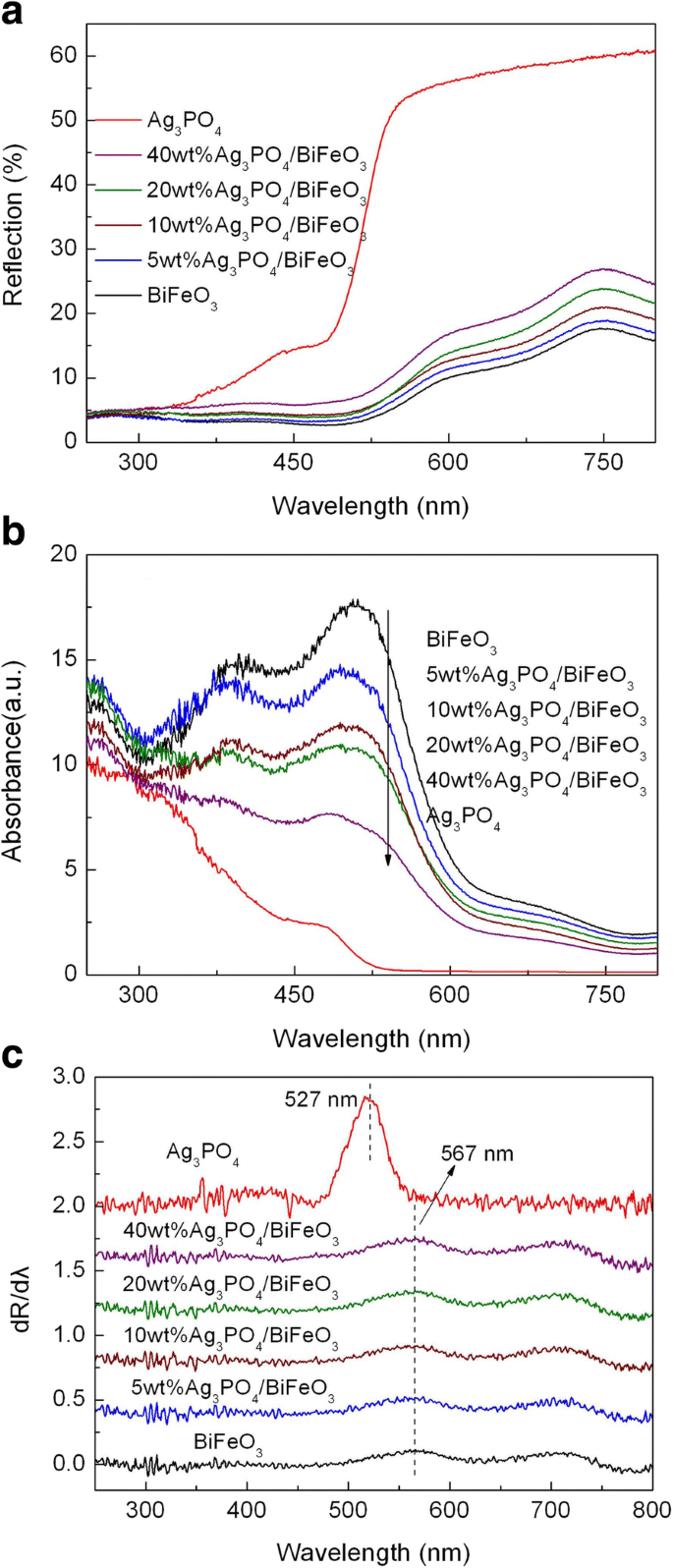
un Spectres de réflectance diffuse UV-visible de BiFeO3 , Ag3 Bon de commande4 , et Ag3 Bon de commande4 /BiFeO3 matériaux composites. b Les spectres d'absorption correspondants et c la dérivée première correspondante des spectres de réflectance diffuse
Mesure de l'activité photocatalytique
AO7 a été sélectionné comme polluant cible pour évaluer les performances photocatalytiques des échantillons. La dégradation photocatalytique de l'AO7 a été étudiée sous irradiation à la lumière visible, et le résultat est montré sur la figure 5. Avant la réaction photocatalytique, des expériences à blanc et d'absorption ont été réalisées. On voit qu'aucune dégradation évidente du colorant n'est détectée sous irradiation sans les catalyseurs ou en présence de catalyseurs sans irradiation, ce qui suggère que l'auto-dégradation et l'absorption de AO7 pendant le processus photocatalytique sont négligeables. Nu BiFeO3 a une faible activité photocatalytique, et seulement ~ 27% de AO7 est dégradé avec 120 min d'irradiation. Lorsque BiFeO3 les microcuboïdes sont combinés avec Ag3 Bon de commande4 microparticules, l'Ag3 formé Bon de commande4 /BiFeO3 les composites présentent une activité photocatalytique supérieure à celle du BiFeO3 nu . Après 120 min d'exposition, le pourcentage de dégradation de l'AO7 sur les échantillons est de l'ordre de 40 % en poids d'Ag3 Bon de commande4 /BiFeO3 (~ 91%) > 20wt%Ag3 Bon de commande4 /BiFeO3 (~ 87%) > 10wt%Ag3 Bon de commande4 /BiFeO3 (~ 69%) > 5wt%Ag3 Bon de commande4 /BiFeO3 (~ 46%) > BiFeO3 (~ 27%). On constate que les performances photocatalytiques des composites présentent une tendance à la hausse avec l'augmentation de Ag3 Bon de commande4 contenu. Parmi ces composites, l'efficacité photocatalytique de 40wt%Ag3 Bon de commande4 /BiFeO3 est très proche de celui de 20wt%Ag3 Bon de commande4 /BiFeO3 . Ainsi, dans la présente étude, le rapport massique le plus approprié d'Ag3 Bon de commande4 peut être considéré comme 20 % dans les composites. De plus, il convient de noter que l'échantillon de mélange mécanique 20wt%Ag3 Bon de commande4 /BiFeO3 -M présente une activité photocatalytique bien inférieure à 20 % en poids d'Ag3 Bon de commande4 /BiFeO3 . Ceci révèle que la construction d'hétérojonction entre BiFeO3 et Ag3 Bon de commande4 est nécessaire pour l'amélioration de l'activité photocatalytique. De plus, par rapport à BiFeO3 /a-Fe2 O3 et BiFeO3 -Bi2 WO6 composites [26, 29], l'Ag3 Bon de commande4 /BiFeO3 les composites à hétérojonction préparés dans la présente étude manifestent une activité photocatalytique plus élevée envers la dégradation du colorant.
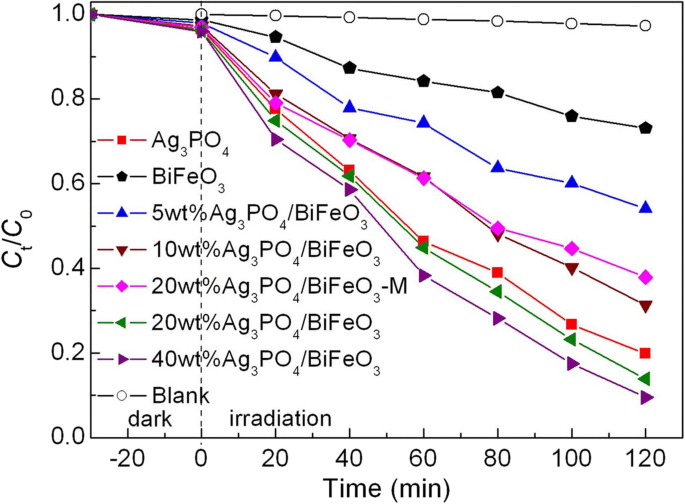
Activités photocatalytiques de BiFeO3 et Ag3 Bon de commande4 /BiFeO3 composites vers la dégradation de l'AO7 sous irradiation à la lumière visible, ainsi que les résultats des expériences de blanc et d'absorption
Pour confirmer davantage la propriété photocatalytique des composites, la dégradation photocatalytique du phénol incolore sur 20 % en poids d'Ag3 Bon de commande4 /BiFeO3 et BiFeO3 sous irradiation de lumière visible a également été étudiée. Comme le montre la figure 6, l'autodégradation et l'absorption du phénol peuvent être négligées sur la base des résultats des expériences à blanc et d'absorption. On peut voir que seulement ~ 9% du phénol est dégradé catalysé par BiFeO3 après 120 min d'exposition. Alors que, lorsque 20wt%Ag3 Bon de commande4 /BiFeO3 est utilisé comme photocatalyseur, le pourcentage de dégradation du phénol peut évidemment être amélioré dans les mêmes conditions. Le résultat suggère que la dégradation du colorant sur l'Ag3 irradié à la lumière visible Bon de commande4 /BiFeO3 composites est attribué à leur activité photocatalytique intrinsèque au lieu de la sensibilisation aux colorants.
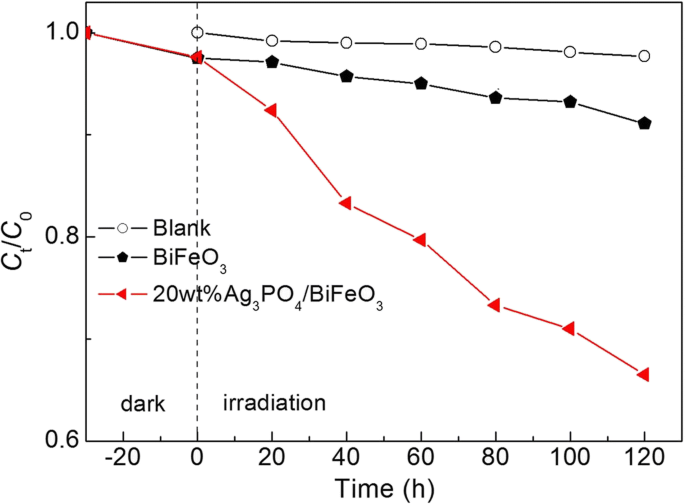
Dégradation photocatalytique du phénol sur BiFeO3 et 20 % en poids d'Ag3 Bon de commande4 /BiFeO3 échantillon sous irradiation à la lumière visible, ainsi que le résultat de l'expérience à blanc et d'absorption
Pour évaluer la réutilisabilité des photocatalyseurs, les expériences de recyclage photocatalytique de dégradation de l'AO7 sur 20 % en poids d'Ag3 Bon de commande4 /BiFeO3 et Ag3 Bon de commande4 ont été réalisées dans les mêmes conditions photocatalytiques. Comme le montre la figure 7, après trois cycles de recyclage successifs, le composite présente toujours une activité photocatalytique relativement élevée, tandis que l'efficacité de dégradation sur Ag3 Bon de commande4 subit une diminution évidente. La figure 8a, b montre l'image MET et le modèle XRD du composite après l'expérience de cyclisme, respectivement. Il est clair que Ag3 Bon de commande4 des microparticules sont encore assemblées à la surface de BiFeO3 microcuboïdes sans destruction des hétérostructures, et aucun changement évident de structure cristalline n'est observé. Cela suggère que Ag3 Bon de commande4 /BiFeO3 Les composites à hétérojonction p-n possèdent une bonne réutilisabilité photocatalytique.
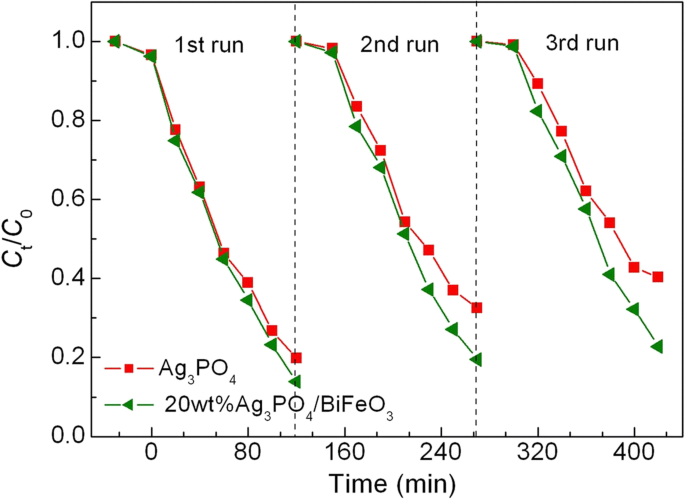
Dégradation photocatalytique de AO7 sur Ag3 Bon de commande4 et 20 % en poids d'Ag3 Bon de commande4 /BiFeO3 échantillon pendant trois cycles
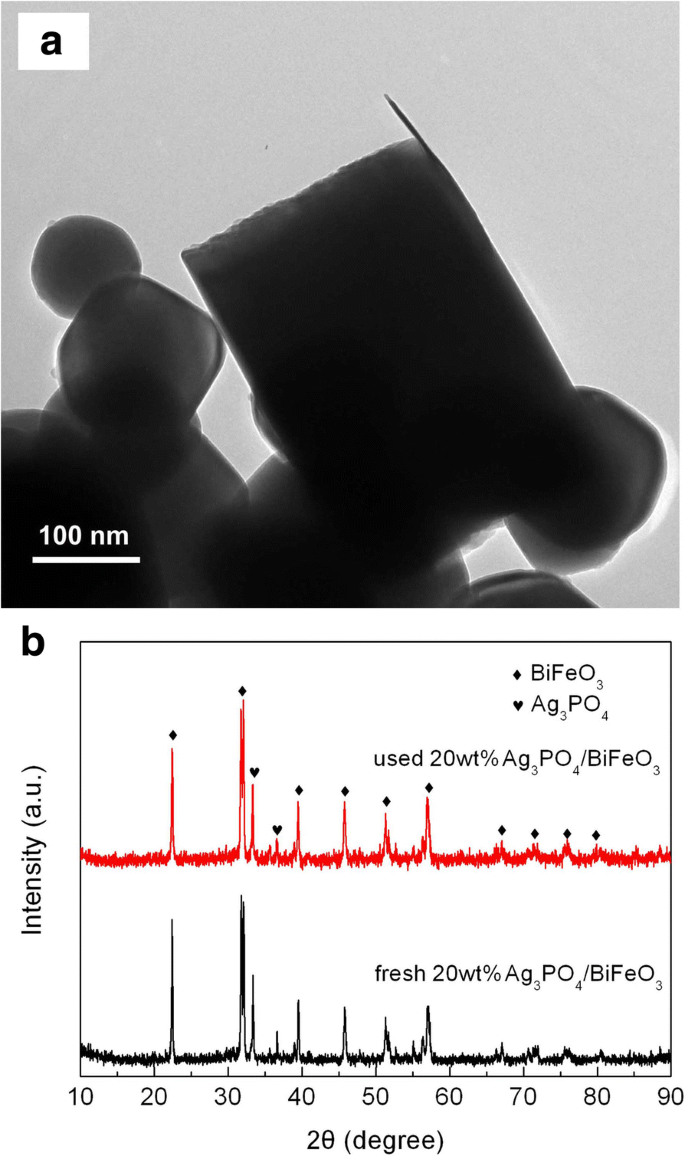
un Image TEM et b Modèle XRD de 20wt%Ag3 Bon de commande4 /BiFeO3 échantillon après cyclage des expériences photocatalytiques
Activité catalytique de type photo Fenton
Outre sa propriété photocatalytique, BiFeO3 présente également une capacité de catalyse de type photo-Fenton [54, 55, 56]. La figure 9 montre la dégradation de type photo Fenton de l'AO7 sur 20 % en poids d'Ag3 Bon de commande4 /BiFeO3 et BiFeO3 en présence de H2 O2 . Par rapport aux systèmes réactionnels sans H2 O2 , l'introduction de H2 O2 améliore remarquablement le pourcentage de dégradation du colorant. Ce résultat est principalement dû au mécanisme de réaction de type photo-Fenton. En présence d'irradiation à la lumière visible et de H2 O2 , Fe 3+ à la surface de BiFeO3 peut être converti en Fe 2+ avec génération de radicaux hydroxyles (•OH) (Eq. 1). Par conséquent, Fe 2+ peut réagir avec H2 O2 pour produire Fe 3+ et •OH (Eq. 2). Au cours de la réaction du cycle ci-dessus, plus de •OH est produit, ce qui est généralement considéré comme une espèce active primaire pour la dégradation du colorant (comme en témoigne l'expérience de piégeage d'espèces actives illustrée à la figure 11). Dans le cas du BiFeO nu3 , le taux de recombinaison élevé des charges photogénérées limite le rendement en électrons photogénérés, ce qui tend à supprimer la réduction de Fe 3+ dans Fe 2+ (Équation 3). Cela conduit à l'amélioration limitée du pourcentage de dégradation. Pour Ag3 Bon de commande4 /BiFeO3 les composites, les électrons photogénérés et les trous peuvent être séparés efficacement, et ainsi, plus d'électrons photogénérés sont disponibles pour favoriser la conversion rapide de Fe 3+ dans Fe 2+ (Éq. 3) [57]. Bénéficiant de cette réduction électronique, le procédé photo-Fenton pour les composites est plus performant que celui pour le BiFeO3 nu. . En conséquence, Ag3 Bon de commande4 /BiFeO3 Les composites à hétérojonction p-n présentent des performances photo-Fenton bien améliorées.
$$ {\mathrm{Fe}}^{3+}+{\mathrm{H}}_2\mathrm{O}+\mathrm{h}\upnu \to {\mathrm{Fe}}^{2+} +\bullet \mathrm{OH}+{\mathrm{H}}^{+} $$ (1) $$ {\mathrm{Fe}}^{2+}+{\mathrm{H}}_2{\ mathrm{O}}_2\to {\mathrm{Fe}}^{3+}+\bullet \mathrm{OH}+{\mathrm{O}\mathrm{H}}^{-} $$ (2) $$ {\mathrm{Fe}}^{3+}+{\mathrm{e}}^{-}\to {\mathrm{Fe}}^{2+} $$ (3)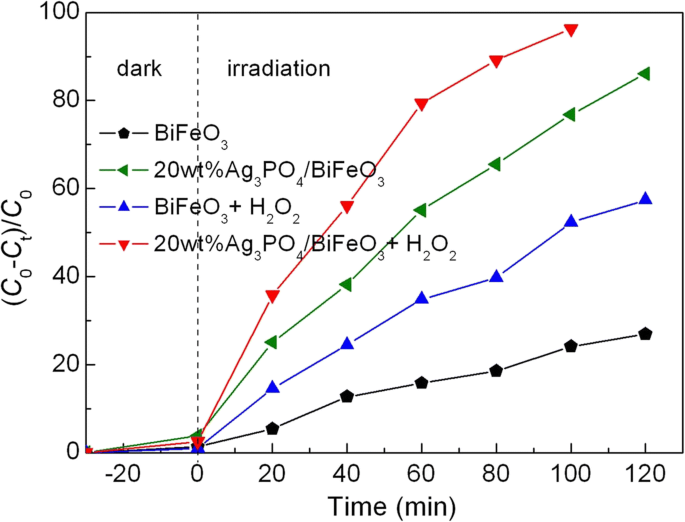
Activités photocatalytiques de BiFeO3 et 20 % en poids d'Ag3 Bon de commande4 /BiFeO3 échantillon vers la dégradation de AO7 sous irradiation de lumière visible en présence de H2 O2
Performance de charge photogénérée
Évaluer le comportement de séparation des charges photogénérées des échantillons, les réponses photoélectriques transitoires, les spectres ESI et les spectres PL de BiFeO3 et 20 % en poids d'Ag3 Bon de commande4 /BiFeO3 ont été mesurés. La figure 10a montre les courbes photocourant-temps (I-t) des photocatalyseurs sous irradiation intermittente de lumière visible avec plusieurs cycles marche-arrêt. On constate que la valeur du photocourant du composite est bien supérieure à celle du BiFeO3 nu , indiquant que la construction de Ag3 Bon de commande4 /BiFeO3 Les hétérojonctions p-n sont bénéfiques pour inhiber la recombinaison des électrons et des trous photogénérés. La figure 10b présente les spectres ESI des échantillons. On peut voir que le composite présente des rayons d'arc d'impédance plus petits par rapport au BiFeO3 , ce qui suggère la plus faible résistance au transfert de charge du composite. These results reveal that the separation and migration of the photogenerated charges can be improved in the composite, thus providing more photoinduced holes and electrons for the photocatalysis. Figure 10c shows the Mott-Schottky plot at frequency of 3000 Hz for Ag3 Bon de commande4 . The negative slope of the plot indicates that Ag3 Bon de commande4 is a p-type semiconductor, which is consistent with the report [43]. The PL spectra of BiFeO3 and 20wt%Ag3 Bon de commande4 /BiFeO3 are shown in Fig. 10d. The two samples exhibit obvious emission peaks at ~ 522 nm, which are mainly attributed to the recombination of the photogenerated electron/hole pairs. It is worth noting that the PL intensity of the composite is much smaller than that of bare BiFeO3 . This further confirms that the construction of Ag3 Bon de commande4 /BiFeO3 heterojunction promotes the separation of photoinduced charges.
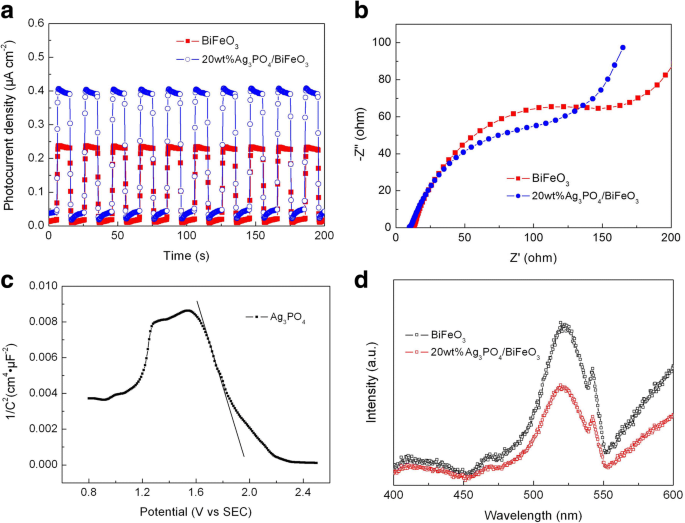
un Transient photocurrent response and b EIS spectra of BiFeO3 and 20wt%Ag3 Bon de commande4 /BiFeO3 goûter. c Mott-Schottky plot of Ag3 Bon de commande4 . d PL spectra of BiFeO3 and 20wt%Ag3 Bon de commande4 /BiFeO3 échantillons
Active Species Trapping
It is well known that photogenerated hole (h + ), hydroxyl (•OH), and superoxide (•O 2− ) are considered to the main active species responsible for the photocatalytic degradation of dye. In order to clarify the role of the active species in the present photocatalytic system, the active species trapping experiments were carried out, as shown in Fig. 11. It can be seen that the degradation percentage of AO7 undergoes an obvious decrease after the introduction of ethanol (scavenger of •OH, 10% by volume) or ethylene diamine tetraacetic acid (EDTA, scavenger of h + , 2 mM). This indicates that •OH and h + are the major active species involved in the photocatalytic reaction. After the addition of benzoquinone (BQ, scavenger of •O 2− , 1 mM), a slight decrease of degradation percentage is detected, suggesting that •O 2− plays a relatively minor role in the dye degradation.
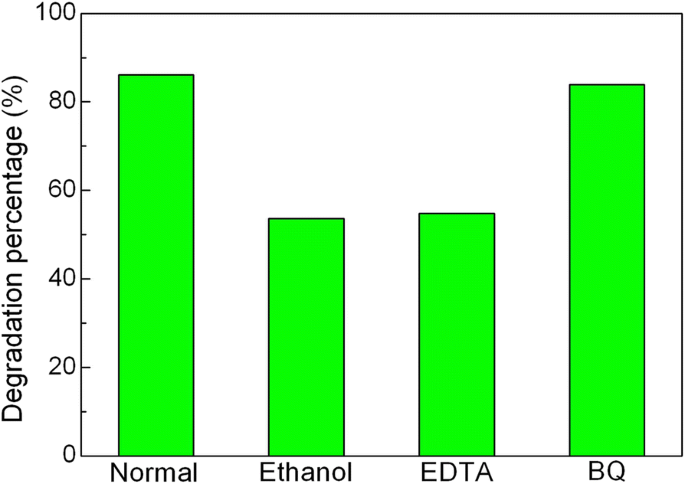
Effects of ethanol, EDTA, and BQ on the degradation percentage of AO7 over 20wt%Ag3 Bon de commande4 /BiFeO3 composite
Proposed Photocatalytic Mechanism
It is well known that the redox ability and migration of photogenerated charges are highly related to the energy-band potentials of photocatalysts. The valence band (VB) and conduction band (CB) of BiFeO3 and Ag3 Bon de commande4 can be obtained using the following equation [58, 59]:
$$ {E}_{\mathrm{VB}}=X-{E}^{\mathrm{e}}+0.5{E}_{\mathrm{g}} $$ (4) $$ {E}_{\mathrm{CB}}=X-{E}^{\mathrm{e}}-0.5{E}_{\mathrm{g}} $$ (5)X is the absolute electronegativity of semiconductor (calculated as the arithmetic mean of the electron affinity and the first ionization of the constituent atoms). E e is the energy of free electrons on the hydrogen scale (~ 4.5 eV). The X values of BiFeO3 and Ag3 Bon de commande4 are estimated to be 5.93 and 5.98 eV, respectively [43, 60]. Based on Eqs. (4) and (5), the CB/VB potentials of BiFeO3 and Ag3 Bon de commande4 are calculated to be 0.34/2.52 V and 0.31/2.66 V vs. NHE, respectively. The energy-band potential diagram of the two photocatalysts is shown in Fig. 12a. It is reported that BiFeO3 is an n-type semiconductor and its Fermi level lies close to the CB [48]. Ag3 Bon de commande4 is demonstrated to be a p-type semiconductor (see Fig. 10c), whose Fermi energy level is close to the VB [43].When BiFeO3 is combined with Ag3 Bon de commande4 to form p-n heterojunction (see Fig. 12b), the diffusion of electrons and holes between the two photocatalysts will build an internal electric field at the interface region of the p-n heterojunction with direction from BiFeO3 to Ag3 Bon de commande4 . Simultaneously, the energy-band potential of BiFeO3 tends to move down along with its Fermi level whereas that of Ag3 Bon de commande4 tends to raise up accompanied by its Fermi level until an equilibrium state of Fermi level of the two photocatalysts is achieved. Upon visible-light irradiation, both BiFeO3 and Ag3 Bon de commande4 can be excited to generate photoinduced electron and hole pairs. Under the promotion of the internal electric field, the photogenerated electrons in the CB of Ag3 Bon de commande4 will migrate to the CB of BiFeO3 , while the photogenerated holes will transfer from the VB of BiFeO3 to that of Ag3 Bon de commande4 . As a result, the recombination of photogenerated charges can be effectively inhibited, as evidenced by the photocurrent and PL analysis (see Fig. 10a, d). Thus, more photogenerated electrons and holes can participate in the photocatalytic redox reaction, leading to the enhancement of the photocatalytic activity for the Ag3 Bon de commande4 /BiFeO3 p-n heterojunction composites.
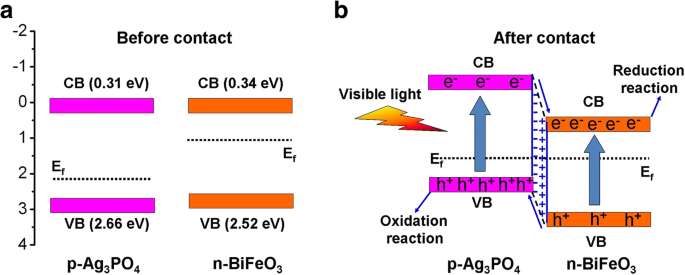
Schematic illustration of proposed photocatalytic mechanism for Ag3 Bon de commande4 /BiFeO3 composite. un Before contact. b After contact
Conclusions
Ag3 Bon de commande4 /BiFeO3 p-n heterojunction composites were synthesized through the decoration of Ag3 Bon de commande4 spherical-like microparticles on the surface of BiFeO3 microcuboids. Compared with bare BiFeO3 , the as-obtained composites exhibit enhanced visible-light photocatalytic activity for the degradation of AO7 and phenol. Moreover, the composites are demonstrated to be excellent photo-Fenton-like catalysts. The improved photocatalytic activity of the composites is mainly attributed to the efficient separation of photogenerated electrons and holes owing to the formation of the p-n heterojunction between BiFeO3 and Ag3 PO4.
Abréviations
- AO7:
-
Acid orange 7
- CB :
-
Bande de conduction
- DRS:
-
UV-vis diffuse reflectance spectra
- EDX :
-
Energy dispersive X-ray
- E g :
-
Bandgap energy
- I-t:
-
Photocurrent-time
- NMP:
-
1-Methyl-2-pyrrolidione
- PVDF :
-
Polyvinylidene fluoride
- R:
-
Reflectance
- SEM :
-
Microscope électronique à balayage
- TEM :
-
Microscope électronique à transmission
- VB:
-
Valence band
- XPS :
-
Spectroscopie photoélectronique aux rayons X
- XRD :
-
Diffractomètre à rayons X
Nanomatériaux
- Nanofibres et filaments pour une administration améliorée des médicaments
- Avancées et défis des nanomatériaux fluorescents pour la synthèse et les applications biomédicales
- Synthèse hydrothermale de nanoparticules d'In2O3 jumelles hybrides disque hexagonal hétérostructures ZnO pour des activités photocatalytiques et une stabilité améliorées
- Un nouveau photocatalyseur à hétérojonction Bi4Ti3O12/Ag3PO4 avec des performances photocatalytiques améliorées
- Synthèse facile d'oxyde d'étain mésoporeux semblable à un trou de ver via l'auto-assemblage induit par l'évaporation et les propriétés de détection de gaz améliorées
- Synthèse en un seul pot de nanoplaques Cu2ZnSnSe4 et leur activité photocatalytique induite par la lumière visible
- Synthèse sonochimique en une étape facile et propriétés photocatalytiques des composites graphène/Ag3PO4 Quantum Dots
- Activité photocatalytique du nanocomposite ternaire attapulgite–TiO2–Ag3PO4 pour la dégradation de la Rhodamine B sous irradiation solaire simulée
- Fabrication et propriété photocatalytique de nouveaux nanocomposites SrTiO3/Bi5O7I



