Application multifonctionnelle du nanocomposite d'oxyde couplé Zn-Fe-Mn assisté par PVA
Résumé
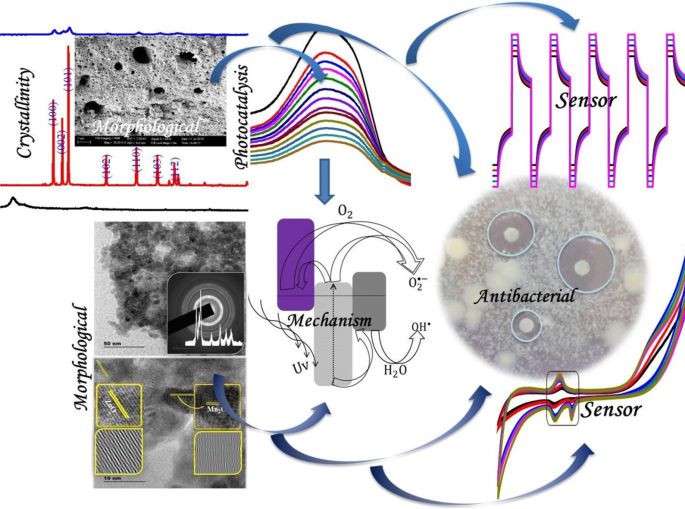
L'oxyde de zinc (ZnO) est un matériau semi-conducteur fascinant avec de nombreuses applications telles que l'adsorption, la photocatalyse, les capteurs et les activités antibactériennes. En utilisant un polymère poly (alcool vinylique) (PVA) comme agent de coiffage et des oxydes métalliques (fer et manganèse) en tant que couple, le matériau nanocomposite d'oxyde ternaire Zn/Fe/Mn poreux assisté par PVA (PTMO-NCM) a été synthétisé. Les propriétés thermiques, optiques, de cristallinité, de liaison chimique, de porosité, morphologiques et de transfert de charge des matériaux synthétisés ont été confirmées par DTG/DSC, UV-Vis-DRS, XRD, FT-IR, BET, SEM-EDAX/TEM-HRTEM- Techniques analytiques SAED et CV/EIS/ampérométrique, respectivement. Le PTMO-NCM a montré une surface spécifique et une capacité de transfert de charge améliorées, par rapport au ZnO. En utilisant le modèle XRD et l'analyse d'images TEM, la taille cristalline des matériaux a été confirmée comme étant dans la plage du nanomètre. La porosité et les capacités supérieures de transfert de charge du PTMO-NCM ont été confirmées par les analyses BET, HRTEM (IFFT)/SAED et CV/EIS. La cinétique d'adsorption (réaction d'adsorption/diffusion d'adsorption) et le test d'isotherme d'adsorption ont confirmé la présence d'une interaction de type chimisorption adsorbat/colorant bleu de méthylène-adsorbant/PTMO-NCM. Les performances photocatalytiques ont été testées sur les colorants rouge Congo et Acide Orange-8. La capacité supérieure de détection de l'acide ascorbique du matériau a été comprise à partir de l'analyse CV et ampérométrique. Les activités antibactériennes nobles du matériau ont également été confirmées sur les bactéries gram-négatives et gram-positives.
Introduction
Les nanoparticules d'oxyde de zinc (NP) sont couramment utilisées dans plusieurs domaines tels que l'adsorption [1], la photocatalyse [2, 3], la conservation des aliments [4] et les capteurs de polluants [5]. Par rapport à TiO2 , le coût de production du ZnO est d'environ 75 % inférieur et a une efficacité d'absorption plus élevée sur une grande partie du spectre solaire [6, 7]. L'application d'un oxyde métallique unique en tant que photocatalyseur est limitée à la propriété de transfert du chargeur en raison de la recombinaison électron/trou photogénérée. Cette recombinaison, en particulier dans la gamme nanométrique, conduit à la diminution de leur efficacité quantique et peut également conduire à la dissipation de l'énergie rayonnante en initiant des réactions hautement souhaitables [8, 9]. Parmi plusieurs efforts appliqués pour réduire le problème de recombinaison électron-trou tels que le dopage, l'hétérojonction, la sensibilisation aux colorants, les dépôts de métaux nobles et non nobles, la formation de matériaux à hétérostructure s'est avérée être l'une des préférences nobles [10,11,12]. Le couplage de ZnO avec d'autres oxydes métalliques a été signalé pour résoudre le problème de recombinaison mentionné [8, 13, 14, 15, 16]. En raison de leur stabilité et de leurs propriétés uniques, l'hématite (α-Fe2 O3 ) [8, 14] et Mn2 O3 [13] sont suggérés pour agir comme un couple décent avec ZnO.
En outre, le polymère PVA en tant qu'agent stabilisant a également une grande utilité pour diminuer les problèmes de recombinaison électron-trou [17]. Comme indiqué [18, 19], 500 °C est la température optimale pour éliminer les impuretés indésirables, y compris le polymère PVA après avoir agi comme agent de coiffage. La modification des matériaux synthétisés pour avoir une propriété mésoporeuse qui permet un processus de transfert de charge rapide a également été rapportée [20, 21]. En utilisant uniquement de l'eau sans danger pour l'environnement comme solvant et en développant une procédure de synthèse efficace, la toxicité, la capacité cancérigène et les propriétés mutagènes des solvants organiques peuvent également être éliminées.
Une petite variation du niveau standard d'acide ascorbique crée beaucoup de maladies chez les êtres humains [16]. Comme indiqué [22], l'acide ascorbique joue un rôle majeur dans le fonctionnement physiologique normal des organismes et est également utilisé comme traitement pour une autre maladie. Par conséquent, il est important de développer de nouvelles méthodes utilisées pour mesurer le niveau d'acide ascorbique. De nos jours, les nanomatériaux d'oxyde métallique sont largement utilisés comme applications de capteurs [23]. Parmi plusieurs techniques qui ont été développées pour améliorer les propriétés de détection du ZnO, la formation d'un composite avec d'autres oxydes métalliques et la modification des matériaux synthétisés pour avoir une propriété mésoporeuse qui permet un processus de transfert de charge rapide ont été rapportées [20, 21]. De plus, les infections nosocomiales causées par des micro-organismes deviennent des problèmes mondiaux [24]. Le ZnO est également répertorié comme agent antimicrobien et matériau sûr pour la conservation des aliments contre les maladies d'origine alimentaire par la FDA des États-Unis (21CFR182.8991) [4, 25].
Compte tenu de tous les aspects mentionnés de l'agrégation/agglomération, du rapport surface/volume et de la toxicité des solvants organiques, ce travail synthétise le PTMO-NCM assisté par PVA à l'aide d'un simple sol-gel suivi de techniques d'auto-propagation accidentelle. Le matériau tel que synthétisé a été caractérisé par des techniques analytiques DTG/DSC, XRD, BET, SEM–EDX/TEM/HRTEM/SAED et CV/EIS/ampérométrique. Une amélioration prononcée de la surface et de la capacité de transfert de charge a été obtenue pour le PTMO-NCM, par rapport au ZnO. L'applicabilité du PTMO-NCM couplé synthétisé a été testée sur l'adsorption et la dégradation de colorants organiques, l'activité antibactérienne et un capteur d'acide ascorbique.
Matériaux et méthodes
Les détails instrumentaux et les réactifs utilisés étaient présents comme matériel supplémentaire (S). Les procédures détaillées de synthèse du ZnO et du PTMO-NCM étaient également présentes dans les travaux antérieurs de l'auteur [1, 26, 27, 28]. Grossièrement, le polymère PVA a été dissous dans de l'eau distillée sous agitation continue sur un agitateur magnétique à ~ ~ ~ 115 °C pendant environ 15 min. Ensuite, les précurseurs du sel, Zn(NO3 )2 .6H2 O, Fe(NON3 )3 .9H2 O, et MnSO4 .H2 O ont été mélangés avec une solution de polymère PVA préalablement dissoute et refroidie sous agitation continue. Après deux jours de vieillissement suivis d'un séchage dans un four à environ 110 °C, le produit a été délicatement broyé pour réduire le matériau auto-propagé hautement amorphe. Enfin, il a été calciné à la température de calcination optimisée DTG de 500 °C pendant 3 h. Le processus de calcination à la température optimisée aide à éliminer les impuretés indésirables ainsi que le polymère PVA. Le PTMO-NCM synthétisé a été utilisé pour la caractérisation continue des échantillons et les tests d'application. L'expérience photocatalytique a été réalisée à l'aide d'une sonde de 176,6 cm 2 réacteur en verre circulaire sous une lampe à vapeur de mercure de 125 W. Les 20 ppm de 250 mL de colorants rouge Congo (CR) et acide orange-8 (AO8) et 0,06 g de photocatalyseur PTMO-NCM ont été utilisés pendant l'expérience. Le test d'adsorption a été réalisé en utilisant les paramètres d'adsorption optimisés expérimentalement [1], un temps de contact adsorbat-adsorbant de 10 à 150 min et 1 à 35 mg L −1 concentrations avec une vitesse d'agitation constante de 140 tr/min. Le test d'activité antibactérienne avait été réalisé en utilisant trois concentrations différentes (75, 100 et 125 μg mL −1 ) de ZnO et PTMO-NCM. L'expérience était accompagnée d'une méthode de diffusion sur disque utilisant une norme McFarland 0,5.
Résultats et discussion
Résultats de la caractérisation
La température de calcination optimale a été déterminée à 500 °C en utilisant l'analyse de stabilité DTG à 50 °C min −1 débit d'azote gazeux. Environ 56 % de la décomposition de l'échantillon a eu lieu et a laissé ~ 42 % de PTMO-NCM pur (Fig. 1a). D'après le tracé DSC (voir Fig. 1b), les deux pics exothermiques sont supposés être dus à l'évaporation des composants volatils adsorbés à 80 °C et aux changements de conformation à 144 °C. Le troisième pic endothermique apparu à environ 210 °C est probablement dû à la transformation de phase d'autres formes d'oxydes de fer ou/et de manganèse en Fe2 stable O3 et Mn2 O3 phase. Par rapport au ZnO, la chute de réflectance élevée dans la région visible pour le PTMO-NCM a été observée à partir de l'analyse spectroscopique UV-Vis-DRS (Fichier supplémentaire 1 :Fig. S1a). Cette analyse optique prend en charge la réduction de l'intensité maximale du motif XRD et l'interprétation de la porosité de l'image SEM. Les graphiques de Kubelka-Munk [29, 30] ont montré l'inexistence de changement de bande interdite entre ZnO et PTMO-NCM (Fichier supplémentaire 1 :Fig. S1b).
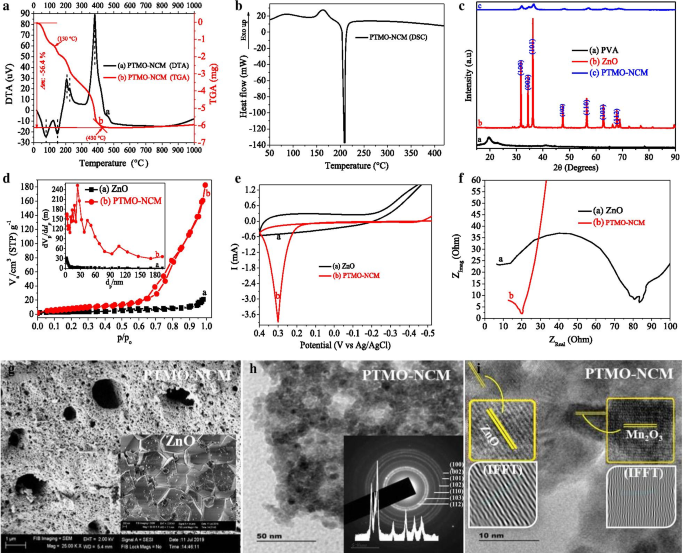
un DTG. b DSC. c XRD. d PARI. e CV. f parcelles EIS. g SEM. h TEM. je Images HRTEM de matériaux nanocomposites simples et ternaires de ZnO
La réduction notable de la taille cristalline moyenne approximative (6×) a été obtenue pour le PTMO-NCM, par rapport au ZnO (Fig. 1c). Les pics du motif XRD du ZnO et du PTMO-NCM sont cohérents avec la phase hexagonale du ZnO (ICSD :00-036-1451, groupe spatial P63mc (#186-1)). Ceci est probablement dû aux plus faibles pourcentages d'oxydes de fer (5 %) et de manganèse (5 %). L'absence de décalage des pics PTMO-NCM par rapport au ZnO montre également la non-apparition de distorsion structurelle sur le réseau ZnO. Ceci peut indiquer la présence d'une seule hétérojonction locale entre les oxydes métalliques ternaires [8, 31, 32]. Les données XRD et la taille respective des particules ont été calculées à l'aide de la formule de Debye-Scherrer (D = Kλ /(β cos(θ )), où est la longueur d'onde du rayonnement X (pour Cu 0,15418 nm), K est constant proche de l'unité, β est la pleine largeur à mi-hauteur (FWHM) en 2θ balances et θ est l'angle de la réflexion de Bragg considérée [33, 34].
Par rapport au ZnO, la grande amélioration de la surface pour PTMO-NCM (15×) et la nature poreuse de PTMO-NCM ont été approuvées à partir de l'analyse d'image BET et SEM, respectivement (voir Fig. 1d, g, (l'image en médaillon de la Fig. . 1 g est pour le ZnO)). Selon les classifications IUPAC, parmi six types d'isothermes d'adsorption (I-VI) et quatre types de boucles d'hystérésis, les tracés BET de ZnO et PTMO-NCM ressemblent à une isotherme IV typique et à une boucle d'hystérésis H3. La distribution moyenne approximative de la taille des pores BJH pour le ZnO et le PTMO-NCM a été déterminée à 9 et 26, respectivement, ce qui est cohérent avec la gamme mésoporeuse de la classification IUPAC [35]. La plus grande augmentation du courant dans l'analyse CV [36] (Fig. 1e) et le diamètre de demi-cercle plus petit du tracé de Nyquist dans les techniques EIS [37] (Fig. 1f) confirment les capacités de transfert de charge améliorées du PTMO-NCM sur ZnO. La taille cristalline nanométrique du PTMO-NCM a été confirmée à partir de l'image MET (Fig. 1h). La composition prévisible et l'actualité du PTMO-NCM ont été caractérisées par EDX (voir Fichier supplémentaire 1 :Fig. S2) et analyse HRTEM (Fig. 1i et ses encadrés), respectivement. Les valeurs d'espacement d (0,2864, 0,2543, 0,1969, 0,1663, 0,1520, 0,1419 et 0,1104) qui ont été déterminées à partir des anneaux SAED (Fig. 1h en médaillon) correspondent également au résultat du modèle XRD. Les défauts d'empilement sur l'image HRTEM (IFFT) et l'inexistence des taches de diffraction dans l'anneau SAED qui confirme la cristallinité des matériaux [38] confirme encore la nature poreuse du PTMO-NCM.
Adsorption de colorant bleu de méthylène
Le dosage optimisé de 0,02 g, un pH de 8 et une vitesse d'agitation constante de 140 tr/min ont été utilisés pour les études de cinétique d'adsorption-réaction et d'adsorption-diffusion [1]. Le coefficient de détermination (R 2 ) et les équations utilisées pour calculer le paramètre des modèles de cinétique d'adsorption ont été indiquées dans les graphiques respectifs en encart (Fig. 2). Parmi les modèles d'adsorption-réaction de pseudo-premier ordre (PFO) (Fig. 2b), de pseudo-second ordre (PSO) (Fig. 2c) et d'Elovich (Fig. 2d), le modèle PSO qui confirme les types de chimisorption d'adsorption s'adapte bien. De plus, la valeur théorique (9,43 mg g −1 ) et expérimental (9,91 mg g −1 ) les valeurs du modèle PSO ont une relation étroite contrairement à celle du PFO qui a les valeurs expérimentales de (3,64 mg g −1 ). Le modèle de diffusion intraparticulaire (IPD) semble bien s'adapter (Fig. 2e) ; cependant, pour dire que la réaction est sous le contrôle de l'adsorption-diffusion, son tracé linéaire doit passer par l'origine. Le tracé IPD pour ce travail ne passe pas par l'origine. De là, il est possible de conclure que la réaction est majoritairement sous le contrôle de l'adsorption-réaction. Cependant, le bon ajustement du modèle de Bangham (Fig. 2f) indique la présence d'une diffusion interstitielle dans le processus d'adsorption [39]. La présence de cette diffusion de pores est également cohérente avec les interprétations BET et SEM.
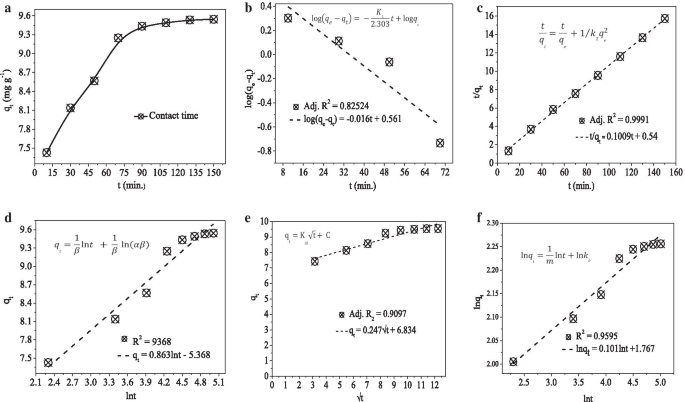
un Graphique de la cinétique d'adsorption. b Pseudo-premier ordre. c Pseudo-second ordre. d Élovitch. e Diffusion intraparticulaire. f Modèles de cinétique de Bangham
Le R 2 La valeur et les équations utilisées pour calculer le paramètre des modèles d'isotherme d'adsorption ont également été indiquées dans les graphiques respectifs en encart (Fig. 3). Selon le R 2 valeurs des modèles d'isothermes d'adsorption (Langmuir (Fig. 2a), Freundlich (Fig. 2b), Dubinin–Radushkevich (D–RK) (Fig. 2c), Temkin (Fig. 2d), Flory–Huggins (FH) (Fig. 2c), . 2e) et Fowler-Guggenheim (FG) (Fig. 2f)), les modèles de Langmuir et FH montrent un ajustement relativement meilleur. Du modèle de Langmuir, se trouvant le facteur de séparation R L une valeur comprise entre 0 et 1 (0,05) indique le caractère favorable du processus d'adsorption. La favorabilité du processus d'adsorption a également été confirmée par la valeur n (1,59) du modèle de Freundlich. Le bon ajustement du modèle de Langmuir indique la présence d'une couverture de colorant bleu de méthylène monocouche, ce qui est cohérent avec l'interprétation du modèle de cinétique PSO. La capacité d'adsorption maximale de l'adsorbant déterminée à partir du modèle d'isotherme de Langmuir est de 7,75 mg g −1 . L'indication de la couverture de surface caractéristique et de la spontanéité de la réaction (− 3,8 kJ mol −1 ) ont également été déduits de l'équation du modèle FH.
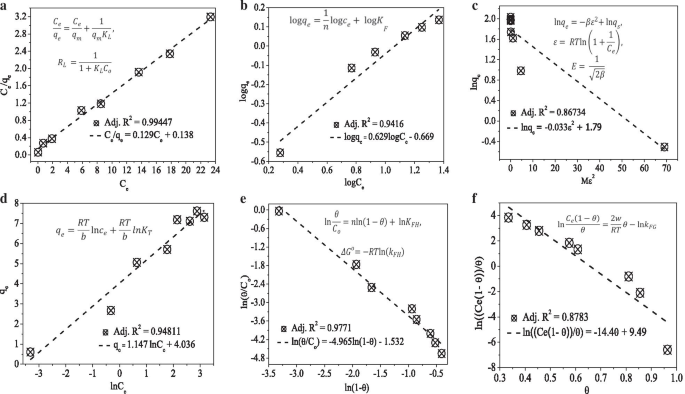
Graphiques des isothermes d'adsorption de a Langmuir. b Freundlich. c Dubinin–Radushkevich. d Temkin. e Flory–Huggins. f Modèles Fowler–Guggenheim
Dégradation et mécanisme du colorant rouge du Congo et orange acide-8
Les capacités de photodégradation du PTMO-NCM ont été étudiées sur la décoloration des colorants CR et AO8 à une longueur d'onde d'absorption maximale de 494 et 484 nm (Fig. 4a, b), respectivement. Au cours des 15 premières minutes, environ 17 % du colorant CR et 15 % de la dégradation du colorant AO8 ont eu lieu. À 180 min, la dégradation maximale de 70 % pour le colorant CR et de 68 % pour le colorant AO8 avait lieu. La constante d'équilibre obtenue k les valeurs pour les colorants CR et AO8 étaient de 0,007141 et 0,005627 min −1 , respectivement. Du point de contact de 1 − C /C o contre t et C /C o contre t graphiques (voir Fig. 4c, d), la valeur de demi-vie de dégradation obtenue était d'environ 105 min pour CR et 119 min pour AO8. Voir l'équation cinétique du PFO utilisée pour étudier la dynamique de réaction dans l'encart de la figure 4d.
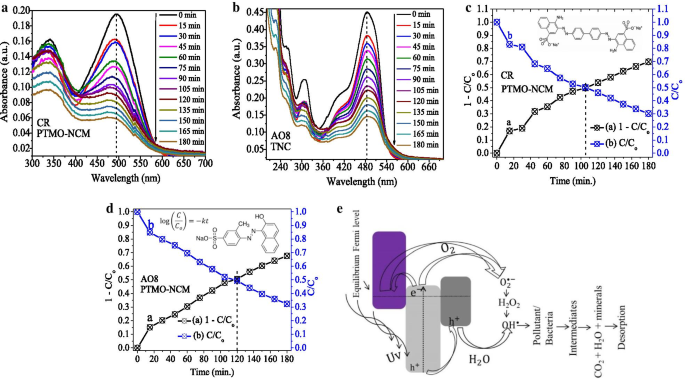
Activités photocatalytiques du PTMO-NCM :a , b courbes d'absorbance en fonction de la longueur d'onde. c , d 1 − C /C o contre t et C /C o contre t parcelles de CR et AO8, respectivement. e Mécanisme proposé
La position du bord de bande des oxydes métalliques dépend fortement de la charge de surface. Pour une réaction photocatalytique efficace, le fond du CB doit être plus négatif que le potentiel redox de H + /H2 et le sommet du VB doit être plus positif que le potentiel redox de O2 /H2 O [40, 41]. Comme rapporté [13], le CB de Mn2 O3 et ZnO sont proches l'un de l'autre. En outre, pour confirmer la présence d'une hétérojonction appropriée et la réalité de la synergie de transfert de charge appropriée, l'analyse utilisant des techniques électrochimiques telles que CV et EIS est importante [42]. Comme le montrent les analyses CV (Fig. 1e) et EIS (Fig. 1f), le PTMO-NCM montre la présence d'une hétérojonction appropriée. Par conséquent, le mécanisme photocatalytique possible a été proposé, comme le montre la figure 4e. Pendant l'hétérojonction, jusqu'à ce que le niveau de Fermi s'égalise, la bande d'énergie des oxydes métalliques commence à monter et descendre en transférant des électrons [8, 43] et conduit à la création d'une couche d'appauvrissement dans l'interface [44]. Le niveau de Fermi de type p Mn2 O3 existe près du VB. Lors d'une irradiation UV, les électrons photogénérés ont la probabilité soit de se localiser sur le ZnO CB soit de se diffuser vers le VB du Mn2 O3 , et les trous se déplacent vers le VB de Fe2 O3 . Par conséquent, la recombinaison des électrons et des trous a diminué et a entraîné une augmentation de l'activité photocatalytique [8].
À partir du graphique CV de PTMO-NCM (Fig. 5a), les pics de réaction de réduction ont été observés. Comme rapporté [45], cette réaction redox rapide et réversible est indiquée comme étant due à la nature poreuse des matériaux. Ceci est également cohérent avec les résultats de caractérisation BET et SEM. La différence de potentiel de crête approximative obtenue (ΔE a,c ) entre E pa (+ 0.401 V) et E ordinateur (+ 0,323 V) le pic est de 0,078 V. Ce plus petit ΔE a,c La valeur montre la capacité du matériau PTMO-NCM à être plus réversible. Avec une augmentation de la vitesse de balayage, les pics redox se sont déplacés positivement vers les potentiels anodique et cathodique. Comme le montrent le tracé CV de la figure 5b et le tracé d'ampérométrie de la figure 5c, la nouveauté du PTMO-NCM en tant que capteur d'acide ascorbique a également été confirmée, car l'augmentation de la concentration d'acide ascorbique entraîne une augmentation de l'augmentation du courant. La noblesse de détection du matériau a également été confirmée par l'analyse par ampérométrie car le cycle de détection a été achevé en quelques secondes. Les cycles ont été répétés pour évaluer la stabilité de l'électrode pendant 1 h. Le résultat obtenu confirme la stabilité et la reproductibilité de l'électrode PTMO-NCM.
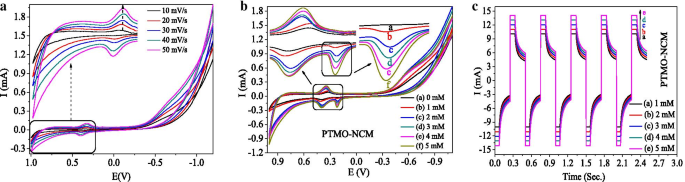
un Tracés CV à différentes vitesses de balayage. b Courbe de détection d'acide ascorbique CV à différentes concentrations. c Graphique de détection ampérométrique de l'acide ascorbique à différentes concentrations
L'activité antibactérienne des oxydes métalliques dépend fortement de la taille des particules [46] et des capacités de génération de ROS [47] des matériaux. En prenant différents pourcentages de précurseur et quantité de polymère PVA [26], les activités antibactériennes optimales de PTMO-NCM envers E. coli et S . aureus (Fig. 6a, b, respectivement) ont été déterminés à 50 % ZnO, 25 % Fe2 O3 , et 25 % Mn2 O3 . Les activités antibactériennes améliorées pour le PTMO-NCM ont été obtenues par rapport aux matériaux à base de ZnO simple et de ZnO binaire [27]. Le mécanisme d'activité antimicrobienne des NP peut suivre trois mécanismes [48], dont la libération d'ions antimicrobiens [25, 49], l'interaction des NP avec des micro-organismes [50] et la formation de ROS par l'effet du rayonnement lumineux [51] . Comme l'ont confirmé le modèle XRD et les spectres UV-Vis-DRS, la distorsion structurelle et le décalage de la position de la bande n'avaient pas été observés. L'absence de cette distorsion et de ce décalage est due à la non-intercalation de Fe 3+ /Mn 3+ ions. Cela indique que l'activité antimicrobienne due aux ions peut ne pas être le mécanisme approprié. Par conséquent, les voies directes et indirectes de génération de ROS [52] ont été proposées comme mécanisme d'activités antibactériennes, comme le montre la figure 6c.
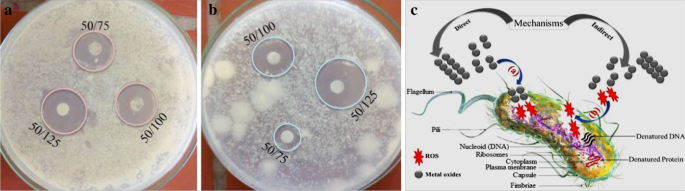
L'activité antibactérienne du PTMO-NCM envers a E. coli. b S. aureus. c mécanisme antibactérien (50/75 : 50 est le pourcentage de PTMO-NCM lors de la synthèse, 75 est la quantité utilisée en g/mL lors de l'activité antibactérienne)
Conclusions
Le PTMO-NCM qui a une porosité élevée, une surface spécifique améliorée et une capacité de transfert de charge supérieure a été synthétisé en utilisant le sol-gel suivi de techniques d'auto-propagation. En utilisant le modèle XRD et l'analyse d'images TEM, la taille cristalline moyenne approximative du PTMO-NCM a été déterminée comme étant comprise entre 10 et 60 nm. La taille cristalline du PTMO-NCM est six fois plus petite que celle du ZnO nu. Par rapport au ZnO, une amélioration de la surface de quinze fois pour le PTMO-NCM a été confirmée par l'analyse BET. La nature moins cristalline du PTMO-NCM a encore été confirmée par les défauts d'empilement présents sur l'image HRTEM (IFFT) et l'absence de taches de diffraction sur l'anneau SAED. Le diamètre semi-circulaire neuf fois plus petit sur l'EIS et une augmentation de courant accrue sur CV indiquent la présence de nouvelles propriétés de transfert de charge pour le PTMO-NCM, par rapport au ZnO. D'après l'étude de la cinétique d'adsorption et des isothermes d'adsorption, l'interaction adsorbat–adsorbant a été examinée comme étant de type chimisorption. À partir du modèle de Langmuir, la capacité d'adsorption maximale a été déterminée à 7,75 mg g −1 . Les constantes d'équilibre photocatalytique se sont avérées être de 0,007141 min −1 et 0,005627 min −1 pour les colorants CR et AO8, respectivement. La capacité de détection supérieure et les nobles activités antibactériennes du PTMO-NCM ont également été vérifiées.
Disponibilité des données et des matériaux
Les ensembles de données utilisés et/ou analysés au cours de la présente étude sont disponibles auprès de l'auteur correspondant sur demande raisonnable.
Abréviations
- PTMO-NCM :
-
Matériau nanocomposite d'oxyde métallique ternaire poreux
- UV– Vis-DRS :
-
UV– Spectroscopie de réflectance vis-diffuse
- FT-IR :
-
Spectroscopie infrarouge à transformée de Fourier
- XRD :
-
Diffraction des rayons X sur poudre
- SEM :
-
Microscopie électronique à balayage
- EDX :
-
Spectroscopie à rayons X à dispersion d'énergie
- TEM :
-
Microscopie électronique à transmission
- HRTEM :
-
Microscopie électronique à transmission haute résolution
- SAED :
-
Diffraction électronique à zone sélectionnée
- PARI :
-
Brunauer–Emmett–Teller
- CV :
-
Voltamétrie cyclique
- EIS :
-
Spectroscopie d'impédance électrique
- FH :
-
Flory–Huggins
- FG :
-
Fowler–Guggenheim
- PFO :
-
Pseudo-premier ordre
- PSO :
-
Pseudo-second ordre
- IPD :
-
Diffusion intraparticulaire
- CR :
-
Rouge Congo
- AO8 :
-
Orange acide-8
- IFFT :
-
Transmission de Fourier rapide inverse
- ROS :
-
Espèces réactives de l'oxygène
- S. aureus :
-
Staphylococcus aureus
- E. coli :
-
Escherichia coli
Nanomatériaux
- PBT résistant à l'hydrolyse qui est également transparent au laser brille dans les applications de moteur automobile exigeantes
- Revue sur l'application des biocapteurs et des nanocapteurs dans les agroécosystèmes
- Cibler les cellules endothéliales avec des nanoparticules GaN/Fe multifonctionnelles
- Croissance directe de structures de ZnO ressemblant à des plumes par une technique de solution facile pour une application de détection photo
- Biosécurité et capacité antibactérienne du graphène et de l'oxyde de graphène in vitro et in vivo
- Synthèse de nanocristaux de ZnO et application dans des cellules solaires polymères inversées
- Performances photocatalytiques induites par la lumière visible des nanocomposites ZnO/g-C3N4 dopés N
- Dépôt en couche atomique de nano-films d'oxyde d'indium pour transistors à couche mince
- Fabrication et caractérisation de nano-clips de ZnO par le procédé à médiation par polyol



