ARTICLE RÉTRACTÉ :Une étude comparative de la toxicité des nanosphères et des nanoparticules de ferrite de cobalt recouvertes de polyéthylèneglycol
Résumé
Nous présentons une étude comparative de la toxicité des nanoparticules et nanosphères de ferrite de cobalt enrobées de polyéthylène glycol (PEG). Les nanoparticules ont été préparées par la méthode hydrothermale tandis que les nanosphères ont été préparées par la technique solvothermique. La surface des nanomatériaux a été modifiée avec succès avec du polyéthylène glycol. Pour étudier la morphologie des échantillons préparés, des techniques de diffraction des rayons X (XRD), de spectroscopie infrarouge à transformée de Fourier (FTIR), de spectroscopie Raman, d'analyse thermogravimétrique (TGA) et de microscopie électronique ont été utilisées. Les analyses structurelles ont confirmé la formation de nanoparticules polycristallines de ferrite de cobalt avec des diamètres compris entre 20 et 25 nm et des nanosphères comprises entre 80 et 100 nm, respectivement. Des souris Kunming SPF (femelles, âgées de 6 à 8 semaines) ont été utilisées pour étudier la toxicité induite par les nanoparticules et les nanosphères de ferrite de cobalt dans différents organes des souris. Des études de biodistribution, des indices biochimiques, des évaluations histopathologiques, des facteurs inflammatoires, des niveaux d'oxydation et d'antioxydants et des tests de cytotoxicité ont été réalisés pour évaluer la toxicité induite par les nanoparticules et nanosphères de ferrite de cobalt chez la souris. Les nanosphères de ferrite de cobalt se sont avérées plus toxiques que les nanoparticules et la curcumine s'est avérée être un bon agent cicatrisant pour la toxicité induite par les nanomatériaux de ferrite de cobalt recouverts de PEG chez la souris.
Introduction
Ces dernières années, les nanomatériaux magnétiques ont suscité un immense intérêt tant dans la recherche fondamentale que dans les applications technologiques. Ces applications incluent, sans s'y limiter, les véhicules d'administration de médicaments [1,2,3], l'imagerie par résonance magnétique (IRM) [4,5,6], l'hyperthermie [7,8,9], les biocapteurs [10], les cellules séparation [11], séparations de protéines [11, 12], magnétofection de gènes [13, 14, 15] et pollution et assainissement de l'environnement [16, 17]. La ferrite de cobalt, en tant que matériau magnétique dur, est utilisée comme agent de contraste pour l'IRM, l'administration ciblée de médicaments et comme médiateur de chauffage dans l'hyperthermie [18,19,20,21,22,23]. Bien que la ferrite de cobalt soit utilisée dans des applications biomédicales, elle présente cependant certaines restrictions telles que sa toxicité élevée en raison de la quantité remarquable de cobalt libéré dans la solution, de l'agrégation en solution et de la mauvaise accessibilité de la surface lorsque des tensioactifs sont utilisés. Par conséquent, ce problème a été surmonté par l'utilisation de la modification de surface avec certains matériaux biocompatibles, non toxiques, stables à l'eau et dispersants [24,25,26,27,28]. De plus, la fabrication de ferrite de cobalt est facile et rentable avec des compositions, des formes et des tailles sur mesure pour toute application particulière. Il existe une variété de techniques adoptées pour la synthèse de ferrite de cobalt nanométrique, y compris mécanochimique [29], sonochimique [30], co-précipitation [31, 32], micro-émulsion [33] et autres [34,35,36,37 ,38]. De même, d'autres techniques, y compris une méthode écologique en une seule étape, ont été adoptées pour la fabrication de nanoclusters de cuivre fluorescent sur mesure en utilisant la curcumine comme modèle [39]. Un inconvénient majeur de la plupart de ces techniques est la faible cristallinité du matériau préparé, qui à son tour conduit à la détérioration significative des caractéristiques magnétiques. À cet égard, les techniques hydrothermales [40] et solvothermes [41] sont les techniques les plus efficaces et efficientes pour synthétiser la ferrite de cobalt avec des morphologies et des cristallinités contrôlées.
Dans la littérature, divers nanomatériaux tels que les nanoparticules d'argent (Ag NP) ont été rapportés comme étant utilisés pour le traitement antimicrobien et les maladies infectieuses associées, ainsi qu'ils sont utilisés comme nanovéhicules pour l'administration de médicaments et le traitement de différentes maladies [42]. Dans un autre article de synthèse, il a été rapporté que les ferrates étaient utilisés pour l'élimination de diverses espèces chimiques et biologiques des eaux usées [43]. Dans l'application biomédicale des nanomatériaux de ferrite de cobalt, le problème principal est l'accumulation de ferrite de cobalt dans les organes, entraînant une toxicité dans le corps qui nécessite l'élimination urgente des nanomatériaux collectés des organes et nécessite la guérison des dommages induits par la ferrite de cobalt. Plusieurs chercheurs ont étudié les médicaments anti-inflammatoires et ont découvert que ces médicaments peuvent réduire la toxicité induite par les nanomatériaux [44, 45]. La curcumine aux caractéristiques antioxydantes, antimutations, antitumorales et cancérigènes peut être utilisée comme agent cicatrisant pour la toxicité induite par les nanomatériaux de ferrite de cobalt [46,47,48]. Il a la capacité d'être utilisé comme bloqueur de TNF in vitro et in vivo en se liant directement au TNF [49].
L'objectif de ce travail était de fabriquer des nanoparticules et des nanosphères de ferrite de cobalt enrobées de polyéthylène glycol (PEG) dans les laboratoires avec des morphologies contrôlées. Différentes doses de nanomatériaux ont été injectées par voie intraveineuse aux souris et des analyses sanguines, la biodistribution, la coloration HE et la viabilité cellulaire étudiées ont été effectuées pour évaluer la toxicité de ces nanomatériaux. Une comparaison de la toxicité des nanoparticules et des nanosphères de ferrite de cobalt a été effectuée et la curcumine a été utilisée comme agent cicatrisant pour la toxicité induite par les nanosphères de ferrite de cobalt chez la souris. Il a été montré que les nanosphères de ferrite de cobalt sont plus toxiques que les nanoparticules en raison de leurs surfaces agrandies, ce qui les rend plus toxiques et plus réactives que les nanoparticules. À notre connaissance, il s'agit de la première étude détaillée de ce type qui n'a pas été réalisée auparavant.
Matériaux et méthodes
Préparation de nanomatériaux
Pour la préparation de nanoparticules de ferrite de cobalt recouvertes de PEG, nous avons adopté la technique hydrothermale [40, 47]. À cette fin, des solutions de chlorure de cobalt (0,2 M) et de nitrate ferrique (0,4 M) ont été préparées séparément dans 25 mL d'eau désionisée (DI) chacune, puis ces solutions ont été mélangées avec 25 mL de solutions aqueuses de polyéthylène glycol (2,5 mM) et hydroxyde de sodium (3 M), respectivement. Le mélange a ensuite été agité pendant 20 min et versé dans l'autoclave en acier inoxydable (SS) qui a été chauffé à 180 °C pendant 6 h. Une fois le processus terminé, le mélange a été refroidi à température ambiante, puis la solution a été lavée 2 à 3 fois avec de l'eau DI et de l'éthanol pour éliminer toutes les impuretés indésirables du mélange. Le mélange a été séché à environ 80 °C pendant la nuit dans le four, puis broyé en poudres fines pour obtenir les nanoparticules de ferrite de cobalt souhaitées.
Pour la préparation de nanosphères de ferrite de cobalt revêtues de PEG, la technique solvothermique a été utilisée. A cet effet, du chlorure de cobalt hexahydraté a été dissous dans 40 mL d'éthylène glycol (2,5 mM) qui a été suivi par l'ajout de 1,35 g de chlorure de fer hexahydraté et 1 g de polyéthylène glycol (PEG). Le mélange a ensuite été agité pendant environ 30 min puis scellé dans un autoclave en acier inoxydable revêtu de téflon. L'autoclave a ensuite été chauffé à 200 °C pendant 8 h et après avoir terminé la réaction, il a ensuite été refroidi à température ambiante. Le mélange a été lavé avec de l'eau déminéralisée et de l'éthanol, puis séché à 80°C pendant une nuit dans le four. Enfin, le mélange a été broyé en poudres fines pour obtenir des nanosphères de ferrite de cobalt recouvertes de PEG avec des diamètres compris entre 80 et 100 nm. La morphologie des nanomatériaux préparés a été étudiée par diffraction des rayons X (XRD) selon la méthode utilisée dans la réf. [50], la microscopie électronique à balayage et à transmission (MEB et MET) telle qu'utilisée dans la réf. [50, 51], spectroscopie infrarouge à transformée de Fourier (FTIR) à température ambiante pour la détermination de groupes fonctionnels dans la ferrite de cobalt similaires à la réf. [51], la spectroscopie Raman et l'analyse thermogravimétrique (TGA) utilisée dans la réf. [52].
Marquage radioactif des nanomatériaux
Le radiomarquage des nanoparticules et nanosphères de ferrite de cobalt enrobées de PEG a été réalisé avec 99m Tc utilisant le chlorure stanneux comme agent réducteur [53,54,55]. A cet effet, frais 99m TcO4 l'éluat du générateur (50 μL avec une activité 4 mCi) a été préparé en l'ajoutant à 30 μL de SnCl2 suspension (1 mg/mL dans 0,5 N HCl). Avec l'aide de NaHCO3 (1 M), le pH de la suspension a été ajusté dans la gamme 8-10. Des solutions de nanoparticules et de nanosphères (40 μL chacune) contenant ~ 0,4% en poids de ferrite de cobalt ont été mélangées avec des suspensions de chlorure stanneux (50 μg), d'acide ascorbique (10 mg/mL) et de 99m TcO4 . Le mélange a ensuite été agité à 10 000 rpm pendant 25 min à 80 °C. Pour des mesures précises, les comptages radioactifs ont été enregistrés dans les 24 h en raison de la courte durée de vie de 99m Tc (~ 6 h). Le surnageant a ensuite été décanté après la centrifugation et le matériau restant a été identifié comme étant 99m Nanoparticules et nanosphères de ferrite Tc-PEG-cobalt. Un chromatogramme sur papier a été utilisé pour mesurer les rendements radioactifs des composés marqués, qui étaient supérieurs à 65 % et reflétaient la biodistribution réelle des nanomatériaux chez les souris in vivo.
Biodistribution des nanomatériaux
Comme indiqué sur la figure 1, des souris Kunming SPF (femelles, âgées de 6 à 8 semaines, poids de 18 à 20 µg) ont été obtenues auprès du Laboratory Center for Medical Science, Université de Lanzhou, Chine. Toutes les souris ont été maintenues dans des cages sous le système de contrôle de température maintenu à 21-22 °C et les lumières ont été allumées de 08h00 à 20h00. Un accès gratuit à la nourriture et à l'eau du robinet a été donné aux souris et elles ont été manipulées selon les protocoles du Laboratoire de soins aux animaux formulés par la National Society of Medical Research et les directives des National Institutes of Health des États-Unis. Les souris ont été réparties au hasard en plusieurs groupes, chaque groupe contenant 5 souris, puis elles ont reçu une injection intraveineuse de 99m Solutions de ferrite Tc-PEG-cobalt de nanoparticules et de nanosphères et tuées après 1 h, 6 h, 16 h et 24 h, respectivement. Les tissus du cœur, des poumons, du foie, de la rate et des reins ont été immédiatement disséqués, enveloppés dans du papier d'aluminium, pesés, puis la radioactivité de 99m La Tc dans chaque tissu a été mesurée à l'aide d'un détecteur de compteur gamma. La biodistribution des nanomatériaux dans différents organes de souris a été présentée en pourcentage de dose injectée par gramme de tissu humide (c'est-à-dire % ID/g).
Schéma de principe du modèle expérimental
Coloration à l'hématoxyline et à l'éosine
Pour la coloration à l'hématoxyline et à l'éosine (HE), la cire de paraffine a été coupée en tranches dans du xylène pour le déparaffinage et le processus a été répété deux fois pendant environ 10 min chacune. L'hydratation de l'échantillon a été réalisée en transférant les lames à travers différentes solutions d'éthanol avec des concentrations de 100 % d'éthanol, 95 % d'éthanol et 70 % d'éthanol chacune pendant 2 min. Rincer les lames sous l'eau du robinet à température ambiante pendant environ 2 min et lorsque le processus est terminé, les noyaux ont été colorés dans une solution de coloration à l'hématoxyline à 60 °C pendant 10 s puis à température ambiante pendant 1 min et les lames ont ensuite été placées sous l'eau courante du robinet à température ambiante pendant environ 5 min. Colorer les échantillons dans une solution d'éosine Y de travail pendant 2 min, puis déshydrater les échantillons d'abord en les trempant dans de l'éthanol à 95 %, puis dans de l'éthanol à 100 % chacun pendant 2 min. Le cytoplasme a été coloré pendant 7 s par immersion dans une solution de coloration à l'éosine pendant 15 s. Après le retrait, le cytoplasme a été lavé et déshydraté avec de l'éthanol absolu deux fois pendant 1 min chacune. Le tissu a ensuite été rendu transparent avec du xylène pendant 15 s et le cytoplasme a été examiné puis photographié à l'aide de joints gingivaux neutres. L'examen microscopique des tissus a été réalisé à l'aide du microscope Olympus Microphot-CX41 couplé à un appareil photo numérique.
Indices biochimiques et facteurs inflammatoires
Deux cent cinquante microgrammes de nanoparticules et de nanosphères de ferrite de cobalt recouvertes de PEG ont été injectés par voie intraveineuse aux souris du groupe d'exposition tandis que le groupe témoin a été traité avec une solution saline normale à 0,9% et toutes les souris ont ensuite été tuées après 24 h. Du sang a été prélevé sur les souris et centrifugé pendant environ 10 min pour obtenir le sérum sanguin. Les teneurs sériques en TB, ALT, AST, BUN, CREA et Cys-C ont été mesurées par le test ELISA (enzyme-linked immunosorbent assay) et western blot. Les enzymes liées au foie, IL-6, IL-8 et TNF-α, jouent un rôle clé dans la réponse inflammatoire induite par la nécrose. Habituellement, des niveaux élevés de ces expressions se produisent lorsqu'un organe répond à l'inflammation.
Test de viabilité cellulaire MTT
Les potentiels cytotoxiques des nanoparticules et nanosphères de ferrite de cobalt enrobées de PEG ont été déterminés par MTT, un test colorimétrique pour évaluer les activités métaboliques cellulaires. Des cellules épithéliales humaines L-132 et des monocytes humains THP-1 achetés à Shanghai, en Chine, ont été exposés à différentes concentrations de nanoparticules comprises entre 30 et 125 g/mL et de nanosphères comprises entre 50 et 250 μg/mL et la densité optique était mesurée à 590 nm pour différents dosages à l'aide d'un système de spectrophotomètre à microplaque (UNICO WFZ UV-2000, Shanghai, Chine). Les cellules L-132 ont été sélectionnées car l'inhalation est une voie majeure d'exposition aux nanomatériaux et les cellules THP-1 ont été utilisées en raison de leur rôle dans l'élimination des matières étrangères. Dans chaque essai, les cellules non traitées ont été évaluées en tant que contrôle négatif. L'inhibition de l'activité enzymatique a été observée dans les cellules, qui a été comparée aux cellules non traitées (témoin négatif) et les valeurs ont été dérivées sous forme de rapport du contrôle négatif et tracées en fonction de la concentration de nanoparticules et de nanosphères.
Analyse statistique
Chaque point de données a été rapporté comme la valeur moyenne (±sem) des expériences réalisées en triple. L'importance des différences a été évaluée à l'aide de l'analyse de la variance et des graphiques statistiques ont été établis à l'aide des logiciels Origin et Microsoft Excel.
Résultats et discussion
Analyse structurelle
Les analyses structurelles (XRD, FTIR, Raman et TGA) des nanomatériaux préparés sont illustrées à la figure 2. Les résultats XRD de la figure 2a représentent la ferrite de cobalt revêtue et non revêtue à l'échelle nanométrique, ce qui confirme que la ferrite de cobalt a été fabriquée avec succès. Les positions et les intensités relatives de tous les pics observés dans les données XRD confirment la nature cristalline de la ferrite de cobalt. Aucun pic supplémentaire n'a été observé, ce qui indique la pureté de la ferrite de cobalt préparée. La taille moyenne des cristallites de la ferrite de cobalt a été déterminée en utilisant l'équation de Scherrer [56], qui s'est avérée être d'environ 24 nm. Une spectroscopie infrarouge à transformée de Fourier (FTIR) a été réalisée pour étudier la distribution des cations (du nickel, du cobalt et du fer) dans la ferrite de cobalt. La figure 2b indique les données FTIR collectées à température ambiante. Théoriquement, la ferrite de cobalt a deux bandes d'absorption fortes (ʋ1 et ʋ2 ) ainsi que quelques autres apparaissant dans la plage 400–600 cm −1 . Tous ces pics sont clairement indiqués dans nos données présentées sur la figure 2b. Dans les données FTIR, 1 correspond aux vibrations d'étirement intrinsèques du métal aux sites tétraédriques, alors que ʋ2 correspond aux vibrations d'étirement des ions métalliques au niveau des sites octaédriques [57,58,59]. Le pic apparaissant en FTIR à 3421 cm −1 correspond au polyéthylène glycol (PEG) qui indique son adhésion réussie à la surface de la ferrite de cobalt. L'analyse Raman de la ferrite de cobalt collectée à température ambiante est illustrée à la figure 2c, qui indique 5 pics différents pouvant être observés dans les données. Le pic apparaissant en dessous de 700 cm −1 est le pic caractéristique principal (A 1g mode) de ferrite de cobalt qui correspond à l'étirement des ions oxygène le long des liaisons Fe–O aux sites tétraédriques [60], tandis que les autres pics apparaissant dans les données appartiennent également à la ferrite de cobalt. Cela confirme la fabrication réussie de ferrite PEG-cobalt dans notre expérience. La figure 2d montre les résultats TGA des échantillons prélevés dans la plage de températures de 50 à 380 °C, ce qui indique que la ferrite de cobalt perd de son poids à différentes températures. Il est également évident dans l'analyse TGA que la stabilité thermique du PEG est relativement faible alors que celle du PEG-ferrite de cobalt est élevée.
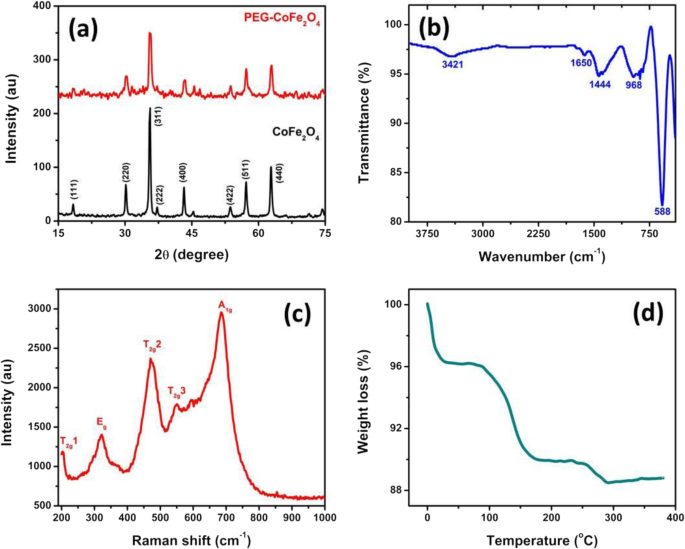
un Résultats XRD de la ferrite de cobalt. b Spectroscopie infrarouge à transformée de Fourier (FTIR) utilisée dans la gamme 500-4000 cm −1 . c Spectre Raman à température ambiante des échantillons prélevés dans 190–1000 cm −1 gamme de fréquences. d Analyse thermogravimétrique (TGA) de CoFe enrobé de PEG2 O4 collecté dans la plage de température 50–400 °C
Les analyses par microscopie électronique des échantillons sont illustrées à la figure 3. Les figures 3 (a) et (b) indiquent les images SEM de nanoparticules et de nanosphères de ferrite de cobalt recouvertes de PEG, respectivement, tandis que les figures 3 (c) et (d) indiquent les analyses MET des nanosphères et des nanoparticules, respectivement. Ces résultats montrent que la taille moyenne des nanoparticules est d'environ 25 nm et celle de la nanosphère est de 80-100 nm. D'après les images MET de nanosphères, il est évident que les nanosphères sont composées d'un grand nombre de nanoparticules plus petites avec de grandes surfaces, ce qui les rend mésoporeuses, ce qui est hautement souhaitable pour les applications médicales des nanomatériaux en tant que véhicules de transport de médicaments. Toutes ces analyses structurelles confirment la formation réussie de nanoparticules et nanosphères de ferrite de cobalt enrobées de PEG en phase pure.

SEM de nanoparticules de ferrite de cobalt (a ) et les nanosphères (b ). Images MET de nanoparticules de ferrite de cobalt recouvertes de PEG (c ) et les nanosphères (d ), collectées à différentes résolutions
Études de biodistribution
Quantitativement, la biodistribution des nanoparticules et nanosphères de ferrite de cobalt enrobées de PE dans le sang, le cœur, le foie, la rate, les poumons et les reins après différents intervalles de temps (1, 6, 16 et 24 h) est illustrée à la Fig. 4. Le la présence de ferrite de cobalt dans le sang et d'autres organes a été évaluée dans les 24h après l'injection intraveineuse de 99m Solution de ferrite Tc-PEG-cobalt (nanoparticules et nanosphères). Dans le cas des nanosphères illustrées à la figure 4 (a), la rétention sanguine de ferrite de cobalt s'est avérée être de 6,5 ± 0,33 % ID/g après 1 h d'exposition, puis elle a progressivement diminué au cours des intervalles de temps suivants (c'est-à-dire, 6, 16 et 24 h). On a vu que les nanosphères étaient principalement distribuées dans le cœur, le foie, la rate, les poumons et les reins; cependant, la plupart d'entre eux étaient principalement accumulés dans la rate. De plus, la biodistribution des nanosphères dans divers organes s'est avérée être la plus élevée après la première heure puis a diminué progressivement et est restée inférieure à 30 % après 6 h. Dans le cas des nanoparticules de ferrite de cobalt, la rétention sanguine des nanoparticules était d'environ 2,8 ± 0,14% ID/g après 1 h d'exposition, indiquant une élimination relativement rapide des matières radioactives de la masse sanguine du corps, puis elle diminuait avec le temps comme le montre la figure 4(b). Les nanoparticules étaient distribuées dans le cœur, le foie, la rate, les poumons et les reins avec des concentrations maximales dans la rate et le foie. Il ressort clairement de la figure que la biodistribution des nanoparticules dans le sang et d'autres organes était la plus élevée après la première heure, puis diminuait progressivement après 6 h et atteignait finalement les valeurs les plus faibles après 24 h. Si nous comparons les résultats de biodistribution des nanosphères et des nanoparticules, on constate que l'accumulation/la présence de nanosphères de ferrite de cobalt recouvertes de PEG dans le sang et d'autres organes des souris était plus importante que celle des nanoparticules. Cela pourrait être associé à une grande surface et à une porosité élevée des nanosphères par rapport aux nanoparticules, qui est l'un des facteurs critiques pour déterminer la réactivité des interactions des nanomatériaux avec les systèmes biologiques. Dans le cas des nanoparticules, leur nature non mésoporeuse à faible surface spécifique les rendait moins réactives que les nanosphères dans les mêmes conditions. Ces caractéristiques pourraient avoir réduit la résistance prolongée des nanoparticules de ferrite de cobalt recouvertes de PEG dans le sang et d'autres organes de souris. De plus, les nanosphères provoquent la formation de complexes avec des biomolécules et entraînent un niveau accru d'espèces radicalaires, augmentant le niveau de stress oxydatif, endommageant l'ADN cellulaire et entraînant le stress oxydatif par peroxydation lipidique.
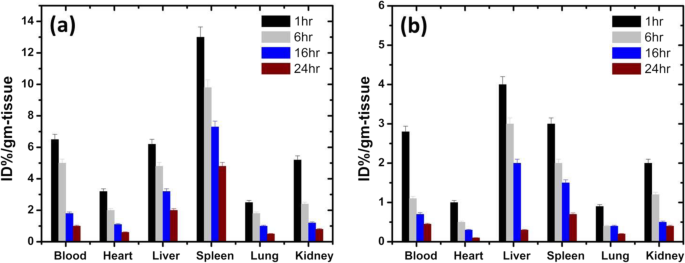
Biodistribution du PEG-CoFe2 O4 dans le sang, le cœur, le foie, la rate, les poumons et les reins après différents intervalles (1, 6, 16, 24 h) exposés à des nanosphères (a ) et des nanoparticules (b )
Indices biochimiques
Pour étudier l'effet de toxicité des nanoparticules et des nanosphères de ferrite de PEG-cobalt chez la souris, des indices biochimiques ont été mesurés et les résultats sont présentés sur la figure 5. Divers paramètres, notamment ALT, AST, BUN, CREA, TB et Cys-C ont été mesurés pour les souris des groupes témoins et exposés. Le logiciel SPSS a été utilisé pour l'extraction des données avec *P <0,05 qui représente des changements significatifs au cours des mesures. Dans les nanosphères et les nanoparticules, on constate que tous les indices biochimiques montrent des changements significatifs par rapport aux souris du groupe témoin (*P <0,05). Dans le cas d'un groupe d'exposition aux nanosphères de ferrite de cobalt, les niveaux d'ALT, d'AST et de BUN présentent des différences significatives (*P <0,05) par rapport aux souris du groupe témoin, alors que dans le cas du groupe d'exposition aux nanoparticules, seul Cys-C présente une différence significative par rapport aux souris du groupe témoin (*P <0,05). On constate que la TB et la Cys-C qui sont principalement responsables du biomarqueur de la fonction rénale ont diminué de manière significative dans le cas des nanosphères. Cela suggère que le rein est davantage affecté par l'exposition des nanosphères de ferrite PEG-cobalt par rapport aux nanoparticules. L'AST, en tant que biomarqueur du foie, était davantage affecté par l'exposition à la fois aux nanoparticules et aux nanosphères. Cela suggère que l'exposition à la ferrite de cobalt peut nuire à la fonction hépatique. D'après tous ces résultats, il est clair que les nanosphères de ferrite PEG-cobalt créent plus de dommages chez les souris in vivo que les nanoparticules de ferrite de cobalt.
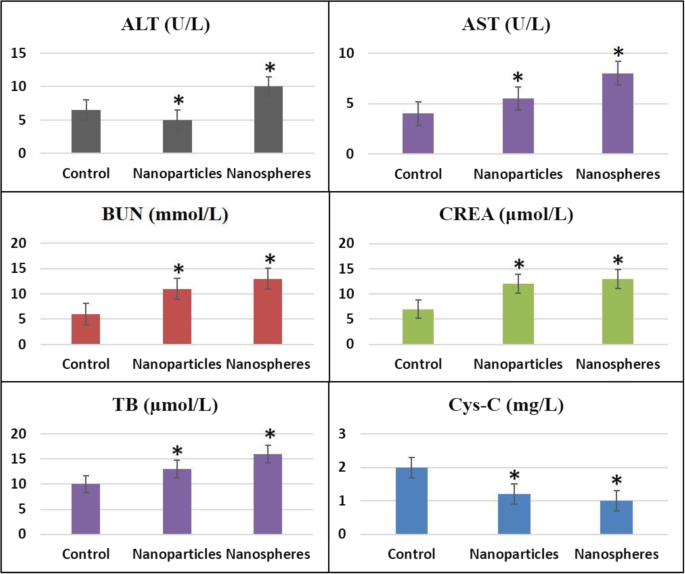
Indices biochimiques dans le sérum sanguin des souris du groupe témoin, exposé aux nanoparticules et aux nanosphères. Les données représentent la moyenne ± S.D de deux expériences indépendantes réalisées en triple. *P <0.01
Étude histopathologique
Nous avons présenté une analyse histopathologique des souris du groupe contrôle, nanoparticule, nanosphère et traitement, comme le montre la figure 6. Si nous comparons les résultats des groupes d'exposition aux nanosphères et aux nanoparticules avec les souris du groupe contrôle, on constate que les nanosphères de ferrite PEG-cobalt sont produisant plus de dommages dans différents organes (foie, rate, rein et poumon) de souris par rapport au groupe d'exposition aux nanoparticules. Dans le rein, une congestion glomérulaire s'est produite, ainsi qu'un léger œdème et des cellules d'inflammation interstitielle sont observés en cas d'ingestion de nanosphères par rapport à l'exposition aux nanoparticules et aux souris du groupe témoin. On constate également que les nanoparticules présentent moins d'inflammation que les nanosphères. En cas d'exposition aux nanoparticules, il a été constaté que les poumons sont relativement moins touchés alors que dans le cas des nanosphères, la paroi alvéolaire s'est avérée épaissie et une légère fibrose a été observée. De plus, pour le groupe d'exposition aux nanosphères, les hépatocytes présentent un gonflement et un œdème s'est produit, alors que relativement moins d'inflammation a été trouvée dans le cas des souris du groupe d'exposition aux nanoparticules.
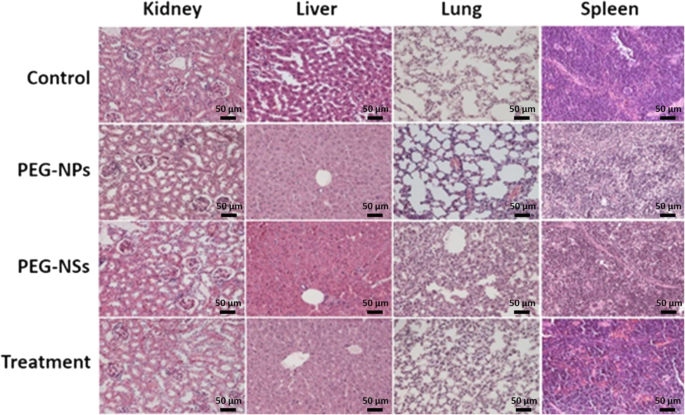
Coupes histologiques des tissus de différents groupes (contrôle, nanoparticules, nanosphères et traitement)
Facteurs inflammatoires et niveau d'oxydation/antioxydant
Les niveaux d'expression d'IL-6, IL-8, TNF-α, MDA et T-AOC ont été mesurés et les résultats sont présentés sur la figure 7. La figure 7a représente les bandes western blot d'IL-6, IL-8, et la β-actine pour les groupes d'exposition de contrôle, de nanoparticules et de nanosphères. Le niveau relatif de protéines d'IL-6 et d'IL-8 pour les groupes d'exposition de contrôle, de nanoparticules et de nanosphères est indiqué sur la figure 7b, tandis que les contenus de TNF-α, MDA et T-AOC sont indiqués sur la figure 7c- e avec *P <0,05 pour le groupe exposé versus groupe témoin ± sem. Les résultats ont révélé que les niveaux d'IL-6, IL-8, TNF-α et MDA pour les souris du groupe d'exposition aux nanosphères de ferrite de cobalt sont plus élevés que ceux du groupe de nanoparticules et que ces deux niveaux sont plus élevés que les souris du groupe témoin. Dans le cas du T-AOC, le niveau de nanosphères était inférieur à celui de l'exposition aux nanoparticules et des souris du groupe témoin. Tous ces résultats indiquent que les nanoparticules et les nanosphères provoquent une inflammation chez la souris, notamment au niveau du foie. Cependant, les nanosphères affectent davantage les organes que les nanoparticules. Il a bien compris que les nanomatériaux dans le corps génèrent des radicaux libres d'oxygène (ROS), qui provoquent une série de réductions qualitatives des antioxydants, entraînant des dommages d'oxydation des tissus biologiques qui affectent négativement les organismes cellulaires [61, 62]. De plus, lorsque les niveaux d'IL-6, IL-8, TNF-α, MDA et T-AOC pour les souris exposées aux nanoparticules ont été comparés à ceux exposés aux nanosphères, il a été constaté que les nanosphères de ferrite de cobalt entraînaient plus d'inflammation. par rapport aux souris du groupe d'exposition aux nanoparticules.
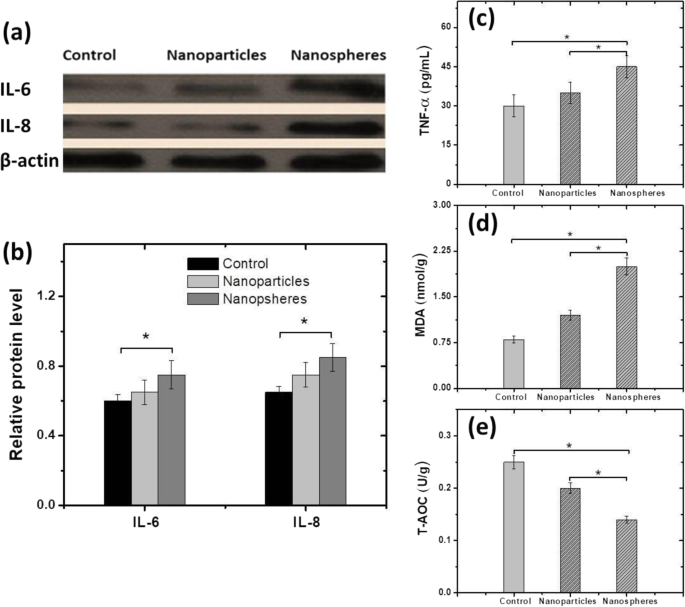
Expressions d'IL-6, IL-8, TNF-α, MDA et T-AOC. un Bandes Western blot pour l'IL-6, l'IL-8 et la -actine dans les groupes d'exposition de contrôle, de nanoparticules et de nanosphères. b Niveaux d'expression relatifs de l'IL-6 et de l'IL-8. c Contenu de TNF-α. d niveau MDA. e Tableau statistique de la teneur en T-AOC des groupes témoins et exposés (nanoparticules et nanosphères). (*P <0,05 pour les groupes exposés versus groupe témoin ± sem)
Évaluation de la cytotoxicité
Les études de cytotoxicité pour différentes concentrations de nanosphères et de nanoparticules de ferrite de cobalt recouvertes de PEG ont été réalisées et les résultats sont présentés sur la figure 8. Le pourcentage de survie des cellules L-132 est indiqué sur la figure 8(a), tandis que la figure 8 (b) représente le pourcentage de survie des cellules THP-1. On voit que pour des concentrations supérieures à 100 g/mL, il y a des changements significatifs dans la viabilité cellulaire observée pour les deux cellules, et on voit que les résultats sont plus prononcés dans le cas des nanosphères de PEG. Cela confirme que les nanosphères de ferrite de cobalt produisent plus de dommages que les nanoparticules. De plus, la viabilité cellulaire diminue avec l'augmentation de la concentration de nanoparticules et de nanosphères, ce qui indique que la ferrite de cobalt recouverte de PEG sous les deux formes produit plus de toxicité chez les souris avec une concentration croissante. En raison des deux cibles cellulaires différentes (L-132 et THP-1), on peut s'attendre à ce que la réponse cellulaire ne soit pas identique, en fonction du mécanisme de mort cellulaire [63]. Une raison possible pour expliquer les spécificités des cibles cellulaires même pour des tailles de particules similaires peut être attribuée à la fonction de phagocytose, qui caractérise les monocytes (cellules THP-1), mais pas les cellules épithéliales pulmonaires [64]. Il est bien entendu qu'une seule nanosphère est composée d'un grand nombre de petites nanoparticules. Ainsi, il possède une grande surface spécifique par rapport aux nanoparticules et, par conséquent, il a plus de réactivité et plus de chances d'interaction avec les systèmes biologiques (tissus) par rapport aux nanoparticules. De plus, en raison de la plus grande taille des nanosphères, elles ne peuvent pas être facilement sécrétées par la circulation sanguine ou urinaire une fois qu'elles pénètrent dans l'organe. Par conséquent, ils restent dans le corps (organes) pendant un temps relativement plus long que les nanoparticules, qui à leur tour affectent négativement les tissus. De plus, les nanosphères entraînent une fonction réduite des macrophages, une phagocytose réduite des nanosphères elles-mêmes, ainsi qu'une mobilité réduite des macrophages et un dysfonctionnement du cytosquelette.
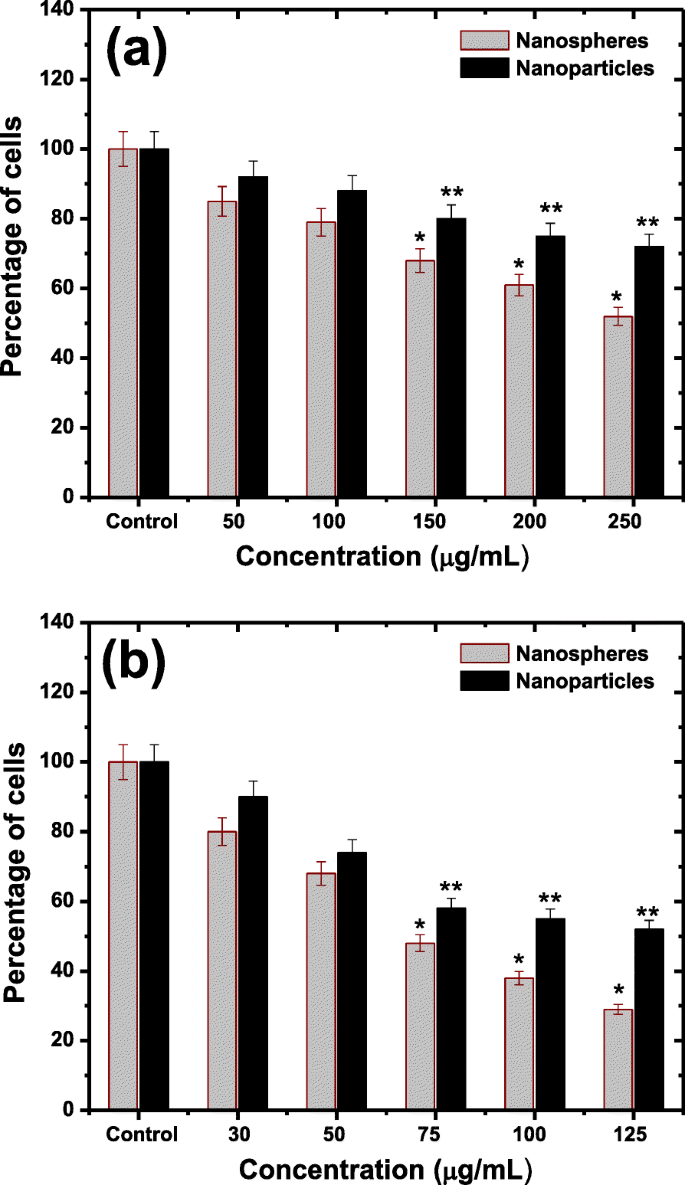
Cytotoxicité des nanoparticules et nanosphères de ferrite de cobalt enrobées de PEG dans les cellules L-132 (a ) et les cellules THP-1 (b ). *P <0,01 et ***i>P <0,05 pour les deux cellules par rapport aux témoins non traités. Les données représentent la moyenne ± S.D de deux expériences indépendantes réalisées en triple
Effet de la curcumine sur la toxicité
Biochemical indexes in blood serum were studied for nanosphere exposure group and curcumin-treated group and the results were compared with control group mice, which are shown in Fig. 9. It was found that all these indices in the treatment group mice showed significant improvements after the administration of curcumin when compared their values with nanosphere exposure and control group mice. In the figure, it is seen that the expression levels of ALT, AST, BUN, CREA, CYS-C, and TB were approached towards the normal values after the administration of curcumin. This can be attributed to the fact that curcumin has strong antioxidant characteristics which reduces the oxidative stress produced as a result of the toxicity induced by cobalt ferrite [47]. It has also been reported that TNF-α and IL-1 play important role in the induction of hepatic necrosis and curcumin reduces the effect of toxicity by inhibiting the secretion of TNF-α and IL-1 by macrophages [48], similar to the work reported earlier in Ref. [65].
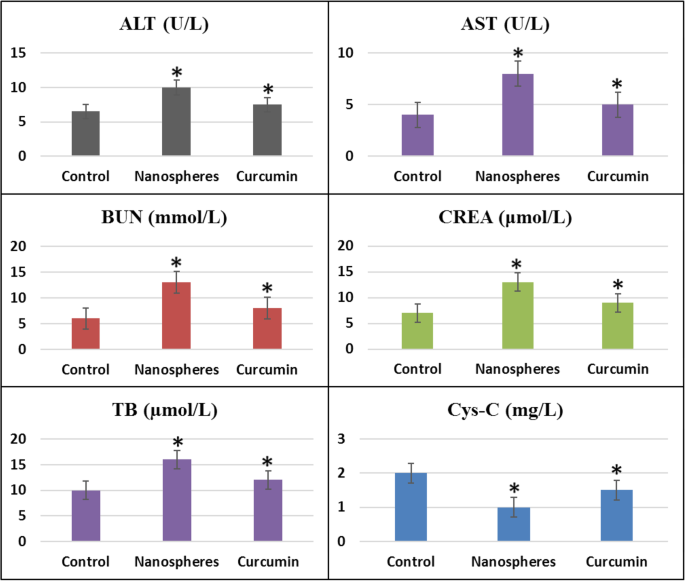
Biochemical indexes in blood serum of the control, nanosphere exposure, and treatment group mice (*P <0.05 compared with untreated controls)
Conclusion
In this work, we successfully fabricated PEG-coated cobalt ferrite nanoparticles and nanospheres via hydrothermal and solvothermal methods, respectively. From structural analyses, it was found that the prepared nanomaterials are highly pure, crystalline, and biocompatible in nature resulting from the successful attachment of PEG. It was found that both nanospheres and nanoparticles of cobalt ferrite are toxic to biological systems. Furthermore, it was shown that nanospheres of cobalt ferrite are more toxic than the nanoparticles due to their large surface area and more reactivity with biological tissues. Positive changes were monitored in biochemical indexes after the administration of curcumin which is a natural chemical possessing no side effects, thus confirming it can be used as the healing agent for the toxicity induced by cobalt ferrite nanospheres.
Change history
Abréviations
- PEG:
-
Polyéthylène glycol
- XRD :
-
Diffraction des rayons X
- FTIR :
-
Spectroscopie infrarouge à transformée de Fourier
- TGA :
-
Analyse thermogravimétrique
- SPF:
-
Specific pathogens free
- MRI:
-
Magnetic resonance imaging
- TNF:
-
Tumor necrosis factor
- LUI :
-
Hematoxylin–eosin
- SS :
-
Stainless steel
- DI:
-
Deionized
- SEM :
-
Microscopie électronique à balayage
- TEM :
-
Microscopie électronique à transmission
- TB:
-
Total bilirubin
- ALT:
-
Alanine aminotransferase
- AST:
-
Aspartate transferase
- BUN:
-
Blood urea nitrogen
- CREA:
-
Creatinine
- Cys-C:
-
Cystatin C
- DNA:
-
Deoxyribonucleic acid
- MDA:
-
Malondialdehyde assay
- ROS :
-
Oxygen free radicals
- T-AOC:
-
Total antioxidant capacity
Nanomatériaux
- Qu'est-ce que l'alliage de cobalt et quelles sont les propriétés de l'alliage de cobalt ?
- Préparation de nanoparticules mPEG-ICA chargées en ICA et leur application dans le traitement des dommages cellulaires H9c2 induits par le LPS
- Étude des premiers principes sur la stabilité et l'image STM du borophène
- Étude in vitro de l'influence des nanoparticules Au sur les lignées cellulaires HT29 et SPEV
- La toxicité potentielle pour le foie, le cerveau et l'embryon des nanoparticules de dioxyde de titane sur des souris
- Formation et propriétés luminescentes de nanocomposites Al2O3:SiOC à base de nanoparticules d'alumine modifiées par le phényltriméthoxysilane
- La préparation de la nanostructure jaune-enveloppe Au@TiO2 et ses applications pour la dégradation et la détection du bleu de méthylène
- Étude expérimentale sur les caractéristiques d'écoulement et de transfert de chaleur de nanofluides TiO2-eau dans un tube cannelé en spirale
- Nouvelle étude :impact de la COVID-19 sur l'avenir du travail et de l'automatisation



