Contrôle de la configuration des contacts des jonctions moléculaires à base d'acide carboxylique via le groupe latéral
Résumé
Dans cet article, la configuration de contact de la jonction moléculaire unique est contrôlée par le groupe latéral, qui est exploré par la jonction de rupture STM de saut à contact électrochimique. Les valeurs de conductance de l'acide 2-méthoxy-1,3-benzènedicarboxylique (2-M-1,3-BDC) sont d'environ 10 –3,65 G0 , qui est différent de celui de l'acide 5-méthoxy-1,3-benzènedicarboxylique (5-M-1,3-BDC) avec 10 –3.20 G0 . Fait intéressant, la valeur de conductance du 2-M-1,3-BDC est la même que celle du 1,3-benzènedicarboxaldéhyde (1,3-BDCA), tandis que les jonctions moléculaires simples du 5-M-1,3-BDC et 1 L'acide ,3-benzènedicarboxylique (1,3-BDC) donne une valeur de conductance similaire. Étant donné que le 1,3-BDCA se lie à l'électrode de Cu par l'intermédiaire d'un atome d'oxygène, la configuration de contact dominée pour le 1,3-BDC se fait par l'intermédiaire de deux atomes d'oxygène. Les différentes valeurs de conductance entre le 2-M-1,3-BDC et le 5-M-1,3-BDC peuvent être attribuées aux différentes configurations de contact causées par la position du groupe latéral. Le travail actuel fournit un moyen réalisable de contrôler la configuration de contact entre le groupe d'ancrage et l'électrode, ce qui peut être utile dans la conception de futures électroniques moléculaires.
Contexte
Une bonne compréhension du transport des électrons à travers des jonctions moléculaires uniques est un intérêt fondamental dans le développement de l'électronique moléculaire [1,2,3,4,5,6,7,8,9,10,11,12,13,14] . Ces dernières années, de nombreuses publications ont indiqué que la conductance moléculaire unique peut être influencée par la structure moléculaire intrinsèque [10, 15, 16, 17, 18], les groupes d'ancrage [19], les configurations de contact [20, 21], les matériaux des électrodes [22 ,23,24], et ainsi de suite [4, 14, 25, 26]. Parmi elles, les configurations de contact jouent un rôle important dans le transport des électrons des jonctions moléculaires uniques [27,28,29]. Cependant, il existe un rapport assez limité sur ce problème, en raison de la difficulté de contrôler la configuration des contacts.
À propos de la configuration de contact, certains travaux expérimentaux montrent plusieurs ensembles de valeurs de conductance pour des jonctions moléculaires uniques correspondant à différentes configurations de contact [20, 30]. Cependant, plusieurs configurations apportent complexité et difficulté dans l'analyse de la conductance moléculaire unique. La capacité de contrôler la configuration de contact entre les électrodes et les groupes d'ancrage est extrêmement importante, car elle peut exclure la complexité des configurations de contact pour l'électronique moléculaire future. Une façon de contrôler les configurations de contact est le contrôle mécanique des jonctions à molécule unique, et les valeurs de conductance peuvent être commutées entre des valeurs basses et élevées en commutant mécaniquement les configurations de contact de molécule et d'électrode [31]. Un tel contrôle mécanique peut encore apporter des configurations différentes et est difficilement utilisable dans l'électronique moléculaire future. Récemment, il a été démontré que l'ajout de groupes latéraux empêche la conductance moléculaire de basculer pendant la modulation mécanique [28], ce qui montre la possibilité de contrôler la configuration des contacts via des groupes latéraux. Par conséquent, l'ajout de groupes latéraux peut fournir un moyen réalisable d'empêcher la formation de plusieurs configurations entre les molécules et les électrodes.
Ici, nous choisissons des molécules d'acide carboxylique à base de benzène avec divers groupes latéraux comme molécules cibles pour étudier les configurations de contact possibles dans des jonctions moléculaires uniques. Il a été démontré que le groupe acide carboxylique forme des jonctions moléculaires uniques avec diverses électrodes [19, 24, 30, 32]. Les molécules cibles comprennent l'acide 2-méthoxy-1,3-benzènedicarboxylique (2-M-1,3-BDC), l'acide 1,3-benzènedicarboxylique (1,3-BDC), l'acide 5-méthoxy-1,3-benzènedicarboxylique (5-M-1,3-BDC) et 1,3-benzènedicarboxaldéhyde (1,3-BDCA) (Fig. 1). La jonction de rupture STM à saut de contact électrochimique (ECSTM-BJ) est utilisée pour construire et mesurer les jonctions moléculaires uniques avec des électrodes en Cu (Fig. 1). L'électrode Cu est choisie, car elle peut former des jonctions moléculaires plus efficaces avec l'acide carboxylique que l'électrode Au comme rapporté dans nos travaux précédents [30]. En particulier, l'environnement électrochimique peut empêcher l'oxydation du Cu, tandis que les jonctions moléculaires uniques de la molécule à base d'acide carboxylique ne peuvent pas être formées avec l'électrode de Cu dans l'air [33].
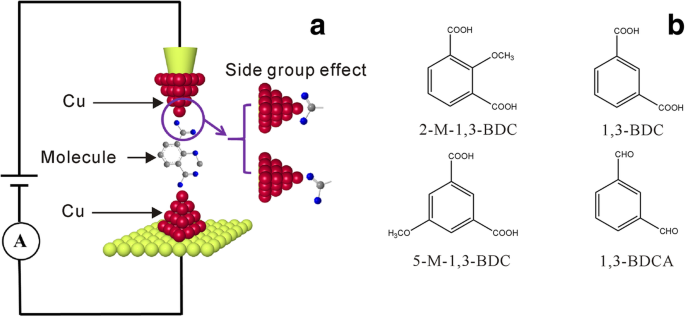
Schéma de principe de la jonction de rupture de microscopie à effet tunnel électrochimique (ECSTM-BJ) et des structures moléculaires. un Illustration schématique de l'approche ECSTM-BJ pour la mesure de conductance de jonctions monomoléculaires (boules rouges, Cu ; boules vertes, Au ; boules bleues, O ; boules grises, C) et b la structure moléculaire cible du 2-M-1,3-BDC, 1,3-BDC, 5-M-1,3-BDC et 1,3-BDCA
Méthodes
Na2 SO4 , CuSO4 , et le 1,3-BDC ont été achetés auprès d'Alfa-Aesar, le 2-M-1,3-BDC et le 5-M-1,3-BDC ont été achetés auprès de Sigma-Aldrich, et le 1,3-BDCA a été obtenu auprès de TCI (Tokyo Chemical Industry Co., Ltd.). Tous ont été utilisés tels que reçus. De l'Au (111) naturellement formé sur une perle monocristalline a été utilisé comme substrat, tandis que le Pt-Ir isolé par de la colle de polyéthylène thermodurcissable a été utilisé comme pointe. Des fils de Pt et de Cu ont été utilisés comme contre-électrode et électrode de référence, respectivement.
La mesure de conductance de jonctions moléculaires simples a été réalisée sur un Nanoscope IIIa STM modifié (Veeco, Plainview, NY, USA) et dans une solution aqueuse contenant 1 mM de CuSO4 + 50 mM Na2 SO4 + 1 mM de molécules cibles. La pointe Pt-Ir et le substrat Au (111) ont été fixés à − 5 et 45 mV par rapport au fil Cu, respectivement. Dans ce cas, le dépôt massif de Cu pourrait se produire sur la pointe mais pas sur le substrat. Après cela, la pointe a été poussée vers le substrat à une distance suffisamment proche, puis le processus de saut au contact s'est produit. La pointe a été retirée du substrat à une vitesse de 20 µnm/s. Au cours de ce processus, la trace de conductance a été enregistrée jusqu'à la rupture de jonctions moléculaires uniques, tandis que des clusters de Cu étaient produits simultanément. Des milliers de traces de conductance ont été collectées pour construire l'histogramme de conductance sans sélection de données. Plus de détails pour l'ECSTM-BJ ont été rapportés dans nos travaux précédents [23, 34, 35].
Nous avons effectué le calcul théorique de la jonction moléculaire unique. La méthode de la théorie fonctionnelle de la densité standard (DFT) est utilisée pour détendre la structure de jonction, où il y a 3 à 4 couches tampons attachées des deux côtés et une grande couche de vide (environ 15 ) insérée à l'extérieur. La méthode de la fonction de Green sans équilibre (NEGF) est adoptée pour calculer les propriétés de transport, c'est-à-dire les coefficients de transmission des jonctions à l'équilibre [36, 37]. Dans tous les calculs ci-dessus, la fonction Perdew-Burke-Ernzerhof (PBE) est utilisée pour le noyau de corrélation d'échange, et pour des raisons de précision et d'efficacité, l'ensemble de base à double polarisation zêta (DZP) est utilisé pour la molécule organique et le la couche la plus externe d'atomes de cuivre et l'ensemble de base à polarisation simple zêta (SZP) sont utilisés pour les autres couches de cuivre profondément enfoncées dans les électrodes. Un échantillonnage K (4,4) est défini le long du plan transversal. Tous les calculs sont effectués avec le package open-source SHINE (Shanghai Integrated Numeric Engineering).
Résultats et discussion
Conduction moléculaire unique du 2-M-1,3-BDC avec le groupe latéral méthoxy sur 2 positions de la molécule
Nous avons d'abord étudié les jonctions moléculaires uniques du 2-M-1,3-BDC, qui possède un groupe latéral méthoxy en position 2 du 1,3-BDC. L'expérience a été réalisée dans une solution aqueuse contenant 1 mM de 2-M-1,3-BDC + 1 mM CuSO4 + 50 mM Na2 SO4 en utilisant l'approche ECSTM-BJ. Des grappes de Cu ont été produites simultanément en tant que produit secondaire (Fig. 2a). La figure 2b affiche des traces de conductance typiques en échelle logarithmique et montre les plateaux de conductance de Cu-(2-M-1,3-BDC)-Cu autour de 10 –3,65 G0 . Des milliers de traces de conductance ont été collectées pour construire un histogramme de conductance du 2-M-1,3-BDC sans sélection de données en échelle logarithmique (Fig. 2c). Un pic évident se trouve autour de 10 -3,65 G0 , ce qui est cohérent avec le pas de conductance dans les traces de conductance. Ici, le pic prononcé montre la conductance moléculaire unique avec la configuration de contact molécule-électrode dominée.
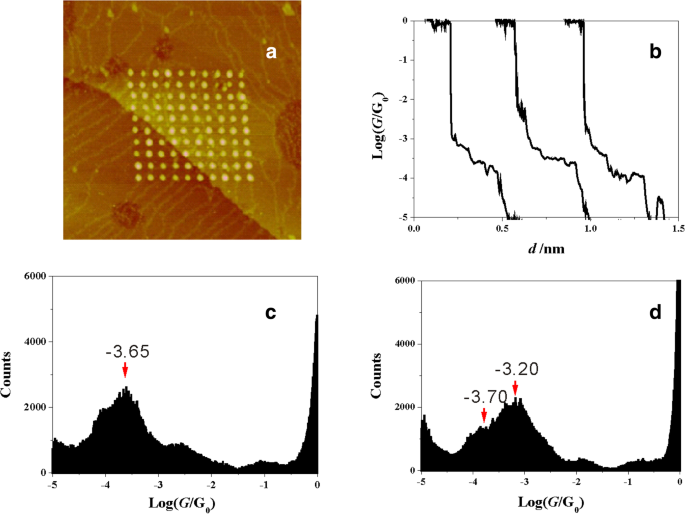
Image STM et conductance moléculaire unique pour le 2-M-1,3-BDC et le 1,3-BDC. un L'image STM (200 × 200 nm 2 ) d'un réseau 10 x 10 d'amas de Cu se formant simultanément avec les traces de conductance. b Typiquement des traces de conductance dans une solution contenant du 2-M-1,3-BDC en échelle logarithmique. Histogrammes de conductance construits sans sélection de données à partir de 1500 traces de conductance mesurées en solution avec c 2-M-1,3-BDC et d 1,3-BDC
Étonnamment, la valeur de conductance du 2-M-1,3-BDC est évidemment différente de la conductance du 1,3-BDC. La figure 2d affiche l'histogramme de conductance du 1,3-BDC et montre un pic de conductance dominé se formant autour de 10 –3.20 G0 , qui est similaire à un rapport précédent [35]. Le groupe latéral méthoxy ne peut pas se lier à l'électrode en formant des jonctions moléculaires efficaces, ainsi le 2-M-1,3-BDC devrait se lier à l'électrode par l'intermédiaire du groupe d'ancrage acide carboxylique. La grande différence de conductance entre le 2-M-1,3-BDC et le 1,3-BDC montre le rôle important du groupe latéral méthoxy sur la conductance d'une molécule unique.
Le groupe latéral méthoxy a pour effet d'attirer les électrons, ce qui peut modifier la valeur de conductance [38]. Cependant, moins de 20 % de changement de conductance est trouvé pour les molécules avec différents groupes latéraux dans la littérature (ne changeant qu'un seul groupe latéral) [38], tandis que la différence de conductance est d'environ 300 % entre le 2-M-1,3-BDC et 1,3-BDC. Ainsi, seul le fait de tirer un effet électronique du groupe latéral ne peut pas provoquer une différence de conductance aussi importante.
Conduction moléculaire unique du 5-M-1,3-BDC avec le groupe latéral méthoxy sur la position 5 de la molécule
Afin d'approfondir l'étude du rôle important du groupe latéral, nous avons étudié la conductance moléculaire unique des molécules avec méthoxy sur la position 5 du 1,3-BDC, nommé 5-M-1,3-BDC. En comparaison avec le 2-M-1,3-BDC, l'ajout du groupe latéral de méthoxy sur le 5-M-1,3-BDC est éloigné des groupes d'ancrage.
La figure 3 présente les histogrammes de conductance du 5-M-1,3-BDC, construits à partir de plus de 1 000 traces de conductance. En comparaison avec la conductance du 2-M-1,3-BDC, l'histogramme de conductance du 5-M-1,3-BDC montre un pic bien distinct autour de 10 –3.20 G0 et donne la même valeur de conductance que celle du 1,3-BDC (10 –3.20 G0 ). Ce résultat illustre que la position du groupe latéral joue un rôle très important dans la conductance moléculaire unique. Bien qu'il existe le même groupe méthoxy dans les molécules de 5-M-1,3-BDC et 2-M-1,3-BDC, il existe des valeurs de conductance assez différentes entre elles.
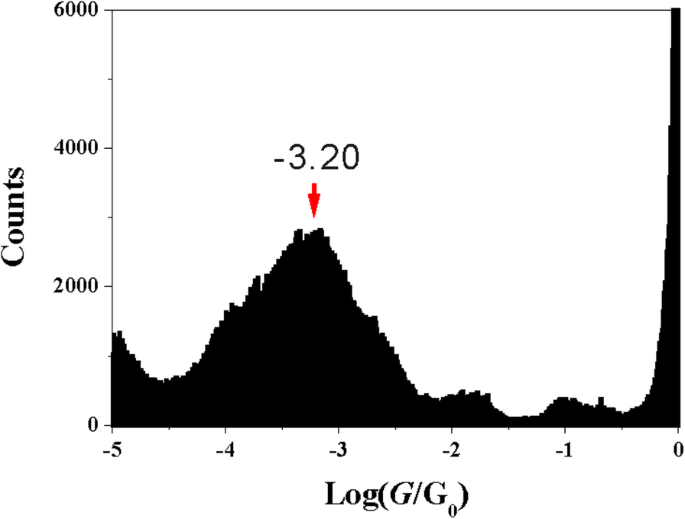
Conductance moléculaire unique du 5-M-1,3-BDC. Les histogrammes de conductance du 5-M-1,3-BDC construits sans sélection de données à partir de 1500 traces
La raison possible des différentes valeurs de conductance entre le 2-M-1,3-BDC et le 5-M-1,3-BDC
Quelle est la raison d'une grande différence de conductance entre le 2-M-1,3-BDC et le 5-M-1,3-BDC ? L'influence du groupe latéral sur les effets d'interférence quantique destructrice (DQI) dans les molécules à base de méta-benzène pourrait provoquer ce phénomène [39, 40]. Typiquement, la conductance d'une molécule à base de méta-benzène est inférieure de plus d'un ordre de grandeur à celle d'une molécule à base de para-benzène, alors qu'il existe d'autres squelettes entre le benzène et le groupe d'ancrage [41,42,43]. L'effet substituant a été théoriquement rapporté sur une telle molécule de méta-benzène avec DQI, qui peut largement ajuster le transport d'électrons des molécules DQI [40]. Cependant, la conductance de la molécule à base de méta-benzène (1,3-BDC avec 10 –3.20 G0 ) est plus gros que celui d'une molécule à base de parabenzène (acide 1,4-benzènedicarboxylique, 1,4-BDC, avec 10 –3,40 G0 ) [35], montrant qu'il n'y a pas d'effet DQI dans le 1,3-BDC. Le DQI n'est pas non plus trouvé pour les molécules ayant le même squelette mais avec un thiol et une amine comme groupes d'ancrage [44].
L'acide carboxylique peut se lier à l'électrode de Cu via la forme carbonyle (un atome d'oxygène) ou carboxylate (deux atomes d'oxygène), tandis que le pic dominé contribue à la configuration via deux atomes d'oxygène pour le 1,4-BDC [30]. Nos calculs démontrent qu'il n'y a pas d'effet DQI dans ces jonctions moléculaires avec des configurations de contact du groupe d'ancrage en contact avec les électrodes de Cu via deux atomes d'oxygène de carboxylate (Fig. 4). Aucune différence de conductance évidente n'est trouvée entre le 2-M-1,3-BDC et le 5-M-1,3-BDC, et la raison possible du DQI influencé par la position du groupe latéral peut être exclue.
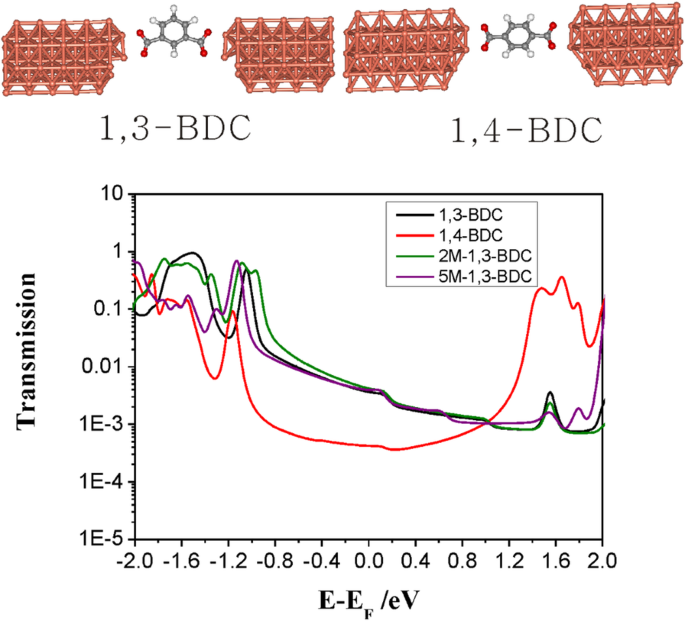
Calcul théorique de jonctions moléculaires uniques. Spectres de transmission calculés pour les molécules de 1,3-BDC, 1,4-BDC, 2-M-1,3-BDC et 5-M-1,3-BDC en contact avec l'électrode de Cu via deux atomes d'oxygène de carboxylate
Une autre possibilité est que la configuration de contact dominée différente soit formée en raison de l'ajout de méthoxy sur différentes positions. Il a été rapporté que l'acide carboxylique peut se lier à l'électrode de Cu via un atome d'oxygène ou deux atomes d'oxygène, tandis que le pic dominé contribue à la configuration via deux atomes d'oxygène pour le 1,4-BDC [30]. Ainsi, la situation peut être similaire à 1,3-BDC et 5-M-1,3-BDC, et la valeur de conductance de 10 –3.20 G0 pourrait être contribué au contact des deux atomes d'oxygène (carboxylate) avec les électrodes de Cu. Pour le 2-M-1,3-BDC, l'existence du groupe latéral méthoxy près de l'acide carboxylique peut empêcher les jonctions moléculaires uniques de contacter l'électrode de Cu via deux atomes d'oxygène de carboxylate, puis la valeur de conductance de 10 -3,65 G0 est trouvé. Ainsi, nous pouvons attribuer la différence de conductance entre le 2-M-1,3-BDC et le 1,3-BDC aux différentes configurations de contact, qui est causée par l'ajout du groupe latéral méthoxy voisin. Ce point est encore démontré par la mesure de la conductance du 1,3-BDCA avec un groupe carbonyle.
La validation de la configuration de contact pour le 2-M-1,3-BDC par la mesure des jonctions moléculaires uniques du 1,3-BDCA
D'en haut, le groupe latéral voisin a un effet sur la conductance moléculaire unique et peut influencer la configuration de contact entre les électrodes d'acide carboxylique et de Cu. Afin de prouver cette hypothèse, nous avons effectué la mesure de conductance du 1,3-BDCA avec uniquement un groupe d'ancrage carbonyle. Le groupe d'ancrage carbonyle peut se lier à l'électrode de Cu via un atome d'oxygène [30, 45]. La figure 5 montre l'histogramme de conductance du 1,3-BDCA avec un pic évident situé autour de 10 –3,65 G0 . En comparaison avec l'histogramme de conductance du 1,3-BDC, la conductance du 1,3-BDCA montre une valeur de conductance plus petite. Cependant, cette valeur est similaire à la conductance du 2-M-1,3-BDC, qui peut montrer la même configuration de contact dominée formée entre le 1,3-BDCA et le 2-M-1,3-BDC. Surtout, nous pouvons toujours trouver un pic d'épaule de 10 –3,70 G0 près de la valeur de crête dominée de 10 –3.20 G0 pour le 1,3-BDC (Fig. 2d). Cette valeur (10 –3,70 G0 ) peut s'expliquer par la configuration de contact à travers un oxygène de carboxylate entre le groupe d'ancrage et l'électrode, tandis que le pic dominé (10 –3.20 G0 ) est causée par la liaison de deux oxygènes de carboxylate à l'électrode. En raison du groupe latéral voisin en position 2, le groupe carboxylate du 2-M-1,3-BDC ne parvient pas à former des jonctions moléculaires via deux oxygènes du carboxylate, et un seul oxygène du groupe carboxylate se lie à l'électrode.
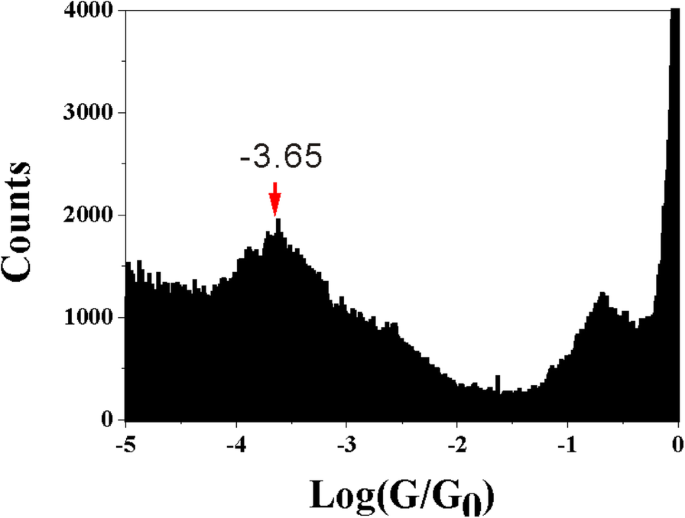
Conductance moléculaire unique du 1,3-BDC. L'histogramme de conductance du 1,3-BDCA construit à partir de 1100 courbes de conductance
Les valeurs de conductance pour toutes les molécules étudiées sont résumées dans le tableau 1. La valeur de conductance du 2-M-1,3-BDC est la même que celle du 1,3-BDCA, tandis que les jonctions moléculaires simples du 5-M-1,3 -BDC et 1,3-BDC donnent une valeur de conductance similaire. Étant donné que le 1,3-BDCA ne peut se lier à l'électrode Cu que par un atome d'oxygène, la configuration de contact dominée pour le 1,3-BDC se trouve à travers deux atomes d'oxygène. Les valeurs de conductance ci-dessus pour différentes molécules montrent la preuve solide que différentes configurations de contact sont formées entre le 2-M-1,3-BDC et le 5-M-1,3-BDC. L'ajout de méthoxy sur un site voisin du groupe d'ancrage peut avoir un effet d'encombrement stérique, qui peut interdire la formation d'une configuration de contact entre l'acide carboxylique et l'électrode à travers deux atomes d'oxygène à une ou aux deux extrémités. Le travail en cours montre la possibilité de contrôler la configuration des contacts grâce à la position du groupe latéral.
Conclusions
En conclusion, nous avons mesuré les molécules à base d'acide carboxylique à conductance moléculaire unique se liant à l'électrode de Cu en utilisant ECSTM-BJ. Il est montré que la configuration de contact peut être contrôlée par la position du groupe latéral, ce qui peut empêcher les jonctions moléculaires uniques de contacter l'électrode de Cu par l'intermédiaire de deux atomes d'oxygène de carboxylate pour le 2-M-1,3-BDC. Un tel effet peut être invalidé en plaçant le groupe latéral sur la position 5 de la molécule (5-M-1,3-BDC). Cette recherche fournit un moyen réalisable de contrôler la configuration de contact entre le groupe d'ancrage et l'électrode, ce qui peut être utile dans la conception de futures électroniques moléculaires.
Disponibilité des données et des matériaux
Les ensembles de données utilisés et/ou analysés au cours de la présente étude sont disponibles auprès de l'auteur correspondant sur demande raisonnable.
Abréviations
- 1,3-BDC :
-
Acide 1,3-benzènedicarboxylique
- 1,3-BDCA :
-
1,3-benzènedicarboxaldéhyde
- 1,4-BDC :
-
Acide 1,4-benzènedicarboxylique
- 2-M-1,3-BDC :
-
Acide 2-méthoxy-1,3-benzènedicarboxylique
- 5-M-1,3-BDC :
-
Acide 5-méthoxy-1,3-benzènedicarboxylique
- DQI :
-
Interférence quantique destructrice
- ECSTM-BJ :
-
Jonction à coupure STM à saut de contact électrochimique
Nanomatériaux
- Contacter « Bounce »
- lentilles de contact
- Les scientifiques d'IBM mesurent le transfert de chaleur via des atomes uniques
- Effet de surface sur le transport du pétrole dans les nanocanaux :une étude de dynamique moléculaire
- Propriétés de photoluminescence des modifications polymorphes du poly(3-hexylthiophène) de bas poids moléculaire
- Modélisation et simulation de dynamique moléculaire de la coupe de diamant de cérium
- Dépendance de la température de la bande interdite dans le MoSe2 cultivé par épitaxie par faisceau moléculaire
- Suivi du produit tout au long de la chaîne d'approvisionnement avec des balises moléculaires
- Linfox International Group stimule l'efficacité opérationnelle grâce à la transformation numérique



