Préparation assistée par acide sulfurique de points de polymère carbonisés émetteurs rouges et application de la bio-imagerie
Résumé
Les points de polymère carbonisé à émission rouge (CPD) ont été préparés à partir de p -phénylènediamine (p -PD) solution aqueuse à l'aide d'acide sulfurique (H2 SO4 ), et les propriétés optiques et l'application de la bio-imagerie ont été étudiées dans cet article. Par rapport à d'autres systèmes assistés par des acides forts, les SA-CPD (préparés à partir de H2 SO4 -système assisté, diamètre moyen ~ 5 nm) est le plus brillant. Les rendements quantiques de photoluminescence (QY) sont de 21,4 % (dans l'eau) et le rendement en produit est de 16,5 %. La solution aqueuse de SA-CPD émet à 600 nm lorsqu'elle est excitée par la lumière de 300 à 580 nm. La longueur d'onde d'émission est indépendante de la longueur d'onde d'excitation. Les énergies de formation des CPD de deux manières ont été calculées pour montrer que la croissance longitudinale (formation de polymères) est difficile et que la croissance transversale (formation de CPD) est facile. De plus, les propriétés de photoluminescence à deux photons (émettant à 602 nm lorsqu'elles sont excitées par un laser à impulsions femtosecondes 850 nm) des SA-CPD ont également été utilisées dans les expériences de coloration des cellules HeLa et ont montré qu'elles avaient des applications potentielles en bio-imagerie.
Contexte
Les points de carbone (CD) ont attiré beaucoup d'attention en raison de leurs avantages, notamment une excellente solubilité dans l'eau, une stabilité optique, des propriétés de fluorescence uniques, une faible toxicité, un faible coût, etc. [1]. La plupart des CD ont été étudiés en tant que candidats potentiels pour diverses applications, telles que les capteurs immunitaires électrochimiques [2], les capteurs de bio-imagerie [3,4,5,6] [7,8,9,10,11,12], photo- la catalyse [13,14,15], les dispositifs électroluminescents [16] et l'optoélectronique [17,18,19]. La synthèse des CD joue un rôle important dans les études sur les propriétés optiques et les applications. Les approches rapportées pour préparer des CD pourraient être principalement résumées comme étant « de haut en bas » à partir de divers matériaux carbonés et « de bas en haut » à partir de molécules organiques, de polymères ou de produits naturels [20]. Les méthodes « bottom-up » sont des voies efficaces pour la synthèse de CD fluorescents à grande échelle [21]. Groupes dans les molécules appliquées, y compris -OH, -COOH, -C=O et -NH2 peut être déshydraté et carbonisé à température élevée par hydrothermie, micro-ondes, combustion, pyrolyse, etc.
Les points émetteurs rouges ont suscité un intérêt considérable en raison, par exemple, de la plus grande profondeur de pénétration dans le champ de bio-imagerie. En particulier, les points de couleur pure sont essentiels à une certaine occasion, car les matériaux de luminescence indépendants de la longueur d'onde d'excitation peuvent fournir une lumière de photoluminescence (PL) unique et stable. La plupart des émissions de CD dépendent de la longueur d'onde d'excitation, et les CD émettent généralement une lumière bleue, verte ou jaune, peu de CD émettent une lumière rouge vif [22].
Récemment, les isomères de la phénylènediamine (PD), tels que o -, m -, et p -PD, avaient été étudiés comme sources de carbone pour préparer des CD [8, 9, 23, 24]. Les CD émettant du bleu, du vert et du rouge peuvent être préparés à partir de m -, o -, et p -PD solution d'éthanol, respectivement [23]. Des CD luminescents en couleur peuvent être préparés à partir de p -PD et solution aqueuse d'urée [24]. Dans nos travaux précédents [25], nous avons proposé que de nouveaux points de carbone rouge (rendements quantiques = 15,8%, dans l'eau) puissent être synthétisés facilement à partir de « p -PD + HNO3 ” système aqueux et appliqué à la détection d'ions métalliques dans l'eau. Récemment, le même « o -PD + H3 Bon de commande4 » [26] et « o -PD + HNO3 ” [27] systèmes ont été signalés, et Liu et al. [27] ont renommé leurs CD (QYs = 10,8 %, dans l'eau) en « points de polymère carbonisés (CPD) ». Contrairement aux points de carbone traditionnels, les longueurs d'onde d'émission des CPD ne dépendent pas de la longueur d'onde d'excitation, et donc les « CD » basés sur les PD devraient être nommés plus précisément en tant que CPD.
Nous rapportons ici une méthode facile et très efficace de voie hydrothermale assistée par acide fort pour préparer des CPD à émission rouge et l'application de la bio-imagerie avec des propriétés de photoluminescence à deux photons. Le mécanisme de formation des DPC est proposé en utilisant le progiciel Gaussien 09.
Méthodes
Synthèse de DPC rouges à partir de p assistés par acide -Systèmes PD
Sur la base de nos précédents travaux [25], nous avons sélectionné l'acide sulfurique (H2 SO4 ), acide chlorhydrique (HCl) et acide perchlorique (HClO4 ) en tant qu'assistants pour la préparation des CPD rouges, les CPD correspondants ont été étiquetés respectivement en tant que SA-CPD, HC-CPD et PA-CPD. Afin d'optimiser les conditions expérimentales de H2 SO4 -système assisté, nous avons sélectionné plusieurs paramètres, tels que c (acide) à c (p -PD), c (p -PD), température (T ), et le temps de réaction (t ). Les produits CPD ont été lavés à l'hexane pour éliminer les p n'ayant pas réagi -PD et par de l'alcool éthylique pour éliminer les acides, centrifugé à 14 000 tr/min pendant 30 min pour éliminer la précipitation du polymère et filtré à travers une membrane filtrante de 0,22 μm. Si la poudre est souhaitable, la solution de CPD purifiée peut être encore évaporée à l'aide d'un évaporateur rotatif jusqu'à un état presque sec à 80 °C et un vide faible (le reste sera sous forme de poudre).
Caractérisation et mesure
Des images MET haute résolution (HR-TEM) ont été enregistrées sur un microscope à transmission JEM-2100 fonctionnant à 200 kV. Les spectres infrarouges des solutions de CPD ont été collectés à l'aide du spectromètre FT-IR Prestige-21 à l'aide de tranches de fenêtre KRS-5 (mélange de TlBr et TlI), généralement, les phases liquides ont été déposées sur une tranche et séchées. La tranche a été recouverte par l'autre tranche et fixée sur le banc d'essai. Ensuite, les spectres infrarouges ont été enregistrés.
Les spectres de fluorescence des CPD ont été mesurés sur un spectrophotomètre à fluorescence F-2500. Les spectres d'absorption UV-Vis ont été enregistrés sur le spectromètre Lambda 950 UV/VIS/NIR. Les spectres d'émission à deux photons des CPD ont été enregistrés par un spectrographe à fibre (QE65000, Ocean Optics) dans le système de microscope. La solution aqueuse de SA-CPD et la solution redissoute de poudres ont été centrifugées sur des lames, et les propriétés de photoluminescence à deux photons ont ensuite été mesurées.
Les rendements quantiques de photoluminescence (QY) des CPD ont été mesurés avec de la Rhodamine B (QYs = 56% dans l'éthanol) comme colorant de référence dans la plage d'émission de 580-610 nm excité par une lumière UV de 365 nm [25, 28], la procédure de Les mesures des QY ont été affichées dans le fichier supplémentaire 1.
Méthodes de calcul
Le package Gaussian 09 a été utilisé pour les calculs de la théorie de la fonction de densité (DFT) [29]. Les structures d'équilibre ont été optimisées par la méthode B3LYP en conjonction avec le niveau de base 6-311++G (d) [30]. Pour étudier le rôle des effets des solvants, l'eau a été utilisée dans un modèle de continuum polarisé (PCM). Des analyses de fréquence ont été faites avec le même niveau pour confirmer que chaque structure optimisée correspondait à un point stationnaire.
Culture cellulaire et traitement
1,35 mL de cellules HeLa dans le milieu Eagle modifié de Dulbecco (DMEM ; Gibco) à une densité initiale de 4 × 10 4 cellules par millilitres ont été ensemencées dans chaque boîte et cultivées à 37 °C pendant 24 h sous une atmosphère humidifiée contenant 5% de CO2 . Les poudres de SA-CPD ont été redissoutes dans l'eau pour préparer la solution de réserve (400 μg mL − 1 ). 1350 μL de cellules ont été cultivées avec 150 μL de solution de réserve de SA-CPD (la concentration finale est de 40 μg mL − 1 ) pendant 12 h puis lavé trois fois avec du PBS pour éliminer les SA-CPD libres. Enfin, les résultats de l'imagerie cellulaire ont été collectés avec un microscope confocal sous excitation laser femtoseconde 850 nm (30 mW).
Résultats et discussion
Optimisation de la préparation aux DPC rouges
Dans des expériences de base, différents systèmes assistés par acide avec divers rapports de concentration, températures de réaction et durées ont été étudiés (voir le fichier supplémentaire 1 :Figure S1). Nous avons constaté que des CPD rouges peuvent se former au-dessus de 180 °C (réagissant pendant 2 h) pour différents systèmes acides et que les réactions ne sont pas affectées par les anions dans les solutions. Longue durée (4-12 h, 240 °C pour H3 Bon de commande4 et les systèmes HF, voir le fichier supplémentaire 1 :Figure S1f) la réaction augmentera la taille des particules et la fluorescence rouge finira par s'estomper, tandis que le changement de fluorescence n'est pas évident pour le système HCl (2 à 6 h, 200 °C, voir les systèmes supplémentaires fichier 1 :Figure S2). Compte tenu de l'économie d'énergie et de la limite de température supérieure du revêtement en téflon, la température et le temps de réaction optimaux sont respectivement de 200 °C et 2 h. Basé sur la stratégie d'optimisation de p -Système PD + HCl (voir Fichier supplémentaire 1 :Figure S2), nous avons optimisé le p -PD + H2 SO4 et p -PD + HClO4 systèmes et obtenu les résultats d'optimisation indiqués dans le tableau 1.
Les SA-CPD, HC-CPD et PA-CPD ont été préparés à partir de p -Solution PD avec l'aide de H2 SO4 , HCl et HClO4 , respectivement. Le c optimisé (acide) à c (p -PD) rapports de H2 SO4 -, HCl- et HClO4 -les systèmes assistés sont respectivement 1, 3 et 3 (voir le fichier supplémentaire 1 :Figure S3a). Le c approprié (p -PD) pour la préparation des CPD rouges est large (de 0,02 à 0,20 mol L − 1 ). La température optimisée (T ) et le temps de réaction (t ) sont de 200 °C et 2 h. Les SA-CPD sont les CPD rouges les plus brillants avec un QY élevé de 21,4 % (Fichier supplémentaire 1 :Figure S3b). Il y a deux raisons pour lesquelles H2 SO4 -les points de carbone assistés ont une meilleure qualité par rapport à HCl-, HClO4 -, et HNO3 -assistées (publiées dans nos précédents travaux [25]). Tout d'abord, H2 SO4 est un acide fort non volatil qui maintient son acidité dans une solution réactionnelle à haute température et haute pression. Deuxièmement, H2 SO4 -Le système assisté est le seul qui peut former une précipitation de sel d'ammonium dans le précurseur, et les précipités libèrent lentement les réactifs libres, évitant la formation de précipitations de polymère à grosses particules et favorisant davantage la formation de points de carbone de haute qualité. Les HA-CPD et les PA-CPD sont des solutions épaisses brun-rouge foncé et émettent un PL rouge foncé sous une irradiation UV de 365 nm, tandis que les SA-CPD tels que préparés sont une solution mince transparente rouge vif et émettent une lumière rouge vif (fichier supplémentaire 1 : Figure S3c). Après avoir été purifiées par lavage, concentration, filtration et évaporation, des poudres brun-rouge foncé de SA-CPD (Fichier supplémentaire 1 :Figure S3d) ont été obtenues avec un rendement de 16,5 %. Les poudres peuvent être redissoutes dans l'eau et la solution émet une fluorescence lumineuse et rouge (Fichier supplémentaire 1 :Figure S3e).
Caractérisation TEM et analyse FT-IR
Images MET de l'échantillon OpPD (sans H2 SO4 ) et SA-CPD (avec H2 SO4 ) ont été présentés sur la figure 1. L'échantillon OpPD est composé de fragments (oligomères, figure 1a) et de polymères (insert de la figure 1a). Les SA-CPD sont des CPD monodispersés avec une taille moyenne d'environ 5 nm (Fig. 1c). Il présente des doigts de réseau bien résolus avec un espace d'environ 0,21 nm (fig. 1b insert), correspondant à l'espacement de réseau dans le plan (100) du graphène [31, 32].
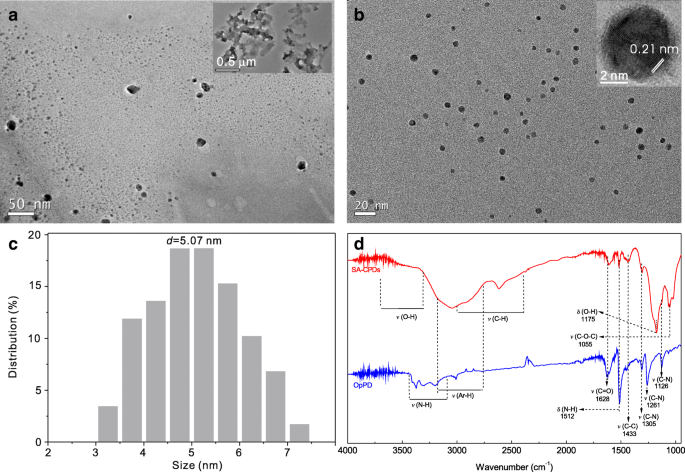
Images MET de l'échantillon OpPD (sans H2 SO4 ) (a ) et SA-CPD (b ). c La distribution de taille des SA-CPD. d Les spectres FT-IR des échantillons OpPD et CPD rouges. Des échantillons d'OpPD et de SA-CPD ont été préparés à partir de p -PD solution aqueuse sans et avec H2 SO4 -assisté
Les états de surface des CPD peuvent affecter les propriétés optiques. Les groupes chimiques de surface des échantillons OpPD et SA-CPD ont été caractérisés par des spectres FT-IR (Fig. 1d). Deux échantillons ont plusieurs groupes similaires, tels que Ar-H (2700-3200 cm − 1 [33], appartient à la vibration d'étirement aromatique C-H), C-C (~ 1433 cm − 1 , appartient à la vibration d'étirement aromatique de l'os C, révèle la présence de vibrations d'étirement aromatiques caractéristiques des unités benzénoïdes) [34], et C=O (1628 cm − 1 , appartient aux groupes –COOH). Par rapport à l'échantillon OpPD, les nouveaux groupes, tels que O-H (3 300 à 3 700 cm − 1 et 1175 cm − 1 appartiennent aux groupes -COOH), C-O-C (1055 cm − 1 , existent dans les esters) et C-H (2 400–3000 cm − 1 appartient aux radicaux alkyle formés dans la réaction d'ouverture de cycle), se trouvent dans les CPD, tandis que le -NH2 ou des groupes liés à –NH– tels que N-H (3100-3300 cm − 1 et 1512 cm − 1 et C-N (1126, 1261 et 1305 cm − 1 appartiennent à la libre –NH2 ou groupes –NH– de p -PD précurseur, sont affaiblis ou ont disparu. L'existence de groupes -OH ou -COOH indique que le degré d'oxydation de la surface des SA-CPD (avec H2 SO4 ajout) est supérieur à celui de l'échantillon OpPD (sans ajout d'acide).
Mécanisme proposé pour la formation de CD
Les énergies de formation ont été calculées à l'aide du progiciel Gaussian 09. Après avoir été protonés par assistance acide, les bi-polymères peuvent être polymérisés de deux manières appelées croissance longitudinale et transversale. L'énergie de formation calculée de la croissance transversale (− 1406.07 kJ mol − 1 ) est significativement plus élevée que celle de la croissance longitudinale (− 616.25 kJ mol − 1 ). Il montre que les bi-polymères entièrement protonés (pH 3, après excès de H + a été ajouté) ont tendance à être polymérisés de manière transversale pour former une structure plane (Fig. 2). Ces structures planes ont ensuite été auto-assemblées pour former des CPD sphériques.
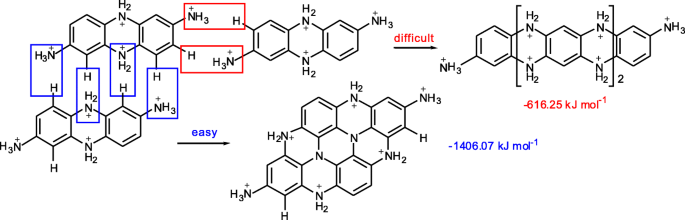
Energies de formation des excroissances longitudinales et transversales
Propriétés optiques
Bien qu'étant préparés à l'aide de différents acides, tous les CPD ont des propriétés optiques similaires [25]. Pour les spectres UV-Vis de la solution aqueuse de SA-CPD (Fig. 3a), le pic d'absorbance situé à ~ 290 nm est associé aux transitions dans le cycle benzénique, et les pics situés à 430 nm et 510 nm pourraient être attribués à π -π* transition de la phénazine substituée conjuguée aux paires d'électrons isolés sur le groupe amine adjacent et la transition électronique du cycle benzénoïde aux cycles quinoïdes, respectivement [32]. La courbe d'excitation décrit une tendance à la hausse large et progressive dans la région visible, et le pic d'excitation maximal (~ 580 nm) est proche du pic d'émission (~ 600 nm). Les CPD émettent dans la zone de lumière rouge (600-700 nm) lorsqu'ils sont excités de 220 nm à 310 nm, tandis qu'ils émettent en lumière orange (~ 600 nm) lorsqu'ils sont excités de 310 nm à 580 nm (Fig. 3b). Il convient de noter que la fluorescence de ce type de CPD à émission rouge est indépendante de la longueur d'onde d'excitation [22, 35].
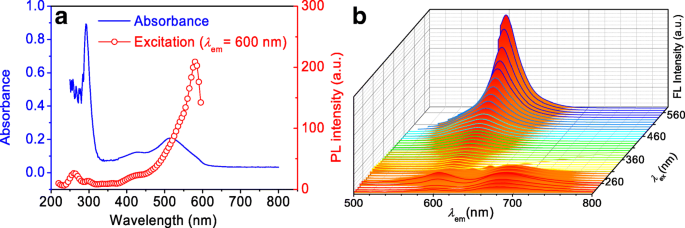
un Absorption UV-Vis, excitation (pic à 600 nm) et b spectres d'émission (excités de 220 à 580 nm) de SA-CPD
Imagerie cellulaire
Les propriétés de photoluminescence à deux photons des SA-CPD avant et après le processus de poudrage sont illustrées à la figure 4a. Il y a un décalage vers le bleu de 602 nm (avant le processus de poudrage) à 529 nm (après le processus de poudrage) à la même longueur d'onde d'excitation de 850 nm par un laser à impulsion femtoseconde (30 mW). L'intensité PL a été augmentée après le processus de poudrage.
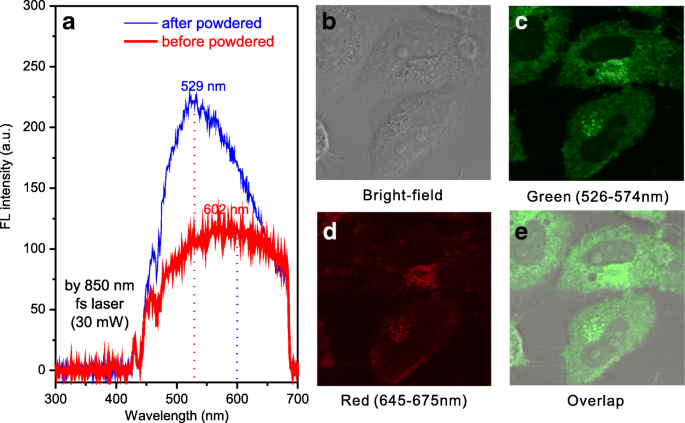
Spectres de photoluminescence à deux photons des SA-CPD (a ) et des images de microscopie à fluorescence confocale de cellules HeLa traitées avec des SA-CPD excitées par un laser à impulsion femtoseconde de 850 nm, 30 mW (b –e )
Les poudres de SA-CPD ont été redissoutes dans du PBS (1X) et appliquées dans l'imagerie des cellules HeLa à l'aide d'une microscopie confocale à fluorescence et d'un laser à impulsions femtosecondes 850 nm (30 mW) (voir Fig. 4b-e). Après avoir été cultivés avec des cellules HeLa pendant 12 h, les SA-CPD ont été avalés par les cellules HeLa et les CPD sont entrés dans le cytoplasme. L'intensité FL du canal rouge (645 à 675 nm) est faible tandis que le canal vert (526 à 574 nm) est brillant, il est cohérent avec le décalage vers le bleu dans le processus de poudrage.
Conclusions
Une méthode facile de voie hydrothermale assistée par acide pour préparer des points de carbone et l'application de la bio-imagerie ont été signalées. Dans H2 SO4 -, HCl- et HClO4 -systèmes assistés, SA-CPD préparés à partir de H2 SO4 Le système assisté est le CPD le plus brillant avec une taille moyenne d'environ 5 nm, un QY de 21,4 % et un rendement de 16,5 %. La solution aqueuse de SA-CPD émet à 600 nm lorsqu'elle est excitée par la lumière de 300 à 580 nm. La longueur d'onde d'émission est indépendante de la longueur d'onde d'excitation. De plus, les SA-CPD ont des propriétés de photoluminescence à deux photons émettant à 602 nm lorsqu'elles sont excitées par un laser à impulsions femtosecondes à 850 nm (30 mW). La méthode a également été utilisée dans l'imagerie pour les cellules HeLa et a un potentiel dans, par exemple, les applications de bio-imagerie.
Abréviations
- CD :
-
Points de carbone
- DPC :
-
Points de polymère carbonisés
- HC-CPD :
-
Les points de carbone ont été préparés à partir de p -PD avec système assisté par HCl
- PA-CPD :
-
Les points de carbone ont été préparés à partir de p -PD avec HClO4 -système assisté
- p -PD :
-
P -phénylènediamine
- QY :
-
Rendements quantiques
- SA-CPD :
-
Les points de carbone ont été préparés à partir de p -PD avec H2 SO4 -système assisté
Nanomatériaux
- Application de teintures acides dans le monde des tissus
- Le développement et l'application de tissu en fibre de verre
- Préparation de nanoparticules mPEG-ICA chargées en ICA et leur application dans le traitement des dommages cellulaires H9c2 induits par le LPS
- Synthèse de points quantiques de type II/Type-I à suppression de réabsorption ZnSe/CdS/ZnS Core/Shell et leur application pour le dosage immunosorbant
- Absorbeur parfait à bande ultra-étroite et son application en tant que capteur plasmonique dans la région visible
- Les effets du rapport Li/Nb sur la préparation et les performances photocatalytiques des composés Li-Nb-O
- La préparation de la nanostructure jaune-enveloppe Au@TiO2 et ses applications pour la dégradation et la détection du bleu de méthylène
- Synthèse de nanocristaux de ZnO et application dans des cellules solaires polymères inversées
- Film de condensateur :les propriétés, la construction et l'application



