Effet de l'agent peptisant acide sur le rapport anatase-rutile et les performances photocatalytiques des nanoparticules de TiO2
Résumé
TiO2 des nanoparticules ont été synthétisées à partir d'isopropoxyde de titane par une simple méthode de peptisation utilisant des acides sulfurique, nitrique et acétique. L'effet de l'acide peptisant sur les propriétés physico-chimiques et photocatalytiques du TiO2 poudres a été étudiée. Les propriétés structurelles du TiO2 synthétisé les poudres ont été analysées en utilisant XRD, TEM, N2 -physisorption, Raman, DR UV-vis , FTIR et techniques de spectroscopie photoélectronique aux rayons X. Les résultats de la caractérisation ont montré que la peptisation à l'acide acétique facilitait la formation d'une phase anatase pure après traitement thermique à 500 °C ; en revanche, la peptisation à l'acide nitrique a conduit à une importante formation de phase rutile (67%). Fait intéressant, l'échantillon peptisé à l'aide d'acide sulfurique a donné des phases d'anatase à 95 % et de rutile à 5 %. L'activité photocatalytique du TiO2 synthétisé les nanoparticules ont été évaluées pour la dégradation de colorants organiques sélectionnés (violet cristal, bleu de méthylène et p -nitrophénol) en solution aqueuse. Les résultats ont confirmé que le TiO2 l'échantillon peptisé à l'aide d'acide nitrique (avec des phases rutile et anatase dans un rapport de 3:1) offrait l'activité la plus élevée pour la dégradation des colorants organiques, bien que TiO2 les échantillons peptisés à l'aide d'acide sulfurique et d'acide acétique possédaient une taille de particules plus petite, une énergie de bande interdite plus élevée et une surface spécifique élevée. Fait intéressant, TiO2 échantillon peptisé avec de l'acide nitrique possédait une densité de photocourant théorique relativement élevée (0,545 mAcm −2 ) et le diamètre des pores (150 Å), qui sont responsables de l'efficacité élevée de la séparation électron-trou, de la diffusion et du transport de masse des réactifs organiques au cours du processus de dégradation photochimique. L'activité supérieure du TiO2 échantillon peptisé avec de l'acide nitrique est dû au transfert efficace des électrons photogénérés entre les phases rutile et anatase.
Contexte
Dioxyde de titane (TiO2 ) est un matériau semi-conducteur largement connu pour son utilisation dans de nombreuses applications, notamment la conversion de l'énergie solaire, le contrôle de la pollution et la photocatalyse [1,2,3]. TiO2 a généralement trois polymorphes, à savoir l'anatase, le rutile et la brookite. Il a été rapporté que l'anatase et la brookite peuvent être transformées en rutile après traitement thermique à haute température (< 610 °C) [4, 5]. TiO2 l'anatase est connue pour être un photocatalyseur actif pour la dégradation des polluants organiques [1, 5,6,7,8]. Il a été observé que la taille, la phase cristalline et la porosité du TiO2 les échantillons ont une forte influence sur leurs applications [9]. Synthèse à basse température de TiO2 poreux nanométrique nécessite des temps de synthèse plus longs [10,11,12]. Li et al. [13] ont synthétisé de l'anatase pure et un mélange de phases rutile et anatase en traitant thermiquement le TiO2 amorphe . La formation d'anatase pure implique un traitement thermique à haute température (500 °C) [14], qui provoque souvent un frittage du TiO2 nanostructures. La synthèse d'anatase cristalline pure à des températures plus basses est un sujet de recherche intéressant [15]. Des méthodes de synthèse sol-gel et hydrothermale [16] ont été utilisées pour préparer un TiO2 bien cristallin à basse température et temps de réaction court [17]. Wang et al. [12] ont synthétisé des nanoparticules d'anatase et de rutile hautement cristallines par HNO3 hydrothermal TiO2 peptisé sols. Cependant, la méthode hydrothermale exige des conditions de synthèse particulières et des équipements coûteux qui pourraient supporter des pH et des températures élevés [18].
La méthode de synthèse sol-gel a été utilisée en utilisant l'alcoxyde de titane comme précurseur de Ti à une température douce (< 100 °C), et elle a donné du TiO2 de taille nanométrique hautement dispersé. échantillons [16]. La méthode de peptisation chimique a été adaptée pour la synthèse de nanostructures d'oxydes métalliques stables incluant TiO2 [19], où la suspension coagulée se dissout et recristallise dans la solution stable de nanoparticules avec l'agent peptisant [20]. Il a été rapporté que la nature de l'acide peptisant a un effet sur les caractéristiques physico-chimiques telles que la taille des cristallites, la composition et la morphologie des particules [21]. Zaban et al. [22] TiO2 synthétisé colloïdes avec HNO3 et CH3 COOH dans des conditions hydrothermales et a observé la formation d'un mélange anatase et brookite dans les deux cas. Liu et al. [23] a obtenu TiO2 hydrolat d'acide métatitanique sous différents agents peptisants et a étudié l'influence des conditions peptisantes sur les propriétés structurales et photocatalytiques du TiO2 hydrolats. Kanna et Wongnawa [24] ont utilisé une méthode de synthèse sol-gel pour obtenir un amorphe-anatase-rutile en utilisant différents acides tels que HCl, HNO3 , H2 SO4 , H3 Bon de commande4 , et CH3 COOH. Les auteurs ont observé que la présence de groupements sulfate et phosphate est responsable de l'inhibition de la croissance de la phase rutile. Plus tard, Alphonse et al. [25] TiO2 synthétisé agrégats, qui sont composés de phase anatase et brookite par hydrolyse de l'isopropoxyde de titane en milieu très acide. Parra et al. [26] ont étudié la voie réactionnelle dans la synthèse de nanoparticules d'anatase avec l'acide acétique. Ils ont utilisé des techniques FTIR et RMN pour conclure que les ions acétate agissent comme un ligand bidenté entre deux centres Ti.
Zhou et al. [27] ont étudié l'effet de HCl, HNO3 , et CH3 COOH en méthode solvothermique pour synthétiser TiO 3D2 structures de morphologie différente. Les auteurs ont conclu que l'échantillon synthétisé avec 0,68 M de HCl possédait à la fois des phases anatase/rutile et offrait la plus haute activité photocatalytique en raison de sa morphologie et de ses propriétés optiques uniques. Tobaldi et al. [28] ont adopté une hydrolyse/peptisation contrôlée de l'isopropoxyde de titane avec HNO3 , HBr et HCl pour synthétiser TiO2 nanoparticules. Il a été observé que les ions halogénures amélioraient la transition de phase anatase-rutile, et les échantillons contenaient jusqu'à 77 % en poids de rutile et 5 % en poids de brookite après calcination à 450 °C.
Dans une publication antérieure [29], la synthèse de TiO2 nanométrique poudres par peptisation acide de xérogels dans des conditions d'humidité atmosphérique a été réalisée. Il a été observé que la peptisation acide accompagnée de vibrations ultrasonores a un effet sur TiO2 propriétés structurelles. Cependant, peu d'études ont été consacrées à l'étude de l'effet des conditions peptisantes sur la formation de la phase rutile et son effet ultérieur sur l'activité photocatalytique du TiO2 nanoparticules. Dans cet article, nous avons examiné l'influence de la nature de l'acide peptisant (H2 SO4 , HNO3 , et CH3 COOH) sur la formation de la phase rutile et son influence sur l'efficacité photocatalytique du TiO2 nanoparticules dans la dégradation de trois polluants organiques différents (cristal violet (CV), bleu de méthylène (MB) et p -nitrophénol (p -NP)).
Méthodes
Préparation de nanoparticules de TiO2 à l'aide de différents acides peptisants
Tétra-isopropoxyde de titane [Ti(OPri)4 ] a été utilisé comme précurseur de Ti, et l'hydrolyse de Ti(OPri)4 a été réalisée dans des conditions atmosphériques standard [29]. La procédure de synthèse typique peut être décrite comme suit : 50 mL de Ti(OPri)4 a été placé dans une bouteille en verre foncé et la bouteille a été laissée sous la hotte pendant 15 jours. La température et l'humidité de la hotte ont été mesurées respectivement à 25 ± 5 °C et 50 ± 10%. L'hydrolyse du précurseur Ti a été achevée en 15 jours, et la solution résultante a été transformée en un gel, qui a ensuite été séché pour obtenir un xérogel. L'acide peptisant (100 mL de 1 N CH3 COOH ou HNO3 ou H2 SO4 ) a été pipeté dans un bécher en verre, et la quantité connue de poudre de xérogel amorphe (2,0 g) a été lentement ajoutée à l'acide peptisant sous agitation constante. Ensuite, le bécher a été placé dans un bain à ultrasons qui a été maintenu à 40 °C, et le mélange a été soumis à un traitement aux ultrasons pendant 10 min. Le TiO2 peptisé les nanoparticules ont été recueillies après centrifugation. Ensuite, les matériaux ont été lavés avec de l'eau distillée et calcinés pendant 3 h à 500 °C. Les échantillons synthétisés ont été étiquetés comme TiO2 acronyme préfixe après leur acide peptisant comme "ace", "nit" et "sul" correspondant à CH3 COOH, HNO3 , et H2 SO4 , respectivement.
Caractérisation des matériaux
Les profils de diffraction des rayons X sur poudre ont été collectés à l'aide d'un diffractomètre Philips PW1700 avec rayonnement Cu Kα et monochromateur graphite avec fente divergente automatique. Les profils XRD ont été indexés avec les données JCPDS standard. Formule de Spurr et Myers [30] [Eq. (1)] a été utilisé pour déterminer les fractions pondérales des phases anatase et rutile.
$$ {X}_{\mathrm{R}}=1/\left[1+k\ \left({I}_{\mathrm{A}}/{I}_{\mathrm{R}}\ à droite)\à droite] $$ (1)où je A et Je R sont les intensités intégrées de (101) réflexion de l'anatase et (110) réflexion du rutile, respectivement. La constante empirique k a été pris comme 0,80 dans ce travail. La taille des cristallites des échantillons synthétisés a été mesurée en utilisant la formule de Scherrer [Eq. (2)] et les réflexions anatase (101) et rutile (110).
$$ D=B\lambda /{\beta}_{1/2}\cos \theta $$ (2)où D est la taille moyenne des cristallites de la phase, B est la constante de Scherrer (0,89), λ est la longueur d'onde du rayonnement X (1,54056 Å), β 1/2 est la pleine largeur à mi-hauteur de la réflexion, et θ est l'angle de diffraction.
L'analyse MET des échantillons a été réalisée à l'aide d'un microscope Philips CM200FEG équipé d'un canon à émission de champ à 200 kV. Le coefficient d'aberration sphérique Cs = 1,35 mm a été appliqué. Les images HRTEM avec une taille de pixel de 0,044 nm ont été prises avec une caméra CCD. L'analyse spectrale laser Raman des échantillons a été réalisée à l'aide du spectromètre Bruker Equinox 55 FT-IR équipé d'un module FRA106/S FT-Raman et d'un liquide N2 -détecteur Ge refroidi utilisant la ligne à 1 064 nm d'un laser Nd:YAG avec une puissance laser de sortie de 200 mW.
N2 -les mesures de physisorption ont été effectuées à l'aide de l'instrument ASAP 2010, Micromeritics Instrument Corporation, USA. Surface spécifique (S PARIER ) des échantillons ont été mesurés à l'aide de N2 -les valeurs d'adsorption et l'équation BET. La largeur des pores et le volume des pores des échantillons ont été déterminés en appliquant la méthode BJH.
Réflectance diffuse UV-vis spectres pour TiO2 synthétisé les échantillons ont été enregistrés à l'aide du spectrophotomètre Thermo Scientific Evolution dans la gamme de longueurs d'onde de 220 à 700 nm. L'énergie de la bande interdite des échantillons a été déterminée en utilisant la transformation de Kubelka-Munk (K ) comme présenté dans l'équation. (3).
$$ K=\frac{{\gauche(1-R\droit)}^2}{2R} $$ (3)où R est la réflectance. Les longueurs d'onde (nm) ont été traduites en énergies (eV), et un tracé de \( {\left(\mathrm{Kh}\upnu \right)}^{0.5} \)vs. hν a été dessiné. L'énergie de la bande interdite (eV) a été estimée comme l'intersection des deux pentes de la courbe tracée.
Les spectres de photoélectrons aux rayons X des échantillons ont été collectés à l'aide de l'instrument Thermo Scientific Escalab 250 Xi XPS avec des rayons X Al Kα ayant une taille de spot de 650 mm. Le décalage de crête dû à la compensation de charge a été corrigé en utilisant l'énergie de liaison de C1s Pic. Les données ont été acquises en utilisant une énergie de passage de 100 eV, un temps d'arrêt de 200 ms avec un pas de 0,1 eV et 10 à 30 scans.
Dégradation photocatalytique du cristal violet, du bleu de méthylène et du p -Nitrophénol
La dégradation photocatalytique de CV, MB et p -Les expériences de NP ont été menées dans un réacteur en verre utilisant du TiO2 synthétisé échantillons comme photocatalyseur sous irradiation UV pour différents temps de réaction. Au total, six lampes UV noires (F20 T8 BLB) d'une puissance de 18 W et de dimensions 60 × 2,5 cm ont été utilisées. La puissance totale de l'irradiation UV à la surface d'une solution aqueuse de colorant organique a été mesurée avec un détecteur Newport 918DUVOD3, et le wattmètre a été mesuré à 13 Wm −2 . Cent milligrammes de catalyseur ont été ajoutés à 100 ml de solution aqueuse de polluant organique (10 ppm). Avant l'évaluation de l'efficacité photocatalytique du catalyseur, la solution de colorant organique a été équilibrée avec le catalyseur en agitant pendant 45 minutes pour stabiliser l'adsorption du colorant organique sur la surface du catalyseur. La dégradation photocatalytique de CV, MB et p -NP a été surveillé en mesurant l'absorbance du colorant organique à intervalle de temps régulier en utilisant un Thermo Fisher Scientific Evolution 160 UV-vis spectrophotomètre. Le pourcentage de dégradation a été calculé à l'aide de l'expression
$$ \eta =\left(1-C/{C}_0\right)\times 100 $$ (4)Où C 0 est la concentration de colorant organique avant illumination et C est la concentration après un certain temps de réaction.
La stabilité des photocatalyseurs a été analysée par les expériences de réutilisation. La régénération du catalyseur a été réalisée en utilisant une procédure simple. Après le premier cycle de mesure d'activité, le catalyseur a été filtré du photoréacteur et des aliquotes par centrifugation. Le catalyseur obtenu a été soigneusement lavé avec de l'eau distillée et de l'acétone. Le catalyseur a été séché à 50 °C pendant 2 h puis réutilisé pour le cycle suivant des mesures de photocatalyse. De même, l'expérience a été répétée pendant plusieurs cycles pour étudier la stabilité du catalyseur.
Résultats et discussion
Diffraction des rayons X sur poudre
Les diagrammes de diffraction des rayons X du TiO2 calciné -as, TiO2 -nit, et TiO2 -sul échantillons sont affichés sur la Fig. 1. Les positions et intensités des pics XRD pour TiO2 les phases présentées dans les exemples sont complétées par la base de données JCPDS. Il est connu que la phase anatase montre des pics de diffraction majeurs à 2θ valeurs de 24,8°, 37,3°, 47,6°, 53,5°, 55,1° et 62,2° correspondant aux plans cristallins (101), (004), (200), (105), (211) et (204) [JCPDS n° 21-1272]. Par contre, la phase rutile montre des pics de diffraction importants à 2θ valeurs de 27,0°, 35,6°, 40,8°, 54,0°, 53,9°, 56,1° et 61,0° ce qui correspond aux plans cristallins de (110), (101), (200), (111), (210), ( 211), (220), (002) et (310) [JCPDS n° 21-1276]. La taille des cristallites et les fractions pondérales des phases anatase et rutile présentées dans les échantillons ont été déterminées à l'aide de la formule de Scherrer et de la méthode de Spurr et Myers, respectivement. Le modèle de poudre XRD de TiO2 -ace a montré qu'il est composé de phase anatase pure (100 %) avec une taille de particule de 48 nm (tableau 1).
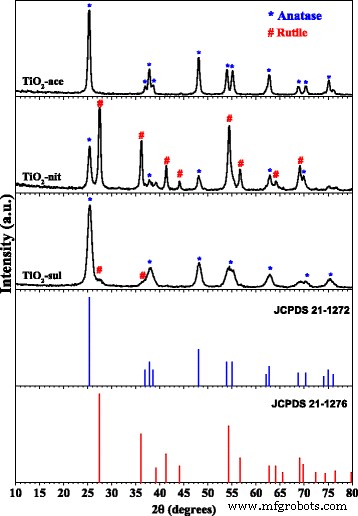
Modèles XRD en poudre du TiO2 calciné échantillons (réimprimés avec la permission de [29]. Copyright @ 2017 Elsevier)
Le TiO2 -sul échantillon possédait principalement une phase anatase (95 %) avec une taille de particules d'environ 23 nm ; cependant, un petit pic de diffraction correspondant au plan (110) de la phase rutile peut être observé dans cet échantillon. En revanche, TiO2 -nit a montré des réflexions XRD pour les phases anatase et rutile avec une taille de cristallite de 41 nm et 50 nm, respectivement. On observe que le rutile est la phase majeure (67%) dans cet échantillon. Ces résultats indiquent que la nature de l'acide peptisant joue un rôle dans la formation de TiO2 phase.
Microscopie électronique à transmission haute résolution
La MET a été réalisée pour examiner la taille des particules, la cristallinité et la morphologie du TiO2 synthétisé nanopoudres. Les images TEM et HRTEM de TiO2 synthétisé les nanopoudres sont affichées sur la Fig. 2. On peut voir que le TiO2 -sul échantillon se compose de particules d'anatase agglomérées étroitement agglomérées avec une taille de grain moyenne estimée à environ 7 nm. Le TiO2 L'échantillon -nit possédait des nanoparticules d'une taille comprise entre 10 et 20 nm avec une morphologie sphérique et également de grandes feuilles d'une largeur de 20 nm. En revanche, TiO2 -l'échantillon d'as se compose de TiO2 les nanoparticules (15-20 nm) consistaient en une morphologie sphérique principalement définie. Vinogradov et Vinogradov [31] ont également observé le même type de résultats que les agrégats de petite taille ont été détectés lors d'acides peptisants forts tels que HNO3 et H2 SO4 ont été utilisés pour la peptisation. La taille des cristallites mesurée par la formule de Scherer a donné des tailles de cristallites plus grandes par rapport à la taille des grains mesurée avec l'analyse MET. Comme indiqué précédemment, la taille des cristallites est différente de la taille des grains; cependant, la taille des cristallites pourrait correspondre à la taille des grains dans certains cas [32]. On peut observer que les images HRTEM de TiO2 -sul et TiO2 -les échantillons d'as montraient des particules contenant des franges correspondant à des plans de réseau cristallin anatase avec d -espacement de 0,356 nm pour le plan (101) [33], alors que l'image HRTEM de TiO2 -L'échantillon de nit a montré des particules avec des franges de réseau pour le plan de réseau cristallin de rutile (110) avec d -espacement de 0,325 nm avec le plan du réseau cristallin anatase (101).

Images TEM et HRTEM du TiO2 calciné échantillons
Spectroscopie Raman
La spectroscopie Raman a également été utilisée pour sonder la formation de phase dans le TiO2 synthétisé échantillons. La figure 3 montre les spectres Raman obtenus pour les trois TiO2 échantillons calcinés à 500 °C. Il est rapporté que les phases anatase et rutile possédaient respectivement six et cinq bandes Raman actives (anatase 143, 195, 395, 512 et 638 cm −1 ; rutile 145, 445, 611 et 826) [34]. Il ressort clairement de la Fig. 3 que les trois échantillons présentaient une bande Raman très intense et nette (E g ) dans la plage de 141 à 146 cm −1 , qui est une bande caractéristique due à la présence de phase anatase. Des bandes Raman de faible intensité dues à la fois aux phases anatase et rutile peuvent être clairement observées sur la figure en médaillon. Le TiO2 -nit et TiO2 -les échantillons sul présentaient des bandes Raman dues à la fois aux phases anatase et rutile ; cependant, l'intensité des bandes Raman due à la présence de phase rutile est élevée dans le cas de TiO2 -nit échantillon. En revanche, TiO2 -l'échantillon d'as présentait des bandes Raman en raison de la phase anatase uniquement.
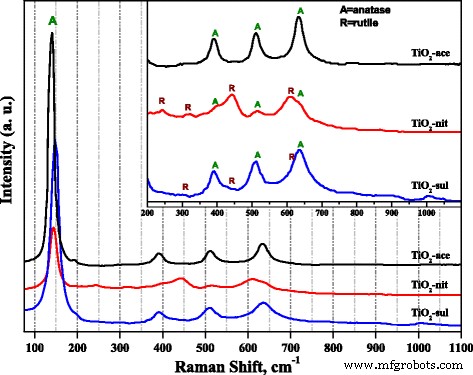
Spectres Raman du TiO2 calciné échantillons
Il a été rapporté que les résultats de la spectroscopie Raman pourraient être utilisés pour étudier la taille des particules de TiO2 nanoparticules, car un décalage inhabituel des bandes Raman pourrait être corrélé à la diminution de la taille des particules des échantillons [35]. Dans la Fig. 3, le TiO2 -échantillon d'as exposé E g bande à 141,5 cm −1 ; cependant, la bande a été décalée à 146 et 150 cm −1 en cas de TiO2 -nit et TiO2 -sul échantillons, respectivement. Les observations des spectres Raman indiquent que TiO2 -sul échantillon possédait une petite taille de particule que les deux autres échantillons, ce qui est conforme aux observations XRD et MET.
Réflectance diffuse UV-vis
Le DR UV-vis spectres du TiO2 synthétisé les échantillons traités thermiquement à 500 °C ont été montrés sur la Fig. 4. La position du pic maximum dans la dérivée du DR UV-vis spectres pour trois échantillons a été montré dans l'encart de la figure. Cela montre clairement que les échantillons ont une forte réflectance électronique dans la région UV. Le maximum de pic de réflectance est différent pour les échantillons synthétisés à l'aide de trois acides différents. Le TiO2 -sul échantillon a montré un pic maximum à 372 nm, alors qu'il est décalé à 383 nm dans TiO2 -ace et 402 nm pour TiO2 -nit échantillon, respectivement. Il est rapporté que l'anatase et le rutile ont une énergie de bande interdite de 3,2 eV (380 nm) et 3,0 eV (415 nm), respectivement [1]. Les différences de réflectance maximale pourraient être attribuées au changement de la taille des cristallites et de la structure de phase des échantillons [36]. Le maximum d'absorption s'est déplacé vers des longueurs d'onde plus élevées pour les échantillons qui ont un pourcentage plus élevé de phase rutile. L'énergie de la bande interdite (eV) a été calculée pour les échantillons calcinés en déterminant la relation entre hν et (αhν) [2] [Fichier supplémentaire 1 :Figure S1]. Les données ont révélé que l'énergie de la bande interdite pour TiO2 -sul (3,12 eV) est plus élevé que TiO2 -ace (2,99 eV) et TiO2 -nit (2,97 eV). La bande interdite du TiO2 diminué lorsque la phase rutile est dominée dans l'échantillon. Il a été rapporté que la bande de valence (VB) des phases anatase et rutile est principalement due à O2p États; d'autre part, la bande de conduction (CB) est composée de Ti 3d déclare [37]. L'énergie de bande interdite de TiO2 est établi par les positions CB et VB, qui sont principalement influencées par la composition des phases. Ainsi, l'énergie de la bande interdite de l'échantillon qui contenait à la fois des phases d'anatase et de rutile doit se situer entre les valeurs d'anatase pure et de rutile.
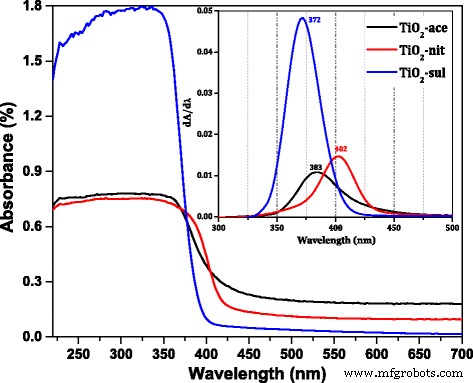
DR UV-vis spectres du TiO2 calciné échantillons (encart ; la dérivée du DR UV-vis spectres)
N2 -Mesures de physisorption
Les isothermes d'adsorption-désorption d'azote pour les trois échantillons synthétisés sont présentés sur la figure 5a. Des isothermes de type IV avec boucle d'hystérésis de type H2 ont été observés pour les échantillons synthétisés par peptisation à l'acide acétique (TiO2 -ace) et l'acide sulfurique (TiO2 -sul). Ceci indique que ces deux échantillons possèdent des mésopores issus des agrégats de TiO2 nanoparticules. Cependant, une isotherme typique de type IV avec une boucle d'hystérésis étroite de type H3 (caractéristique des pores ouverts et/ou en forme de fente) a été observée pour TiO2 -nit échantillon. On peut également observer que la boucle d'hystérésis était fermée à haute pression relative (P/P 0 = 1) et cette observation indiquant la présence de pores de grande taille [38].
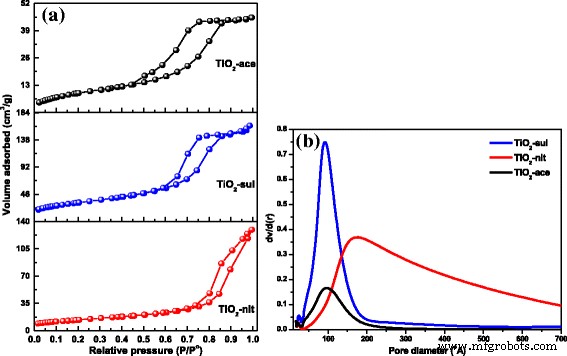
un N2 isothermes d'adsorption-désorption. b Distribution de la taille des pores pour le TiO2 calciné échantillons (réimprimés avec la permission de [29]. Copyright @ 2017 Elsevier)
Les distributions de taille de pores du modèle BJH pour les matériaux synthétisés ont été obtenues à partir des valeurs de la branche d'adsorption des isothermes. Les distributions de la taille des pores BJH des échantillons sont illustrées à la figure 5b. Des distributions de taille de pores monomodales étroites ont été observées pour TiO2 -as et TiO2 -sul échantillons. Cependant, une distribution plus large du diamètre des pores a été observée pour l'échantillon préparé avec de l'acide nitrique, probablement en raison de l'existence d'espaces vides entre les particules plus grosses. Les propriétés de texture des échantillons sont présentées dans le tableau 1. Les résultats ont montré qu'une grande surface (115 m 2 g −1 ) a été observée pour le TiO2 -Ace échantillon calciné à 500 °C. L'ordre de S PARIER le changement était TiO2 -ace> TiO2 -sul> TiO2 -lente. Les résultats observés indiquent clairement que les conditions de peptisation adaptées ont été très efficaces dans la génération de nanoparticules à texture poreuse.
Spectroscopie infrarouge à transformée de Fourier
L'activité photocatalytique du TiO2 dépend de la cristallinité, de la taille des cristallites, de la composition, du taux de recombinaison électron-trou, de la surface et également de la densité des groupes hydroxyles de surface [39]. Des techniques spectroscopiques FTIR et XPS ont été utilisées pour étudier la nature des groupes -OH présentés dans le TiO2 calciné échantillons. La figure 6 montre les spectres FTIR pour les trois TiO2 échantillons compris entre 1 600 et 4 000 cm −1 . Il est rapporté que TiO2 le support pourrait posséder différents types de groupes hydroxyle de surface; ils peuvent être classés comme Ti-OH isolé, groupes hydroxyle liés les uns aux autres par liaison hydrogène et H2 liés chimiquement Molécules O [40].
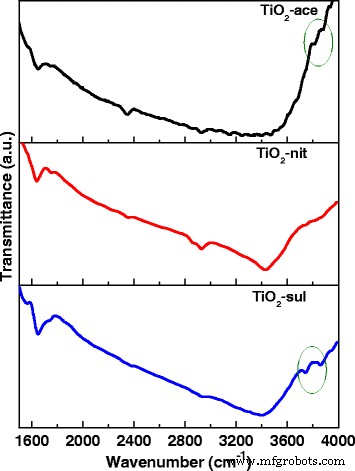
Spectres FTIR du TiO2 calciné échantillons
Les trois échantillons présentaient une large bande centrée à 3408 cm −1 , qui est attribuée à la vibration d'étirement des groupes O-H (molécules d'eau et les groupes -OH de surface libre). Des bandes supplémentaires sont également apparues à 2 340 et 1 640 cm −1 , qui pourrait être attribué à la vibration d'étirement O-H et au H2 moléculairement adsorbé O, respectivement [41]. Une existence de deux vibrations d'étirement -OH en cas d'anatase (à 3715 et 3675 cm −1 ) et une bande faible à 3680 cm −1 avec le rutile ont été rapportés précédemment [42]. Un résultat très similaire peut être observé dans le cas du TiO2 synthétisé échantillons.
Spectroscopie photoélectronique à rayons X
La figure 7 montre le Ti2p déconvolué et O1s Spectres XP pour le TiO2 synthétisé échantillons. Les trois échantillons ont montré deux pics majeurs à 457,2 et 463,1 eV correspondant à 2p 3/2 et 2p 1/2 de Ti 4+ en TiO2 [43]. Des valeurs d'énergie de liaison très similaires ont été observées dans Ti 2p région pour les trois TiO2 échantillons indiquant que les atomes de Ti dans ces échantillons existaient dans le même état d'oxydation. Deux petits pics d'épaulement à 455,8 et 458,7 eV ont également été observés pour tous les échantillons. L'épaule à 455,8 eV pourrait être attribuée à un Ti 3+ état, en raison d'un manque d'oxygène en TiO2 [44], tandis que l'autre pic d'épaule à 458,7 eV provient d'un Ti 4+ l'état de l'espèce Ti-OH [45]. Il ressort du Ti2p spectres que la contribution du TiO2 pauvre en oxygène l'espèce est plus élevée en TiO2 -nit que TiO2 -sul et TiO2 -As échantillons. Tous les échantillons ont montré des O1s XP culmine à 528,4, 529,3 et 531,3 eV. Le pic XPS à 528,4 eV peut être attribué à l'O-Ti 4+ espèces dans le TiO2 réseau cristallin, tandis que deux autres pics à 529,3 et 531,3 eV peuvent être attribués aux espèces d'oxygène présentées dans les groupes hydroxyle adsorbés en surface [46].
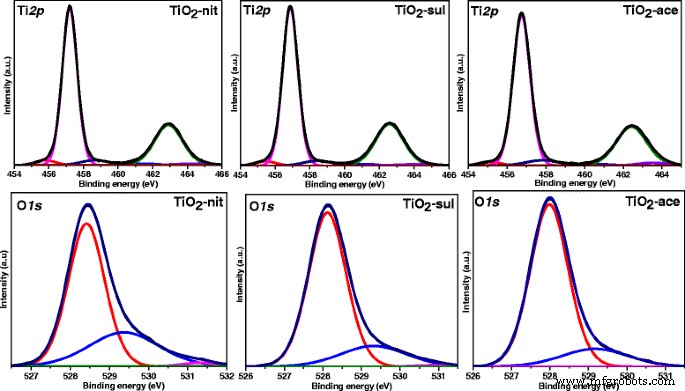
Ti 2p et O1s Spectres de photoélectrons X pour le TiO2 calciné échantillons
McCafferty [47] a également observé que les O1s Le pic possédait un pic de queue aux valeurs d'énergie de liaison élevées, ce qui pourrait être dû à la présence de groupes Ti-OH. Depuis la surface physiquement adsorbée, les groupes Ti-OH peuvent être facilement éliminés sous le vide ultra poussé utilisé pour faire fonctionner l'instrument XPS [48]. Ces groupes -OH présentés dans les échantillons doivent être dus à Ti-OH qui sont chimiquement liés aux défauts de surface de TiO2, où les pourcentages de groupes -OH dans les espèces oxygénées totales pour TiO2 -nit est légèrement supérieur à celui de TiO2 -sul et TiO2 -as (tableau 2).
Dégradation photocatalytique du cristal violet, du bleu de méthylène et du Para -Nitro Phénol Colorants
L'activité photocatalytique du TiO2 calciné nanoparticules pour la dégradation de CV, MB et p -NP a été estimé. Il est rapporté que la réaction de dégradation photocatalytique suit généralement la cinétique de Langmuir-Hinshelwood [1]. Par conséquent, la dégradation photocatalytique des colorants organiques peut être exprimée sous la forme
$$ -\mathrm{dc}/\mathrm{dt}=\mathrm{kC} $$ (5)et après l'intégration, l'Eq. (4) peut être dérivé
$$ C={C}_0{\exp}^{\left(-\mathrm{kt}\right)} $$ (6)où C 0 est la concentration initiale (ppm) des colorants organiques, et k est la constante de vitesse, qui dépend du temps de réaction, de la température et du pH de la solution. Normalement, l'efficacité photocatalytique du catalyseur augmente avec le temps de fonctionnement.
Des expériences à blanc ont été réalisées pour confirmer l'importance à la fois du photocatalyseur et de l'irradiation UV. Aucune réaction n'a eu lieu lorsque le catalyseur et l'irradiation UV ont été appliqués seuls. Des résultats similaires ont été observés dans nos résultats précédents [49]. Comme indiqué dans la section expérimentale, le TiO2 les photocatalyseurs ont été équilibrés avec la solution de colorant organique pendant 45 min pour déterminer l'adsorption des colorants organiques sur du TiO2 synthétisé échantillons. Les UV-vis spectres d'absorption de CV, MB et p -NP ont été enregistrés après l'équilibrage du photocatalyseur. Fichier supplémentaire 1 :les figures S2, S3 et S4 affichent la variation de l'UV-vis spectres d'absorbance de CV, MB et p -Solutions NP (10 ppm) avec des temps de réaction différents sur TiO2 -as, TiO2 -sul, et TiO2 -nit échantillons, respectivement. The intensity of absorption peaks which corresponds to the CV, MB, and p -NP was decreased with the increase of reaction time. The UV-vis spectra of reaction products indicate that organic dyes were degraded during the photoreaction. The TiO2 -nit sample found to be the most effective photocatalyst in comparison with TiO2 -sul and TiO2 -ace samples. Degradation of 50% of p -NP was observed within 60 min for the TiO2 -nit sample, whereas 75 and 100 min were needed for the degradation of 50% p -NP for the TiO2 -ace and TiO2 -sul samples under similar conditions. Similar photocatalytic activity patterns were observed for degradation of MB and CV dyes.
The percentage degradation efficiency of the investigated catalysts was calculated using Eq. (4). Figure 8 shows the percentage changes of CV, MB, and p -NP aqueous solution at room temperature in the presence of calcined TiO2 samples. After just 10 min of the reaction, the TiO2 -nit sample showed 29% CV degradation efficiency, while TiO2 -ace and TiO2 -sul samples showed only 17 and 9%, respectively. The photocatalytic activity steeply increased with the increase of reaction time over the three samples. However, after 120 min, TiO2 -nit and TiO2 -ace samples showed 99% efficiency; however, TiO2 -sul sample showed only 65% efficiency.
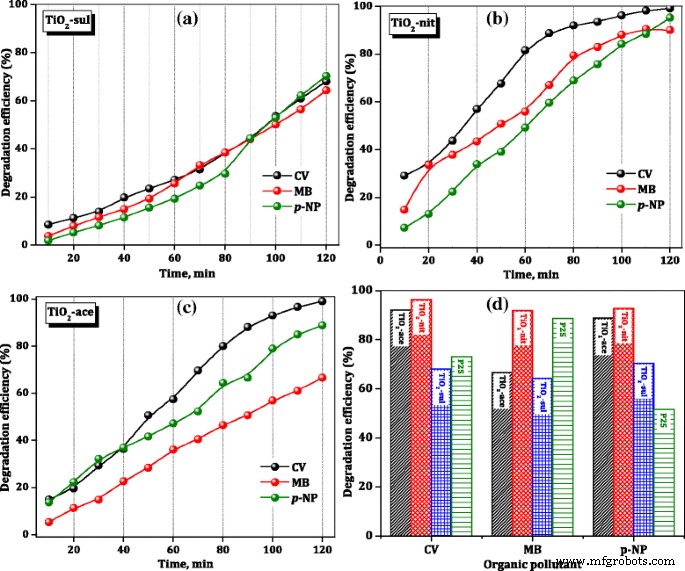
Photocatalytic degradation efficiency of TiO2 catalysts
To compare the photocatalytic performance of synthesized TiO2 samples, the degradation efficiency of the commercial P25 sample for organic dyes after 120 min is included in Fig. 8d. It is clear that TiO2 -nit sample showed better performance than the P25 sample in the degradation of three organic dyes; however, TiO2 -ace and TiO2 -sul samples showed lower activity than the P25 catalyst in case of p -NP degradation. These results are suggesting that the performance of catalysts is influenced by the physicochemical characteristics of the TiO2 samples and nature of the organic dye.
The rate constants for photocatalytic degradation of CV, MB, and p -NP over synthesized TiO2 samples and commercial P25 sample were determined from the slope of the straight line which is plotted between ln(C 0 /C t ) and t , and the results are presented in Table 3. The observed results are indicating that the photocatalytic activity of the degradation of organic dyes was greatly influenced by the composition of TiO2 sample and amount of the surface hydroxyl groups. The activity indeed is not influenced by the particle size, crystallinity, and surface area of TiO2 synthesized in this work. This observation is not consistent with the results observed by Fujishima et al. [8] that the catalyst which possesses lower particle size offered high photocatalytic efficiency.
Previously, it was reported that anatase is a better photocatalyst than rutile due to its high band gap energy and a large number of surface OH groups [50]. It was thought that TiO2 -nit sample would offer low photocatalytic activity due to the presence of more rutile phase (67%). However, Masahashi et al. [51] claimed that rutile exhibited higher performance than anatase MB degradation due to its superior crystalline nature.
Determination of photocurrent values was carried out to obtain a better insight responsible factor for the superior photocatalytic performance of the samples containing more rutile. It was reported that photocatalytic activity is directly related to the electron-hole separation efficiency of a catalyst which is influenced by the photocurrent density [52]. Theoretical photocurrent density of the TiO2 samples was calculated from the absorption edge of the TiO2 samples (obtained from DR UV-vis spectroscopy measurements) and theoretical equations (supporting information) presented in the literature [53]. The results of photocurrent of TiO2 samples are presented in Table 4 along with the percentage of rutile and photocatalytic efficiency values. The photocurrent density of TiO2 -nit (0.545 mA/cm 2 ) is higher than other two synthesized TiO2 samples and also commercial P25 sample (0.401 mA/cm 2 ), manifesting the beneficial role of rutile phase in improving the photoactivity of TiO2 samples.
Previously, Melcher et al. [54] reported that photocatalytic capability of the commercial P25 material originates due to the presence of a mixture of rutile and anatase phases in the sample (75% anatase and 25% rutile). Hirakawa et al. [55] indicated that pure rutile itself is not a powerful photocatalyst, and it is also reported that the light with a wavelength of 380 nm is not powerful enough to generate charge carriers in the pure anatase [56]. Based on XPS spectroscopy results and theoretical calculations, Scanlon et al. [57] concluded that electrons were moved from rutile to anatase and the holes were transported from anatase to rutile, which inhibited the electron-hole recombination. Yu et al. [58] reported a similar observation that TiO2 sample with mixed phases was beneficial to decrease the rate of h + -e − recombination and thus enhance the photocatalytic efficiency of the catalyst.
In literature reports, two possible transfer mechanisms have been proposed for anatase-rutile composite samples [59]. The first mechanism is the interfacial electron transfer from CB of anatase to that of the rutile [60], and the second one is an electron transfer from CB of rutile to lower energy anatase active sites [61]. It is known that the anatase CB possesses higher negative potential than the rutile CB due to the fact that anatase has a higher band gap (3.12 eV) than rutile. Therefore, it is not possible for an electron to move from the rutile CB to the anatase CB because it would have to overcome the energetic barrier between the two bands. The band gap of anatase VB is also slightly higher, than the rutile VB, so the generated holes could be moved to the anatase VB, to achieve an effective charge separation. Most probably, the electron-hole pair is formed in the composite of rutile and anatase in case of TiO2 -nit and TiO2 -sul samples (Fig. 9), and this rate is much higher in TiO2 -nit sample due to predominant rutile formation.
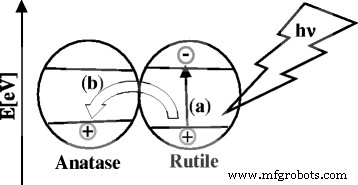
Plausible model of a generation of electron-hole pairs and b effective charge carrier separation via transfer of the generated holes into the anatase valence band
It was reported that increase of crystal growth of initial phase is possible by increasing the mobility of ions presented in precursor solution [62]. Several researchers added small volumes of mineral acids (such as hydrochloric acid and sulfuric acid) to improve the mobility of dissociated ions [63]. Their role is not only to increase the rate of diffusion of ions in a solution but also to alter the surface charge. Under humidity conditions, titanium isopropoxide can subsequently undergo hydroxylation and polymerization to TiO2 .
$$ \mathrm{Ti}{\left(\mathrm{OPri}\right)}_4+4{\mathrm{H}}_2\mathrm{O}\to \mathrm{Ti}{\left(\mathrm{OH}\right)}_4+4\ \mathrm{PriOH}\kern2.5em \left(\mathrm{hydroxylation}\right) $$ (7) $$ \mathrm{Ti}{\left(\mathrm{OH}\right)}_{4\kern0.5em }\to {\mathrm{TiO}}_{2.}x{\mathrm{H}}_2\mathrm{O}+\left(2\hbox{-} x\right)\ {\mathrm{H}}_2\mathrm{O}\kern5em \left(\mathrm{condensation}\right) $$ (8)Depending on the nature of peptizing acid, the transformation of TiO2 leads to anatase or rutile phase [64]. Formation of amorphous TiO2 or metastable anatase phase was observed when the condensation initiated before hydrolysis of Ti precursor. Under highly acidic conditions, the rutile phase formation is favorable as the rate of condensation is slow. Accordingly, the rutile phase was obtained when sulfuric and nitric acids were used for the peptization. The use of weak acid (acetic acid) as a peptizing agent allows the control of both the degree of condensation and oligomerization and persuades the preferential crystallization of TiO2 in the anatase phase. Zeng et al. [20] used polycarboxylic acid as a peptizing agent and observed the formation of nanoparticles of anatase which they attributed to chelation effect of organic acid.
It is known that TiO6 octahedra are a fundamental structural unit for both anatase and rutile phases (D 4h system), and the only difference between these two structures is the assembly of the octahedral chains [65]. Face-shared linking of TiO6 units results in anatase structure, while edge-shared linking results in rutile structure [66]. It is clear that NO 3− anions possessed weaker affinity to Ti atoms in an aqueous solution than CH3 COO − and SO4 2− anions. The strong affinity of CH3 COO − and SO4 2− anions with Ti atoms is responsible for the inhibition of the phase transformation.
In the previously reported studies, many of the photocatalysts have not been tested for reuse mainly due to undergo photocorrosion; hence, their photostability is reduced for further usage. The reusability of the calcined TiO2 samples was examined to study the effectiveness of these photocatalysts. It was observed that the used photocatalyst offered 90% efficiency for three consecutive cycles. The efficiency of the catalyst was reduced to 80 and 75% during fourth and fifth cycle, respectively. The decrease is due to the loss of some amount of catalyst during the filtration and regeneration procedures.
Conclusions
A simple peptization method was adapted to synthesize TiO2 nanoparticles by using sulfuric, nitric, and acetic acid as peptizing agents and titanium isopropoxide as Ti precursor. The influence of acid species on the crystal phase, morphology, textural, and surface composition of TiO2 were studied in detail. The TiO2 sample peptized with acetic acid possessed pure anatase phase, while the formation of minor (5%) and major (67%) of rutile phase was observed in case of samples peptized with sulfuric acid and nitric acid, respectively. It is observed that TiO2 peptized with nitric acid showed sheet-like structures along with nanoparticles, while TiO2 samples peptized with sulfuric and acetic acids possessed near spherical nanoparticles. The photocatalytic properties of synthesized TiO2 nanostructures were evaluated for photodegradation of aqueous CV, MB, and p -NP solutions. The TiO2 peptized using nitric acid showed the best photocatalytic activity than commercial P25 and other two peptized samples, and its photodegradation efficiency was reached to 95% in 120 min for p -NP degradation. Although TiO2 samples peptized using sulfuric acid and acetic acid possessed smaller particle size, higher band gap energy, and high surface area, TiO2 sample peptized with nitric acid possessed a higher percentage of rutile and photocurrent density. The observed photocurrent density is dominated by the photoactivity of TiO2 . The results indicate a direct correlation between the photocatalytic activity and the photocurrent density of the TiO2 samples. The superior activity of TiO2 sample peptized with nitric acid is due to the effective transfer of photogenerated electrons between rutile and anatase phases, and large pore diameter could have enhanced the diffusion and mass transportation of reacting molecules and OH radicals during the photochemical reaction. The synthesized TiO2 photocatalysts can be recycled with a minor change in the activity.
Abréviations
- CV:
-
Crystal violet
- DR UV-vis :
-
Diffuse-reflectance ultraviolet-visible spectroscopy
- FTIR:
-
Fourier transform infrared spectroscopy
- HRTEM:
-
High-resolution transmission electron microscopy
- MB:
-
Methylene blue
- NMR:
-
Nuclear magnetic resonance
- p –NP:
-
para –nitro phenol
- TEM :
-
Microscopie électronique à transmission
- TiO2 :
-
Titanium oxide
- XPS:
-
X-ray photoelectron spectroscopy
- XRD:
-
X-ray powder diffraction
Nanomatériaux
- Route d'électrofilage en une étape des nanofibres Rutile TiO2 modifiées par SrTiO3 et ses propriétés photocatalytiques
- Haute performance photocatalytique de deux types de photocatalyseurs composites TiO2 modifiés au graphène
- Des nanoparticules comme pompe à efflux et inhibiteur de biofilm pour rajeunir l'effet bactéricide des antibiotiques conventionnels
- Vers les nanofluides TiO2 – Partie 2 :Applications et défis
- Effet de la distribution de nanoparticules d'or dans le TiO2 sur les caractéristiques optiques et électriques des cellules solaires à colorant
- Les effets du rapport Li/Nb sur la préparation et les performances photocatalytiques des composés Li-Nb-O
- Activités photocatalytiques renforcées par des nanoparticules Au-Plasmonic sur une photoélectrode de nanotube de TiO2 recouverte de MoO3
- Préparation et performances photocatalytiques des photocatalyseurs à structure creuse LiNb3O8
- Propriétés structurelles et optiques dans le proche infrarouge du TiO2 dopé au Cr pour les pigments froids colorés



