Synthèse de points quantiques de sulfure d'antimoine solubles dans l'eau et de leurs propriétés photoélectriques
Résumé
Sulfure d'antimoine (Sb2 S3 ) est appliquée depuis longtemps dans les dispositifs photoélectriques. Cependant, il y avait un manque d'informations sur Sb2 S3 points quantiques (QD) en raison des difficultés de synthèse. Pour combler cette vacance, Sb2 soluble dans l'eau S3 Les QD ont été préparés par injection à chaud en utilisant un mélange de bromure d'hexadécyltriméthylammonium (CTAB) et de dodécylsulfate de sodium (SDS) comme tensioactif anionique-cationique, d'alcanolamide (DEA) comme stabilisant et d'acide éthylènediaminetétraacétique (EDTA) comme dispersant. Les propriétés photoélectriques, y compris l'absorption et l'émission, ont été caractérisées par un spectrophotomètre UV-Vis-IR et une technique spectroscopique de photoluminescence (PL). Une émission PL intensive à 880 nm a été trouvée, indiquant Sb2 S3 Les QD ont de bonnes perspectives dans les applications laser proche infrarouge et laser proche infrarouge. Sb2 S3 Des films minces QD ont été préparés par croissance par auto-assemblage puis recuits dans de la vapeur d'argon ou de sélénium. Leurs bandes interdites (E g s) ont été calculés en fonction des spectres de transmission. Le E g de Sb2 S3 Le film mince QD s'est avéré être réglable de 1,82 à 1,09 eV via recuit ou sélénylation, démontrant les bonnes perspectives dans les applications photovoltaïques.
Contexte
Les points quantiques (QD) ont reçu beaucoup d'attention au cours de la dernière décennie en raison de leurs propriétés photoélectriques manipulées et de leur capacité de traitement supérieure pour l'ingénierie des dispositifs [1,2,3]. En règle générale, les QD composés de plomb tels que le PbS et les pérovskites aux halogénures de plomb sont récemment apparus comme des matériaux candidats prometteurs dans des applications photoélectriques telles que le photovoltaïque, les OLED, les lasers et les photodétecteurs en raison de leur synthèse simple et de leurs performances satisfaisantes [4,5,6]. En outre, une gamme de QD semi-conducteurs, tels que CdS, CdSe, ZnS, ZnSe, HgTe, CuInSe2 , CuInS2 , et CdHgTe, et l'appareil de base ont été signalés partout.
Sb2 S3 est connu comme le sulfure d'antimoine le plus courant, qui est un matériau semi-conducteur prometteur pour la fabrication de semi-conducteurs photoélectriques [7, 8]. Il a une bande interdite modérée d'environ 1,7 à 1,8 eV sous forme cristalline (stibine). Curieusement, la bande interdite est accordable dans la plage de 1,1 à 1,8 eV lorsque le soufre est en partie remplacé par le sélénium [9]. Naturellement, Sb2 S3 est un matériau multifonction qui pourrait être utilisé comme absorbeur ou sensibilisateur pour dispositif photovoltaïque, catalyse photochimique et photodétecteur. En outre, Sb et S sont des éléments relativement abondants, peu coûteux et peu toxiques, ce qui en fait un potentiel pour une application à grande échelle. Le sulfure d'antimoine a une aptitude au traitement unique. Ils peuvent être évaporés sous vide à basse température (~ 400 °C) ou mis en solution à l'aide de divers matériaux. Sb2 S3 était généralement appliqué dans les cellules solaires sensibilisées. Utilisation d'un Sb2 traité au thioacétamide S3 sensibilisateur déposé par dépôt chimique en solution (CBD), une cellule solaire hybride sensibilisée avec un rendement de conversion de puissance (PCE) de 7,5% a été réalisée [10]. Récemment, les cellules solaires à hétérojonction planaire traitées en solution avec une structure simple ont atteint un PCE très satisfaisant de 4,3%, dans lequel un Sb2 S3 le film a été préparé par la technique conventionnelle de centrifugation avec un précurseur contenant du Sb2 O3 , CS2 , et la n-butylamine [7]. Nanostructure Sb2 S3 synthétisé par la méthode de la solution a été largement appliqué pour les photodétecteurs haute performance [11,12,13]. Sb2 S3 Les photodétecteurs basés sur le NW ont présenté une bonne photo-réponse dans une large gamme spectrale de 300 à 800 nm. Surtout à 638 nm, ils ont montré des valeurs optimales avec un rapport ON/OFF de courant élevé d'environ 210, une sensibilité spectrale de 1152 A/W, une détectivité de 2 × 10 13 Jones, et les temps de montée et de descente d'environ 37 ms [11]. Sb2 traité par la solution S3 Le nanotige était généralement utilisé comme photocatalyseur efficace pour la dégradation des colorants [14] et les batteries sodium-ion hautes performances [15]. Malheureusement, il y avait peu d'informations rapportées sur Sb2 S3 QD.
Nous croyons Sb2 S3 les matériaux à dimension zéro doivent avoir des propriétés optiques et électriques inhabituelles par rapport aux matériaux multidimensionnels en raison de l'effet de confinement quantique. Pour combler cette vacance, le présent article a d'abord rapporté la synthèse de QD de sulfure d'antimoine soluble dans l'eau en utilisant un mélange CTAB et SDS comme tensioactif anionique-cationique, DEA comme stabilisant et EDTA comme dispersant dans des conditions de bain d'huile à 120 °C. Afin de surmonter l'interférence de l'hydroxyle, la réaction a été conduite dans du 2-méthoxyéthanol anhydre au lieu de l'eau. Ces précurseurs sont non toxiques, inodores et peu coûteux par rapport aux additifs conventionnels [16, 17]. Avant l'application substantielle, les propriétés structurelles, optiques et électriques ont été étudiées ici.
Expérimental
Sb2 S3 Les QD ont été synthétisés par la méthode d'injection rapide à chaud. Dans une procédure typique pour la préparation, SDS (0,05 mmol, 99,5 %), CTAB (0,05 mmol, 99,5 %), EDTA (0,2 mmol, 99,5%) et DEA (4 ml, 99,9 %) ont été mélangés dans le 100- ml de 2-méthoxyéthanol anhydre et dissous après 20 min d'agitation magnétique dans un bain d'huile à 120 °C. Ensuite, 0,5 mmol de thioacétamide (TAA) a été dissous dans la solution chaude. Ensuite, 2 ml d'acétate d'antimoine - solution d'acide acétique (0,25 M) - ont été injectés dans la solution de précurseur sous agitation magnétique. Immédiatement, la solution est passée du transparent au jaune vif, indiquant la formation de sulfure. Le récipient a ensuite été transformé en bain de glace pour terminer la réaction. Le produit final a été centrifugé à 15 000 tr/min pendant 10 min, puis lavé à l'isopropanol à plusieurs reprises pendant au moins trois fois et enfin centrifugé à 6 000 tr/min pendant 5 min pour éliminer les particules grossières.
Sb2 S3 Les QD ont été séchés sous vide à température ambiante puis testés à l'aide d'un analyseur thermique simultané (STA 449 F3, NETZSCH). La structure cristalline a été caractérisée par diffraction des rayons X (XRD, Bruker D8). La mesure de la composition a été effectuée par un spectromètre à dispersion d'énergie (EDS, EDAX Inc.). Sb2 S3 de la poudre (99,99%, Aladdin) a été utilisée comme standard pour l'étalonnage des mesures EDS. Les informations à l'échelle nanométrique des QD ont été caractérisées par microscopie électronique à transmission à haute résolution (HRTEM; Zeiss Libra200) avec diffraction électronique à zone sélectionnée (SAED). Les spectres d'émission ont été enregistrés en utilisant la technique de spectroscopie de photoluminescence (PL, Horiba iHR550) avec un laser He-Ne (325 nm) comme source d'excitation. Les spectres de transmittance optique ont été réalisés sur la dispersion QD et les films en utilisant un spectrophotomètre UV-Vis-IR (Agilent Cary 5000).
Résultats et discussion
La synthèse de Sb2 S3 QDs est un processus peu coûteux, facile à utiliser et reproductible. La réaction chimique peut être décrite dans les deux équations de réaction simples suivantes.
$$ {\mathrm{CH}}_3{\mathrm{CSNH}}_2+2{\mathrm{CH}}_3{\mathrm{OCH}}_2{\mathrm{CH}}_2\mathrm{O}\ mathrm{H}\à {\mathrm{CH}}_3\mathrm{C}{\left({\mathrm{CH}}_3{\mathrm{OCH}}_2{\mathrm{CH}}_2\mathrm{ O}\right)}_2{\mathrm{NH}}_2+{\mathrm{H}}_2\mathrm{S} $$ (1) $$ 2\mathrm{S}\mathrm{b}{\left( {\mathrm{CH}}_3\mathrm{COO}\right)}_3+3{\mathrm{H}}_2\mathrm{S}\à {\mathrm{S}\mathrm{b}}_2{\ mathrm{S}}_3+6{\mathrm{CH}}_3\mathrm{COO}\mathrm{H} $$ (2)Selon le modèle LaMer [18], la séparation des étapes de nucléation et de croissance cristalline est la principale exigence pour la formation de petites particules avec des distributions de taille étroites. Au début de cette réaction, la solution contenant du SDS/CTAB équimolaire avait tendance à former des vésicules catanioniques relativement plus grosses plutôt que des micelles mixtes [16]. La réaction entre S 2− et Sb 2+ a eu lieu rapidement, conduisant à la nucléation explosive. Ensuite, en raison de l'effet de chélation, la formation des complexes ions métalliques-ETDA réduit la concentration en ions métalliques libres [19]. Ainsi, la croissance des grains a été efficacement inhibée, restant Sb2 S3 QD dans la solution.
L'effet de la température et du temps de réaction sur les morphologies des QDs a été étudié en premier. Nous avons trouvé que la forme et la taille étaient presque invariables lorsque la température variait de 90 à 120 °C et que le temps de réaction était contrôlé de 30 s à 15 min. La figure 1a, b montre une image MET et une image haute résolution de la synthèse de l'échantillon à 120 °C. Les images révèlent une bonne monodispersité des QD avec une forme sphérique uniforme, et les diamètres se situent principalement dans la plage de 3 à 5 nm. L'image haute résolution montre une frange de réseau claire, révélant que chaque particule est un quantum monocristallin. SAED présente des cercles concentriques avec des limites indistinctes, indiquant que le nanomatériau synthétisé a une faible cristallinité. Les compositions chimiques ont été analysées par EDS comme le montre la figure 1c. Une analyse EDS élémentaire quantitative des QD révèle que le rapport atomique moyen (S%:Sb%) est de 1,68, indiquant que le rapport stoechiométrique de l'élément soufre est légèrement plus élevé. Nous en avons déduit qu'une partie du soufre était chimisorbée ou physiquement adsorbée à la surface des QDs. La figure 1d montre le spectre XRD des QD séchés sous vide. En gros, le modèle XRD correspond à orthorhombique Sb2 S3 (JCPDS n° 73-0393), confirmant les résultats de l'analyse EDS. Les pics XRD indistincts indiquent la faible cristallinité qui est tout à fait agréable avec le modèle SAED.
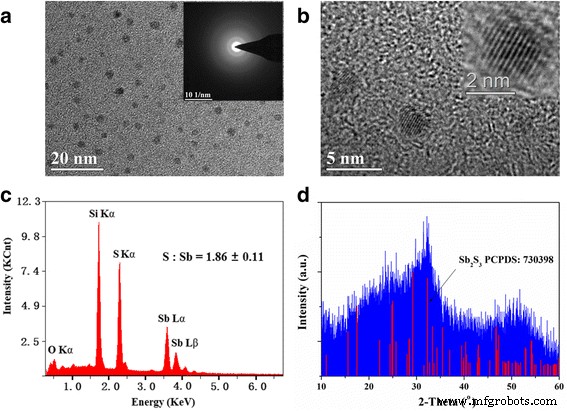
Morphologie et propriétés structurales de Sb2 S3 QD. un Image TEM et modèle SAED. b Image MET haute résolution. c Analyse EDS et d modèle XRD
L'absorption optique de la dispersion QDs-isopropanol a été mesurée par le spectrophotomètre Agilent Cary 5000. Comme on le voit sur la figure 2a, Sb2 S3 La dispersion des QDs est jaune vif et a une large absorption dans presque toute la plage visible. Il montre une absorption presque complète à courte longueur d'onde de 300 à 500 nm et une transmittance élevée dans une région proche infrarouge. La figure 2b montre les spectres de photoluminescence (PL) de dispersion avec une concentration de 2 mg/ml où Sb2 S3 a été préparé avec des temps de réaction différents. Spectres PL pour tous les Sb2 S3 les échantillons présentent deux pics d'émission distincts à environ 510 nm (2,43 eV) et 880 nm (1,41 eV), ce qui est très différent du Sb2 nanostructuré S3 préparé par dépôt chimique en solution (CBD) [20]. Selon le rapport précédent, le CBD synthétisé Sb2 S3 les nanocristaux montrent une faible émission de bord de bande culminant à environ 610 nm (2,03 eV) probablement due à des excitons et une forte émission liée à la lacune de soufre a culminé à 717 nm (1,72 eV). Pour Sb2 hydrosoluble S3 QDs ici, l'émission verte autour de 510 nm résulte vraisemblablement des excitons [21, 22], qui sont bien connus et largement rapportés pour les nanocristaux semi-conducteurs [23], suggérant que l'effet de taille quantique (QSE) apporte une bande interdite plus large pour Sb2 S3 QD. L'émission dans le proche infrarouge autour de 880 nm peut être attribuée à la présence de défauts ponctuels liés à la stœchiométrie. Selon l'analyse EDS discutée ci-dessus, le rapport atomique moyen (S%:Sb%) est de 1,68; nous en avons déduit que le soufre est excessif et le type de défauts ponctuels ici est susceptible d'être des lacunes d'antimoine (V * Sb ). Une observation attentive des courbes révèle que l'émission a culminé à 880 nm de Sb2 S3 Les QD préparés avec un temps de réaction long présentent un léger décalage vers le bleu par rapport aux QD synthétisés rapidement. Ce décalage est probable du fait de la légère amélioration du rapport stoechiométrique. L'émission PL intensive et la transmittance élevée dans une région proche de l'infrarouge font que Sb2 S3 Les QD ont de bonnes perspectives dans la fabrication de LED proche infrarouge [17, 24] et de lasers proche infrarouge appliqués à la détection et au sondage.
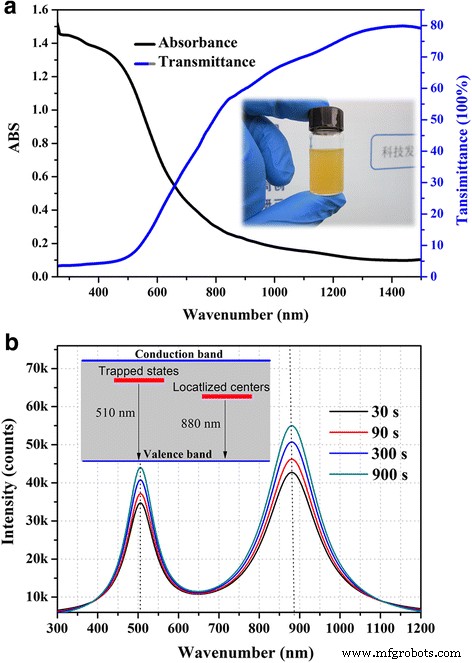
Propriétés optiques de Sb2 S3 Dispersion QD. un Absorbance et b Spectre PL de Sb2 S3 dispersion
Pour approfondir les applications de Sb2 S3 QDs dans le traitement des semi-conducteurs, Sb2 S3 les films ont été préparés par croissance auto-assemblée sur verre à partir d'une dispersion QDs-isopropanol de 5 mg/ml. Avant le traitement de recuit, une analyse thermogravimétrique a été utilisée pour le test de stabilité. Selon les profils TG et DSC pour les QD séchés sous vide illustrés à la Fig. 3a, Sb2 S3 Les QD ont un accroissement de poids d'environ 12 % à partir de la température ambiante, ce qui indique qu'ils ont une activité élevée et ont probablement été partiellement oxydés ou collés à la surface. Sb2 S3 Les QD présentent une stabilité relative dans l'argon à température ambiante, puis montrent la première perte de poids évidente suivie de l'élimination de l'excès de S commencée à 236 °C. Le point de fusion de Sb2 S3 Les QD ont été mesurés à 508 °C, ce qui est remarquablement inférieur à celui du Sb2 cristallin S3 poudre (550 °C, Sigma Aldrich). Nous avons remarqué qu'il y avait une perte de poids lente et progressive sur toute la plage de température d'essai accompagnée d'une perte de constituant S. Sb2 S3 Le traitement de recuit des films QD dans les vapeurs d'Ar et de Se a ensuite été étudié. Les spectres de transmission optique pour les films non traités, recuits et sélénisés sont illustrés à la figure 3b, et la photographie des trois échantillons est illustrée à la figure 3c. Pour les échantillons recuits et sélénisés, les deux ont été traités à 250 °C pendant 5 min. Les bords absorbants des échantillons recuits et sélénisés ont été déplacés de 500 nm à 650 et 850 nm, respectivement. Parce que les deux Sb2 S3 et Sb2 Se3 sont des semi-conducteurs à bande interdite directe [24, 25], la bande interdite moyenne peut être calculée par la formule :
$$ \upalpha =\left(A/\mathrm{h}\upnu \right)\times {\left(\mathrm{h}\upnu -\mathrm{Eg}\right)}^{1/2} $ $ (3)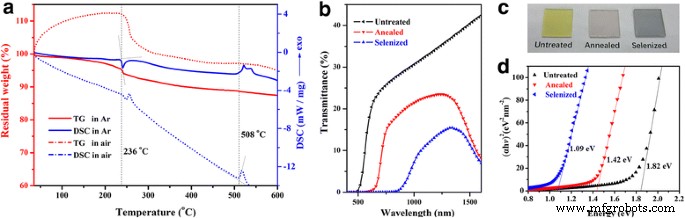
Propriétés photoélectriques de Sb2 S3 Films minces QD. un Profils TG et DSC de Sb2 séché S3 QDs testés dans l'Ar et l'air. b Spectre de transmission, c une photographie, et d analyse de bande interdite de Sb2 pré-et post-recuit S3 Films minces QD
où A est une constante, h est la constante de Planck, et ν est la fréquence du photon incident. Nous avons ajusté la zone linéaire en traçant (αhv ) 2 versus (hv ) et calculé le E moyen g comme le montre la Fig. 3. Comme nous le voyons, le E g de l'échantillon non traité était de 1,82 eV et a diminué à 1,42 eV après 5 min de recuit à 250 °C. La variation de E g indique la cristallinité de Sb2 S3 a été amélioré avec une transformation ordre-désordre accompagnée de la suppression de l'élément S excessif [26]. Pour l'échantillon sélénisé, le E g diminué à un minimum de 1,09 eV, ce qui est très proche du silicium cristallin. L'analyse EDS élémentaire quantitative a révélé que Sb2 S3 a été transformé en Sb2 (S1−x Se x )3 et enfin à Sb2 Se3 après que la plupart du soufre ont été remplacés par le sélénium [7, 9]. Étant donné que la sélénylation est inférieure à 250 °C, nous pensons qu'elle a été bénéfique pour la fabrication et l'amélioration des performances des dispositifs flexibles. Comme nous le savons, la bande interdite optimale pour l'absorbeur de cellules solaires était de 1,45 eV. Ainsi, le Sb2 recuit et sélénisé S3 Les films QD sont de bons candidats pour les matériaux absorbants photovoltaïques.
Conclusions
Une nouvelle façon de synthétiser du Sb2 soluble dans l'eau S3 Les QD ont été développés par injection à chaud en utilisant un mélange CTAB et SDS comme tensioactif anionique-cationique, DEA comme stabilisant et EDTA comme dispersant. Le processus de synthèse est facile à utiliser et reproductible. Tous les réactifs et additifs sont non toxiques, inodores et peu coûteux. Sb2 S3 Les QD ont une émission PL intensive à 880 nm et une transmittance élevée dans une région proche infrarouge, ce qui indique qu'il a de bonnes perspectives dans la fabrication de LED et de lasers proche infrarouge. Sb2 S3 Les QD présentent une bonne monodispersité et une bonne aptitude au traitement, qui peuvent être déposés pour former Sb2 S3 cinéma. Le E g de Sb2 S3 Les films QD ont pu être tournés à 1,42 et 1,09 eV après un traitement de recuit sous vapeur d'Ar ou de Se à moins de 250 °C, démontrant leurs bonnes perspectives dans l'application photovoltaïque.
Abréviations
- CBD :
-
Dépôt de solution chimique
- CTAB :
-
Bromure d'hexadécyltriméthylammonium
- DEA :
-
Alcanolamide
- DSC :
-
Calorimètre différentiel à balayage
- EDS :
-
Spectromètre à dispersion d'énergie
- EDTA :
-
Acide éthylènediaminetétraacétique
- HRTEM :
-
Microscopie électronique à transmission haute résolution
- LED :
-
Diode électroluminescente
- OLED :
-
Diode électroluminescente organique
- PL :
-
Photoluminescence
- QD :
-
Point quantique
- QSE :
-
Effet de taille quantique
- SAED :
-
Diffraction électronique à zone sélectionnée
- FDS :
-
Dodécyl sulfate de sodium
- STA :
-
Analyseur thermique simultané
- TAA :
-
Thioacétamide
- TGA :
-
Analyse thermogravimétrique
- XRD :
-
Diffraction des rayons X
Nanomatériaux
- Synthèse facile et propriétés optiques de petits nanocristaux et nanotiges de sélénium
- Synthèse de points quantiques de type II/Type-I à suppression de réabsorption ZnSe/CdS/ZnS Core/Shell et leur application pour le dosage immunosorbant
- Synthèse de points quantiques de carbone co-dopés en pyridinique N, S en tant qu'imitateurs d'enzymes efficaces
- Effet de la méthode de synthèse des nanoparticules de manganite La1 − xSr x MnO3 sur leurs propriétés
- Synthèse en un seul pot de nanoplaques Cu2ZnSnSe4 et leur activité photocatalytique induite par la lumière visible
- Synthèse sonochimique en une étape facile et propriétés photocatalytiques des composites graphène/Ag3PO4 Quantum Dots
- Dépendance de la toxicité des nanoparticules sur leurs propriétés physiques et chimiques
- 20 types de métaux différents et leurs propriétés
- Types de métaux et leurs propriétés



