Synthèse et propriétés des points quantiques de CdTe alliés au Mn et solubles dans l'eau
Résumé
Dans ce travail, nous avons préparé des boîtes quantiques CdTe et des séries de Cd1-x Mnx Points quantiques en alliage de Te avec une distribution de taille étroite par une réaction d'échange d'ions dans une solution aqueuse. Nous avons constaté que les pics de photoluminescence sont déplacés vers des énergies plus élevées avec l'augmentation de Mn 2+ contenu. Jusqu'à présent, il s'agit du premier rapport de points quantiques à base de CdTe à émission bleue. Au moyen de la voltamétrie cyclique, nous avons détecté des caractéristiques d'activité électrochimique des niveaux d'énergie du manganèse formés à l'intérieur du Cd1-x Mnx Bande interdite des points quantiques en alliage de Te. Cela nous a permis d'estimer leur position énergétique. Nous démontrons également le comportement paramagnétique pour Cd1-x Mnx Points quantiques alliés au Te qui ont confirmé la réussite de la réaction d'échange d'ions.
Contexte
Les propriétés optiques des points quantiques (QD) peuvent être manipulées par dopage/alliage lors de la conception de la composition. Par conséquent, la possibilité de contrôler l'incorporation d'éléments de dopage/alliage dans les réseaux QDs joue un rôle important pour un grand nombre d'applications. En particulier, les QD alliés au Mn sont l'un des matériaux les plus prometteurs pour la détection de fluorescence et l'imagerie par résonance magnétique. Par conséquent, des techniques de synthèse ont déjà été développées pour obtenir Mn 2+ -ZnS, ZnSe, CdSe, CdS dopés/alliés et QDs cœur/coque CdTe/CdS [1,2,3,4,5,6]. Il existe également un certain nombre d'ouvrages qui décrivent les capacités de Mn 2+ - et Zn 2+ -synthèse de QDs CdTe dopés/alliés [7,8,9,10]. L'obtention de telles compositions en solution aqueuse est fortement dépendante du pH ce qui rend le dopage difficile. Cheng et al. ont montré que le milieu alcalin empêchait la nucléation et la croissance des QD de CdTe alliés au Zn [10]. De plus, il existe une forte probabilité d'apparition de Zn(OH)2 à la surface des QD qui inhibe la croissance des QD initiaux en formant une couche de ZnO à la surface des QD. Des processus similaires ont lieu dans une tentative de préparation d'un QD de CdSe allié au Mn en solution aqueuse alcaline [11]. Dans ce cas, Mn 2+ la solvatation se produit à la place de l'échange d'ions de Cd 2+ par Mn 2+ . D'autre part, la différence de constante de solubilité du MnTe et du CdTe indique une réaction de substitution inefficace entre Mn 2+ et CdTe [12].
Dans ce travail, nous appliquons la procédure de synthèse décrite dans nos travaux précédents [13] pour la synthèse de Cd1−x Mnx QD en alliage de Te. Pour assurer un processus d'alliage de Mn réussi, les conditions optimales de pH neutre ont été choisies. Une telle approche a éliminé la formation d'hydroxyde de manganèse lors de la synthèse qui nous a permis d'obtenir du Cd1−x émettant du bleu Mnx QDs alliés au Te par une réaction d'échange d'ions. Les études systématiques de leurs propriétés optiques et électrochimiques permettent de mieux comprendre les changements dans la structure de bande lors de la transformation des QD de CdTe en Cd1−x Mnx QD en alliage de Te.
Méthodes
Synthèse de CdTe et Cd1-x Mnx QD en alliage de Te
CdTe et Cd1-x hydrosolubles stabilisés à l'acide thioglycolique Mnx Les QD alliés au Te ont été synthétisés selon notre méthode en trois étapes modifiée précédemment rapportée [13]. Premièrement, des nanoclusters de CdTe ont été synthétisés en utilisant une méthode facile à température ambiante [14] avec de l'acide thioglycolique comme stabilisant. Les nanoclusters de CdTe obtenus ont été divisés en six aliquotes différentes de 50 ml. Deuxièmement, les solutions colloïdales obtenues de nanoclusters de CdTe ont été soumises à Mn 2+ alliage dû au processus d'échange d'ions avec différentes quantités de MnSO4 sel dans 50 ml de solutions aliquotes sous sonication. Les concentrations de Mn 2+ les ions ajoutés étaient de 1, 5, 10, 15 et 20 % de Cd 2+ contenu dans les mélanges réactionnels (MR). En outre, une aliquote de nanoclusters de CdTe pur a été utilisée comme témoin. L'étape finale était un traitement thermique par chauffage par micro-ondes dans le four à micro-ondes à 700 W pendant 3 min.
Procédures de caractérisation et de mesure des matériaux
Les spectres d'absorption et de photoluminescence (PL) ont été mesurés à température ambiante par le spectrophotomètre OceanOptics USB-2000. Les voltamogrammes cycliques (CV) ont été enregistrés à l'aide d'un potentiostat/galvanostat « ΠИ-50-1 » contrôlé par ordinateur. Un système à trois électrodes consistait en une électrode de travail en platine, une contre-électrode en carbone vitreux et une électrode de référence Ag/AgCl a été utilisée. Les voltamogrammes cycliques ont été obtenus en balayant le potentiel de − 2 à 2 V à une vitesse de balayage de 100 mV s −1 . Images de microscopie électronique à transmission (MET) obtenues avec le microscope Selmi TEM-125 K à une tension d'accélération de 80,00 kV. L'analyse élémentaire du Cd1-x hydrosoluble Mnx Les échantillons QD alliés au Te purifiés par précipitations multiples ont été mesurés par spectroscopie d'émission atomique (AES) С115М1. Les spectres EPR ont été enregistrés à l'aide du spectromètre EPR en bande « Radiopan » à 300 K. Modulation de cent kilohertz du champ magnétique avec une amplitude de 0,1 mT. Des programmes visuels EPR ont été utilisés pour le traitement (déconvolution, ajustement et modélisation) des spectres obtenus [15]. Des échantillons de poudre contenant des QD ont été préparés par précipitation de QD à partir de la solution aqueuse par la méthode décrite dans [16]. Les échantillons ont été séchés à 35 °C pendant 5 h. La composition de phase des échantillons a été déterminée par des mesures XRD de poudre à l'aide du diffractomètre Bruker D8 Advance. L'identification de la phase cristalline de Cd1-x Mnx Te a été fait à l'aide de la carte de base de données XRD :ICSD no. 040413 (Match! version 3.6.0.111 du logiciel).
Résultats et discussion
Caractérisation structurelle du CdTe et du Cd1-x Mnx QD en alliage de Te
Analyse TEM
Les images MET de Cd0.91 Mn0,09 Les QD alliés au Te ont indiqué que le diamètre moyen est cohérent avec le diamètre des QD CdTe calculé à partir des mesures spectroscopiques selon la méthode décrite dans [14]. La figure 1 montre une image TEM pour Cd0.91 Mn0,09 QD en alliage de Te. La grande majorité des QD d'une taille moyenne de 2,3 ± 0,3 nm ont été observées. Cela confirme notre hypothèse selon laquelle la taille des particules reste inchangée pendant l'alliage du Mn. De plus, de plus gros objets de forme irrégulière ont été observés. On peut voir que ces objets sont constitués de plusieurs QD de plus petit diamètre. Sur la base de ces données, nous pouvons conclure que les objets plus gros sont des agrégats formés lors de la préparation des échantillons pour l'analyse MET.
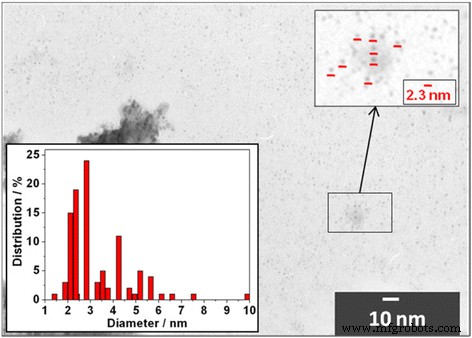
Image TEM de Cd0.91 Mn0,09 QD en alliage de Te. En médaillon :histogramme illustrant le Cd0.91 Mn0,09 Distribution de diamètre QD en alliage de Te
Analyse par spectroscopie d'émission atomique
Il a été démontré précédemment que seulement environ 20 % des Cd 2+ les ions de la solution précurseur participent à la formation des QD CdTe par cette méthode de synthèse [13].
La composition élémentaire du CdTe et la série des Cd1-x Mnx Les QD alliés au Te ont été déterminés par spectroscopie d'émission atomique (AES). La teneur en cadmium et manganèse a été évaluée par le rapport Cd:Mn (mg/l) pour les séries de Cd1-x Mnx QD en alliage de Te avec un contenu différent de Mn 2+ (tableau 1).
Il est intéressant de noter que l'alliage de Mn s'est produit de manière inégale avec l'augmentation de Mn 2+ concentration dans les mélanges réactionnels. On voit clairement que l'addition à environ 1% Mn 2+ ions (par rapport au contenu de Cd 2+ ions dans le mélange réactionnel) à la solution colloïdale fraîchement préparée de nanoclusters de CdTe conduit à la formation de Cd0.96 Mn0,04 QD en alliage de Te. Par contre lorsque la concentration de Mn 2+ ajouté était de 5%, la formation de Cd0.97 Mn0,03 Des QD en alliage de Te ont été observés. Ce désaccord peut suggérer que le procédé d'alliage au Mn est plus efficace en présence d'un excès mineur du composant d'alliage. Un ajout supplémentaire de 10, 15 et 20 % Mn 2+ ions conduit à un alliage cohérent de Mn avec des QD de CdTe.
Caractérisation spectroscopique
Les propriétés optiques du CdTe et du Cd1-x préparés Mnx Les QD alliés au Te ont été étudiés au moyen de spectres d'absorption de la région Vis et de fluorescence. La figure 2 illustre un spectre d'absorption (a) et PL (b) typique de CdTe et une série de Cd1-x Mnx QD en alliage de Te. En fonction du Mn 2+ incorporé en CdTe, nous avons observé un décalage hypsochrome des pics d'absorption vers la plus courte longueur d'onde. De plus, le décalage vers le bleu des pics PL de 542 à 496 nm a été observé. Il existe un certain décalage entre le décalage hypsochrome d'absorption et les pics de PL pour les échantillons 2 (ligne rouge) et 3 (ligne bleue) qui est probablement causé par un alliage irrégulier de Mn.
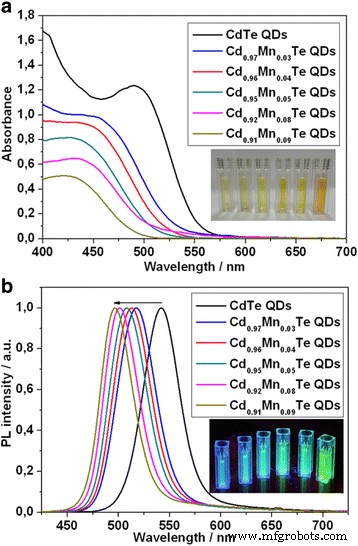
Absorption (a ) spectres de CdTe et séries de Cd1-x Mnx QD en alliage de Te avec un contenu différent de Mn 2+ ions. En médaillon :les images de CdTe et la série de Cd1-x Mnx QD en alliage de Te sous la lumière du jour. PL normalisé (b ) spectres de CdTe et séries de Cd1-x Mnx QD en alliage de Te avec un contenu différent de Mn 2+ ions. En médaillon :les images de CdTe et la série de Cd1-x Mnx Te QDs sous lumière UV
Il est à noter que l'intensité de fluorescence du Cd1-x Mnx Les QD alliés au Te ont diminué avec l'augmentation de Mn 2+ contenu en ions (Fichier supplémentaire 1 :Figure S1). Elle peut s'expliquer par la conjonction partielle de Mn 2+ ions qui ne participent pas au processus d'alliage et présence d'un stabilisant (acide thioglycolique), qui peut éteindre la fluorescence QDs [17].
Caractérisation voltamétrique cyclique
Une méthode de voltamétrie cyclique (CV) a été appliquée pour comprendre les changements de structure de bande résultant de la transformation des QD de CdTe en Cd1-x Mnx QDs alliés au Te en raison de l'augmentation de Mn 2+ contenu.
Sur le CV typique des QD de CdTe colloïdal, nous avons observé (Fig. 3a) des pics cathodiques et anodiques à − 1,00 V (marqué comme C1) et 1,48 V (marqué comme A1), respectivement. La valeur d'énergie de la bande interdite de 2,48 eV, calculée selon la méthode décrite dans [18], s'accorde bien avec la bande interdite optique de 2,50 eV obtenue à partir des pics d'absorption maximaux.
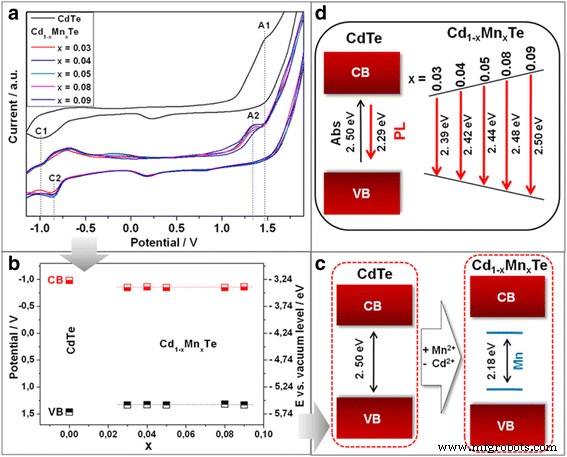
Voltammogrammes cycliques de CdTe colloïdal et séries de Cd1-x Mnx QD alliés au Te avec différents Mn 2+ teneur en ions (a ). Tracé des positions de bord de bande de valence (VB) et de conduction (CB) pour CdTe et la série de Cd1-x Mnx QD alliés au Te, obtenus à partir des positions de pic respectives anodique (A) et cathodique (C) (b ). Schéma de l'électrochimique (c ) et optique (d ) formation du signal
Basé sur les propriétés optiques de Cd1-x Mnx QDs alliés au Te, nous nous attendions à observer une oxydation à des potentiels plus positifs et une réduction à des potentiels plus négatifs pour Cd1-x Mnx QDs alliés au Te, avec augmentation de Mn 2+ contenu en Cd1-x Mnx QDs alliés au Te en raison de l'augmentation de l'énergie de la bande interdite. Cependant, la séparation entre le pic d'oxydation A2 et le pic de réduction C2 est trop petite pour être corrélée à l'énergie de la bande interdite calculée à partir des spectres de photoluminescence. Fait intéressant, la différence de potentiel de 2,18 V entre C2 et A2 est absolument identique pour toute la série de Cd1-x Mnx Échantillons de QD en alliage de Te (Fig. 3a, b).
Comme montré par Beaulac et al., des temps de décroissance excitonique de la PL aussi longs que 5 μs ont été observés pour le Cd1-x colloïdal Mnx Se (x = 0,004 ± 0,002) QD (d ≈ 2,2 nm) à 293 K, qui résultent de l'équilibre thermique entre les états excitoniques du CdSe et l'état excité de champ de ligand à très longue durée de vie du Mn 2+ dopants. Par conséquent, le dopage au Mn n'éteint pas le PL excitonique de Cd1-x Mnx Se QDs. Au lieu de cela, les effets d'auto-extinction de Mn 2+ PL par transfert de contre-énergie thermiquement assisté vers le Cd1-x Mnx Se QDs états excitoniques ont lieu. [4].
On peut supposer que dans le cas du Cd1-x colloïdal Mnx QDs alliés au Te (d ≈ 2,3 nm) à température ambiante, un phénomène très similaire se produit. En utilisant la méthode CV, l'activité électrochimique des niveaux d'énergie "sombres" du manganèse à l'intérieur du Cd1-x Mnx La bande interdite des QDs alliés au Te a été détectée (Fig. 3b, c). Propriétés optiques du Cd1-x Mnx Les QD alliés au Te montrent une augmentation de l'énergie de la bande interdite avec une augmentation de Mn 2+ contenu résultant de phénomènes de transfert d'énergie en retour (Fig. 3d).
Analyse XRD
Fichier 1 supplémentaire :la figure S2 montre les spectres XRD pour le CdTe et les séries de Cd1-x Mnx Échantillons séchés QD alliés au Te qui ont été précipités à partir d'une solution aqueuse à l'aide d'alcool isopropylique.
Le spectre XRD pour le balayage des QDs de CdTe sur la plage des deux thêta de 20 ° à 60 ° montre un pic de diffraction à 25 °, qui est attribué aux plans cristallins (111) de CdTe avec une structure cristalline cubique [19]. Ce pic est significativement plus large que celui des matériaux en vrac en raison de la petite taille des QD avec une distribution de taille étroite. Le signal sur les modèles XRD de toutes les séries de Cd1-x Mnx Les QD en alliage de Te sont décalés vers des angles plus élevés. Le pic à 30°–35° peut être déconvolué en deux pics à 30° et 35°, qui sont affectés aux plans (200) et (220) de Cd1-x Mnx Te alliage. Ces résultats peuvent indiquer la formation de Cd1-x Mnx Te à structure cubique. Ces données XRD confirment que les QD CdTe ont subi avec succès le processus d'alliage de Mn. Notamment, ce pic centré à 25° décroît sur le modèle XRD de Cd0.97 Mn0,03 Tes alliés QDs et disparaissent sur les modèles XRD des échantillons avec un Mn 2+ plus élevé contenu. Dans le cas de Cd0.97 Mn0,03 Dans l'échantillon QDs, nous avons conclu à la formation de core/shell CdTe/Cd1-x Mnx Te QDs où le signal de Cd1-x Mnx La coque filtre le signal du noyau CdTe. Pour tous les échantillons suivants, un large pic de diffraction à 30°–35° peut témoigner de la poursuite de l'alliage de Mn des QD de CdTe et de la formation d'un Cd1-x plus épais. Mnx La coquille. Généralement, cela conduit à la formation de QD avec des teneurs en manganèse plus élevées.
Mesures EPR
Les spectres EPR de Cd0.97 Mn0,03 Les QD alliés au Te sont illustrés à la figure 4. Le spectre se compose de six raies asymétriques qui se superposent au large signal sous-jacent. La présence de six raies dans le spectre est typique pour Mn 2+ ions dans les systèmes désordonnés [2, 20,21,22]. Cependant, la forme du spectre est plus complexe que le trivial Mn 2+ -signal lié. Une analyse détaillée a montré que le spectre EPR expérimental peut être décrit comme une superposition de trois signaux :un large gaussien avec une largeur de raie de 50 mT et deux sextuors avec des raies espacées de 10 et 6 mT, respectivement.
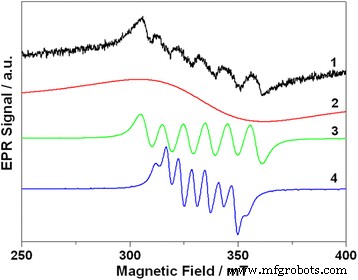
Spectre EPR de Cd0.97 Mn0,03 QDs alliés au Te et sa déconvolution :1-spectre expérimental; 2 :courbe de Gauss avec une largeur de ligne crête à crête de 50 mT. 3-sextuor avec division de ~ 10 mT. 4-sextuor avec division de ~ 6 mT. Détails voir dans le texte
Signal EPR de forme gaussienne centré sur g = 2,0069 (signal 2 ) peut être attribué à Mn 2+ ions interconnectés par interaction dipôle-dipôle. Ces ions sont localisés dans des régions à forte concentration locale de manganèse et interagissent entre eux. En raison de l'élargissement des raies, une forte interaction dipôle-dipôle entre les ions manganèse masque les caractéristiques spectrales spécifiques caractéristiques des ions manganèse isolés et conduit à un signal EPR monoligne. Les deux autres signaux EPR (marqués 3 et 4 ) doit être affecté à Mn 2+ isolé ions. Pour déterminer les paramètres de Mn 2+ isolé ions et son emplacement, le spin-Hamiltonien contenant l'interaction électronique, nucléaire de Zeeman, l'interaction hyperfine et l'interaction du spin de l'électron avec le champ cristallin (terme de division du champ zéro) a été utilisé :
$$ \widehat{H}=g\beta \mathbf{BS}-{g}_{\mathrm{N}}{\beta}_{\mathrm{N}}\mathbf{BI}+A\mathbf{ SI}+\somme \limits_{n,m}{b}_m^m{O}_m^m $$où β et β N désignent respectivement les magnétons de Bohr et nucléaires; B est le champ magnétique externe ; g et g N sont les tenseurs g électroniques et nucléaires, respectivement ; Un est le tenseur de l'interaction hyperfine; S et Je sont les opérateurs de spin de la mécanique quantique électronique et nucléaire, respectivement ; et b n m et O n m sont respectivement les constantes de champ cristallin et les opérateurs de mécanique quantique. Les valeurs de g , g N , β , β N , et А sont supposées isotropes (cela étant caractéristique pour Mn 2+ dans les composés II-VI). L'ensemble de b n m paramètres est déterminé par l'environnement de Mn 2+ et dépend de la symétrie des positions des ions.
Le signal 2 peut être décrit par les paramètres g = 2.0069 et A = − 94,5×10 −4 cm −4 pouvant être affecté au Mn 2+ isolé ions situés dans la position près de la surface des QDs. En même temps, signalez 3 s'est avéré être caractérisé par les paramètres g = 2.0069, A = − 57,5×10 −4 cm −4 et b 4 0 = 27,7×10 −4 cm −4 . Cet ensemble de paramètres est typique pour Mn 2+ en position cationique (MnCd ) de cristaux de CdTe en vrac.
Conclusions
La synthèse de Cd1-x émettant du bleu Mnx Des QD en alliage de Te de petite taille ont été développés. L'étude systématique de leurs propriétés optiques et électrochimiques a été fournie. Le décalage vers le bleu du PL culmine de 542 à 496 nm lors de l'augmentation du Mn 2+ contenu en Cd1-x Mnx Des QD en alliage de Te ont été observés. Les analyses XRD et EPR confirment le remplacement réussi du cadmium par des ions manganèse dans le processus de synthèse. Cd colloïdal1-x Mnx Les QD alliés au Te montrent une augmentation de l'énergie de la bande interdite avec l'augmentation de Mn 2+ contenu à température ambiante en raison du transfert de contre-énergie thermiquement assisté.
Abréviations
- CV :
-
Voltamétrie cyclique
- EPR :
-
Résonance paramagnétique électronique
- PL :
-
Photoluminescence
- QD :
-
Points quantiques
- TEM :
-
Microscopie électronique à transmission
- TGA :
-
Acide thioglycolique
- XRD :
-
Diffraction des rayons X
Nanomatériaux
- Synthèse facile et propriétés optiques de petits nanocristaux et nanotiges de sélénium
- Composite hybride nanostructuré silice/or-cellulose Amino-POSS par procédé Sol-Gel et ses propriétés
- Synthèse de points quantiques de type II/Type-I à suppression de réabsorption ZnSe/CdS/ZnS Core/Shell et leur application pour le dosage immunosorbant
- Synthèse de points quantiques de carbone co-dopés en pyridinique N, S en tant qu'imitateurs d'enzymes efficaces
- L'effet du plasma de contact hors équilibre sur les propriétés structurelles et magnétiques des spinelles Mn Х Fe3 − X О4
- Propriétés de synthèse et de luminescence des nanoparticules hydrosolubles α-NaGdF4/β-NaYF4:Yb,Er Core–Shell
- Synthèse verte de points quantiques InP/ZnS Core/Shell pour une application dans des diodes électroluminescentes sans métaux lourds
- Synthèse de points quantiques de sulfure d'antimoine solubles dans l'eau et de leurs propriétés photoélectriques
- Synthèse sonochimique en une étape facile et propriétés photocatalytiques des composites graphène/Ag3PO4 Quantum Dots



