Comprendre la fabrication du fer dans les études de haut fourneau et de dissection au Japon
Comprendre la fabrication du fer dans les études de haut fourneau et de dissection au Japon
La fabrication du fer dans les hauts fourneaux (BF) est le moyen le plus viable de produire de la métallurgie (HM) principalement en raison de ses performances bien établies et éprouvées, de son utilisation flexible des matières premières et de sa capacité élevée de conservation de l'énergie thermique. Il n'y a pas de dates définitives disponibles pour le lancement de la fabrication du fer BF. Cependant, d'importantes conceptions de processus et une réingénierie ont commencé à être mises en œuvre dans les fours de fabrication du fer en Europe dès le 14ème siècle. Depuis lors, la voie BF a dominé en tant que processus de préférence par rapport aux autres méthodes alternatives de production de fer.
Depuis sa création, le processus de fabrication du fer BF, afin de se maintenir et de rester viable, a subi des développements évolutifs durables pour devenir un processus hautement efficace. Les développements les plus importants à ce jour comprennent (i) la modernisation des installations, (ii) l'augmentation de la productivité du four, (iii) la réduction du taux de coke, (iv) la durée de vie prolongée de la campagne du four et (v) la flexibilité et les améliorations des matériaux. Les progrès technologiques qui ont été réalisés pour améliorer l'économie, l'efficacité et rendre le processus respectueux de l'environnement comprennent (i) diverses pratiques de gestion et de contrôle du processus, (ii) le chargement central du coke, (iii) les opérations à haute pression en haut du four, (iv ) fonctionnement du four avec enrichissement en oxygène (O2), (v) remplacement du coke coûteux par d'autres sources de carbone supplémentaires, à savoir le charbon pulvérisé, le gaz naturel, les huiles et les plastiques, et (vi) bien d'autres. L'évolution technologique du procédé sidérurgique BF l'a conduit d'une petite unité de production, consommant de grandes quantités de combustibles, à son état actuel où les fours conçus pour produire 10 000 tonnes de ML par jour sont assez répandus dans plusieurs pays. Même avec cette augmentation spectaculaire de la taille et de la production du BF, de nombreuses réactions se produisant dans le four ne sont toujours pas connues.
Les BF modernes fonctionnent principalement avec des charges d'aggloméré, de granulés, de minerai de fer fritté/calibré ou d'aggloméré/granulés. Le type et la qualité de ces matériaux dépendent de la philosophie d'exploitation de chaque usine, ainsi les caractéristiques de production et de réduction de ces matériaux sont d'une importance suprême pour le procédé BF.
Le développement du processus BF
Les développements qui ont eu lieu dans le processus BF ont été introduits progressivement, pour finalement devenir des pratiques d'exploitation standard. Il est possible d'énumérer les principaux développements dans un ordre chronologique approximatif consistant en (i) l'utilisation efficace des charges préparées, (ii) les injecteurs de soufflage, (ii) la pression supérieure élevée, (iv) la température de soufflage élevée et (v) un contrôle amélioré. de la répartition des charges. Simultanément à ces développements, il y a eu une augmentation progressive de la taille physique du BF.
Utilisation de fardeaux préparés
La première préparation des matériaux de charge était simplement le dimensionnement des minerais de fer chargés dans le four. Le dimensionnement plus étroit de la charge a amélioré la perméabilité du four, permettant à plus de vent d'être soufflé, augmentant ainsi la sortie du BF. De plus, l'efficacité des réactions de réduction a également augmenté en raison de l'élimination des gros morceaux de minerai, diminuant ainsi le taux de coke.
Le frittage des minerais de fer avant le chargement était la deuxième étape importante de la préparation de la charge, mais le frittage a été développé à l'origine pour transformer des déchets contenant du fer tels que la poussière de combustion BF, la calamine et les fines de minerai en une alimentation BF utilisable. Cependant, ce concept a changé rapidement après le succès obtenu avec le fritté auto-fondant au milieu des années 1950, permettant aux flux d'être retirés de la charge de charge BF et d'être introduits à travers le fritté. Cela a également conduit à la réduction du taux de coke tout en augmentant la productivité du BF. La situation actuelle est que l'aggloméré est maintenant un composant de charge établi dans les usines BF modernes et il fait toujours l'objet d'une enquête continue afin d'améliorer encore ses propriétés.
L'épuisement des minerais de fer de haute qualité facilement disponibles a obligé les fournisseurs à améliorer leur produit au moyen d'un enrichissement suivi de la production de boulettes de minerai de fer de haute qualité à partir du concentré. Ce procédé a été largement accepté, ce qui a entraîné la charge imposée aux fours BF à haute teneur en fer et à faible teneur en gangue, ce qui a entraîné une nouvelle augmentation de la production couplée à une baisse du taux de coke. Une autre amélioration revendiquée avec les granulés a été que la perméabilité de la charge a augmenté en raison du dimensionnement plus étroit. Cependant, l'utilisation de boulettes n'est pas universelle et dans plusieurs pays, les BF fonctionnent principalement avec une charge d'agglomération, les boulettes et/ou le minerai de fer calibré contribuant à une petite proportion de la charge globale. En effet, certains pensent qu'un taux de frittage élevé est essentiel pour le fonctionnement stable des grands BF car le fritté a une température élevée supérieure et de meilleures propriétés de distribution, car les pastilles roulent facilement, ce qui rend difficile le contrôle de la distribution. En raison également de l'utilisation d'aggloméré dans le BF, le poussier de coke généré à l'usine de four à coke est consommé dans l'aciérie.
Injectants de souffle
Il y a trois injecteurs qui sont normalement utilisés dans le BF. Ce sont (i) la vapeur, (ii) l'O2 et (iii) les combustibles auxiliaires. Les injecteurs affectent la température de la flamme, c'est-à-dire la température de la flamme dans la zone de combustion de la tuyère. La vapeur et le combustible auxiliaire abaissent la température de la flamme tandis que l'O2 l'augmente. La température théorique de la flamme peut être calculée et elle est extrêmement importante pour maintenir un fonctionnement en douceur et augmenter la productivité avec de grandes quantités d'O2 et de combustible auxiliaire. Une température de flamme basse empêche la réaction dans le four et conduit au refroidissement du four. Une température de flamme élevée peut endommager la perméabilité en raison de l'expansion de la zone de fusion et de l'évaporation des alcalis et de la silice (SiO2) dans la charge. Afin d'assurer un bon fonctionnement, il est nécessaire de contrôler la température théorique de la flamme en faisant varier les quantités d'injectants.
En regardant les trois injectants séparément, la vapeur réagit avec le coke pour produire de l'hydrogène (H2) qui augmente l'ampleur de la réduction des matériaux de charge, diminuant ainsi le taux de combustible. Les carburants auxiliaires sont les principaux injecteurs. Le type de combustible auxiliaire utilisé dépend des conditions locales. L'injection de combustible auxiliaire fournit des quantités supplémentaires de H2 et de monoxyde de carbone (CO) dans le BF, augmentant le degré de réduction de la charge, ce qui à son tour entraîne une diminution du taux de coke. Il est essentiel d'assurer une combustion complète du combustible auxiliaire au niveau de la tuyère car une combustion incomplète peut altérer la perméabilité du four, provoquant des effets néfastes sur le fonctionnement du four. Une combustion insuffisante peut être contrôlée en fournissant un excès suffisant d'O2 dans le souffle.
L'injection d'oxygène augmente la quantité d'O2 en excès et augmente la température de la flamme, ce qui compense la baisse de température de la flamme provoquée par l'injection de vapeur et de combustible auxiliaire. Il est également utile pour diminuer la quantité de gaz bosh, minimisant ainsi l'étendue de la canalisation du gaz dans le BF et l'étendue de l'inondation et du chargement. L'inondation provoque un fonctionnement irrégulier du four. Le chargement est la situation dans laquelle le laitier fondu est empêché de descendre en raison de la vitesse ascendante du gaz. A terme le poids du laitier doit devenir suffisant pour vaincre le flux de gaz pour qu'il descende. Lorsque le rapport d'O2 dans le vent est progressivement augmenté, le volume de gaz produit par tonne de HM diminue, entraînant une baisse de la quantité de transfert de chaleur des gaz vers les solides dans le puits, entraînant une diminution de la température de l'arbre. De plus, l'augmentation de la productivité grâce à l'enrichissement en O2 accélère le taux de descente de la charge, ce qui réduit le temps de transfert de chaleur. En conséquence, les matériaux de la charge pénètrent dans la zone à haute température sans être suffisamment préchauffés, refroidissant ainsi le four et provoquant le glissement et la suspension de la charge.
La pratique de l'utilisation d'injectants nécessite un contrôle minutieux en ce qui concerne trois limites à savoir (i) la limite du transfert de chaleur entre les gaz et les solides, (ii) la limite de la température théorique de la flamme et (iii) la limite de la combustion complète du combustible auxiliaire. Le contrôle à l'intérieur de ces limites permet d'obtenir de faibles taux de carburant et une productivité élevée.
Pression supérieure élevée
L'avantage de la pression supérieure élevée est qu'elle réduit la vitesse du gaz dans le four, laissant ainsi plus de temps pour la réduction gazeuse, ce qui entraîne une diminution du débit de combustible. Les pertes de poussière diminuent également parce que la vitesse inférieure du gaz est insuffisante pour transporter les particules de poussière plus grossières. Alternativement, plus de vent peut être soufflé et ainsi la production peut être augmentée tout en maintenant la même vitesse de gaz dans le four, empêchant ainsi la canalisation, l'inondation et le chargement. Le principal inconvénient est que pour s'adapter à l'augmentation de la pression de gaz, une construction robuste est nécessaire dans tous les équipements BF des poêles, à travers les tuyaux d'agitation, les parois du four, le dessus du four et l'usine de nettoyage des gaz, etc., ce qui est évidemment coûteux. Il est certain que le dessus BF seul nécessite une conception spéciale afin d'égaliser la pression du gaz dans le système de charge et d'empêcher l'usure de l'équipement de charge du haut du four. Un autre inconvénient est la perte d'énergie dans les gaz de gueulard à haute pression, bien que la turbine de récupération des gaz de gueulard puisse récupérer une partie de cette énergie.
Bien qu'il y ait des problèmes avec l'application d'une pression supérieure élevée d'un point de vue technique, le fonctionnement de grands hauts fourneaux nécessite son utilisation pour (i) réduire le taux de combustible et (ii) permettre une productivité plus élevée du four.
Température de soufflage élevée
L'air entrant dans le BF par les tuyères est chauffé par la combustion du coke et, par conséquent, plus l'air entrant est chaud, moins le coke est consommé lors d'un chauffage supplémentaire à l'intérieur de la région des tuyères. Le préchauffage de l'air n'est pas une nouveauté. En effet, il y a plus d'un siècle, les poêles BF existaient. Cependant, ce n'est que relativement récemment que des températures supérieures à 1300°C ont été atteintes. L'obtention de températures plus élevées est due à des modifications de la conception du poêle. Ces modifications sont (i) l'augmentation de la surface de surface chauffée du damier par modification de la forme des briques, (ii) l'utilisation d'un réfractaire de meilleure qualité capable de résister à des températures plus élevées, et (iii) la fourniture de chambres de combustion externes qui augmente la surface chauffée.
Améliorations dans la répartition des charges
Le contrôle de la distribution des matériaux de charge est important pour améliorer l'utilisation du gaz et abaisser le taux de carburant. Une distribution correcte est également nécessaire pour contrôler la forme de la zone cohésive du BF, maximisant ainsi la production et minimisant le flux de gaz à la paroi du BF, ce dernier prolongeant la durée de vie du four.
Au fur et à mesure que la taille du four augmente, la distribution du matériau de charge nécessaire pour fournir une distribution de gaz stable à l'intérieur du BF ne peut pas être maintenue avec un équipement de charge conventionnel en raison des différences d'angle de compilation, de densité et de forme. Ces problèmes ont été partiellement surmontés par l'installation d'un blindage mobile pour contrôler la distribution du matériau à la sortie de la cloche de chargement. Le développement des systèmes de chargement sans cloche et Gimble top, qui sont dotés d'une goulotte rotative capable de distribuer avec précision la charge à n'importe quelle position sur la ligne de stockage du four, a dans une large mesure aidé à résoudre le problème.
Frite de minerai de fer
Dans de nombreux BF, l'agglomération est le principal composant des charges de BF. La composition chimique de l'aggloméré dépend des autres composants constituant la charge du four. Normalement, le fritté varie de fluxé (CaO/SiO2 autour de 1,2) à superfluxé (CaO/SiO2 autour de 1,7 à 2,2). L'aggloméré fluxé est généralement utilisé lorsque la majorité de la charge du four est de l'aggloméré. Un fritté superflux est utilisé lorsque le reste de la charge est de nature acide, équilibrant ainsi la chimie du laitier pour fournir une composition de laitier acceptable. Le frittage est extrêmement hétérogène en raison de la nature du processus de frittage.
Structure du fritté – Les fondants, qui sont mélangés au minerai de fer, réagissent lors du frittage, fondent et attaquent les particules de minerai. Une agglomération complète de petites particules de minerai peut se produire, mais généralement les plus grosses particules ne subissent qu'une attaque de surface. Pendant le refroidissement, la précipitation de différentes phases se produit dans la matrice de laitier, le résultat global étant un mélange de phases qui sont très éloignées d'un état d'équilibre et un matériau hétérogène dont les phases dépendent de la ségrégation des composants dans le mélange initial, par ex. là où des particules de chaux existaient avant le frittage, une région riche en chaux se forme. Globalement les phases présentes dépendent de la quantité de fondants ajoutés. L'aggloméré auto-fondant est principalement constitué d'hématite et de magnétite avec de petites quantités de ferrites de calcium, produites par une réaction entre le minerai de fer et la chaux. Ici, le terme «ferrites» fait référence aux quantités combinées des différentes espèces de ferrites qui peuvent être produites, en fonction de la basicité et des particules de minerai dans la zone de réaction. Plus la basicité augmente, plus la proportion de ferrites augmente.
Dans le frittage, normalement, les ferrites sont contaminées par SiO2 et Al2O3 (alumine) et le produit est connu sous le nom de SFCA (silico-ferrite de calcium et d'alumine). Le SFCA se conformait normalement à une formule générale 'n1(Fe2O3).n2(SiO2).n3(Al2O3).5CaO', où la somme de n1,n2 et n3 est d'environ 12. La teneur en calcium est assez constante à environ 15 %. En pratique, généralement dans les frittés, les ferrites se trouvent généralement sont 7 Fe2O3.2SiO2.3AI2O3.5CaO et 9Fe2O3.2SiO2.0.5AI2O3.5CaO.
Réduction de l'agglomération – Le type et la quantité de ferrites présentes dans le fritté jouent un rôle important dans les propriétés de réduction. Les réductibilités des ferrites ne sont pas constantes, mais varient d'une espèce à l'autre. On voit que la proportion de ferrites augmente à mesure que la basicité du fritté augmente. Cependant, la réductibilité ne suit pas la même tendance. Entre les gammes de basicité de 1,0 à 1,5, la réductibilité augmente du fait de l'augmentation des ferrites de type CaO.2Fe2O3 et CaO.FeO.Fe203. A un domaine de basicité de 1,4 à 1,5 la réductibilité diminue du fait d'une baisse de la proportion d'hématite présente dans les agglomérés et de la disparition de CaO.2Fe203 couplée à l'apparition du 2CaO.Fe2O3 peu réductible. L'augmentation de la basicité au-delà de 1,5 montre à nouveau une tendance à la hausse due à l'apparition de CaO.Fe2O3 et CaO.FeO.Fe2O3.
Le comportement de réduction des ferrites est complexe en ce qu'ils doivent se décomposer pour que la réduction de l'oxyde de fer se produise. Au cours du processus de réduction, les oxydes de fer supérieurs et les ferrites, riches en oxyde de fer, sont d'abord réduits jusqu'à ce qu'il ne reste plus que de la ferrite dicalcique et de la wustite. Le gaz attaque alors la ferrite dicalcique selon la réaction réversible 2CaO.Fe2O3 + 3H2 =2CaO + 2Fe + 3H2O. Le CaO libéré réagit alors immédiatement avec la wustite selon la réaction réversible 2CaO + 3FeO =2CaO.Fe2O3 + Fe. La réaction se déroule ensuite selon l'équation précédente et ainsi de suite. Cependant, les micro-photographies montrent que la wustite n'est pas présente à la frontière gazeuse et qu'un processus de diffusion entre les deux réactions doit donc avoir lieu. Des études ont indiqué qu'à la surface de l'oxyde, la ferrite dicalcique est d'abord réduite. Le fer libéré se sépare dans la phase oxyde et le calcium se diffuse et réagit avec la wustite et à nouveau le fer se sépare ou se diffuse dans le Fe3O4.
Boules de minerai de fer
Au cours du processus de production de boulettes de minerai de fer, le minerai de fer est enrichi en écrasant et en éliminant le matériau de gangue libéré. Généralement, du quartz est ajouté dans la production de pastilles acides pour améliorer les propriétés des pastilles. La majorité des granulés produits sont de type acide, c'est-à-dire sans aucun ajout substantiel intentionnel de fondant. Lors de la production de pastilles acides, les pastilles vertes sont cuites à environ 1300°C dans une atmosphère oxydante. Cela favorise la liaison des particules par (i) le frittage des grains d'hématite, (ii) l'oxydation et le frittage subséquent des grains de magnétite, et (iii) la liaison du laitier. Ce dernier est causé par la fusion des petites traces de gangue et de la bentonite, utilisée dans le processus de granulation pour assurer une résistance suffisante des granulés verts. Cette phase de laitier est constituée essentiellement de chaux, de silice, d'oxyde de fer et de petites traces d'alcalis, de magnésie, d'alumine, etc.
Une indication de la composition chimique de la phase laitier peut être obtenue en se référant au diagramme de phase CaO-SiO2-Fe2O3. Un point à noter est que les diagrammes d'équilibre doivent être utilisés avec précaution car dans la majorité des processus, les réactions sont rarement à l'équilibre, néanmoins, ces diagrammes sont des outils utiles. Très peu de réaction, le cas échéant, se produit entre les grains de quartz et l'hématite pendant la cuisson et donc les pastilles acides sont composées d'hématite, de quartz, d'une phase de laitier et, dans certains cas, si une cuisson suffisante n'a pas eu lieu, de magnétite, provenant de n'importe quel minerais de magnétite dans le mélange de granulés.
Les pastilles d'acide sont utilisées dans certains BF dans la charge du four. La quantité utilisée dans la charge dépend de la pratique d'exploitation adoptée. Dans le cas de BF fonctionnant entièrement sur des pastilles d'acide comme source d'unités de fer, le flux (calcaire et dolomie) nécessaire au processus de formation de laitier est chargé dans le BF en tant que charge.
granulés fluxés – Actuellement, l'utilisation de granulés fluxés est préférée. Dans les pastilles fluxées, les fondants sont incorporés dans la pastille, évitant ainsi la nécessité de les charger séparément dans le four. Les granulés fluxés peuvent être produits avec des ajouts de chaux, comme fondant, ou de dolomie. Au fur et à mesure que la basicité des granulés augmente avec l'ajout du fondant, une modification de la microstructure se produit. En ce qui concerne les granulés à la chaux, l'ajout de chaux a une influence sur la composition et la quantité de laitier, ainsi que sur la quantité d'hématite. L'ajout de chaux crée la possibilité d'une réaction entre l'hématite et la chaux pour produire des ferrites de calcium CaO.Fe2O3 ou 2CaO.Fe2O3 selon la concentration en chaux. Avec les pellets fluxés, la température de cuisson est inférieure à celle des pellets acides pour éviter la formation de scories excessives.
Dans le cas de pastilles fluxées, on s'attend à trouver des grains d'hématite entourés de ferrites de calcium provoqués par la réaction chimique de la chaux. Dans certains cas, le grain d'hématite d'origine peut être entièrement converti en ferrites de calcium, ce qui dépend clairement de la taille du grain d'hématite d'origine. L'effet de la chaux sur la phase laitier est double. Premièrement, il y a une augmentation générale de la quantité de laitier et deuxièmement un changement de basicité. La composition exacte dépend naturellement de la quantité de phases réagissant, mais les possibilités peuvent être supposées à partir du diagramme de phase CaO-Fe2O3-SiO2. L'un des problèmes avec les granulés fluxés est leurs propriétés de réduction relativement médiocres. Cette lacune des pellets fondus à la chaux a conduit à la production de pellets fluxés avec de la dolomite, au lieu de la chaux.
L'ajout de magnésie à l'oxyde de fer entraîne une réaction à l'état solide entre les deux et une augmentation de la température de fusion. Ainsi, dans les pastilles fluxées de dolomite, des magnésio-ferrites MgO.Fe2O3 ou (Mg.Fe)O.Fe2O3 sont produites. Le quartz ne peut pas être entièrement absorbé dans les pastilles de dolomite car la fusion entre la magnésie et la silice ne se produit pas à la température de cuisson et seules les réactions qui se produisent à l'état solide peuvent avoir lieu.
Les mécanismes de réduction associés aux pastilles acides peuvent être expliqués par la réduction gazeuse, la cinétique de réaction et la réduction directe. En cas de réduction gazeuse, lorsque l'O2 est éliminé de l'oxyde de fer, les pastilles d'acide suivent un chemin de réduction de l'hématite à la magnétite à la wustite (à des températures supérieures à 560 deg C) au fer métallique. Ces changements de phase sont représentés par les réactions gazeuses réversibles, utilisant le CO comme agent réducteur. Les équations sont 3Fe2O3 + CO =2Fe3O4 + CO2, Fe3O4 + CO =3FeO + CO2, Fe3O4 + 4CO =3Fe + 4CO2 et FeO + CO =Fe + CO2.
Le mécanisme de la réduction de l'hématite a été largement étudié et il a été noté que la réduction de l'hématite ne se produit pas par étapes discrètes, c'est-à-dire en magnétite, puis en wustite, etc., mais la réduction produit une structure chimique de haut en bas, à condition que la réduction potentiel du gaz est suffisamment élevé, c'est-à-dire que la structure est constituée d'une particule d'hématite, entourée d'une couche de magnétite, puis de wustite et enfin d'une couche externe de fer métallique. La wustite est non stoechiométrique, c'est-à-dire qu'elle est déficiente en ions de fer. Ces lacunes sont les défauts importants dans le comportement de réduction des oxydes de fer car elles rendent possible la diffusion du fer à travers le réseau d'oxyde de fer. L'élimination de l'O2 de la wustite produit un remplissage des lacunes en ions de fer à la surface de l'oxyde.
La réduction de surface déclenche une diffusion de lacunes et de défauts électroniques de l'intérieur de l'oxyde vers l'interface réactionnelle. Avec la réduction de la wustite, le flux entrant d'ions métalliques réagit avec la couche de magnétite, réduisant ainsi la magnétite. La réaction a alors lieu et le cycle se répète en réduisant progressivement la magnétite.
La cinétique de la réduction des oxydes de fer a été largement étudiée mais il existe des points de vue contradictoires en ce qui concerne l'étape de contrôle de la vitesse. Le processus de réduction gazeuse des oxydes de fer nécessite de nombreuses étapes telles que (i) la diffusion du gaz réactif de la phase gazeuse en vrac à travers la couche limite, (ii) la diffusion du gaz à travers la couche de produit jusqu'à l'interface de réaction, (iii) adsorption du gaz sur l'interface de réaction, (iv) réaction chimique à l'interface, (v) désorption du produit gazeux de l'interface de réaction, (vi) diffusion des produits de réaction gazeux de l'interface de réaction vers la surface des particules, et (vii) la diffusion du produit gazeux à travers la couche limite dans la phase gazeuse en vrac.
Bien qu'il existe un grand conflit quant à l'étape ou aux étapes de limitation de vitesse, généralement la réduction des oxydes de fer est conforme à l'équation dérivée de McKewan K1 =Kw/do =ro[1 – (1- R1/3)]/t où K1 est la vitesse d'avance de l'interface hématite/magnétite en mm/minute, Kw est la constante de vitesse en g / mm² / minute, do =densité de la sphère d'oxyde de fer pur en g/mm3, ro est le rayon de la sphère d'oxyde de fer en mm, R est la conversion fractionnée de l'hématite en magnétite et t est le temps de réaction en minutes. On prétend que, comme le taux de réduction des oxydes de fer est conforme à cette équation, l'étape limitant le taux est la réaction chimique.
Hills a utilisé les principes du transport de masse pour montrer qu'une réaction contrôlée par le transfert de masse et la diffusion seuls peut avoir les caractéristiques spécifiques fréquemment utilisées pour identifier une réaction chimiquement contrôlée, en particulier la linéarité de [1 – (1 – R)1/3)] avec le temps . Hills a postulé que la réaction est contrôlée à la fois par les processus (i) de diffusion de gaz à travers la couche de produit et (ii) de transport à travers la couche limite externe à la particule. Une forme d'équation de taux de Hills peut être exprimée comme 3[1 - (1 - R)2/3]- 2R(1- Bm) =C2.t où R est la réduction fractionnaire, t est le temps de réduction en secondes, Bm =DE/Kg.ro, Bm est le module de transfert de masse, c'est-à-dire le rapport entre la résistance de diffusion dans la couche de produit et la résistance de transfert de masse à l'extérieur de la particule, DE est le coefficient de diffusion dans la couche de produit en mm²/sec, Kg est le coefficient de transfert de masse à la surface de la sphère de réaction en mm/sec et ro est le rayon de la sphère en mm. C2 est une constante pour une réaction de réduction et dépend des propriétés de la sphère d'oxyde de fer et des conditions environnementales.
Dans le cas d'une réduction à des températures de 800 °C et plus, une augmentation de la température de réduction gazeuse entraîne une augmentation de la vitesse de réaction, à condition que la fusion des particules ne se produise pas. Une augmentation de la porosité produit également une augmentation du taux de réduction.
Le mécanisme de réduction directe des oxydes de fer avec du carbone (C) est extrêmement important dans le BF et il a été constaté que la réduction directe ne se produit qu'en quantités appréciables à des températures supérieures à 900 ° C. La réaction de réduction directe peut en fait être divisée en équations FexOy + C =FexO(y-1) + CO. La réduction par le gaz est CO + FexOy =FexO(y-1) + CO2. Dans ces réactions x =1, 2 ou 3 et y =1, 3 ou 4. La réaction de perte de solution (Boudouard) CO2 + C =2CO fournit du CO pour la réaction gazeuse. Étant donné que la réaction de réduction directe se produit en fait via une réaction de réduction indirecte, cela indique que la réduction directe des oxydes solides dans le procédé BF n'a aucune importance en ce qui concerne l'avancement de la réaction.
La situation des oxydes de fer liquides réagissant avec C est bien sûr assez différente en ce que la zone de contact entre l'oxyde liquide et le solide C est beaucoup plus grande que celle de l'oxyde solide et du solide C. De plus, la diffusion des espèces réagissantes et des produits dans le liquide est beaucoup plus rapide qu'à l'état solide. Ces effets conduisent à des vitesses de réaction beaucoup plus élevées dans les systèmes oxyde liquide/C solide que dans les systèmes oxyde solide/C solide. Plus la température de réaction est élevée, plus le degré de réduction est élevé. Il a été trouvé que l'étape de limitation de vitesse pour la réduction des scories riches en FeO change avec l'étendue de la réduction. La nucléation du fer réduit et la réaction chimique à l'interface C/liquide semblent constituer l'étape limitant la vitesse jusqu'à ce qu'un degré élevé de réduction soit atteint. À des niveaux de réduction plus élevés, l'étape la plus lente est la diffusion de l'O2 à travers la couche limite du laitier.
Influence de l'alcali sur la réduction
L'alcali recircule à l'intérieur du BF par vaporisation dans la zone à haute température et dépôt ultérieur sur la charge et le coke dans les régions plus froides. L'alcali déposé descend ensuite avec la charge et le coke pour être finalement vaporisé. La nature de cet effet de recirculation est telle que des niveaux assez élevés d'alcali peuvent s'accumuler à l'intérieur du BF, ce qui peut influencer la réduction de la charge de matériaux. Les ajouts d'alcali augmentent le taux de réduction des granulés acides et basiques. Il a été remarqué qu'il existe un niveau optimal d'ajouts d'alcali, au-dessus duquel le taux de réduction est diminué en raison de la formation importante de laitier. De plus, les granulés de dolomite fluxés présentent une diminution du taux de réduction lorsqu'il y a des vapeurs alcalines dans le gaz réducteur. De plus, le type de type alcalin est important, c'est-à-dire que l'hydroxyde de sodium (NaOH) est un meilleur promoteur de la réaction de réduction que le chlorure de sodium (NaCl) pour la même concentration du cation sodium.
L'augmentation du taux de réduction qui se produit lorsqu'un alcali est ajouté à l'oxyde de fer est provoquée par le gonflement accru exposant une plus grande surface au gaz réducteur. De plus, l'alcali provoque une réduction chimique non liée à la surface, ce qui signifie que la surface de la wustite est continuellement exposée au gaz réducteur au lieu d'être protégée par une couche de fer métallique. La réduction chimique non liée à la surface est causée par l'incorporation de cations alcalins dans le réseau wustite qui provoque une homogénéisation de l'activité wustite, modifiant le comportement de nucléation du fer, conduisant ainsi à une réduction chimique non liée à la surface. Le gonflement des pellets semble généralement considéré comme un symptôme d'une teneur excessive en alcalins.
Comportement de la charge dans le BF
Au cours de la durée de vie du procédé BF, une richesse considérable de connaissances sur les caractéristiques de réduction des oxydes de fer, des pastilles et des frittés a été accumulée, jusqu'à des températures de réaction d'environ 1 000 °C. À des températures supérieures, on sait très peu de choses sur les réactions qui se produisent ou leur effet sur les propriétés des matériaux de charge BF. Même avec la grande quantité d'informations disponibles sur le comportement des matériaux de charge à des températures allant jusqu'à 1000 ° C, il n'est pas facile de l'appliquer pour la simple raison que l'examen interne du BF pendant le fonctionnement est extrêmement difficile. Les principaux « outils » pour obtenir des échantillons à partir de BF en fonctionnement sont les sondes de gaz, les sondes de température et les sondes de charge, etc., bien que leur couverture utile ne soit qu'un très petit volume de BF.
Il est juste de dire, cependant, que les corrélations entre le comportement du matériau pendant la réduction et le processus BF ont été raisonnablement établies. A titre d'exemple, on sait que les matériaux qui présentent un degré élevé de dégradation de la taille physique pendant la réduction à basse température provoquent une diminution de la perméabilité du four dans la pratique et que les matériaux de charge hautement réductibles diminuent le taux de combustible. De plus, les pellets qui gonflent fortement pendant la réduction entraînent une perte de perméabilité du four.
Études de dissection
Une avancée majeure concernant le comportement des matériaux au sein du BF est intervenue avec la trempe à l'eau de plusieurs fours en fonctionnement et la dissection et l'étude méthodique de leur contenu. La répartition de la charge à l'intérieur du BF dépend de la séquence de charge, des poids de charge, des composants de la charge et du fonctionnement du four et entraîne le fonctionnement de chaque four d'une manière différente. La figure 1 montre la structure interne du Kukioka BF n°4. Les couches de minerai et de coke sont maintenues jusqu'à ce que la zone d'adoucissement-fusion ou zone cohésive soit atteinte. Le début de la zone cohésive pendant la procédure de dissection a été assuré par la résistance physique accrue à l'enlèvement du matériau par les moyens mécaniques. La zone cohésive est l'endroit où les matériaux commencent à se ramollir et finissent par fondre. La découverte que la zone cohésive n'est pas dans une région du four, mais est distribuée dans une forme raisonnablement géométrique a été l'une des principales informations sur les réactions se produisant dans le BF pendant son fonctionnement.
Il a été constaté que la structure de la zone cohésive variait en fonction du fonctionnement du four. A titre d'exemple, la figure 1 montre également les structures trouvées dans trois fours différents. Hirohata BF non. 1 montre les couches ramollies ayant une forme de « beignet » disposées dans une structure en « V » inversé, tandis que Kukioka BF n° 4 a une zone cohésive en forme de « W ». Higashida BF n°5 révèle un « V » inversé déformé causé par un fonctionnement irrégulier du four avant l'opération de trempe.
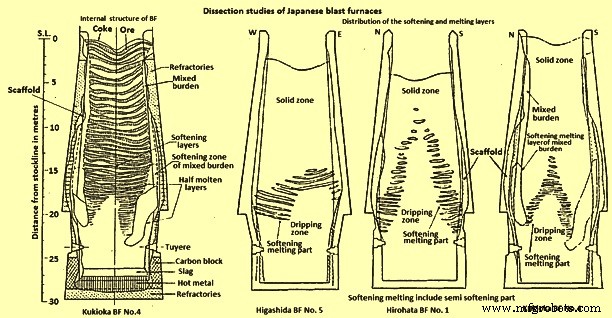
Fig 1 Études de dissection de hauts fourneaux japonais
Niveaux de réduction – L'étude de l'étendue de la réduction de chaque couche de charge de Hirohata BF no. 1 et Kukioka BF n°4 a fait ressortir des fonctionnalités intéressantes. One of the interesting features is the fact that very little reduction occurs until the burden reaches the cohesive zone, wherein reduction proceeds rapidly. One of the major problems with water quenching is the possible reoxidation of the burden material during the cooling period and laboratory tests were conducted to determine the extent of reoxidation which might be taking place. One study was made to measure the reoxidation of sinter, in the laboratory, under the same cooling conditions existing during quenching of a BF, using a series of different initial reduction levels. The another study used another technique employing burden materials of various reduction degrees cooled from three different temperatures (400 deg C, 800 deg C and 1000 deg C) at a cooling rate of 200 deg C per hour in a nitrogen (N2) atmosphere. In this study it has been found that although the reduction temperatures and reduction degrees were different, the final reoxidation degree was around constant at 20 % to 25 %, i.e. the reoxidation increased in proportion to the initial reduction degree. At temperatures below 300 deg C, no reoxidation occurred. The result of these experiments is that the reduction levels were required to be increased, for example, from 10 % to 30 % to 15 % to 40 %. These corrected levels were in agreement with the reduction levels found in Russian dissection studies on a N2 quenched furnace.
Temperature profiles – The temperature isotherms within the furnaces were estimated by a combination of several methods. In one method, ‘Tempil’ pellets encased in numerous graphite holders were charged prior to blowing out the furnaces. This technique allowed the estimation of the temperature within the range 200 deg C to 1800 deg C, but one of the problems with this technique was that there was no method of controlling the distribution of the graphite holders within the BF. The other methods employed were measurement of the extent of coke graphitization, thus estimating the temperature between 1200 deg C and 1700 deg C. Measurement of the coke electrical resistance, which allowed temperature estimation between 1100 deg C and 1700 deg C and finally the degree of iron ore fusion was measured to estimate temperatures within the range of 900 deg C to 1400 deg C.
Comparing the isotherms with the distribution of the softening-melting burden layers (Fig 1 and Fig 2), it was found that the cohesive zone exists over a temperature range of around 1100 deg C to 1500 deg C for BFs operating mainly on sinter burdens.
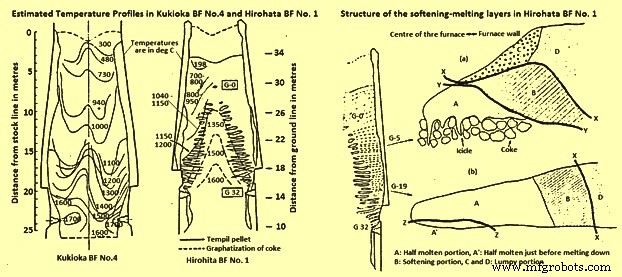
Fig 2 Estimated temperature profiles in Kukioka BF no. 4 and Hirohata BF no. 1 and structural of the softening-melting layers in Hirohata BF no. 1.
Burden layer structure within the cohesive zone – The type of structure of an individual burden layer in the cohesive zone depends upon the position of the layer within the BF. Two layers from Hirohato BF no.1 are shown in Fig 2. Layer G-5 is near the apex of the cohesive zone, while layer G-19 is situated near the base of the cohesive zone. Layer G-5 has four distinct zones, two of which are lumpy or granular portions (C and D). Layer G-19, on the other hand, contains only one lumpy portion, D. Apart from the obvious shape differences between the layers, the other main difference is the replacement of the icicles’ in layer G-5 by a half-molten portion just prior to melting down, A in layer G-19.
As seen earlier a substantial amount of reduction takes place in the cohesive zone and this has been proved by the reduction data obtained for each portion as given in Tab 1, and Tab 2. The figures are on the low side, as reoxidation, caused by the act of water quenching, certainly have taken place. The reason for the high reduction level of portion C is attributed to the slightly lower reduction temperature while in contact with the coke.
| Tab 1 Degree of reduction of the burden materials in the softening-melting layers of Hirohata BF no. 1 | ||||
| Softening-melting layer | Portion* | Reduction degree % | ||
| Sinter | Ore lump | Pellet | ||
| G-5 | A | 65.6 | 65 | 79.3 |
| C | 72.8 | 68.2 | 81.2 | |
| D | 11.5 | 12.3 | 14.6 | |
| G 19 | D | 35.4 | 36.6 | 41.3 |
| * B:Softening portion, C and D:Lumpy portion | ||||
| Tab 2 Degree of reduction of the pellets in the lumpy portion | ||
| Softening-melting layer | Sampling position (distance from the boundary*) (m) | Mean value of the reduction of the sample pellets (%) |
| G3 | 2 | 12.7 |
| 0.2-around 0.3 | 23.1 | |
| G10 | 1 | 14.1 |
| 0.2-around 0.3 | (55)** | |
| G12 | 1.3 | 13.9 |
| 0.9 | 14.3 | |
| 0.5 | 12.3 | |
| * Between the lumpy and softening portions | ||
| ** The value of the reduced pellet being not reoxidized | ||
The thickness of the softening-melting layers in Hirohata BF no. 1 ranged from 400 mm to 500 mm, in the case of the upper layers, to 70 mm – 100 mm for the layers near the base of the cohesive zone. The diminishing thickness is due to compaction, caused by the pressure exerted by the weight of material above the layer and also because of a natural thinning of material due to the increase in furnace diameter as the material descends. In the softening portions iron ore granules were combined in contact with each other. Sinter particles in the layers deformed very little, unlike pellets, which showed signs of deformation.
The process of pellet metallization can take place in one of three modes namely (i) the metallic iron is uniformly distributed within a pellet, (ii) a metallic shell is formed, leaving a wustite core, and (iii) wustite within the pellet reacts to form a slag and moves towards the metallic iron shell, leaving a central cavity. The reason for these three possible modes is not connected with the distribution within the softening-melting layer, but can be due to differences between the pellets or uneven gas flow in the softening-melting layer.
It has been found that the half molten portion consisted of highly compacted metallic iron and a small quantity of slag. Any limestone or olivine present remained unslagged. The icicles extend into the coke voids and consist of a metallic shell with a hollow interior, with small droplets of slag adhering to the iron. The higher the softening-melting layer within the furnace, the greater the length of the icicles, e.g. level G-1 produced some icicles of several hundreds of millimeters in length, while the lower layers produced icicles only 10 to 20 millimeters long.
The structure of the softening-melting layers in Kukioka BF no.4 was basically identical to those described for Hirohata BF no.1, except the thinner burden layers made the structure less distinct and the icicles smaller.
Slag composition changes – The major chemical change of the slag phase in the softening-melting layers is a decrease in the FeO content as the slag trickles down from the melting portion. Although large differences were detected by x-ray microanalyses of slags in portion A, ranging from 2 % to 20 % FeO, depending upon the location, the FeO content of the slag immediately prior to separation from the softening-melting layer was only 2 % to 3 %. The type of slag was not significantly different to that found in the normal sinter product, but in the ore granules a considerable quantity of fayalite was produced. Descent of the slag results in a gradual change in composition. The gradual increase in the CaO/SiO2 ratio is attributed to fluxing with limestone and a drop in the SiO2 content, caused by SiO2 reduction. The rise in Al2O3 is created by the incorporation of coke ash into the descending slag.
Metal composition changes – Considering the changes in metal composition as it descends the furnace; the carbon content of the metal in the half-molten portion of the softening-melting layer is around 0.2 % in the upper part and 0.35 % to 0.57 % in the lower part. The source of C in these half-molten layers is attributed to the carburizing action of the CO, except for the metal in contact with coke. Similar trends are visible in the layers found in Kukioka BF no.4. The rise in the C content of the icicles is attributed to the metal being in direct contact with particles of coke. Two distinct processes have been identified which are operating for the separation of metallic iron from the layers. The first mechanism is via the icicles which form at 1350 deg C to 1400 deg C and drip into the coke bed. Reduction of the iron oxides present in the icicles occurs rapidly to produce metallic iron. The second process occurs in layers in which no icicles form. In this situation, the metallic iron is carburized by the underlying coke until it reaches a C level such that melting can occur at the pertaining temperature. In this case the temperature of meltdown is around 1500 deg C.
The question of the mechanism of silicon pick-up by the metal within the furnace has been the subject of considerable discussion. Studies carried out in the experimental BF at Liege, Belgium fitted with sampling probes have found that the silicon level rise gradually from the melting zone to the hearth, such that 75 % of the final HM silicon is achieved by the time the metal reached the tuyere level. The Japanese dissection studies on the other hand reveal that the silicon level of the metal at the tuyere level is far in excess of that of the tapped HM. An explanation for this discrepancy between the two groups of studies can be that silicon pick-up had occurred during the process of water quenching the Japanese furnaces. During the experiments conducted to determine the probability of silicon pick-up during quenching, it was found that silicon pick-up from any slag present could be a possibility. Hence, this is to be borne in mind when analyzing the Japanese dissection data.
The sulphur (S) level of the metal within the softening-melting region is much higher than the concentration in the tapped HM. In the granular zones very little increase in S level occurs, which can be due to the materials in the softening-melting zone absorbing the S from the ascending gases, rather than a lack of absorption capacity by the burden in the granular zones. The lack of substantial quantities of S in the gas in the stack of the furnace can explain the horizontal profile at temperatures below 800 deg C. Further, as the temperature and slag basicity rise, the distribution of S between the slag and metal increases accordingly. Some idea of how S recirculates within the BF can be seen in Fig 3 in which the circulation of S within Hirohata BF no. 1 is shown.
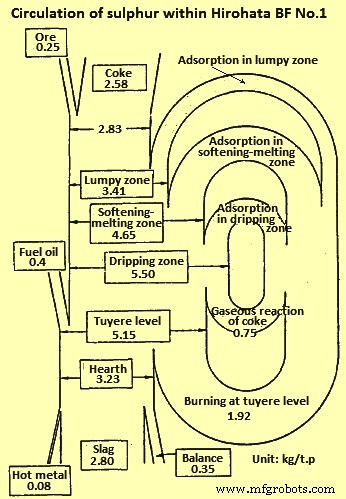
Fig 3 Circulation of sulphur within Hirohata BF no. 1
Size distribution – The change in physical size of the burden components during their descent was determined from the quenched furnace data and one of the major problems with this part of the study was that breakdown of material occurs during the quenching operation. Degradation of sinter reaches a maximum at temperatures of 400 deg C to 600 deg C and increases with the retention time. At levels of reduction in excess of 30 %, very little degradation occurs. Estimation of the cooling pattern of Kokura BF no.2 shows that the burden materials are exposed for a lengthy period of time to conditions which lead to considerable breakdown. The effect of the water quenching operation on the degradation of sinter was calculated. This calculation indicates that the sinter degradation increases with time after blow out and considerable degradation occurs in the region around the middle of the shaft.
Applying this to a centre working furnace (centre working means that the majority of the gas flows up the central axis of the furnace), it has been noticed that the degradation of sinter in the central zone of the furnace, where the reduction degree is high, is mainly caused by the reduction processes during operation. The situation in the peripheral zone is that the reduction degree is low and in this situation the breakdown is mainly caused by the long residence time of materials around 500 deg C during blowing out of the furnace. This was illustrated with the dissection results for the centre working Hirohata BF no.1. Another factor in maintaining the size of the burden materials is that in the central region of Hirohata BF no. 1, cracks if generated fused immediately because of the high temperatures and the rapid reduction taking place. Degradation is generally a problem having maximum concerns with sinters. Examination of the size distribution of pellets revealed that they were hardly pulverized and maintained their original shape.
Influence of gas flow – To further prove that the determination of the shape of the cohesive zone is by the gas flow within the furnace, core samples were taken from the Hirohata BF no.1 and Kukioka BF no.4 and their permeability was determined. Then their permeability was related to gas flow and gas velocity distribution profiles were prepared. These profiles can be directly related to the softening-melting layer distribution. The gas flow in the lower part of the BF is fast, 7 m/sec to 9 m/sec but slows considerably in the softening-melting layers to 2 m/sec to 4 m/sec thus indicating the poor permeability of the softening-melting layers. As the gas ascends the shaft its velocity naturally decreases due to the drop in gas temperature.
Cohesive zone control
It has been shown that the shape of the cohesive zone varies from BF to BF and much attention needs to be given for its control. The control of the cohesive zone is very dependent upon burden distribution. For maximum production, at the expense of fuel rate, a strong centre working profile is to be adopted, but if the fuel rate is to be minimized, then a less centre working practice is to be followed. Indeed, this is very much visible when comparing a strong centre working furnace, like Hirohata BF no.1 with moderate centre working furnace, like Kukioka BF no. 4. This point can be well explained by relating productivity to the height of the cohesive zone above the tuyeres (Fig 4). The higher the position of cohesive zone in the furnace, the greater is the productivity, although at the expense of an increase in fuel rate.
Another point concerning control of the cohesive zone is its effect on the refractory lining. If the wall temperature of the furnace is too high, then refractory wear is appreciable and one can expect a reduced life of the BF. Thus, for maintaining the refractory thickness, it is necessary to control the cohesive zone so that the wall temperatures are maintained at minimum levels.
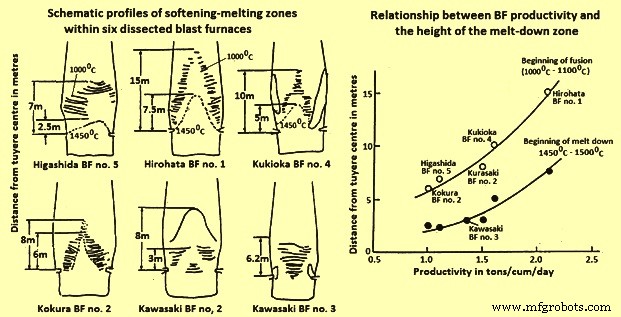
Fig 4 Schematic profiles of softening-melting zones and relationship BF productivity and height of the melt-down zone
Melting processes
The role of S in the melting process is governed by the Fe-S-O phase diagram. There is a necessity of a reaction between solid metallic iron and wustite in the burden with gaseous S, in the ascending gases. These phases react to form a eutectic of chemical composition 24 % S, 9 % O2, and 67 % Fe, having a melting point of 915 deg C. Once formed this liquid gains temperature as it descends the furnace, dissolving solid metallic iron and wustite which cause a change in liquid composition along a path until at certain point, the liquid splits into two conjugate liquid phases. Further increases in the temperature cause first part of the liquid to dissolve more solid iron, moving its composition along a path while the second part of the liquid dissolves more iron oxide and moves along the another composition path. Thus there are two phases (i) a liquid metal phase, and (ii) a liquid slag phase. The presence of silica in the system does not appreciably alter this mechanism. Indeed it moves the miscibility gap. Hence the separation of the nascent liquid into liquid metal and liquid slag phases occur at lower temperatures.
Once formed the two liquids go their own separate ways. The liquid metal dissolving solid iron, C and S become the final metal phase. The slag during its descent dissolves alumina, silica and lime from the coke ash, burden gangue and fluxes to form the final slag phase. A study has also shown that that the presence of hydrogen sulphide, in a CO / N2 gas mixture, lowered the melting point of iron ore sinters and pellets due to the formation of the liquid Fe-S-0 phase.
Alkalis are also thought to be closely associated with the initial melting process in the BF. Study with regards to the distribution of alkali, shows that the alkali is concentrated in the softening-melting layers. The reason for this is that alkali compounds, inherent within the burden and coke charged into the furnace are reduced and at temperatures in excess of 800 deg C to 900 deg C, the alkalis vapourize, as a metallic element or as a cyanide, and are swept into the softening-melting layers where they concentrate . As the softening-melting layers descend the alkali evaporates and continues the cycle.
Processus de fabrication
- Système d'automatisation, de mesure et de contrôle du processus de haut fourneau
- Génération et utilisation de gaz de haut fourneau
- Productivité des hauts fourneaux et paramètres d'influence
- Exploitation du laitier à haute teneur en alumine et du haut fourneau
- Chimie de la fabrication du fer par procédé de haut fourneau
- Procédés FASTMET et FASTMELT de fabrication du fer
- Salle de coulée de haut fourneau et son fonctionnement
- Fabrication du fer par haut fourneau et émissions d'oxyde de carbone
- Comprendre le processus d'usinage et la machine-outil



