Effet d'amélioration du champ proche dépendant des groupes de terminaux des nanofeuillets Ti3C2Tx
Résumé
Ti3 à la fois multicouche (ML) et à quelques couches (FL) C2 Tx des nanofeuillets ont été préparés par une procédure typique de gravure et de délaminage. Diverses caractérisations confirment que les groupes terminaux dominants sur ML-Ti3 C2 Tx et FL-Ti3 C2 Tx sont différents, qui ont été attribués aux groupes liés à O et hydroxyle, respectivement. Une telle déviation des terminaux dominants entraîne des performances physiques et chimiques différentes et fait finalement que les nanofeuilles ont des applications potentielles différentes. En particulier, avant couplage aux nanoparticules d'Ag, ML-Ti3 C2 Tx peut présenter un effet d'amélioration de champ proche plus fort ; cependant, Ag/FL-Ti3 C2 Tx la structure hybride peut confiner un champ proche plus fort en raison de l'injection d'électrons, qui peut être offerte par les groupes hydroxyle terminés.
Introduction
Ti3 C2 Tx , un carbure de métal de transition en couches bidimensionnel typique avec une structure semblable au graphène, a attiré une grande attention en raison de ses vastes applications potentielles dans les domaines de la catalyse, de l'énergie et de la médecine grâce à ses propriétés uniques, en particulier une grande surface spécifique, etc. [1,2,3,4,5,6]. Il a été démontré que les performances physiques et chimiques du Ti3 C2 Tx pourrait être déterminé par ses groupes terminaux, appelés Tx dans la formule (sont généralement –F, –O et/ou –OH), qui peut être ajustée en choisissant différentes procédures de préparation [7, 8]. Par exemple, certains résultats expérimentaux indiquent que l'équilibre hydrophile hydrophobe de Ti3 C2 Tx peut être modulé en interagissant certains groupes d'agents avec des groupes de terminaux –O sur Ti3 C2 Tx [9], et la capacité d'adsorption du Pb peut être améliorée en se connectant avec des groupes hydroxyle sur Ti3 C2 Tx [dix]. En attendant, certains travaux théoriques ont déterminé que les groupes méthoxy attachés pourraient améliorer la stabilité de Ti2 C et Ti3 C2 [11], et les groupes terminaux liés à O pourraient améliorer la capacité de stockage des ions lithium de diverses nanofeuillets [12]. Outre les applications multiples en tirant parti de la structure en couches unique avec certains groupes de terminaux, il s'avère que Ti3 C2 Tx peut également présenter des performances plasmoniques, et la longueur d'onde de résonance peut être réglée par les bornes et/ou l'épaisseur [13], indiquant que Ti3 C2 Tx pourraient confiner le champ électromagnétique sous excitation et peuvent éventuellement être utilisés comme absorbeurs parfaits à large bande [14, 15], dispositifs de blindage térahertz [16] et détecteurs ou capteurs photoniques et/ou moléculaires [17, 18, 19]. Cependant, la plupart des travaux antérieurs portaient soit sur les groupes terminaux dépendants des conditions de gravure [20], soit sur les performances plasmoniques globales [21]. Par conséquent, il est intéressant d'étudier systématiquement la relation entre les groupes terminaux de Ti3 C2 Tx avec différentes couches et leur effet d'amélioration du champ proche, car cet effet a été largement utilisé dans de nombreux domaines liés à l'optique, tels que la détection de diffusion Raman améliorée en surface, en raison du fort champ électromagnétique confiné [22,23,24].
Dans ce travail, afin de simplifier les options terminales et d'éviter d'utiliser du HF dangereux, l'agent de gravure mixte de LiF et HCl a été utilisé pour minimiser les terminaux fluorés (–F) dans le processus de gravure [25]. De plus, la procédure de sonication dans l'eau a été réalisée pour délaminer le Ti3 multicouche C2 Tx (ML-Ti3 C2 Tx ) en quelques couches Ti3 C2 Tx (FL-Ti3 C2 Tx ) sans introduire d'autres réactifs. En conséquence, le Ti3 obtenu C2 Tx avec différentes couches dans ce travail sera principalement terminé par des groupes liés à O ou à OH, ce qui rend ML-Ti3 C2 Tx ou FL-Ti3 C2 Tx les nanofeuillets révèlent différentes propriétés physiques et chimiques et présentent finalement différentes performances d'amélioration quasi-limées. De plus, les structures hybrides composées de Ti3 C2 Tx et des nanoparticules d'Ag ont été préparées et les effets de couplage correspondants ont également été explorés. Une telle exploration concernant les performances plasmoniques dépendantes du terminal de ces Ti3 C2 Tx avec différentes couches et configurations pourrait aider les gens à sélectionner le Ti3 approprié C2 Tx -matériaux à base de certains domaines optiques spécifiques.
Méthodes
Préparation du Ti3 C2 Tx Nanofeuilles
ML-Ti3 C2 Tx a été préparé en suivant une méthode modifiée précédemment rapportée [26]. Le processus de gravure typique a commencé par la préparation de la solution de LiF en dissolvant 1 g de LiF dans 20 mL de solution de HCl diluée (6 M) sous agitation. Ensuite, 1 g de Ti3 AlC2 la poudre a été lentement ajoutée à la solution ci-dessus, et le processus de gravure a été maintenu à 70 °C pendant 45 h sous agitation. Le sédiment humide a ensuite été lavé plusieurs fois avec de l'eau déminéralisée jusqu'à ce que le pH de la suspension liquide soit supérieur à 6. Ensuite, la suspension a été collectée et nommée ML-Ti3 C2 Tx . Pour obtenir FL-Ti3 C2 Tx , ML-Ti3 C2 Tx a ensuite été délaminé par sonication pendant 2 h dans une atmosphère d'Ar et suivi d'une centrifugation à 3 500 tr/min pendant 1 h.
Préparation Ag/Ti3 C2 Tx Nanocomposites
La synthèse des matériaux hybrides a commencé avec la préparation de la solution mixte d'AgNO3 (12,5 mL, 2 mmol/L) et NaC6 H5 O7 (12,5 mL, 4 mmol/L) à température ambiante. Après avoir ajouté rapidement la solution PVP (25 mL, 0,1 g/mL), Ti3 C2 Tx La solution (5 mL, 0,05 mg/mL) a ensuite été ajoutée lentement dans la solution mélangée sous agitation pendant 10 min à température ambiante. Par la suite, la solution mélangée ci-dessus a été chauffée jusqu'à 70 °C pour réagir pendant 45 h. Après centrifugation, les produits ont été conservés dans l'eau et nommés Ag/ML-Ti3 C2 Tx et Ag/FL-Ti3 C2 Tx , respectivement, selon le type de Ti3 C2 Tx utilisé dans la procédure.
Caractérisation
Un microscope électronique à balayage à émission de champ (Carl ZEISS Sigma) et deux microscopes électroniques à transmission (JEM-2100F et JEM-1400Flash) ont été utilisés pour déterminer les morphologies des échantillons. Les diagrammes de diffraction des rayons X (DRX) dans la plage de 2θ = 5°–80° avec un pas de 0,02° ont été enregistrés sur un diffractomètre à poudre (X'Pert PRO MPD). Potentiels zêta et états de surface du ML-Ti3 C2 Tx et FL-Ti3 C2 Tx ont été mesurés par un Malvern Zetasizer (Nano-ZS90) et une spectroscopie photoélectronique à rayons X (XPS, ESCALAB 250Xi), respectivement. L'absorption et la performance Raman des échantillons ont été enregistrées par un spectrophotomètre UV-Vis (CARY 5000) et une spectroscopie Raman (LabRAM HR Evolution), respectivement. La longueur d'onde d'excitation de la détection Raman était de 532 nm, et les puissances laser pour les mesures Raman habituelles et les caractérisations de diffusion Raman améliorée en surface (SERS) étaient respectivement de 12,5 mW et 0,05 mW.
Résultats et discussion
Les deux morphologies de ML-Ti3 C2 Tx et FL-Ti3 C2 Tx sont représentés sur les Fig. 1a, b et c, d, respectivement. On peut voir que FL-Ti3 C2 Tx semble plus transparent, indiquant que son numéro de couche est bien inférieur à ML-Ti3 C2 Tx . La figure 1e montre les modèles XRD de tous les échantillons. Ti3 AlC2 et ML-Ti3 C2 Tx montrent leurs caractéristiques de phase typiques, qui concordent bien avec certains rapports précédents [26,27,28]. On peut facilement observer que le pic intense (002) de ML-Ti3 C2 Tx passe à l'angle inférieur par rapport à celui de Ti3 AlC2 , impliquant l'élimination des atomes d'Al de la phase MAX et l'expansion le long de l'axe c. Par rapport aux pics de diffraction du ML-Ti3 C2 Tx , à la fois élargi (002) pic et disparu (004) et (008) pics de FL-Ti3 C2 Tx ont déterminé la préparation réussie de l'échantillon à quelques couches [29]. De plus, le (002) pic de FL-Ti3 C2 Tx se localise à un angle un peu plus élevé que celui du ML-Ti3 C2 Tx , indiquant que ML-Ti3 C2 Tx et FL-Ti3 C2 Tx doit se terminer par des groupes différents, qui peuvent être attribués à -O et -OH, respectivement, puisque le Ti3 tel que préparé C2 Tx (ML-Ti3 C2 Tx ) ne se terminera pas principalement avec -F sans HF comme agent de gravure et les paramètres c correspondants attirés par les modèles XRD sont en bon accord avec ce que les travaux précédents ont rapporté [25, 30].
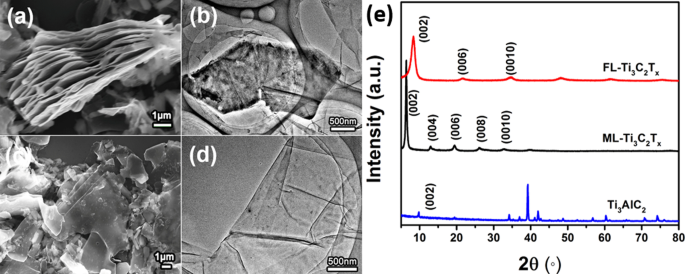
Morphologie et déterminations de phase. un , b Images SEM et TEM de ML-Ti3 C2 Tx . c , d Images SEM et TEM de FL-Ti3 C2 Tx . e Modèles XRD de Ti3 AlC2 , ML-Ti3 C2 Tx et FL-Ti3 C2 Tx
La figure 2a montre les spectres Raman de ML-Ti3 C2 Tx et FL-Ti3 C2 Tx . Comme on peut le voir, les signaux Raman sont compris entre 200 et 800 cm −1 pour les deux échantillons sont assez similaires. Parmi eux, le pic à 717 cm −1 est dû au A1g vibration hors plan symétrique des atomes Ti et C, tandis que les pics à 244, 366 et 570 cm −1 sont issus des modes dans le plan (cisaillement) de Ti, C et des groupes terminaux de surface, respectivement [31, 32]. Quant aux signaux Raman allant de 800 à 1800 cm −1 , en comparaison avec ML-Ti3 C2 Tx , FL-Ti3 C2 Tx montre non seulement un signal Raman plus fort à 1580 cm −1 (bande G), mais présente également deux bandes Raman émergentes à 1000–1200 cm −1 et 1 300 cm −1 (bande D). Ici, l'apparition de la bande D indique que certains atomes de Ti ont été arrachés et que davantage d'atomes de C sont exposés à l'environnement [33]. Par conséquent, l'intensité Raman intégrée de FL-Ti3 C2 Tx dans cette plage est légèrement plus grande que celle de ML-Ti3 C2 Tx , ce qui implique que FL-Ti3 C2 Tx adsorbe plus de groupes terminaux. Potentiels zêta de ML-Ti3 C2 Tx et FL-Ti3 C2 Tx sont de −4,38 et −26,9 mV, respectivement, comme indiqué dans le fichier supplémentaire 1 : Fig. S1, qui confirment en outre que FL-Ti3 C2 Tx sont terminés par plus de groupes avec des charges négatives.
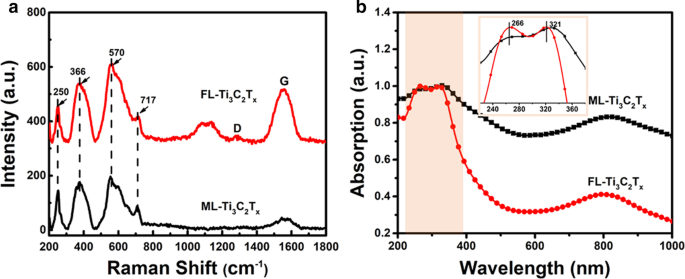
un Spectres Raman et b Spectres d'absorption normalisés du FL-Ti3 C2 Tx et ML-Ti3 C2 Tx . L'encart dans b présente les bandes d'absorption du FL-Ti3 C2 Tx et ML-Ti3 C2 Tx dans la région UV
Les spectres UV-Vis illustrés à la Fig. 2b révèlent que les deux FL-Ti3 C2 Tx et ML-Ti3 C2 Tx présentent deux bandes d'absorption dominantes. Dans la région UV (225-325 nm), FL-Ti3 C2 Tx affiche une bande d'absorption relativement plus forte qui correspond à la transition de bande interdite [34], ce qui implique qu'il y a plus de groupes -OH terminés sur FL-Ti3 C2 Tx [35]. D'autre part, la comparaison entre les bandes d'absorption à grande longueur d'onde (600-1000 nm) des deux échantillons montre que l'intensité relative de FL-Ti3 C2 Tx dans cette plage est évidemment inférieur à celui du ML-Ti3 C2 Tx , indiquant que ML-Ti3 C2 Tx se terminent principalement par –O [35]. FL-Ti3 C2 Tx peuvent être bien dispersés dans la solution aqueuse puisque les groupes -OH terminés montrent une hydrophilie et une répulsion électrostatique entre les feuilles [31, 36]. Comme pour ML-Ti3 C2 Tx avec plus de bornes -O, il ne peut former qu'une suspension au début et se déposera par la suite comme indiqué dans le fichier supplémentaire 1 :Fig. S2a.
Afin d'éclairer davantage les groupes de surface terminés sur ML-Ti3 C2 Tx et FL-Ti3 C2 Tx , les spectres XPS des deux échantillons ont été collectés et sont présentés sur la figure 3. Toutes les informations détaillées correspondantes concernant les états de surface sont résumées dans le fichier supplémentaire 1 :tableau S1. La fraction de Ti-C dans FL-Ti3 C2 Tx (9,80 %) est inférieur à celui de ML-Ti3 C2 Tx (17,31 %), tandis que le rapport C–C dans FL-Ti3 C2 Tx (44,62%) est plus élevé. Un tel changement d'état de surface met en évidence la perte d'atomes de Ti et les atomes de C plus exposés à la surface du FL-Ti3 C2 Tx , qui est en accord avec la bande D émergente dans son spectre Raman illustré à la Fig. 2a. L'augmentation du C-Ti-Tx rapport en FL-Ti3 C2 Tx (21,27 %) indique qu'il devrait y avoir plus de groupes terminaux actifs adsorbés à sa surface que ML-Ti3 C2 Tx , qui est en accord avec les résultats du potentiel Zeta indiqués dans le fichier supplémentaire 1 :Fig. S1. Outre la quantité des groupes terminaux, l'analyse des résultats XPS révèle également que FL-Ti3 C2 Tx et ML-Ti3 C2 Tx ont été terminés par différents groupes fonctionnels dominants, ce qui a également été suggéré par les pics de diffraction (002) illustrés à la Fig. 1e. En ce qui concerne les spectres O 1 de ces deux échantillons, on peut clairement voir que davantage d'états liés à O ont été trouvés à la surface de ML-Ti3 C2 Tx , et certaines d'entre elles sont des molécules d'oxygène adsorbées, qui peuvent se dissocier pour former Ti3 C2 Ox et repoussera donc O2 dans l'air pour empêcher une oxydation supplémentaire du ML-Ti3 C2 Tx [37]. En conséquence, ML-Ti3 C2 Tx semble présenter une meilleure résistance à l'oxydation avec un TiO2 plus faible rapport (13,98 %) que FL-Ti3 C2 Tx (19,60 %).
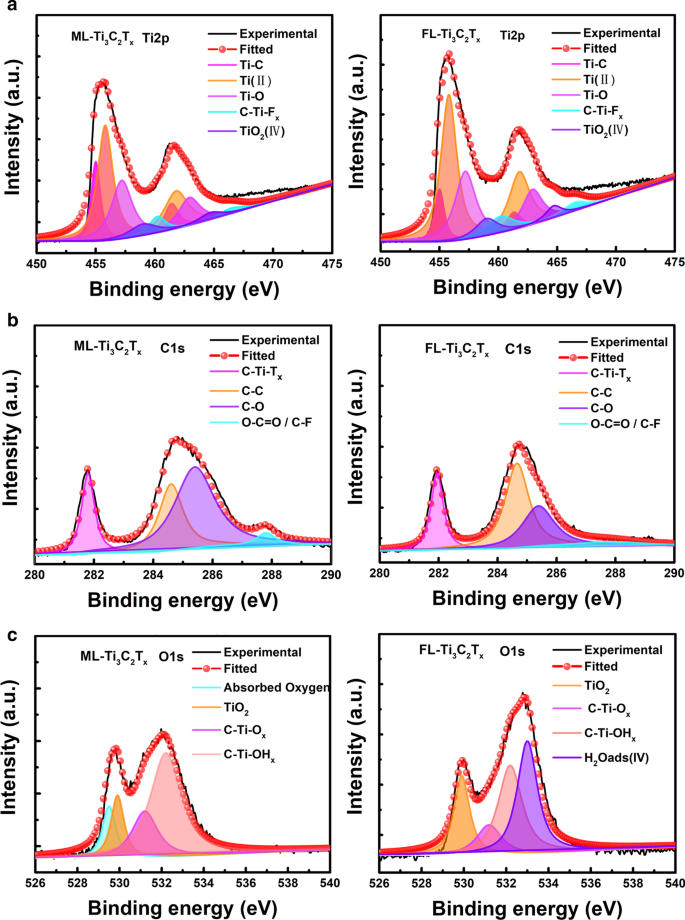
Spectres XPS de ML-Ti3 C2 Tx et FL-Ti3 C2 Tx un Ti2p, b C1, c O1
Sur la base des observations et des analyses des Fig. 1, 2 et 3, on peut conclure que bien que les deux ML-Ti3 C2 Tx et FL-Ti3 C2 Tx sont terminés par des groupes fonctionnels avec une charge négative, la quantité et le type dominant des groupes sont assez différents. D'une part, la quantité de groupes terminaux sur FL-Ti3 C2 Tx est plus grand que celui de ML-Ti3 C2 Tx . Par contre, la structure terminale dominante sur ML-Ti3 C2 Tx est Ti3 C2 O2 , ce qui fait de ML-Ti3 C2 Tx pour être plus stable dans l'air [38], tandis que pour FL-Ti3 C2 Tx , il est principalement terminé par Ti3 C2 (OH)2 , ce qui aide FL-Ti3 C2 Tx être bien dispersé dans les solutions aqueuses [36].
Ti3 C2 Tx avec des groupes terminaux fonctionnels pourrait révéler de bonnes performances d'adsorption et pourrait donc agir comme un substrat de diffusion Raman amélioré en surface (SERS) pour améliorer l'activité Raman des molécules sondes chargées positivement [3, 39, 40]. Comparaison avec ML-Ti3 C2 Tx , FL-Ti3 C2 Tx devrait présenter une meilleure capacité d'adsorption puisqu'il a été déterminé qu'il se termine par plus de charges négatives. Ces meilleures performances d'adsorption ont été démontrées par les photographies optiques de la solution mélangée avec R6G et FL-Ti3 C2 Tx comme indiqué dans le fichier supplémentaire 1 :Fig. S2b. Cependant, la figure 4a révèle que le ML-Ti3 C2 Tx substrat exécute évidemment une meilleure activité SERS que FL-Ti3 C2 Tx un. Considérant ML-Ti3 C2 Tx avec -O terminal présente une bande d'absorption plus forte centrée à environ 800 nm, qui peut être attribuée à l'absorption résonante des plasmons de surface [3, 15, 39, 41], on peut donc conclure que ML-Ti3 C2 Tx avec une activité SERS plus forte devrait résulter de l'effet de champ proche plus fort induit par la résonance plasmonique de surface relativement plus forte, comme le montre la figure 2b.
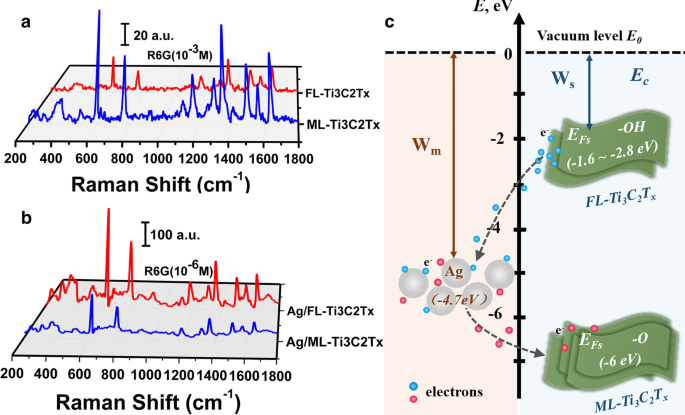
un Spectres SERS de R6G (10 –3 M) avec ML-Ti3 C2 Tx et FL-Ti3 C2 Tx . b Spectres SERS de R6G (10 –6 M) avec Ag/ML-Ti3 C2 Tx et Ag/FL-Ti3 C2 Tx . c Schéma de principe du transfert d'électrons du FL-Ti3 C2 Tx à Ag NP en raison de leur différence de fonction de travail. Wm et Ws représentent les travaux de sortie de Ag NP et FL-Ti3 C2 Tx , respectivement
Afin d'explorer davantage la relation entre les groupes terminaux et l'effet quasi-classé de Ti3 C2 Tx nanofeuillets, les structures hybrides composées de Ti3 C2 Tx des nanofeuillets, dont quelques couches et multicouches, et des nanoparticules d'Ag (NP) ont été synthétisés, qui sont donc étiquetés Ag/FL-Ti3 C2 Tx et Ag/ML-Ti3 C2 Tx , respectivement. Les morphologies des deux échantillons hybrides sont présentées dans le fichier supplémentaire 1 :Fig. S3. Les encarts indiquent les distributions de taille correspondantes du chargement des Ag NPs sur ML-Ti3 C2 Tx (5-40 nm) est plus grand que celui du FL-Ti3 C2 Tx (2-20 nm). Intuitivement, on pourrait conclure que Ag/ML-Ti3 C2 Tx pourrait effectuer une meilleure activité SERS que Ag/FL-Ti3 C2 Tx puisque à la fois des Ag NPs plus grands et une résonance plasmonique de surface relativement plus forte de ML-Ti3 C2 Tx sont bénéfiques pour confiner un champ proche plus fort. Cependant, les spectres SERS illustrés à la figure 4b révèlent un résultat contre-intuitif. Il est clair que l'effet d'amélioration offert par Ag/FL-Ti3 C2 Tx est près de 3 fois supérieur à Ag/ML-Ti3 C2 Tx , impliquant que le couplage entre Ag NPs et FL-Ti3 C2 Tx devrait jouer un rôle important pendant le processus de détection. Comme confirmé ci-dessus, FL-Ti3 C2 Tx a été principalement terminé par des groupes -OH avec beaucoup d'électrons de surface, ce qui entraînera la formation de Ti3 C2 (OH)2 structure avec un travail de sortie de 1,6 à 2,8 eV [42, 43]. Comme le montre la figure 4c, les électrons de surface abondants seront donc transférés de FL-Ti3 C2 Tx aux Ag NPs avec un travail de sortie de 4,7 eV [44]. Avec l'injection supplémentaire d'électrons chauds de FL-Ti3 C2 Tx , Ag NPs avec une plus petite taille pourraient présenter une résonance plus forte sous l'excitation et éventuellement effectuer une meilleure activité SERS en raison de l'effet électromagnétique plus fort induit par le couplage. Il est à noter que la fonction travail de Ti3 C2 O2 structure formée à la surface du ML-Ti3 C2 Tx est d'environ 6,0 eV [43], ce qui entraînera un transfert d'électrons de la surface des Ag NPs vers le ML-Ti3 C2 Tx nanofeuillets et affaiblira donc l'effet amélioré en champ proche soutenu par les Ag NPs. Par contre pas comme FL-Ti3 C2 Tx avec bornes -OH, ML-Ti3 C2 Tx avec des bornes -O ne peut pas offrir suffisamment d'électrons sous excitation [42]. Il est donc raisonnable que l'activité SERS de Ag/ML-Ti3 C2 Tx est pire que celle d'Ag/FL-Ti3 C2 Tx .
Conclusions
En résumé, ML-Ti3 C2 Tx et FL-Ti3 C2 Tx terminés par différents groupes fonctionnels dominants ont été préparés avec succès. Il a été démontré que ML-Ti3 C2 Tx est plus stable dans l'air en raison de la structure de surface du Ti3 C2 O2 et montre une activité SERS plus forte que FL-Ti3 C2 Tx car il peut révéler un effet de champ proche plus fort. Cependant, FL-Ti3 C2 Tx terminé par Ti3 C2 (OH)2 peut être bien dispersé dans une solution aqueuse et montrera de meilleures performances SERS après couplage aux Ag NP en raison de l'injection d'électrons suffisante. Une telle recherche concernant les performances d'amélioration du champ proche dépendant des groupes terminaux aidera les gens à étendre les applications potentielles de Ti3 C2 Tx dans les domaines liés à l'optique.
Disponibilité des données et des matériaux
L'ensemble de données brutes obtenues et analysées au cours du travail expérimental est disponible auprès de l'auteur correspondant sur demande raisonnable.
Abréviations
- ML-Ti3 C2 Tx :
-
Ti3 multicouche C2 Tx
- FL-Ti3 C2 Tx :
-
Peu de couches Ti3 C2 Tx
- SERS :
-
Diffusion Raman améliorée en surface
- NP :
-
Nanoparticules
Nanomatériaux
- Qu'est-ce que la corrosion des bornes de batterie ?
- Effet de l'irradiation ultraviolette sur les caractéristiques des diodes 4H-SiC PiN
- Effet de surface sur le transport du pétrole dans les nanocanaux :une étude de dynamique moléculaire
- L'effet d'une petite quantité de SiO2 sur la cinétique de frittage des nanopoudres de zircone tétragonale
- L'effet des anions sulfate sur la nucléation ultrafine du titane
- Effet optique non linéaire amélioré dans les cellules hybrides à cristaux liquides basées sur des cristaux photoniques
- Qu'est-ce qu'une borne négative ?
- Qu'est-ce qu'une borne positive ?
- Comprendre le capteur à effet Hall



