Phosphore émetteur vert Eu2+ activé obtenu à partir d'ions Eu3+ dopant la zéolite-3A dans l'air ambiant et ses diodes électroluminescentes vertes efficaces
Résumé
Eu 2+ -les phosphores activés sont largement appliqués dans les zones d'éclairage et d'affichage en raison de leurs bonnes performances optiques. Dans cet article, une excellente zéolite-3A émettant dans le vert :1,3 % en poids de phosphore Eu est préparée par une méthode de réaction à haute température verte et respectueuse de l'environnement, sans atmosphère ni agents réducteurs. Pendant ce temps, le mécanisme de réduction de Eu 3+ ions à Eu 2+ ions est étudiée. Les résultats de l'expérience montrent que la morphologie, la structure cristalline et la propriété luminescente sont affectées par la température de frittage. L'échantillon résultant montre que la large bande d'excitation se situe dans la plage de 310 à 450 nm et que le pic de la large bande d'émission est situé à 523 nm. De plus, la zéolite-3A :1,3 % en poids de phosphore Eu est encapsulée sur une puce commerciale émettant des UV pour fabriquer une diode électroluminescente (DEL) verte de pureté avec les coordonnées de couleur de la Commission Internationale de L'Eclairage (CIE) à (0,295, 0,537 ).
Contexte
Les matériaux luminescents sont largement utilisés dans de nombreux domaines, tels que les dispositifs d'éclairage et d'affichage [1,2,3,4,5]. Au fil des ans, les matériaux luminescents activés par l'europium (Eu) des terres rares (RE) ont reçu plus d'attention en raison de leurs propriétés optiques uniques, telles qu'une luminosité élevée [6, 7], une stabilité chimique élevée [8, 9] et une excellente respect de l'environnement [8, 10]. En particulier, les ions Eu ont deux états d'oxydation divalents (Eu 2+ ) et trivalent (Eu 3+ ), présentant des caractéristiques d'émission différentes. Généralement, Eu 3+ les ions sont principalement comme un activateur émetteur rouge qui provient de 5 D0 → 7 FJ (J = 1, 2, 3, 4 et 5) transitions [11,12,13]. Cependant, Eu 2+ les ions, leurs électrons 5d situés dans les orbitales externes, sont sensibles à leur environnement. Ainsi, leurs émissions sont facilement affectées par l'environnement du champ cristallin, ayant une large région allant de l'ultraviolet (UV) au rouge. Chen et al. préparé Eu 2+ -fluorophosphates activés Ba3 GdNa(PO4 )3 F avec du phosphore bleu et rouge émettant deux couleurs [14]. Sato et al. signalé émettant du Ca2 rouge SiO4 :Eu 2+ phosphores [15]. Lin et al. synthétisé Eu 2+ , Mn 2+ -activé Ca9 Mg(PO4 )6 F2 phosphores à émission de couleur bleue à jaune [16]. Il est suggéré que Eu 2+ -les luminophores activés causés par les transitions électroniques 5d-4f autorisées par la parité montrent une large bande d'émission forte [7]. Par conséquent, l'Eu 2+ -les luminophores activés sont le principal objectif des matériaux luminescents ces dernières années.
De nos jours, Eu 2+ -les matériaux luminescents dopés sont obtenus en réduisant Eu 3+ à Eu 2+ , car il n'y a pas d'Eu 2+ naturel -matériaux dopés. Habituellement, il peut être réalisé dans une atmosphère réductrice comprenant H2 , H2 /N2 , ou CO. Par exemple, Gao et al. Eu 2+ récemment obtenu -phosphore activé de Eu 3+ -USY échangé (Na28 Si168 Al28 ·240H2 O, Si/Al ratio = 6) zéolithes par traitement thermique en H2 /N2 atmosphère réductrice [17]. Chen et al. a signalé que Eu 2+ -sensibilisé Sr6 Ca4 (PO4 )6 F2 :Tb 3+ le phosphore pourrait être obtenu en utilisant la méthode à l'état solide à haute température dans H2 /N2 atmosphère réductrice [18]. Néanmoins, la réaction en atmosphère réductrice est relativement dangereuse et nécessite un environnement de travail bien équipé, ce qui conduit à un coût plus élevé des luminophores. De plus, la pollution de l'environnement sera produite si la réaction se déroule dans des conditions réductrices de CO. Par conséquent, une méthode de préparation verte, écologique et à moindre coût a attiré plus d'attention.
Comme on le sait, Eu 3+ parmi certains hôtes composés spéciaux, tels que les borates [19], les phosphates [20] et les aluminates [21], peut également être réduit à Eu 2+ dans l'air à haute température. Il est suggéré que tous ces composés contiennent du tétraèdre rigide BO4 , bon de commande4 , AlO4 , ou octaédrique AlO6 ossature de groupe, entourant et isolant l'Eu 2+ produit ions de l'oxygène [21, 22]. Les zéolites, en tant que type d'aluminosilicate, sont non seulement des minéraux naturels, mais peuvent également être synthétisées dans l'industrie à moindre coût [23,24,25,26,27,28]. Notamment, leur structure peut satisfaire les exigences susmentionnées, réduisant Eu 3+ ions à Eu 2+ ions et faire Eu 2+ ions stables. Ils sont également largement utilisés comme excellents matériaux hôtes pour les applications de matériaux luminescents en raison de leur stabilité chimique élevée [29, 30] et ainsi de suite. Parmi les différentes zéolithes, la zéolite-3A (\( \frac{2}{3} \)K2 O·\( \frac{1}{3} \)Na2 O·Al2 O3 ·2SiO2 ·\( \frac{9}{2} \)H2 Le rapport O, Si/Al ≈ 1) a été utilisé comme matériau hôte pour le phosphore à conversion descendante. Ici, nous atteignons Eu 2+ phosphore zéolite-3A activé par une méthode de traitement thermique élevée sans atmosphère réductrice. L'Eu 2+ obtenu -le phosphore zéolite-3A activé a un rendement quantique d'environ 36,6 %. Cette méthode de préparation est sûre, verte et écologique. La large bande d'excitation de l'échantillon que nous avons obtenu est de l'ordre de 310 à 450 nm, et le pic de la bande d'émission est situé à 523 nm. Et les échantillons sont stables et faciles à préparer à nouveau. En encapsulant de la zéolite 3A émettant du vert :1,3 % en poids de phosphore Eu sur une puce émettant des UV, nous acquérons une bonne LED verte avec des coordonnées de couleur de la Commission Internationale de L'Eclairage (CIE) à (0,295, 0,537) et une luminosité de 231,6 cd/m 2 sous une tension de 3 V. Ces résultats montrent non seulement une approche de préparation simple et écologique, mais fournissent un excellent phosphore à émission verte avec des applications prometteuses dans les domaines de l'éclairage et de l'affichage.
Méthodes
L'objectif de l'étude
Nous visons à préparer Eu 2+ -des phosphores activés avec une émission verte brillante grâce à une méthode de synthèse sûre, verte et respectueuse de l'environnement, sans aucune atmosphère réductrice.
Matériaux
Zéolite-3A (\( \frac{2}{3} \)K2 O·\( \frac{1}{3} \)Na2 O·Al2 O3 ·2SiO2 ·\( \frac{9}{2} \)H2 O, rapport Si/Al ≈ 1) acheté auprès de Shanghai Tongxing Molecular Sieve Co., LTD, et oxyde d'europium (Eu2 O3 ) obtenus auprès de Sinopharm Co., Ltd, ont été utilisés sans autre purification. Résine de silicone et puce bleue InGaN (5 mm × 5 mm, λ = 375 nm) ont été reçues de Shenzhen Looking Long Technology Co., Ltd.
Synthèse d'échantillons
Eu 2+ Des échantillons de zéolite 3A activée ont été préparés en utilisant une méthode de réaction typique à l'état solide à haute température. Premièrement, différentes quantités stoechiométriques de zéolite-3A et Eu2 O3 ont été bien mélangés et soigneusement broyés dans un mortier d'agate pendant 40 min. Et puis, ils ont été frittés à différentes températures sans atmosphère réductrice. Enfin, les échantillons cibles ont été obtenus après refroidissement.
Fabrication de LED vertes
Eu 2+ -la poudre de zéolite-3A activée et la résine de silicone ont été mélangées selon un rapport massique de 1:5, puis sous agitation homogène. La composition a été appliquée sur une puce InGaN et durcie à 60°C pendant environ 2h. Enfin, l'épaisseur du composite a été mesurée à environ 1 mm.
Caractérisation
La morphologie et la structure des produits résultants ont été caractérisées au microscope électronique à balayage à émission de champ (FESEM, FEI Sirion-200) et par diffraction des rayons X (XRD, Philips X'Pert) avec un rayonnement Cu Kα (λ = 0,15405 nm). Les courbes d'analyse thermogravimétrique (TG) ont été mesurées par SDT Q600 V20.9 Build 20, qui ont été obtenues de la température ambiante à 800 °C avec une vitesse de chauffe de 10 °C/min dans une atmosphère d'azote (débit 10 ml/min) . Les spectres d'excitation de photoluminescence (PLE) et de photoluminescence (PL) ont été obtenus à température ambiante en utilisant des spectromètres de fluorescence à résolution temporelle et à état stable FLS920 d'Edinburgh Instruments équipés d'une lampe Xe de 450 W. L'état d'oxydation de l'élément europium a été étudié par spectroscopie photoélectronique aux rayons X (XPS, ESCALAB 250). Le spectre d'électroluminescence (EL) a été étudié par le spectromètre Ocean Optics FLAME-S-VIS-NIR avec une sphère d'intégration de fibre (FOIS-1) et un électromètre Keithley 2400.
Résultats et discussion
La figure 1a montre l'image SEM de la zéolite-3A vierge. On peut observer que la morphologie de la zéolite-3A vierge est de structure cubique irrégulière avec une longueur de côté d'environ 1,5 µm. Zéolite-3A :1,3 % en poids de phosphore Eu sont obtenus par une méthode de réaction à l'état solide à haute température, sans aucune atmosphère réductrice. La morphologie et la structure de la zéolite-3A :1,3 % en poids de phosphore Eu obtenu à 1400 °C pendant 3 h sont caractérisées par le microscope électronique à balayage à émission de champ et les mesures de diffraction des rayons X, comme le montrent les Fig. 1b, c, respectivement. La figure 1b montre que les particules présentent une structure morphologique irrégulière et que la distribution des tailles de cristallites n'est pas uniforme. En comparant la figure 1b avec a, on peut constater que les particules de zéolite sont agrégées les unes avec les autres après frittage à 1400°C pendant 3h. Comme on peut le voir sur la figure 1c, tous les pics de diffraction dans le diagramme XRD de la zéolite-3A :1,3 % en poids de phosphore Eu sont en bon accord avec la phase pure de la zéolite-3A (JCPDS n° 00-019-1227), et aucun d'autres pics d'impuretés sont observés. Cela signifie que Eu 2+ les ions sont introduits avec succès dans les réseaux hôtes de la zéolite et une certaine quantité d'Eu 2+ le dopage ionique ne modifie évidemment pas la structure cristalline [10]. La figure 1d montre les courbes TG de la zéolite-3A pure et de la zéolite-3A :1,3 % en poids de phosphore Eu fritté à 1400 °C. On peut voir qu'il y a une perte de masse continue pendant le chauffage jusqu'à environ 266°C dans la courbe TG pour la zéolithe-3A pure, où elle atteint une valeur d'environ 19,45%. Ceci correspond à la libération d'eau physiquement liée localisée dans les cavités et canaux de la zéolithe-3A [31]. Le phénomène de perte de masse n'est pas évident car la température augmente de manière séquentielle. Comme le montre la courbe TG de la zéolite-3A :1,3 % en poids de phosphore Eu fritté à 1400 °C, il n'y a pratiquement pas de perte de masse. Ces résultats indiquent que la zéolite-3A :1,3 % en poids Eu frittée à 1400 °C est très stable.
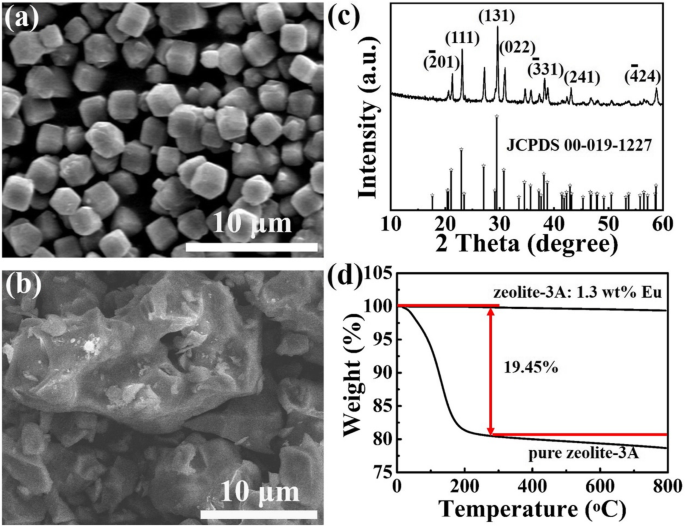
Les images SEM de a zéolite-3A pure et b zéolite-3A :1,3 % en poids de phosphore Eu fritté à 1400 °C pendant 3 h. c Diagramme XRD de la zéolite-3A :1,3 % en poids de phosphore Eu fritté à 1400 °C pendant 3 h. d Courbes TG de zéolithe-3A et zéolithe-3A pures :1,3 % en poids de phosphore Eu fritté à 1400 °C pendant 3 h
La figure 2 montre les images SEM et les motifs XRD de la zéolite-3A :1,3 % en poids de phosphores Eu frittés à différentes températures. D'après les images SEM (Fig. 2a–d), il est clair d'observer que la morphologie change de manière significative avec l'augmentation de la température de frittage. Lorsque la température de frittage est relativement plus basse (600 °C et 800 °C), la morphologie des échantillons reste celle de la zéolite-3A vierge, c'est-à-dire de forme cubique avec une taille moyenne de 1,5 μm (illustrée à la Fig. 1a) . Cependant, on peut observer que les particules commencent à s'agréger lorsque la température de frittage atteint 1000 °C et 1200 °C. À mesure que la température de frittage augmente, les particules peuvent continuer à s'agréger et former une structure massive (Fig. 1b). Pendant ce temps, leurs modèles XRD sont illustrés à la figure 2e. On remarque que les pics de diffraction des échantillons préparés à 600°C et 800°C ne sont pas absolument indexés sur la carte étalon de zéolithe-3A pure (JCPDS n°00-019-1227). Deux échantillons existent des pics de diffraction supplémentaires situés à 12,5° et 16,3°, qui sont attribués aux pics de Eu2 O3 (JCPDS n° 00-012-0384). Cela signifie que les ions Eu ne peuvent pas être incorporés avec succès dans les réseaux hôtes de la zéolite lorsque la température de calcination est inférieure à 800°C [32]. Néanmoins, les échantillons frittés à plus de 1000 °C présentent des pics correspondant aux principaux pics caractéristiques de la carte standard de zéolite-3A pure.
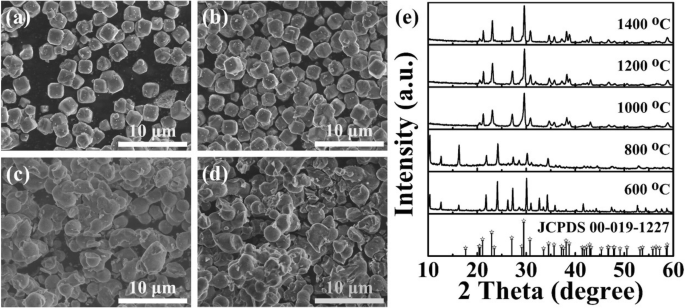
Images SEM de zéolite-3A :1,3 % en poids de phosphore Eu fritté à 600 °C (a ), 800 °C (b ), 1000 °C (c ), et 1200 °C (d ), respectivement. e Modèles XRD de la zéolite-3A :1,3 % en poids de phosphores Eu frittés à différentes températures, respectivement
Pour étudier l'effet de la température de calcination sur l'émission PL, les spectres d'émission PL des échantillons à différentes températures de calcination sont testés et illustrés à la figure 3a. Comme on le voit dans l'encart, les échantillons frittés à 600 °C et 800 °C ne montrent que le pic d'émission rouge centré à 617 nm qui est attribué au 5 D0 → 7 F2 transition électrique-dipôle de Eu 3+ ion [33]. Au fur et à mesure que la température de frittage augmente, le pic d'émission rouge s'affaiblit progressivement et le pic d'émission vert (centré à 523 nm) est évidemment observé. Surtout, l'échantillon préparé à 1400 °C montre principalement une caractéristique typique Eu 2+ émission centrée à 523 nm, qui est due au 4f 6 5d → 4f 7 transition [34]. En comparant les différentes courbes PL de la Fig. 3a, on peut observer que la quantité d'Eu 3+ → Eu 2+ augmente continuellement avec l'augmentation de la température de frittage. Ce résultat coïncide avec celui des modèles XRD de la figure 2e. À savoir, Eu 3+ L'ion est la forme principale lorsque la température de calcination est inférieure à 1000°C. Eu 3+ les ions sont progressivement réduits à Eu 2+ ions lorsque la température de frittage est supérieure à 1000 °C. La figure 3b montre les spectres PLE et PL de l'échantillon fritté à 1400 °C. On constate que le spectre PLE montre une large bande d'excitation entre environ 310 et 450 nm [7, 35]. Et l'encart est la photographie montrant une émission de lumière verte brillante avec l'éclairage d'une lampe UV de 365 nm. Le spectre PL de la figure 3b correspond à la couleur observée sur la photo.
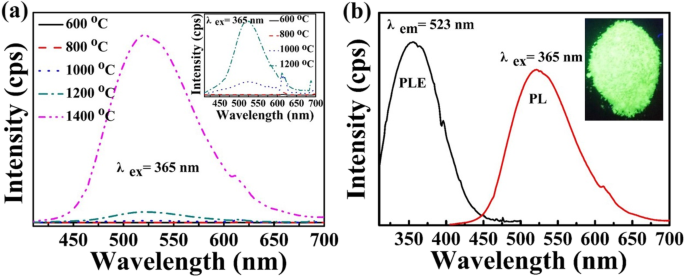
un Spectres d'émission PL pour la zéolite-3A :1,3 % en poids de phosphores Eu frittés à différentes températures, respectivement. L'encart montre les spectres grossissants. b Spectres d'excitation de photoluminescence (PLE) et d'émission de photoluminescence (PL) pour la zéolite-3A :1,3 % en poids de phosphores Eu frittés à 1400 °C pendant 3 h. L'encart est la photographie de l'échantillon avec l'éclairage d'une lampe UV de 365 nm
Afin d'approfondir l'étude de l'état d'oxydation de l'élément Eu, le modèle XPS de Eu3d pour l'échantillon obtenu à 1400 °C est surveillé et présenté sur la figure 4. Les pics situés à 1165 eV et 1135 eV correspondent à Eu 3+ état d'oxydation, mais les pics autour de 1155 eV et 1125 eV sont attribués à Eu 2+ état d'oxydation [11, 36]. Ce résultat montre que certains des Eu 3+ les ions sont réduits à Eu 2+ ions dans la zéolite hôte sous une réaction de traitement thermique élevée, et ce résultat est cohérent avec les spectres PL (Fig. 3). Le mécanisme de réaction possible peut être montré dans les équations suivantes :
$$ {\mathrm{Eu}}_2{\mathrm{O}}_3\overset{{\mathrm{K}}_2\mathrm{O}}{\to}\kern0.5em 2{\left[{\ mathrm{Eu}}^{3+}\right]}_{\mathrm{K}}^{\ast \ast }+\kern0.5em 4{V}_{\mathrm{K}}^{\prime }+3{\mathrm{O}}_{\mathrm{O}}^{\times } $$ (1) $$ {V}_{\mathrm{K}}^{\prime}\à {V }_{\mathrm{K}}^{\times}\kern0.5em +{\mathrm{e}}^{\prime } $$ (2) $$ {\left[{\mathrm{Eu}}^ {3+}\right]}_{\mathrm{K}}^{\ast \ast}\kern0.5em +{\mathrm{e}}^{\prime}\to {\left[{\mathrm{ Eu}}^{2+}\right]}_{\mathrm{K}}^{\ast } $$ (3) $$ {\left[{\mathrm{Eu}}^{2+}\right ]}_{\mathrm{K}}^{\ast }+{\mathrm{e}}^{\prime}\to {\left[{\mathrm{Eu}}^{2+}\right]} _{\mathrm{K}}^{\times } $$ (4)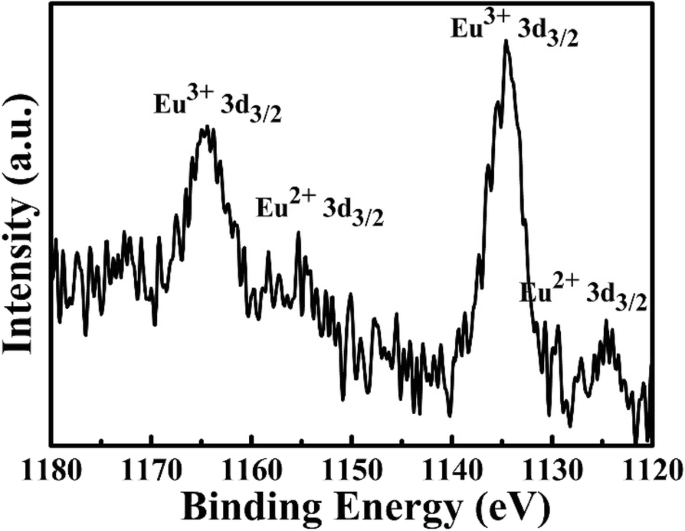
Spectre XPS pour l'élément Eu de la zéolite-3A :1,3 % en poids de phosphores Eu frittés à 1400 °C pendant 3 h
Ici, [Eu 3+ ][sub>K et [Eu 2+ ][sub>K représentent Eu 3+ et Eu 2+ substitution d'ions pour K + position des ions, respectivement; Oo représente la position d'un oxygène pour l'oxygène dans le cristal matriciel; et VK est la vacance de K + ion. L'exposant « * », « ** », « ′ » et « × » indiquent respectivement une charge positive, deux charges positives, une charge négative et l'électroneutralité. Pendant le frittage, Eu 3+ ion remplace K + position dans la zéolite. Pour garder le solde de charge, un Eu 3+ ion remplacera trois K + ions. Ainsi, deux défauts de vacance de K + ions (V K ′ ) et un défaut de Eu 3+ ion ([Eu 3+ ][sub>K ** ), qui porte une charge négative et deux charges positives en apparence, respectivement, créera dans la zéolite hôte (vu de l'équation (1)). Ensuite, la vacance V K ′ agira comme un donneur d'électrons (vu de l'équation (2)), et le [Eu 3+ ][sub>K ** le défaut est l'accepteur des électrons. A haute température, [Eu 3+ ][sub>K ** va capturer un électron de la vacance de K + ions (V K ′ ) et cet électron sera placé dans l'orbite 4f de l'ion Eu. Par conséquent, Eu 3+ l'ion est réduit à Eu 2+ et [Eu 3+ ][sub>K ** le défaut devient [Eu 2+ ][sub>K * défaut (vu de l'équation (3)). A cette époque, le poste de Eu 2+ ion est avec une charge positive apparente. [Eu 2+ ][sub>K * défaut attirerait l'électron négatif d'un autre K + vacance à l'entourage de lui-même et devient électroneutralité apparente [Eu 2+ ][sub>K × (montré dans l'équation (4)) [11, 21, 22, 37,38,39,40,41].
Il est suggéré que le cadre tétragonal tridimensionnel rigide de AlO4 et SiO4 peut entourer Eu 2+ ions et les isoler de l'oxygène, puis, Eu 2+ peut exister régulièrement dans nos luminophores de visée.
Pour optimiser la propriété de la zéolite-3A :1,3 % en poids de phosphore Eu et observer l'effet de l'élément Eu sur le PL, les spectres d'émission PL et l'intensité relative du PL pour différentes quantités stoechiométriques de zéolite-3A et d'Eu2 O3 sont illustrés à la Fig. 5. On peut voir sur la Fig. 5a que l'intensité d'émission de Eu 2+ augmente avec la concentration de dopage en Eu2 O3 passant de 0,9 à 1,3 %. Cependant, elle diminue avec l'augmentation continue de la concentration de dopant. On observe clairement que l'effet PL est le meilleur lorsque la concentration de dopage Eu est d'environ 1,3 %. On peut expliquer que plus Eu 2+ ions, les centres les plus luminescents. Lorsque la concentration de l'élément Eu est supérieure à 1,3%, la diminution de l'intensité PL peut être attribuée à l'extinction de la concentration, qui est principalement causée par le transfert d'énergie entre Eu 2+ ions. Lorsque la concentration d'Eu 2+ les ions augmentent, la distance entre Eu 2+ les ions seront courts, puis le transfert d'énergie augmentera [42,43,44]. La courbe à barres d'erreur de l'intensité relative de la PL en fonction de la concentration de dopage à l'Eu est illustrée à la figure 5b. Cela indique que la plage de changement d'intensité relative de PL pour chaque concentration d'Eu est petite, ce qui signifie que ces échantillons sont très reproductibles.
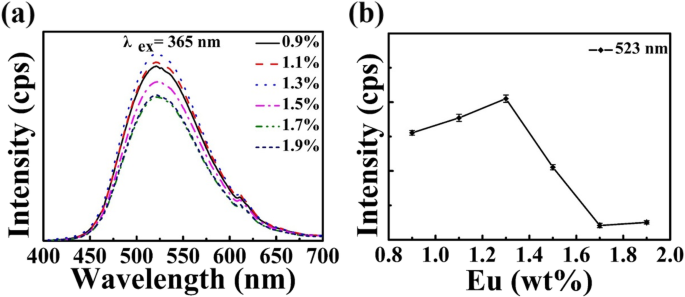
un Spectres d'émission PL et b l'intensité relative PL varie avec la concentration en élément Eu pour la zéolite-3A :1,3 % en poids de phosphore Eu (x = 0.9~1.9) fritté à 1400 °C pendant 3 h
Comme preuve d'application d'éclairage, la zéolite 3A émettant dans le vert :1,3 % en poids de phosphore Eu est encapsulée sur une puce émettant des UV pour fabriquer une LED verte. Le spectre d'émission EL à une tension de 3 V est illustré à la Fig. 6a. On peut constater que les pics d'émission de la puce émettant des UV et du phosphore émettant dans le vert sont situés respectivement à ~ 375 nm et ~ 523 nm. Et l'encart est la photographie d'une LED verte en fonctionnement qui émet une lumière verte brillante à une tension de 3 V. Les coordonnées de couleur (Fig. 6b) sont calculées pour être (0,295, 0,537) pour la LED verte résultante, indiquant une pureté de couleur verte supérieure.
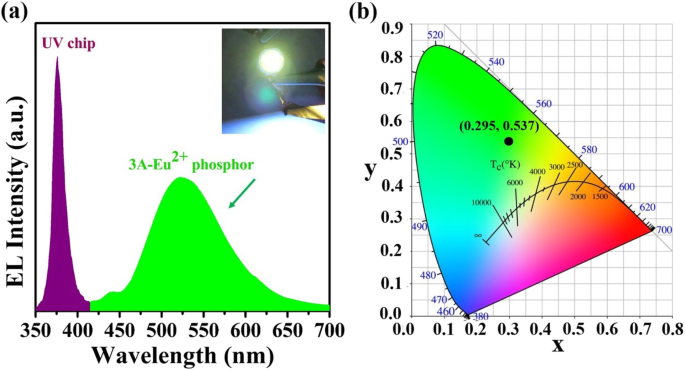
un Spectre d'émission d'électroluminescence à une tension de 3 V pour la zéolite-3A :1,3 % en poids de phosphore Eu fritté à 1400 °C pendant 3 h, et l'encart est une photographie d'une LED verte fonctionnant à une tension de 3 V. b Coordonnée de couleur dans le diagramme CIE1931
Conclusions
Dans ce travail, nous avons obtenu une zéolithe 3A d'émission verte brillante :Eu 2+ phosphore avec un rendement quantique d'environ 36,6% et le pic d'émission situé à 523 nm grâce à une méthode de réaction à haute température verte et écologique sans aucune atmosphère réductrice. De plus, l'échantillon a une large bande d'excitation dans la plage de 310 à 450 nm, ce qui peut correspondre à l'excitation de la puce UV commerciale (en fait, λ = 375 nm). Eu 2+ les ions peuvent être progressivement incorporés dans les réseaux hôtes de la zéolite à mesure que la température de calcination augmente. Nos recherches montrent que la température de frittage optimale est de 1400°C et que la meilleure concentration de dopage en ions Eu est de 1,3%. Exploitation de la zéolite 3A émettrice verte :Eu 2+ phosphore encapsulé sur une puce émettant des UV, une bonne LED verte avec des coordonnées de couleur de la Commission Internationale de L'Eclairage (CIE) à (0,295, 0,537) et une luminosité de 231,6 cd/m 2 Est obtenu. Et la zéolite-3A à émission verte :1,3 % en poids de phosphore Eu avec des propriétés luminescentes croissantes seront des applications prometteuses pour l'éclairage et l'affichage.
Disponibilité des données et des matériaux
Les ensembles de données soutenant les conclusions de cet article sont disponibles dans l'article.
Abréviations
- CIE :
-
Commission Internationale de L'Eclairage
- EL :
-
Électroluminescence
- UE :
-
Europium
- FESEM :
-
Microscope électronique à balayage à émission de champ
- LED :
-
Diode électroluminescente
- PL :
-
Photoluminescence
- PLE :
-
Excitation de photoluminescence
- RE :
-
Terre rare
- TG :
-
Analyse thermogravimétrique
- XPS :
-
Spectroscopie photoélectronique aux rayons X
- XRD :
-
Diffraction des rayons X
Nanomatériaux
- Logiciel de maintenance mobile et son rôle dans la création de flux de travail efficaces
- Élimination par adsorption des ions cuivre (II) d'une solution aqueuse à l'aide d'un nano-adsorbant de magnétite à partir de déchets de broyage :synthèse, caractérisation, adsorption et modél…
- Dopage de substitution pour les minéraux d'aluminosilicate et performances supérieures de fractionnement de l'eau
- Synthèse verte à un pot de microsphères de SnO2 décorées d'Ag :un catalyseur efficace et réutilisable pour la réduction du 4-nitrophénol
- Synthèse verte de points quantiques InP/ZnS Core/Shell pour une application dans des diodes électroluminescentes sans métaux lourds
- Préparation de nanosphères polymères à empreinte ionique de palladium(II) et son élimination du palladium(II) d'une solution aqueuse
- Saponines de Platycodon de Platycodi Radix (Platycodon grandiflorum) pour la synthèse verte de nanoparticules d'or et d'argent
- Diodes émettant de la lumière ultraviolette à base d'AlGaN presque efficace et sans chute avec une couche de blocage d'électrons de type p à super-réseau spécialement conçue pour une efficacit…
- Fabrication de nanofibres hélicoïdales CA/TPU et son analyse de mécanisme



