Influence de la modification de groupe aux bords des points quantiques de carbone sur les émissions fluorescentes
Résumé
Nous présentons une enquête détaillée sur l'effet de la modulation de groupe fonctionnel aux bords des points quantiques de carbone (CQD) sur la fluorescence des CQD. Les CQD attachés par les éléments N, S et P sont synthétisés par pyrolyse d'un mélange d'acide citrique et de NH3 H2 O, H2 SO4 , et H3 Bon de commande4 , respectivement. Ainsi, une partie de -COOH aux bords des CQD peut être convertie en -C=O et des groupes fonctionnels tels que -NH2 , –SO2 , –HSO3 , et –H2 Bon de commande4 peut se connecter aux liaisons carbone. Nous constatons que la formation des N/S/P-CQD peut réduire la quantité de -COOH qui s'attache aux bords de sp 2 -conjugué π -domaines situés au centre de ces CQD. Cet effet peut entraîner la réduction de la recombinaison non radiative pour la transition électronique dans ces CQD. En conséquence, le rendement quantique (QY) pour la fluorescence des CQD peut être efficacement amélioré. Nous démontrons expérimentalement que les QY pour les N/S/P-CQD peuvent atteindre jusqu'à 18,7 %, 29,7 % et 10,3 %, respectivement, par rapport à 9 % pour ceux-ci sans modulation de groupe fonctionnel. Ce travail peut fournir une approche expérimentale pratique pour améliorer les propriétés optiques des CQD fluorescents.
Contexte
Les points quantiques de carbone (CQD) sont des nanomatériaux émergents [1] dotés de propriétés fluorescentes supérieures [2] et de propriétés chimiques, électroniques et optiques uniques [3]. Contrairement aux molécules de colorant traditionnelles et aux points quantiques à base de semi-conducteurs, les CQD présentent non seulement une bonne résistance à la lumière et une résistance au blanchiment à la lumière par scintillation [4], mais également des caractéristiques importantes telles qu'une faible toxicité, une biocompatibilité, un faible coût, une photostabilité élevée [5 ], etc. Par conséquent, les CQD ont été proposés en tant que matériaux électroniques et optoélectroniques avancés pour des applications dans des domaines tels que les dispositifs optoélectroniques [6], la conversion d'énergie [7], la photocatalyse [8], les capteurs [9], la bio-imagerie [ 10], les marqueurs cellulaires [11, 12] et l'administration de médicaments [13], pour n'en citer que quelques-uns. Ces dernières années, l'investigation des CQD est devenue un domaine de recherche en pleine expansion et en pleine croissance dans les communautés scientifiques et industrielles.
À l'heure actuelle, la méthode expérimentale la plus couramment utilisée pour la synthèse chimique des CQD est une approche ascendante qui peut être appliquée pour produire des CQD fluorescents simplement, à moindre coût et en grande quantité. Dans cette méthode, de petites molécules de composés organiques ou de polymères sont prises comme sources de carbone et sont déshydratées et carbonisées pour réaliser les CQD. Lors de la préparation des CQD, la surface et le bord des CQD sont souvent attachés par certains groupes chimiques tels que OH, COOH, C=O, etc. La présence de ces groupes chimiques peut affecter grandement les propriétés électroniques et optiques des CQD. En particulier, les caractéristiques fluorescentes des CQD dépendent sensiblement de la présence de ces groupes [14]. D'un point de vue physique, les groupes chimiques attachés à la surface et au bord des CQD peuvent induire de nouveaux types d'états de surface et de bord dans les systèmes CQD et, ainsi, peuvent modifier la structure électronique et les canaux de transition électroniques et optiques correspondants dans le CQD. Dans ce cas, la photoluminescence (PL) des CQD peut être obtenue via une transition électronique entre les états de bord et les états de carbone tels que le conjugué π états (ou sp 2 région). Ainsi, le mécanisme de l'émission PL des CQD est très similaire à celui de l'émission de lumière photo-induite à partir d'états d'impuretés dans un semi-conducteur dopé [15] de la manière suivante :(i) les photons peuvent être absorbés via des transitions électroniques de et des états électroniques de carbone occupés à des états supérieurs et vides sous l'action du pompage optique, (ii) les électrons photo-excités peuvent être détendus dans les états électroniques dans les états de bord via des événements de transition électronique non radiatifs, et (iii) le PL l'émission peut être réalisée via des transitions électroniques des états de bord aux états électroniques à plus faible teneur en carbone accompagnées de l'émission de photons. Par conséquent, les états électroniques de bord jouent un rôle comme les états d'impuretés radiatives dans un semi-conducteur et les électrons peuvent être combinés avec les trous pour la luminescence. Généralement, le sp 2 -conjugué π -les domaines sont considérés comme les centres inhérents à l'émission de PL [16] et à la sp 2 aromatique la zone de carbone d'un CQD est entourée de sp 3 états du carbone (C-OH). Par conséquent, la recombinaison des paires électron-trou dans le sp 2 zone et les transitions électroniques entre le carbone et les états de bord peuvent favoriser l'émission de PL des CQD [17, 18].
Le rendement quantique de fluorescence (QY) est un paramètre clé pour mesurer l'efficacité de l'émission lumineuse photo-induite d'un matériau ou d'un dispositif, qui est définie par le nombre de photons émis par rapport au nombre de photons absorbés. Dans les premières années où les CQD ont été découverts, le QY pour les CQD préparés chimiquement était assez faible (même moins de 2 %) [1]. Comment améliorer le QY fluorescent pour les CQD a été un problème central pour la recherche fondamentale et pour l'application matérielle. En général, le QY pour les CQD réalisés chimiquement via une approche ascendante dépend du choix de la source de carbone, de la technique de synthèse et de la modulation de bord. Plus précisément, l'intensité et la fréquence de l'émission PL des CQD sont les conséquences des paramètres d'échantillon des CQD, la présence des groupes fonctionnels ou états de bord, l'interaction entre les états électroniques dans sp 2 -conjugué π -domaines et en groupes chimiques, et les propriétés du fluorophore dans les CQD [19]. Ces dernières années, le QY fluorescent pour les CQD a été largement amélioré [20]. En particulier, Lingam et al. ont examiné l'effet des états de bord induits dans la synthèse des CQD sur l'émission PL. Ils ont constaté que si les bords des CQD sont endommagés, l'émission de PL chute fortement pour être même incommensurable [21]. Un travail similaire de Kumar et al. a également démontré que la présence des états de bord est le facteur clé pour la PL des CQD, et l'origine de la PL hétérogène accordable est amino-fonctionnalisée pour les CQD [22]. Tang et al. ont rapporté une simple synthèse hydrothermale assistée par micro-ondes des CQD en utilisant le glucose comme seule source de carbone [23]. En prolongeant simplement le temps de réaction de 1 min à 9 min, ils ont pu ajuster la taille des CQD de 1,65 nm à 21 nm. Fait intéressant, ils ont constaté que le PL des CQD était indépendant de la taille des CQD, où les CQD avec les tailles de 9,6 nm et 20 nm montrent à peu près les mêmes comportements d'absorption et d'émission de lumière. Les résultats obtenus à partir des travaux de recherche ultérieurs de Lin et al. indiquent également que l'émission PL des CQD dépend faiblement de l'effet du confinement quantique de la sp 2 -conjugué π -domaines [24] et la présence des groupes fonctionnels de surface attachés aux CQD est le facteur clé pour l'émission de PL. Dong et al. réalisé les CQD fluorescents bleus avec les nanofeuillets en forme de disque (la taille de 15 nm et l'épaisseur de 0,5 à 2,0 nm) en ajustant le degré de carbonatation de l'acide citrique. Ils ont constaté que le PL des CQD est indépendant de la longueur d'onde d'excitation et que le QY fluorescent peut aller jusqu'à 9,0 % [25]. Il est à noter que selon la relation entre la taille d'un CQD et la longueur d'onde de l'émission PL pour un CQD nu [26], les CQD avec la taille d'environ 2,25 nm peuvent émettre la fluorescence bleue, tandis que les CQD avec le taille de 15 nm ne peut émettre qu'une fluorescence de longueur d'onde plus longue. L'émission de PL bleu intense des CQD d'une taille de 15 nm [25] suggère une fois de plus que la présence des états de bord induits par les groupes chimiques attachés aux CQD est principalement responsable de l'émission de PL des CQD. Par conséquent, la fonctionnalité de bord des CQD peut affecter non seulement la fluorescence des CQD, mais aussi les propriétés physiques et chimiques des CQD en général [19].
Il convient de noter qu'à l'heure actuelle, la fréquence de l'émission fluorescente des CQD ne peut pas être facilement contrôlée et modifiée artificiellement. De plus, le QY fluorescent correspondant n'a pas encore atteint les exigences pour l'application en tant que dispositifs pratiques. Les résultats obtenus à partir de recherches expérimentales [27,28,29] et théoriques [30, 33] ont confirmé que la passivation des bords peut améliorer efficacement les propriétés optiques électroniques des CQD. Les agents de passivation sont largement utilisés pour ajuster les propriétés fluorescentes des CQD [21,22,23]. Jing Liu et al. ont développé une préparation en une étape de points quantiques de carbone dopés à l'azote et passivés en surface [27]. Ils ont constaté que le QY des CQD sans passivation de surface est généralement assez faible (QY < 10%), les CQD passivés montrent un QY de 37,4%. Un travail similaire de Shen et al. ont étudié les CQD passivés au PEG ont un QY de 28 % [28], et Kwon et al. ont rapporté que l'hexadécylamine (HDA)-passivée donne 19-35% [29]. Dimos et ses collègues ont également découvert que la passivation des bords peut induire efficacement les électrons dans la bande de conduction et augmenter l'énergie de surface des CQD pour empêcher la décroissance de la fluorescence ou l'extinction causée par l'agrégation des CQD [30]. De plus, la génération de fluorescence à partir de CQD fabriqués par réaction chimique ou approche ascendante est principalement induite par la présence des groupes fonctionnels radiatifs ou fluorophore attachés au bord des CQD [31]. Chimiquement, ces groupes fonctionnels peuvent être modifiés en plaçant les CQD dans différentes solutions chimiques. La fluorescence de ces CQD chimiquement modifiées peut être obtenue via l'émission excitonique accompagnée d'une recombinaison électronique et d'une séparation de paires électron-trou piégées sur le bord des CQD [32]. Ainsi, la fréquence de l'émission PL peut être réglée en sélectionnant différents groupes de bords pour former les états de bord requis.
La principale motivation de cette étude est d'explorer comment les propriétés fluorescentes des CQD peuvent être modifiées dans différentes solutions chimiques pour leur passivation ou leur fonctionnalité de bord. Récemment, nous avions produit des CQD à partir d'eaux usées de tofu sans ajout de substances toxiques et révélé le mécanisme de luminescence [33]. Nous avons constaté que différentes couleurs de l'émission fluorescente de ces CQD peuvent être obtenues en mettant ces matériaux de points dans de l'eau ou dans une solution de NaOH [33]. Nous avions également fabriqué les CQD à partir de jus de citron frais et les avions appliqués à l'imagerie cellulaire [34]. Il a été constaté que la présence de groupes contenant de l'oxygène sur la surface et le bord des CQD est principalement responsable de la fluorescence des CQD [34]. Notre attention de la présente étude se concentre principalement sur la façon d'obtenir un moyen efficace d'améliorer le rendement quantique de la fluorescence des CQD.
Méthode
Synthèse des N-, S- et P-CQD
Dans ce travail, l'acide citrique (C6 H8 O7 , 99,5 %), hydroxyde de sodium (NaOH, 96 %), solution d'ammoniaque (NH3 H2 O, 25-28%), solution d'acide sulfurique (H2 SO4 , 98%), solution d'acide phosphorique (H3 Bon de commande4 , 85 %), et de l'eau déminéralisée ont été utilisées pour fabriquer les CQD et pour modifier les états de bord.
Les B-CQD ont été synthétisés par pyrolyse d'acide citrique comme seule source de carbone. Les N/S/P-CQD ont été fabriqués par pyrolyse d'ammoniac, d'acide sulfurique et d'acide phosphorique avec de l'acide citrique, respectivement. Le principe et les processus expérimentaux pour la réalisation des CQD et des N/S/P-CQD correspondants sont illustrés à la Fig. 1. Grâce à la pyrolyse de l'acide citrique, les B-CQD peuvent être fabriqués par déshydratation intermoléculaire, carbonisation , et réaction de condensation. Cette approche peut former (i) la structure aromatique (à savoir le sp 2 états carbonés avec liaisons C-C et C=C) avec une zone conjuguée comme noyau des CQD, (ii) les bords des CQD attachés par hydroxyle (OH) et carboxyle (COOH/–O–C=O), et (iii) le sp 3 zone de carbone (C–C–OH/–C–O) qui peut être passivée dans, par exemple, une solution de NaOH. Les N-CQD peuvent être obtenus via un procédé de pyrolyse de la solution mixte d'acide citrique et de NH3 H2 O. Dans un tel cas, la réaction de déshydrogénation entre les groupes adjacents avec le carboxyle peut favoriser la formation de N pyrrolique dans le squelette de graphène des CQD. Les bords des N-CQD sont ensuite attachés avec des groupes chimiques supplémentaires tels que -C-N et -NH2 [35]. Semblable à la réalisation des N-CQD, les S-CQD et les P-CQD peuvent être fabriqués via la pyrolyse de la solution mixte d'acide citrique et de H2 SO4 et H3 Bon de commande4 , respectivement. La déshydratation intermoléculaire, la carbonisation et la réaction de condensation peuvent former le squelette de graphène des CQD avec la connexion à des groupes chimiques tels que -SO2 , –HSO3 , et –H2 Bon de commande4 . De plus, les atomes S et P sont susceptibles de s'attacher au bord de sp 2 zone de conjugué de carbone pour former les défauts de bord. Les structures matérielles des N/S/P-CQD sont présentées sur la figure 1. Dans la présente étude, les N/S/P-CQD sont dispersés dans une solution de NaOH à température ambiante pour les rendre passivables. Ainsi, nous pouvons convertir une partie du –COOH au bord des CQD en –COONa et réduire la quantité de –COOH au bord de sp 2 -conjugué π -domaines. Par conséquent, la modification de groupe au bord des CQD peut être réalisée.
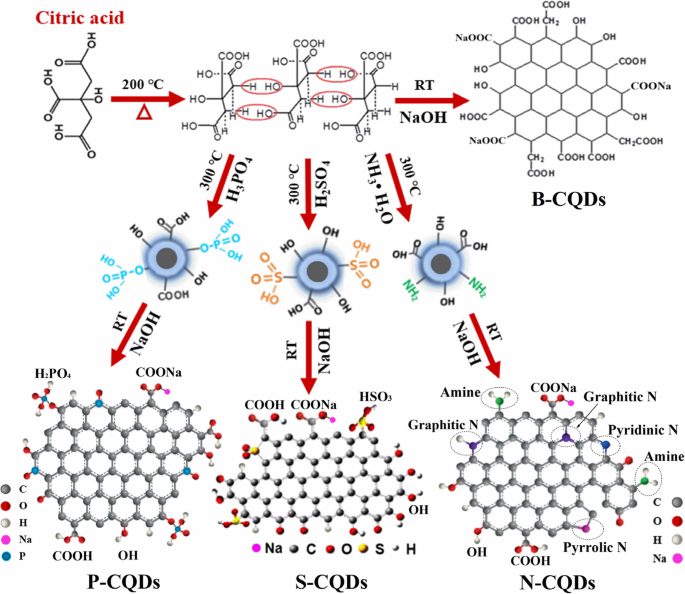
Processus de synthèse schématique des CQD et des structures N-, S- et P-CQD correspondantes
Plus précisément, les N/S/P-CQD fluorescents sont préparés de la manière suivante :(i) 2 g d'acide citrique analytiquement pur ont été ajoutés dans 60 ml de NH3 H2 O (pH = 7,5), 60 ml H2 SO4 (pH = 3), et 60 ml H3 Bon de commande4 (pH = 3), respectivement. (ii) Nous plaçons la solution mélangée sur la plate-forme de chauffage pour un chauffage constant à 300 °C, où le temps de chauffage est de 20 à 30 min. (iii) 50 ml de solution d'hydroxyde de sodium (NaOH) sont ajoutés dans le bécher après le refroidissement naturel du bécher jusqu'à la température ambiante. (iv) Le mélange est agité magnétiquement pendant 10 min et soumis à un choc ultrasonique pendant 10 min et encore centrifugé à une vitesse de 12 000 r/min pendant 10 à 30 min. Ensuite, le surnageant est prélevé, dans lequel les N/S/P-CQD modifiés par des solutions d'ammoniac, d'acide sulfurique et d'acide phosphorique, respectivement, et passivés par des groupes tels que -OH, -COOH, -C=O, -COONa, –NH2 , –SO2 , –HSO3 , et –H2 Bon de commande4 peut être obtenu dans des solutions de NaOH. Dans la préparation des N/S/P-CQD, sauf que les N/S/P-CQD ont été modifiés par NH3 H2 O, H2 SO4 , et H3 Bon de commande4 , respectivement, les autres conditions expérimentales étaient à peu près les mêmes. Nous avons utilisé la même quantité d'acide citrique pour se dissoudre dans NH3 H2 O, H2 SO4 , et H3 Bon de commande4 , respectivement, pour la pyrolyse, puis ajouté la même quantité et la même concentration de solution d'hydroxyde de sodium lorsque les substances dans le bécher étaient presque sèches. Cela peut garantir que la densité des CQD dans la solution de NaOH est presque la même.
Mesures
Dans ce travail, la morphologie et la microstructure des CQD ont été observées en utilisant la microscopie électronique à transmission (TEM, JEM 2100) à une tension d'accélération de 300 kV. La spectroscopie photoélectronique à rayons X (XPS) a été appliquée pour caractériser les échantillons, en utilisant le spectromètre photoélectronique PHI5000 Versa Probe II avec Al Kα à 1486,6 eV. Le spectre d'absorption ultraviolet-visible (UV-Vis) des CQD a été mesuré par un spectrophotomètre UV-Vis (Specord200, Allemagne). L'émission de PL des CQD a été mesurée à l'aide d'un système PL standard (IHR320, Jobin Yvon, USA) à température ambiante. Le QY fluorescent des CQD est évalué sur la base des données PL.
Résultats et discussions
La caractérisation des échantillons
La morphologie et les structures des CQD tels que synthétisés ont été étudiées par MET. La figure 2 montre les images MET (a) et les distributions de diamètre (b) des S-CQD. On peut clairement voir que les S-CQD sont des feuilles de type circulaire et sont dispersées uniformément dans une solution de NaOH. Grâce à une moyenne statistique des images MET pour les CQD, nous constatons que la distribution de la taille des S-CQD est principalement située dans la plage de 3 à 8 nm et que la taille moyenne des CQD est d'environ 5,73 nm. Ces résultats sont obtenus par analyse statistique de plus de 300 particules CQD à l'aide de l'Image J Logiciel. Les résultats présentés sur la figure 2c indiquent que ces S-CQD sont hautement cristallisés avec une structure de réseau typique de carbone. Les franges de réseau des CQD sont claires et l'espacement de réseau correspondant est d'environ 0,215 nm compatible avec la facette (100) du graphène [32].
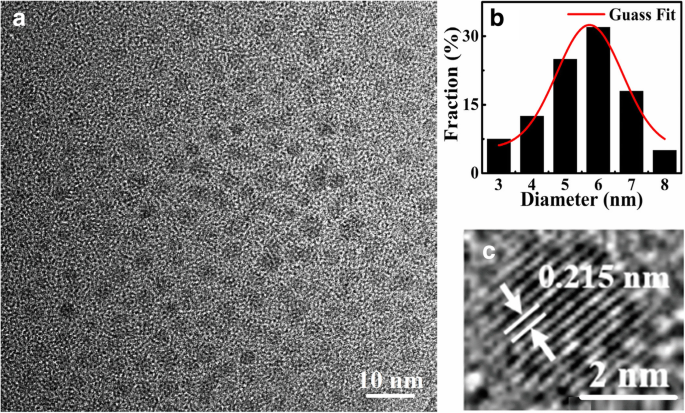
Images MET de S-CQD dans une solution de NaOH (pH = 12) dans a et leurs franges en treillis en c . La distribution des diamètres des S-CQD est indiquée dans b
Dans la présente étude, nous appliquons la spectroscopie photoélectronique aux rayons X (XPS) pour la mesure et l'examen des groupes fonctionnels de bord attachés aux CQD. Nous utilisons des feuilles de verre comme substrats et enduisons les échantillons sur les feuilles de verre pour les mesures. Sur la figure 3, nous montrons les spectres XPS pour les N-, S- et P-CQD. Comme le montre la figure 3a, le spectre XPS à balayage complet pour les N-CQD indique que le pourcentage atomique de N1 est de 9,6 %. Les figures 3 b et c indiquent que (i) les S- et P-CQD présentent des pics de réponse pour les S2 (à 169 eV) et les P2 (à 133 eV), respectivement, contrairement aux CQD préparés sans modification de groupe fonctionnel et (ii) les pourcentages atomiques de S2 pour les S-CQD et de P2p pour les P-CQD sont respectivement de 2,7% et 0,6%. La principale raison pour laquelle la teneur en P dans les P-CQD est inférieure à la teneur en S dans les S-CQD est que P a un rayon atomique relativement plus grand (le nombre de protons des noyaux est de 15) que S (le nombre de protons des noyaux est de 16). Ainsi, les atomes P sont relativement moins susceptibles d'être absorbés par les liaisons chimiques à la surface des CQD que les atomes S. En comparaison avec la Fig. 3a et c pour les spectres XPS pour les N- et P-CQD, la Fig. 3b montre que le pourcentage d'atomes C1s dans les S-CQD est beaucoup plus élevé (76,9%) et les proportions d'atomes O1s ( 20,2%) et les atomes d'impuretés (S, Na) sont très faibles. Ces résultats indiquent qu'il y a moins de défauts dans le sp 2 zone de carbone dans les S-CQD. La Fig. 3d montre que les spectres haute résolution de C1 présentent trois pics typiques, respectivement, à 284,8 eV, 286,6 eV et 288,5 eV pour les N-CQD, ce qui indique que le sp 2 la zone de carbone (C–C/C=C) a une bonne structure réticulaire [14, 25, 36]. De plus, sp 3 le carbone (C–O/C–N, 286,4 eV) et le carboxyle (O–C=O/COOH, 288,1 eV) ont une énergie de liaison similaire [33], ce qui suggère qu'il existe des quantités similaires d'hydroxyle (C–O/C– OH) et carboxyle (O–C=O/COOH) autour du sp 2 zone de carbone. Les spectres haute résolution correspondants des C1 pour les S- et P-CQD sont illustrés à la Fig. 3 e et f. Comme le montre la figure 3e, le pic de sp 3 le carbone (C-O) est très fort et le pic d'hydroxyle (O-C=O/COOH) est faible pour les S-CQD, indiquant que la quantité d'hydroxyle (C-O/C-OH) est beaucoup plus élevée que le carboxyle (O–C=O/COOH) autour du sp 2 zone de carbone pour les S-CQD. De plus, la figure 3 h indique que la quantité d'hydroxyle (C–O/C–OH) est inférieure à celle de carboxyle (O–C=O/COOH) autour de la sp 2 zone de carbone pour les P-CQD. En comparant avec la Fig. 3 d, e et f, nous constatons que le pic des hydroxyles (C–O/C–OH) est le plus fort tandis que le pic des hydroxyles (O–C=O/COOH) est le plus faible pour les S-CQD. Lorsque la quantité de groupes hydroxyle est augmentée, la quantité de groupes carboxyle est réduite, et vice versa, lorsque la quantité de groupes carboxyle est augmentée, la quantité de groupes hydroxyle est diminuée.
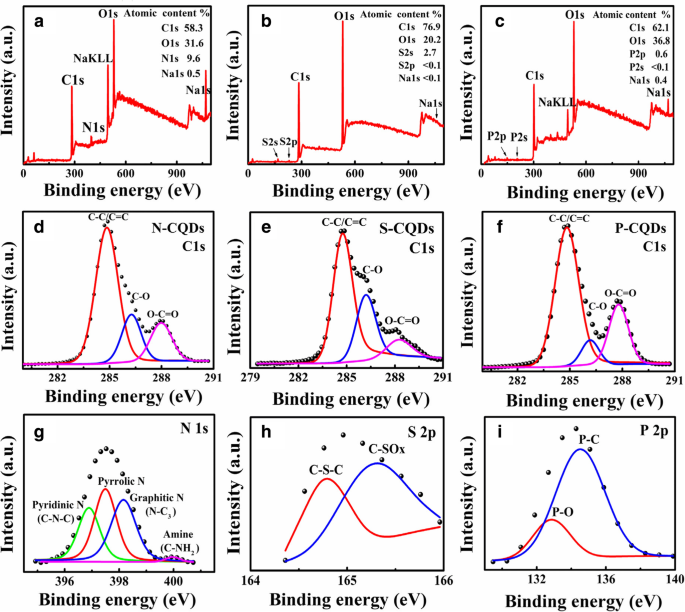
Les spectres XPS à balayage complet dans a /b /c et les spectres haute résolution des C1 en d /e /f et N1 s/S2p/P2p dans g /h /je pour respectivement les N/S/P-CQD
Sur la figure 3 g, les spectres haute résolution des N1 montrent quatre pics liés à l'azote pyridinique (N pyridinique, 396,9 eV), l'azote pyrrolique (N pyrrolique, 397,6 eV), l'azote du graphite (N–C3 , 398.5 eV, situé au centre de sp 2 carbone) et le groupe amide (C–NH2 , 399.9 eV, situé au bord de sp 2 carbone), respectivement [22, 37, 38, 39]. Ces résultats vérifient la structure matérielle des N-CQD illustrée à la Fig. 1. Dans les N-CQD, les fluorophores sont formés par l'hybridation de groupes fonctionnels de bord tels que C-OH et C-NH2 avec sp 2 -conjugué π -domaines [40], qui peuvent jouer un rôle dans l'amélioration de la fluorescence des N-CQD. Le spectre haute résolution des S2 et P2p correspondant aux résultats XPS pour les S- et P-CQD est illustré sur la Fig. 3 h et i, cela implique que les bords des S-CQD et P-CQD sont liés par des liaisons chimiques telles que comme C–S–C (164,8 eV) [41], C–SOX (X = 2, 3, 4, 165,1 eV) [42], P–C (135,0 eV) [43] et P–O (132,7 eV) [44]. Ainsi, les liaisons chimiques telles que C–SO2 , –HSO3 , C–P–C, –H2 Bon de commande4 , etc. peuvent être formés sur les bords des S- et P-CQD, comme le montre la figure 1.
La figure 4 montre les spectres d'absorption et d'émission mesurés à partir des B- et N/S/P-CQD dans des solutions de NaOH. Les spectres d'absorption UV-Vis des B/N/S/P-CQD sont illustrés à la Fig. 4a. Le spectre d'absorption des B-CQD présente des pics d'absorption UV à 278 nm, tandis que le spectre d'absorption UV-Vis des N-, S- et P-CQD représente deux bandes d'absorption claires. Le pic d'absorption à 253 nm est attribué à π –π * transition de la liaison aromatique C=C et l'épaulement à 302 nm correspond à n –π * transition de la liaison C=O [40]. Les liaisons C=C proviennent de sp 2 -domaines conjugués dans les noyaux des N/S/P-CQD, tandis que les liaisons C=O proviennent des nombreux groupes électroattracteurs contenant de l'oxygène tels que les groupes carboxyle et carbonyle existant aux bords des N/S/P-CQD . Les deux pics d'absorption révèlent l'existence de sp 2 -structures conjuguées et groupes fonctionnels contenant de l'oxygène (C=O et O–C=O/COOH) dans les N-, S- et P-CQD.
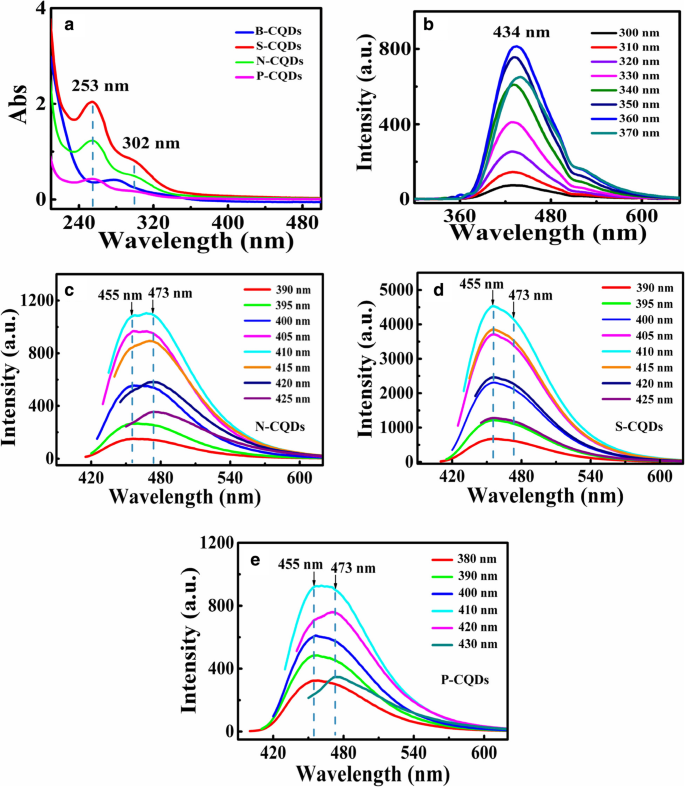
Les spectres d'absorption UV-Vis par B- et N/S/P-CQD en a . Les spectres PL de b B-CQD, c N-CQD, d S-CQD et e P-CQD avec différentes longueurs d'onde d'excitation comme indiqué. Ces résultats sont obtenus à température ambiante
La figure 4 b–e montre les spectres PL des B- et N/S/P-CQD. Comme on peut le voir, la forte émission de PL peut être observée dans ces CQD. Nous constatons que l'intensité de l'émission PL augmente d'abord puis diminue avec l'augmentation de la longueur d'onde d'excitation. Cet effet a été trouvé dans la plupart des matériaux nanostructurés (voir, par exemple, Réf. [45]). Comme l'a souligné la Réf. [38], la dépendance de l'intensité de l'émission PL sur l'excitation pour les CQD est principalement due aux états de surface hétérogènes et aux tailles et propriétés électroniques des hétéroatomes. Pour le cas des CQD à modulation de groupe de surface, la présence des états de surface peut altérer la bande interdite et les états d'énergie radiative des CQD. Sous une excitation de longueur d'onde relativement plus courte, les électrons sont pompés dans des états d'énergie plus élevés dans une bande de conduction plus éloignée des états électroniques radiatifs induits par la modulation de surface. Ainsi, la possibilité d'émission de photons à partir des CQD est réduite par une excitation de longueur d'onde plus courte. A savoir, l'intensité de l'émission PL augmente avec la longueur d'onde d'excitation dans un régime de longueur d'onde plus courte. Dans un régime de longueur d'onde relativement longue, une excitation de longueur d'onde plus longue implique que relativement moins d'électrons peuvent être pompés dans la bande de conduction dans les CQD. En conséquence, l'intensité de l'émission PL diminue avec l'augmentation de la longueur d'onde d'excitation dans un régime de longueur d'onde d'excitation longue. De plus, les émissions PL des N/S/P-CQD consistent en deux bandes spectrales qui se chevauchent [25]. Les doubles pics PL peuvent être mesurés respectivement à environ 455 nm et 473 nm via une excitation de longueur d'onde de 410 nm. Ceci est une conséquence des émissions PL des N/S/P-CQD modifiées par différents groupes fonctionnels pour affecter la recombinaison radiative des paires électron-trou (e-h) formées par sp 2 -conjugué π -domaines et groupes d'états périphériques [32, 40]. Le mécanisme possible proposé ici est que (i) la photo-excitation des électrons dans les N/S/P-CQD est réalisée via π –π * transitions de sp 2 -conjugué π -domaines à n –π * transitions, (ii) les électrons sont relaxés de n –π * états aux niveaux d'énergie C=O via des canaux de transition non radiatifs, et (iii) la recombinaison radiative pour les trous dans sp 2 discrets -les états apparentés et les électrons dans les états de bord peuvent être induits par des groupes fonctionnels abondants [46].
Sur la figure 4 b–e, dans les mêmes conditions expérimentales, nous constatons que l'intensité de fluorescence des N/P/S-CQD était significativement plus élevée que celle des B-CQD. L'intensité des émissions de PL des S-CQD est la plus forte, suivie des N-CQD, et l'émission de PL des P-CQD est la plus faible. Ce résultat correspond aux résultats montrés dans les spectres haute résolution des C1 pour les N/S/P-CQD (voir Fig. 3d, e, f). L'intensité de l'émission PL augmente avec l'augmentation de la hauteur du pic de C–O (C–OH) et avec la diminution de la hauteur du pic de O–C=O (COOH). Par conséquent, il est raisonnable de croire que les N/S/P-CQD avec divers groupes de bords, tels que C-OH, COOH, C=O et C-H, peuvent induire différents types d'états de bord et influencer l'intensité de ses photoluminescence. Plus intéressant encore, nous constatons que les positions de pic pour l'émission PL des N/S/P-CQD dépendent de la longueur d'onde d'excitation, ce qui implique que les états électroniques radiatifs induits par les groupes fonctionnels attachés aux bords des CQD sont assez stables.
Comme mentionné ci-dessus, sp 2 la zone de carbone des S-CQD a moins de défauts, de sorte que l'émission de lumière inhérente des S-CQD est la plus forte, par rapport aux N- et P-CQD. Après avoir utilisé la formule d'évaluation du rendement quantique de fluorescence [33], nous obtenons que les QY pour les N/S/P-CQD sont respectivement de 18,7 %, 29,7 % et 10,3 %. Ainsi, le plus grand QY peut être atteint pour les S-CQD, suivis des N- et P-CQD. Comme nous le savons, le QY des CQD est une conséquence du processus concurrentiel entre la transition électronique radiative et les pièges non radiatifs [32]. L'hydroxyle (C–O/C–OH) aux bords des CQD peut être hybridé en synergie avec les états électroniques dans sp 2 -conjugué π -domaines pour former les fluorophores, tandis que ceux carboxyle (-COOH) peuvent jouer un rôle comme centre de recombinaison non radiative au bord des CQDs [40]. Par conséquent, le QY des CQD est affecté par les groupes C–O/C–OH et O–C=O/COOH. De plus, nous constatons que l'utilisation d'acide sulfurique pour la modification des groupes fonctionnels au bord des S-CQD peut affecter de manière significative l'amélioration de l'émission de PL des S-CQD, par rapport aux N- et P-CQD. Le QY de 29,7 % pour les S-CQD, réalisé dans cette étude, est supérieur à 18,7 % pour les N-CQD, à 10,3 % pour les P-CQD et à 9 % pour les CQD [23] préparés sans ammoniaque, acide sulfurique ou acide phosphorique .
Dans ce travail, les N/S/P-CQD sont synthétisés par pyrolyse de ces mélanges d'acide citrique et de NH3 H2 O, H2 SO4 , et H3 Bon de commande4 , ensuite dispersé dans les solutions de NaOH. Il peut favoriser la déshydratation intermoléculaire, la carbonisation et la réaction de condensation de l'acide citrique. Le carboxyle (-COOH) aux bords des CQD peut être converti en carbonyle (-C=O) [19], et les bords des N/S/P-CQD peuvent être attachés par des groupes chimiques tels que -OH, -COOH , –C=O, –NH2 , –SO2 , –HSO3 , et –H2 Bon de commande4 . Par conséquent, la formation des N/S/P-CQD peut réduire la quantité de -COOH attachée aux bords de sp 2 -conjugué π -domaines et peut entraîner la réduction de la recombinaison non radiative [47]. Par conséquent, le QY fluorescent des CQD peut être efficacement amélioré.
Conclusions
Dans cette étude, nous avons développé une méthode expérimentale efficace pour améliorer le rendement quantique fluorescent des CQD. Les N/S/P-CQD ont été synthétisés par pyrolyse d'acide citrique et en utilisant, respectivement, de l'ammoniac, de l'acide sulfurique et de l'acide phosphorique pour les modifications des groupes marginaux. Les résultats ont montré que la présence des groupes fonctionnels de bord peut jouer un rôle important dans la génération et l'amélioration de la fluorescence de ces CQD. En particulier, les groupes hydroxyle (C–O/C–OH) aux bords de sp 2 -conjugué π -domaines peuvent affecter de manière significative les rendements quantiques fluorescents des CQD. Néanmoins, l'attachement des groupes carboxyle (O–C=O/–COOH) aux bords de sp 2 -conjugué π -domains conduit principalement à des centres de recombinaison non radiatifs, ce qui peut affaiblir l'émission PL des CQD. Dans la présente étude, les QY pour les N/S/P-CQD peuvent atteindre jusqu'à 18,7 %, 29,7 % et 10,3 %, respectivement. Ces valeurs sont bien supérieures à celle de 9 % pour les CQD préparés sans modification de groupe fonctionnel. La conclusion la plus importante que nous tirons de cette étude est que la modification de groupe aux bords des CQD par l'acide sulfurique peut affecter fortement l'émission de fluorescence et le QY des CQD.
Disponibilité des données et des matériaux
Les ensembles de données générés et/ou analysés au cours de la présente étude sont disponibles auprès des auteurs correspondants sur demande raisonnable.
Abréviations
- CQD :
-
Points quantiques de carbone
- PL :
-
Photoluminescence
- QY :
-
Rendement quantique
- TEM :
-
Microscope électronique à transmission
- UV-Vis :
-
Ultraviolet visible
- XPS :
-
Spectroscopie photoélectronique aux rayons X
- XRD :
-
Diffraction des rayons X
Nanomatériaux
- Les nanotubes de carbone repoussent les limites de l'électronique flexible
- Ocean Carbon imagé à l'échelle atomique
- Coût de la fibre de carbone :facteurs qui influencent le plus
- N,N-diméthylformamide régulant la fluorescence des points quantiques MXene pour la détermination sensible de Fe3+
- Dévoilement de la structure atomique et électronique des nanofibres de carbone empilées
- La conception de la couche d'émission pour les multiplicateurs d'électrons
- Synthèse de points quantiques de carbone co-dopés en pyridinique N, S en tant qu'imitateurs d'enzymes efficaces
- Points quantiques de bismuth dans des puits quantiques recuits GaAsBi/AlAs
- Défauts à la surface du nanophosphore MgAl2O4 dopé Ti



