Défauts à la surface du nanophosphore MgAl2O4 dopé Ti
Résumé
Nano MgAl dopé Ti2 O4 pour l'émission blanche a été synthétisé par la méthode de combustion. Défauts Schottky extrinsèques, lacunes Al et Ti 4+ dopant dans les sites Al, qui sont considérés comme responsables de l'émission blanc bleuté, ont été observés par STEM sur la surface de nano MgAl2 dopé Ti O4 poudre. Les stabilités du défaut Schottky associent, (TiAl · –VAl ′′′)′′, ont été démontrés par calcul DFT. Le comportement d'émission a été interprété avec ces résultats.
Contexte
La transition du domaine de la masse ou du micron au domaine nanométrique affecte grandement un matériau, altérant, par exemple, ses propriétés mécaniques, optiques et électriques [1,2,3,4,5,6]. Ces changements sont principalement attribués à la taille et à la structure de non-équilibre associée. Un exemple est les propriétés uniques de phosphorescence et d'émission pouvant être obtenues par les nanoparticules [2, 7]. Les propriétés d'émission des nanophosphores peuvent être modulées par dopage, en plus des effets de confinement quantique décrits [8, 9]. La valence de charge d'un dopant et le site dans la structure qu'il occupe affectent généralement les propriétés d'émission d'un luminophore. Les dopants peuvent souvent être situés dans un nanophosphore à des sites (par exemple, sur la surface d'une particule) autres que les sites habituels dans un phosphore de la taille d'un micron. Ainsi, les surfaces des nanoparticules deviennent des sites importants pour les dopants qui n'occupent normalement pas de tels sites dans les systèmes en vrac ou micrométriques. Les changements dans le comportement d'émission ont été signalés en raison du site d'occupation, qui est associé à d'autres défauts [8, 9].
MgAl pur2 O4 a un défaut intrinsèque d'un Mg 2+ poste vacant, VMg , qui est le centre d'une émission rouge à 720 nm. Une forte émission bleue est observée à partir de monocristaux de MgAl2 dopé Ti O4; la disparition de l'émission rouge est attribuée à la compensation de charge par l'ajout de Ti 4+ [10, 11]. Cependant, dans nos travaux précédents, nous avons constaté que du MgAl2 dopé au Ti de la taille du micron O4 la poudre traitée thermiquement dans l'air a produit une émission blanche [12]. La différence s'expliquait par l'apparition d'émissions rouges et vertes en plus du bleu observé à partir de MgAl dopé Ti2 O4 monocristaux. Nos travaux antérieurs [12] ont également simulé le mécanisme de l'émission rouge via l'association intrinsèque du défaut de Schottky, (VO ·· –VMg ) x . Le présent travail rapporte l'observation visuelle de défauts Schottky extrinsèques à la surface de MgAl dopé Ti2 O4 nanopoudre et la relie à la différence des spectres d'émission entre les systèmes micron et nano.
Méthodes
Mg(NON3 )2 ·6H2 O (Nitrate de Mg ; 2,46 g, Aldrich), Al(NO3 )3 ·9H2 O (nitrate d'Al ; 7,246 g, Aldrich), CO(NH2 )2 (urée ; 5,231 g, Aldrich) et C10 H14 O5 Ti (Ti oxy-acétyl-acétonate ; 0,1 g, Aldrich) ont été utilisés comme matériaux de départ pour la synthèse de nano MgAl2 dopé Ti O4 . Le nitrate de magnésium et le nitrate d'Al ont été utilisés dans un rapport molaire de 1:2 dans la synthèse, et un dopage à 2 % en mole de Ti a été fourni par l'oxy-acétyl-acétonate de Ti. Les matières de départ ont été dissoutes dans de l'eau désionisée et le mélange a été homogénéisé par agitation, avant que l'eau ne soit évaporée sur une plaque chauffante. Le mélange restant a été placé dans un creuset en alumine et cuit à 500 pendant 1 h à l'air.
Les phases de la nanopoudre synthétisée ont été analysées par diffractométrie aux rayons X (XRD ; Rigaku) et les propriétés de photoluminescence ont été mesurées par spectrophotométrie de fluorescence (PSI, système PL Darsa pro-5000) en utilisant une lumière monochromatée à 260 et 360 nm provenant d'une lampe Xe. La morphologie et la taille de la poudre ont été observées par microscopie électronique à transmission à haute résolution (MET; JEOL, JEM-2100F). Des images du dopant Ti et des lacunes d'Al ont également été obtenues par balayage MET haute résolution (HR-STEM ; JEOL, JEM-2100F).
Les premiers calculs de la théorie fonctionnelle de la densité (DFT) ont été effectués sur la base de l'approximation du gradient généralisé de Perdew-Burke-Ernzerhof et des pseudopotentiels d'ondes planes augmentées par projecteur mis en œuvre dans le package de simulation ab initio de Vienne (VASP) [13,14,15] avec un coupure d'énergie de 500 eV et convergence de champ d'auto-cohérence de 10 −5 eV. Les stabilités de divers défauts associés ont été examinées par calcul pour étudier leur dépendance vis-à-vis des positions des dopants et des lacunes et des distances relatives entre eux.
L'énergie de surface du plan de surface (100) dans le MgAl2 O4 le cristal a été calculé; sa variation avec le site Ti a également été examinée. La cellule unitaire, dont la structure cristalline était précédemment optimisée pour permettre une relaxation complète du paramètre de réseau, de la forme cristalline et des positions atomiques, a été étendue à une supercellule 4 × 1. {100} surfaces ont été créées en insérant une plaque à vide à l'intérieur de la supercellule. La position d'insertion de la plaque sous vide qui est de la taille de 2 x 1 supercellule a été modifiée pour examiner le changement de l'énergie de formation de surface avec la distance entre la surface et le dopant Ti. La terminaison de surface avec 50% de couche de Mg a été principalement considérée car il s'est avéré que c'était la surface la plus stable (1 0 0) de MgAl2 O4 .
Résultats et discussion
La figure 1 montre le modèle XRD pour le MgAl dopé Ti2 O4 nano phosphores avec des graphiques TEM. La figure 1a confirme clairement que MgAl2 O4 a été synthétisé à 500 °C par la méthode de combustion, étant donné sa similitude avec le modèle JCPDS XRD pour le MgAl2 pur O4 . Les pics larges indiquent la présence de nanocristallites et sont liés aux particules de < 20 nm illustrées sur la figure 1b. En revanche, le MgAl2 de taille micronique dopé Ti O4 de nos travaux antérieurs [12] montre une cristallinité élevée, attribuée au traitement à haute température du MgAl2 O4 poudre (1300 °C pendant 2 h).
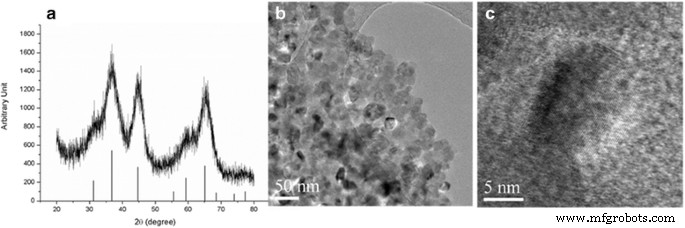
un Modèle XRD pour nano MgAl2 dopé Ti O4 poudre synthétisée à 500 °C 1 h avec des pics de référence de MgAl2 O4 de JCPDS et b , c Images TEM de la poudre
Les spectres d'émission de photoluminescence du MgAl dopé Ti2 O4 montrent une émission blanche à 260 nm d'excitation (Fig. 2a) pour des échantillons de taille nanométrique et micron synthétisés à 500 °C pendant 1 h et 1 300 °C pendant 2 h sur les Fig. 2b, c, respectivement. Cependant, les deux bandes d'émission donnent des couleurs légèrement différentes :celle de la nanopoudre synthétisée à 500 °C est décalée vers le bleu par rapport à celle de la poudre micrométrique préparée à 1300 °C. L'émission bleue de MgAl dopé Ti2 O4 monocristaux est attribué à Ti 4+ dans les sites Al (octaédriques), qui était la seule forme d'ions Ti dans les monocristaux [10, 11]. Cependant, MgAl2 dopé Ti O4 une poudre de la taille d'un micron s'est avérée avoir à la fois Ti 3+ et Ti 4+ occupant à parts égales les sites Al (octaédrique) et Mg (tétraédrique) [12].
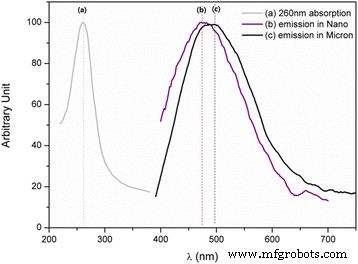
Photoluminescence du MgAl2 dopé Ti O4 :a Excitation à 260 nm, b nano, et c microns [12] poudres synthétisées à 500 °C, 1 h et 1 300 °C, 2 h, respectivement
La figure 3a montre une image HR-STEM prise près de la surface d'un nano MgAl2 dopé au Ti O4 . L'image agrandie de la figure 3b montre que la distance entre les réseaux est de 0,2057 nm, ce qui correspond bien à la distance planaire (400) de MgAl2 O4 (0,202 nm). Il montre que l'arrangement atomique a laissé une lacune relativement sombre parmi les taches (voir les flèches sur la Fig. 3a, b). La luminosité mineure au niveau de la lacune pourrait provenir des atomes des couches inférieures. Le point de défaut est également identifié dans le tracé d'intensité de contraste dans l'encart, qui montre les pics de contraste pour les atomes à l'intérieur de la boîte rouge de la figure 3b. La vacance est clairement indiquée par la faible intensité de contraste du cinquième site à partir de la gauche. Pour identifier le site vacant, nous avons effectué la transformation de Fourier de l'image de la Fig. 3a et avons trouvé que l'axe du faisceau est proche de [001] (encadré, Fig. 3a). Il est noté à partir de la vue projetée [001] d'un MgAl2 O4 cristal que les atomes de Mg sont situés indépendamment dans le plan (004), tandis que les atomes d'Al et d'O semblent se chevaucher dans le même plan. Ainsi, si la fluctuation montrée dans l'intensité du contraste n'est due qu'aux atomes constitutifs du plan, il est plus probable que la vacance provienne d'un site Al vacant plutôt que d'un site Mg vacant.
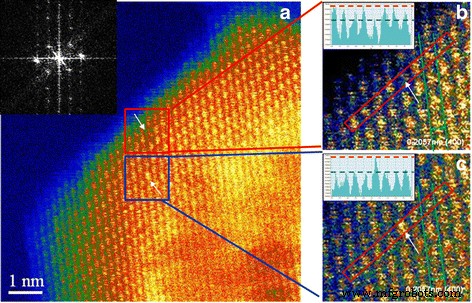
Images HR-STEM de nano MgAl2 dopé Ti O4; un . L'image montre Al 3+ vacance et Ti 4+ dopant au voisinage avec transformation de Fourier de l'image. b L'image agrandie dans la boîte rouge de (a ) et Al 3+ la vacance est révélée à partir de l'image STEM avec une intensité de contraste correspondante, en médaillon de (b ). c L'intensité du contraste, en médaillon de (c ), confirme que Ti 4+ le dopant occupe un site Al. Les flèches indiquent les emplacements de la vacance Al et Ti dans le site Al, respectivement
Sur la figure 3c, le point du réseau indiqué par une flèche dans le cadre rouge est beaucoup plus lumineux que les autres. Considérant que les atomes de Mg et d'Al ne peuvent pas être distingués par le contraste z en raison de leurs numéros atomiques similaires et qu'il est difficile de détecter les atomes d'oxygène en raison de son faible numéro atomique, ce point plus brillant est dû au dopant Ti. Le tracé d'intensité de contraste correspondant (en médaillon, Fig. 3c) met l'accent sur la tache la plus lumineuse, indiquant la présence d'un élément de numéro atomique plus élevé, certainement Ti dans ce système. Ti dans un site Al provoque une erreur de déplacement, car sa valence de charge et son rayon ionique sont différents de ceux de Al 3+ . L'atome le plus brillant de la figure apparaît plus gros que les autres, en accord avec les plus grands rayons ioniques effectifs de Ti 3+ (0,081 nm) et Ti 4+ (0,0745 nm) par rapport à celui d'Al 3+ (0,0675 nm) [16]. Le rayon ionique effectif de Mg 2+ est rapporté à 0,086 nm, ce qui est plus grand que ceux des ions Ti. Ainsi, nous avons conclu que les défauts montrés dans la Fig. 3 (c'est-à-dire, Fig. 3b, c) sont VAl et TiAl · , respectivement, s'attendant à ce que Ti 4+ les ions de plus petite taille (0,0745 nm) ont plus de chances de prendre des sites Al vacants que Ti 3+ (0,081 nm).
La figure 4a montre l'évolution de l'énergie de surface d'un MgAl2 dopé Ti O4 cristal parfait calculé par rapport à la position du dopant. L'énergie de surface, qui peut être un facteur majeur influençant l'énergie de formation d'un nanosystème, diminue à mesure que Ti se rapproche de la surface, indiquant que le cristal est plus stable lorsque Ti est plus proche de la surface. Le résultat indique une tendance commune pour Ti sur un site Al et Ti sur un site Mg; cependant, le dopant est plus stable sur un site Mg que sur un site Al. Ceci est attribué au plus grand rayon ionique effectif de Mg 2+ (0,086 nm) que Ti 4+ (0,0745 nm) ou Al 3+ (0,0675 nm) [16]. Ainsi, la tendance est plus probable lorsque MgAl dopé Ti2 O4 a une cristallinité élevée. Cependant, cela peut ne pas être toujours vrai pour un nanosystème à faible cristallinité, au moins près de la région de surface.
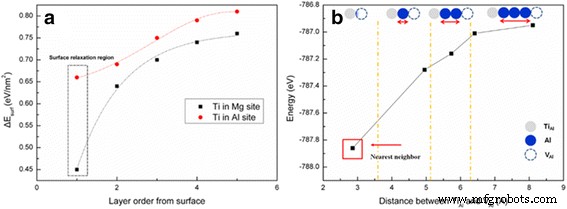
un Stabilités du Ti dans le site de lacune Mg ou Al à la surface de MgAl2 O4 :le cercle rouge montre l'énergie de surface du Ti dans le site Al et le point noir est celui du Ti dans le site Mg et b l'énergie de liaison des défauts associés, TiAl · –VAl ′′′ en fonction de la distance
Des calculs DFT ont également été effectués pour étudier le positionnement du dopant Ti et la lacune d'Al. L'énergie calculée d'un Ti1 Mg15 Au31 O64 cristal, spinelle contenant un dopant Ti (TiAl · ) et une vacance Al (VAl ′′′), augmente à mesure que le dopant et la lacune sont écartés, comme le montre la figure 4b. Par conséquent, une plus grande stabilité est obtenue lorsque les deux défauts sont proches l'un de l'autre et forment des défauts associés tels que (TiAl · –VAl ′′′)′′ qui sont responsables de l'émission bleue. Ce résultat est attribué à la stabilité structurelle et à la force coulombienne entre les deux défauts ponctuels. Cependant, un compromis émerge entre ces facteurs et l'entropie configurationnelle pour stabiliser le système à température élevée, ce qui entraîne un espacement des deux défauts de 2 à 3 atomes, comme le montre la figure 3a.
En général, l'énergie de formation d'une lacune d'Al ou de Mg est bien inférieure (~4,5 eV) à celle d'un interstitiel d'oxygène (~ 7,0 eV) dans MgAl2 O4 [17, 18]. Aussi, l'énergie de formation des défauts intrinsèques de Schottky pour MgAl2 O4 (4,15 eV/défaut) est bien inférieur à ceux des oxydes individuels, MgO (7,7 eV) et α-Al2 O3 (4,2-5,1 eV). Selon les estimations de Coulomb, les énergies d'association de défauts des paires de Schottky extrinsèques sont plus petites que celles des paires de Schottky intrinsèques dans divers systèmes ioniques [19]. Lorsque Ti-dopé MgAl2 O4 est synthétisé chimiquement par la méthode de combustion via des processus de nucléation et de précipitation, comme pour le nano système de cette étude, au lieu de par diffusion à l'état solide, la formation de défauts et d'associations de défauts, y compris O 2− les lacunes qui sont couramment observées dans les céramiques d'oxyde, seraient considérablement facilitées sur les surfaces des particules. Les résultats globaux indiquent que le défaut est associé, c'est-à-dire (TiAl · –VAl ′′′)′′, prévalent à la surface du MgAl dopé Ti2 O4 nanopoudres, provoquant le décalage vers le bleu de l'émission blanche des nanopoudres par rapport à celle des poudres microniques.
Conclusions
La substitution de Ti dans les sites Al de MgAl2 O4 a été observée par HR-STEM. Une lacune d'Al et un dopant Ti ont été détectés près de la surface du nano MgAl2 dopé Ti O4 . Ces observations démontrent la présence de Ti 4+ dans les sites d'Al. Le décalage vers le bleu par rapport au spectre du système à l'échelle du micron est attribué à la présence de plus de Ti 4+ ions dans les sites Al à la surface. Ce serait énergétiquement plus favorable pour Ti 4+ ions pour prendre des sites Mg dans la structure spinelle. Cependant, Ti 4+ les ions ont tendance à prendre des sites Al dans le nano MgAl2 dopé Ti O4 . Cette différence de luminescence du nanosystème est due à sa faible cristallinité résultant de la faible température de traitement.
Abréviations
- Nitrate d'Al :
-
Al(NON3 )3 ·9H2 O
- DFT :
-
Théorie fonctionnelle de la densité
- RH-STEM :
-
TEM de numérisation haute résolution
- Nitrate de magnésium :
-
Mg(NON3 )2 ·6H2 O
- PL :
-
Photoluminescence
- TEM :
-
Microscopie électronique à transmission
- Ti oxy-acétyl-acétonate :
-
C10 H14 O5 Ti
- Urée :
-
CO(NH2 )2
- VASP :
-
Package de simulation ab initio de Vienne
- XRD :
-
Diffractométrie aux rayons X
Nanomatériaux
- Défauts à la surface des alliages de titane
- Du début à la fin :les bases de la mesure de surface
- Analyse des émissions photo-induites pour identifier les contaminants de surface
- Comment atteindre le zéro défaut ?
- Logiciel :la voie vers le zéro défaut
- Quels sont les différents types de drainage des eaux de surface ?
- Les principes fondamentaux de la rectification plane
- Meulage de surface à l'ancienne
- Montage en surface par rapport au trou traversant :quelle est la différence ?



