Réseaux de carbone poreux dérivés du nitrure de carbone graphitique pour une réaction efficace de réduction de l'oxygène
Résumé
De grands efforts ont été consacrés à la recherche d'une réaction de réduction de l'oxygène (ORR) économique et efficace pour la technologie des piles à combustible. Parmi divers catalyseurs, les nanomatériaux à base de carbone dopé N ont attiré beaucoup d'attention en raison de leur faible coût, de leur absence de métaux nobles et de leur bonne durabilité. Ici, nous avons développé une stratégie facile et économique pour préparer des réseaux de carbone dopé à l'azote pour une application efficace de l'ORR. Le g-C3 N4 est utilisé comme matrice et source d'azote, et la dopamine est utilisée comme source de carbone. Par simple traitement hydrothermal et frittage, des structures de réseau de carbone dopé N avec une surface spécifique élevée, une activité ORR efficace et une durabilité supérieure pourraient être acquises. La stratégie actuelle n'implique généralement pas de réactifs toxiques en plusieurs étapes et ne complique pas le retrait du gabarit pour la fabrication de structures en carbone 3D.
Contexte
La réaction de réduction de l'oxygène (ORR) est une étape cruciale pour le développement ultérieur de stratégies de conversion d'énergie propre telles que les piles à combustible et les batteries métal-air [1,2,3]. Les matériaux cathodiques traditionnels à base de Pt pour l'ORR souffrent généralement d'un coût élevé, d'une stabilité limitée et d'une mauvaise tolérance au méthanol [1, 4, 5, 6, 7, 8]. Par conséquent, développer un matériau à faible coût, hautement actif et durable vers l'ORR a reçu une grande attention [9, 10]. De nombreux efforts ont été consacrés à la recherche de remplacements pour les électrocatalyseurs à base de Pt, tels que les catalyseurs de métaux de transition [5, 11,12,13] et les nanomatériaux à base de carbone [4, 8, 13,14,15,16].
Notamment, en tant qu'électrocatalyseurs sans métal, les nanomatériaux à base de carbone sont des matériaux prometteurs pour l'ORR en raison de leur bonne durabilité, de leur absence de métal noble et de leur faible coût [17]. Grâce à une conception élégante du système de matériaux, des structures en carbone poreux 3D ont pu être obtenues et ont fourni une surface spécifique et un volume de pores élevés, ce qui est extrêmement important pour un ORR efficace [7, 18]. Structures de carbone tridimensionnelles souhaitables généralement dérivées de divers modèles, notamment la glace, la silice et le polystyrène [19]. La fabrication de la structure de carbone 3D impliquait généralement des réactifs toxiques en plusieurs étapes et une complication du retrait du gabarit [6, 20, 21]. Ainsi, la stratégie de préparation facile reste un obstacle majeur. De plus, l'introduction d'atomes de N dans les matériaux carbonés améliore considérablement l'activité électrocatalytique, induisant ainsi un ORR efficace [22, 23]. De grands efforts ont rapporté des matériaux carbonés dopés N en introduisant des sources riches en azote telles que la mélamine [24, 25], l'urée [26], la dopamine [27] et le pyrrole suivis d'un frittage. Pour les applications ORR, un moyen facile de réaliser une structure poreuse et un dopage N efficace est toujours fortement souhaité.
Ici, nous avons développé une stratégie pour préparer des réseaux de carbone dopé à l'azote pour une application efficace de l'ORR en utilisant du nitrure de carbone graphitique sans métal (g-C3 N4 ) et la dopamine (DA) comme source N et source C, respectivement. g-C3 sans métal N4 a été intensivement étudié en raison de son application potentielle pour la photocatalyse [9, 28,29,30] et ORR [30,31,32,33] etc. Les matériaux dopés N pourraient être obtenus en utilisant gC3 N4 comme source de N en raison de sa teneur élevée en N [20, 23, 34, 35]. Le g-C3 N4 est un matériau polymère conjugué bidimensionnel typique [36, 37]. Il a reçu une grande attention en tant que photocatalyseur peu coûteux, sans métal et sensible à la lumière visible [38, 39]. Le g-C3 N4 a une excellente structure de bande électronique, une modification de fonctionnalisation de surface et une stabilité physique et chimique élevée et est non toxique et riche en matières premières [40,41,42]. De plus, la teneur en azote est élevée, ce qui en fait l'un des composés riches en N connus [43]. Le plus important est qu'il possède une variété de structures 2D ou 3D qui peuvent être obtenues en contrôlant les conditions de synthèse [44,45,46]. Les matériaux carbonés dopés à l'azote ont généralement une température de synthèse supérieure à 800 °C, ce qui satisfait aux exigences de retrait du gabarit [47]. Par conséquent, il est possible d'utiliser g-C3 N4 qui ne contient que des éléments carbonés et azotés pour synthétiser des matériaux carbonés dopés N [48]. Dans le présent travail, g-C3 N4 est utilisé simultanément comme matrice et source d'azote pour préparer des structures poreuses en carbone à haute surface spécifique (954 m 2 g −1 ) et une teneur en N de 5,71 % est atteinte, ce qui présente une activité ORR comparable, une durabilité supérieure et une tolérance au méthanol par rapport à l'électrocatalyseur de référence Pt/C.
Méthodes
Matériaux
L'hydroxyde de potassium (KOH) et le chlorure de potassium (KCl) ont été obtenus auprès de Sinopharm Chemical Reagent Co., Ltd. Hexacyanoferrate de potassium (K3 [Fe(CN)6 ]) ont été obtenus auprès de Tianjin Yongsheng Fine Chemical Co., Ltd. L'urée a été obtenue auprès de Beijing Chemical Corp. Tous les médicaments ci-dessus sont analytiquement purs. La solution perfluorée Naifon® (5% en poids dans un mélange d'alcools aliphatiques inférieurs et d'eau, contient 45% d'eau) a été achetée chez Sigma-Aldrich.
Synthèse de g-C3 N4 Modèle
Typiquement, 15 g d'urée dans un creuset de 100 ml ont été maintenus à 550°C pendant 4 h. Le g-C3 N4 a été acquis et broyé en poudre jaune clair pour une utilisation ultérieure après refroidissement à température ambiante.
Synthèse des précurseurs g-C3N4@dopamine
0,5 g g-C3 N4 a été dispersé dans 20 ml de solution de DA. La concentration de DA était de 0,3 M. Le mélange a été soumis aux ultrasons pendant 2 h et transféré dans un autoclave suivi d'un chauffage à 120 °C pendant 10 h. L'échantillon résultant a été centrifugé et lavé puis séché à 80°C pendant une nuit. Trois températures de chauffage de 120 °C, 140 °C et 160 °C ont été utilisées pour préparer g-C3 N4 /PDA précurseurs, et les échantillons correspondants ont été nommés g-C3 N4 /PDA-120, g-C3 N4 /PDA-140 et g-C3 N4 /P DA-160, respectivement.
Préparation de matériaux carbonés 2D dopés à l'azote
Les précurseurs de g-C3 N4 /PDA-120, g-C3 N4 /PDA-140 et g-C3 N4 /PDA-160 ont été chauffés à 900°C pendant 2 h dans une atmosphère d'azote. Après refroidissement à température ambiante, des échantillons de carbone poreux dopé à l'azote nommés NC-120, NC-140 et NC-160 (NC-T) ont été synthétisés. Cependant, la tentative de réduire davantage la température de chauffage à 100 °C a induit un très mauvais revêtement de DA sur g-C3 N4 , ce qui a entraîné un faible rendement après frittage à 900 °C. Par conséquent, trois températures de 120 °C, 140 °C et 160 °C ont été choisies pour une étude plus approfondie. Le processus de synthèse d'échantillons de carbone poreux dopé à l'azote est illustré dans le schéma 1.
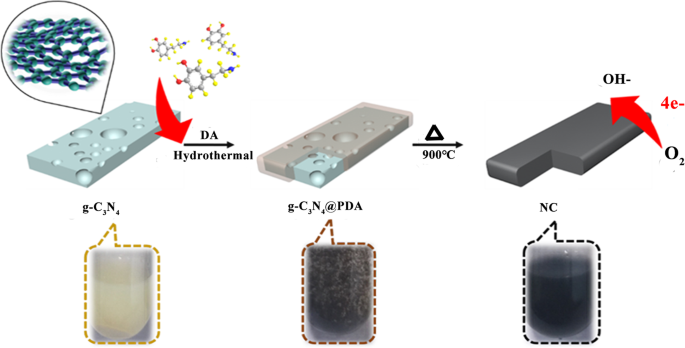
Le procédé de synthèse des électrocatalyseurs NC-T
Mesure électrochimique
L'analyse électrochimique a été réalisée par le poste de travail électrochimique DyneChem, et Ag/AgCl et le platine sont utilisés comme électrode de référence et contre-électrode, respectivement. Le voltampi cyclique a été testé dans une solution de potasse 0,1 µM. L'électrode en verre carbone (GCE) a été polie et lavée avant utilisation. Pour préparer les électrodes de travail, des aliquotes de 5 L et 2,5 mg/mL de solutions NC-120, NC-140, NC-160, Pt/C ont été trempées dans du GCE pour un test plus approfondi.
Caractérisation
La structure et la composition chimique du NC-T ont été analysées par diffraction des rayons X (XRD) (diffractomètre à rayons X D-MAX II A), microscopie électronique à transmission (MET) (Tecnai F20), microscope électronique à balayage (MEB) ( JEOL7610), spectres infrarouges à transformée de Fourier (FT-IR) (Nicolet iS50), spectroscopie photoélectronique à rayons X (XPS) (Kratos Axis UltraDLD) et Raman (Horiba, Japon) ; Les isothermes d'adsorption-désorption de N2 (77 K) ont été réalisées sur un instrument Micromeritics ASAP 2020 (MICROSENSOR, USA).
Résultats et discussion
Caractérisation SEM et TEM
Afin de déterminer la morphologie des échantillons synthétisés, SEM et TEM sont utilisés pour l'observation de la structure, comme le montre la figure 1. La figure 1a représente la structure en feuille de g-C3 tel que synthétisé. N4 . La structure 2D de g-C3 N4 est encore confirmé par la figure 1b, qui est similaire au rapport précédent [48]. Pour g-C3 N4 /PDA-120 comme le montre la Fig. 1c, d, l'image SEM est similaire à celle de g-C3 N4 . Cependant, l'image TEM de g-C3 N4 /PDA-120 montre une morphologie de type feuille bien dispersée, par rapport au g-C3 tel que synthétisé N4 . Avec l'augmentation de la température de chauffage de 120 à 160 °C, la structure lamellaire mince de la couche carbonisée a pu être observée (Fichier supplémentaire 1 :Figure S1). Après frittage à 900 °C, les images MEB apparaissent comme des structures en nid d'abeilles comme le montre la figure 1e en raison de la pyrolyse de g-C3 N4 modèle, induisant des structures de carbone poreuses comme le montrent la figure 1f et le fichier supplémentaire 1 :figure S2. Le test de thermogravité de g-C3 N4 a été réalisée pour déterminer le résidu de g-C3 N4 , et g-C3 N4 commence à se décomposer à 520 °C. Sous protection à l'azote, la décomposition complète est confirmée à 760 °C, comme indiqué dans le fichier supplémentaire 1 :Figure S3. Entre 80 et 100 °C, g-C3 N4 perdra légèrement sa qualité en raison de l'évaporation de l'humidité, et le résultat de la recherche est cohérent avec les rapports précédents [47]. Cela indique que g-C3 N4 pourrait être utilisé comme modèle efficace pour préparer des structures en carbone poreux.

Caractérisations structurelles d'échantillons comme des nanofeuillets de carbone. un SEM et b Images MET de g-C3 N4 , c SEM et d Images MET de g-C3 N4 /PDA-120, e SEM et f Images MET du NC-120
Caractérisation XRD, FT-IR et Raman
La température hydrothermale affecte non seulement la structure des échantillons, mais modifie également le pic de XRD. Les trois g-C3 revêtus de DA N4 les échantillons présentent tous deux pics de diffraction à 13,0° et 27,4° attribués aux plans cristallins (100) et (002) de g-C3 N4 gabarit comme illustré à la Fig. 2a. Après calcination à 900 °C, la variation évidente pour les trois échantillons a pu être trouvée. Le pic à 13,0° a disparu et deux nouveaux pics se produisent autour de 26,3° et 44,1° relatifs aux plans (002) et (100) du graphène, indiquant la formation d'une nouvelle structure de carbone graphitique comme indiqué dans le fichier supplémentaire 1 :Figure S4 [4]. Avec l'augmentation de la température hydrothermale, le degré de graphitisation et de cristallisation augmente progressivement. Ceci est encore confirmé par le test Raman et FT-IR.
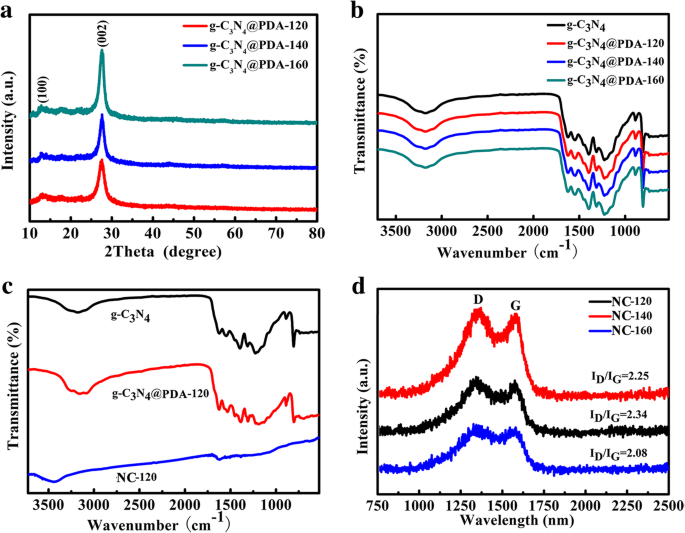
un Modèles XRD de g-C3 N4 @PDA-120, g-C3 N4 @PDA-140, et g-C3 N4 @PDA-160 ; b Spectres FT-IR de g-C3 N4 , g-C3 N4 @PDA-120, g-C3 N4 @PDA-140, et g-C3 N4 @PDA-160 ; c Spectres FT-IR de g-C3 N4 , g-C3 N4 /PDA-120 et NC-120 ; d Spectres Raman de NC-120, NC-140 et NC-160
La spectrométrie FT-IR a été réalisée pour analyser les groupes fonctionnels présents sur les surfaces des hybrides NC-T. Spectres FT-IR de g-C3 N4, g-C3 N4 /PDA-120, g-C3 N4 /PDA-140 et g-C3 N4 /PDA-160 indiquent que ces échantillons comprennent des groupes fonctionnels similaires contenant du carbone et de l'oxygène, comme le montre la figure 2b. Les pics entre 1200 et 1650 cm −1 appartiennent aux méthodes d'étirement des hétérocycles CN, et les pics larges situés dans la gamme de 3000~3500 cm −1 sont attribuées à la vibration d'étirement du groupe N-H [49]. Avec l'augmentation de la température hydrothermale, les deux pics à 1650 cm −1 (C=C) et 3350 cm −1 (O-H) sont plus évidents en raison de DA enveloppé sur g-C3 N4 . Après carbonisation à haute température, il ne reste que trois pics faibles pour le NC-120 à 1600 cm −1 , 1260 cm −1 , et 3450 cm −1 (Fig. 2c), qui sont attribuées aux vibrations C-C et C-N. Cela indique que la carbonisation à haute température détruit O-H, N-H et d'autres liaisons chimiques, tandis que les liaisons C-N sont stables, assurant ainsi le dopage efficace des éléments azotés.
La spectroscopie Raman est utilisée pour évaluer l'évolution structurelle de NC-T. La figure 2d est les spectres Raman de NC-120, NC-140 et NC-160, et les pics à 1350 et 1580 cm −1 correspondent respectivement aux bandes D et G [50, 51]. Avec l'augmentation de la température hydrothermale, le rapport d'intensité de I D /Je G diminue de 2,34 à 2,08, indiquant le degré de graphitisation amélioré avec l'augmentation de la température.
Caractérisation XPS
XPS est utilisé pour explorer la composition élémentaire des échantillons comme le montre la figure 3. Par rapport à g-C3 N4 , trois g-C3 N4 Les échantillons /PDA-T présentent une teneur en oxygène accrue en raison du revêtement DA carbonisé sur g-C3 N4 (Fichier supplémentaire 1 :Tableau S1). Avec l'augmentation de la température hydrothermale de 120 à 160 °C, la teneur en N diminue (Fig. 3a). Pour les pics liés au C, les intensités des pics C-C/C=C et C-O augmentent, tandis que le pic de N-C=C diminue progressivement avec l'augmentation de la température hydrothermale, comme le montre la figure 3b. Selon le rapport précédent [24], les performances électrochimiques souhaitables pourraient être atteintes par des échantillons à forte teneur effective en dopage N. Sur la base des spectres XPS de NC-T, la teneur en C augmente après un traitement thermique à 900 °C avec l'augmentation de la température hydrothermale (Fichier supplémentaire 1 :Figure S6). Le tableau 1 donne la teneur effective en N des trois échantillons. Le NC-T montre la présence de N pyridinique (398,5 eV) et graphitique (401,1 eV) [25]. Lorsque la température hydrothermale est élevée à 160 °C, la teneur en N diminue considérablement. La figure 4 montre des spectres XPS haute résolution N 1 s d'échantillons NC-T. Le pourcentage d'azote pyridinique et d'azote graphitique en fonction de la température hydrothermale est indiqué sur la figure 4d. La teneur en N diminue progressivement avec l'augmentation de la température hydrothermale.
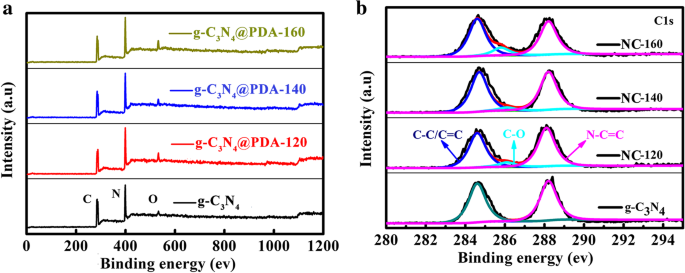
un Enquête XPS et b Spectres XPS C1s de g-C3 N4 @PDA-T préparé à un HT différent de g-C3 N4 et 120 °C, 140 °C, à 160 °C, respectivement
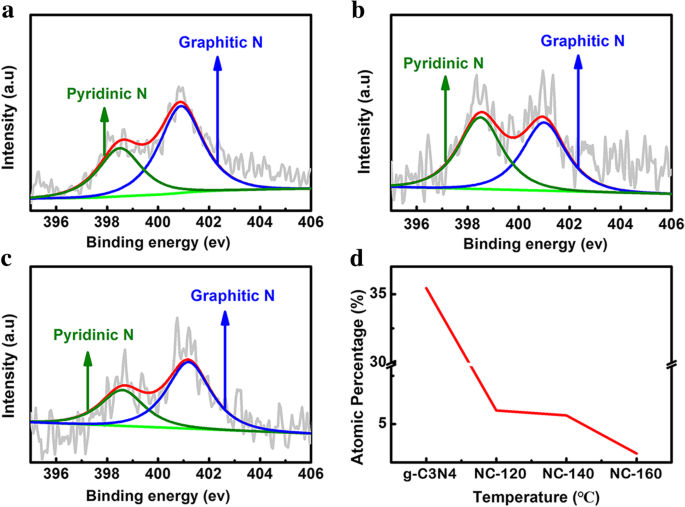
Spectres XPS haute résolution de NC-T a 120 °C, b 140 °C, et c 160 °C ; d Le changement de contenu atomique absolu de N dopé à différentes températures
Caractérisation Brunauer–Emmett–Teller (BET)
L'activité catalytique est liée à la surface spécifique et à la structure des pores.
Les surfaces spécifiques BET des échantillons sont décidées par N2 test des isothermes d'adsorption à 77 K, et tous les échantillons présentent des courbes de type IV [19]. Cela implique que les échantillons ont des micropores et des structures mésoporeuses comme indiqué dans le fichier supplémentaire 1 :Figure S5. Les surfaces spécifiques des NC-120, NC-140 et NC-160 sont de 954, 824 et 517 m 2 g −1 , respectivement, qui sont significativement plus élevés que ceux de l'original g-C3 N4 (85 m 2 g −1 ). Les résultats montrent qu'une température plus basse contribue à la formation d'une grande surface spécifique et d'une grande taille de pores. Pour le catalyseur ORR, l'avantage de la structure en couches, des surfaces spécifiques élevées et des teneurs élevées en azote sont très importants. Les images SEM et MET de g-C3 N4 /PDA-T a montré que les trois échantillons ont une structure en couches similaire avec un g-C3 vierge N4 (Fichier supplémentaire 1 :Figure S1). Le NC-120 présente la plus grande grande surface spécifique (954 m 2 g −1 ), et il a une structure mésoporeuse appropriée (≈ 5 nm). La grande surface spécifique permet d'augmenter la surface de contact avec les réactifs et d'accélérer la réaction [52].
Performances électrocatalytiques et discussion
On pourrait conclure des résultats ci-dessus que le NC-120 a la plus grande surface spécifique et la plus forte teneur en azote, ce qui est très bénéfique pour l'ORR [46]. Les propriétés électrochimiques des échantillons sont étudiées par voltamétrie cyclique (CV) et comparées avec des catalyseurs commerciaux Pt/C. Les résultats sont présentés sur la figure 5 et le tableau 2. Aucun pic de réduction d'oxygène n'est observé pour tous les échantillons dans des conditions de saturation en azote (figure 5a et fichier supplémentaire 1 :figure S8). Pour les conditions de saturation en oxygène, il existe un pic évident de réduction de l'oxygène, et cela devient plus évident avec la diminution de la température hydrothermale. Les résultats suggèrent que les comportements CV sont associés à la structure des catalyseurs. Dans O2 -solutions de KOH 0,1 M saturées, l'échantillon NC-120 exprime les meilleures performances, qui sont proches du catalyseur à base de Pt et son potentiel demi-crête est de 0,224 V, et sa densité de courant ultime est de 5,04 mA cm −1 (Fichier supplémentaire 1 :Figure S7). La figure 5b est la courbe de voltamogramme à balayage linéaire (LSV), montrant la densité de courant limite et les potentiels d'apparition des échantillons NC-T. Avec la diminution de la température hydrothermale, la tension et la densité de courant sont améliorées et les performances du catalyseur sont améliorées progressivement. On peut voir à partir de la figure 5c qu'un petit mouvement de cette courbe est trouvé après l'ajout de méthanol, suggérant que le NC-120 a une excellente tolérance au méthanol. Sur la figure 5(e), le NC-120 présentait de bonnes propriétés de réduction de l'oxygène, ce qui pourrait être dû à la grande surface spécifique et à la teneur en azote (Fichier supplémentaire 1 :Figure S7). Pour le NC-120 (Fig. 5d, f), le nombre de transfert d'électrons dans le processus de réduction de l'oxygène est calculé entre 3,9 et 4,1, indiquant que la réaction de réduction de l'oxygène du NC-120 catalytique est constituée de quatre processus électroniques. Le NC-120 a la meilleure performance électrochimique, qui est attribuée au dopage N efficace par la stratégie actuelle.
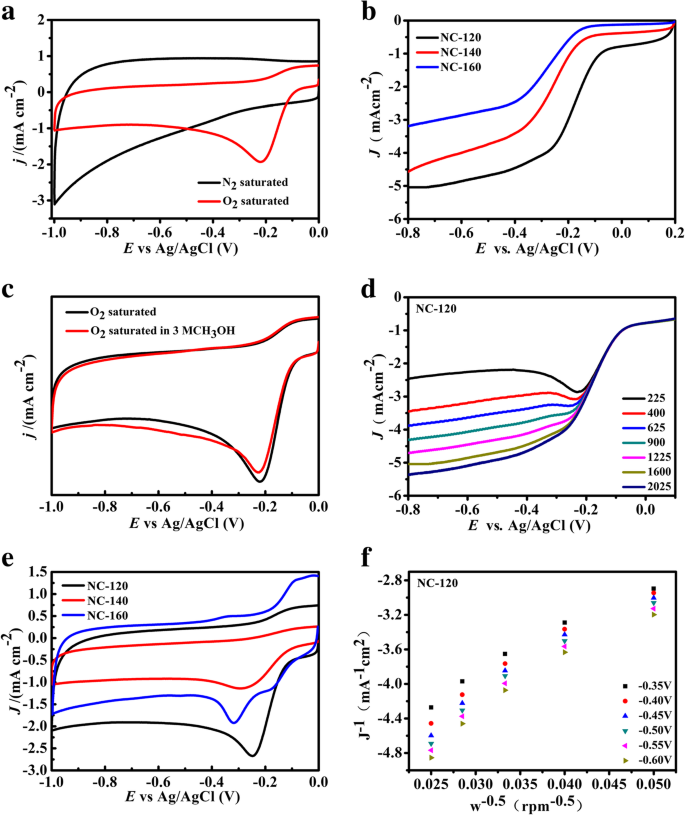
un Courbes CV du NC-120 en N2 et O2 solution aqueuse saturée de KOH 0,1 M avec une vitesse de balayage de 100 mV s −1 . b Courbes LSV de NC-T à des vitesses de rotation de 1600 tr/min. c Courbes de polarisation linéaire du NC-120 avec différentes vitesses de rotation à une vitesse de balayage de 5 mV s −1 en O2 -KOH 0,1 µM saturé. d Graphiques K-L à différents potentiels sur la base des résultats de c . e CV du NC-120 en O2 -solution saturée de KOH 0,1 M avec 3 M CH3 OH. f Courbes CV de NC-T dans une solution aqueuse saturée en O2 0,1 M KOH avec une vitesse de balayage de 100 mV s −1
Comme le montre le schéma 1, DA est utilisé comme source de carbone et g-C3 N4 nanosheet est utilisé comme modèle et source d'azote. Il y a trois raisons pour choisir cette stratégie :Premièrement, g-C3 N4 peut fournir une structure multicouche et il pourrait disparaître complètement à 900 °C. Deuxièmement, DA peut fournir un atome de carbone et DA carbonisé pourrait couvrir des deux côtés de g-C3 N4 . PDA a été formé sur le modèle de g-C3 N4 dans un procédé hydrothermal utilisant le DA comme source de carbone. Dans les processus hydrothermaux, le PDA peut fortement adhérer à la surface du substrat de matériaux organiques ou inorganiques en formant de fortes liaisons covalentes et non covalentes à la surface du substrat. Une fois le matériau de revêtement formé, la pyrolyse dans des conditions d'azote entraîne la formation de matériaux carbonés poreux avec une grande surface spécifique. Enfin, le g-C3 décomposé N4 fournirait des atomes de N pour le dopage de la structure carbonée, augmentant ainsi efficacement les sites actifs pour l'ORR. Dans des rapports précédents, Liu et al. préparé g-C3 N4 @PDA composites en déposant la solution DA directement dans g-C3 N4 solution sous agitation pour rehausser la lumière visible photocatalytique H2 activité de production, qui présente des résultats prometteurs [37]. Dans le présent travail, comme discuté ci-dessus, nous avons développé une nouvelle stratégie pour préparer des structures en carbone poreux dopé N avec une surface spécifique élevée (954 m 2 g −1 ) et une teneur élevée en N (5,71 %) en utilisant g-C3 N4 comme modèle et N source simultanément. Les composites acquis présentent une activité ORR comparable, une durabilité supérieure et une tolérance au méthanol par rapport à l'électrocatalyseur de référence Pt/C.
Conclusion
En résumé, nous avons développé une stratégie pour synthétiser des structures carbonées dopées N. La première étape est principalement le processus hydrothermal, et la deuxième étape est le processus de traitement thermique. Avec g-C3 N4 en tant que modèle et DA en tant que source de carbone, des réseaux de carbone poreux à forte teneur en dopage en N pourraient être obtenus. Les structures de réseau résultantes peuvent augmenter la surface spécifique du catalyseur et ainsi fournir d'excellentes propriétés électrochimiques, y compris un bon effet de tolérance au méthanol et une bonne stabilité par rapport au catalyseur Pt/C. Les performances de ces excellentes électrocatalyses peuvent être attribuées aux raisons suivantes :(1) La structure en couches C dopée N avec une teneur élevée en espèces graphite-N et pyridine-N fournit un site hautement actif pour la réaction de réduction de l'oxygène. (2) La surface spécifique élevée (954 m 2 g −1 ) coexiste avec du carbone graphitique élevé et du carbone amorphe, contribuant à la conduction électronique de l'ORR. (3) Les structures poreuses accélèrent le transfert d'électrons et favorisent la pleine utilisation des sites actifs. Ces avantages déterminent tous le bon effet catalytique de ce matériau. De plus, la présente méthode de préparation de nanomatériaux à base de carbone dopé N est économique, écologique et efficace, ce qui les rend largement disponibles dans les piles à combustible à l'avenir.
Disponibilité des données et des matériaux
Les ensembles de données utilisés ou analysés au cours de la présente étude sont disponibles auprès de l'auteur correspondant sur demande raisonnable.
Abréviations
- BET :
-
Bunauer–Emmett–Teller
- CV :
-
Voltamétrie cyclique
- DA :
-
Dopamine
- g-C3 N4 :
-
Nitrure de carbone graphite
- GCE :
-
Electrode carbone verre
- LSV :
-
Voltammogramme à balayage linéaire
- ORR :
-
Réaction de réduction d'oxygène
- SEM :
-
Microscope électronique à balayage
- TEM :
-
Microscope électronique à transmission
- XPS :
-
Spectroscopie photoélectronique aux rayons X
Nanomatériaux
- Fibres de carbone activées avec nanostructure hiérarchique dérivées de déchets de gants de coton en tant qu'électrodes hautes performances pour supercondensateurs
- Nanosphères de carbone monodispersées à structure poreuse hiérarchique comme matériau d'électrode pour supercondensateur
- Microsphères de carbone magnétique comme adsorbant réutilisable pour l'élimination des sulfamides de l'eau
- Une approche simple pour la synthèse de points quantiques de carbone fluorescent à partir d'eaux usées de tofu
- Polymère fonctionnel poreux à base de triphénylphosphine comme catalyseur hétérogène efficace pour la synthèse de carbonates cycliques à partir de CO2
- Carbone à haute porosité autodopé fortement graphitique-azote pour l'électrocatalyse de la réaction de réduction de l'oxygène
- Réaction de réduction de l'oxygène sur le nanocatalyseur PtCo :empoisonnement aux anions (bi)sulfate
- Électrocatalyseurs de réduction d'oxygène Fe-N-C hautement actifs et stables dérivés de l'électrofilage et de la pyrolyse in situ
- Composite Carbon Dots @ Platinum Porphyrin comme nanoagent théranostique pour une thérapie photodynamique efficace du cancer



