Carbone à haute porosité autodopé fortement graphitique-azote pour l'électrocatalyse de la réaction de réduction de l'oxygène
Résumé
La production à grande échelle de catalyseurs de carbone poreux actifs et stables pour la réaction de réduction de l'oxygène (ORR) à partir de biomasse riche en protéines est devenue un sujet brûlant dans la technologie des piles à combustible. Nous rapportons ici une stratégie facile pour la synthèse de nanocarbones poreux dopés à l'azote au moyen d'un simple processus de pyrolyse en deux étapes combiné à l'activation du chlorure de zinc et du processus de traitement à l'acide, dans lequel le haricot rouge via la carbonisation à basse température a été préférentiellement adopté comme les seules sources de carbone-azote. Les résultats montrent que ce matériau carboné présente une excellente activité électrocatalytique ORR, une durabilité et une propriété de tolérance au méthanol plus élevées par rapport au catalyseur Pt/C de pointe pour l'ORR, ce qui peut être principalement attribué à une teneur élevée en azote graphitique. , une surface spécifique élevée et des caractéristiques poreuses. Nos résultats peuvent encourager la synthèse d'électrocatalyseurs ORR à base de carbone de haute performance dérivés de la biomasse naturelle largement existante.
Contexte
Les matériaux à base de platine (Pt), les catalyseurs de pointe pour les piles à combustible, souffrent d'un prix élevé, de ressources limitées, d'une durabilité insuffisante et d'une propriété de tolérance au méthanol dans le processus d'électrocatalyse de la réaction de réduction de l'oxygène (ORR) [1] . De grands efforts ont été récemment consacrés à la recherche d'alternatives hautement actives, durables et peu coûteuses aux électrocatalyseurs ORR à base de Pt à cette fin [2]. Parmi les différents catalyseurs sans Pt, les carbones poreux dopés à hétéroatome (HDPC) sont un nouveau type de catalyseurs sans métal avec une activité et une durabilité élevées pour l'ORR grâce à leur faible coût, leur non-toxicité et leur renouvelabilité [3,4, 5,6], et ainsi, les recherches approfondies sont attendues avec impatience à ce jour. Le HDPC est généralement synthétisé par des méthodes chimiques ou des modèles naturels, mais ils ne peuvent pas répondre aux exigences de faible coût, de synthèse facile et d'excellentes performances [7, 8]. Par conséquent, la recherche d'une méthode raisonnable et efficace pour synthétiser le matériau HDPC est toujours un problème scientifique important pour réaliser une catalyse hautement efficace pour la réduction de l'oxygène.
Comme indiqué précédemment, la biomasse enrichie en protéines (p.> [14]) peut être largement utilisé comme précurseur à source unique pour le catalyseur HDPC vers l'ORR. Nous avons récemment proposé une stratégie pour former le catalyseur HDPC avec une structure de réseau 3D poreuse via une carbonisation à haute température de déchets biologiques à base d'écailles de poisson avec un activateur de chlorure de zinc [6]. Il est intéressant de constater que le prétraitement de la biomasse de première étape peut non seulement aider à améliorer les caractéristiques de la structure carbonée du catalyseur ORR final, mais également augmenter sa teneur en azote de surface et l'efficacité de dopage des atomes d'azote dans la structure carbonée. Sur la base de cette découverte, ici, nous rapportons d'abord une stratégie pour fabriquer des charbons poreux fortement dopés à l'azote graphitique (KB350Z-900) en convertissant directement la biomasse de haricot blanc (KB) avec un processus de carbonisation en deux étapes, suivi de chlorure de zinc processus d'activation et de traitement acide. La biomasse KB, qui est aujourd'hui l'une des fèves comestibles les plus célèbres, peut être obtenue en abondance et à moindre coût dans divers pays. La teneur totale en protéines biologiques de la biomasse KB déshydratée est généralement de 20 à 30 %. Au meilleur de notre connaissance, il est rarement rapporté sur l'activité ORR du catalyseur de carbone dopé dérivé de la biomasse KB. Le rôle du ZnCl2 dans le processus d'activation peut principalement stimuler la déshydratation rapide et la déshydroxylation catalytique de la biomasse KB de sorte que l'hydrogène et l'oxygène à l'intérieur de la biomasse KB sont libérés dans la formation de vapeur d'eau. Ce processus peut faciliter la formation de davantage de micro/mésopores, produisant finalement des matériaux carbonés à haute porosité auto-dopés à l'azote. Le catalyseur à base de carbone obtenu présente une activité électrocatalytique élevée, une durabilité à long terme et une propriété de tolérance au méthanol, ce qui peut être une alternative prometteuse au catalyseur à base de Pt vers l'ORR en milieu alcalin.
Méthodes
Tout d'abord, le haricot blanc (KB) a été lavé à l'eau désionisée et complètement séché à 80 °C dans une étuve de séchage sous vide. Par la suite, KB a été prétraité dans le flux-N2 atmosphère à 350 °C pendant 2 h pour une décomposition efficace de la protéine pour donner le précurseur KB350. Bien que la décomposition la plus rapide de la biomasse KB blanche se produise à environ 300 °C (Fichier supplémentaire 1 :Figure S1), mais une température de 350 °C a été choisie comme température de carbonisation de première étape afin de dépasser la température de décomposition de la tyrosine (344 °C), le plus élevé parmi les acides aminés des bioprotéines. KB350 et chlorure de zinc (ZnCl2 ) ont été mélangés mécaniquement par broyage à boulets à 500 tr/min selon un rapport de masse de 1:1. Le mélange obtenu a été pyrolysé dans un four tubulaire à différentes températures (700, 800, 900 ou 1000 °C) pendant 2 h avec une vitesse de chauffe de 10 °C min − 1 . Le nanocarbone produit est ci-après dénommé KB350Z-X (X = 700, 800, 900 ou 1000). En tant que témoin, le KB-Z-900 a été fabriqué de la même manière en pyrolysant un mélange mécanique de KB et de ZnCl2 avec le même rapport de masse. La pyrolyse directe du KB à 900 °C pendant 2 h a été utilisée pour préparer le KB900. Tous les échantillons préparés ont ensuite été post-traités dans 0,5 mol l − 1 solution de HCl pendant 2 h. L'objectif de la lixiviation acide est d'éliminer efficacement les espèces de Zn et les impuretés métalliques avant les tests électrochimiques.
Les données de spectroscopie Raman ont été testées avec une unité Renishaw inVia avec un excité de 514,5 nm. Les images de microscopie électronique à balayage à émission de champ (FE-SEM) ont été obtenues par Hitachi UHR S4800 (Japon). La microscopie électronique à transmission à haute résolution (HR-TEM) a été réalisée sur l'instrument FEI Tecnai F30 et la tension d'accélération est de 300 kV. La spectroscopie photoélectronique aux rayons X (XPS) a été réalisée à l'aide d'un spectromètre Kratos XSAM800. Un analyseur Micromeritics (ASAP 2010) a été appliqué pour mesurer N2 isothermes d'adsorption/désorption à 77 K.
Les mesures électrochimiques ont été effectuées sur une station de travail Zennium-E (Allemagne) avec un système classique à trois électrodes. Une électrode à disque de rotation verre-carbone (GC-RDE, Φ = 4 mm, modèle 636-PAR), une électrode au calomel saturé (SCE) et une tige de graphite (Φ = 0,5 cm) ont été utilisées comme électrode de travail, électrode de référence, et électrode auxiliaire, respectivement. La fabrication de l'électrode de travail fait référence à nos précédents rapports [6]. Généralement, 5,0 μl de 10 mg ml − 1 la dispersion a été transférée sur la surface du GC-RDE et séchée naturellement. La charge de masse de tous les échantillons testés a été contrôlée à ~ 400 μg cm − 2 . Tous les potentiels (par rapport à SCE) ont été transformés en potentiels par rapport à l'électrode à hydrogène réversible (RHE).
Résultats et discussion
Nous avons d'abord testé les spectres Raman des catalyseurs KB900, KB-Z-900 et KB350Z-900 pour comprendre leurs différences de propriétés structurelles. Les spectres Raman sont représentés sur la figure 1a. Le rapport d'intensité (ID /IG ) de la bande « D » à la bande « G » a été utilisée pour caractériser les degrés désordonnés et graphitiques. Le ID /IG est de 0,85 pour le KB350Z-900 uniquement, mais le ID /IG est de 0,94 pour KB900 et de 0,88 pour KB-Z-900, respectivement. Cela peut montrer qu'un degré graphitique plus élevé peut être obtenu à KB350Z-900 par rapport aux catalyseurs à base d'azote/carbone (NC) tels que préparés, ce qui peut être directement confirmé par comparaison de l'intensité Raman. De plus, l'utilisation de ZnCl2 activateur dans la synthèse de catalyseurs à base de NC peut faciliter l'amélioration du degré graphitique pendant le processus de pyrolyse en raison d'un ID le plus bas /IG rapport de KB350Z-900. Le prétraitement de la première étape du KB à 350 °C peut encore améliorer le degré graphitique des catalyseurs à base de NC, ce qui peut aider à produire davantage de structures carbonées dopées à l'azote graphitique. N2 des isothermes d'adsorption-désorption ont été utilisés pour étudier les effets de ZnCl2 activateur et prétraitement de première étape sur la surface spécifique et la distribution des pores des catalyseurs à base de NC. La figure 1b présente clairement une courbe d'isotherme de Langmuir IV avec une boucle d'hystérésis de type H2, démontrant que les structures mésoporeuses sont également incluses dans les catalyseurs préparés (par exemple, KB-Z-900 et KB350Z-900). La surface spécifique BET est d'environ 380 m 2 g − 1 pour KB-Z-900 et 1132 m 2 g − 1 pour KB350Z-900, respectivement. Un volume de pores total plus élevé de KB350Z-900 est de ~ 0,62 m 3 g − 1 , et la zone méso- et macropore de KB350Z-900 est de ~ 664 m 2 g − 1 (encadré de la figure 1b). Le prétraitement de la première étape du KB à 350 °C peut favoriser la formation de davantage de méso- et de macropores et l'augmentation de la surface spécifique BET, favorisant ainsi l'exposition des sites actifs et la diffusion de la molécule d'oxygène pendant le test électrochimique. Les images de microscopie électronique à transmission (MET) (Fig. 1c, d) confirment également qu'un grand nombre de micro/macropores et de structures carbonées amorphes peuvent être observés dans KB350Z-900. De manière significative, des bords défectueux et exposés dans la nanostructure de carbone en raison d'un pourcentage plus élevé de dopage N sont formés, ce qui est également censé offrir des sites efficacement réactifs pour l'ORR [15].
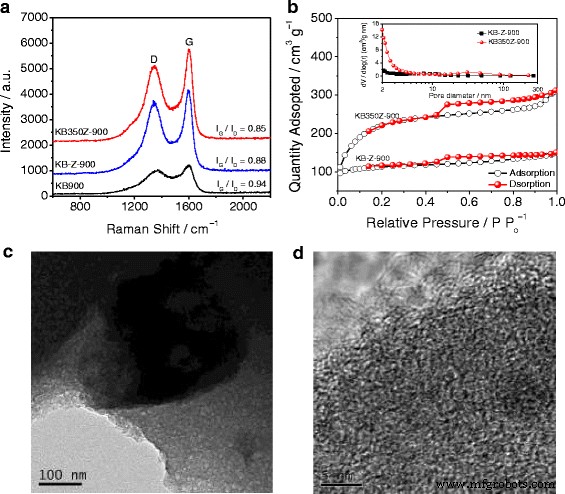
un Spectres Raman de KB900, KB-Z-900 et KB350Z-900. b Isothermes d'adsorption-désorption d'azote et distributions correspondantes de la taille des pores BJH (encadré) de KB-Z-900 et KB350Z-900. c Basse résolution et d images de microscopie électronique à transmission haute résolution de KB350Z-900
La figure 2a, b montre que les atomes d'azote sont dopés avec succès dans la structure carbonée de trois types de catalyseurs ORR. La teneur en azote de surface de l'analyse XPS est de 1,23, 1,92 et 2,70 % at. pour le KB-900, le KB-Z-900 et le KB350Z-900, respectivement. Il indique que la perte d'azote peut être diminuée grâce à l'activation de ZnCl2 et procédé de carbonisation en deux étapes [6]. Les spectres XPS N1 de KB-900 et KB-Z-900 peuvent être ajustés à trois pics (voir Fichier supplémentaire 1 :Figure S2), qui peuvent être attribués au N pyridinique, N graphitique et N oxydé [6, 7,8, 12, 13], respectivement. Cependant, le spectre XPS N1 du KB350Z-900 ne peut être intégré que dans deux pics (voir Fichier supplémentaire 1 :Figure S2), centrés à 398,5 et 401,1 eV, qui peuvent être attribués au pyridinique-N et au graphitique-N, respectivement. Notamment, l'espèce N oxydée n'est pas observée au spectre XPS N1 de KB350Z-900, et le pourcentage d'espèces N graphitiques peut atteindre 88,8 % at. dans la teneur en azote total. Le contenu des espèces graphitiques-N suit l'ordre de KB350Z-900 > KB-Z-900 > KB-900, impliquant que le ZnCl2 Le processus d'activation peut être facile pour faciliter l'augmentation de la teneur en N graphitique à l'intérieur du matériau NC et l'utilisation du précurseur KB350 dérivé du prétraitement de la première étape du matériau KB peut réduire efficacement la formation d'espèces N oxydées.
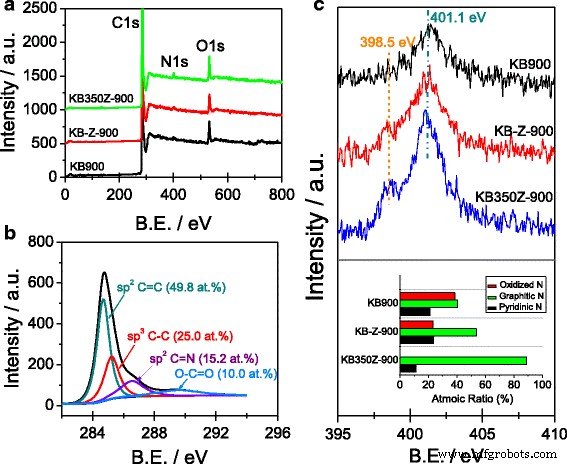
un Enquête XPS sur KB900, KB-Z-900 et KB350Z-900 ; b Spectre XPS C1s de KB350Z-900 ; c Spectres XPS N1 de KB900, KB-Z-900 et KB350Z-900
Courbes CV (voir Fig. 3a) obtenues en N2 contre O2 les solutions KOH saturées démontrent que le KB350Z-900 présente la densité de courant de crête ORR la plus élevée et le potentiel de crête le plus positif (0,90 V) par rapport aux KB-Z-900 et KB-900, ce qui peut être dû à la teneur élevée en espèces graphitiques-N à l'intérieur du catalyseur [13, 16]. De plus, les courbes LSV (Fig. 3b) obtenues en O2 Une solution de KOH saturée indique en outre que le potentiel demi-onde ORR et la densité de courant limitée du KB350Z-900 se rapprochent de ceux du catalyseur de première classe à 20 % en poids de Pt/C. La méthode de Tafel a été utilisée pour analyser les courbes courant-potentiel (j-E) dans la gamme cinétique. La densité de courant ORR est presque indépendante de la vitesse de rotation de l'électrode dans la plage de potentiel de 0,8 à 1,0 V (vs RHE), ce qui suggère que la densité de courant dans cette plage de faible surtension est dominée par la densité de courant cinétique électrochimique. Les tracés de Tafel de E en fonction de log (j) sont présentés dans (Fichier supplémentaire 1 :Figure S3). Une pente de Tafel de 143 mV décade − 1 est obtenu pour KB350Z-900. L'écart des pentes de Tafel pour le catalyseur KB350Z-900 et Pt/C implique que leur adsorption intermédiaire peut suivre un modèle différent [17]. Des pentes de Tafel plus élevées (valeur absolue) correspondent à une augmentation rapide du surpotentiel avec la densité de courant, conduisant probablement à une activité catalytique ORR relativement inférieure [18]. Cependant, l'activité électrocatalytique ORR de KB350Z-900 peut être plus excellente par rapport aux catalyseurs à base de carbone précédemment rapportés dérivés d'autres biomasses ou biomatériaux [9,10,11,12,13,14]. L'étude de l'effet de la température de pyrolyse sur les catalyseurs NC via le ZnCl2 l'activation affiche également que l'activité ORR suit l'ordre de KB350Z-900 > KB350Z-800 > KB350Z-1000 > KB350Z-700, suggérant la meilleure activité électrocatalytique de KB350Z-900, car des températures plus élevées ou plus basses aggraveront l'activité ORR en milieu alcalin [19]. Cela peut être principalement attribué à une raison valable selon laquelle une porosité et une surface spécifique élevées, une teneur élevée en N de surface et un pourcentage d'espèces N de KB350Z-900 peuvent faciliter le transport rapide de O2 molécule et l'exposition de sites actifs accessibles [6], ce qui peut aider à améliorer l'activité électrocatalytique vers l'ORR.
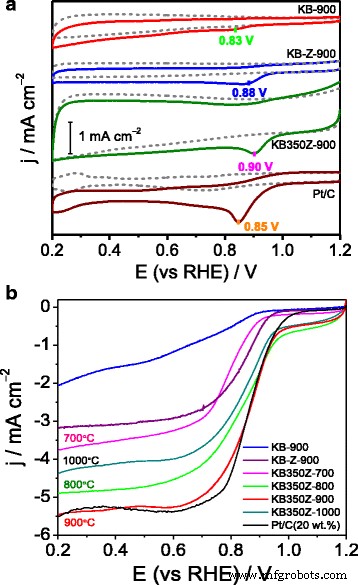
un Courbes CV de KB900, KB-Z-900 et KB350Z-900 en N2 contre O2 solution saturée de KOH; b Courbes LSV des catalyseurs préparés et catalyseur JM Pt/C
De plus, les courbes LSV pour l'ORR de KB-Z-900 et KB350Z-900 à différentes vitesses de rotation (400 à 3600 tr/min) sont illustrées à la Fig. 4a, b. La bonne linéarité des tracés de Koutecky-Levich (Fig. 4c) indique la cinétique ORR de premier ordre en ce qui concerne l'O2 dissous concentration. Le nombre moyen de transfert d'électrons (n) de l'ORR sur le KB-Z-900 et le KB350Z-900 est estimé à ~ 3,93 et ~ 3,98 (encadré de la Fig. 4c), respectivement, selon l'équation de Koutecky-Levich [20 ]. L'équation de Koutecky-Levich est la suivante :
$$ 1/{j}_d=1/{j}_k+1/B{\omega}^{1/2} $$ $$ \mathrm{B}=0.62\mathrm{nF}{\mathrm{C }}_{\mathrm{O}}{\mathrm{D}}_{\mathrm{O}}^{2/3}{\nu}^{-1/6}{\upomega}^{1/ 2} $$où F est la constante de Faraday, C O est le O2 concentration de saturation dans l'électrolyte, D O est le O2 coefficient de diffusion dans l'électrolyte, ν est la viscosité cinétique de l'électrolyte, et ω est la vitesse de rotation de l'électrode, et 0,62 est une constante lorsque la vitesse de rotation est exprimée en tr/min. Cela suggère que le processus ORR sur KB-Z-900 et KB350Z-900 suit principalement une voie de transfert direct à quatre électrons pour produire H2 O (par exemple, O2 + 2 H2 O + 4e − → 4 OH − ), qui est très similaire à l'ORR catalysé par un catalyseur Pt/C [21].
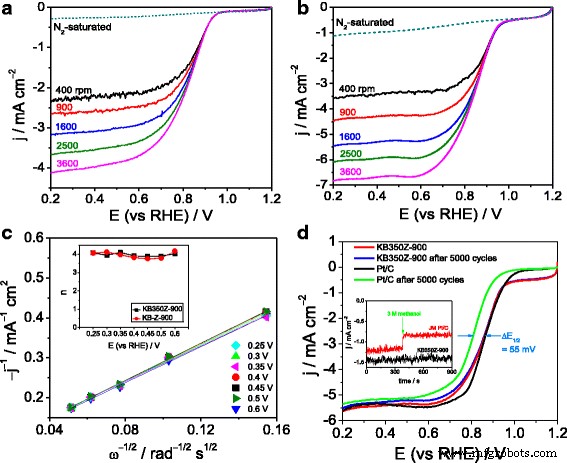
un Courbes LSV de KB-Z-900 en N2 contre O2 solution saturée de KOH à différentes vitesses de rotation ; b Courbes LSV du KB350Z-900 en N2 contre O2 solution saturée de KOH à différentes vitesses de rotation ; c Tracés de Koutecky-Levich de jd − 1 contre ω − 1/2 obtenu de (b ) aux potentiels donnés (0,25-0,6 V). L'encart est le tracé de n en fonction du potentiel obtenu à partir de (a ) et (b ); d Courbes LSV de KB350Z-900 et JM Pt/C avant et après CV pour 5000 cycles en O2 solution saturée de KOH; L'encart représente les courbes i-t ampérométriques à 0,9 V par rapport à RHE pour les tests de tolérance au méthanol
Ici, nous utilisons le test de vieillissement accéléré (AAT) par balayage continu CV pendant 5000 cycles sur une plage de potentiel de 0,2 à 1,2 V par rapport à RHE pour évaluer la stabilité électrochimique du catalyseur KB350Z-900 et Pt/C dans un O2 -électrolyte KOH saturé. Après le test CV, le potentiel demi-onde de l'ORR sur l'électrode catalysée KB350Z-900 est décalé négativement de seulement 2 mV, mais le potentiel demi-onde réduit de l'ORR sur l'électrode catalysée JM Pt/C est d'environ 55 mV (Fig. 4d). De plus, une dégradation plus élevée de la densité de courant limitée est également trouvée pour le catalyseur Pt/C, indiquant une stabilité électrocatalytique plus excellente du KB350Z-900 vers l'ORR. Courbes i-t ampérométriques à 0,9 V dans O2 -l'électrolyte KOH saturé (encadré de la Fig. 4d) confirme que la réaction d'électro-oxydation du méthanol 3 M se produit à peine à KB350Z-900, suggérant une bonne performance de tolérance au méthanol du KB350Z-900 et les applications prometteuses dans les piles à combustible alcalines au méthanol.
Conclusions
Ici, nous développons une méthode facile et facile pour la production à grande échelle de carbones à haute porosité dopés avec de l'azote fortement graphitique à partir de la pyrolyse en deux étapes de la biomasse de haricots rouges combinée à l'activation du chlorure de zinc et du processus de traitement à l'acide, qui peut être fonctionnait comme un électrocatalyseur de réduction d'oxygène en milieu alcalin. Premièrement, nous constatons qu'une grande surface BET (~ 1132 m 2 g − 1 ) peut être obtenu à KB350Z-900 avec un volume de pores élevé de ~ 0,62 m 3 g − 1 . Deuxièmement, le processus de pyrolyse en deux étapes avec activation au chlorure de zinc peut aider à augmenter considérablement la teneur en azote graphitique à l'intérieur du catalyseur à base de carbone. Nous observons également que l'activité catalytique ORR de ce matériau carboné peut se comparer favorablement à celle du catalyseur commercial de pointe à 20 % en poids de Pt/C, mais également à la stabilité de l'électrocatalyse du premier à l'ORR et aux performances de tolérance au méthanol. sont meilleurs, suggérant des applications prometteuses dans les piles à combustible alcalines. Les excellentes performances ORR du KB350Z-900 peuvent être principalement dues à la teneur élevée en azote graphitique, à la surface spécifique élevée et aux caractéristiques poreuses. Nos résultats peuvent favoriser davantage la production à grande échelle d'électrocatalyseurs ORR à base de carbone hautement actifs et stables dérivés de la biomasse naturelle largement existante.
Nanomatériaux
- Les scientifiques d'IBM inventent un thermomètre pour l'échelle nanométrique
- Les nanotubes de carbone repoussent les limites de l'électronique flexible
- Ocean Carbon imagé à l'échelle atomique
- Comment l'industrie aérospatiale utilise la fibre de carbone pour ses besoins
- 5 conseils pour trouver le meilleur fabricant de pièces en fibre de carbone
- La conception de la couche d'émission pour les multiplicateurs d'électrons
- Saponines de Platycodon de Platycodi Radix (Platycodon grandiflorum) pour la synthèse verte de nanoparticules d'or et d'argent
- Réaction de réduction de l'oxygène sur le nanocatalyseur PtCo :empoisonnement aux anions (bi)sulfate
- Électrocatalyseurs de réduction d'oxygène Fe-N-C hautement actifs et stables dérivés de l'électrofilage et de la pyrolyse in situ



