Effet des tensioactifs sur les microstructures des nanofleurs en floraison SnO2 hiérarchique et leurs propriétés de détection de gaz
Résumé
SnO hiérarchique2 des nanofleurs en fleurs ont été fabriquées avec succès via une méthode hydrothermale simple mais facile à l'aide de différents tensioactifs. Ici, nous nous concentrons sur l'exploration des effets de promotion des tensioactifs sur l'auto-assemblage de SnO 2D2 nanofeuilles en 3D SnO2 structures en forme de fleur ainsi que leurs performances de détection de gaz. Le SnO2 polyporeux en forme de fleur le capteur présente d'excellentes performances de détection de gaz vis-à-vis de l'éthanol et du H2 Gaz S en raison de la porosité élevée lorsque de la polyvinylpyrrolidone est ajoutée à la solution de précurseur en tant que tensioactif. Les temps de réponse/récupération étaient d'environ 5 s/8 s pour 100 ppm d'éthanol et de 4 s/20 s pour 100 ppm de H2 S, respectivement. En particulier, la valeur de réponse maximale de H2 S est estimé à 368 à 180 °C, ce qui est un ou deux ordres de grandeur supérieur à celui des autres gaz d'essai dans cette étude. Cela indique que le capteur fabriqué à l'aide de polyvinylpyrrolidone a une bonne sélectivité pour H2 S.
Contexte
Les capteurs de gaz ont attiré une large attention en raison de leurs applications potentielles dans la détection de gaz toxiques, nocifs, inflammables et explosifs [1]. À l'heure actuelle, les semi-conducteurs à oxyde métallique occupent une place importante dans divers capteurs en raison de leur processus de préparation simple, de leur coût inférieur et de leur sensibilité plus élevée aux gaz cibles [2,3,4]. Dioxyde d'étain (SnO2 ), un matériau multifonctionnel de type n avec une bande interdite directe de 3,6 eV [5], a été largement utilisé dans les études fondamentales et les applications pratiques, telles que les capteurs de gaz [6], la catalyse [7] et les dispositifs optoélectroniques [8 ]. Surtout, SnO2 a été considéré comme le matériau de détection le plus potentiel en raison de sa non-stœchiométrie naturelle [9], de sa sensibilité élevée, de sa vitesse de réponse/récupération rapide et de sa stabilité chimique élevée [10].
Il est bien connu que le mécanisme de détection de gaz des oxydes métalliques est lié aux processus d'adsorption et de désorption du gaz cible sur la surface du capteur, entraînant une modification de la conductivité électrique [11]. Ces processus dépendent fortement de la taille, de la morphologie et de la dimension ainsi que de la structure cristalline des échantillons [12]. Il existe deux manières principales d'améliorer efficacement les performances de détection de SnO2 [13]. L'une consiste à synthétiser des matériaux composés à base de SnO2 , telles que la fabrication de jonctions p-n, la décoration de surface ou le dopage [14]. L'autre consiste à préparer divers SnO purs2 matériaux comprenant des nanotubes [15], des nanotiges [16], des nanosphères [17], des structures creuses [14] et des nanofleurs [18], qui ont des nanostructures uniques, une surface spécifique élevée et de fortes capacités de capture d'électrons [19]. Récemment, SnO2 hiérarchique tridimensionnel (3D) les nanostructures ont beaucoup attiré l'attention en raison de leurs meilleures performances de détection de gaz causées par une grande surface spécifique et une diffusion gazeuse rapide par rapport aux nanostructures 1D et 2D [20]. Diverses techniques ont été utilisées pour fabriquer des nanostructures 3D de SnO2 [21], tels que le dépôt chimique en phase vapeur [22], la méthode synthétique solvothermique [23], la méthode modèle [24], la méthode sol-gel [25] et la voie hydrothermale [26]. Parmi elles, les voies solvothermiques et hydrothermales à faible coût [27], à haut rendement et à manipulation simple se sont avérées être les méthodes prometteuses pour synthétiser le SnO2 hiérarchique 3D. nanostructures. Par exemple, Dong et al. préparé creux SnO2 nanosphères d'un diamètre allant de 200 à 400 nm en utilisant une méthode de synthèse solvothermique [28]. Li et al. a fabriqué un nouveau SnO2 semblable à un flocon de neige architecture hiérarchique avec d'excellentes propriétés de détection de gaz via une méthode hydrothermale facile [29]. De plus, Chen et al. synthétisé avec succès le SnO2 en forme de fleur hiérarchique nanofleurs épanouies construites par auto-assemblage de nombreuses nanofeuillets de forme régulière par la méthode hydrothermale conventionnelle [30].
L'application pratique de SnO2 capteurs est encore limitée dans une certaine mesure en raison de la température de fonctionnement relativement plus élevée et de la plus faible sélectivité des gaz d'essai [31]. Afin d'améliorer les propriétés de détection de gaz, les chercheurs se sont intéressés à la synthèse contrôlable de SnO2 semblable à une fleur en 3D. nanostructures avec des effets tensioactifs [32], pourtant un défi important est posé en raison de la variété des tensioactifs.
Dans la présente étude, nous rapportons une optimisation bien contrôlée de SnO2 hiérarchique 3D nanofleurs basées sur l'auto-assemblage de nanofeuillets minces à l'aide de différents tensioactifs en condition hydrothermale. Notre étude de détection de gaz systématiquement comparative entre les capteurs fabriqués se concentre sur l'effet de promotion des tensioactifs sur le comportement des capteurs. Les résultats montrent que les tensioactifs non ioniques amphiphiles, tels que le PVP et le Triton X-100, peuvent être des candidats potentiels pour optimiser la morphologie des nanofleurs 3D avec une porosité élevée et une grande surface spécifique. En particulier, le capteur basé sur PVP présente une réponse élevée, un temps de réponse rapide et une bonne sélectivité vis-à-vis de H2 S à une température relativement plus basse. De plus, un éventuel mécanisme de croissance bien contrôlé de SnO2 nanostructures est proposé.
Méthodes/Expérimental
Le citrate trisodique dihydraté et le chlorure d'étain dihydraté de Sinopharm Chemical Reagent Co., Ltd. ont été utilisés comme précurseurs du SnO2 la synthèse. La polyéthylèneimine, l'hexaméthylène tétramine, le TritonX-100 et la polyvinylpyrrolidone ont été achetés auprès d'Aldrich Chemistry et utilisés comme agents de direction de structure. De l'eau distillée a été utilisée tout au long des expériences. Tous les produits chimiques étaient de qualité analytique et utilisés tels qu'ils ont été achetés sans autre purification.
Synthèse de SnO2 Nanofleurs avec différentes architectures
Une procédure de synthèse typique avec une méthode hydrothermale simple peut être décrite comme suit (Fig. 1). Ensuite, 20 mmol Na3 C6 H5 O7 ·2H2 O et 10 mmol SnCl2 ·2H2 O ont été dissous dans la solution mélangée successivement sous agitation vigoureuse pendant 1 h à température ambiante. La solution mélangée a ensuite été transférée dans un autoclave en acier inoxydable revêtu de téflon de 100 ml et maintenue à 180 °C pendant 12 h, puis refroidie à température ambiante naturellement. Après réaction, le précipité obtenu a été recueilli par centrifugation, lavé avec de l'eau désionisée et de l'éthanol anhydre plusieurs fois, et séché à 60 °C pendant 6 h. Le SnO2 les nanofleurs ont finalement été obtenues après calcination du précipité dans un four à moufle sous air ambiant à 500 °C pendant 2 h. Afin de synthétiser SnO2 nanofleurs avec différentes microstructures, différents agents tensioactifs (1,0 g) ont été introduits dans la solution respectivement avant la dissolution de Na3 C6 H5 O7 ·2H2 O. Dans ce travail, quatre types différents de tensioactifs ont été utilisés, notamment le PVP, le PEI, le HMT et le TritonX-100, et les produits finaux correspondants sont nommés SPVP , SÎ.-P.-É. , SHMT , et STritonX-100 , respectivement, tandis que le produit sans tensioactif est signé S0 .
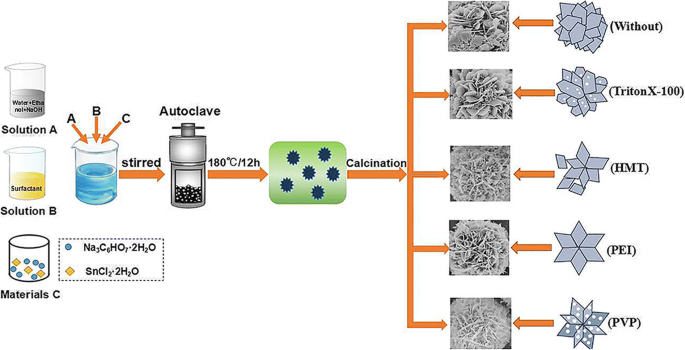
Illustration schématique du processus de formation du SnO2 en forme de fleur hiérarchique nanostructures utilisant différents types de tensioactifs
Caractérisations
Il est bien connu que les propriétés de détection de gaz des capteurs de gaz sont étroitement liées à la morphologie, la taille et la dispersibilité des nanomatériaux. Les produits tels que préparés ont été analysés en termes de structures et de morphologies au moyen de la diffraction des rayons X polycristallins (XRD, Allemagne Bruker AXS D8 Advance), de la microscopie électronique à balayage (SEM, USA FEI Sirion 200) et de la microscopie électronique à transmission à émission de champ. (FETEM, États-Unis Tecnai G2 F20 S-TWIN). La surface est mesurée à l'aide de l'analyseur élémentaire (USA ASAP 2460) basé sur la méthode Brunauer-Emmett-Teller (BET).
Fabrication de capteurs et test de détection de gaz
Le capteur de gaz a été fabriqué à l'aide d'une méthode de sérigraphie sur le dessus d'un tube d'alumine (voir la figure 2a). Typiquement, une quantité appropriée de poudre telle que préparée a d'abord été mélangée avec de l'éthanol anhydre pour former une suspension en suspension. Par la suite, la suspension en suspension a été appliquée sur le tube d'alumine par une petite brosse, qui est supportée par deux électrodes Au et quatre fils conducteurs Pt. Ensuite, un fil chauffant Ni-Cr a été inséré dans le tube d'alumine pour contrôler la température de travail en réglant la tension de chauffage. Enfin, le produit a été vieilli à 80 °C pendant 72 h avant d'être testé.

un Schéma de principe de la configuration du capteur de gaz. b Schéma électrique du dispositif capteur
Les propriétés de détection de gaz ont été mesurées à l'aide d'un système d'analyse intelligent de détection de gaz (Beijing Elliott Technology Co., Ltd., Chine) dans des conditions de laboratoire. La figure 2b affiche le circuit électrique schématique typique. Rs est la résistance du capteur et Rl est la résistance de charge, et une tension de chauffage (Vh ) est utilisé pour régler la température de travail. Dans le présent travail, la réponse du capteur a été définie comme S = (Rs − Rg )/Rg , où Rs est la résistance initiale et Rg est la résistance après injection de gaz. Les temps de réponse et de récupération sont définis comme le temps mis par le capteur pour atteindre 90 % du changement total de résistance dans le cas de l'adsorption et de la désorption, respectivement.
Résultats et discussion
Caractérisation structurale et morphologique
La phase cristalline du SnO2 tel que préparé produits a été identifié par diffraction des rayons X de puissance comme le montre la Fig. 3. À partir du diagramme XRD, tous les pics de diffraction observés peuvent être facilement attribués à la structure rutile tétragonale du SnO2 pur avec la carte de fichier standard JCPDS no. 41-1445, et aucun autre pic ne peut être identifié en raison d'impuretés. Les pics nets indiquent le haut degré de cristallinité de notre SnO2 échantillons, et aucun décalage notable n'est détecté dans les pics de diffraction, révélant que les échantillons sont d'une grande pureté.
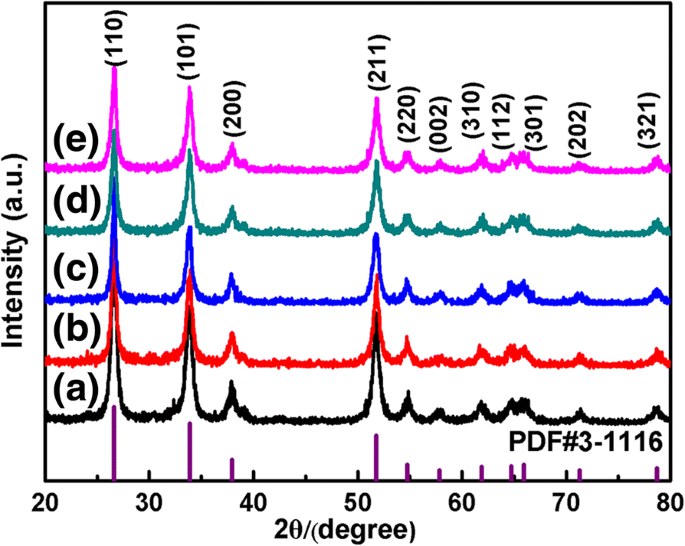
Modèles XRD du SnO2 échantillons de morphologies différentes. un S0 , b STritonX100 , c SHMT , d SÎ.-P.-É. , et e SPVP
La figure 4a montre l'image SEM du produit sans tensioactif. Une architecture hiérarchique en forme de fleur peut être observée et les nanofleurs uniques sont assemblées par des nanofeuilles ultrafines d'une épaisseur moyenne de 20 nm environ. Malheureusement, ces nanofeuillets sont étroitement décalés les uns par rapport aux autres, ce qui se traduit par une forte diminution de ses espaces de réaction. La figure 4b-e montre les morphologies des produits obtenus en introduisant différents agents tensioactifs tout en gardant les autres conditions expérimentales inchangées. On peut voir que lors de l'ajout de tensioactif TritonX-100 (Fig. 4b), les nanofeuillets sont faiblement intersectés les uns avec les autres, et certains mésopores sont façonnés au bord des nanofeuillets. Lorsque du HMT a été ajouté au mélange réactionnel en tant qu'agents tensioactifs (Fig. 4c), on peut voir que les nanofeuillets sont disposés de manière aléatoire et qu'un certain nombre de nanofeuillets plus petits sont formés entre les nanofeuillets ultrafins. La figure 4d montre les images SEM des produits obtenus en introduisant le tensioactif PEI dans la solution de précurseur, ce qui révèle que les nanofeuillets avec des surfaces lisses sont disposés de manière ordonnée et se coupent verticalement les uns avec les autres, laissant un plus grand espace de réaction. La figure 4e, f présente les images SEM typiques des produits obtenus lors de l'ajout de tensioactif PVP dans les mêmes conditions. On peut voir que les nanofeuillets sont uniformément répartis le long du rayon sur tout l'échantillon pour former une structure en forme de fleur. De plus, par rapport aux autres structures du STritonX-100 , SHMT , et SÎ.-P.-É. , les nanofeuillets de SPVP sont enfermés dans un cône triangulaire inversé avec un espace creux relativement plus grand (Fig. 4e). Une image agrandie plus loin révèle que les architectures en forme de fleur sont assemblées par des nanofeuillets mésoporeux pour former une structure hiérarchique poreuse ouverte, et chaque nanofeuille a été fabriquée avec de nombreux mésopores (Fig. 4f).

Les images SEM du SnO2 nanofleurs de morphologies différentes. un S0 , b STritonX-100 , c SHMT , d SÎ.-P.-É. , et e , f SPVP
Afin d'étudier plus avant les microstructures et les propriétés cristallines des nanofleurs, un MET à faible grossissement et un HRTEM typique combinés avec les techniques d'analyse de diffraction électronique de zone (SAED) sélectionnées sont utilisés. À partir des images MET (Fig. 5a-e), on peut voir que les nanofleurs d'un diamètre moyen de 3 μm sont assemblées de nombreuses nanofeuillets individuels, et sa morphologie et sa taille sont similaires aux images SEM. Surtout, l'image TEM de SPVP (Fig. 5e) montre que la structure la plus semblable à une fleur avec la couleur foncée uniforme dans la région médiane est construite à partir de la dispersion de puits de nombreuses nanofeuillets uniformes le long de la direction du rayon. En combinant le SEM avec les mesures TEM, une conclusion peut être tirée que les structures obtenues lors de l'ajout de tensioactif PVP sont les plus stables. Les images TEM haute résolution (HRTEM) montrent que pour les échantillons S0 , SHMT , SÎ.-P.-É. , et SPVP , l'espacement de réseau de 0,335 nm observé est cohérent avec le plan de réseau (110) du rutile tétragonal SnO2 (La figure 5f ne montre qu'une image HRTEM typique pour SHMT en tant que représentant). L'exposition du plan de réseau (110) révèle que le plan de réseau (110) est le plan le plus stable pour SnO2 dans l'air, ce qui est cohérent avec l'étude théorique. A noter que le STritonX-100 est un cas particulier dans ce travail (Fig. 5b). Lors de l'ajout de tensioactif TritonX-100, la croissance et la dispersion des nanofeuilles conduisent de manière aléatoire à un diamètre relativement plus grand (3 ~ 4 μm ) des nanofleurs par rapport aux autres échantillons. De plus, son image HRTEM montre que l'espacement de réseau calculé est de 0,264 nm, ce qui correspond au plan de réseau (101) de la structure rutile tétragonale de SnO2 . De plus, le modèle SAED révèle que SPVP a une structure monocristalline presque parfaite, et les taches de diffraction correspondent à (110),(\( 1\;\overline{1}\;0 \)), (\( \overline{1}\;1\;0 \)), et (200) plans de réseau de SnO2 (Fig. 5h). Au contraire, pour d'autres échantillons tels que S0 , SHMT , SÎ.-P.-É. , et STritonX-100 , le motif SAED montre une structure polycristalline et l'anneau de diffraction est indexé sur les plans (110), (101) et (211) de la structure rutile tétragonale de SnO2 (Fig. 5g).
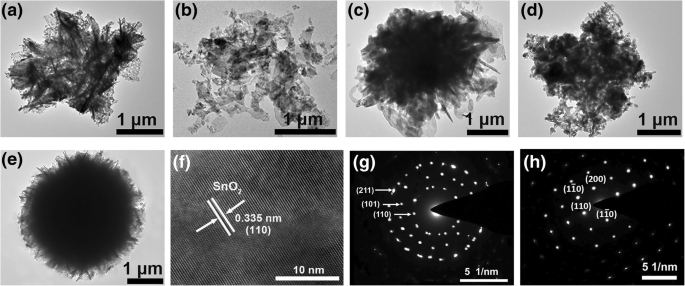
Images MET à faible grossissement de SnO2 échantillons. un S0 , b STritonX-100 , c SHMT , d SÎ.-P.-É. , et e SPVP . f Micrographie HRTEM montrant des images de réseau agrandies de SHMT . g Modèles SAED de S0 . h Modèles SAED de SPVP
Mécanisme de croissance du SnO2 Nanofleurs
Sur la base des observations expérimentales et de l'analyse ci-dessus, on pense que les tensioactifs jouent un rôle important dans la formation de divers SnO2 nanofleurs [33]. Le mécanisme de croissance possible de la feuille-fleur hiérarchique SnO2 nanostructures est brièvement illustré sur la Fig. 1. Dans ce travail, tous les SnO2 les nanofleurs sont synthétisées à l'aide de SnCl2 comme précurseur [34]. Dans les conditions hydrothermales, la réaction globale pour la croissance de SnO2 les cristaux à haute température et pression peuvent être exprimés comme suit [35] :
$$ {\mathrm{SnCl}}_2+2{\mathrm{OH}}^{-}\à \mathrm{Sn}{\left(\mathrm{OH}\right)}_2+2{\mathrm{ Cl}}^{-} $$ (1) $$ \mathrm{Sn}{\left(\mathrm{OH}\right)}_2\à \mathrm{Sn}\mathrm{O}+{\mathrm{ H}}_2\mathrm{O} $$ (2) $$ \mathrm{SnO}+\frac{1}{2}{\mathrm{O}}_2\à {\mathrm{SnO}}_2 $$ (3) $$ \mathrm{Sn}{\left(\mathrm{OH}\right)}_2+\frac{1}{2}{\mathrm{O}}_2+{\mathrm{H}}_2\mathrm {O}\à \mathrm{Sn}{\left(\mathrm{OH}\right)}_4\à {\mathrm{SnO}}_2+2{\mathrm{H}}_2\mathrm{O} $ $ (4)Pendant tout le processus, trois produits chimiques affectent considérablement la croissance morphologique de SnO2 nanofleurs, y compris NaOH, le citrate de sodium et le tensioactif. Premièrement, un certain nombre de minuscules nanocristaux primaires se sont formés en raison de l'hydrolyse de Sn 2+ dans une solution basique éthanol-eau ainsi que sa réaction rapide avec OH − ions de NaOH. A noter que le milieu basique éthanol-eau est important pour stimuler le SnO2 nucléation et croissance [36]. L'ajout de citrate de sodium joue un rôle crucial dans la distribution spatiale des précurseurs en raison de sa forte capacité de coordination, qui peut favoriser une anisotropie dans la croissance rapide et l'agrégation de SnO2 nanofeuillets avec la force motrice de la diminution de l'énergie de surface et accélèrent l'assemblage des nanofeuillets dans les nanofleurs florissantes hiérarchiques stables [37].
Généralement, l'ajout de tensioactifs est favorable à l'agrandissement de la surface ainsi qu'à l'amélioration de l'activité de surface [38]. Parmi les tensioactifs utilisés dans ce travail, le PEI est un type de tensioactifs cationiques. Lorsque le PEI est ajouté dans les solutions réactionnelles, en raison du N + existant ions à queue hydrophile, le PEI s'adsorbera préférentiellement sur une certaine facette cristalline, ce qui est propice à la nucléation de SnO2 nanocristaux ainsi que la croissance ordonnée de SnO2 nanofeuillets avec une sélectivité directionnelle. Le PVP et le TritonX-100 sont tous deux des tensioactifs non ioniques amphiphiles, qui peuvent servir de modèle souple dans la fabrication de matériaux mésoporeux. Prenons par exemple PVP pour expliquer le mécanisme de croissance des structures poreuses sur le SnO2 nanofeuillets comme suit :lorsque le PVP est ajouté à la solution, les molécules de PVP s'auto-assemblent en micelles sphériques en raison de la forte attraction hydrophobe entre les queues alkyles droites. En raison de son amphiphilie, le radical hydrophile se déplacera vers la direction de la solution aqueuse, et le radical hydrophobe se déplacera dans la direction opposée, conduisant à la formation de domaines inorganiques autour des micelles PVP disposées périodiquement. Ensuite, Sn 2+ et OH − les ions sont facilement adsorbés sur les surfaces externes de ces micelles via des interactions électrostatiques jusqu'à SnCl2 est oxydé en SnO2 nanofeuillet, qui sont suivis de l'auto-assemblage de nanofeuillets en nanofleurs épanouies à l'aide de citrate de sodium. Enfin, les micelles de PVP soft-template sont retirées au cours du processus de calcination, produisant un SnO2 hiérarchique nanofleurs à structures mésoporeuses. Bien que le PVP et le Triton X-100 aient tous deux contribué à la formation de structures poreuses, il convient de noter que le PVP peut également jouer un rôle d'agent dispersant, ce qui rend le SnO2 les nanofeuillets se développent plus uniformément et séparément en raison des interactions fortes et des courtes distances d'interaction électrostatique entre le SnO2 nanofeuillets et PVP.
Propriétés de détection de gaz
Comme indiqué précédemment, les nanostructures hiérarchiques en forme de fleur étaient favorables à l'absorption et à la diffusion des gaz de sonde dans les matériaux des capteurs. Pour faire la lumière sur l'effet de promotion des tensioactifs et la morphologie correspondante sur le comportement des capteurs, une étude de détection de gaz systématiquement comparative entre les capteurs fabriqués est réalisée dans ce travail.
Comportements de détection de gaz des capteurs fabriqués à l'éthanol
La température de fonctionnement optimale est un facteur clé pour l'application des capteurs de gaz à oxyde semi-conducteur. Tout d'abord, les réponses des capteurs à 100 ppm d'éthanol gazeux à diverses températures de fonctionnement de 180 à 360 °C sont testées, comme le montre la figure 6a. Il est clairement observé que tous ces capteurs présentent un comportement de détection de gaz similaire, c'est-à-dire que les valeurs de réponse augmentent d'abord avec une augmentation de la température, atteignent une valeur maximale à 270 °C, puis diminuent progressivement avec une nouvelle augmentation de la température. Par conséquent, 270 °C peut être choisi comme température de fonctionnement optimisée pour l'étude de détection de gaz de tous les SnO2 fabriqués en forme de fleur. capteurs dans notre travail. La raison de la dépendance de la réponse à la température est la suivante :lorsque la température de fonctionnement est trop basse, une valeur de réponse relativement plus petite est attribuée à la réponse inerte due à l'activation chimique, tandis que pour une température de fonctionnement trop élevée, la cible de gaz absorbé les molécules peuvent s'échapper des capteurs avant les réactions, ce qui entraîne également une mauvaise réponse. De plus, on peut voir sur la Fig. 6a que de tous les cinq SnO2 capteurs à base de différents tensioactifs, SPVP montre la réponse la plus élevée au gaz éthanol et la plus grande valeur de réponse au gaz (38). Les valeurs de réponse maximales des quatre autres capteurs sont de 27 pour SPEI , 16 pour SHMT , 11 pour STritonX-100 , et 8 pour S0 .
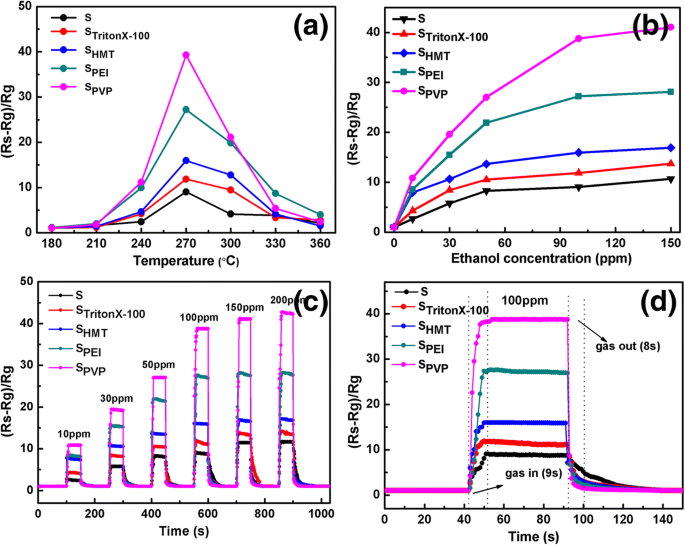
un La réponse des capteurs à 100 ppm d'éthanol à différentes températures de fonctionnement (180-360 °C). b Les courbes de réponse dynamique des capteurs à l'éthanol avec différentes concentrations (10-150 ppm) à 270 °C. c Courbes de réponse en fonction du temps des capteurs à 10-200 ppm d'éthanol consécutivement à 270 °C. d Détection dynamique transitoire des capteurs à 100 ppm d'éthanol à 270 °C
La figure 6b montre la réponse de tous les SnO2 capteurs vers l'éthanol dans la plage de concentration de 10 à 150 ppm à la température de travail optimale de 270 °C. On peut clairement observer que la réponse de tous les capteurs augmente rapidement avec la concentration de gaz en dessous de 50 ppm, et cette tendance devient lisse de 50 à 150 ppm, tendant à être saturée à environ 100 ppm. Comme prévu, les tensioactifs et les morphologies induites peuvent produire une grande influence sur la détection de gaz des capteurs fabriqués. Parmi ces capteurs fabriqués, le SPVP le capteur présente le meilleur comportement de détection vis-à-vis de l'éthanol gazeux et SPEI vient en second. Pour obtenir un aperçu approfondi du mécanisme de détection de gaz, une adsorption-désorption d'azote BET (Brunaure-Emmett-Teller) est également effectuée pour déterminer les surfaces spécifiques de ces échantillons, comme indiqué dans le tableau 1. On peut voir que S Î.-P.-É. a la plus grande surface spécifique (38,4 m 2 g −1 ) à la majorité absolue. Il est à noter que malgré la surface relativement plus petite (15,5 m 2 g −1 ), SPVP est le meilleur candidat pour le capteur de gaz éthanol en raison de son architecture en forme de fleur parfaite avec un auto-assemblage ordonné et une porosité relativement plus élevée, fournissant des sites d'adsorption plus actifs pour les molécules d'éthanol. Même à une faible concentration d'éthanol de 10 ppm, la sensibilité de S0 , STritonX-100 , SHMT , SÎ.-P.-É. , et SPVP les capteurs peuvent atteindre 2, 4, 7, 9 et 11, respectivement, indiquant leur application potentielle pour les capteurs d'éthanol même à de faibles concentrations.
La figure 6c affiche les courbes dynamiques de réponse et de récupération de détection de gaz des capteurs fabriqués vers l'éthanol avec une température de fonctionnement de 270 °C, à partir de laquelle on peut voir que les réponses de tous les capteurs fabriqués augmentent avec l'augmentation de la concentration en éthanol, et une remarquable modulation de la résistance est atteint à environ 100 ppm. Les réponses montrent une augmentation drastique une fois que le capteur a été exposé aux gaz cibles, puis a chuté à sa valeur initiale dans l'air. Comme le montre la figure 6d, le temps de réponse et de récupération à 100 ppm d'éthanol est d'environ 16 s et 28 s pour S0 , 14 s et 18 s pour le STritonX-100 , 11 s et 15 s pour SHMT , 9 s et 11 s pour SÎ.-P.-É. , et 5 s et 8 s pour SPVP , respectivement. Il est évident que le SPVP le capteur a les meilleures caractéristiques de réponse/récupération par rapport aux autres capteurs.
Le tableau 2 présente une comparaison des performances de détection d'éthanol sur la base de différents SnO2 approches fabriquées rapportées dans d'autres littératures et ce travail à la concentration de 100 ppm. On peut voir que notre polyporeux SnO2 nanoflower présente des comportements de détection d'éthanol remarquables avec une température de fonctionnement optimale plus basse et une valeur de réponse plus élevée ainsi qu'un temps de récupération de réponse plus rapide, ce qui pourrait être attribué à la présence de nombreux mésopores dans le capteur SPVP, conduisant à une porosité élevée en faveur de l'adsorption et diffusion de gaz éthanol.
Comportements de détection de gaz des capteurs fabriqués à H2 S
Comme discuté dans la sous-section précédente, SPVP Le capteur présente la meilleure propriété de détection de gaz à 100 ppm d'éthanol en raison de sa porosité élevée. Afin de connaître son gaz de détection optimal, nous testons la réponse de SPVP capteur vers différents gaz, y compris l'acétone, le méthanol, le formaldéhyde et H2 S, avec une concentration de 100 ppm à différentes températures de fonctionnement (comme indiqué sur la Fig. 7a, b). On peut noter que la réponse optimale apparaît à 330 °C de méthanol, à 210 °C de formaldéhyde, à 360 °C d'acétone, et à 180 °C de H2 S. De plus, la valeur de réponse maximale de SPVP à H2 S est estimé à 368, ce qui correspond à un ou deux ordres de grandeur (\( {\mathrm{S}}_{{\mathrm{H}}_2\mathrm{S}}/{\mathrm{S}}_ {\mathrm{éthanol}}=9 \), \( {\mathrm{S}}_{{\mathrm{H}}_2\mathrm{S}}/{\mathrm{S}}_{\mathrm{ formaldéhyde}}=45 \)) supérieur à celui des autres gaz d'essai. La température de travail optimale la plus basse ainsi que la meilleure valeur de réponse indiquent SPVP a l'excellente sélectivité à H2 S.
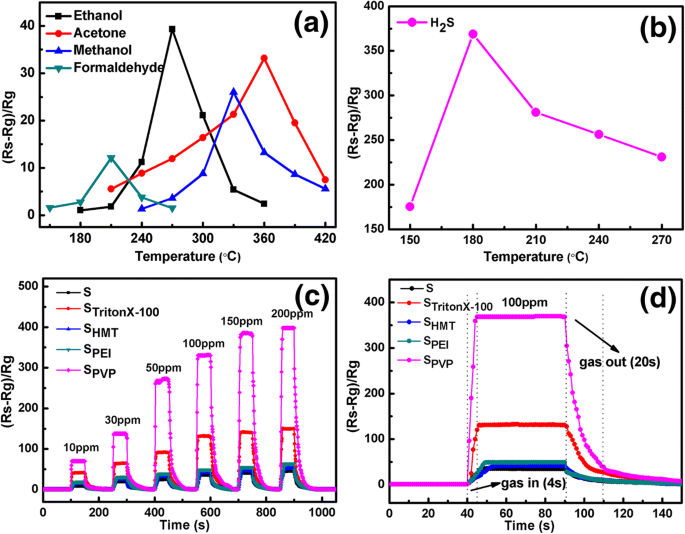
un Réponse de SPVP capteur à 100 ppm d'éthanol, d'acétone, de méthanol et de formaldéhyde à différentes températures de fonctionnement. b Réponse de SPVP capteur à 100 ppm H2 S à différentes températures de fonctionnement. c Courbes de réponse en fonction du temps des capteurs jusqu'à 10-200 ppm H2 S consécutivement à 180 °C. d Détection dynamique transitoire des capteurs à 100 ppm H2 S à 180 °C
Compte tenu de la forte réponse de SPVP capteur à H2 S, nous avons également effectué une mesure systématique de détection de gaz de tous les autres capteurs. Une réponse dynamique de détection de gaz et des courbes de récupération des capteurs fabriqués vers H2 S à 180 °C sont affichés sur la Fig. 7c. De toute évidence, les valeurs de réponse de tous les capteurs fabriqués montrent une fonction croissante monotone de H2 concentration S. Pour 100 ppm H2 S, le temps de réponse et de récupération est d'environ 9 s et 43 s pour S0 , 5 s et 30 s pour le STritonX-100 , 14 s et 40 s pour SHMT , 8 s et 38 s pour SÎ.-P.-É. , et 4 s et 20 s pour SPVP , tandis que les valeurs de réponse maximales sont de 35, 132, 41, 49 et 368 pour S0 , STritonX-100 , SHMT , SÎ.-P.-É. , et SPVP , respectivement. Il est évident que le SPVP le capteur a les meilleures caractéristiques de réponse/récupération et la réponse la plus élevée à H2 gaz S par rapport à d'autres capteurs, tandis que STritonX-100 atteint le deuxième.
La figure 8 affiche le graphique à barres de la réponse de cinq capteurs fabriqués au formaldéhyde, au méthanol, à l'éthanol, à l'acétone et au H2 S. Tous les gaz ont été testés avec une concentration de 100 ppm à la température de fonctionnement optimale. STritonX-100 et SPVP montre une réponse distincte à H2 S, tandis que SÎ.-P.-É. montre la réponse de gaz la plus élevée au méthanol et à l'acétone. Il convient de mentionner que la surface spécifique et la porosité sont deux facteurs importants pour les capteurs de gaz. La plus grande surface spécifique fournira des sites plus actifs pour l'adsorption et la désorption des gaz d'essai, tandis que la plus grande porosité induirait une plus grande vitesse de diffusion des gaz en raison de la présence de mésopores. En comparaison, SÎ.-P.-É. possède une surface spécifique relativement plus grande que les autres (voir le tableau 1), ce qui montre la réponse de gaz la plus élevée au méthanol et à l'acétone (Fig. 8), tandis que SPVP et STritonX-100 présentent la réponse gazeuse la plus élevée à H2 S due to their polyporous flower-like nanostructures, proving good selectivity of STritonX-100 and SPVP toward H2 S. The good selectivity of the samples to H2 S can be explained as follows:when the SnO2 sensor is exposed in H2 S gas, both chemisorbed oxygen species and SnO2 nanostructure react with H2 S during sensing measurement to form SO2 and SnS2 , respectivement. Compared with SnO2 , the body resistance of SnS2 is relatively smaller, leading to the sensitivity enhancement of the gas sensor [39]. On the contrary, the SnO2 sensor does not react with any other target gases, such as formaldehyde, methanol, ethanol, and acetone.
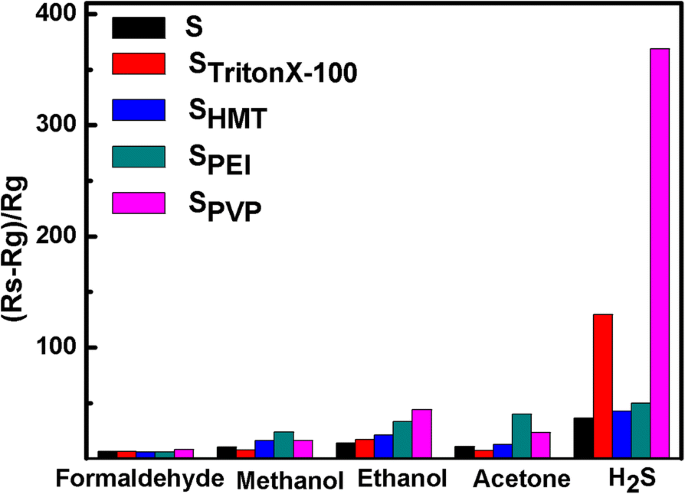
The comparison among sensor response of SnO2 nanomaterials to 100 ppm of various gases at the optimal operating temperature
Good stability and long service duration are expected from the viewpoint of practical application. To verify the stability of the sensor, the successive gas-sensing behavior of SPVP to 100 ppm ethanol was tested under the same conditions after 1 month. The samples were stored in the vacuum drying vessel during the 1-month interval. It can be seen from Fig. 9 that SPVP exhibits an excellent repeatability and stability even after 1 month. The three cyclic curves are similar to that measured 1 month ago, including the response value as well as the response-recovery time.
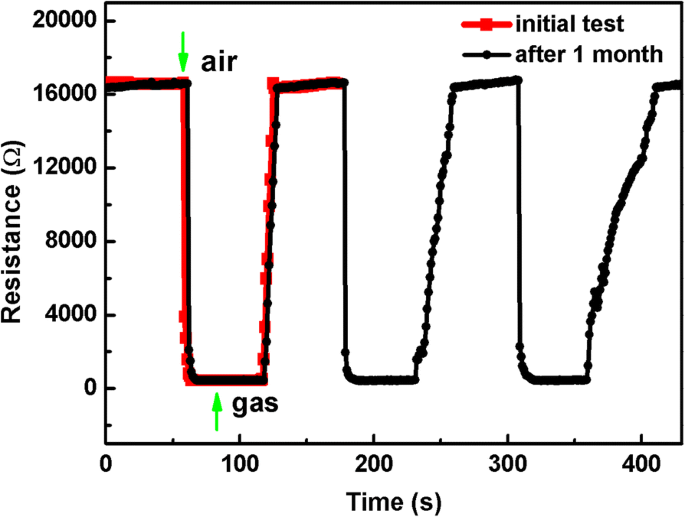
Stability of SPVP over 1 month of aging for 100 ppm ethanol at 270 °C
Gas-Sensing Mechanism
Up to now, the most widely accepted gas-sensing mechanism of semiconductor oxide is the model based on the electron transfer dynamics during an adsorption–oxidation–desorption process, which can change the resistance value of the sensors [40]. The response of typical n-type semiconductor greatly depends on the electron concentration. As shown in Fig. 10, at elevated temperature, electrons in the valence band are thermally excited to the conductive band. Once the SnO2 sensor is exposed to ambient air, oxygen molecules will be chemisorbed on the surface of SnO2 nanoflowers. Oxygen ions (O2 − , O − , and O 2− ) are then formed by capturing electrons from the conductive band of SnO2 [41], which is accompanied by an effective enlargement of electron-depleted layer. As a typical n-type semiconductor, the broadening of electron-depleted region means the decrease of carrier concentration within SnO2 nanoflowers, which will lead to the increase of resistance of the sensors. Conversely, when the SnO2 sensor is exposed in the reductive ambient, the absorbed oxygen species will quickly react with the target gas, which results in releasing the trapped electrons back to the conduction band and a reduction of the resistance of the sensors. Among the sensors fabricated in this work, SPEI and SPVP show relative better gas-sensing performances. The underlying physical mechanisms are as follows:the gas sensing properties are strongly dependent on the surface special area and the porosity. In comparison, SPEI possesses a relative larger specific surface area than others, which will provide more active sites for adsorption and desorption of test gases. SPVP exhibits a relative higher porosity due to the polyporous flower-like nanostructures, which is favorable to the rapid diffusion of gas (as shown in Fig. 10).
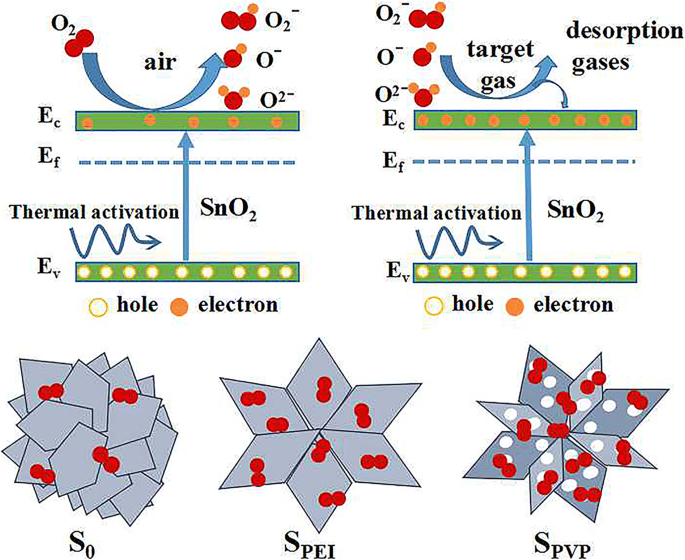
Schematic diagrams on the gas-sensing mechanism of flower-like SnO2 hierarchical nanostructures
Conclusions
We have successfully prepared the 3D hierarchical flower-like SnO2 nanostructures through a simple and low-cost facile hydrothermal route with the assistance of different surfactants. The images of SEM and TEM showed that the fabricated 3D hierarchical SnO2 nanoflowers with an average diameter of 2~4 μm were composed of many 2D nanosheets. The addition of surfactant plays an important role in the formation of nanoflowers. Based on the experimental observations, the possible growth process and gas-sensing mechanism of SnO2 nanoflowers were proposed. As a cationic surfactant, the addition of PEI is conducive to the nucleation of SnO2 nanocrystals as well as the orderly growth of SnO2 nanosheets, leading to a relative larger specific surface area. As amphiphilic non-ionic surfactants, PVP and TritonX-100 can make the nanosheets grow more uniformly and separately, which can serve as a soft template in the synthesis of advanced material, especially in the fabrication of mesoporous materials. In comparison, the sensor with the help of PVP (SPVP ) exhibits excellent gas-sensing performances to ethanol and H2 S due to its relative higher porosity. Especially, SPVP shows a high response (368), fast response/recovery time (4 s/20 s), and good selectivity toward H2 S gas. In addition, it is found that NaOH and sodium citrate are also important for the morphological formation of SnO2 nanoflowers.
Abréviations
- 1D:
-
One-dimensional
- 2D:
-
Two-dimensional
- 3D:
-
Three-dimensional
- BET:
-
Brunauer-Emmett-Teller
- FETEM:
-
Field emission transmission electron microscopy
- HMT:
-
Hexamethylene tetramine
- Na3 C6 H5 O7 ·2H2 O:
-
Trisodium citrate dihydrate
- Île-du-Prince-Édouard :
-
Polyethyleneimine
- PVP:
-
Polyvinylpyrrolidone
- SAED :
-
Selected area electron diffraction
- SEM :
-
Microscopie électronique à balayage
- XRD :
-
X-ray diffraction
Nanomatériaux
- L'effet du plasma de contact hors équilibre sur les propriétés structurelles et magnétiques des spinelles Mn Х Fe3 − X О4
- Propriétés paramagnétiques des nanomatériaux dérivés du fullerène et de leurs composites polymères :effet de pompage drastique
- Propriétés des oscillations électromagnétiques longitudinales dans les métaux et leur excitation sur des surfaces planes et sphériques
- Influence de l'eau sur la structure et les propriétés diélectriques de la microcristalline et de la nano-cellulose
- Réglage des morphologies de surface et des propriétés des films de ZnO par la conception de la couche interfaciale
- Nanocomposites de poly(N-isopropylacrylamide) magnétique :effet de la méthode de préparation sur les propriétés antibactériennes
- Synthèse de points quantiques de sulfure d'antimoine solubles dans l'eau et de leurs propriétés photoélectriques
- Synthèse facile d'oxyde d'étain mésoporeux semblable à un trou de ver via l'auto-assemblage induit par l'évaporation et les propriétés de détection de gaz améliorées
- Types de métaux et leurs propriétés



