Amélioration des performances électrochimiques du matériau cathodique à structure spinelle LiNi0.5-xGaxMn1.5O4 par dopage Ga
Résumé
Une méthode sol-gel a été adoptée pour obtenir LiNi0,5-x Gax Mn1,5 O4 (x = 0, 0,04, 0,06, 0,08, 0,1) échantillons. L'effet du dopage Ga sur LiNi0,5 Mn1,5 O4 et son contenu optimal ont été étudiés, et les propriétés électrochimiques à température ambiante et à haute température ont été discutées. Les caractéristiques structurelles, morphologiques et vibrationnelles de LiNi0.5-x Gax Mn1,5 O4 (x = 0, 0,04, 0,06, 0,08, 0,1) les composés ont été caractérisés par diffraction des rayons X (XRD), microscopie électronique à balayage (MEB) et spectroscopie infrarouge à transformée de Fourier (FT-IR). Les résultats XRD démontrent que tous les échantillons ont une structure spinelle désordonnée avec un groupe spatial de Fd3m, et le dopage Ga restreint la formation du Lix Ni1-x O phase secondaire. L'analyse FT-IR révèle que le dopage au Ga augmente le degré de désordre cationique. Les résultats du MEB révèlent que tous les échantillons possèdent un fin cristal d'octaèdre de spinelle. Les performances électrochimiques des échantillons ont été étudiées par des tests de charge/décharge galvanostatique, des tracés dQ/dV et une spectroscopie d'impédance électrochimique (EIS). Le LiNi0.44 Ga0,06 Mn1,5 O4 l'échantillon avec le contenu optimal montre une performance de débit et une stabilité de cycle supérieures après dopage au Ga, en particulier à un débit de décharge élevé et à haute température. De plus, le LiNi0.44 Ga0,06 Mn1,5 O4 l'échantillon a conservé 98,3 % de sa capacité initiale de 115,7 mAhg −1 au taux de décharge de 3 C après 100 cycles, alors que l'échantillon vierge a fourni une capacité de décharge de 87,3 mAhg −1 à 3 C avec une capacité de rétention de 80% au 100ème cycle. Comparé au matériau vierge, le LiNi0.44 Ga0,06 Mn1,5 O4 l'échantillon a montré une capacité de rétention élevée de 74 à 98,4 % après 50 cycles à un taux de décharge de 1 C et de 55 °C.
Contexte
Avec l'utilisation croissante des batteries lithium-ion, leurs exigences augmentent également. Des batteries à longue durée de vie, à haute densité énergétique et à faible coût pourraient répondre aux besoins des consommateurs. Spinelle LiNi0,5 Mn1,5 O4 (LNMO) a attiré l'attention des chercheurs dans des domaines connexes [1] en raison de son potentiel de travail élevé [2], de son faible coût [3] et de sa densité énergétique élevée [4] de 658 Wh kg −1 . Tous les avantages de LiNi0.5 Mn1,5 O4 sont dus à son chemin de diffusion lithium-ion tridimensionnel et à sa tension de fonctionnement élevée [5].
Cependant, le spinelle LiNi0,5 Mn1,5 O4 les matériaux ont également plusieurs problèmes à résoudre. Premièrement, un Lix Ni1-x O phase secondaire se forme au cours du processus de préparation du spinelle LiNi0,5 Mn1,5 O4 matériaux [6]. Deuxièmement, l'électrolyte est sujet à la décomposition à haute tension de fonctionnement (4,7 V) (vs Li/Li + ) [1], ce qui entraîne une diminution de capacité et de mauvaises performances électrochimiques.
De nombreuses tentatives ont été proposées pour améliorer les performances électrochimiques. Le dopage élémentaire et l'application de revêtements, tels que le dopage Cr [7], Mg [8], Y [9], Ce [10], Al [11], Cu [12] et Ga [13], ainsi que BiFeO3 [14] et Al2 O3 [15] revêtements, pourraient améliorer la durée de vie du cycle ou les performances de taux de LiNi0,5 Mn1,5 O4 échantillons à des degrés divers. Par exemple, LiNi dopé Ce0,5 Mn1,5 O4 peut améliorer la stabilité du cycle (rétention de capacité de 94,51 % après 100 cycles) [10], Al2 O3 couche de revêtement réduit les réactions secondaires survenues. La première enquête sur la substitution de sites Mn par Ga dans le LiMn2 O4 La structure spinelle a été rapportée par Liu et al. Ils ont découvert que le dopage au Ga peut inhiber la distorsion coopérative Jahn-Teller de la structure spinelle [16]. En 2011, Shin et al. ont publié un article dans lequel ils ont déterminé que les échantillons dopés au Ga peuvent former une interface plus stable et stabiliser la structure du spinelle en raison de la présence de Ga à la surface des échantillons [13]. Un an plus tard, Shin [17] a synthétisé LiMn1.5 Ni0,5 − x Mx O4 (M = Cr, Fe et Ga) par une méthode de précurseur d'hydroxyde et a constaté que l'échantillon dopé au Ga et l'échantillon vierge présentent une baisse de la capacité de vitesse après recuit à 700 °C. De plus, ils ont également constaté que la faible capacité de débit était causée par la ségrégation étendue de Ga 3+ après recuit. Wei Wu et al. ont publié un article dans lequel ils avancent que la caractéristique de la méthode à l'état solide est que les particules n'étaient pas uniformes en taille et en distribution [9]. La méthode sol-gel est en faveur de la formation d'octaèdres bien cristallisés et d'une distribution de particules étroite selon Wang [18]. Cependant, peu d'attention a été consacrée à l'étude systématique de la capacité de débit et de la conductivité électrique à différentes teneurs de dopage au Ga et du rôle du Ga à haute température. Comprendre comment les concentrations de dopage au Ga influencent les propriétés électrochimiques en détail et étudier les contenus dopés au Ga appropriés de LiNi0,5 Mn1,5 O4 matériaux, des échantillons avec diverses concentrations de dopage au Ga ont été préparés par une méthode sol-gel pour la première fois. La structure, la morphologie et les performances électrochimiques des échantillons ont été étudiées systématiquement.
Résultats et discussion
Analyse structurale et morphologique
Modèles XRD du LiNi0.5-x Gax Mn1,5 O4 (x = 0, 0,04, 0,06, 0,08, 0,1) des échantillons sont fournis sur la Fig. 1, qui montre clairement que les principaux pics de diffraction des échantillons sont cohérents avec les cartes (JCPDS n° 80-2162) pour la structure spinelle désordonnée avec espace groupe Fd3m. Une autre découverte primordiale était que des pics de diffraction supplémentaires sont apparus à 37,4°, 43,7° et 63,8° (marqués d'un *) dans le LiNi0,5 Mn1,5 O4 échantillon en plus des principaux pics de diffraction, qui doivent être attribués au Lix Ni1-x O phase secondaire. Le résultat est en accord avec les résultats rapportés précédemment, dans lesquels la formation du Lix Ni1-x La phase secondaire O doit être attribuée au frittage à haute température, et elle a été considérée comme diminuant la quantité de matière active [19]. L'existence du Lix Ni1-x O phase secondaire pourrait inhiber le Li + diffusion ionique selon Wu [9]. Cependant, aucune phase secondaire supplémentaire n'a été détectée dans les échantillons dopés au Ga, suggérant que le dopage au Ga pourrait inhiber la formation de Lix Ni1-x O phases impures et fournir une seule phase.
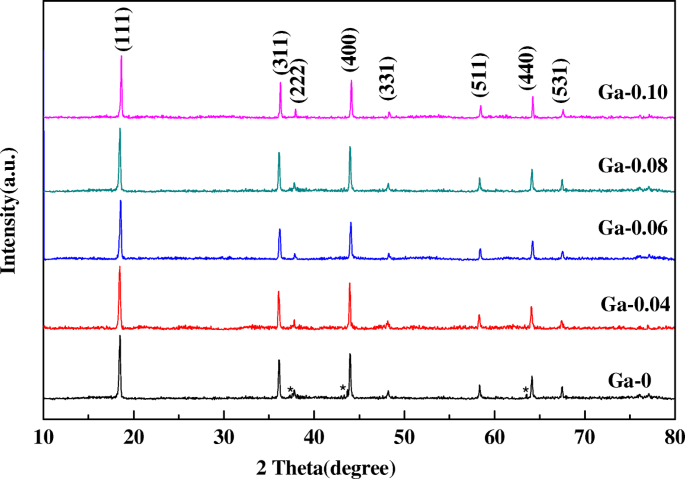
Modèles XRD du LiNi0.5-x Gax Mn1,5 O4 (x = 0, 0,04, 0,06, 0,08, 0,1) échantillons
Selon un rapport que le rapport d'intensité de I311 /I400 les pics pourraient refléter la stabilité de la structure [20], où une corrélation positive existe entre la valeur de I311 /I400 et la stabilité de la structure. Les rapports d'intensité du I311 /I400 pics pour le LiNi0,5-x Gax Mn1,5 O4 (x = 0, 0,04, 0,06, 0,08, 0,1) les échantillons sont respectivement 0,8636, 0,9115, 0,9216, 0,9097 et 0,8966 (comme indiqué dans le tableau 1). Selon la valeur de I311 /I400 , nous pouvons en déduire que le dopage au Ga peut favoriser la stabilité structurelle. De plus, le tableau 1 montre clairement l'augmentation du rapport d'intensité de I311 /I400 des pics puis une baisse à mesure que la teneur en dopage au Ga augmentait davantage ; le ratio atteint un maximum dans le LiNi0.44 Ga0,06 Mn1,5 O4 échantillon, suggérant que cet échantillon a la structure la plus stable. Le résultat est cohérent avec la courbe de performance cyclique à un taux élevé et à haute température.
Pour approfondir l'étude du groupe spatial du LiNi0.5-x Gax Mn1,5 O4 (x = 0, 0,04, 0,06, 0,08, 0,1) échantillons, la spectroscopie FT-IR (illustrée à la Fig. 2) a été réalisée dans la plage de 400 à 700 cm −1 . La clé pour déterminer le groupe spatial désordonné Fd3m et le P43 ordonné Le groupe d'espace 32 est le degré de désordre du Ni 2+ et Mn 4+ dans la structure spinelle. Les bandes à 588 et 621 cm −1 correspondent respectivement à la liaison Ni-O et à la liaison Mn-O. Une intensité de crête plus forte à 621 cm −1 plutôt qu'à 588 cm −1 est caractéristique de la structure Fd3m [21]. Kunduraci et al. [22] ont publié un article dans lequel ils ont observé que plus la valeur de I588 est faible /I621 était, plus le degré de désordre du Mn 4+ est élevé et Ni 2+ les ions dans la structure spinelle seraient. Le degré élevé de désordre cationique conduit à une conductivité élevée. Nous avons calculé les rapports d'intensité de I588 /I621 comme 0,9524, 0,9187, 0,708, 0,8525 et 0,9263 (comme indiqué dans le tableau 2) pour les échantillons Ga-0, Ga-0,04, Ga-0,06, Ga-0,08 et Ga-0,1 respectivement. Fait intéressant, la valeur de I588 /I621 diminue d'abord puis augmente avec l'augmentation de la teneur en Ga, indiquant l'augmentation du degré de désordre cationique puis une diminution suite à l'augmentation de la teneur en dopage en Ga. Ga-0.06 montre la valeur la plus basse de I588 /I621 , suggérant qu'il a le plus haut degré de désordre cationique. La valeur de I588 /I621 est inférieur à 1, caractéristique de la structure désordonnée Fd3m [21], ce qui est cohérent avec le résultat de l'analyse XRD ci-dessus. Par rapport au P4 commandé 332, la structure désordonnée Fd3m a montré de meilleures propriétés électrochimiques que celles du P4 ordonné 332 structure [23].
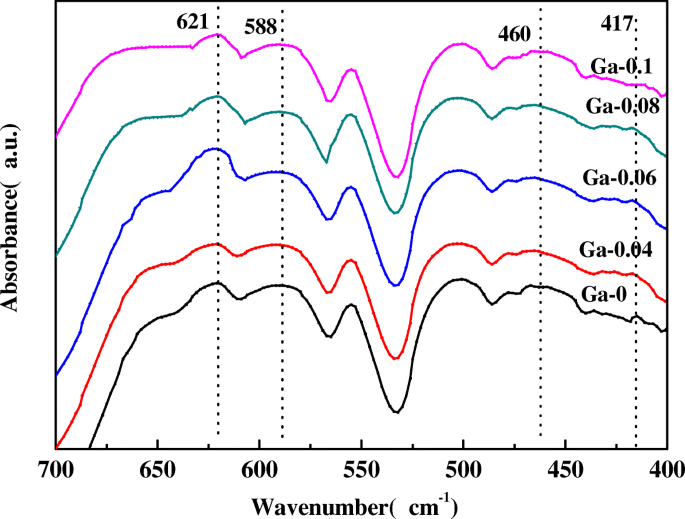
Spectres FT-IR du LiNi0,5-x Gax Mn1,5 O4 (x = 0, 0,04, 0,06, 0,08, 0,1) échantillons
Les morphologies des particules des échantillons sont observées par SEM. Les résultats, comme le montre la figure 3, impliquent que tous les échantillons ont une structure d'octaèdre de spinelle et possèdent un cristal fin. Certaines particules ont pu être observées à la surface des échantillons dopés au Ga, mais étaient absentes dans LiNi0,5 Mn1,5 O4 . Comme le montre la figure 4, l'EDS est une méthode d'analyse qualitative qui illustre la présence de Ga dans des échantillons dopés au Ga. Évidemment, suite à l'ajout de x valeur, une augmentation significative de la concentration de Ga a été enregistrée, indiquant que Ga avait été dopé dans le réseau cristallin.

Images SEM du LiNi0,5-x Gax Mn1,5 O4 (x = 0, 0,04, 0,06, 0,08, 0,1) a Ga-0, b Ga-0,04, c Ga-0.06, d Ga-0.08, et e Ga-0.10
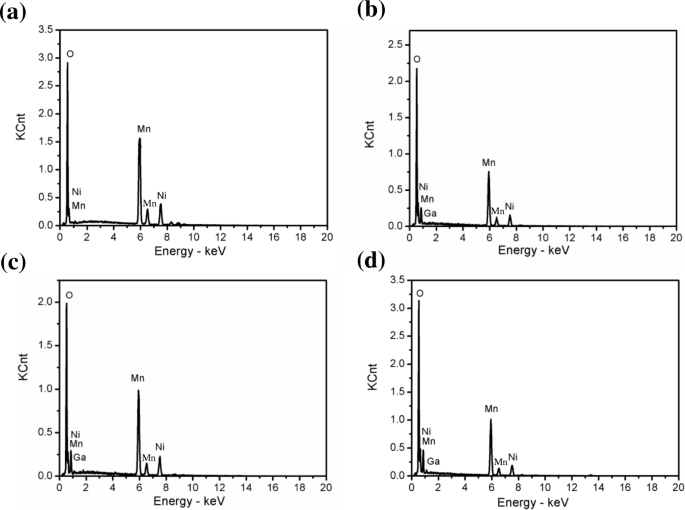
Image EDS du LiNi0.5-x Gax Mn1,5 O4 (x = 0, 0,04, 0,06, 0,08, 0,1) a Ga-0, b Ga-0,04, c Ga-0.06, et d Ga-0.08
Analyse des performances électrochimiques
Examiner les impacts du dopage au Ga sur l'amélioration de la capacité de débit de LiNi0,5-x Gax Mn1,5 O4 (x = 0, 0,04, 0,06, 0,08, 0,1), les capacités des échantillons vierges et dopés au Ga à des taux de décharge de 0,2, 0,5, 1, 2 et 3 C ont été étudiées. D'après la figure 5a, la capacité de débit a été manifestement favorisée après le dopage au Ga. Il est à noter que le Ga-0.06 a atteint des performances de débit exceptionnelles, 122,5, 120,9, 120,3, 117,5, 115,7 mAh/g à des débits de 0,2, 0,5, 1, 2 et 3 C, respectivement, par rapport au 124,4, 114,2, 108 , 99,8, 87,3 mAh/g de LiNi0,5 Mn1,5 O4 aux mêmes tarifs. La capacité de décharge des échantillons dopés était inférieure à celle de l'échantillon vierge à un taux de décharge de 0,2 C en raison du Ni 2+ électrochimiquement actif qui a été remplacé par le Ga. Pour les plateaux de décharge, la découverte la plus évidente qui ressort de la figure 5a est que deux plateaux de décharge à ~ 4,0 V et ~ 4,7 V ont pu être observés conformément à Mn 3+ /Mn 4+ et Ni 2+ /Ni 4+ couples redox, ce qui signifie que le dopage au Ga ne modifie pas le mécanisme de décharge. La figure 5b montre les courbes de capacité de débit du LiNi0,5-x Gax Mn1,5 O4 (x = 0, 0,04, 0,06, 0,08, 0,1) échantillons. Cependant, la capacité de décharge de l'échantillon vierge diminue rapidement avec l'augmentation des taux de C. L'excellente capacité de taux de Ga-0.06 peut être attribuée à la réduction Lix Ni1-x O phase d'impureté, conductivité électronique améliorée et coefficient de diffusion amélioré de Li + . La phase d'impureté gênerait le Li + ions de décoller ou de s'incruster. La conductivité électrique a été améliorée grâce à l'augmentation du Mn 3+ contenu par dopage au Ga. Ce résultat est en accord avec les tracés dQ/dV. Il existe deux sources de Mn 3+ ; une source de Mn 3+ est une carence en oxygène [24], entraînant Mn 3+ , tandis qu'un autre est la substitution de Ga 3+ pour Ni 2+ dans lequel quelques portions de Mn 4+ devrait se transformer en Mn 3+ pour maintenir la neutralité de charge. Cependant, la réaction de dismutation de Mn 3+ qui se produit dans l'électrolyte n'est pas propice à la stabilité structurelle. Simultanément, le Ga dopé forme une couche de passivation et réduit le contact direct entre l'électrolyte et le matériau d'électrode. Cela a inhibé l'apparition d'une disproportion, conduisant à d'excellentes propriétés de vitesse. Toutes les analyses ci-dessus sont également conformes aux résultats SEM et EDS.
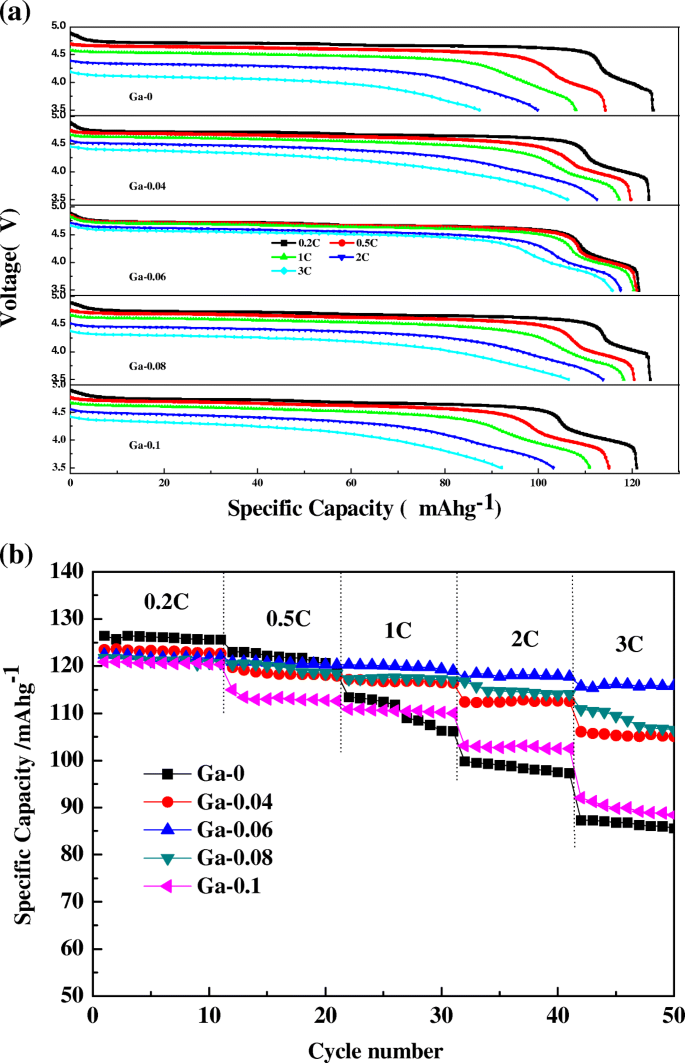
un Les courbes de décharge de LiNi0,5-x Gax Mn1,5 O4 (x = 0, 0,04, 0,06, 0,08, 0,1) échantillons à des taux de 0,2 C, 0,5 C, 1 C, 2 C, 3 C. b Capacités d'évaluation du LiNi0.5-x Gax Mn1,5 O4 (x = 0, 0,04, 0,06, 0,08, 0,1) échantillons
La performance cyclique de la cellule est un paramètre essentiel pour les propriétés électrochimiques. À partir de la figure 6a, nous avons calculé que la capacité de rétention à 1 C et 25 °C des échantillons de Ga-0, Ga-0,04, Ga-0,06, Ga-0,08 et Ga-0,1 est de 90,8, 94,9, 98, 94,6, et 91,2 %, respectivement. Les performances de cyclisme se sont clairement améliorées à différents degrés après le dopage au Ga, et les échantillons de Ga-0,06 ont montré les paramètres de performance les plus élevés. La figure 6b montre les performances du cycle des échantillons Ga-0, Ga-0,04, Ga-0,06, Ga-0,08 et Ga-0,1 à 1 C et 55 °C. La capacité de rétention des échantillons de Ga-0,06 était de 98,4 % de sa capacité initiale (121,5 mAh/g) à 1 C et 55 °C après 50 cycles, mais l'échantillon de Ga-0 a fourni une capacité de décharge de 113 mAhg − 1 et s'est fortement estompée, avec une rétention de capacité de 74% au 50ème cycle. Par conséquent, les échantillons Ga-0.06 sont meilleurs que les échantillons Ga-0 pour améliorer la stabilité du cycle à haute température, ce qui devrait être attribué à la réduction de Lix Ni1-x O phase d'impureté et la structure stable apportée par l'effet de passivation résultant du dopage au Ga. La figure 6c, d fournit les courbes de décharge des composites Ga-0 et Ga-0,06 à 3 C. La capacité de rétention de l'échantillon de Ga-0,06 a atteint 98,3 % après 100 cycles à 3 C, ce qui était supérieur à celui de l'échantillon vierge. (80%). Le plateau de décharge à 3 C de l'échantillon vierge était inférieur à celui de Ga-0,06, ce qui impliquait que le degré de polarisation de l'échantillon vierge était plus grand que celui de Ga-0,06. On peut conclure qu'une teneur appropriée en dopage au Ga est bénéfique pour l'amélioration des propriétés électrochimiques, en particulier pour la stabilité du cycle à des températures élevées et des taux de décharge élevés.
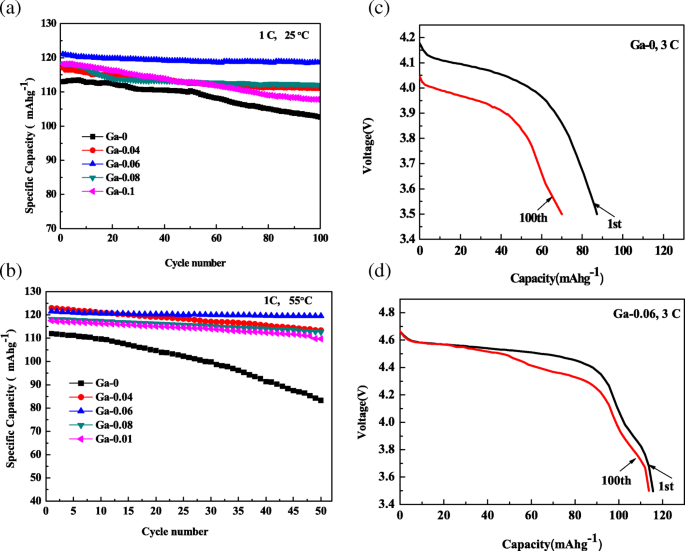
un Performances cycliques du LiNi0.5-x Gax Mn1,5 O4 (x = 0, 0,04, 0,06, 0,08, 0,1) échantillons à 1 C et 25 °C, b performances de cycle du LiNi0.5-x Gax Mn1,5 O4 (x = 0, 0,06) échantillons à 1 C et 55 °C, c courbes de décharge des échantillons de Ga-0, et d échantillon Ga-0,06 à 3 C
Pour une analyse plus détaillée du comportement électrochimique, les tracés dQ/dV sont représentés sur la figure 7a–e. Le pic à environ 4,0 V est indiqué sur la figure 7f, qui doit être attribué à Mn 3+ /Mn 4+ couple redox [25], indiquant les caractéristiques de la structure désordonnée du spinelle Fd3m [9]. Les deux pics de séparation sont à environ 4,7 V, correspondant à Ni 2+ /Ni 3+ et Ni 3+ / Ni 4+ couples redox [26]. Il est clair que l'intensité du pic à environ 4,7 V avait tendance à diminuer avec la teneur en Ga, ce qui est dû à la substitution de Ni électriquement actif par du Ga. L'intensité du pic à environ 4,0 V a augmenté, ce qui est attribué à la concentration de Mn 3+ ions croissant avec la teneur en Ga. Plus la différence de potentiel entre le pic redox et le pic d'oxydation est faible, plus la polarisation est faible. Le degré de polarisation est un indicateur de la réversibilité de Li + ions dans l'électrode. À partir de la figure 7a–e, nous avons déterminé que la plus petite différence de tension entre les pics d'oxydation et de réduction de Ni 3+ /Ni 4+ couple redox est de 0,011 V pour l'échantillon Ga-0,06, ce qui est inférieur à celui de l'échantillon vierge (0,037 V), reflétant la meilleure réversibilité de Li + insertion et désinsertion d'ions dans l'électrode. Les résultats d'analyse des tracés dQ/dV ont indiqué qu'une teneur appropriée en dopage Ga a un effet positif sur la réversibilité des échantillons. Ce résultat est en bon accord avec les résultats de la capacité tarifaire et de D Li + indiqué dans le tableau 3.
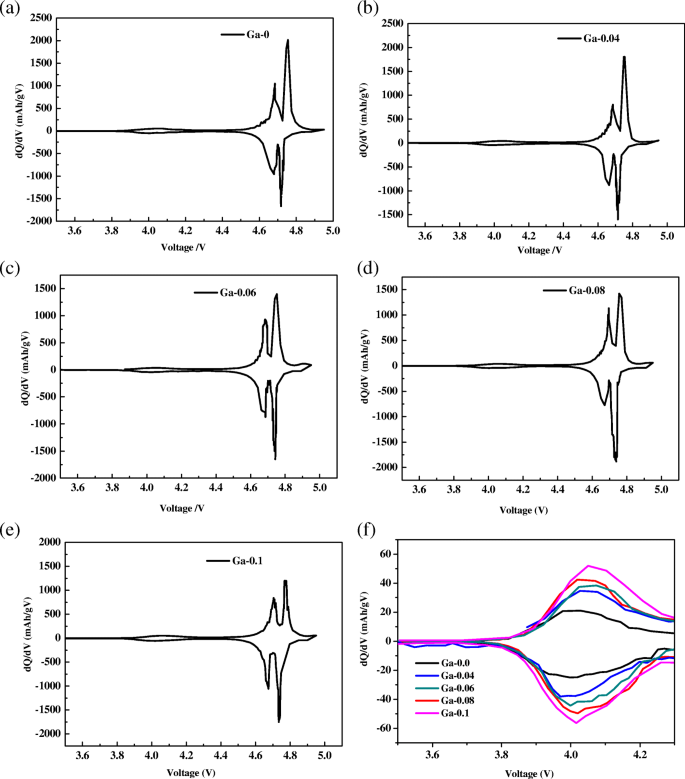
un ~e Tracés dQ/dV du LiNi0,5-x Gax Mn1,5 O4 (x = 0, 0,04, 0,06, 0,08, 0,1) échantillons ; f les tracés dQ/dV agrandis entre 3,5 et 4,3 V
Pour étudier plus en profondeur l'impact du dopage au Ga sur la cinétique de la réaction électrochimique, la Fig. 8a fournit les spectres EIS des échantillons obtenus après 3 cycles à une vitesse de 0,1 °C. Les tracés de Nyquist et circuits équivalents (en médaillon) du LiNi0,5-x Gax Mn1,5 O4 (x = 0, 0,04, 0,06, 0,08, 0,1) les composites sont présentés dans la Fig. 8a. CPE correspond à l'élément à phase constante de la double couche, R e indique la résistance de la solution, et R ct signifie impédance de transfert de charge, qui est décrite par le diamètre d'un demi-cercle. W représente l'impédance de Warburg, qui reflète une vitesse de diffusion lithium-ion. Nous pouvons déterminer que le R ct du LiNi0,5-x Gax Mn1,5 O4 (x = 0, 0,04, 0,06, 0,08, 0,1) les échantillons sont respectivement de 168,4, 133, 86,73, 113,3, 143,66 Ω (comme indiqué dans le tableau 3). Le R ct diminué avec la concentration de dopage au Ga et le R minimum ct valeur s'est produite pour le contenu de dopage Ga de 0,06, indiquant une amélioration de la cinétique de réaction électrochimique. Le R inférieur ct La valeur des échantillons Ga-0,06 reflète la polarisation électrochimique inférieure, qui est conforme aux tracés dQ/dV. Le coefficient de diffusion de Li + (D Li + ) est obtenu à partir de l'équation suivante [27] :
$$ {D}_{L{\mathrm{i}}^{+}}=\frac{R^2{T}^2}{2{A}^2{n}^4{F}^4 {C}_{L{i}^{+}}^2{\sigma}^2} $$ (1)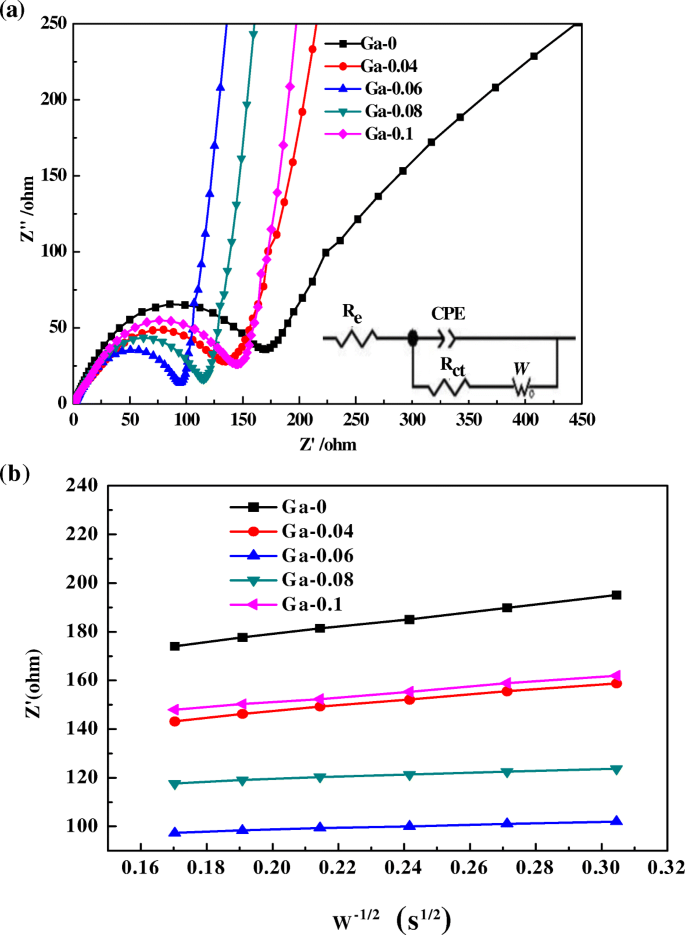
un Spectres EIS du LiNi0.5-x Gax Mn1,5 O4 (x = 0, 0,04, 0,06, 0,08, 0,1) échantillons. b Graphique de Z' en fonction de ω -1/2 dans la région des basses fréquences pour le LiNi0,5-x Gax Mn1,5 O4 (x = 0, 0,04, 0,06, 0,08, 0,1) échantillons
Dans cette équation, R représente la constante de gaz, (R = 8.314 JK mol −1 ), T représente la température (298 K), A correspond à la surface de l'électrode, n représente le nombre d'électrons par molécule participant à la réaction de transfert électronique, F représente la constante de Faraday (F = 96 500 C mol −1 ), C Li + est la teneur en ions lithium dans les échantillons et est le facteur de Warburg. Une relation entre σ et Z' est répertoriée dans l'équation. (2) et a été déterminé à partir de la pente de la ligne de la zone de basse fréquence de la figure 8b, (comme indiqué dans le tableau 3).
$$ {Z}^{\hbox{'}}={R}_{\mathrm{e}}+{R}_{ct}+\sigma {\omega}^{-1/2} $$ ( 2)Il est clair qu'il y a eu une augmentation puis une diminution du D Li + , qui était l'opposé de l'impédance de transfert de charge (R ct ). Le D Li + les valeurs sont 3,89 × 10 −12 , 6,99 × 10 −12 , 7.99 × 10 −11 , 4,88 × 10 −11 , 8.43 × 10 −11 cm 2 s −1 pour Ga-0, Ga-0,04, Ga-0,06, Ga-0,08, Ga-0,1 respectivement. La différence dans le D Li + entre les échantillons dopés au Ga et les échantillons vierges s'élèvent à 1 ordre de grandeur, ce qui indique que le dopage au Ga est un bon moyen d'améliorer la conductivité ionique. L'impédance de transfert de charge la plus faible et le coefficient de diffusion le plus élevé de Li + de Ga-0,06 lui a conféré d'excellentes propriétés de cyclage et de vitesse par rapport à tous les échantillons. L'augmentation de D Li + peut être attribué au Lix réduit Ni1-x O phase d'impureté. Ces résultats indiquent qu'un contenu de dopage Ga approprié peut non seulement améliorer la conductivité du LNMO mais également augmenter le coefficient de diffusion de Li + .
Conclusions
Une méthode sol-gel a été utilisée pour synthétiser LiNi0,5-x Gax Mn1,5 O4 (x = 0, 0,04, 0,06, 0,08, 0,1) échantillons. Tous les échantillons ont une structure Fd3m désordonnée et possèdent un fin cristal de spinelle octaèdre. Le dopage au Ga a limité la formation du Lix Ni1-x O phase secondaire et a augmenté le degré de désordre cationique. Les performances exceptionnelles doivent être attribuées à la conductivité améliorée, à la polarisation électrochimique réduite et à la couche de passivation par le dopage Ga, qui est plus prononcé à des vitesses élevées et à des températures élevées. De plus, l'échantillon Ga-0,06 avec une teneur optimale en Ga présente d'excellentes performances électrochimiques par rapport aux autres échantillons; la capacité de rétention à 1 C et 55 °C de l'échantillon de Ga-0,06 était de 98,4 % de sa capacité initiale (121,5 mAh/g) après 50 cycles, mais l'échantillon de Ga-0 a fourni une capacité de décharge de 113 mAhg − 1 et s'estompe fortement, avec une rétention de capacité de 74% au 50ème cycle dans les mêmes conditions d'essai. Nos travaux fournissent un concept prometteur pour améliorer la stabilité de cycle des matériaux cathodiques des batteries Li-ion à haute température.
Méthodes
Synthèses de matériaux
LiNi0,5-x Gax Mn1,5 O4 (x = 0, 0,04, 0,06, 0,08, 0,1) a été synthétisé par une méthode sol-gel. Les matières premières sont répertoriées comme suit :CH3 COOLi·2H2 O (99,9 %, Aladin), Mn(CH3 COO)2 ·4H2 O (98 %, Tianjin Damao), Ni(CH3 COO)2 ·4H2 O (99,9 %, Aladin), Ga(NO3 )3 ·xH2 O (99,9 %, Aladdin), acide citrique (99,5 %, Aladdin) et hydroxyde d'ammonium (25 %, Tianjin Damao). Les étapes de synthèse sont présentées ci-dessous. Premièrement, un certain rapport stoechiométrique de CH3 COOLi·2H2 O, Mn(CH3 COO)2 ·4H2 O, Ni(CH3 COO)2 ·4H2 O, et Ga(NO3 )3 ·xH2 O a été dissous dans une certaine qualité d'eau distillée sous agitation vigoureuse à température ambiante. Plus de 5% CH3 COOLi·2H2 O a été ajouté pour compenser la perte de sel de lithium. Deuxièmement, une certaine quantité d'acide citrique a été ajoutée à la solution ci-dessus dans un bain-marie sous agitation à 80 °C. Troisièmement, de l'hydroxyde d'ammonium a été utilisé pour ajuster le pH du mélange à 7, et l'agitation a été poursuivie jusqu'à obtention d'un gel. Enfin, le gel résultant a été séché à 1 10°C dans une étuve à vide pendant 10 h. Les précurseurs séchés ont été pré-calcinés à 650 °C pendant 5 h, broyés en poudre, puis calcinés à 850 °C pendant 16 h dans un four à moufle. Des échantillons avec différentes teneurs en dopage Ga ont été obtenus après refroidissement à température ambiante, pour des raisons de commodité, notés respectivement Ga-0, Ga-0.04, Ga-0.06, Ga-0.08, Ga-0.1.
Caractérisation des matériaux
La diffraction des rayons X (DRX, Cu Kα, 36 kV, 20 mA) a été utilisée sur un système Rigaku D/max-PC2200 pour évaluer la structure des échantillons sur une plage de 10 à 80° à 4°/min. Les spectres infrarouges à transformée de Fourier (FT-IR) ont été mesurés par un instrument Nicoletis 6700. La microscopie électronique à balayage (MEB, JEOL JMS-6700F) a été utilisée pour enregistrer la morphologie des composites. La composition élémentaire a été analysée à l'aide de la spectrométrie à dispersion d'énergie (EDS) avec SEM.
Mesures électrochimiques
Les performances électrochimiques des échantillons ont été évaluées par des piles bouton CR2032. Pour préparer les électrodes de travail, 90 % en poids de LiNi0,5-x Gax Mn1,5 O4 (x = 0, 0,04, 0,06, 0,08, 0,1) échantillons, 5 % en poids d'agent conducteur super P et 5 % en poids de liant au fluorure de polypropylène (PVDF) ont été dissous dans N -méthyl-2-pyrrolidone (NMP) pour former une suspension homogène. La suspension obtenue a été coulée sur une feuille d'aluminium et séchée sous vide à 85 °C pendant une nuit. Ensuite, la feuille a été pressée et découpée en disques d'un diamètre de 14 mm. Des piles bouton CR2032 avec une feuille de lithium comme contre-électrodes et électrodes de référence ont été utilisées pour évaluer les performances électrochimiques des matériaux, et elles ont été assemblées dans une boîte à gants remplie d'argon dans laquelle la teneur en eau et les niveaux d'oxygène étaient maintenus en dessous de 0,1 ppm. Ici, l'électrolyte avec une résistance à haute tension était de 1 M LiPF6 dans un mélange de carbonate d'éthylène (EC), de carbonate de propylène (PC) et d'éthylène méthyl carbonate (EMC) (EC:PC:EMC = 1:2:7, v :v :v ). Des mesures galvanostatiques de charge-décharge ont été effectuées à 25 °C et 55 °C à une tension de 3,5 à 4,95 V par le système de test de batterie LAND. Des tests de spectroscopie d'impédance électrochimique (EIS) ont été effectués sur un poste de travail électrochimique CHI600A. Une spectroscopie EIS dans la gamme de fréquences de 0,01 Hz à 100 kHz avec une perturbation de 5 mV a été réalisée.
Abréviations
- A :
-
Surface de l'électrode
- CLi + :
-
Teneur en ions lithium
- CPE :
-
Phase constante
- CV :
-
Voltamétrie cyclique
- D Li + :
-
Coefficient de diffusion de Li +
- EC/PC/EMC :
-
Carbonate d'éthylène/carbonate de propylène/carbonate d'éthylène méthyle
- EDS :
-
Spectrométrie à dispersion d'énergie
- EIS :
-
Spectroscopie d'impédance électrochimique
- F :
-
Constante de Faraday
- FT-IR :
-
Spectrophotomètre à transformée de Fourier
- Ga-0,04 :
-
LiNi0.46 Ga0,04 Mn1,5 O4
- Ga-0.06 :
-
LiNi0.44 Ga0,06 Mn1,5 O4
- Ga-0.08 :
-
LiNi0.42 Ga0,08 Mn1,5 O4
- Ga-0.1 :
-
LiNi0.4 Ga0.1 Mn1,5 O4
- I311 :
-
L'intensité du (311) pic de diffraction
- I400 :
-
L'intensité du (400) pic de diffraction
- I588 :
-
L'intensité de 588 cm −1 groupe
- I621 :
-
L'intensité de 621 cm −1 groupe
- LNMO/Ga-0 :
-
LiNi0,5 Mn1,5 O4
- n :
-
Le nombre d'électrons par molécule
- NMP :
-
N -méthyl-2-pyrrolidinone
- PVDF :
-
Fluorure de polyvinylidène
- R :
-
Constante de gaz
- Rct :
-
Résistance de transfert de charge
- Re :
-
Résistance de la solution
- SEM :
-
Microscope électronique à balayage
- T :
-
Température
- W :
-
Impédance Warburg
- XRD :
-
Diffraction des rayons X
- σ :
-
The Warburg factor
Nanomatériaux
- Les performances de la fibre de verre
- Vespel® :le matériau aérospatial
- Quel est le matériau des tubes de chaudière ?
- Dévoilement de la structure atomique et électronique des nanofibres de carbone empilées
- Composite mécanique de LiNi0.8Co0.15Al0.05O2/Nanotubes de carbone avec des performances électrochimiques améliorées pour les batteries lithium-ion
- Dopage de substitution pour les minéraux d'aluminosilicate et performances supérieures de fractionnement de l'eau
- Quelle est la structure du graphite?
- Comprendre la flexibilité d'un matériau
- Les complexités du broyage électrochimique



