Préparation et caractérisation de nanoparticules d'hémine en forme de têtard et de sphère pour une solubilité améliorée
Résumé
Hemin est un puissant supplément de fer. Une limitation majeure de l'applicabilité de l'hémine est sa solubilité aqueuse et sa biodisponibilité extrêmement faibles. Le but de ce travail est de préparer des nanoparticules d'hémine avec une solubilité améliorée. Les images au microscope électronique à transmission ont montré que des nanoparticules d'hémine avec différentes concentrations initiales d'hémine (0,1 et 0,5 mg/mL) étaient en forme de têtard (tête d'environ 200 nm et queue de 100 nm) et en forme de sphère (50-100 nm), respectivement. De plus, les nanoparticules d'hémine présentaient une solubilité plus élevée que l'hémine libre. La solubilité des nanoparticules en forme de sphère était 308,2 fois supérieure à celle de l'hémine pure à 25 °C. Les nanoparticules d'hémine étaient stables dans des conditions acides et présentaient une excellente stabilité thermique. Ces résultats suggèrent que les nanoparticules d'hémine pourraient servir de supplément de fer potentiel avec des applications potentielles dans les domaines de la thérapie alimentaire, biomédicale et photodynamique-photothermique.
Introduction
Le fer est un élément essentiel dans les processus métaboliques du corps, tels que le transfert d'électrons, le stockage et le transport d'oxygène [1]. La carence en fer est l'une des carences nutritionnelles les plus courantes, affectant environ 20 % de la population mondiale [2]. La conséquence la plus négative de la carence en fer est l'anémie sidéropénique. Elle est principalement causée par un apport alimentaire insuffisant en fer, souvent lorsque la demande est élevée. Chez l'homme, le fer alimentaire peut pénétrer dans l'organisme sous deux formes principales :l'une est le fer inorganique (fer non hémique), principalement libéré par les légumes et les aliments à base de plantes, et l'autre est le fer hémique, acquis par la dégradation de l'hémoglobine ou de la myoglobine présente dans animaux. L'hémine a été trouvée dans le sang et les produits carnés, est un composant de nombreuses hémoprotéines (y compris la myoglobine, l'hémoglobine et les cytochromes b et c) et est deux ou trois fois plus facilement absorbée (50 à 87 %) que le fer non hémique [3] . Récemment, les chercheurs ont assisté à des avancées majeures dans notre compréhension du rôle physiologique de l'hémine. Malheureusement, l'hémine est hydrophobe en raison de la présence d'un grand macrocycle tétrapyrrolique [4]. En raison de la forte hydrophobie et de la faible solubilité de l'hémine dans une solution aqueuse neutre, son application dans divers domaines a été limitée. Il est donc urgent d'augmenter la solubilité de l'hémine.
Pour relever ce défi, de nombreux efforts ont été consacrés à l'amélioration de la solubilité de l'hémine. Berner [5] a découvert que la protéine en solution enzymatique partielle (isolat de soja, farine de soja ou concentré de soja) pouvait s'unir au fer hémique pour améliorer l'absorption du fer, ce qui améliorait la biodisponibilité du fer. Wang et al. [6] ont indiqué que l'hémine cristalline et le L-arginate pourraient préparer une coacervation hémine-arginate hydrosoluble, qui pourrait être utilisée comme nouveau supplément de fer hémique dans les additifs alimentaires, les aliments fonctionnels et les produits pharmaceutiques. Zhang et al. [7] ont rapporté que l'hémine pouvait se combiner avec la -cyclodextrine par un oligosaccharide cyclique de sept unités de glucose liées en α [1, 4], conduisant à une amélioration significative de la solubilité de l'hémine. Bien qu'il y ait eu quelques progrès sur l'amélioration de la solubilité du fer hémique, l'industrialisation n'a pas été facile en raison du processus de préparation compliqué. Par conséquent, le développement d'une méthode simple pour améliorer la solubilité de l'hémine reste un défi majeur.
Les nanosciences et les nanotechnologies ont le potentiel d'apporter de nouvelles solutions dans le développement de substances fonctionnelles, en particulier l'inclusion de composés bioactifs sans affecter la perception sensorielle des consommateurs et en améliorant l'absorption de certains composants [8]. Les nanoparticules présentent plusieurs avantages [9], dont celui de favoriser la solubilité des substances hydrophobes [10]. Duhem et al. [11] ont développé de nouveaux nanomédicaments à base de vitamine E grâce aux nanotechnologies, qui offraient de multiples avantages dans l'administration de médicaments, tels que la biocompatibilité, l'amélioration de la solubilité des médicaments et l'activité anticancéreuse. Chang et al. [12] ont rapporté que les nanoparticules préparées par de courtes chaînes de glucanes modifiées par l'anhydride succinique pourraient charger de la lutéine hydrophobe, ce qui pourrait améliorer la solubilité dans l'eau de la lutéine. Malgré l'énorme potentiel des nanoparticules, l'hémine à l'échelle nanométrique n'a pas encore été signalée. Nous avons postulé que la solubilité des nanoparticules d'hémine pourrait être augmentée par rapport à l'hémine libre, ce qui pourrait avoir des applications intéressantes.
L'objectif principal du présent travail est de développer des nanoparticules d'hémine de différentes formes en utilisant une technique de dialyse facile et d'améliorer leur solubilité. Les paramètres de préparation de la concentration d'hémine initiale et les conditions de dialyse ont été évalués. De plus, la solubilité et la stabilité contre le pH, le traitement thermique et le sel des nanoparticules d'hémine formées ont été évaluées. Dans l'ensemble, les améliorations de la solubilité de l'hémine ont une variété de domaines d'application potentiels.
Matériaux et méthodes
Matériaux
Des membranes d'hémine et de dialyse avec un poids moléculaire seuil de 8 à 12 kDa ont été achetées auprès de Beijing Solarbio Science &Technology Co., Ltd. (Pékin, Chine). Acétone (CH3 COCH3 , 99,5%) a été acheté auprès de Kant Chemical Co., Ltd. (Laiyang, Chine). Tous les autres réactifs utilisés étaient de qualité analytique.
Préparation de nanoparticules d'hémine
Des nanoparticules d'hémine ont été préparées selon une méthode de dialyse :0,1 mg/mL (ou 0,5 mg/mL) d'hémine dissoute dans de l'acétone acidifiée avec 0,1 ml d'acide chlorhydrique concentré. La solution d'hémine a été dialysée pendant différents jours, l'eau a été changée tous les jours et elle a été lyophilisée pour obtenir des nanoparticules d'hémine. Pour déterminer l'effet de paramètres variables sur la préparation de nanoparticules d'hémine, les rapports de volume d'hémine/eau ont été fixés à 1:3, 1:5, 1:10 et 1:50 ; les températures de culture ont été fixées à 4 et 25°C; et les temps d'incubation ont été fixés à 1, 3 et 5 jours.
Microscopie électronique à transmission (MET)
Des images MET de nanoparticules ont été prises avec un microscope électronique à transmission 7700 (Hitachi, Tokyo, Japon) avec une tension d'accélération de 80 kV. Une minuscule goutte d'échantillon a été déposée sur une grille de cuivre recouverte de carbone, puis lyophilisée pour observation.
Mesures de la taille moyenne et du potentiel Zeta
La taille moyenne, le potentiel zêta (potentiel ζ) et l'indice de polydispersité (PDI) des particules ont été mesurés par diffusion dynamique de la lumière (DLS), à l'aide d'un Malvern Zetasizer Nano (Malvern Instruments Ltd., Royaume-Uni). Les échantillons ont été dilués dans de l'eau MilliQ et analysés à 25°C. La concentration des échantillons dilués était de 0,05 %.
Spectre d'absorption UV-Vis
Des mesures par spectroscopie UV-Vis de l'hémine libre et des nanoparticules d'hémine dissoutes dans de l'acétone aqueuse acidifiée ont été effectuées sur un spectrophotomètre UV-Vis (TU-1810, Pékin, Chine). L'absorption moléculaire a été balayée à une longueur d'onde de 200 à 800 nm à des intervalles de 1 nm pour obtenir un spectre.
Test de solubilité
La solubilité aqueuse quantitative de l'hémine pure et des nanoparticules a été étudiée selon la méthode rapportée par Gidwani et al. [13]. En bref, des solutions sursaturées d'hémine pure et de nanoparticules ont été ajoutées séparément à 5 ml d'eau déminéralisée dans des tubes à essai, respectivement. Les tubes à essai ont été agités constamment (500 tr/min) à différentes températures (25, 37, 60 et 80 °C) pendant 30 min. Ensuite, la solution a été centrifugée à 3500g et le surnageant a été dilué de manière appropriée avec de l'acétone aqueuse acidifiée. La concentration des échantillons a été déterminée à 640 nm par un spectrophotomètre UV-Vis. Pour chaque mesure, la ligne de base a été établie en utilisant de l'acétone aqueuse acidifiée à blanc comme référence.
pH, température et stabilité du sel
La taille, le potentiel , le PDI et la turbidité des nanoparticules (0,5 mg/mL) ont été mesurés et comparés aux valeurs initiales pour évaluer la stabilité des nanoparticules. Les suspensions de particules ont été divisées en dix groupes :six groupes ont été ajustés aux valeurs de pH souhaitées [2, 3, 5, 7, 9, 11], et en utilisant de l'acide chlorhydrique (0,1 µM) ou une solution d'hydroxyde de sodium (0,1 µM); trois groupes ont été chauffés à 25, 60 et 80°C puis refroidis à température ambiante; une autre a été réalisée avec différentes concentrations de chlorure de sodium (NaCl, 0, 10, 50, 100, 250 et 500 mM), respectivement. Les solutions mélangées sont restées une nuit à 25°C.
Spectroscopie infrarouge à transformée de Fourier (FTIR)
Les structures chimiques des nanoparticules d'hémine ont été confirmées à l'aide de spectres FTIR (Tensor 27, Jasco Inc., Easton, MD, USA). Un total de 32 numérisations à une résolution de 4 cm − 1 ont été accumulés à l'aide du logiciel de balayage rapide dans OMNIC 8.0 pour obtenir un spectre unique. La gamme spectrale était de 400-4000 cm − 1 .
Spectroscopie de fluorescence
Les mesures de fluorescence de l'hémine libre et des nanoparticules ont été effectuées à l'aide d'un spectrophotomètre à fluorescence (F-7000, Hitachi, Japon). Les spectres de fluorescence des échantillons ont été obtenus à des longueurs d'onde comprises entre 300 et 600 nm avec une excitation à 402 nm.
Diffractogramme des rayons X (XRD)
Le XRD de l'hémine libre et des nanoparticules a été obtenu à l'aide d'un diffractomètre à rayons X (AXS D8 ADVANCE ; Bruker, Karlsruhe, Allemagne), et les échantillons ont été étudiés dans le 2θ plage de 4 à 40°. La cristallinité relative de l'hémine libre et des nanoparticules a été déterminée en traçant la ligne de base des pics sur le diffractogramme et en calculant l'aire à l'aide du logiciel de visualisation de spectre basé sur la méthode rapportée par Jivan et al. [14]. La zone au-dessus et sous la courbe correspond respectivement aux domaines cristallins et aux régions amorphes. Le rapport de la surface supérieure à la surface totale a été pris comme la cristallinité relative :
Cristallinité relative (%) = Aire sous les pics/Aire totale de la courbe × 100.
Analyse statistique
Des échantillons en triple de tous les résultats quantitatifs ont été obtenus. Les résultats ont été rapportés sous forme de valeurs moyennes et d'écarts types. L'analyse statistique a été effectuée par les tests à plusieurs plages de Duncan à l'aide du progiciel statistique SPSS V.17 (SPSS Inc., Chicago, IL, États-Unis).
Résultats et discussion
Formation et caractérisation de nanoparticules d'hémine
La morphologie et la taille des nanoparticules d'hémine fabriquées à l'aide de la méthode de dialyse ont été examinées par MET. Lorsque la concentration d'hémine était de 0,5 mg/mL, des nanostructures d'hémine de différentes tailles se sont formées à divers rapports de volume d'hémine/eau et pour différents jours de dialyse (Fig. 1, Fichier supplémentaire 1 :Figure S1-S3). Les nanoparticules avaient des formes sphériques bien définies et des diamètres de 50 à 100 nm lorsque le rapport volumique hémine/eau était de 1:10 après 3 jours de dialyse. Avec une augmentation du rapport volumique hémine/eau (1:50), les nanoparticules ont été rassemblées en particules en forme de bâtonnets (Fig. 1). En particulier, nous avons constaté que lorsque le temps de dialyse augmentait de 1 à 3 jours, les nanoparticules d'hémine devenaient uniformément dispersées (Fichier supplémentaire 1 :Figure S1-S3). La température (4 et 25°C) de la dialyse a eu peu d'influence sur la taille des particules et la dispersion des nanoparticules d'hémine (Fichier supplémentaire 1 :Figure S4).

Images MET de nanoparticules d'hémine préparées par dialyse pendant 3 jours avec divers rapports de volume hémine/eau, y compris 1:3 (a ), 1:5 (b ), 1:10 (c ) et 1:50 (d ) à 25°C. La concentration d'hémine était de 0.5 mg/mL
La figure 2 montre les images MET typiques de nanoparticules d'hémine préparées pour différents jours de dialyse avec la concentration d'hémine de 0,1 mg/mL. Les produits étaient principalement des nanoparticules bien définies, dispersées individuellement, structurellement inhabituelles et en forme de têtard. Les nanoparticules ressemblant à des têtards ont été de préférence distribuées avec 3 jours de dialyse. Le têtard présentait une disparité de taille significative de la largeur maximale de la tête (200 nm) à la queue (100 nm). Nos résultats ont montré que des nanoparticules uniformément dispersées pouvaient être formées à un rapport volumique hémine/eau de 1:10 et après dialyse pendant 3 jours à 25 °C pour les nanoparticules en forme de sphère et de têtard. Ainsi, nous avons choisi ces deux types de nanoparticules d'hémine pour la recherche suivante.

Images MET de nanoparticules d'hémine préparées avec un rapport volumique hémine/eau de 1:10 à différents jours de dialyse, dont 1 jour (a ), 3 jours (b ) et 5 jours (c ) à 25°C. La concentration d'hémine était de 0,1 mg/mL
Pour examiner plus en détail la taille des nanoparticules d'hémine, la détermination DLS a été utilisée pour confirmer la formation de nanostructures. Les diamètres des nanoparticules en forme de sphère et de têtard étaient d'environ 218,2 ± 6,2 et 299,8 ± 7,6 nm, respectivement (Fig. 3a). La taille des nanoparticules mesurées par DLS était un peu plus grande que les résultats mesurés par MET; cette différence a été attribuée au gonflement des nanoparticules en solution aqueuse. La mesure DLS était connue pour indiquer les diamètres hydrodynamiques des nanoparticules dans une solution [15]. Le potentiel ζ des nanoparticules en forme de sphère (− 21,4 mV) était environ deux fois plus élevé que celui des nanoparticules en forme de têtard (− 10.8 mV) (Fig. 3b). Le PDI des nanoparticules d'hémine a également été déterminé pour analyser la distribution granulométrique. Les résultats ont montré que le PDI des nanoparticules en forme de sphère et de têtard était respectivement de 0,348 et 0,402 (Fig. 3c). Cette découverte a indiqué que les nanoparticules d'hémine obtenues avaient une bonne polydispersité.
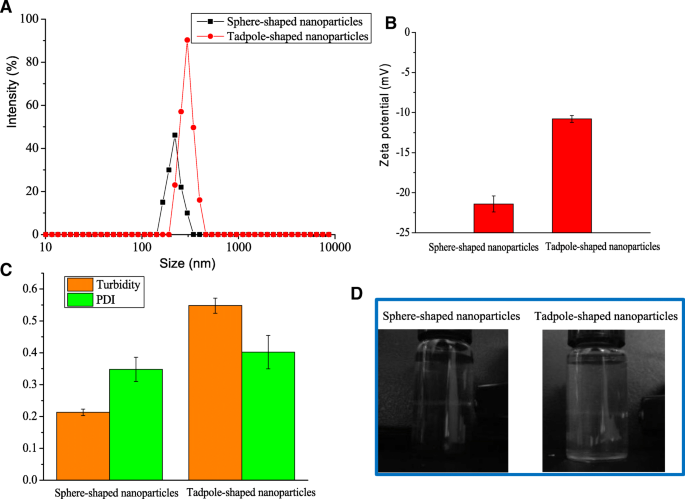
La taille moyenne (a ), ζ-potentiel (b ), PDI et turbidité (c ), et effet Tyndall (d ) de nanoparticules d'hémine de formes différentes
Lorsqu'un faisceau lumineux traverse une dispersion colloïdale, une partie de la lumière est diffusée par les particules colloïdales présentes dans la solution, entraînant une divergence du faisceau lumineux. Ce comportement est appelé effet Faraday-Tyndall [16]. Dans ce cas, la solution d'hémine libre n'a pas présenté d'effet Tyndall (Fichier supplémentaire 1 :Figure S5). Néanmoins, l'effet Tyndall a été observé dans la suspension de nanoparticules en forme de sphère et de têtard (Fig. 3d), vérifiant la formation de colloïdes ou de nanoparticules dans la suspension fine. Le mécanisme de formation de nanoparticules d'hémine par la méthode de dialyse peut être dû à la diffusion du solvant à travers l'interface entre la phase aqueuse à l'extérieur et la phase de solvant organique à l'intérieur, ce qui a entraîné une diminution de la solubilité de l'hémine et la formation d'un noyau cristallin. Par la suite, des nanoparticules d'hémine de formes différentes se sont formées en raison de la croissance et de l'auto-assemblage du noyau monocristallin de différentes manières.
Analyse d'absorption UV-Vis
Selon les résultats ci-dessus, nous avons recherché s'il y avait des différences entre les deux formes de nanoparticules d'hémine dans leur génération de chromophore. Le spectre UV-Vis des nanoparticules en forme de sphère et de têtard a montré les mêmes bandes d'absorption à 265 nm (Fig. 4a). Les nanoparticules en forme de sphère présentaient une bande d'absorption étroite à 667 nm et 775 nm. En comparaison, la solution de nanoparticules en forme de têtard a montré un large pic à 658 nm sans un pic de 775 nm. De plus, l'intensité d'absorption des nanoparticules en forme de sphère était plus élevée que celle des nanoparticules en forme de têtard. Une si grande différence ne pouvait s'expliquer ni en considérant le têtard comme la somme d'une sphère et d'une tige conique ni par une configuration de sphère quelque peu imparfaite. L'oscillation électronique correspondant à une absorption de plasmon selon le grand axe est retardée et/ou sur un trajet réfléchissant. Ainsi, les propriétés optiques des nanoparticules d'hémine dépendaient de la forme, similaire au rapport de Hu et al. [17], qui ont découvert que les nanoparticules d'or en forme de têtard et de sphère avaient des propriétés optiques différentes.
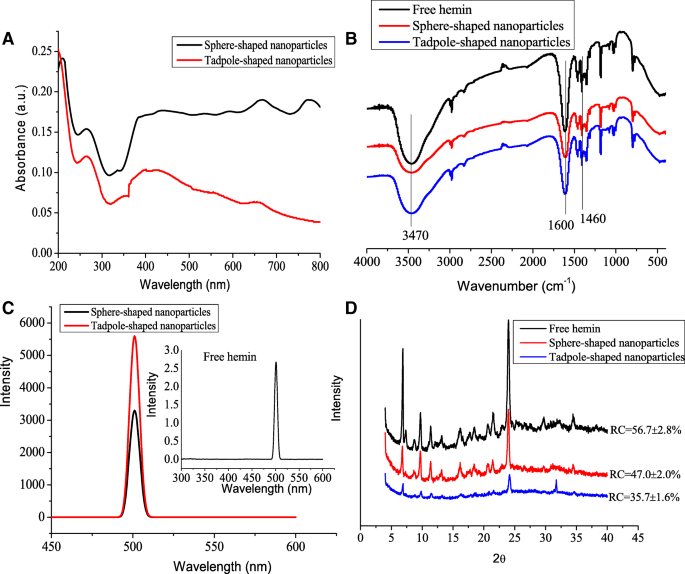
un Spectre UV-Vis, b Spectres FTIR, c spectres d'émission de fluorescence, et d Modèles XRD d'hémine libre, de nanoparticules en forme de sphère et de nanoparticules en forme de têtard. Les nanoparticules ont été dispersées dans de l'eau déminéralisée. RC, cristallinité relative
La solution d'hémine libre a affiché une absorption maximale à 344 nm, ce qui a été attribué à la bande de Soret couramment associée aux porphyrines (Fichier supplémentaire 1 :Figure S5). La bande d'absorption des nanoparticules d'hémine est passée de 344 à 265 nm, ce qui suggère que l'effet conjugatif π-π des nanoparticules d'hémine a été amélioré. Étonnamment, par rapport à l'hémine libre, les deux types de nanoparticules présentaient une absorption élevée et forte dans le proche infrarouge, ce qui est très approprié pour les applications basées sur l'absorption, telles que la thérapie photothermique et l'imagerie photoacoustique [18]. Magno et al. [19] ont également signalé que les nanoparticules de porphyrine à absorption proche infrarouge ont suscité un intérêt considérable pour des applications en photothérapie et en photodiagnostic, même en tant que nanoparticules magnétiques pour la thérapie par hyperthermie magnétique et les systèmes d'administration de médicaments.
Solubilité
La solubilité de l'hémine est un facteur important, qui peut affecter directement l'efficacité d'absorption dans le corps. La solubilité aqueuse quantitative de l'hémine pure et des nanoparticules d'hémine à différentes températures a été testée (tableau 1). Au fur et à mesure que la température augmentait, la solubilité aqueuse de tous les échantillons augmentait. Par exemple, la solubilité de l'hémine libre à 25, 37, 60 et 80°C était de 0,009 ± 0,000, 0,060 ± 0,002, 0,144 ± 0,004 et 0,245 ± 0,008 mg/mL, respectivement (Tableau 1).
La quantité de nanoparticules en forme de sphère dissoutes à 25, 37, 60 et 80°C était de 1,333 ± 0,023, 1,499 ± 0,072, 1,889 ± 0,081 et 3,853 ± 0,124 mg/mL, respectivement, et celle des nanoparticules en forme de têtard ont été 0,997 ± 0,045, 1,231 ± 0,035, 1,521 ± 0,058 et 1,795 ± 0,050 mg/mL, respectivement. Les résultats de l'étude de solubilité aqueuse des nanoparticules ont montré une augmentation significative par rapport à l'hémine pure. Les nanoparticules en forme de sphère présentaient une solubilité plus élevée à des températures de 25, 37, 60 et 80 °C que celles des nanoparticules en forme de têtard. Cette découverte suggère que la solubilité des nanoparticules en forme de sphère pourrait être 308,2 fois supérieure à celle de l'hémine libre à 25 °C. Cette augmentation de la solubilité était principalement due à la taille unique des particules à l'échelle nanométrique. Ce résultat était cohérent avec d'autres études rapportées par Gidwani et Vyas [13].
Analyses de spectres FTIR
Les spectres FTIR peuvent être utilisés pour identifier les types de groupes fonctionnels. La bande à 3470 cm − 1 est principalement attribuée à la vibration d'étirement des groupes N-H et hydroxyle de l'hémine (Fig. 4b). Une bande à 1460 cm − 1 est attribuée à la vibration dans le plan N–H due à la vibration de flexion hors du plan de –CH3 du cycle pyrrole aromatique de l'hémine. Le pic à 1600 cm − 1 est le pic caractéristique de la liaison amide dû à la vibration d'étirement de C=O du groupe carboxyle lié à la surface de l'hémine, qui révèle que la liaison amide secondaire existe dans l'hémine. Ces résultats sont cohérents avec ceux de Xi et al. [20]. Cependant, le pic à 3470 cm − 1 des nanoparticules d'hémine était plus large que celle de l'hémine libre, indiquant clairement l'interaction renforcée de liaison hydrogène entre les nanoparticules.
Spectres de fluorescence
Les propriétés de fluorescence de l'hémine libre et des nanoparticules d'hémine ont également été contrôlées par spectroscopie de fluorescence. Les signaux de fluorescence des nanoparticules en forme de sphère et de têtard ont augmenté dans le maximum d'émission apparente à 500 nm par rapport à l'hémine libre (Fig. 4c). Cela pourrait être dû à la solubilité accrue de l'hémine après la formation de nanoparticules [21].
Analyse XRD
La nature cristalline de l'hémine libre et des nanoparticules d'hémine a été confirmée par XRD. Comme illustré sur la figure 4d, les modèles XRD d'hémine libre ont affiché plusieurs pics de réflexion relativement forts à 2θ = 6,8, 9,6, 11,5, 16,2, 21,5 et 23,9°. Les pics caractéristiques des nanoparticules en forme de sphère étaient les mêmes que ceux de l'hémine libre, indiquant ainsi que la structure cristalline des nanoparticules en forme de sphère n'a pas changé dans les formulations de nanoparticules. Cependant, pour les nanoparticules en forme de têtard, les pics les plus caractéristiques ont disparu. De plus, la cristallinité relative des nanoparticules en forme de sphère et de têtard a été significativement réduite à 47,0 % et 35,7 %, respectivement, contre 56,7 % pour l'hémine libre. Ces résultats ont indiqué que les formulations de nanoparticules pourraient détruire les régions cristallines partielles de l'hémine.
Effets du pH, de la température et de la concentration en sel sur la stabilité
Les variations de la taille, du PDI, du potentiel et de la turbidité des nanoparticules d'hémine après incubation à différents niveaux de pH [2,3,4,5,6,7,8,9,10,11] ont été mesurées (Fig. 5a , b). La taille des nanoparticules d'hémine est restée presque inchangée avec des diamètres moyens d'environ 200 nm dans des conditions acides (Fig. 5a). À des valeurs de pH faibles de 2, la taille des nanoparticules d'hémine a été réduite à environ 122,4 nm. À un pH de 7, la taille des nanoparticules a augmenté à 293,6 nm, et elle a augmenté de manière significative (P < 0,05) dans des conditions alcalines (un pH de 9 et 11,0) avec des diamètres moyens supérieurs à 400 nm. Le PDI des nanoparticules était inférieur à 0,5 dans des conditions acides, ne démontrant aucune agrégation apparente de nanoparticules [22]. Le potentiel ζ des nanoparticules diminuait avec l'augmentation des valeurs de pH (Fig. 5b). La turbidité des nanoparticules a montré la même tendance en taille. Ces résultats ont indiqué que les nanoparticules étaient stables dans des conditions acides et instables dans des conditions alcalines.
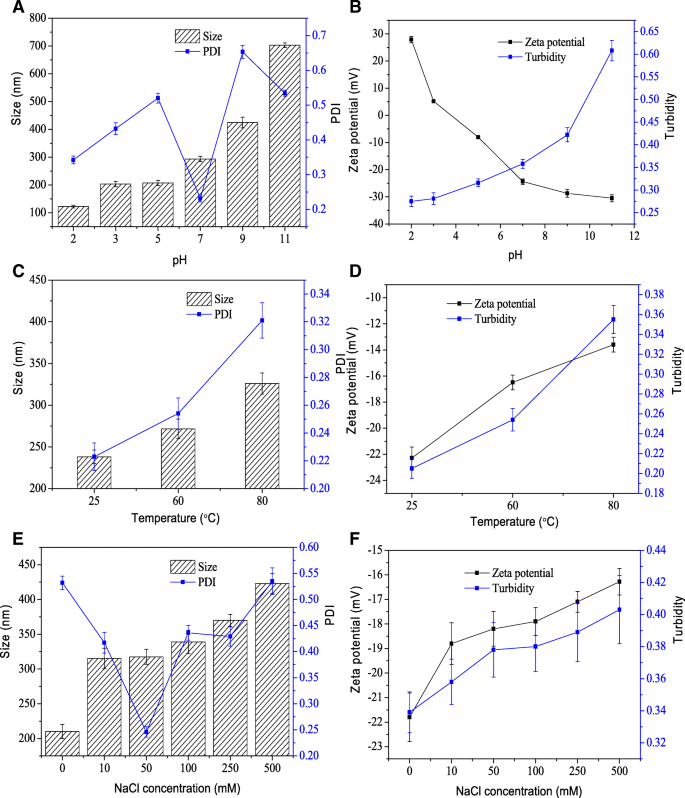
Stabilité des nanoparticules d'hémine. L'effet de divers niveaux de pH (a ), températures (c ) et les concentrations de sel (e ) sur la taille des particules et le PDI des nanoparticules. L'effet de divers niveaux de pH (b ), températures (d ) et les concentrations de sel (f ) sur le potentiel ζ et la turbidité
Les effets du traitement thermique (25, 60 et 80 °C) pendant 30 min sur la taille, le PDI, le potentiel et la turbidité des nanoparticules d'hémine ont été déterminés (Fig. 5c, d). Lorsque la température a augmenté, la taille des particules, le PDI, le potentiel et la turbidité des nanoparticules ont légèrement augmenté. Les résultats suggèrent que les nanoparticules d'hémine avaient une excellente stabilité thermique. De même, à mesure que la force ionique augmentait, la taille, le potentiel ζ et la turbidité des nanoparticules augmentaient également, ce qui provoquait la dissociation des nanoparticules (Fig. 5e, f).
Conclusions
Dans ce travail, nous avons d'abord développé des nanoparticules d'hémine en forme de têtard et de sphère en utilisant une technique de dialyse facile, qui pourrait considérablement augmenter la solubilité de 308,2 fois à 25 °C. De plus, les nanoparticules d'hémine étaient stables dans des conditions acides et présentaient une excellente stabilité thermique. De plus, les deux nanoparticules présentaient une forte absorption dans le proche infrarouge. Les travaux futurs se concentreront sur l'étude approfondie de la conception d'un système de nanoporteur d'hémine à réponse optothermique pour le chargement d'ingrédients actifs. Les nanoparticules d'hémine à solubilité améliorée pourraient avoir des applications potentielles dans les domaines biomédical, alimentaire, de la thérapie photodynamique et de la thérapie photodynamique et photothermique.
Abréviations
- DLS :
-
Diffusion dynamique de la lumière
- FTIR :
-
Transformée de Fourier infrarouge
- TEM :
-
Microscopie électronique à transmission
- XRD :
-
Diffractogramme aux rayons X
Nanomatériaux
- Nanofibres et filaments pour une administration améliorée des médicaments
- Nanoparticules d'or multifonctionnelles pour des applications diagnostiques et thérapeutiques améliorées :une revue
- Nanoparticules pour le traitement du cancer :progrès actuels et défis
- Préparation et propriétés magnétiques des nanoparticules de spinelle FeMn2O4 dopées au cobalt
- Activité de préparation et d'hydrogénation catalytique améliorée des nanoparticules de Sb/Palygorskite (PAL)
- Nanoparticules de chitosane chargées de génistéine et de bioflavonoïdes ciblés sur les récepteurs folates pour un effet anticancéreux amélioré dans les cancers du col de l'utérus
- Synthèse hydrothermale de nanoparticules d'In2O3 jumelles hybrides disque hexagonal hétérostructures ZnO pour des activités photocatalytiques et une stabilité améliorées
- Nouveaux nanoparticules Au Nanostars@PEG biocompatibles pour l'imagerie CT in vivo et les propriétés de clairance rénale
- Tours améliorés pour le polissage et l'ébavurage



