Synthèse et étude de nanofils CuGeO3 comme matériaux d'anode pour les batteries sodium-ion avancées
Résumé
Le germanium est considéré comme un matériau d'anode potentiel pour les batteries sodium-ion en raison de sa capacité spécifique théorique fascinante. Cependant, sa faible cyclabilité résultant de la cinétique lente et du grand changement de volume lors de charges/décharges répétées constitue des menaces majeures pour son développement ultérieur. Une solution consiste à utiliser son composé ternaire comme alternative pour améliorer la stabilité en cyclage. Ici, CuGeO3 de haute pureté des nanofils ont été préparés via une méthode hydrothermale facile, et leurs performances de stockage du sodium ont d'abord été explorées. Le CuGeO3 tel qu'obtenu a fourni une capacité de charge initiale de 306,7 mAh g −1 ainsi que des performances de cyclisme favorables, affichant une grande promesse en tant que matériau d'anode potentiel pour les batteries sodium-ion.
Contexte
Au cours des deux dernières décennies, les batteries lithium-ion (LIB) ont dominé avec succès le marché dans le domaine du stockage et de la conversion d'énergie [1, 2]. Les LIB servent désormais de source d'alimentation pour une variété d'appareils, allant des smartphones aux véhicules électriques (VE) [3,4,5,6,7]. Cependant, le développement futur des LIB est fortement entravé par la pénurie de ressources en lithium qui limite inévitablement leur application à grande échelle [8]. Par conséquent, la recherche d'autres alternatives pour remplacer le lithium est d'une importance vitale. Sur la base des caractéristiques physiques et chimiques abondantes et similaires du lithium, le sodium s'avère l'un des candidats les plus prometteurs dans les batteries rechargeables [9]. Au cours des dernières années, un progrès significatif des batteries sodium-ion (SIB) pour les matériaux cathodiques a été obtenu en tirant l'expérience des systèmes LIB [9,10,11]. Alors que les matériaux potentiels pour le côté anode restent encore sous-développés. Il est généralement connu que la taille de l'ion sodium est significativement plus grande que celle de l'ion lithium, ce qui conduit à une cinétique de réaction électrochimique lente et à un changement de volume important accompagné d'une couche d'interphase d'électrolyte solide (SEI) instable, entraînant une stabilité de cyclage et une capacité de vitesse inférieures. SIB [12]. Ainsi, la recherche de candidats potentiels pour l'anode est particulièrement importante mais difficile.
Le germanium (Ge) en tant que matériau d'anode a été largement étudié pour les SIB en raison de leurs capacités spécifiques théoriques élevées (369 mAh g −1 basé sur NaGe) [13]. Néanmoins, il est intéressant de noter que le Ge élémentaire n'affiche des capacités fascinantes que dans les électrodes à couche mince et à structure amorphe [14]. Afin d'améliorer les propriétés électrochimiques des structures plus grossières, une stratégie réalisable consiste à introduire des matériaux carbonés. Par exemple, Yin et ses collaborateurs ont conçu et synthétisé des boîtiers en carbone creux/matériau hybride Ge comme anode dans les SIB et ont obtenu une capacité réversible élevée même après 500 cycles, ce qui se rapproche de sa valeur théorique [15]. Une autre méthode efficace consiste à utiliser des composés à base de Ge binaires ou ternaires avec une nanostructure. Il a été rapporté que les composés binaires ou ternaires incorporés avec des matériaux carbonés offrent des performances de cyclage et de vitesse considérablement améliorées par rapport au Ge unique [16,17,18]. Sur la base des résultats expérimentaux dans les LIB, il convient de noter que les composés ternaires présentent d'excellentes propriétés électrochimiques dues à la formation de produits intermédiaires au cours du processus de décharge, qui servent de matrice inerte pour atténuer les changements de volume et empêcher l'agglomération de matière active. particules [19]. Il est important de noter que les produits intermédiaires des composés ternaires à base de Ge incluent le Ge amorphe, qui améliorerait la cinétique de sodiation [14, 20]. CuGeO3 (CGO) est un oxyde ternaire I-V-VI typique à base de Ge et présente des performances de stockage de lithium supérieures [21]. Basé sur l'hypothèse de sept Na + réaction calculée, la capacité spécifique théorique de CGO est de 1018 mAh g −1 . Cependant, la propriété de stockage du sodium du CGO est rarement explorée à ce jour.
Dans ce travail, le nanofil CGO a été synthétisé avec succès par une réaction hydrothermale facile et fiable et a d'abord été exploré comme matériau d'anode pour ses performances de stockage de sodium. Il présente d'excellentes performances électrochimiques en termes de capacité réversible, d'efficacité coulombique (CE), de stabilité en cyclage et de propriété de vitesse, qui sont considérablement améliorées par rapport à celle du Ge élémentaire. Les résultats indiquent que l'utilisation de composés ternaires est l'une des approches les plus efficaces pour promouvoir l'étude du matériau d'anode à base de Ge pour les SIB.
Méthodes
Préparation du matériel
Les nanofils CGO ont été préparés via une méthode hydrothermale facile. Tout d'abord, 0,1 g de bromure de cétyltriméthylammonium (CTAB) a été ajouté dans 15 ml d'eau distillée pour former une solution homogène sous agitation magnétique pendant 1 h à température ambiante. Ensuite, 5 mM Cu(CH3 COO)2 ·H2 O et 5 mM GeO2 ont été ajoutés à la solution ci-dessus, respectivement, et la solution mélangée a été agitée en continu pendant 1 h. Après cela, le mélange réactionnel a été chargé et scellé dans un autoclave en acier inoxydable revêtu de téflon avec un volume intérieur de 20 ml et chauffé à 180 °C pendant 24 h avant de refroidir à température ambiante. Enfin, les nanofils CGO ont été collectés par lavage à l'eau distillée et à l'éthanol trois fois et séchés à 60 °C pendant 24 h dans une étuve. Les matériaux Ge ont été préparés par broyage à billes à haute énergie de poudres cristallines de Ge (Alfa Aesar).
Caractérisation des matériaux
Les détails de la diffraction des rayons X (XRD) des échantillons ont été collectés sur un micro-diffractomètre Bruker-AXS (D8 ADVANCE) sous rayonnement CuKα (λ = 1,5406 Å) à une tension de 30 kV. Les images de la microstructure des échantillons ont été acquises sur une microscopie électronique à balayage (MEB) à émission de champ HITACHI S-4800 et une microscopie électronique à transmission (MET) HITACHI H-7650. Les diagrammes de diffraction électronique (SAED) sélectionnés ont été obtenus à l'aide d'un JEM 2100HR TEM.
Mesures électrochimiques
Pour la préparation de l'électrode de travail, 80 % en poids de nanofils CGO, 10 % en poids de carbone Super P et 10 % en poids de liant acide poly(acrylique) ont été mélangés avec une quantité appropriée d'eau distillée pour former une suspension, puis uniformément coulés sur un support en cuivre. déjouer. Ensuite, les électrodes ont été séchées dans une étuve à vide à 60 °C pendant 24 h pour éliminer l'humidité. L'électrode Ge a été préparée par des procédés similaires. L'électrolyte était composé de 1 M de NaClO4 sel dissous dans du carbonate d'éthylène/carbonate de diméthyle (EC/DMC, 1:1 v /v ) avec 5 % en volume de carbonate de fluoroéthylène (FEC) comme additif. Les électrodes de travail ont été assemblées dans des cellules de type pièce (CR2032) dans une boîte à gants remplie d'argon avec un filtre en microfibre de verre et du Na métallique comme séparateur et contre-électrode, respectivement, et une quantité appropriée d'électrolyte ci-dessus. Les mesures électrochimiques ont été évaluées par voltamétrie cyclique (CV, station de travail électrochimique CHI 660B) et des tests de charge/décharge galvanostatique (LAND 2001A Battery Tester) dans la plage de tension de 0,05 à 2,0 V vs Na/Na + . La charge pondérale du matériau actif CGO dans l'électrode de travail était d'environ. 1,0 mg cm −2 , et la capacité spécifique a été calculée en fonction de la matière active.
Résultats et discussion
Une illustration schématique du processus de préparation des nanofils CGO est présentée sur la figure 1a. La solution homogène a été formée en mélangeant le CTAB, GeO2 , et Cu(CH3 COO)2 ·H2 O avec une quantité appropriée d'eau distillée. Parmi eux, le CTAB a été utilisé comme tensioactif. Après 24 h, les nanofils CGO ont été produits dans le milieu hydrothermal. Au processus hydrothermal, la matière première GeO2 peut être dissous dans l'eau pour donner H2 GeO3 [22]. Par la suite, H2 GeO3 a réagi avec Cu(CH3 COO)2 ·H2 O pour former CGO orthorhombique [23]. Sur la base de la discussion ci-dessus avec le mécanisme de nucléation [24], il est proposé d'exprimer un mécanisme de synthèse possible pour les nanofils CGO, tel que :
$$ {\displaystyle \begin{array}{l}{\mathrm{GeO}}_2+{\mathrm{H}}_2\mathrm{O}\to {\mathrm{H}}_2{\mathrm{GeO} }_3\\ {}\mathrm{Cu}{\left({\mathrm{CH}}_3\mathrm{COO}\right)}_2+{\mathrm{H}}_2{\mathrm{GeO}}_3\ à {\mathrm{CuGeO}}_3+2{\mathrm{CH}}_3\mathrm{COO}\mathrm{H}\end{array}} $$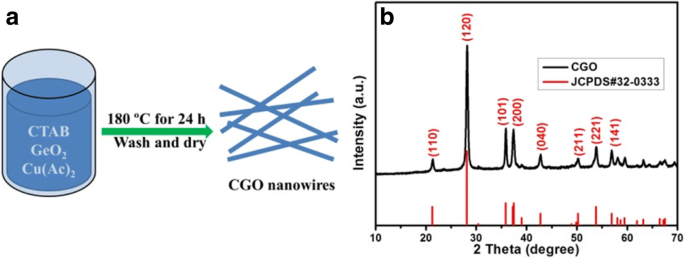
un Illustration schématique de la préparation et b Schéma XRD des nanofils CGO
Le motif XRD a été utilisé pour confirmer les structures cristallines et la composition chimique des échantillons tels que préparés. Comme le montre la figure 1b, tous les pics du spectre XRD correspondent bien à la carte JCPDS standard (n° 32-0333) sans pics d'impuretés, ce qui permet de conclure que le nanofil CGO tel que synthétisé est en phase pure. Les 2θ les pics à 21,238°, 28,09°, 35,787°, 37,408°, etc. sont attribués aux plans de réseau (110), (120), (101), (200), etc. de phase orthorhombique, respectivement. De plus, les forts pics de diffraction indiquent une bonne cristallinité des produits.
Les images SEM et MET ont été utilisées pour observer la morphologie de ces produits hydrothermaux. Comme le montre l'image SEM (Fig. 2a), les CGO obtenus sont des nanofils uniformes d'une longueur supérieure à 1 μm, ce qui est bien en accord avec le résultat rapporté [25]. L'image SEM à fort grossissement (Fig. 2b) révèle que le diamètre moyen des nanofils CGO est d'environ 20 nm. Les images MET sont affichées sur les Fig. 2c, d ; on peut clairement voir que la microstructure des nanofils CGO est cohérente avec les résultats SEM ci-dessus. Il a été démontré que les matériaux d'anode nanostructurés améliorent les performances électrochimiques en raison de leur grande surface et de leur voie de diffusion réduite [26]. Le nanofil à haute uniformité est bénéfique pour s'adapter aux changements de volume et améliorer la diffusion des ions sodium dans les matériaux actifs pendant les processus de charge/décharge [27].

un , b SEM et c , d Images MET des nanofils CGO
Pour explorer les caractéristiques de stockage du sodium des nanofils CGO, une série de mesures électrochimiques ont été effectuées. CV est une voie efficace pour évaluer le mécanisme de réaction au cours du processus de sodiation/désodiation. La figure 3a illustre les courbes CV typiques du matériau d'anode CGO avec une vitesse de balayage de 0,2 mV s −1 dans la fenêtre de tension de 0,05 à 2,0 V (vs. Na/Na + ). Le premier balayage cathodique montre un pic large et fort situé à 0,8 V, évidemment différent des cycles ultérieurs, qui peut être attribué à la conversion en plusieurs étapes de CGO pour produire Cu, Ge, Nax Oy , Nak Gél Om , et décomposition irréversible de l'électrolyte pour former la couche SEI [17, 28]. Ce pic s'est séparé en deux pics et transféré à environ 0,6 et 0,75 V dans les cycles suivants, ce qui pourrait être attribué à la diminution de la réaction irréversible et à la stabilisation de la couche SEI telle que formée. Des phénomènes similaires ont été rapportés pour les matériaux des anodes ternaires [29]. Le pic de réduction à la tension d'environ 0,01 V est attribué à l'alliage de Naz Ge, et le pic d'oxydation à environ 0,2 V correspond au désalliage réversible de Naz Ge [30]. Le pic anodique chargé à 1,5 V représentait l'oxydation supplémentaire des produits de décharge. Les changements de phase de l'électrode CGO ont été étudiés pour explorer davantage le mécanisme de stockage du sodium, et la mesure XRD ex situ a été effectuée sur les premiers produits chargés et déchargés. La figure 4a montre les modèles XRD de l'électrode CGO déchargée à 0,05 V, tous les pics de CGO ont complètement disparu et quelques nouveaux pics de Cu, Ge4 Na, Na2 O2 , NaO3 , et Nak Gél Om (comme Na4 GeO4 , Na2 Ge2 O5 , Na6 Ge2 O7 ) est apparu, indiquant que le CGO a réagi avec Na pendant le processus de décharge. Notez que les pics de réflexion de Nak Gél Om ont été clairement trouvés, qui pourraient être attribués à la structure cristalline unique CGO orthorhombique. Le CGO orthorhombique a été structuré par le partage de coin GeO4 tétraèdres comme blocs de construction de base et Cu 2+ comme jonction pour former des chaînes le long du c -axe [25]. Chaque atome de Cu a été assigné pour former CuO6 fortement déformé octaèdre entouré de six atomes de O. Lorsqu'ils sont chargés à 2,0 V (Fig. 4b), tous les pics de diffraction sont devenus indistincts, à l'exception du substrat de Cu, et deux pics faibles peuvent être bien indexés sur le CGO, indiquant que le CGO récupéré est de faible cristallinité ou amorphe. Ce résultat a été confirmé par les modèles SAED de CGO vierge et de produits déchargés et chargés (Fig. 4c, d). Fait intéressant, ces produits à faible cristallinité ou amorphes sont bénéfiques pour la diffusion ultérieure à l'état solide de Na + [12]. Sur la base des résultats et de la discussion ci-dessus, nous proposons que le processus de stockage du sodium de CGO soit attribué à la combinaison de la conversion et de la réaction d'alliage telle que :
$$ {\displaystyle \begin{array}{l}{\mathrm{CuGeO}}_3+{\mathrm{Na}}^{+}\to \mathrm{Cu}+\mathrm{Ge}+{\mathrm{ Na}}_x{\mathrm{O}}_y+{\mathrm{Na}}_k{\mathrm{Ge}}_l{\mathrm{O}}_m\\ {}\mathrm{Ge}+{\mathrm{ Na}}^{+}\to {\mathrm{Na}}_z\mathrm{Ge}\end{array}} $$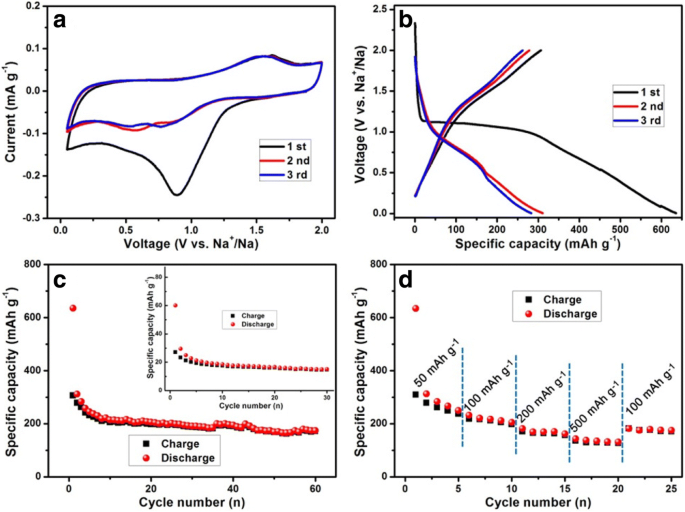
un Les trois courbes CV initiales des nanofils CGO à une vitesse de balayage de 0,2 mV s −1 . b Les trois courbes de charge/décharge initiales et c performances de cyclage des nanofils CGO à une densité de courant de 50 mA g −1 . Encart dans c est la performance de cyclage du Ge élémentaire à une densité de courant de 50 mA g −1 . d Capacité de débit des nanofils CGO à différentes densités de courant (de 50 à 500 mA g −1 )
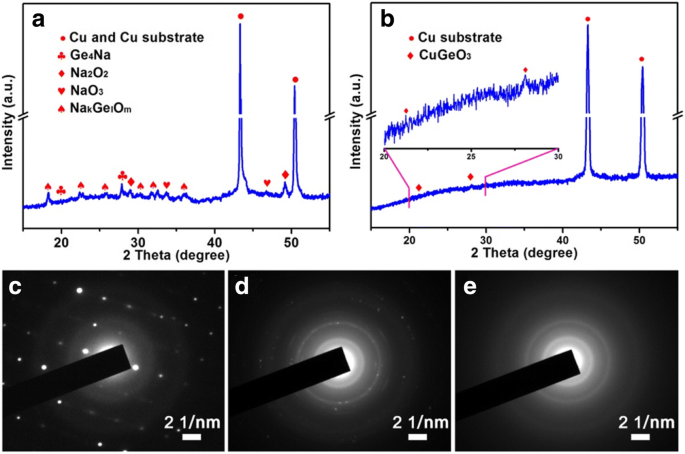
Modèles XRD ex situ de l'électrode CGO lorsque a déchargé à 0,05 V et b chargé à 2,0 V. c Modèle SAED des échantillons CGO. Modèles SAED de l'électrode CGO lorsque d déchargé à 0,05 V et e chargé à 2,0 V
Les zones intégrées des deuxième et troisième courbes CV sont presque les mêmes, indiquant une bonne réversibilité après le cycle initial.
Les performances électrochimiques ont été étudiées plus avant via des mesures de cyclage de charge/décharge galvanostatique dans la même plage de tension. Les performances de cyclage des matériaux d'anodes élémentaires Ge à une densité de courant de 50 mA g −1 est incrusté dans la Fig. 3c, la capacité de charge/décharge initiale était de 27,1/60,1 mAh g −1 (CE de 45,09 %), ce qui est nettement inférieur à celui de la valeur théorique. De plus, la capacité retenue n'était que de 15 mAh g −1 après 30 cycles. Il est rapporté que la cinétique de sodiation lente de Ge est la raison directe pour laquelle l'utilisation de matériaux de structure amorphe réussit à obtenir une capacité spécifique élevée [14]. Il est important de noter que les CGO forment du Ge amorphe, qui peut être distribué de manière homogène dans le Cu et le Li2 matrice O avant la réaction de l'alliage au cours de chaque processus de décharge [20, 31, 32]. La figure 3b montre les trois courbes de charge/décharge initiales des nanofils CGO à une densité de courant de 50 mA g −1 . Tous les plateaux de tension correspondaient bien aux résultats CV ci-dessus.
Les performances de cyclage et la capacité de débit sont les deux principaux problèmes pour évaluer les caractéristiques de stockage du sodium du CGO en tant que matériau d'anode. Comme le montre la figure 3c, les nanofils CGO ont fourni une capacité de charge initiale allant jusqu'à 306,7 mAh g −1 et un CE initial de 61,74 % à une densité de courant constante de 50 mA g −1 . La perte de capacité élevée au cours du cycle initial pourrait être attribuée à la formation d'une couche SEI sur la surface du matériau actif et à d'autres réactions irréversibles, ce qui est une caractéristique commune des anodes nanostructurées [33, 34]. De plus, la capacité de charge est rapidement tombée à 205 mAh g −1 au 10e cycle et diminue lentement jusqu'à 171 mAh g −1 au 60e (seulement 0,68 mAh g −1 perte de capacité par cycle du 10e au 60e cycle). Ce résultat indique que l'utilisation de composés ternaires avec nanostructure est une alternative efficace potentielle pour améliorer les propriétés électrochimiques du Ge élémentaire pour les SIB. Un autre paramètre important des CGO est leur capacité de débit. Comme le montre la figure 4b, les nanofils CGO ont présenté des capacités de charge réversibles de 261, 212, 164 et 130 mAh g −1 à des densités de courant de 50, 100, 200 et 500 mA g −1 , respectivement. De plus, comme la densité de courant est revenue à 100 mA g −1 , CGO peut toujours fournir une capacité de charge élevée de 175 mAh g −1 . Il est à noter que la capacité diminue très légèrement lorsque les densités de courant passent de 50 à 500 mA g −1 . Cela pourrait être confirmé que les composés ternaires à base de Ge sont un matériau d'anode prometteur pour les SIB.
Conclusions
En conclusion, les nanofils CGO hautement uniformes ont été préparés par une méthode hydrothermale à un pot, et leurs propriétés électrochimiques de stockage de sodium en tant qu'anode ont d'abord été explorées. Les nanofils CGO tels que synthétisés ont affiché une capacité réversible exceptionnelle (306,7 mAh g −1 ) pour le premier cycle), un CE élevé (CE initial de 61,74 %), une performance cyclique favorable et une bonne capacité de cadence. Les composés nanostructurés ternaires en tant que matériaux d'anode utilisent non seulement pleinement les produits intermédiaires pour améliorer la cinétique de sodiation, offrant ainsi une capacité élevée, mais également en tant que matrice inerte pour améliorer la stabilité du cycle.
Abréviations
- CE :
-
Efficacité coulombienne
- CGO :
-
CuGeO3
- CTAB :
-
Bromure de cétyltriméthylammonium
- CV :
-
Voltamétrie cyclique
- EC/DMC :
-
Carbonate d'éthylène/carbonate de diméthyle
- EV :
-
Véhicules électriques
- FEC :
-
Carbonate de fluoroéthylène
- Voir :
-
Germanium
- LIB :
-
Batterie lithium-ion
- SEI :
-
Interphase à électrolyte solide
- SEM :
-
Microscopie électronique à balayage
- SIB :
-
Batteries sodium-ion
- TEM :
-
Microscopie électronique à transmission
- XRD :
-
Diffraction des rayons X
Nanomatériaux
- Avancées et défis des nanomatériaux fluorescents pour la synthèse et les applications biomédicales
- Synthèse facile de nanoparticules SiO2@C ancrées sur MWNT en tant que matériaux anodiques hautes performances pour batteries Li-ion
- Synthèse et propriétés électrochimiques des matériaux cathodiques LiNi0.5Mn1.5O4 avec dopage composite Cr3+ et F− pour batteries lithium-ion
- Composite MoS2/noir d'acétylène à quelques couches comme matériau d'anode efficace pour les batteries lithium-ion
- Préparation de micromatériaux hybrides MnO2 revêtus de PPy et de leurs performances cycliques améliorées en tant qu'anode pour batteries lithium-ion
- Synthèse d'un matériau d'anode sphérique Li4Ti5O12 revêtu d'argent par une méthode hydrothermale assistée par sol-gel
- Composite Na4Mn9O18/Nanotube de Carbone en tant que matériau à hautes performances électrochimiques pour les batteries sodium-ion aqueuses
- Composite Si/Graphène intégré fabriqué par réduction thermique au magnésium comme matériau d'anode pour les batteries lithium-ion
- Un système de refroidissement avancé pour ordinateurs et batteries



