Carbone poreux hiérarchique avec pores ordonnés interconnectés à partir de biodéchets pour électrodes de supercondensateur hautes performances
Résumé
L'utilisation des biodéchets comme précurseurs pour la préparation de nanomatériaux à valeur ajoutée est essentielle au développement durable des dispositifs. Les lignosulfonates sont les sous-produits des industries de fabrication de pâtes et papiers et sont généralement rejetés comme déchets. Dans la présente étude, le lignosulfonate est utilisé comme précurseur pour préparer du carbone poreux ordonné hiérarchiquement avec des pores interconnectés pour l'application de stockage d'énergie électrochimique. La structure moléculaire et les propriétés uniques du lignosulfonate garantissent l'acquisition de carbone poreux de haute qualité avec une structure de pores contrôlable et des propriétés physiques améliorées. En conséquence, le carbone poreux d'ordre hiérarchique tel que préparé présente d'excellentes performances de stockage d'énergie lorsqu'il est utilisé pour assembler le supercondensateur symétrique, qui présente une capacité spécifique élevée de 289 F g −1 à une densité de courant de 0,5 A g −1 , avec une densité énergétique de 40 Wh kg −1 à la densité de puissance de 900 W kg −1 . La présente étude propose une stratégie prometteuse pour la fabrication de dispositifs de stockage d'énergie haute performance à faible coût.
Introduction
Les supercondensateurs sont prometteurs en tant que dispositifs de stockage d'énergie pour les systèmes de sauvegarde et divers appareils électroniques en raison de leur densité de puissance élevée, de leur longue durée de vie, de leur légèreté par rapport aux batteries et aux condensateurs conventionnels [1,2,3,4,5,6]. Les nanomatériaux à base de carbone sont connus pour leurs excellentes performances de stockage d'énergie en tant que matériaux d'électrode actifs dans les supercondensateurs qui stockent l'électricité à travers la double couche électrochimique. Leurs performances de stockage d'énergie sont déterminées par les propriétés physiques des matériaux actifs des électrodes, en particulier la structure poreuse [7,8,9]. Les macropores (plus grands que 50 nm) servent de réservoirs tampons ioniques, les mésopores (2 à 50 nm) de canaux de transport d'ions électrolytiques et les micropores généralement de sites de stockage de charge [10]. Nos travaux antérieurs basés sur l'enquête de corrélation linéaire indiquent que la capacité spécifique et la capacité de débit sont fortement liées au volume des micropores et des mésopores [11, 12], respectivement. Les supercondensateurs à base de nanomatériaux de carbone devraient avoir une structure poreuse hiérarchique avec une distribution équilibrée de macropores, mésopores et micropores interconnectés.
Des efforts considérables ont été faits pour préparer le carbone poreux hiérarchique pour une meilleure performance de stockage d'énergie [13,14,15,16]. Les chercheurs ont développé divers modèles durs, notamment la zéolite, le MCM-41, le MCM-48, le SBA-15, le SBA-16 et le KIT-6 pour préparer du carbone poreux avec des mésopores ordonnés [17, 18]. Les traitements d'activation chimique et physique sont également largement utilisés, ce qui entraîne généralement des pores fermés répartis de manière aléatoire [13], et montre donc une mauvaise maîtrise de la structure des pores.
La biomasse et les biodéchets ont été chimiquement et physiquement activés à des températures élevées pour la préparation de charbon poreux [19]. Peu d'entre eux ont été utilisés dans les méthodes de matrice pour la synthèse de carbone poreux à structure de pores ordonnée [11, 12, 20]. De nombreux charbons poreux sont préparés à partir de tensioactifs et de copolymères séquencés coûteux et non renouvelables. La lignine est la deuxième matière organique la plus abondante et le polymère aromatique le plus abondant existant dans les espèces végétales [21]. Dans l'industrie papetière, la lignine est convertie en lignosulfonates au cours du processus de réduction en pâte et généralement rejetée en tant que déchets, ce qui entraîne de graves problèmes environnementaux [22]. Les lignosulfonates sont généralement de petites molécules avec un cycle aromatique et des groupes contenant de l'oxygène. Ils ont généralement un poids moléculaire beaucoup plus faible que la lignine et présentent une excellente solubilité dans l'eau en raison des groupes contenant de l'oxygène [23]. Ces mérites font des lignosulfonates les précurseurs idéaux qui peuvent être utilisés dans la méthode des modèles pour la synthèse de carbone poreux à valeur ajoutée avec une structure de pores ordonnée.
Dans la présente étude, nous avons utilisé le KIT-6 comme modèle dur pour sa bonne interconnectivité des pores ordonnés et la contrôlabilité de la taille des pores pour préparer le carbone mésoporeux ordonné combiné à l'activation post-chimique pour créer des micropores dans la structure mésoporeuse. Le lignosulfonate de sodium a été utilisé comme précurseur. Le carbone poreux ordonné hiérarchique (HOPC) tel que préparé a été utilisé pour assembler le supercondensateur symétrique qui présente des performances de stockage d'énergie exceptionnelles.
Méthodes
Préparation du KIT-6
La matrice de silice mésoporeuse ordonnée (KIT-6) a été synthétisée selon la référence [24]. Dans une procédure modifiée, 5,53 g de Pluronic P123 (OE20 Bon de commande70 OE20 , PM =5800, Aldrich) a d'abord été dissous dans 200 g d'eau déminéralisée contenant 10,9 g de HCl concentré (35 %) dans une bouteille en verre de 250 mL. 5,53 g de butanol ont ensuite été ajoutés au flacon sous agitation à 35 o Après 1 h d'agitation, 11,9 g de TEOS (tétraéthylorthosilicate, Aldrich) ont été ajoutés à la solution ci-dessus, puis le mélange a été agité pendant 24 h à 35 o C. La bouteille a ensuite été vieillie pendant 24 heures supplémentaires à 100 o C dans des conditions statiques. Le produit solide a été recueilli par filtration et séché à 100 o C sans lavage. Le résidu organique a été éliminé par extraction dans le mélange d'éthanol et d'HCl, suivie d'une calcination à 550 o C pendant 6 h.
Préparation du Carbone Mésoporeux Ordonné
Le carbone mésoporeux ordonné (OMC) a été préparé en utilisant le KIT-6 tel que synthétisé comme matrice dure et le lignosulfonate de sodium comme source de carbone. Le modèle de silice synthétisé ci-dessus KIT-6 a été utilisé pour charger le lignosulfonate. Typiquement, 0,6 g de lignosulfonate de sodium acheté auprès de Lanyi Reagent (Beijing, Chine) a été dissous dans 15 ml d'eau désionisée, suivi de l'ajout de 0,6 g de matrice KIT-6. Le mélange a été maintenu sous agitation pendant 24 h à température ambiante, suivi d'un séchage à 70 o C. Le composite séché contenant de la silice et du lignosulfonate de sodium a été utilisé comme précurseur pour la carbonisation. Le processus de carbonisation a été mené à 900 o C pendant 2 h dans Ar avec un débit de gaz de 30 sccm. Après carbonisation, la matrice de silice a été retirée en immergeant le composite dans une solution aqueuse de NaOH 2,5 M pendant 12 h à température ambiante. Après un traitement de lavage utilisant une solution diluée de HCl et de l'eau désionisée, du carbone mésoporeux ordonné (en abrégé OMC) a été obtenu et enregistré en tant que OMC-900 (le nombre numérique fait référence à la température de carbonisation). OMC-700, OMC-800 et OMC-1000 se réfèrent aux échantillons obtenus carbonisés à 700 o C, 800 o C, et 1000 o C, respectivement.
Préparation du Carbone Poreux Hiérarchisé
Pour préparer le carbone poreux ordonné hiérarchique (en abrégé HOPC), un processus d'activation post-chimique a été utilisé. En bref, l'OMC-900 tel que préparé a été mélangé de manière homogène avec du ZnCl2 solution avec un rapport pondéral carbone/ZnCl2 de 1:1 et séché à 110 o C pendant 6 h. Le traitement d'activation a été réalisé en chauffant les composites à 900 o C pendant 3 h dans Ar avec un débit de gaz de 30 sccm. Pour étudier l'effet de la température de carbonisation, les modèles KIT-6 imprégnés de lignosulfonate de sodium ont également été carbonisés à 700 o C et 800 o C, marqué comme OMC-700 et OMC-800. A titre de comparaison, le lignosulfonate de sodium pur sans aucun traitement a été directement carbonisé dans les mêmes conditions et le carbone obtenu a été enregistré en tant que lignine-carbone.
Caractérisation
La morphologie de la matrice KIT-6 telle que synthétisée et des échantillons de carbone poreux ont été caractérisées à l'aide d'une microscopie électronique à balayage (MEB) Hitachi SU8020. La structure poreuse fine a été examinée plus avant sur un microscopie électronique à transmission (MET) JEOL 2100F. Le diagramme de diffraction XRD à faible angle a été enregistré sur un diffractionmètre à rayons X sur poudre avancé XD-2/XD-3. La structure chimique a été étudiée à l'aide d'une spectroscopie photoélectronique à rayons X (XPS) ESCALAB250Xi. La caractérisation Raman a été réalisée à l'aide d'une spectroscopie Raman HORIBA Science. Les spectres infrarouges transformés de Fourier (FTIR) ont été enregistrés à l'aide d'une spectroscopie FTIR NEXUS 670. Les caractéristiques poreuses du modèle KIT-6 et du carbone poreux ont été analysées par N2 expériences d'adsorption/désorption à 77 K à l'aide d'un Micromeritic ASAP2020 V3.02 H. La surface spécifique a été mesurée selon la méthode Brunauer-Emmett-Teller (BET), et la distribution de la taille des pores a été calculée en utilisant une densité non locale de pores fendus modèle de théorie fonctionnelle (NLDFT).
Mesure électrochimique
La performance électrochimique des échantillons de carbone poreux tels que préparés a été examinée en utilisant une configuration à trois électrodes. Le HOPC optimisé a finalement été étudié en utilisant une configuration à deux électrodes. L'électrode de travail dans le système à trois électrodes a été fabriquée en mélangeant physiquement le carbone poreux tel que préparé et le PVDF qui a été dissous dans du solvant NMP à l'avance avec un rapport pondéral du carbone au PVDF de 9:1. La suspension homogène a été coulée sur une feuille de nickel avec une zone de couverture d'environ 1 cm 2 , suivi d'un séchage à 80 o C pendant 12 h pour éliminer le solvant résiduel. Dans le test à trois électrodes, une plaque de platine (1 cm 2 ) et Ag/AgCl ont été utilisés comme contre-électrode et électrode de référence, respectivement. L'électrode de travail dans le système à deux électrodes a été préparée par la même procédure tout en remplaçant la feuille de nickel par de la mousse de nickel. Des mousses de nickel avec la même quantité de charge de matériaux d'électrode actifs ont été utilisées pour assembler le supercondensateur symétrique dans lequel le papier filtre a été utilisé comme séparateur. Dans les configurations à trois et à deux électrodes, des solutions aqueuses de KOH 6 M ont été utilisées comme électrolyte.
La voltamétrie cyclique (CV), la spectroscopie d'impédance électrochimique (EIS) et la charge/décharge galvanostatique constante ont été effectuées sur un instrument Gamry référence 3000. La mesure CV dans la configuration à trois électrodes a été effectuée à une fenêtre de potentiel de − 1 à 0 V par rapport à Ag/AgCl, tandis que la fenêtre de potentiel dans le supercondensateur symétrique était de 0 à 1 V. La caractérisation EIS a été réalisée à l'amplitude AC de 5 mV dans la gamme de fréquences de 1 MHz à 0,01 Hz. La capacité spécifique des courbes CV collectées à partir du test à trois électrodes a été calculée par l'équation C =ʃJe dt/mV . La capacité spécifique dérivée de la courbe CV dans les tests à deux électrodes et les tests galvanostatiques a été déterminée via C =4ʃJe dt/MV et C =v4Je t/MV , respectivement, où I est le courant de décharge, t est le temps de décharge, V est la fenêtre de tension de travail, m est la masse du matériau actif à l'électrode de travail dans la configuration à trois électrodes, et M est la masse totale du matériau actif au niveau des deux électrodes dans le supercondensateur symétrique. La densité énergétique (E ) et la densité de puissance (P ) ont été calculés à partir des tests de charge/décharge galvanostatique via E =CV 2 /2 et P =E /t , respectivement, où C est la capacité spécifique des deux électrodes testées et t est le temps de décharge.
Résultats et discussion
L'échantillon HOPC a été synthétisé en cinq étapes, comme illustré sur la figure 1. (a) Le modèle de silice KIT-6 a été préparé par une méthode modifiée dans la littérature [24] ; (b) du lignosulfonate de sodium a été imprégné dans la matrice KIT-6 en immergeant la matrice de silice KIT-6 dans la solution aqueuse de lignosulfonate de sodium; (c) le KIT-6 chargé de lignosulfonate de sodium a été carbonisé pendant 2 h dans du gaz Ar. Afin d'optimiser le processus de carbonisation, nous avons effectué la carbonisation à 700 o C, 800 o C, 900 o C, et 1000 o C. (d) après la carbonisation, la matrice de silice KIT-6 a ensuite été retirée dans une solution chaude de NaOH 2,5 M pour obtenir le carbone mésoporeux ordonné (OMC); (e) l'échantillon de carbone OMC a ensuite été activé chimiquement à l'aide de ZnCl2 à 900 o C pendant 3 h pour préparer HOPC.
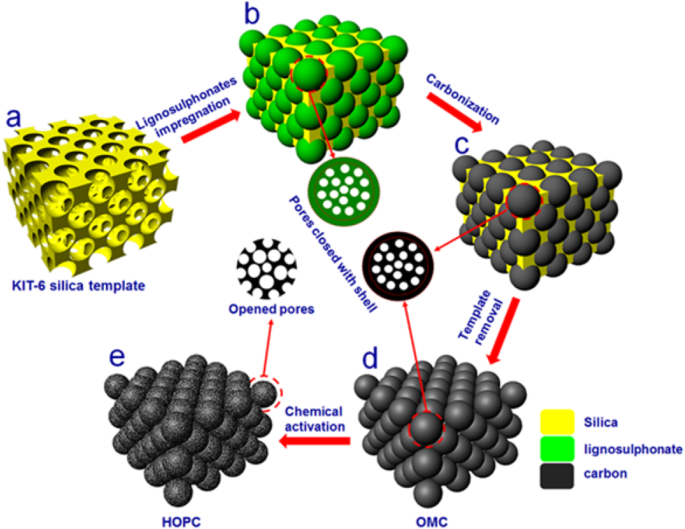
Illustration des processus de synthèse du carbone poreux hiérarchisé (HOPC) utilisant la méthode du modèle dur combinée à une activation post-chimique
Le modèle de silice KIT-6 tel que préparé a d'abord été analysé à l'aide d'un diagramme de diffraction des rayons X (XRD) sur poudre à faible angle, comme le montre la figure 2a. La silice KIT-6 telle que synthétisée appartient à l'Ia3d cubique avec deux pics de diffraction caractéristiques à 1 o et 1.2 o des plans (211) et (220) de la structure mésoporeuse ordonnée cubique [24]. Les résultats du N2 L'analyse d'adsorption/désorption montre que la matrice de silice KIT-6 est composée de mésopores majoritaires et de quelques micropores, avec une bonne interconnectivité (Fig. 2b). La distribution de la taille des pores est centrée à 2,5 nm et 7,5 nm (Fig. 2c). La superficie BET (Brunauer-Emmett-Teller) est de 1481 m 2 g −1 et le volume poreux total est de 2,62 cm 3 g −1 . Nous avons en outre étudié la micromorphologie et la structure des pores du modèle KIT-6 synthétisé par microscopie électronique à transmission (MET), comme le montre la figure 2d. Les points clairs représentent les pores et la zone sombre des parois (silice). L'épaisseur de paroi et la taille moyenne des pores sont mesurées à 3,1 nm et 6,4 nm, respectivement. L'image d'insertion du motif FFT de la figure 2d confirme la structure des pores périodiquement ordonnée.
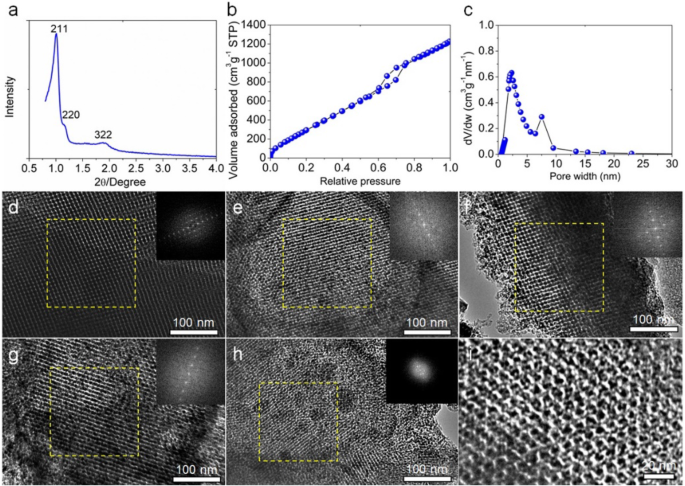
Caractérisation du modèle de silice KIT-6 préparé, a Modèle XRD à angle faible du modèle de silice KIT-6. b N2 isotherme d'adsorption/désorption du modèle KIT-6. c La distribution de taille de pores correspondante pour N2 calculé à l'aide d'un modèle NLDFT à pores fendus. Images TEM de (d ) KIT-6 silice, les échantillons de carbone OMC préparés à (e ) 700 o C, (f ) 800 o C, et (g ) 900 o C, et l'échantillon HOPC (h –je ). Les images d'insertion sont les modèles de transformée de Fourier rapide correspondants des zones sélectionnées
Les échantillons de carbone OMC ont été caractérisés par SEM et MET. Sur la figure S1, les échantillons de carbone OMC préparés à différentes températures de carbonisation présentent la morphologie en nid d'abeille avec des pores ordonnés. Nous avons ensuite utilisé la MET pour étudier la structure microporeuse, comme le montre la figure 2e–g. Les images MET montrent des nanodomaines ordonnés. Les parties sombres sont le carbone isolé et les parties brillantes sont des pores interconnectés. Les images FFT affichent des points nets et lumineux pour tous les échantillons de carbone OMC, confirmant davantage la structure des pores ordonnée. La taille des pores est de 2,9 nm, 2,1 nm et 2,4 nm pour OMC-700, OMC-800 et OMC-900, respectivement, ce qui est très proche de l'épaisseur de paroi du modèle de silice. En revanche, l'échantillon préparé à partir de la carbonisation du lignosulfonate de sodium sans l'utilisation du modèle de silice ne montre aucune structure poreuse (figure S2). Il est conclu que le carbone mésoporeux ordonné est préparé avec succès en utilisant du lignosulfonate de sodium et le modèle de silice KIT-6 aux températures de carbonisation sélectionnées.
Des expériences d'adsorption/désorption d'azote ont été menées pour étudier les propriétés physiques et chimiques des échantillons de carbone OMC tels que synthétisés, comme le montre la figure S3. Toutes les courbes isothermes ont un intermédiaire similaire et le volume adsorbé augmente à très faible pression relative et augmente rapidement avec la pression relative, suggérant la coexistence de micropores et de mésopores avec le volume de pores élevé pour tous les échantillons d'OMC tels que préparés. La distribution de la taille des pores pour les échantillons OMC est centrée à 0,6 nm et 2,3 nm. Nous avons encore augmenté la température de carbonisation à 1000 o C et la courbe isotherme de l'échantillon OMC-1000 montré dans FigureS4 affiche un profil similaire, indiquant une structure de pores similaire. La figure 3a montre la surface spécifique, le volume total des pores, le volume des micropores et le volume des mésopores en fonction de la température de carbonisation. L'augmentation de la surface spécifique est liée à l'augmentation du volume poreux total. Augmenter encore la température de carbonisation à 1000 o C, la surface spécifique diminue à 1948 m 2 g −1 , avec une diminution du volume des micropores et une augmentation du volume des mésopores. Il est suggéré que la température de carbonisation optimale soit de 900 o C. Le tableau S1 résume les propriétés physiques des échantillons de carbone OMC tels que préparés. On constate que l'échantillon OMC-900 présente la surface spécifique la plus élevée de 2 201 m 2 g −1 et un volume poreux total de 3,74 cm 3 g −1 .
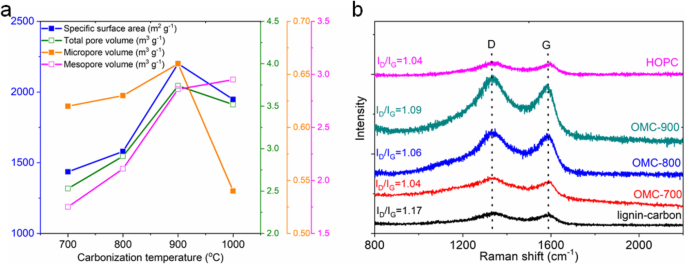
Caractérisation du carbone OMC tel que préparé et des échantillons HOPC. un La surface spécifique, le volume total des pores, le volume des micropores et le volume des mésopores en fonction de la température de carbonisation. b Spectres Raman
Nous avons donc effectué une activation chimique à l'aide de ZnCl2 comme réactif d'activation en utilisant l'échantillon OMC-900 afin de créer davantage une structure poreuse hiérarchique. Comme le montre l'image SEM de la figure S5, le réseau de pores tridimensionnels ordonné a été partiellement détruit après activation chimique pour former de nombreuses nanoparticules isolées. L'image MET de la figure 2e montre clairement des pores ordonnés et le motif FFT correspondant affiche des points lumineux, indiquant l'existence de nanodomaines ordonnés. L'image HRTEM de la figure 2f montre que des micropores se forment sur les parois des mésopores après l'activation chimique. Les résultats de N2 l'adsorption/désorption indiquent qu'après activation chimique, l'échantillon HOPC présente une surface spécifique significativement augmentée de 2602 m 2 g −1 , avec un volume microporeux de 1,03 cm 3 g −1 et volume des mésopores de 3,49 cm 3 g −1 (Tableau S1 et Figure S6a et b).
Les propriétés des lignosulfonates facilitent la formation de carbone mésoporeux ordonné. La figure S7 montre la structure moléculaire représentative du lignosulfonate, et les groupes hydroxyle permettent aux molécules de lignosulfonate de se produire une réaction de réticulation [25]. Dans la présente étude, il est proposé que les molécules de lignosulfonate soient adsorbées sur les parois de silice hydrophile à travers les groupes hydroxyle et réticulées les unes avec les autres par des liaisons hydrogène pour former des réseaux tridimensionnels. Les spectres FTIR du modèle KIT-6, du lignosulfonate de sodium et des lignosulfonates imprégnés du modèle KIT-6 sont illustrés à la figure S8. Les pics de lignosulfonate de sodium situés à 3429 cm −1 , 2950 cm −1 , 1635 cm −1 , 1514 cm −1 , 1041 cm −1 peut être affecté à l'étirement O–H, à l'étirement C–H, à l'étirement C=O, à l'étirement C–C et à l'étirement C–O [26], respectivement. Les pics du modèle de silice KIT-6 situés à 463 cm −1 , 802 cm −1 , et 1090 cm −1 sont attribués au basculement de Si–O–Si. Le pic situé à 967 cm −1 est due à la vibration de Si–O des silanols de surface [27]. Dans les spectres lignosulfonate-silice, les pics caractéristiques du lignosulfonate et de la silice coexistent, confirmant l'imprégnation du lignosulfonate dans le modèle de silice. De plus, le pic situé à 3429 cm −1 dans le lignosulfonate-silice est élargie, indiquant la formation de liaisons hydrogène entre les molécules de lignosulfonate par une réaction de réticulation. Les molécules de lignosulfonate adsorbées et orientées sont converties en couches de carbone solides au cours du processus de carbonisation, ce qui peut induire de nombreux pores fermés, comme illustré aux étapes b et c de la figure 1. L'activation chimique aide à ouvrir ces pores fermés pour améliorer davantage les propriétés physiques. .
La caractérisation Raman a été utilisée pour étudier le degré de graphite des échantillons de carbone tels que préparés et les résultats sont présentés sur la figure 3b. Tous les spectres Raman affichent la bande D et la bande G caractéristiques situées à 1340 cm −1 et 1590 cm −1 , respectivement. Le rapport d'intensité de la bande D (le carbone désordonné) et de la bande G (le carbone ordonné) pour les échantillons OMC et l'échantillon HOPC est d'environ 1,06, inférieur à 1,17 de l'échantillon de carbone préparé par la carbonisation du lignosulfonate sans utilisation de silice modèle. Ce résultat indique que les échantillons de carbone OMC ont un degré de graphite plus élevé que l'échantillon de carbone provenant de la carbonisation directe du lignosulfonate. La raison en est probablement attribuée à la réaction de réticulation mentionnée ci-dessus parmi les molécules de lignosulfonate qui aide à l'orientation des cycles aromatiques. Le résultat de l'analyse XPS de la figure S9 montre que tous les échantillons contiennent principalement du carbone et de l'oxygène. Il n'y a pas de signal détectable d'impureté dans les produits carbonés finaux. La décomposition du lignosulfonate de sodium peut donner lieu à la formation de CO2 et Na2 CO3 [28], qui peut être complètement éliminé lors du traitement de lavage ultérieur avec de l'eau déminéralisée. Le niveau de base C1s peut être déconvolué en quatre composants pour tous les échantillons de carbone tels que préparés. C'est-à-dire C–O (286,7 eV), C=O (288,0 eV) [29], le sp 2 carbone (284,8 eV, carbone ordonné), et le sp 3 carbone (285,4 eV, carbone désordonné) [30].
Les performances électrochimiques des échantillons de carbone OMC tels que préparés et de l'échantillon HOPC activé ont été évaluées via une configuration à trois électrodes dans un électrolyte aqueux KOH 6 M. L'échantillon de carbone provenant de la carbonisation directe du lignosulfonate montre des performances de stockage d'énergie négligeables (Figure S10). Les échantillons de carbone OMC affichent des profils CV rectangulaires indiquant l'amélioration des performances électrochimiques (Figure S11 et Fig. 4a). A 2 mV s −1 , la capacité spécifique est de 59 F g −1 , 93 F g −1 , 130 F g −1 , et 120 F g −1 pour OMC-700, OMC-800, OMC-900 et OMC-1000 (Fig. 4b). L'électrode OMC-900 présente les meilleures performances électrochimiques parmi tous les échantillons de carbone OMC. Après activation chimique, la capacité spécifique augmente encore jusqu'à 243 F g −1 pour l'échantillon HOPC, presque deux fois plus élevé que celui de l'échantillon OMC-900 avant activation. La capacité spécifique de HOPC dans cette étude est beaucoup plus élevée que celle du carbone dérivé des champignons (196 F g −1 à 5 mV s −1 ) [31], et également supérieur à celui du carbone mésoporeux à base d'aérogel de graphène préparé à partir d'un modèle de silice dure (226 F g −1 à 1 mV s −1 ), qui diminue à 83 F g −1 à 100 mV s −1 [32]. Pour le carbone dérivé de champignons, la capacité spécifique diminue à 90 F g −1 à 100 mV s −1 . Cependant, la capacité spécifique de HOPC est toujours aussi élevée que 128 F g −1 au même taux de balayage.
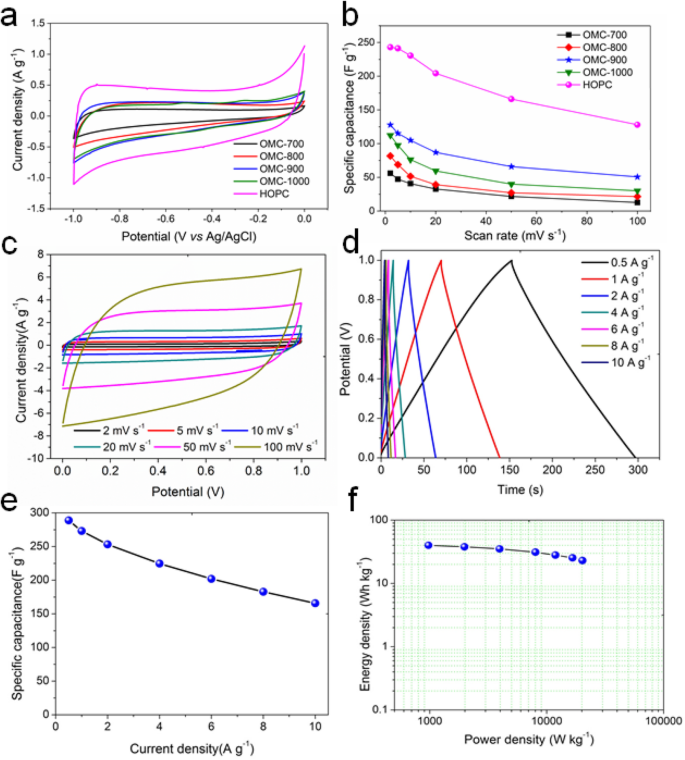
un Profils de voltamétrie cyclique (CV) des électrodes OMC-700, OMC-800, OMC-900, OMC-1000 et HOPC à une vitesse de balayage de 2 mV s −1 en utilisant la configuration à trois électrodes et b capacité spécifique correspondante. c Profils CV de l'électrode HOPC dans le supercondensateur symétrique à deux électrodes à des vitesses de balayage variant de 2 mV s −1 à 100 mV s −1 dans un électrolyte aqueux KOH 6 M. d Courbes de charge-décharge à différentes densités de courant de 0,5 A g −1 à 10 A g −1 . e Capacité spécifique calculée à partir des courbes de décharge du test de charge-décharge. f Graphiques de Ragone montrant la densité d'énergie en fonction de la densité de puissance
Des mesures d'impédance ont été effectuées pour étudier la conductivité des échantillons. La figure S12 révèle les spectres d'impédance de Nyquist dans la plage de fréquences de 1 MHz à 0,01 Hz, et le circuit équivalent correspondant qui se compose de la résistance série équivalente (R s ), résistance de transfert de charge (R ct ), et la capacité électrochimique à double couche. La résistance série équivalente R s est de 0,7 Ω cm −2 pour toutes les électrodes, indiquant la conductivité électrique élevée des échantillons et la haute qualité des électrodes. Les tracés de Nyquist indiquent que l'électrode HOPC présente la plus faible résistance de transfert de charge de 5 Ω.
L'énergie livrable et la densité de puissance sont fortement liées à la capacité dépendante de la fréquence [33, 34], qui peut être exprimée comme suit
$$ C=\frac{1}{jwZ}=\frac{-{Z}_{\mathrm{image}}}{W{\left|Z\right|}^2}-j\frac{-{ Z}_{\mathrm{real}}}{W{\left|Z\right|}^2}={C}_{\mathrm{real}}-j{C}_{\mathrm{image}} $$où C et Z sont respectivement la capacité et la résistance. Z réel et Z image se référer aux parties réelles et imaginaires de Z . C réel est la partie réelle de la capacité représentant la capacité livrable des matériaux d'électrode, et C image est la capacité imaginaire liée à la perte de résistivité irréversible dans le dispositif. La figure S13a montre que l'échantillon HOPC a eu la réponse la plus rapide. La fréquence ƒ est la fréquence de caractères à laquelle C image atteint le maximum, et t =1/ƒ est la constante de temps du supercondensateur. Les deux f et t sont la capacité de débit caractéristique. Les supercondensateurs à haute densité de puissance ont généralement une fréquence de caractères élevée ƒ et petit t . La figure S13b montre les tracés de C image en fonction de la fréquence. La fréquence des caractères des échantillons OMC-700, OMC-800, OMC-900, OMC-1000 et HOPC est de 0,01 Hz, 0,1 Hz, 0,01 Hz, 0,01 Hz et 0,5 Hz, et la constante de temps correspondante est de 100 s, 10 s, 100 s, 100 s et 2 s. L'échantillon HOPC montre la fréquence de caractères la plus élevée et la constante de temps la plus faible, indiquant la réponse la plus rapide à la puissance de sortie.
Il a été démontré que HOPC affiche des performances électrochimiques élevées. Cependant, pour les applications pratiques, les tests de configuration à trois électrodes ne peuvent pas révéler la capacité réelle de stockage d'énergie [33, 35]. Par conséquent, nous avons utilisé un échantillon HOPC pour préparer des électrodes afin d'assembler des supercondensateurs symétriques. La figure 4c illustre les courbes CV de l'électrode HOPC. Les profils CV présentent une forme presque rectangulaire avec une bonne symétrie à toutes les vitesses de balayage à partir de 2 mV s −1 à 100 mV s −1 , indiquant les bonnes propriétés électrochimiques et la stabilité de vitesse de l'électrode HOPC. Les mesures de charge-décharge galvanostatique à des densités de courant constantes ont également été effectuées sur le supercondensateur symétrique tel qu'assemblé et les résultats sont présentés sur la figure 4d. Les profils linéaires de tension en fonction du temps pendant le processus de charge et de décharge montrent une forme triangulaire idéale avec une bonne symétrie, représentant la capacité exceptionnelle de stockage d'énergie de l'électrode HOPC. Lorsque la densité de courant était de 0,5 A g −1 , le temps de décharge est aussi long que 150 s, ce qui correspond à la capacité spécifique d'environ 289 F g −1 . La capacité spécifique du HOPC du lignosulfonate à 10 A g −1 est toujours aussi élevé que 166 F g −1 , comme le montre la figure 4e. La performance du HOPC dans cette étude est meilleure que les valeurs des échantillons de carbone dans les littératures [3, 36,37,38,39].
La capacité spécifique élevée de HOPC contribue à la faible résistance ohmique et à la résistance de transfert de charge, qui est d'environ 0,6 cm −1 et 2,4 Ω cm −1 , respectivement, comme le montre la figure S14. L'angle de phase du supercondensateur symétrique à la fréquence la plus basse de 0,01 Hz est d'environ 81,7 o (Figure S15), qui est très proche de la valeur du supercondensateur idéal (90 o ). La fréquence des caractères est d'environ 0,2 Hz, correspondant à la constante de temps de 5 s. Cela signifie que l'électrode HOPC a une bonne capacité de livraison de puissance. La capacité livrable atteint 290 mF (Figure S16). La figure 4f illustre le tracé de Ragone du supercondensateur symétrique. La densité énergétique est de l'ordre de 40 Wh kg −1 à 23 Wh kg −1 avec une densité de puissance d'environ 0,9 kW kg −1 à 20 kW kg −1 .
La capacité spécifique élevée et la densité d'énergie de HOPC peuvent contribuer à la structure optimisée des pores. L'échantillon HOPC contient un volume poreux élevé des micropores et des mésopores. Comme démontré dans les littératures précédentes par analyse de corrélation [40, 41], les micropores sont fortement liés au stockage d'énergie et les mésopores sont fortement liés à la rétention de capacité puisque les mésopores sont principalement responsables du transport des ions. Il est également conclu que les mésopores ont des contributions au stockage de charge. Gardez les instructions ci-dessus à l'esprit, nous avons utilisé avec dévouement la méthode du modèle dur et l'activation chimique pour préparer l'échantillon HOPC. Les présents résultats non seulement démontrent davantage les conclusions ci-dessus, mais montrent également la conception pour la préparation de matériaux de stockage d'énergie à haute performance. Afin de mesurer la cyclabilité, le supercondensateur symétrique utilisant du HOPC comme matériau d'électrode est chargé et déchargé à plusieurs reprises à 2 A g −1 pour 3000 cycles (Figure S17). On constate qu'après 3000 cycles, la capacité spécifique est de 218 F g −1 avec une légère diminution par rapport aux 253 F initiaux g −1 avec une rétention de capacité de 86,2 %. La capacité spécifique de notre échantillon HOPC du système à deux électrodes est supérieure et comparable après 3000 cycles avec les valeurs rapportées dans le tableau S2. Par conséquent, la présente étude fournit une voie potentielle pour le développement de matériaux actifs d'électrode de supercondensateur à haute performance à partir de déchets industriels.
Conclusion
In this study, we have successfully prepared ordered mesoporous carbon materials using biowaste lignosulphonate as the carbon source using the mold casting technique based on KIT-6 template. During the mold casting process, lignosulphonate can easily be cast into the pores of KIT-6. The crosslinking reaction of lignosulphonate molecules not only increases the pore volume, but also bridges the aromatic rings to promote the graphitization. The as-synthesized ordered mesoporous carbons exhibit high electrical conductivity, high-specific surface area, and pore volume, which are highly dependent on the carbonization temperature. The results of Raman analysis and N2 adsorption/desorption experiments show that the OMC-900 sample has the best physical properties. The pore structure of OMC-900 was further optimized through ZnCl2 chemical activation to prepare HOPC. The specific capacitance of HOPC in the symmetric supercapacitor was about 289 F g −1 with the energy density as high as 40 Wh kg −1 . The present study indicates lignosulphonate is very suitable to prepare hierarchical ordered porous carbon at low cost with high-performance supercapacitors.
Disponibilité des données et des matériaux
All data generated or analyzed in this study are included in the manuscript and the supplementary information files. All the materials are available from the corresponding author on request.
Abréviations
- HOPC:
-
Hierarchical ordered porous carbon
- KIT-6:
-
The ordered mesoporous silica template
- OMC :
-
The ordered mesoporous carbon
- NMP :
-
N-methyl pyrrolidone
- PVDF :
-
Fluorure de polyvinylidène
- CV :
-
Voltamétrie cyclique
- EIS :
-
Spectroscopie d'impédance électrochimique
- CA :
-
Courant alternatif
Nanomatériaux
- Composites de graphène et polymères pour applications de supercondensateurs :une revue
- Fibres de carbone activées avec nanostructure hiérarchique dérivées de déchets de gants de coton en tant qu'électrodes hautes performances pour supercondensateurs
- Synthèse facile de nanofils d'argent avec différents rapports d'aspect et utilisés comme électrodes transparentes flexibles hautes performances
- Nanosphères de carbone monodispersées à structure poreuse hiérarchique comme matériau d'électrode pour supercondensateur
- Microsphères de carbone magnétique comme adsorbant réutilisable pour l'élimination des sulfamides de l'eau
- Une approche simple pour la synthèse de points quantiques de carbone fluorescent à partir d'eaux usées de tofu
- Évaluation des structures graphène/WO3 et graphène/CeO x en tant qu'électrodes pour les applications de supercondensateurs
- Composite aérogel/soufre de charbon actif revêtu de polyaniline pour batterie lithium-soufre hautes performances
- Synthèse et performances des supercondensateurs de composites de carbone mésoporeux ordonnés polyaniline/azote



