Synthèse contrôlée par nanocanaux d'une efficacité de dopage à l'azote ultra-élevée sur des catalyseurs Fe/N/C mésoporeux pour la réaction de réduction de l'oxygène
Résumé
La conception de méthodes appropriées pour améliorer efficacement l'efficacité du dopage à l'azote et la densité des sites actifs est essentielle pour stimuler l'activité de la réaction de réduction de l'oxygène (ORR) des électrocatalyseurs de type Fe/N/C sans platine. Ici, nous proposons une stratégie simple et efficace pour concevoir un catalyseur Fe/N/C à structure mésopore pour l'ORR avec une surface BET ultra-élevée et une conductivité exceptionnelle via des nanocanaux de pyrolyse confinée au tamis moléculaire de Fe 2+ ions coordonnés avec des complexes 2,4,6-tri(2-pyridyl)-1,3,5-triazine en tant que nouveau précurseur avec un effet de coordination stable. La combinaison de l'effet confiné dans les nanocanaux avec l'effet de coordination stable peut améliorer de manière synergique la stabilité thermique et stabiliser les sites actifs enrichis en azote, et aider à contrôler la perte d'atomes N actifs pendant le processus de pyrolyse et à obtenir en outre une densité de sites actifs élevée pour l'amélioration de l'activité de l'ORR. L'électrocatalyseur Fe/N/C tel que préparé a présenté une excellente activité catalytique avec un potentiel d'apparition de ~ 0,841 V (par rapport à RHE) approchant étroitement le catalyseur Pt/C et une stabilité élevée à long terme dans l'électrolyte alcalin. En outre, un faible rendement en peroxyde d'hydrogène (<6,5%) et un nombre élevé de transfert d'électrons (3,88 à 3,94) peuvent être trouvés sur ce catalyseur, indiquant qu'il est un substitut précieux aux catalyseurs Pt/C traditionnels. Ce travail ouvre une nouvelle voie pour concevoir des électrocatalyseurs Fe/N/C hautes performances et approfondit la compréhension du site actif et du mécanisme de catalyse ORR.
Introduction
L'exploration de dispositifs avancés d'énergie propre (par exemple, les piles à combustible et les batteries métal-air) est actuellement une solution efficace pour résoudre la pollution de l'environnement et la crise énergétique. Dans ces systèmes, la réaction de réduction de l'oxygène (ORR) possédant les caractéristiques d'une cinétique lente et d'une diversité de voies réactionnelles est un processus crucial [1, 2]. À l'heure actuelle, les électrocatalyseurs de première classe et largement utilisés pour l'ORR sont les nanoparticules de platine ancrées sur divers matériaux carbonés, mais elles présentent certains inconvénients (par exemple, coût élevé, rareté, stabilité médiocre et empoisonnement facile) pour limiter largement le applications commerciales à grande échelle [3]. Ainsi, la conception d'électrocatalyseurs ORR bon marché et très efficaces sans platine ou métaux non nobles est extrêmement indispensable.
Ces dernières années, les électrocatalyseurs au carbone dopé sont considérés comme l'un des électrocatalyseurs potentiels non nobles en tant que substituts des catalyseurs commerciaux à base de Pt en termes d'avantages tels qu'un faible coût, des performances élevées, une résistance à la corrosion et des ressources abondantes. [4, 5]. Les carbones dopés aux métaux de transition/azote (TM/N/C) servant de type le plus important de catalyseurs ORR à carbone dopé sont devenus un domaine de recherche populaire [4,5,6]. D'une part, la synthèse de catalyseurs TM/N/C non platine dérivés de la phtalocyanine, de la porphyrine, et de leurs dérivés contenant un TM-Nx (x =2, 4, 6, et al.) structure en tant que précurseurs prometteurs [4,5,6,7,8,9,10], mais le sujet de préoccupation est généralement limité à une raison pour laquelle la structure de TM-N
L'une des préoccupations est que la fabrication de catalyseurs Fe/N/C à partir de la carbonisation directe de polymères macromoléculaires [12, 19, 20], de complexes chimiques et de protéines biologiques contenant du Fe-Nx structures [15, 21, 22], et d'autres sources de fer-azote [17, 23, 24] est généralement réalisée dans un système ouvert. En outre, la plupart des précurseurs enrichis en azote peuvent facilement se produire lors de l'accumulation ou de l'agglomération dans le processus de carbonisation, ce qui empêchera l'exposition efficace des sites actifs catalytiquement ORR, favorisera la perte thermique d'atomes de N et réduira la densité des sites actifs, entraînant la limitation des performances ORR des catalyseurs Fe/N/C [25]. Une autre préoccupation est que la conductivité électronique des matériaux Fe/N/C synthétisés détermine également leur activité ORR. Généralement, lorsque la conductivité élevée des catalyseurs Fe/N/C est obtenue, les atomes d'azote actifs perdent sérieusement pendant le processus de calcination. En d'autres termes, la conductance et le nombre de sites actifs ne peuvent pas être pris en compte simultanément dans un système ouvert. Contrôler la perte d'atomes d'azote actifs pendant le processus de pyrolyse est toujours un problème urgent pour améliorer l'activité électrocatalytique. Plusieurs groupes de recherche ont proposé des stratégies efficaces de réaction confinée pour améliorer ce phénomène. Quelques échantillons typiques sont les suivants :(i) la montmorillonite avec un espace intercalaire confiné de ~ 1 nm est utilisée comme réacteur confiné dans l'espace 2D pour éviter le tassement et la perte thermique des atomes d'azote actifs et augmenter les caractéristiques de conductance [26] , (i) les chlorures de sodium sursaturés sont émergés comme un réacteur totalement fermé pour contrôler la perte d'azote et augmenter la densité de site actif [27], et (iii) notre groupe a récemment utilisé des agrégats 3D-NaCl auto-assemblés comme semi-fermé réacteur confiné pour diminuer efficacement la vitesse de décomposition des structures actives riches en azote, conduisant à l'augmentation de la densité du site actif et à l'amélioration de l'activité ORR [25]. Cependant, ces méthodes nécessitent généralement un prétraitement lourd, une technologie compliquée ou une résistance limitée à la température trop élevée.
Ici, nous proposons une stratégie simple et facile pour concevoir un nouveau catalyseur Fe/N/C via des nanocanaux de pyrolyse confinée au tamis moléculaire de Fe coordonnée avec 2,4,6-tri(2-pyridyl)-1,3,5- complexes de triazine (Fe-TPTZ) en tant que nouveau précurseur avec un effet de coordination stable. Dans le processus de carbonisation à haute température, cette méthode confinée peut diminuer la perte partielle d'atomes de N, améliorer la surface BET et les caractéristiques mésoporeuses, favoriser l'efficacité de dopage à l'azote et la densité de site actif, et augmenter la conductivité électronique, ce qui peut augmenter efficacement l'activité électrocatalytique ORR du catalyseur Fe/N/C. Le comportement cinétique de l'ORR et le mécanisme de catalyse du catalyseur Fe/N/C ont été étudiés plus en détail. L'excellente activité ORR avec un potentiel d'apparition de ~ 0,841 V (versus RHE) s'approchant de près du catalyseur Pt/C et une stabilité élevée à long terme peuvent être observées au niveau du catalyseur Fe/N/C, indiquant qu'il est un substitut précieux au traditionnel Catalyseurs Pt/C en solution alcaline. L'impact futur de cette étude fournit une nouvelle idée ou méthode pour concevoir un catalyseur Fe/N/C non noble de haute performance en intégrant l'effet de coordination stable au niveau moléculaire et les effets confinés dans les nanocanaux et approfondit la compréhension du site actif et Mécanisme de catalyse ORR.
Méthodes
Synthèse de catalyseurs Fe/N/C mésoporeux
Afin de synthétiser le précurseur de catalyseur Fe/N/C, 0,2 g de tamis moléculaires KIT-6 (KIT-MS) (fournis par Jiangshu Jichang Nano-Technology Co., Ltd.) avec une surface BET de 780 m 2 g -1 est dispersé par ultrasons dans 0,2 mol l -1 Solution de HCl (volume total 20 ml). Par la suite, 0,2 g de 2,4,6-tri(2-pyridyl)-1,3,5-triazine (TPTZ) fourni par Shanghai Aladdin Biochemical Technology Co., Ltd. et 0,0423 g de FeCl2 ·4H2 O ont été successivement ajoutés sur la base d'une condition fixe :n (Fe 2+ ):n (TPTZ) =1 :3 et ont été encore agités pendant 5 h à 25°C pour garantir adéquatement la réaction de coordination entre Fe 2+ ions et le TPTZ et fixent efficacement les complexes Fe-TPTZ formés dans les nanocanaux (taille des pores de 4 à 10 nm) du KIT-MS. Après avoir été séché à 80 °C dans une étuve, l'échantillon obtenu est marqué comme précurseur Fe-TPTZ@KIT-MS, qui est ensuite chauffé à différentes températures (800 °C, 900 °C et 950 °C) pendant 2 h dans un four à résistance tubulaire avec un N2 -débit de 0.5 L min -1 . Les échantillons obtenus ont été absolument gravés par de l'acide fluorhydrique (40 % en poids) et lavés à plusieurs reprises par de l'eau redistillée pour produire trois types de catalyseurs Fe/N/C mésoporeux (marqués comme m -Fe/N/C-800, m -Fe/N/C-900 et m -Fe/N/C-950, respectivement). Le processus conçu de catalyseurs Fe/N/C mésoporeux à haute densité de sites actifs est indiqué sur la figure 1. Il est à noter que le KIT-MS peut être considéré comme un nouveau réacteur confiné à nanocanaux pour contrôler efficacement la perte de décomposition thermique de atomes d'azote et en améliorant encore la densité de sites actifs dopés à l'azote dans le cadre du processus de pyrolyse à haute température. De plus, la principale raison pour laquelle le complexe Fe-TPTZ est un matériau de départ précieux pour la production d'électrocatalyseurs Fe/N/C à structure mésoporeuse avec une densité de sites actifs élevée est due au rôle de coordination important entre Fe 2+ des ions et des atomes d'azote dans le ligand TPTZ, qui peuvent stabiliser thermiquement la structure complexe Fe-TPTZ et favoriser la dispersité des espèces contenant du Fe dans les catalyseurs Fe/N/C finaux. Pendant ce temps, il peut réduire efficacement la vitesse de décomposition thermique des atomes N pendant le processus de pyrolyse et améliorer la densité de site catalytiquement actif dopé à l'azote pour optimiser les performances de l'ORR. En guise de contrôle, nous avons préparé le m -Ni/N/C-900 et m -Cu/N/C-900 en utilisant la même méthode de synthèse à 900°C et en utilisant le KIT-MS comme nouveau réacteur confiné à nanocanaux. Nous avons également synthétisé les catalyseurs Fe/N/C-900 et N/C-900 à la même température de traitement thermique, dérivés respectivement du complexe Fe-TPTZ et du ligand TPTZ, sans utiliser KIT-MS comme réacteur confiné à nanocanaux. .
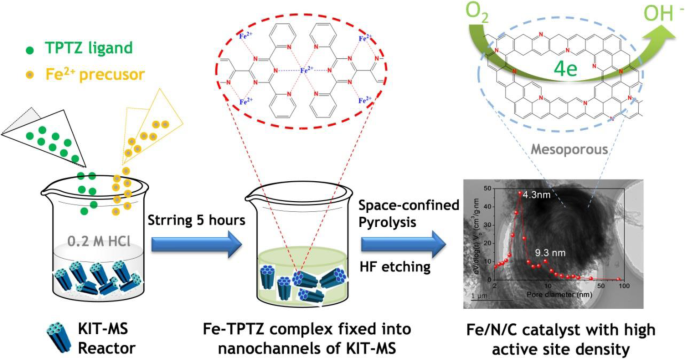
Un schéma pour la synthèse de catalyseurs Fe/N/C mésoporeux
Caractérisation des catalyseurs Fe/N/C mésoporeux
Les données d'analyse thermogravimétrique ont été obtenues sur un analyseur thermique différentiel Shimadzu DTG-60H sous atmosphère d'azote avec une vitesse de chauffage de 10 °C min -1 . Les données de spectroscopie photoélectronique aux rayons X (XPS) ont été recueillies sur un spectromètre Kratos XSAM800. Des images de microscopie électronique à balayage et à transmission à haute résolution ont été obtenues sur les instruments Hitachi UHR S4800 et FEI Tecnai-G2 F30, respectivement. Les isothermes d'adsorption/désorption d'azote ont été testés sur un analyseur Micromeritics ASAP 2010 à 77 K. Les données de diffraction des rayons X (XRD) ont été obtenues sur un diffractomètre à rayons X Shimadzu XRD-6000 (Cu Ka1 rayonnement, λ =1,54178 Ǻ) à une vitesse de balayage de 4° min -1 . Le système Horiba HR800 Raman a été utilisé pour mesurer la spectroscopie Raman avec une longueur d'onde d'excitation de 532 nm.
Tests électrochimiques
Toutes les données électrochimiques ont été recueillies sur un bipotentiostat CHI760E (Shanghai Chenhua Instruments Co. Ltd., Chine) avec un système à trois électrodes, composé d'un anneau de rotation (Pt)-disque (carbone vitreux, Φ =5 mm) électrode de travail (RRDE, American Pine Instrument Co., Ltd.), une électrode de référence au calomel saturé (SCE) et une contre-électrode en feuille de Pt (1 cm 2 ). La préparation du RRDE revêtu de catalyseur fait référence aux rapports précédents [21, 25]. Généralement, 10 μl de 10 mg ml −1 la dispersion de catalyseur a été déposée sur du RRDE et séchée naturellement. Le chargement en masse du catalyseur était limité à environ 600 μg cm −2 . Tous les potentiels d'électrode par rapport au SCE dans l'électrolyte alcalin ont été convertis en potentiels par rapport à l'électrode à hydrogène réversible (RHE) sur la base de l'équation de Nernst. En d'autres termes, la conversion de potentiel suit cette équation :E (vs. RHE)/V =E (vs. SCE)/V + 1.0 V Avant de faire le test électrochimique, l'activation du RRDE revêtu de catalyseur a été réalisée par le test de voltamétrie cyclique de 1,2 à 0,2 V vs RHE en 0,1 mol l -1 Solution de KOH saturée en azote pendant 20 cycles. Le taux de balayage est de 5 mV s -1 et l'électrolyte est 0,1 mol l -1 KOH dans tous les tests de voltampérométrie.
Résultats et discussion
L'analyse thermogravimétrique (TGA) de trois précurseurs (Fe-TPTZ@KIT-MS, Fe-TPTZ et TPTZ) est d'abord indiquée sur la figure 2a. On voit que la décomposition thermique du ligand TPTZ est rapide après que la température dépasse 300 °C et que seulement ~ 9,0 % de la masse résiduelle peut être économisée. Cependant, la masse résiduelle est de ~ 40,3% à la courbe TGA du complexe Fe-TPTZ, suggérant la formation de l'interaction de coordination relativement stable de Fe 2+ des ions et des atomes d'azote tels que les atomes d'azote pyridinique sur le bord ou les atomes d'azote du cycle aromatique dans le ligand TPTZ [28]. Cet effet de complexation au niveau moléculaire peut principalement améliorer la stabilité thermique du complexe Fe-TPTZ et également aider à produire des molécules TPTZ pontées et réticulées. Le comportement de décomposition du Fe-TPTZ peut être encore retardé grâce à l'utilisation du rôle confiné dans l'espace des nanocanaux de KIT-MS en tant que nouveau nanoréacteur, conduisant à la plus grande masse résiduelle (47,4%) de Fe-TPTZ@KIT- MME. Ce rôle peut être en faveur de l'augmentation de l'efficacité dopé à l'azote et de la densité de sites actifs lors de la pyrolyse à haute température, facilitant l'optimisation des performances ORR des catalyseurs Fe/N/C mésoporeux. Pour examiner plus en détail si l'interaction de coordination stable était complètement formée, nous avons d'abord caractérisé TPTZ, Fe-TPTZ et Fe-TPTZ@KIT-MS par des spectres XPS N1s haute résolution (Fig. 2b). De toute évidence, l'énergie de liaison (B.E.) de l'azote pyridinique est passée positivement de 398,8 eV pour le ligand TPTZ à 399,1 eV pour le complexe Fe-TPTZ ou le précurseur Fe-TPTZ@KIT-MS. Il fournit la preuve directe de la réduction de la densité électronique autour des atomes pyridiniques-N après Fe 2+ ions sont introduits, car le décalage positif dans B.E. peut être attribuable à l'interaction de complexation qui s'est produite entre Fe 2+ ions et atomes pyridiniques-N sur le bord de la molécule TPTZ dans lesquels les orbitales 3d-inoccupées de Fe 2+ les ions peuvent être efficacement remplis par les électrons de la paire isolée d'atomes d'azote pyridinique. La formation du complexe Fe-TPTZ peut en outre induire plus d'atomes d'azote pyridinique à se rassembler autour des atomes de Fe, ce qui peut être bénéfique pour produire plus de Fe-Nx structures de sites actifs entraînant l'amélioration de l'activité électrocatalytique de l'ORR des catalyseurs Fe/N/C à structure mésoporeuse tels que préparés.
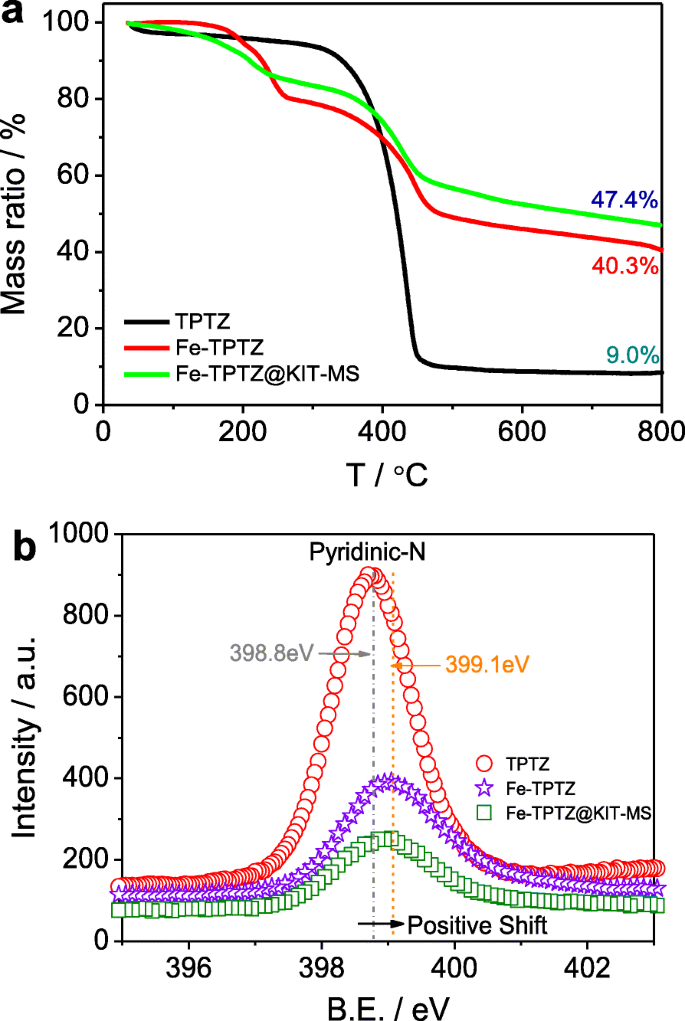
un Courbes TGA et b N1s haute résolution Spectres XPS des précurseurs TPTZ, Fe-TPTZ et Fe-TPTZ@KIT-MS
Sur la base du fait que la caractéristique de conductance des électrocatalyseurs de type Fe/N/C maintenait un lien étroit avec leurs performances catalytiques ORR, nous avons mesuré la conductivité électronique de m -Fe/N/C-800, m -Fe/N/C-900 et m -Fe/N/C-950 par la spectroscopie d'impédance électrochimique (EIS). Les données EIS ont été obtenues dans une solution mixte composée de 0,1 M de KCl comme électrolyte et de 1 mM [Fe(CN)6 ] 3- /[Fe(CN)6 ] 4- comme sonde redox. Les résultats de Bode sont présentés sur la figure 3a, et les graphiques de Nyquist sont indiqués dans l'encart de la figure 3a. Les tracés de Nyquist sont équipés d'un circuit équivalent (voir Fichier complémentaire 1 :Figure S1) avec cinq composantes de R s , C dl , R p , R int , et C ϕ , où R s représente la résistance de l'électrolyte survenue entre l'électrode de référence et l'électrode de travail. C dl représente la capacité double couche sur l'interface électrode solide/électrolyte, C ϕ est la relaxation de charge associée à la formation d'intermédiaires de surface, R p représente la résistance de transfert de charge pendant l'ORR, et R int représente la facilité avec la formation d'intermédiaires. La somme de R p et R int est lié au taux de l'ORR. Les résultats ajustés sont suggérés dans le fichier supplémentaire 1 :tableau S1. On peut trouver que la somme de R p et R int est seulement 2232.2 Ω pour m -Fe/N/C-900, mais est d'environ 2475.5 Ω pour m -Fe/N/C-800 et jusqu'à 4418.6 Ω pour m -Fe/N/C-950, respectivement. Une somme plus petite suggère un taux ORR relativement plus rapide, ce qui signifie que le catalyseur correspondant (m -Fe/N/C-900) a présenté une meilleure activité électrocatalytique ORR.
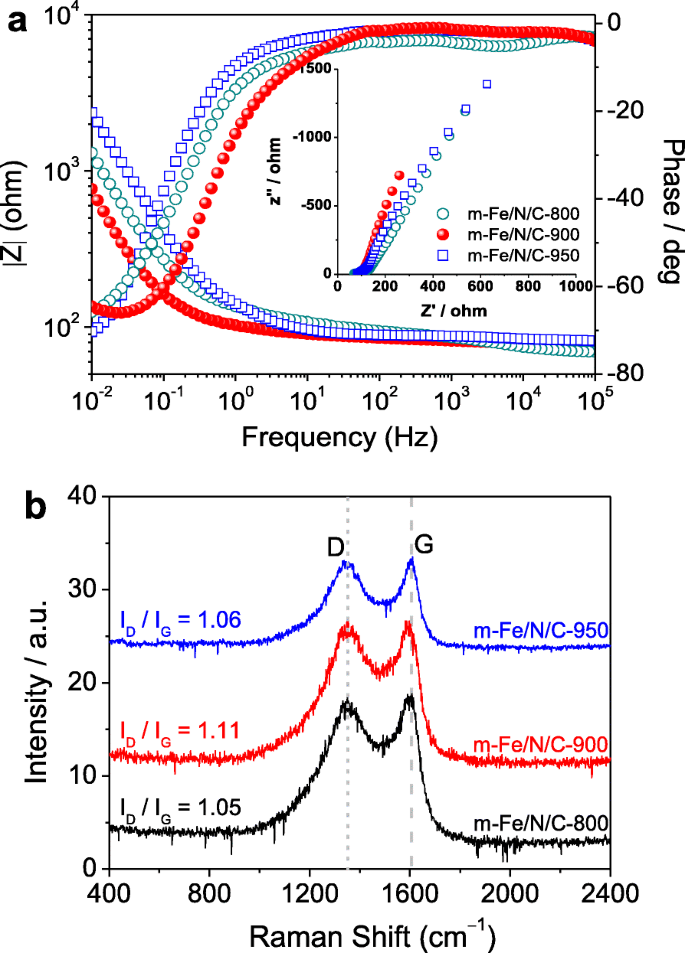
un EIS augure un tracé de m-Fe/N/C-800, m-Fe/N/C-900 et m-Fe/N/C-950 ; l'encart est le tracé de Nyquist correspondant. b Spectres Raman de m-Fe/N/C-800, m-Fe/N/C-900 et m-Fe/N/C-950
Spectres Raman de m -Fe/N/C-800, m -Fe/N/C-900 et m -Fe/N/C-950 (voir Fig. 3b) ont été mesurés puis ont été placés dans deux pics lorentziens. Le pic centré à ~ 1350 cm -1 correspond à la bande D désordonnée induite par la structure, qui est généralement due à l'apparition de divers défauts dopés par hétéroatomes dans le plan [18]. Le pic centré à ~ 1600 cm -1 représente toute la bande G induite par la structure graphitique avec le E dans le plan 2g mode vibration [25]. Leur rapport d'intensité (I D /Je G ) a été utilisé de manière significative pour discriminer les degrés de désordre et de graphitisation. On constate que le I D /Je G valeur sur m -Fe/N/C-900 est d'environ 1,11, ce qui est évidemment plus élevé que sur m -Fe/N/C-800 (I D /Je G =1,05) ou m -Fe/N/C-950 (I D /Je G =1,06). Cela implique qu'il peut exister plus de structures défectueuses contenant de l'azote et une teneur en dopage plus élevée d'atomes d'azote dans m -Fe/N/C-900, ce qui est en bon accord avec les résultats de l'analyse XPS. Dans cette étude, nous avons directement fixé les complexes Fe-TPTZ dans des nanocanaux de tamis moléculaires, car un nouveau réacteur de nanoconfinement peut les protéger de manière significative de la décomposition pyrogène. En outre, le fort effet de coordination au niveau moléculaire entre Fe 2+ Les ions et les atomes d'azote dans le ligand TPTZ peuvent également stabiliser le précurseur Fe-TPTZ dans une certaine mesure et favoriser davantage la teneur totale en N et l'efficacité de dopage N pendant le processus de pyrolyse. Certains résultats précédemment rapportés ont proposé que la teneur en dopage des atomes N peut influencer positivement la conductivité électrique des catalyseurs au carbone dopé [22, 26], soutenant de manière adéquate la caractéristique de conductance optimale et l'efficacité de dopage N la plus élevée du m -Fe/N/C-900 électrocatalyseur préparé dans ce travail.
L'analyse de la spectroscopie photoélectronique aux rayons X (XPS) a été appliquée pour étudier la structure électronique et la composition chimique à la surface de m -Fe/N/C-800, m -Fe/N/C-900 et m -Fe/N/C-950. D'après les spectres XPS de l'enquête (Fig. 4 et Fichier supplémentaire 1 :Figure S2), nous constatons que tous les catalyseurs de type Fe/N/C contiennent en grande partie les éléments C, N, O et Fe, prouvant que Fe et N les atomes ont été dopés avec succès dans la structure carbonée. Les teneurs totales en Fe, C et N de l'analyse de surface XPS et tous les rapports N/C dans les électrocatalyseurs ORR de type Fe/N/C mésoporeux tels que préparés sont résumés dans le tableau 1. Il est montré que le rapport N/C dans m -Fe/N/C-900 est jusqu'à 10,3, ce qui est évidemment plus grand que celui en m -Fe/N/C-800 (~ 10,0) ou m -Fe/N/C-950 (~ 4,4), suggérant en outre l'efficacité de dopage à l'azote la plus élevée et la teneur totale en azote en m -Fe/N/C-900. Les C1s Analyse XPS de m -Fe/N/C-900 (Fig. 4b) approuve également le dopage des atomes d'azote grâce à l'apparition d'un pic caractéristique correspondant à la sp 2 Liaison C=N à l'énergie de liaison (B.E.) de ~ 286,5 eV. De plus, le signal de l'élément Fe dans les spectres XPS d'étude des électrocatalyseurs de type Fe/N/C tels que préparés est relativement faible car la teneur en Fe est très faible après lixiviation en solution acide. Pour examiner l'état électronique des atomes de Fe, nous avons analysé le Fe 2p Spectre XPS de m -Fe/N/C-900 sur la figure 2b, qui a été ajusté dans quatre pics avec B.E. de 710,3, 712,9, 716,8 et 725,3 eV, respectivement. Le pic situé à ~ 710.3 eV peut être attribué au pic caractéristique de la liaison Fe-N, montrant l'occurrence du Fe 2+ état en m -Fe/N/C-900 [29, 30]. L'être. situé à environ 712,9 eV et 725,3 eV correspond au Fe 3+ 2p 3/2 et Fe 3+ 2p 1/2 , respectivement (Fig. 4c), ce qui suggère que les atomes de Fe du complexe Fe-TPTZ peuvent être partiellement oxydés; cependant, le pic situé à 716,8 eV peut représenter le pic satellite de la liaison Fe-N. Pour assurer davantage l'état chimique des oxydes de Fe, nous avons analysé les O1s spectre de m -Fe/N/C-900 (Fig. 4d). Il est divisé en trois pics avec B.E. de 531,0, 532,3 et 533,2 eV, ce qui correspond à C–O–C, C=O et Fe–O séparément [31]. Les résultats mentionnés ci-dessus peuvent indiquer que l'état existant des atomes de Fe est en grande partie composé de liaisons Fe-N et Fe-O dans le m -Électrocatalyseur Fe/N/C-900.
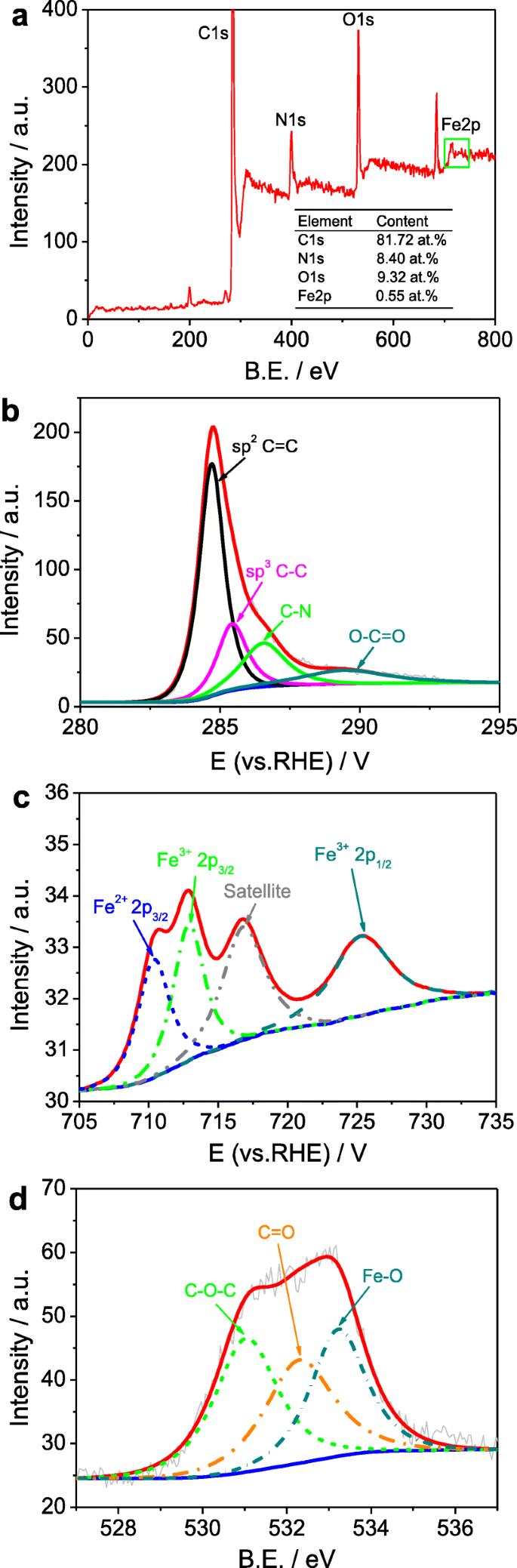
Sondage (a ), Fe 2p (b ), O 1s (c ), et C 1s (d ) Spectres XPS de m -Fe/N/C-900
Les N1s équipés Spectres XPS de m -Fe/N/C-800 et m -Fe/N/C-900 (voir Fig. 5a, b) affiche quatre pics avec B.E. de 398,3, 399,5, 401,1 et 406,1 eV, qui sont individuellement attribuables au N pyridinique, au N Fe-N, au N graphitique et au N oxydé (-NO2 ) [10, 16, 25, 26, 32, 33]. Cependant, les N1s équipés Spectre XPS de m -Fe/N/C-950 (Fig. 5c) n'a montré que trois pics avec B.E. de 399,2, 401,4 et 406,4 eV, correspondant au Fe–N, au N graphitique et au N oxydé (–NO2 ), respectivement. Il est à noter que la densité du nuage d'électrons des atomes d'azote est décalée en raison d'une électronégativité plus forte des atomes d'oxygène, ce qui entraîne l'apparition du pic d'oxydation au stade de haute énergie. Le rapport relatif des groupes graphitiques-N domine dans la teneur totale en azote, mais le rapport relatif du N oxydé inactif (–NO2 ) augmente de 17,8 à 38,7 at.% avec une augmentation de la température de pyrolyse, comme indiqué sur la figure 5d. En outre, une température de pyrolyse plus élevée entraînera la disparition du groupe pyridinique-N dans m -Fe/N/C-950. Les résultats ci-dessus montrent que le groupe Fe-N peut être formé dans des catalyseurs de type Fe/N/C tels que préparés, mais les groupes N pyridiniques et graphitiques actifs sont d'une grande importance pour déterminer l'activité ORR de Fe/N/C- électrocatalyseurs de type.
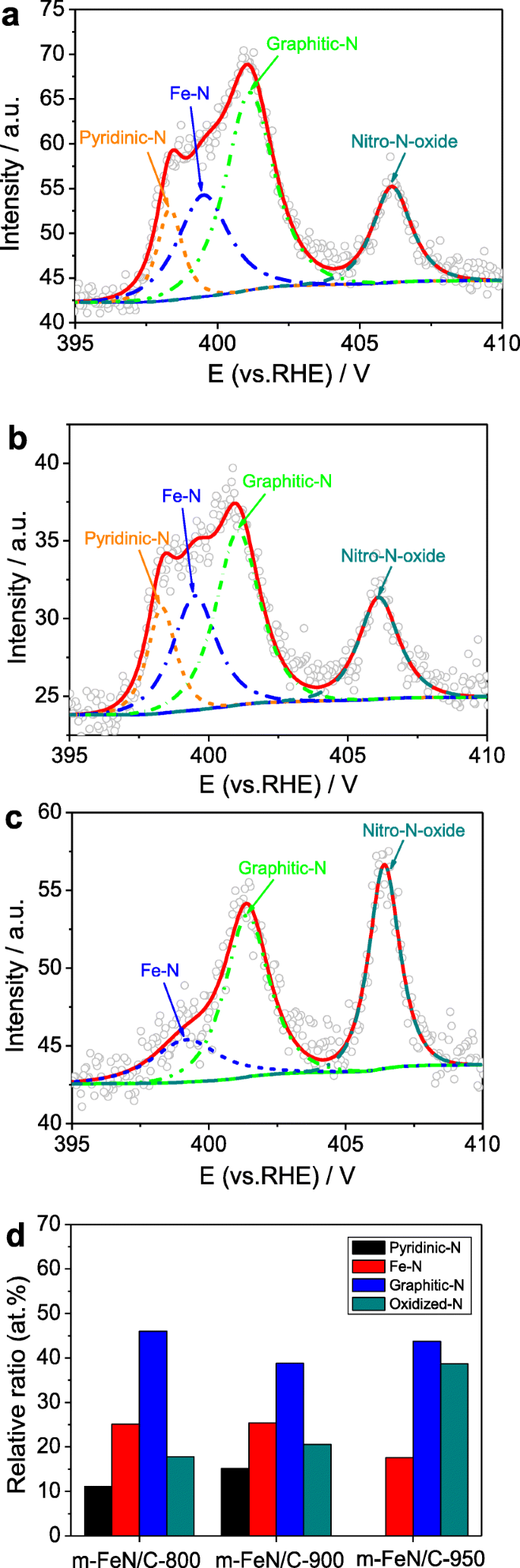
N 1s Spectres XPS de m -Fe/N/C-800 (a ), m -Fe/N/C-900 (b ), m -Fe/N/C-950 (c ), et leur contenu relatif dans le total N contenu (d )
L'analyse morphologique de m Le catalyseur -Fe/N/C-900 a été représenté sur la figure 6 et le fichier supplémentaire 1 :figure S3. Un grand nombre de formes spongieuses peuvent exister pour m -Fe/N/C-900 (Fig. 6a, b) synthétisé par pyrolyse à haute température de complexes métal-organiques (Fe-TPTZ) fixés de manière confinée dans des nanocanaux de tamis moléculaires. Les images MET haute résolution (Fig. 6c, d) montrent de manière significative qu'il existe de nombreuses structures mésoporeuses hautement ordonnées à l'intérieur de m -Fe/N/C-900, qui peut en grande partie dériver de l'élimination du tamis moléculaire en tant que réacteur confiné à nanocanaux. En outre, les structures carbonées désordonnées sur le bord et plusieurs mésopores sont clairement visibles sur la figure 6e, ce qui est dû au dopage des atomes d'azote. Pour cette raison, caractéristique poreuse et surface Brunauer-Emmett-Teller (BET) de m -Fe/N/C-900 ont également été étudiés par des isothermes d'adsorption/désorption d'azote (encart de la Fig. 6f). Une courbe isotherme de type Langmuir IV peut être observée, suggérant la caractéristique hautement mésoporeuse du m -Électrocatalyseur Fe/N/C-900. Cela peut être confirmé par la distribution de la taille des pores BJH de m -Fe/N/C-900 (Fig. 6f), qui a affiché une surface BET élevée (A PARIER ~ 1035 m 2 g -1 ) et le volume poreux total (V total ~ 1,22 cm 3 g -1 ) avec un diamètre moyen des pores (D p ) d'environ 4,7 nm. Les deux tailles de pores maximales exposées (4,3 et 9,3 nm) sont attribuées à la position maximale des mésopores en m -Fe/N/C-900. Ces mésopores peuvent fournir des nanocanaux plus pratiques pour un transport rapide de l'électrolyte, des réactifs et des produits ; diminuer la résistance au transport de la molécule d'oxygène vers les sites actifs dopés à l'azote; et augmenter les performances catalytiques ORR de m -Fe/N/C-900. De plus, l'utilisation de nanocanaux de tamis moléculaire en tant que réacteur nanoconfiné est bénéfique pour produire des carbones mésoporeux tridimensionnels de type spongieux avec une surface ultra-élevée, facilitant l'amélioration de l'exposition des sites catalytiquement ORR-actifs. Les images de cartographie élémentaire (Fig. 7) affichent la distribution homogène de quatre types d'éléments principaux (Fe, N, C et O) sur la surface de m -Fe/N/C-900, qui peut résulter des rôles synergiques de l'effet confiné dans les nanocanaux des tamis moléculaires et de l'effet stable de coordination moléculaire des complexes Fe-TPTZ dans une certaine mesure.
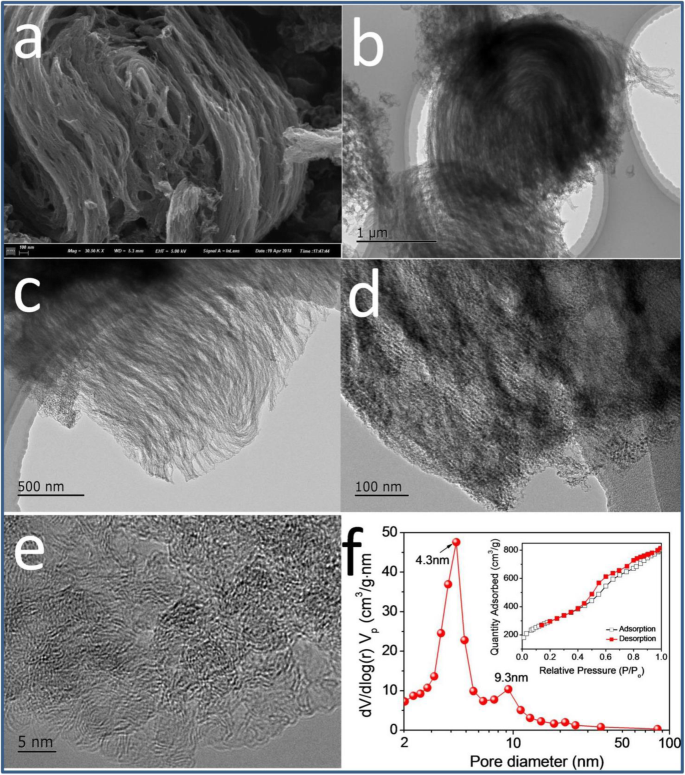
SEM (a ) et des images MET haute résolution (b –e ) de m -Fe/N/C-900 ; f la distribution de la taille des pores de m -Fe/N/C-900 ; l'encart est des isothermes d'adsorption-désorption d'azote

Image TEM (a ) de m -Fe/N/C-900 et les images de cartographie élémentaire correspondantes de C, O, Fe et N (b –f )
Les activités électrocatalytiques vis-à-vis de l'ORR de tous les catalyseurs préparés ont été testées par le voltamogramme cyclique (CV) ou le voltamogramme à balayage linéaire (LSV). La figure 8a montre les CV de m -Fe/N/C-900 en N2 contre O2 -saturé 0,1 mol l -1 électrolyte KOH. Un pic ORR pointu s'est produit à 0,86 V contre RHE dans O2 -électrolyte saturé; cependant, une courbe CV sans particularité a été observée dans N2 -électrolyte saturé, suggérant l'activité catalytique ORR de m -Fe/N/C-900 avec un potentiel d'apparition (E début ) de 1,0 V. En outre, l'effet de la température de traitement thermique (800–950 °C) sur les performances de l'ORR a été étudié sur la figure 8b. Une température de traitement thermique supérieure ou inférieure fait contre l'amélioration de l'activité basée sur la plus grande densité de courant de crête (j p ), et le potentiel de crête le plus positif (E p ) peut être obtenu à m -Fe/N/C-900. L'activité ORR de m -Fe/N/C-900 peut être comparable à d'autres catalyseurs au carbone dopé rapportés (voir le fichier supplémentaire 1 :tableau S2). Pour avoir un aperçu du comportement cinétique de l'ORR des électrocatalyseurs de type Fe/N/C, nous avons en outre testé les courbes de polarisation ORR par la méthode LSV combinée avec le RRDE, comme indiqué sur la figure 8c. Sur la base des données RRDE, le nombre d'électrons transféré (n ) et H2 O2 rendement (H2 O2 %) au cours de l'ORR ont été estimés à l'aide des équations suivantes. (1) et (2), respectivement. Les équations calculées sont les suivantes [34] :
$$ \%H{O}_2^{-}=100\times \frac{2{I}_r/N}{I_d+\left({I}_r/N\right)} $$ (1) $$ n=4\times \frac{I_d}{I_d+{I}_r/N} $$ (2)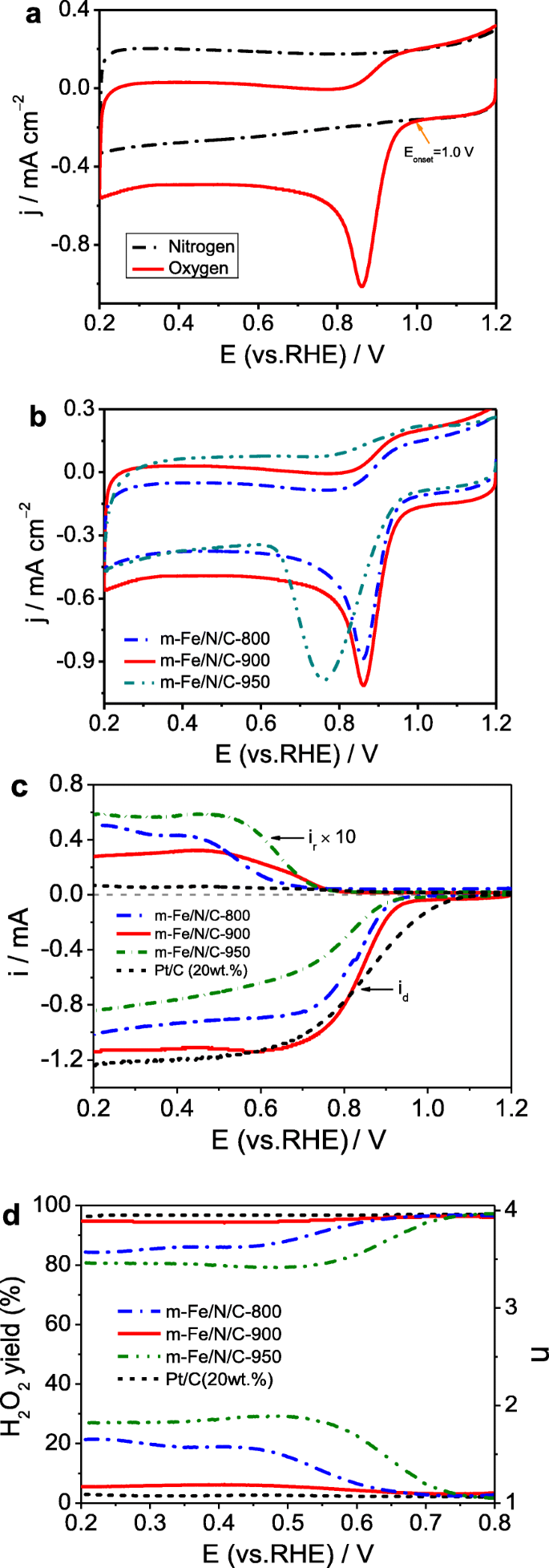
un Courbes CV de m -Fe/N/C-900 en N2 contre O2 -solution saturée de KOH 0,1 M. b Courbes CV de m -Fe/N/C-800, m -Fe/N/C-900 et m -Fe/N/C-950 en O2 -saturé 0,1 mol l -1 solution de KOH. c Courants de disque et d'anneau obtenus avec des LSV sur RRDE pour m -Fe/N/C-800, m -Fe/N/C-900 et m -Fe/N/C-950 en O2 -saturé 0,1 mol l -1 solution de KOH. d Les numéros de transfert d'électrons correspondants et H2 O2 rendements de m -Fe/N/C-800, m -Fe/N/C-900, et m -Fe/N/C-950 dérivé de c
où je d is the Faradaic disk-current, I r is the Faradaic ring-current, and N est l'efficacité de collecte de l'électrode annulaire (0,38). The Pt-ring potential was set at 1.5 V (vs. RHE) as reported elsewhere. Figure 8d displays the relatively calculated results. Le H2 O2 yield (<6.5%) and n value (3.88–3.94) are obtained on m -Fe/N/C-900, dominating a four-electron ORR pathway. It suggests that this catalyst is a valuable substitute for the traditional 20 wt.% Pt/C catalyst (purchased from Aladdin Industrial Co. Ltd.), although the H2 O2 yield on m -Fe/N/C-900 is slightly higher. In addition, the half-wave potential (E 1/2 ) for ORR of m -Fe/N/C-900 is about 0.841 V approaching that of 20 wt.% Pt/C (~ 0.848 V), and the limited current density (j d ) of m -Fe/N/C-900 is almost identical to that of 20 wt.% Pt/C. Compared to the m -Fe/N/C-900 catalyst, higher H2 O2 yield and smaller n value can be gained on both m -Fe/N/C-800 and m -Fe/N/C-950, but the electron transfer number on both m -Fe/N/C-800 and m -Fe/N/C-950 still belongs to the range (3.4–4.0), showing that the ORR on two Fe/N/C-type happens with a mixed process of two and four-electron transfer pathways. The above results further approve that the m -Fe/N/C-900 synthesized by nanochannel-confined control of the pyrolysis process to improve the nitrogen-doping efficiency and increase the nitrogen-doped active-site density has exhibited the optimal ORR catalytic performance in alkaline electrolyte.
We also discuss the effect of different transition metals on the ORR catalytic activity of Fe/N/C-type electrocatalysts. The obtained LSV curves on the RRDE are indicated in Fig. 9a, and the corresponding n value and H2 O2 yield are demonstrated in Fig. 9b. Le E 1/2 values are about 0.785 V for m -Cu/N/C-900 and 0.780 V for m -Ni/N/C-900, respectively, which are lower compared to the m -Fe/N/C-900. The j d follows the order of m -Fe/N/C-900> m -Cu/N/C-900> m -Ni/N/C-900, further suggesting the best ORR catalytic activity of m -Fe/N/C-900 in 0.1 mol l -1 solution de KOH. Compared to the m -Fe/N/C-900 catalyst, higher H2 O2 yield and smaller n value are obtained on both m -Cu/N/C-900 and m -Ni/N/C-900. What is noteworthy is that the H2 O2 yield on m -Cu/N/C-900 and m -Ni/N/C-900 is over twice as large as that on m -Fe/N/C-900. However, the n value on both m -Cu/N/C-900 and m -Ni/N/C-900 is 3.5–4.0, indicating that the ORR process on two Fe/N/C-type electrocatalysts follows a two- and four-electron mixed transfer pathway but is dominant in a four-electron reaction pathway. Besides, the electrochemical long-term stability for ORR catalysis of m -Fe/N/C-900 is of great significance in the practical applications. An accelerated aging test (AAT) was carried out by successive CV scanning tests from 0.2 to 1.2 V vs RHE for 5000 cycles at 200 mV s -1 in oxygen-saturated 0.1 M KOH electrolyte. The ORR electrocatalytic behavior of m -Fe/N/C-900 has been further evaluated under the same conditions as above experiments. CV curves for ORR activity of m -Fe/N/C-900 before and after doing the AAT are almost unchanged on the E p (~ 0.86 V), but the j p is slightly reduced (Fig. 9c). LSV curves of m -Fe/N/C-900 (Fig. 9d) also reveal an only ~ 12 mV negative shift in the E 1/2 and a negligible decrease in the j d . However, the commercial Pt/C (20 wt.% Pt) catalyst after doing the AAT has exhibited about 55 mV of the negative shift in E 1/2 and an obvious reduction in the j d (Fig. 9d). Results show that the m -Fe/N/C-900 has more excellent electrocatalytic stability compared to the Pt/C catalyst, further suggesting that it is a valuable and promising substitute for the conventional Pt-based materials in alkaline electrolytes.
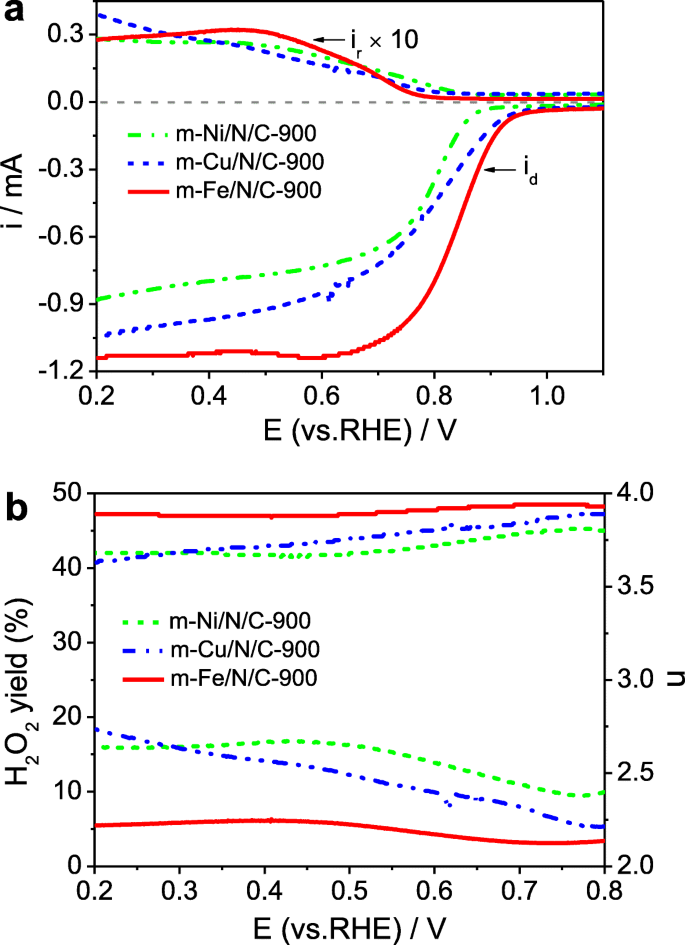
un Disk and ring currents obtained with LSVs on RRDE for m -Ni/N/C-900, m -Cu/N/C-900, and m -Fe/N/C-900 in O2 -saturated 0.1 mol l -1 solution de KOH. b Le nombre de transfert d'électrons correspondant et H2 O2 yield of m -Ni/N/C-900, m -Cu/N/C-900, and m -Fe/N/C-900 derived from a . c CV curves and d LSV curves of m -Fe/N/C-900 before and after continuous scanning for 5000 cycles in O2 -saturated 0.1 M KOH solution
In order to discuss the catalytically active sites of Fe/N/C-type catalysts and study the role of the molecular coordination and nanochannel-confined effects, we have further examined the N/C-900, Fe/N/C-900, and 20 wt.% Pt/C catalysts for comparison of the ORR catalytic behavior. The tested results of the ORR activity are indicated in Fig. 10a. The onset potentials of ORR are about 0.683 V for N/C-900 and 0.740 V for Fe/N/C-900, being largely lower than those of m -Fe/N/C-900 (0.841 V) and 20 wt.% Pt/C catalysts (0.848 V). Figure 10b shows the corresponding H2 O2 yields and transferred electron numbers in the ORR process. Given other Fe/N/C-type catalysts and the Pt/C catalyst, the H2 O2 yield on N/C-900 is the highest and the transferred electron number on N/C-900 is the smallest, suggesting the worst ORR catalytic activity of N/C-900. In addition, the H2 O2 yield on Fe/N/C-900 is mainly higher than that on m -Fe/N/C-900 and the transferred electron number on Fe/N/C-900 is far lower than that on m -Fe/N/C-900 in the same range (0.2–0.8 V vs RHE), indicating a relatively inferior ORR activity. Thus, it can be concluded that the ORR performance complies with the sequence of Pt/C> m -Fe/N/C-900> Fe/N/C-900> N/C-900. These results show that the formation of Fe-TPTZ compounds with the strong molecular-level coordination effect is beneficial to produce the Fe/N/C-type catalysts with high ORR activity, and the utilization of the nanochannel-confined effect can reduce the decomposition speed of Fe-TPTZ compounds and protect the nitrogen-rich active sites (e.g., Fe–N, graphitic-N, or pyridinic-N) from the thermal loss during the pyrolysis process (see the TG analysis, Fig. 2a), which can enhance the ORR performance of Fe/N/C-type catalysts in alkaline medium.
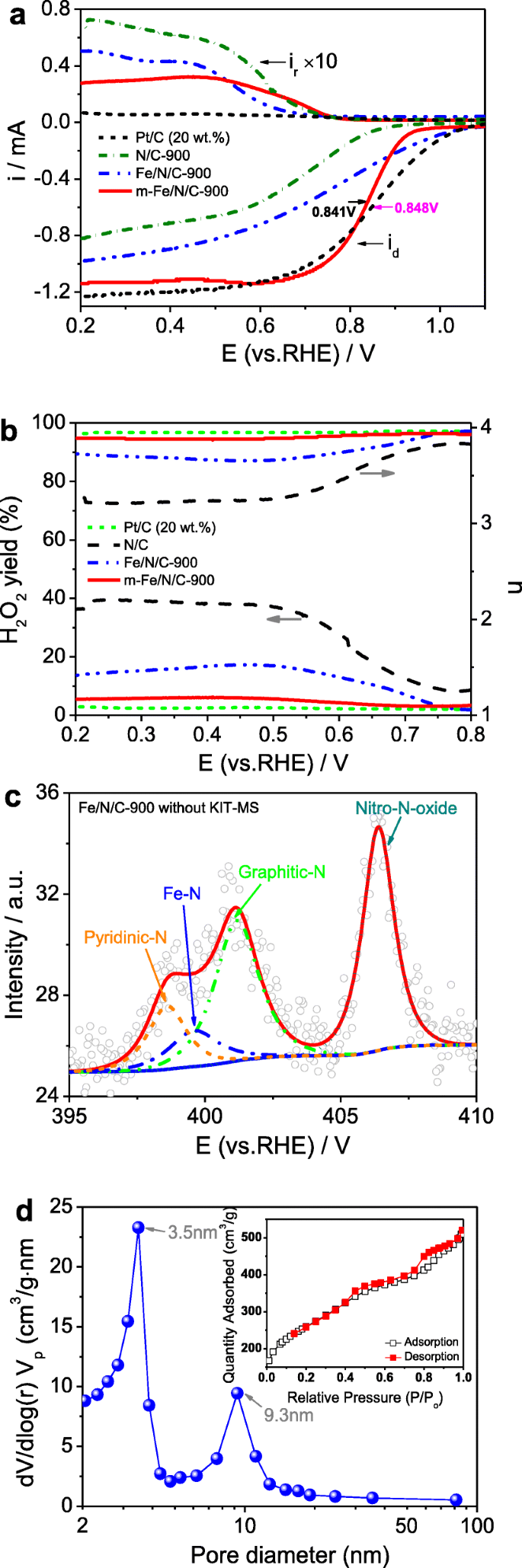
un Disk and ring currents obtained with LSVs on RRDE for N/C-900, Fe/N/C-900, m -Fe/N/C-900, and Pt/C (20 wt.%) in O2 -saturated 0.1 mol l -1 solution de KOH. b Le nombre de transfert d'électrons correspondant et H2 O2 yield of N/C-900, Fe/N/C-900 m -Fe/N/C-900, and Pt/C (20 wt.%) derived from a
To deepen the understanding of active sites and their ORR catalysis mechanism, we also characterized the prepared Fe/N/C-type catalysts by the spectra of X-ray diffraction (XRD) and X-ray photoelectric spectroscopy (see Additional file 1:Figures S4 and S5). The XRD data display that the density of carbon (002) peak follows the sequence of N/C-900> Fe/N/C-900> m -Fe/N/C-900, and the positions for carbon (002) peak in three catalysts are negatively shifted because of the production of more sp 2 C–N groups into the graphitic layers and the decrease of graphitization. It also implies that the different N content may be doped into the carbon skeleton in the catalyst, and both N-doping efficiency and N content can follow the similar order with their ORR activity. More significantly, we further compare the structural and porous differences between Fe/N/C-900 and m -Fe/N/C-900 to better study the nanochannel-confined effect of molecular sieves. The tested XPS survey spectrum of Fe/N/C-900 was indicated in Additional file 1:Figure S5, and its surface contents of Fe, C, and N and the N/C ratio were summarized in Table 1. The Fe content and N content are ~ 0.41 at.% and ~ 4.48 at.%, but the N/C ratio is only 5.1 in the Fe/N/C-900, being lower compared to the m -Fe/N/C-900. It suggests the N-doping efficiency was improved by introducing the nanochannel-confined protection strategy into the carbonization process, which can prove our key views of this work. Besides, the fitted N1s XPS spectrum of Fe/N/C-900 is indicated in Fig. 10c. It displays the existence of four peaks with B.E. of 398.6, 399.6, 401.2, and 406.4 eV, which still correspond to the pyridinic-N, Fe–N, graphitic-N, and oxidized-N (–NO2 ) with a relative percentage of 14.0, 10.2, 35.4, and 40.4 at.%, respectively. Compared with the m -Fe/N/C-900, the total ratio of active N-rich groups such as pyridinic-N, Fe–N, and graphitic-N obviously decreases about 19.8 at.%; however, the relative ratio of Fe–N groups is reduced about 15.2 at.%. Thus, associating with fore-mentioned XPS data and the catalytic activity data, we conclude that the electrocatalytically active sites may be pyridinic- and graphitic-N groups for holding the ORR performance, but the enhancement of the ORR activity may be related to the relative ratio of Fe–N groups for our system. The role of the nanochannel-confined effect cannot only reduce the loss of total N content, but also can largely increase the N-doping efficiency and improve the effective ORR active-site density in the catalyst. Besides, we further analyzed porous characteristic and BET specific surface area of Fe/N/C-900 without the usage of the KIT-MS nanoreactor. The nitrogen adsorption/desorption isotherms with a similar Langmuir IV-type isotherm curve are seen in the inset of Fig. 10d. It suggests that highly mesoporous characteristic is still existed in Fe/N/C-900, supported by the analysis of BJH pore-size distribution (Fig. 10d). Le A PARIER (~ 875 m 2 g -1 ) et V total (~ 0.76 cm 3 g -1 ) with an average D P of only ~ 3.5 nm are obtained on the Fe/N/C-900, which are obviously lower than those on the m -Fe/N/C-900. The large difference on pore structures between Fe/N/C-900 and m -Fe/N/C-900 can be derived from the stable coordination effect and the nanochannel-confined role of a KIT-MS reactor in the preparation of m -Fe/N/C-900. It will also influence their inherent ORR performance because higher A PARIER et V total can help to supply abundant catalytic sites and increase the exposed surface active-site density, being beneficial to the adsorption and electro-reduction process of O2 molecule [35]. Notably, we should pay much attention to the effect of the conductivity characteristic. Generally, a higher conductivity characteristic of m -Fe/N/C-900 corresponds to a relatively faster ORR electron transportation process. Therefore, facile design and control of active nitrogen-rich groups (pyridinic-N, graphitic-N, and Fe–N, etc.) is of great importance to fabricate mesopore-structured Fe/N/C electrocatalysts for the ORR, but further improving the conductance, N-doped active-site density, and mesoporous characteristic is another key issue of concern to obtain the high performance.
Conclusions
In conclusion, here, we propose a new and effective strategy to design a Fe/N/C-type electrocatalyst (m -Fe/N/C-900) with ultrahigh BET surface area (1035 m 2 g -1 ) and total pore volume (1.22 cm 3 g -1 ) via nanochannel-confined high-temperature carbonization of Fe 2+ ions coordinated with 2,4,6-tri(2-pyridyl)-1,3,5-triazine compound as a single-source Fe, N, and C precursor. The elemental mapping images of m -Fe/N/C-900 further prove the homogeneous distribution of Fe, N, C, and O elements on its surface. On the one hand, the strong molecular-coordination role in Fe-TPTZ complex can enhance the thermal stability and stabilize higher contents of Fe–N active sites during pyrolysis process. On the other hand, the utilization of abundant nanochannels of molecular sieve as a novel nanoconfined reactor does not only benefit to produce spongy-like mesoporous carbons with excellent pore structure and conductivity characteristic, but also facilitate to decrease the loss of N atoms and improve the N-doping efficiency and N-doped active-site density, resulting in the ORR activity enhancement. Electrochemical tests indicate the m -Fe/N/C-900 displays unexpected catalytic performance with an ORR half-wave potential of ~ 0.841 V versus RHE and high limited current density approaching the commercial Pt/C catalyst. Additionally, low H2 O2 yield (<6.5%) and high electron transfer number (3.88–3.94) on m -Fe/N/C-900, indicating that it is a valuable substitute for the traditional Pt/C catalyst. The comparison analysis of XPS data and electrocatalytic activity data can point out that active pyridinic and graphitic-N groups may be the electrocatalytically ORR-active sites, but the enhancement of the ORR activity may be related to the relative ratio of Fe–N groups for our system. This study provides a new idea or method for the synthesis of high-performance Fe/N/C electrocatalysts via integrating molecular-level coordination and nanochannel-confined effects and does also help the researchers better deepen the understanding of nitrogen-doped active sites and their ORR catalysis mechanism for Fe/N/C-type electrocatalysts to a certain extent. However, what cannot be ignored is that effective improvement and optimization of nitrogen-doping active site density, conductivity, and porous characteristics is essential to boost the ORR electrocatalytic activity.
Disponibilité des données et des matériaux
The authors declare that the materials and datasets used or analyzed during the current study are available from the corresponding author on reasonable request.
Abréviations
- AAT:
-
Accelerated aging test
- AE:
-
Auxiliary electrode
- PARI :
-
Brunauer-Emmett-Teller
- CV :
-
Voltamétrie cyclique
- E 1/2 :
-
Half-wave potential
- E p :
-
Peak potential
- Fe/N/C catalyst:
-
Iron/nitrogen/carbon catalyst
- Fe-TPTZ:
-
Fe coordinated with 2,4,6-tri(2-pyridyl)-1,3,5-triazine complexes
- GC :
-
Carbone vitreux
- HR-TEM :
-
Microscopie électronique à transmission haute résolution
- KIT-MS:
-
KIT-6 molecular sieves
- LSV :
-
Voltamétrie à balayage linéaire
- ORR:
-
Oxygen reduction reaction
- Pt/C:
-
Platinum/carbon catalyst
- RDE :
-
Rotation disk electrode
- RE:
-
Reference electrode
- RHE :
-
Électrode à hydrogène réversible
- RRDE:
-
Rotation ring-disk electrode
- SCE :
-
Électrode au calomel saturé
- SEM :
-
Microscopie électronique à balayage
- TGA :
-
Analyse thermogravimétrique
- TPTZ:
-
2,4,6-Tri(2-pyridyl)-1,3,5-triazine
- WE:
-
Working electrode
- XPS :
-
Spectroscopie photoélectronique aux rayons X
- XRD :
-
Diffraction des rayons X
Nanomatériaux
- Avancées et défis des nanomatériaux fluorescents pour la synthèse et les applications biomédicales
- Synthèse verte à un pot de microsphères de SnO2 décorées d'Ag :un catalyseur efficace et réutilisable pour la réduction du 4-nitrophénol
- Méthode de post-traitement pour la synthèse de nanoparticules binaires monodisperses FePt-Fe3O4
- Carbone à haute porosité autodopé fortement graphitique-azote pour l'électrocatalyse de la réaction de réduction de l'oxygène
- Activité de synthèse et d'oxydation du CO des catalyseurs d'or pris en charge par l'oxyde binaire mixte 1D CeO2-LaO x
- Nanopétales d'oxyde de nickel mésoporeux (NiO) pour la détection ultrasensible du glucose
- Saponines de Platycodon de Platycodi Radix (Platycodon grandiflorum) pour la synthèse verte de nanoparticules d'or et d'argent
- Synthèse facile de nanocomposites magnétiques fonctionnalisés en surface pour une adsorption sélective efficace des colorants cationiques
- Réaction de réduction de l'oxygène sur le nanocatalyseur PtCo :empoisonnement aux anions (bi)sulfate



