Fabrication d'hétérostructures en Z Ag3PO4/TiO2 pour améliorer l'activité photocatalytique visible
Résumé
Dans cet article, une étude synthétique du composite Ag3 Bon de commande4 /TiO2 photocatalyseur, synthétisé par une méthode simple en deux étapes, est réalisé. Des outils de caractérisation supplémentaires tels que la diffraction des rayons X, la microscopie électronique à balayage, la microscopie électronique à transmission, la microscopie électronique à transmission haute résolution, la spectroscopie à rayons X à dispersion d'énergie, la spectroscopie photoélectronique à rayons X et la spectroscopie à réflectance diffuse UV-vis ont été adoptés dans cette recherche . Les résultats ont montré qu'une morphologie hautement cristalline et bonne peut être observée. Dans l'expérience des performances photocatalytiques, TiO2 400/Ag3 Bon de commande4 montre la meilleure activité photocatalytique, et le taux de dégradation photocatalytique atteint presque 100 % après illumination pendant 25 min. La constante de vitesse de réaction de TiO2 400/Ag3 Bon de commande4 est le plus grand, qui est de 0,02286 min −1 , le double de Ag3 Bon de commande4 et 6,6 fois celle de la valeur minimale de TiO2 400. L'effet de dégradation du TiO2 400/Ag3 Bon de commande4 montre une bonne stabilité après recyclage du photocatalyseur quatre fois. Des expériences de piégeage des espèces catalytiques actives révèlent que les principaux facteurs sont les trous (h + ) et les anions superoxydes (O·− 2), tandis que le radical hydroxyle (·OH) joue partiellement la dégradation. Sur cette base, un Z -schéma du mécanisme de réaction de Ag3 Bon de commande4 /TiO2 une structure hétérogène est mise en avant et son mécanisme de dégradation est exposé.
Contexte
Les photocatalyseurs semi-conducteurs ont suscité un intérêt croissant en raison de leur utilisation intensive dans la dégradation des polluants organiques et les cellules solaires [1,2,3,4,5,6]. En tant que représentant des photocatalyseurs à base de semi-conducteurs, TiO2 a été largement étudiée en raison de ses excellentes propriétés physico-chimiques [7, 8]. Cependant, le TiO2 pur photocatalyseur présente certains inconvénients dans des applications pratiques telles que sa large bande interdite (3,2 eV pour l'anatase et 3,0 eV pour le rutile), ce qui conduit à une mauvaise réponse visible.
Un composé à base d'argent tel que Ag2 O, AgX (X =Cl, Br, I), Ag3 Bon de commande4 , Ag2 CrO4 , ont été récemment utilisés pour des applications photocatalytiques [9,10,11,12]. Entre autres, l'orthophosphate d'argent (Ag3 Bon de commande4 ) a déjà attiré l'attention de nombreux chercheurs car Ag3 Bon de commande4 a une bande interdite de 2,45 eV et une forte absorption à moins de 520 nm. Le rendement quantique de Ag3 Bon de commande4 est supérieur à 90 %. C'est un bon photocatalyseur à lumière visible. Cependant, en raison de la formation d'Ag 0 à la surface du catalyseur (4Ag3 Bon de commande4 + 6H2 O + 12h + + 12e − → 12Ag 0 + 4H3 Bon de commande4 + 3O2 ) lors de la réaction photocatalytique, la réutilisation d'Ag3 Bon de commande4 est un problème majeur. Par conséquent, il est courant de réduire la corrosion photocatalytique de Ag3 Bon de commande4 et assurer une bonne activité catalytique de Ag3 Bon de commande4 . Sur la base des précédents de la littérature, il est connu que le compoundage peut améliorer efficacement les performances photocatalytiques des deux matériaux semi-conducteurs. Après la composition, l'effet de séparation des électrons et des trous photogénérés est renforcé, contribuant à améliorer l'activité photocatalytique des matériaux composites. De nombreux chercheurs ont étudié les hétérojonctions telles que Bi2 O3 -Bi2 WO6 , TiO2 /Bi2 WO6 , ZnO/CdSe et Ag3 Bon de commande4 /TiO2 [2, 13,14,15]. Par rapport aux photocatalyseurs monophasés, les photocatalyseurs à hétérojonction peuvent étendre la plage de réponse lumineuse en couplant des matériaux de structure électronique adaptés. Et en raison de l'effet synergique entre les composants, la charge peut être transférée de plusieurs manières pour améliorer encore l'activité photocatalytique à hétérojonction.
Sur la base de l'analyse ci-dessus, Ag3 Bon de commande4 -Les composites semi-conducteurs à effet d'amélioration synergique ont été conçus pour améliorer les défauts de recombinaison des porteurs et Ag3 Bon de commande4 -composés semi-conducteurs à base de performances catalytiques. Dans cet article, TiO2 de taille nanométrique a été préparé par méthode solvothermique, puis les nanoparticules de TiO2 400 ont été déposés à la surface d'Ag3 Bon de commande4 à température ambiante pour obtenir TiO2 /Ag3 Bon de commande4 matériaux composites. L'activité photocatalytique du TiO2 /Ag3 Bon de commande4 le composite a été testé avec un colorant RhB (rhodamine B).
Méthodes
Préparation hydrothermale de TiO de taille nanométrique2
0,4 g de P123 ont été ajoutés à une solution mixte contenant 7,6 mL d'éthanol absolu et 0,5 mL d'eau déminéralisée et agités jusqu'à ce que P123 soit complètement dissous. La solution clarifiée a été étiquetée comme solution A. Ensuite, une solution mixte contenant 2,5 mL de titanate de butyle (TBOT) et 1,4 mL d'acide chlorhydrique concentré (12 mol/L) a été préparée et étiquetée comme solution B. La solution B a été ajoutée goutte à goutte à la solution A. Après agitation pendant 30 min, 32 mL d'éthylène glycol (EG) ont été ajoutés à la solution et agités pendant 30 min. Ensuite, la solution a été placée dans un four à 140°C, haute température et haute pression pendant 24h. Refroidissement naturel, lavage centrifuge, séparation, récupération des sédiments et séchage à l'étuve à 80°C pendant 8 h. La précipitation blanche a été calcinée dans un four à moufle à différentes températures (300 °C, 400 °C, 500 °C) et marquée comme réserve de TiO2 300, TiO2 400, et TiO2 500, respectivement.
Préparation du TiO2 /Ag3 Bon de commande4 Photocatalyseur
Le 0,1 g TiO2 de la poudre a été ajoutée à la solution de nitrate d'argent de 30 mL contenant 0,612 g d'AgNO3 puis traité par ultrasons pendant 30 min pour faire du TiO2 dispersés uniformément. Nous avons ajouté une solution de 30 ml contenant 0,43 g de Na2 HPO4 .12H2 O et agité 120 min à température ambiante. Par centrifugation, nettoyage avec de l'eau déminéralisée et de l'éthanol anhydre, les précipités ont été séparés, collectés et séchés à 60°C. Les produits ont été nommés TiO2 300/Ag3 Bon de commande4 , TiO2 400/Ag3 PO4, et TiO2 500/Ag3 Bon de commande4 , respectivement. Ag3 Bon de commande4 a été préparé sans ajout de TiO2 dans les mêmes conditions que le procédé ci-dessus.
Caractérisation
Les diagrammes de diffraction des rayons X (XRD) des échantillons obtenus ont été réalisés sur un diffractomètre à rayons X D/MaxRB (Japon), qui a un Cu-Ka de 35 kV avec une vitesse de balayage de 0,02° s −1 , allant de 10 à 80°. Un assemblage de microscopie électronique à balayage (SEM), JEOL, JSM-6510 et JSM-2100 pour la microscopie électronique à transmission (TEM) avec spectroscopie à rayons X à dispersion d'énergie (EDX) a été utilisé pour étudier sa morphologie à une tension d'accélération de 10 kV. Les informations de spectroscopie photoélectronique aux rayons X (XPS) ont été recueillies à l'aide d'un spectromètre d'électrons ESCALAB 250 sous un rayonnement Cu Kα de 300 W. La pression de base était d'environ 3 × 10 −9 mbar, Combine pour se référer à la ligne C1s au carbone amorphe 284,6 eV.
Mesure de l'activité photocatalytique
Les performances photocatalytiques du TiO2 /Ag3 Bon de commande4 catalyseurs a été testé en utilisant la photodégradation de RhB en solution aqueuse comme objet de recherche. Cinquante milligrammes du photocatalyseur ont été mélangés avec 50 mL de solution aqueuse de RhB (10 mg L −1 ) et agité dans l'obscurité pendant un certain temps avant illumination pour assurer l'équilibre d'adsorption. Dans le processus de réaction, de l'eau de refroidissement est utilisée pour maintenir la température du système constante à la température ambiante. Une lampe au xénon de 1000 W fournit un éclairage pour simuler la lumière visible. Le spectrophotomètre UV/Vis LAMBDA35 a été utilisé pour caractériser la concentration (C ) changement de solution RhB à λ = 553 nm. Le taux de décoloration est indiqué en fonction du temps vs C t /C 0 . Où C 0 est la concentration avant illumination, et C t est la concentration après illumination. Les catalyseurs usagés ont été récupérés pour détecter la stabilité de cycle des catalyseurs. L'expérience a été répétée quatre fois.
Résultats et discussion
L'analyse XRD est utilisée pour déterminer la structure de phase et le type cristallin du catalyseur. Les spectres XRD des catalyseurs préparés ont été montrés sur la figure 1, y compris TiO2 400, Ag3 Bon de commande4 , TiO2 /Ag3 Bon de commande4 , TiO2 300/Ag3 Bon de commande4 , TiO2 400/Ag3 Bon de commande4 , et TiO2 500/Ag3 Bon de commande4 . Il peut être obtenu à partir de la figure que la structure cristalline de TiO2 400 est l'anatase (JCPDS n° 71-1166). Dans les spectres XRD de Ag3 Bon de commande4 , les pics de diffraction situés à 20,9°, 29,7°, 33,3°, 36,6°, 47,9°, 52,7°, 55,1°, 57,4°, 61,7° et 72,0° appartiennent aux pics caractéristiques de (110), (200), (210), (211), (310), (222), (320), (321), (400) et (421) plans de Ag3 Bon de commande4 (JCPDS n° 70-0702), respectivement. Les photocatalyseurs composites synthétisés ont montré des pics caractéristiques compatibles avec TiO2 et Ag3 Bon de commande4 , et les pics caractéristiques de TiO2 étaient de 25,3° au composite TiO2 , TiO2 300/Ag3 Bon de commande4 , TiO2 400/Ag3 Bon de commande4 , TiO2 500/Ag3 Bon de commande4 , ce qui était cohérent avec la température de calcination de TiO2 augmenter, la cristallinité de TiO2 devient plus élevé.
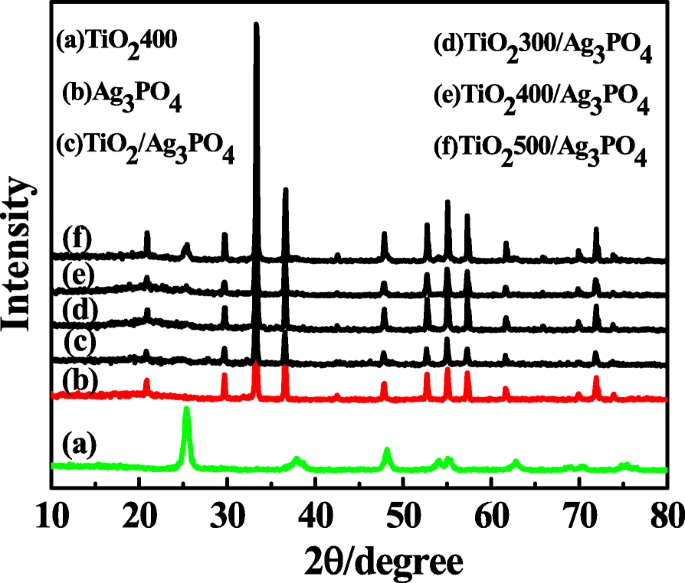
Les modèles XRD des échantillons tels que préparés
La figure 2 montre les diagrammes SEM, TEM et EDX des catalyseurs de TiO2 400, Ag3 Bon de commande4 , et TiO2 400/Ag3 Bon de commande4 . La figure 2a est la nanostructure sphérique TiO2 400 préparé par méthode solvothermique avec un diamètre allant de 100 à 300 nm. La figure 2b est l'Ag3 Bon de commande4 cristal à structure hexaédrique régulière. Sa granulométrie varie de 0,1 à 1,5 µm et présente une surface assez lisse. La figure 2c est l'image SEM du composite TiO2 400/Ag3 Bon de commande4 . On constate que les nanoparticules de TiO2 400 sont déposés à la surface d'Ag3 Bon de commande4 . La morphologie du TiO2 400/Ag3 Bon de commande4 a été exploré plus avant avec le TEM et le diagramme TEM de TiO2 400/Ag3 Bon de commande4 est affiché sur la figure 2d. On peut observer que du TiO2 de taille nanométrique à 200 nm les particules adhèrent à la surface d'Ag3 Bon de commande4 . La figure 2e est le HRTEM de TiO2 400/Ag3 Bon de commande4 . On peut fonder que TiO2 les particules sont étroitement liées à Ag3 Bon de commande4 , et l'espacement du réseau de TiO2 400 et Ag3 Bon de commande4 sont respectivement de 0,3516 et 0,245 nm, correspondant aux surfaces (101) et (211) de TiO2 et Ag3 Bon de commande4 . La figure 2f est le diagramme EDX de TiO2 400/Ag3 Bon de commande4 . On peut voir que l'échantillon se compose de quatre éléments :Ti, O, Ag et P. Le pic de diffraction évident de l'élément cuivre est produit par la source d'excitation EDX, Cu Ka. L'EDX a confirmé les éléments chimiques correspondants de TiO2 400/Ag3 Bon de commande4 . En conclusion, on peut clairement juger que TiO2 est chargé à la surface d'Ag3 Bon de commande4 cristaux sous forme granulaire et a une bonne morphologie d'hexaèdre.
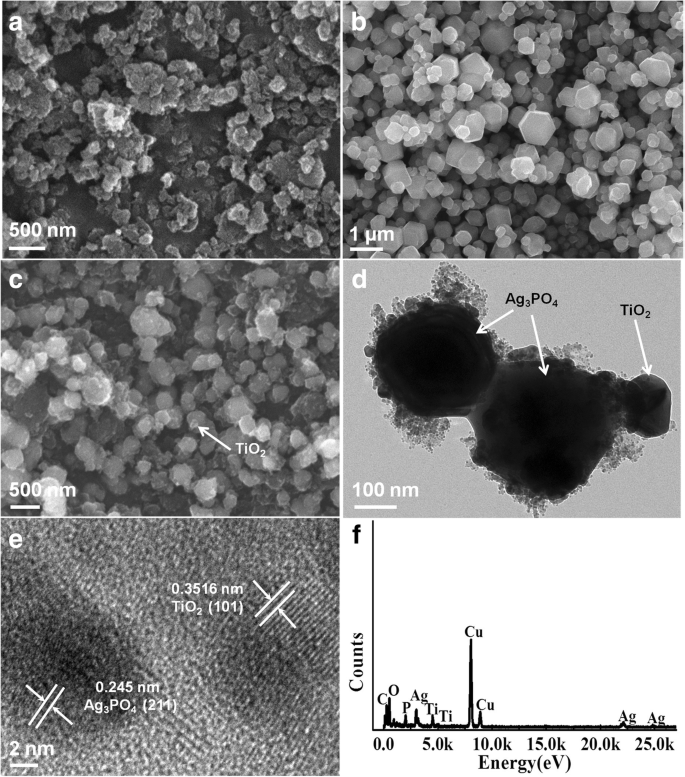
Images SEM de photocatalyseurs préparés :a TiO2 400, b Ag3 Bon de commande4 , c TiO2 400/Ag3 Bon de commande4 , d Image TEM de TiO2 400/Ag3 Bon de commande4 , e Image HRTEM de TiO2 400/Ag3 Bon de commande4 , et f motif EDX correspondant de TiO2 400/Ag3 Bon de commande4
La spectroscopie photoélectronique à rayons X (XPS) du produit est étudiée sur la figure 3. La figure 3a est le spectre XPS d'étude du produit. Ti, O, Ag, P et C cinq éléments peuvent être observés dans le graphe, dont C est la base, ce qui implique que le composite a coexisté avec TiO2 et Ag3 Bon de commande4 . La figure 3b est le spectre haute résolution de Ag 3d. Les deux pics principaux étaient centrés à l'énergie de liaison 366,26 eV et 372,29 eV, attribués respectivement à Ag 3d5/2 et Ag 3d3/2. Il montre que Ag est principalement Ag + dans le photocatalyseur de TiO2 400/Ag3 Bon de commande4 [16]. La figure 3c montre le pic XPS de P 2p, qui correspond à P 5+ dans le bon de commande4 3+ structure à 131,62 eV. Deux pics situés à 457,43 eV et 464,58 eV peuvent être attribués à Ti 2p3/2 et Ti 2p1/2 dans le spectre XPS de l'orbitale Ti 2p (Fig. 3d). La figure 3e est le XPS de O 1s. Le pic entier peut être divisé en trois pics caractéristiques, 528,9 eV, 530,2 eV et 532,1 eV. Les pics à 528,9 eV et 530,2 eV sont attribués à l'oxygène dans Ag3 Bon de commande4 et TiO2 treillis, respectivement. Les pics à 532,1 eV indiquent les hydroxyles ou l'oxygène adsorbé à la surface du TiO2 /Ag3 Bon de commande4 . Les résultats de l'analyse XPS prouvent en outre que Ag3 Bon de commande4 et TiO2 ont été aggravés.
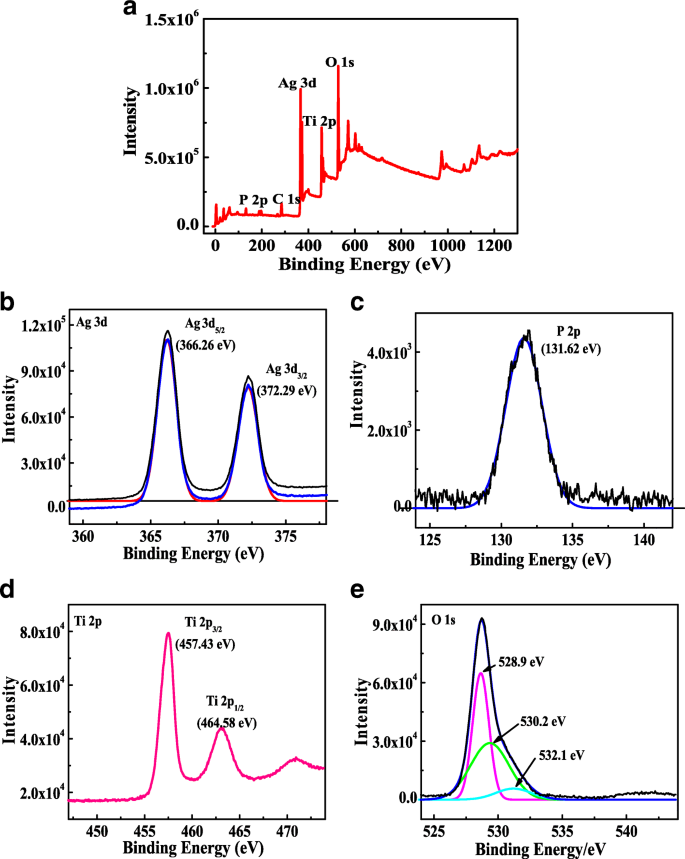
Spectre XPS de TiO2 400/Ag3 Bon de commande4 :a scan d'enquête, b Ag 3d, c P 2p, d Ti 2p, et e O1
Les spectres d'absorption de réflectance diffuse UV-Vis des catalyseurs de TiO2 400, Ag3 Bon de commande4 , et TiO2 400/Ag3 Bon de commande4 sont présentés sur la figure 4a. On peut voir sur la figure que les longueurs d'onde de coupure d'absorption optique de TiO2 400 et Ag3 Bon de commande4 sont respectivement de 400 et 500 nm. Quand Ag3 Bon de commande4 est chargé sur TiO2 400, la plage d'absorption de la lumière du composite s'élargit évidemment à 500-700 nm, indiquant qu'il existe une interaction entre Ag3 Bon de commande4 et TiO2 400 dans le système composite de TiO2 400/Ag3 Bon de commande4 , et le mécanisme nécessite une étude plus approfondie. Bande passante de Ag3 Bon de commande4 , TiO2 400, et TiO2 400/Ag3 Bon de commande4 catalyseurs est calculé avec la formule de Kubelka-Munk [17] :
$$ A\mathrm{hv}=c{\left(\mathrm{hv}-\mathrm{Eg}\right)}^n $$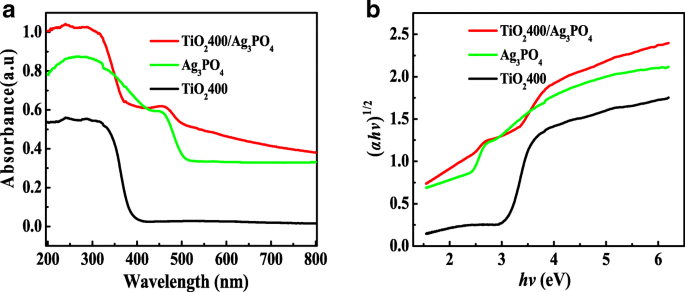
TiO2 400, Ag3 Bon de commande4 , et TiO2 400/Ag3 Bon de commande4 catalyseurs :a UV-Vis DRS, b parcelles de (α hv) 1/2 versus énergie (hv)
où A , hv, c , et Eg sont respectivement le coefficient d'absorption, l'énergie du photon incident, la constante d'absorption et l'énergie de la bande interdite. La valeur de n pour le semi-conducteur direct est de 1/2, et celui pour le semi-conducteur indirect est de 2. Anatase TiO2 et Ag3 Bon de commande4 sont des semi-conducteurs indirects, donc n prend 2.
Les parcelles représentant (α hv) 1/2 par rapport à l'énergie photonique incidente (hv) de la figure 4b indique les diagrammes d'énergie de bande interdite (Eg) de Ag3 Bon de commande4 , TiO2 400, et TiO2 400/Ag3 Bon de commande4 les catalyseurs sont respectivement de 2,45 eV, 3,1 eV et 2,75 eV. Cela prouve encore que TiO2 400/Ag3 Bon de commande4 est un bon photocatalyseur de lumière visible avec une largeur de bande interdite appropriée et une capacité de capture de lumière visible.
Dégradation photocatalytique de RhB par TiO2 400, Ag3 Bon de commande4 , TiO2 300/Ag3 Bon de commande4 , TiO2 400/Ag3 Bon de commande4 , et TiO2 500/Ag3 Bon de commande4 a été étudiée sur la figure 5a. Les résultats ont montré que le TiO2 pur 400 avait le pire effet photocatalytique, et le taux de dégradation photocatalytique n'était que de 30 % en 25 min. L'efficacité de dégradation photocatalytique de l'Ag3 pur Bon de commande4 était de 69% après 25 min d'irradiation. Le taux de dégradation photocatalytique du TiO2 300/Ag3 Bon de commande4 atteint 40% après 25 min. Le taux de dégradation photocatalytique du TiO2 500/Ag3 Bon de commande4 était de 80% après 25 min d'irradiation. La meilleure activité photocatalytique était TiO2 400/Ag3 Bon de commande4 , et 100 % de RhB ont été décomposés après 25 min d'éclairage.
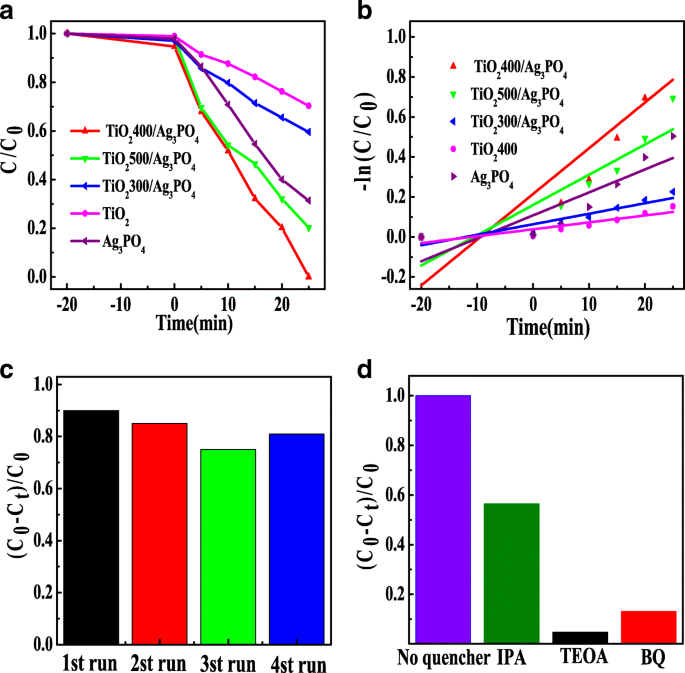
un Effets de différents catalyseurs sur la dégradation photocatalytique de RhB sous lumière visible. b Tracés d'ajustement cinétique de premier ordre de la dégradation photocatalytique de RhB avec différents catalyseurs. c Pistes cyclables de TiO2 400/Ag3 Bon de commande4 . d Expériences de piégeage d'espèces actives
La figure 5b a étudié le modèle cinétique de dégradation photocatalytique de RhB. A partir de la figure, la photodégradation de RhB a été suivie d'une cinétique de pseudo-premier ordre et de la constante de vitesse de réaction (k ) a été calculé avec la pente des courbes d'ajustement. La constante de vitesse de réaction (k ) les valeurs de chaque échantillon ont été présentées dans le tableau 1. Les constantes de vitesse de réaction de TiO2 400, Ag3 Bon de commande4 , TiO2 300/Ag3 Bon de commande4 , TiO2 400/Ag3 Bon de commande4 , et TiO2 500/Ag3 Bon de commande4 étaient 0,00345 min −1 , 0,01148 min −1 , 0,00525 min −1 , 0,02286 min −1 , et 0,01513 min −1 , respectivement. L'échantillon TiO2 400/Ag3 Bon de commande4 a la plus grande constante de vitesse de réaction, qui est de 0,02286 min −1 , le double de Ag3 Bon de commande4 et 6,6 fois celle de la valeur minimale de TiO2 400. Cela indique que la combinaison de Ag3 Bon de commande4 et TiO2 peut grandement contribuer à l'amélioration d'Ag3 Bon de commande4 activité photocatalytique.
La figure 5c est le résultat du test de stabilité de quatre fois la dégradation de la solution de RhB par recyclage de TiO2 400/Ag3 Bon de commande4 . L'effet de dégradation du TiO2 400/Ag3 Bon de commande4 montre une bonne stabilité dans quatre temps de recyclage, et dans l'expérience du quatrième cycle, l'effet de dégradation de TiO2 400/Ag3 Bon de commande4 était légèrement supérieur à celui du troisième cycle. Cela peut être dû à la formation de matériau composite entre Ag3 Bon de commande4 et TiO2 pour accélérer le transfert photogénéré de paires électron-trou et la formation in situ d'une petite quantité d'Ag dans Ag3 Bon de commande4 pendant la photocatalyse pour inhiber une nouvelle photo-corrosion.
Les résultats de TiO2 /Ag3 Bon de commande4 les facteurs de capture sont indiqués sur la figure 5d. Après l'ajout d'agent de piégeage IPA, l'activité de dégradation a diminué partiellement. Lorsque BQ et TEOA ont été ajoutés, le degré de dégradation de RhB a diminué de manière significative, même proche de 0. On peut donc en déduire que les principaux facteurs sont les trous (h + ) et les anions superoxyde (O·− 2), tandis que le radical hydroxyle (·OH) joue partiellement la dégradation.
Un mécanisme possible de dégradation photocatalytique du schéma Z a été proposé dans le schéma 1 pour étendre la dégradation photocatalytique de RhB par TiO2 /Ag3 Bon de commande4 basé sur des expériences de capture de radicaux libres et de photodégradation. La bande interdite de Ag3 Bon de commande4 est de 2,45 eV, et son E CB et E VB les potentiels sont d'environ 0,45 eV et 2,9 eV (vs NHE) [18], respectivement. Comme le montre le schéma 1, sous irradiation de lumière visible, Ag3 Bon de commande4 est stimulé par des photons avec une énergie supérieure à sa bande interdite pour produire des paires électron-trou photogénérées. Les trous laissés dans la bande de valence de Ag3 Bon de commande4 migré vers la bande de valence de TiO2 puis participé directement au processus d'oxydation et de décomposition du RhB, qui s'adsorbe à la surface du TiO2 . Parallèlement, lors de la migration des trous photogénérés, le H2 O et OH − adsorbé sur la surface composite peut également être oxydé pour former ·OH, et le ·OH hautement oxydant peut oxyder et dégrader davantage les polluants. Ceci est principalement dû à l'énergie des trous dans la bande de valence de Ag3 Bon de commande4 qui est de 2,9 eV, supérieure à l'énergie potentielle de réaction de OH − /OH (E(OH − /OH) = 1.99 eV (vs. NHE)). Cependant, le potentiel de conduction de Ag3 Bon de commande4 est de 0,45 eV, l'énergie des électrons photogénérés est de 0,45 eV et l'énergie d'activation de l'oxygène à électron unique est E(O2 /O·− 2) = 0.13 eV (vs NHE). Les électrons photogénérés sur Ag3 Bon de commande4 la bande de conduction ne peut pas être capturée par l'oxygène dissous. Avec l'accumulation d'électrons photogénérés sur Ag3 Bon de commande4 bande conductrice, une petite quantité de nanoparticules d'Ag s'est formée en raison de la corrosion photocatalytique d'Ag3 Bon de commande4 photocatalyseur. Les nanoparticules d'Ag formées peuvent également être stimulées par l'énergie lumineuse pour former des paires électron-trou photogénérées. Puis les électrons ont migré vers la bande de conduction de TiO2 , tandis que les trous laissés sur les nanoparticules d'Ag peuvent être combinés avec les électrons photogénérés générés sur la bande de conduction d'Ag3 Bon de commande4 , empêchant ainsi la corrosion supplémentaire de Ag3 Bon de commande4 photocatalyseur. En raison de la bande interdite de TiO2 est de 3,1 eV, il ne peut pas être excité sous la lumière visible et le E CB et E VB sont env. − 0,24 eV et 2,86 eV (vs NHE), respectivement. Électrons injectés dans TiO2 la bande de conduction peut dégrader les polluants en piégeant l'oxygène adsorbé sur le TiO2 surface. Ceci est principalement dû au E CB = − 0.24 eV (vs. NHE) qui est plus négatif que E(O2 /O·- 2) = 0.13 eV (vs NHE). Les résultats sont en accord avec les expériences de piégeage. Les principaux facteurs sont les trous (h + ) et les anions superoxyde (O·- 2), tandis que le radical hydroxyle (·OH) joue partiellement la dégradation.
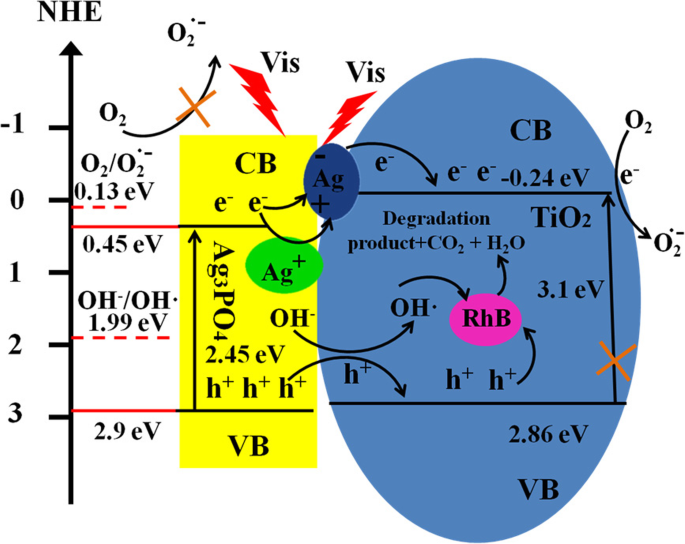
Illustration schématique du mécanisme photocatalytique du TiO2 /Ag3 Bon de commande4
Sur la base de la discussion ci-dessus, la réaction de dégradation de TiO2 /Ag3 Bon de commande4 est exprimé par l'équation chimique comme suit :
Génération de paires de trous de photoélectrons :
$$ {\mathrm{Ag}}_3\mathrm{P}{\mathrm{O}}_4+\mathrm{hv}\to {\mathrm{Ag}}_3\mathrm{P}{\mathrm{O}} _4\gauche({\mathrm{e}}^{-}\right)+{\mathrm{Ag}}_3\mathrm{P}{\mathrm{O}}_4\gauche({\mathrm{h}} ^{+}\right) $$$$ {\mathrm{Ag}}^{+}+{\mathrm{Ag}}_3\mathrm{P}{\mathrm{O}}_4\left({\mathrm {e}}^{-}\right)\to \mathrm{Ag}+{\mathrm{Ag}}_3\mathrm{P}{\mathrm{O}}_4 $$$$ \mathrm{Ag}+ \mathrm{hv}\to \mathrm{Ag}\left({\mathrm{e}}^{-}\right)+\mathrm{Ag}\left({\mathrm{h}}^{+}\ à droite) $$Migration et transformation de paires d'électrons de trous photogénérés :
$$ {\mathrm{Ag}}_3\mathrm{P}{\mathrm{O}}_4\left({\mathrm{h}}^{+}\right)+\mathrm{Ti}{\mathrm{ O}}_2\à \mathrm{Ti}{\mathrm{O}}_2\left({\mathrm{h}}^{+}\right)+{\mathrm{Ag}}_3\mathrm{P} {\mathrm{O}}_4 $$$$ {\mathrm{Ag}}_3\mathrm{P}{\mathrm{O}}_4\left({\mathrm{e}}^{-}\right) +\mathrm{Ag}\gauche({\mathrm{h}}^{+}\right)\to \mathrm{Ag}+{\mathrm{Ag}}_3\mathrm{P}{\mathrm{O} }_4 $$$$ \mathrm{Ag}\left({\mathrm{e}}^{-}\right)+\mathrm{Ti}{\mathrm{O}}_2\à \mathrm{Ti}{ \mathrm{O}}_2\left({\mathrm{e}}^{-}\right)+\mathrm{Ag} $$$$ \mathrm{Ti}{\mathrm{O}}_2\left( {\mathrm{e}}^{-}\right)+{\mathrm{O}}_2\à {\mathrm{O}}_2^{\cdotp -}+\mathrm{Ti}{\mathrm{O }}_2 $$$$ {\mathrm{Ag}}_3\mathrm{P}{\mathrm{O}}_4\left({\mathrm{h}}^{+}\right)+0{\mathrm {H}}^{-}\à \mathrm{OH}\cdotp +{\mathrm{Ag}}_3\mathrm{P}{\mathrm{O}}_4 $$Dégradation des polluants :
$$ \mathrm{Ti}{\mathrm{O}}_2\left({\mathrm{h}}^{+}\right)+\mathrm{RhB}\to \mathrm{Dégradation}\ \mathrm{produit }+{\mathrm{CO}}_2+{\mathrm{H}}_2\ \mathrm{O} $$$$ {\mathrm{O}}_2^{\cdotp -}+\mathrm{RhB}\to \mathrm{Dégradation}\ \mathrm{produit}+{\mathrm{CO}}_2+{\mathrm{H}}_2\ \mathrm{O} $$$$ \mathrm{OH}\cdotp +\mathrm{RhB }\à \mathrm{Dégradation}\ \mathrm{produit}+{\mathrm{CO}}_2+{\mathrm{H}}_2\ \mathrm{O}+{\mathrm{Cl}}^{-} $ $Conclusions
En résumé, une étude complète du composite Ag3 Bon de commande4 /TiO2 photocatalyseur, préparé par une méthode simple en deux étapes est présenté. Des outils de caractérisation complémentaires tels que la diffraction des rayons X (XRD), la microscopie électronique à balayage (MEB), la microscopie électronique à transmission (MET), la microscopie électronique à transmission haute résolution (HR-TEM), la spectroscopie à dispersion d'énergie (EDX), X La spectroscopie photoélectronique (XPS) et la spectroscopie de réflectance diffuse UV-vis (DRS) ont été utilisées dans cette étude. Les résultats ont montré que le composite Ag3 Bon de commande4 /TiO2 photocatalyseur est hautement cristallin et a une bonne morphologie. Pour Ag3 Bon de commande4 /TiO2 dégradation de RhB, TiO2 400/Ag3 Bon de commande4 montre l'activité photocatalytique la plus élevée. Après 25 min de réaction, le taux de dégradation photocatalytique atteint presque 100%. La constante de vitesse de réaction de TiO2 400/Ag3 Bon de commande4 est de 0,02286 min −1 , qui est le double de Ag3 Bon de commande4 et 6,6 fois celle de la valeur minimale de TiO2 400. Le TiO2 400/Ag3 Bon de commande4 présente également une bonne stabilité après recyclage quatre fois. Les principales espèces catalytiques actives sont les trous (h + ) et les anions superoxyde (O·− 2), tandis que le radical hydroxyle (·OH) joue partiellement la dégradation à partir des expériences de piégeage. De plus, un mécanisme de réaction de schéma Z de Ag3 Bon de commande4 /TiO2 Une structure hétérogène est proposée pour expliquer le mécanisme de dégradation de RhB. L'accumulation d'électrons photogénérés sur Ag3 Bon de commande4 la bande conductrice provoque une photogravure de Ag3 Bon de commande4 photocatalyseur pour former une petite quantité de nanoparticules d'Ag, accélérant par conséquent le transfert d'électrons photogénérés dans l'Ag3 Bon de commande4 bande de conduction, empêchant ainsi d'autres Ag3 Bon de commande4 corrosion du photocatalyseur.
Disponibilité des données et des matériaux
Les auteurs déclarent que les matériaux et la date sont rapidement disponibles pour les lecteurs sans qualifications indues dans les accords de transfert de matériel. Toutes les données générées dans cette étude sont incluses dans cet article.
Abréviations
- BQ :
-
p -benzoquinone
- DRS :
-
Spectroscopie de réflectance diffuse UV-vis
- EDX :
-
Spectromètre à rayons X à dispersion d'énergie
- HR-TEM :
-
Microscopie électronique à transmission haute résolution
- IPA :
-
Isopropanol
- RhB :
-
Rhodamine B
- SEM :
-
Microscopie électronique à balayage
- TEM :
-
Microscopie électronique à transmission
- TEOA :
-
Triéthanolamine
- XPS :
-
Spectroscopie photoélectronique aux rayons X
- XRD :
-
Diffraction des rayons X
Nanomatériaux
- Composites de graphène quantique/TiO2 co-dopé S, N pour une génération d'hydrogène photocatalytique efficace
- Synthèse hydrothermale de nanoparticules d'In2O3 jumelles hybrides disque hexagonal hétérostructures ZnO pour des activités photocatalytiques et une stabilité améliorées
- Performances photocatalytiques induites par la lumière visible des nanocomposites ZnO/g-C3N4 dopés N
- Un nouveau photocatalyseur à hétérojonction Bi4Ti3O12/Ag3PO4 avec des performances photocatalytiques améliorées
- Effets synergiques des nanoparticules d'Ag/BiV1-xMoxO4 avec une activité photocatalytique améliorée
- Activité photocatalytique du nanocomposite ternaire attapulgite–TiO2–Ag3PO4 pour la dégradation de la Rhodamine B sous irradiation solaire simulée
- Fabrication et propriété photocatalytique de nouveaux nanocomposites SrTiO3/Bi5O7I
- Fabrication d'hétérostructures Hiérarchiques ZnO@NiO Core–Shell pour de meilleures performances photocatalytiques
- Synthèse facile et amélioration de l'activité photocatalytique en lumière visible de nouveaux composites à hétérojonction p-Ag3PO4/n-BiFeO3 pour la dégradation des colorants



