Évaluation de la biodégradation de poly (acide lactique) rempli de nanoparticules de titane fonctionnalisées (PLA/TiO2) dans des conditions de compost
Résumé
Cet article présente une étude de biodégradation menée pendant 90 jours dans des conditions de compostage contrôlé normalisé de poly (acide lactique) (PLA) rempli de nanocharge anatase-titane fonctionnalisée (PLA/TiO2 nanocomposites). La morphologie de la surface, les propriétés thermiques, le pourcentage de biodégradation et les changements de poids moléculaire à différents temps d'incubation ont été évalués par inspection visuelle, microscopie électronique à balayage (MEB), diffraction des rayons X (XRD), calorimétrie différentielle à balayage (DSC) et perméation de gel chromatographie (GPC) en prélevant des échantillons dégradés du compost à la fin de l'intervalle de temps de biodégradation cible. L'augmentation rapide de la cristallinité a indiqué que le PLA et le PLA/TiO2 les nanocomposites avaient des mécanismes de dégradation hétérogènes dans des conditions de compostage contrôlées. Le taux de biodégradation du PLA/TiO2 nanocomposites était plus élevé que celui du PLA pur car les molécules d'eau pénétraient facilement les nanocomposites. La dispersion des nanoparticules dans le PLA/TiO2 les nanocomposites ont affecté le taux de biodégradation du PLA. De plus, la biodégradation du PLA pourrait être contrôlée en ajoutant une quantité de TiO2 dispersé nanocharges dans des conditions de compostage contrôlées.
Introduction
Le poly (acide lactique) (PLA), un polymère synthétique biodégradable, est étudié dans le monde entier pour des applications biomédicales et grand public en raison du besoin croissant de matériaux renouvelables qui constituent des alternatives durables aux produits dérivés de la pétrochimie [1,2,3,4]. Le PLA est le produit qui résulte de la polymérisation du lactide ou de l'acide lactique, qui est l'acide carboxylique le plus produit dans la nature par fermentation microbienne des glucides [5]. Cependant, l'applicabilité du PLA a été relativement limitée car sa température de déformation thermique, sa ténacité et son taux de dégradation ne sont pas satisfaisants [6, 7]. L'une des méthodes pour résoudre ces inconvénients consiste à modifier le PLA en ajoutant des nanoparticules inorganiques, notamment de la nanoargile typique, des nanotubes de carbone, de l'oxyde de zinc et de l'anatase (A-TiO2 ) [8,9,10,11,12,13,14,15]. Récemment, le PLA/TiO2 les nanocomposites ont été préparés par nos soins par fusion et mélange de PLA avec du TiO2 chimiquement modifié (solution acide lactique greffé TiO2 , ci-après dénommé g-TiO2 ) [16]. Les résultats ont montré que TiO2 les nanoparticules ont eu un effet significatif sur l'amélioration des propriétés mécaniques du PLA/TiO2 mélanges, tels que la déformation à la rupture et l'élasticité, par rapport au PLA pur. En même temps, g-TiO2 les nanoparticules ont eu une forte influence sur la dégradation hydrolytique et la photodégradation du PLA [17, 18].
L'étude de la biodégradabilité et du mécanisme de biodégradation des matériaux biodégradables à l'aide de tests à l'échelle du laboratoire est une méthode extrêmement importante d'un point de vue industriel et scientifique qui permet de comprendre la durée de vie de ces matériaux [15]. Il existe plusieurs méthodes actuellement disponibles pour évaluer la biodégradabilité des matériaux biodégradables, qui sont généralement basées sur une mesure indirecte, telle que la production de dioxyde de carbone, la génération de biogaz ou la consommation d'oxygène [19, 20].
Les caractéristiques de biodégradation du PLA dans le compost ont été étudiées et rapportées [21,22,23]. Le compostage est une biodégradation accélérée des matières organiques dans un environnement chaud, humide et aérobie sous une combinaison de population microbienne et de conditions de compostage contrôlées [24, 25]. De plus, la biodégradation du PLA dans des conditions de compostage, un processus dépendant de la température et de l'humidité, implique plusieurs processus, à savoir l'absorption d'eau, le clivage des esters et la formation et la dissolution de fragments d'oligomères [26]. Le mécanisme le plus accepté de la biodégradation du PLA implique un processus de dégradation en deux étapes. Initialement, la chaleur et l'humidité du compost attaquent les chaînes PLA et les séparent, produisant ainsi de petits polymères Mw et, éventuellement, de l'acide lactique. Par la suite, les micro-organismes du compost et du sol minéralisent les fragments d'oligomères et l'acide lactique pour générer du méthane et du dioxyde de carbone (CO2 ) dans des conditions anaérobies et aérobies, respectivement [27,28,29].
Récemment, l'effet des charges sur la biodégradation du PLA a attiré une grande attention et une attention particulière s'est portée sur les nanocharges, telles que les nanoargiles, les nanotubes de carbone et l'hydroxyapatite [23, 30,31,32,33,34,35,36, 37,38]. Certains auteurs [32,33,34] ont découvert que l'ajout de nanoparticules pouvait accélérer la biodégradation du PLA, ce qui était attribué à l'hydrophilie relative élevée des nanoparticules, permettant ainsi une perméabilité aisée de l'eau dans la matrice polymère et déclenchant une dégradation hydrolytique. Cependant, d'autres études [35,36,37,38] ont rapporté que la biodégradation était retardée en raison des propriétés de barrière améliorées des nanocomposites.
Bien qu'il y ait eu quelques littératures se concentrant sur la biodégradation des matériaux PLA, le rôle que TiO2 joue dans la dégradation du PLA reste controversée. Comment le TiO2 nanoparticules affectent la biodégradation du PLA n'était pas clair. Ainsi, une étude de la biodégradation du PLA, modifié par TiO2 nanocharges à l'état de compost, est toujours nécessaire. L'étude actuelle, basée sur l'estimation de l'évolution du CO2 , a évalué la biodégradation du PLA/TiO2 nanocomposites abondamment dans des conditions de compostage contrôlées en laboratoire, un complément de dégradabilité du PLA/TiO2 nanocomposites dans différentes conditions de dégradation, pourraient étendre l'utilisation du PLA dans diverses applications finales à l'avenir.
Méthodes
Matériaux
PLA (fabriqué par Natureworks @ (4032D)) présentaient un poids moléculaire moyen en poids (Mw) de 19 600 kDa et une polydispersité de 1,89 telle que déterminée par chromatographie par perméation de gel (GPC). PLA séché à 65 °C pendant 24 h sous pression réduite et conservé sous vide avec absorbeur d'humidité avant utilisation. L'acide lactique (88 %, Guangshui National Chemical Co.) a été distillé à 80°C pour éliminer l'eau avant utilisation. Les nanoparticules d'oxyde de titane anatase, avec une taille de particule primaire moyenne d'env. 20 um, ont été fournis par Pangang Co., Ltd. Le toluène et le chloroforme ont été utilisés tels qu'ils ont été reçus. La cellulose microcristalline de qualité chromatographique a été fournie par Shanghai Chemical Reagent Co., Ltd. Les inoculums de compostage, qui ont été obtenus à partir d'une fraction organique de déchets solides municipaux (MSW), ont été fournis par le Degradable Plastics Professional Committee de la China Plastics Processing Industry Association ( CPPIA).
Préparation de l'échantillon
Informations détaillées sur la fonctionnalisation du TiO2 nanoparticules et préparation du PLA/TiO2 nanocomposites a été rapportée [16]. G-TiO2 des nanocharges ont été préparées en greffant un oligomère d'acide lactique sur la surface de l'anatase. PLA/TiO2 les nanocomposites ont été préparés par mélange à l'état fondu via une extrudeuse à double vis corotative. Le PLA pur a été soumis au même traitement de mélange afin d'avoir le même historique thermique que les nanocomposites. Les échantillons avec 0, 0,5, 1,0, 2,0, 5,0, 8,0 et 15,0 % en poids g-TiO2 ont été préparés et étiquetés comme PLA, PLA/TiO2 –0,5, PLA/TiO2 –1, PLA/TiO2 –2, PLA/TiO2 –5, PLA/TiO2 –8, et PLA/TiO2 -15 nanocomposites.
Petits spécimens de puces de PLA et de g-TiO2 à différents rapports ont été convertis en feuilles d'environ 0,5 mm d'épaisseur par pressage à 190 °C pendant 4 min sous 10 MPa suivi d'un refroidissement à température ambiante pendant 5 min sous 5 MPa. Par la suite, les échantillons moulés par compression ont été découpés en 5 mm × 5 mm et pesés.
Tests de dégradation
Un essai de biodégradation a été mené dans une installation à l'échelle du laboratoire sur la base de méthodes d'essai standard conçues pour les plastiques biodégradables (GB/T19277-2003/ISO 14855-1:2005) (détermination de la biodégradabilité aérobie ultime des matières plastiques dans des conditions de compostage contrôlées - méthode par analyse du CO évolué2 ). La plupart du carbone dans les substrats métabolisés génère de l'énergie par transformation chimique en CO2 en milieu aérobie [39]. Par conséquent, les mesures de la génération de CO2 sont considérées comme la mesure de biodégradation la plus appropriée dans la plupart des circonstances. La norme spécifie une procédure pour déterminer la biodégradabilité aérobie ultime en mesurant la quantité de CO2 dégagé. et le pourcentage du degré de biodégradation des matériaux d'essai dans des conditions de compostage contrôlées. L'inoculum de compostage a été obtenu à partir d'une fraction organique de MSW, qui a été tamisée à des tailles inférieures à 5 mm. Ensuite, la fraction fine a été utilisée comme inoculum. Le tableau 1 montre les propriétés physico-chimiques déterminées des inoculums de compostage. Dans chaque essai, une série de réacteurs de compostage (chaque échantillon en triple) a été chargée avec 15 µg du matériau de référence (c'est-à-dire de la cellulose microcristalline (MCE), suggérée par la norme) ou du matériau d'essai (chaque film pesé et étiqueté avant dégradation), 85 g d'inoculum et 320 g de sable de mer sec (fournit de bonnes conditions homogènes et un environnement aérobie amélioré à l'intérieur de l'inoculum). Ensuite, les réacteurs ont été placés dans un incubateur sans lumière à 58 ± 2 °C pendant une durée d'expérimentation de 90 jours. L'aération a été initiée en utilisant du CO2 saturé en eau -air gratuit; le débit à travers chaque réacteur a été fixé à 25 mL·min −1 . L'humidité, le mélange et l'aération dans tous les réacteurs ont été contrôlés conformément aux exigences GB/T19277-2003/ISO 14855-12,005. À des moments choisis, trois à quatre spécimens de chaque échantillon ont été sélectionnés, lavés à l'eau distillée et séchés à température ambiante pendant au moins 24 h jusqu'à poids constant.
Le CO2 qui a évolué au cours du processus de biodégradation a été piégé dans des solutions de NaOH et mesuré à intervalles réguliers en utilisant la méthode de titrage. Le NaOH a été titré avec une solution de HCl standard jusqu'au point final de phénolphtaléine. Le CO total2 évolué au cours de la biodégradation a été calculé par rapport au flacon témoin. Les données rapportées pour chaque échantillon étaient la valeur moyenne obtenue à partir de trois échantillons.
Caractérisation
Examen au microscope
Des images de microscopie électronique à balayage (MEB) ont été obtenues à l'aide d'un instrument Philips FEI INSPECT F fonctionnant à 5 kV. Tous les spécimens ont été recouverts d'or par pulvérisation cathodique avant l'analyse.
Analyse Thermique
Les propriétés thermiques des échantillons ont été étudiées par calorimétrie différentielle à balayage (DSC) (TA Q20, TA Instruments). Les thermogrammes ont été obtenus sous flux d'azote (50 mL/min) à des vitesses de chauffage et de refroidissement de 10 °C/min dans la plage de température allant de la température ambiante à 200 °C et de 200 à - 50 °C, respectivement.
Études XRD
Les analyses par diffraction des rayons X (XRD) ont été effectuées à l'aide d'un diffractomètre à rayons X DX-1000 (Dandong Fanyuan Instrument Co. LTD. Chine) équipé d'un Cu Kα (λ = 0,154 nm). Le générateur fonctionnait à 25 mA et 40 kV. Les échantillons ont été numérisés sous différents angles (c'est-à-dire de 2 à 70°) à une vitesse de numérisation de 6°/min.
Détermination du pourcentage de biodégradation (D t , %)
Pourcentage de biodégradation (D t , %) peut être calculé à l'aide de l'équation. 1, qui a été adopté comme pour l'Eq. 2 [1, 40].
$$ {D}_t\left(\%\right)=\frac{{\left({\mathrm{CO}}_2\right)}_T-{\left({\mathrm{CO}}_2\right )}_B}{{\mathrm{Th}}_{\mathrm{CO}2}}\times 100 $$ (1)où (CO2 )T est la quantité de CO2 (en g/flacon) a évolué à partir des matériaux d'essai, (CO2 )B est la quantité de CO2 (en g/flacon) évolué dans le ballon témoin, et ThCO2 est le CO2 théorique quantité produite par les matériaux polymères.
Le CO2 théorique quantité pouvant être produite dans chaque flacon (ThCO2 , g 2 /g échantillon) a été calculé à l'aide de l'équation suivante :
$$ {\mathrm{Th}}_{\mathrm{CO}2}={M}_{\mathrm{TOT}}\times {C}_{\mathrm{TOT}}\times \frac{44} {12} $$ (2)où M TOT est le poids total (g) de la matière solide polymère sèche ajoutée dans le flacon de compostage au début de l'expérience, C TOT est le poids (g) du carbone organique total dans le total des solides polymères secs dans l'échantillon, et 44 et 12 sont la masse moléculaire de CO2 et masse atomique de C , respectivement.
Mesure du poids moléculaire
Les poids moléculaires des nanocomposites PLA avant et après le compostage ont été déterminés par GPC. Le système GPC était équipé d'une pompe HPLC isocratique Waters 1515, d'un détecteur d'indice de réfraction Waters 2414 et d'un échantillonneur automatique Waters 717 plus. Le chloroforme a été utilisé comme éluant à un débit de 0,8 mL/min à 30°C. L'étalonnage a été réalisé avec des étalons de polystyrène.
Résultats et discussion
La dégradation des polymères est associée à des changements de caractéristiques, telles que la couleur, la morphologie de la surface et les propriétés mécaniques. Les changements temporels dans l'apparence du PLA pur et du PLA/TiO2 les nanocomposites étaient différents dans des conditions de laboratoire. Les surfaces de la matrice PLA pure, qui étaient initialement transparentes en accord avec la structure amorphe, sont devenues relativement blanchâtres après 2 jours de biodégradation [41]. Cette caractéristique augmentait avec le temps d'incubation jusqu'à l'opacité complète après 10 jours. Des plaques jaunâtres à brun foncé, causées par la perméation de l'eau et l'incubation de micro-organismes, ont commencé à être observées à la surface des films de PLA purs après 30 jours. Cependant, une grande surface de plaques brun foncé a émergé à la surface du nanocomposite PLA après 6 jours (la figure n'a pas été montrée). Les taches brunes impliquent les colonies de micro-organismes et les fissures représentent l'effet de biodégradation. La figure 1 montre la morphologie de surface du PLA et de son TiO2 nanocomposites sous observation SEM. Avant dégradation, la surface de pur et PLA/TiO2 les nanocomposites étaient lisses. Le PLA pur n'a pas présenté de changements significatifs à la surface après 5 jours de biodégradation dans des conditions de compost. Après 20 jours, la rugosité de surface du PLA pur a augmenté (Fig. 1a, a’). Cependant, PLA/TiO2 nanocomposite a présenté des changements progressifs montrant clairement que la dégradation considérable du PLA/TiO2 composite s'est produit. Des fissures et des vides évidents (Fig. 1b, b’ ; c, c’ ; et d, d’ ; respectivement) ont été observés à la surface des nanocomposites. Cela pourrait être dû à l'hydrolyse du PLA et aux activités des micro-organismes. Avec l'augmentation du temps d'incubation, les fissures et les vides sont devenus substantiellement profonds et larges (Fig. 1 b', c' et d', respectivement), suggérant ainsi une perte de chaîne et une érosion de surface au fil du temps. Le phénomène d'érosion en vrac pour tous les matériaux d'essai était similaire au processus de dégradation hydrolytique du PLA et du PLA/TiO2 nanocomposites [17].

Photographie SEM de la surface du PLA pur (a 0 , a , a' ), PLA/TiO2 –2 (b 0 , b , b' ), PLA/TiO2 –5 (c 0 , c , c' ) et PLA/TiO2 –8 (d 0 , d , d' ) nanocomposites en fonction du temps d'incubation. un 0 , b 0 , c 0 , d 0 :0 jour; un , b , c , d :5 jours; a' , b' , c' , d' :20 jours
Pour évaluer la cristallinité du PLA et du PLA/TiO2 nanocomposites au cours de la biodégradation, des échantillons sélectionnés à différents temps d'incubation ont été analysés pour leurs propriétés thermiques (Fig. 2 et 3). La figure 2 montre que la température de transition vitreuse (T g ) a légèrement diminué pour tous les échantillons avec un temps de dégradation. La diminution de T g était clairement due à une mobilité accrue des molécules, conséquence du processus d'hydrolyse et de l'effet plastifiant des fragments d'oligomères et de l'eau pendant la biodégradation [33, 42]. La disparition du pic de cristallisation froide (T cc ) pour tous les échantillons seulement après 2 jours pourrait être attribué à l'hydrolyse du PLA et à l'augmentation rapide de la cristallinité de la matrice polymère [43]. La diminution de T m a été attribuée à la réduction rapide de la masse moléculaire [44, 45]. Le pic de fusion bimodal s'est progressivement transformé en pic monomodal, ce qui implique que les cristaux petits et imparfaits ont disparu avec le temps de dégradation. Ce résultat a prouvé que la dégradation du PLA s'est déroulée rapidement dans les régions amorphes au cours du stade précoce de la dégradation dans des conditions de compostage contrôlées. Le balayage de refroidissement (voir Fig. 3) montre que le pic de cristallisation du PLA pur a augmenté progressivement. Cependant, les pics de cristallisation du PLA/TiO2 les nanocomposites ont initialement augmenté de manière significative et ont diminué légèrement par la suite avec une augmentation du temps d'incubation. De plus, plus la teneur en nanocharges était élevée, plus les pics de cristallisation arrivaient tôt à son pic. La diminution du pic de cristallisation a en outre vérifié que la région cristalline commençait à se dégrader après la dégradation de la région amorphe. Giuliana et Roberto [42] ont rapporté qu'à de courts moments pour l'échantillon de PLA, certaines régions amorphes se transforment en cristal, puis le degré de cristallinité augmente en raison de l'effet de l'érosion des parties amorphes. De plus, les régions cristallines subissent une hydrolyse de longue durée.
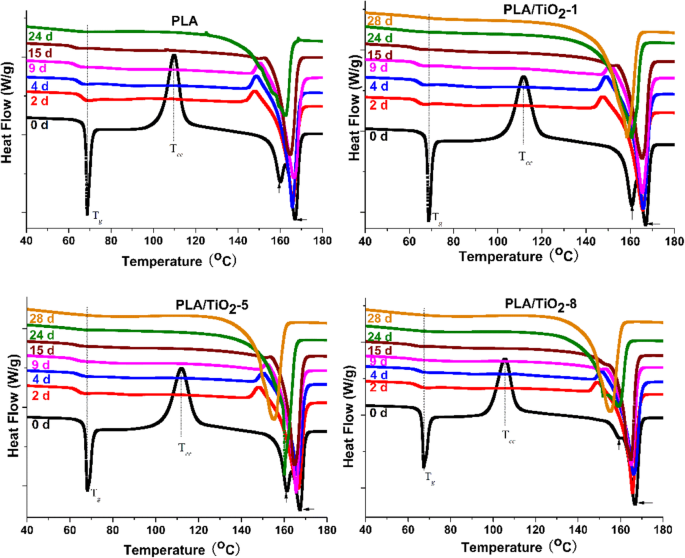
Thermogrammes DSC des produits de biodégradation du PLA pur et du PLA/TiO2 nanocomposites à différents temps d'incubation, premier balayage de chauffage
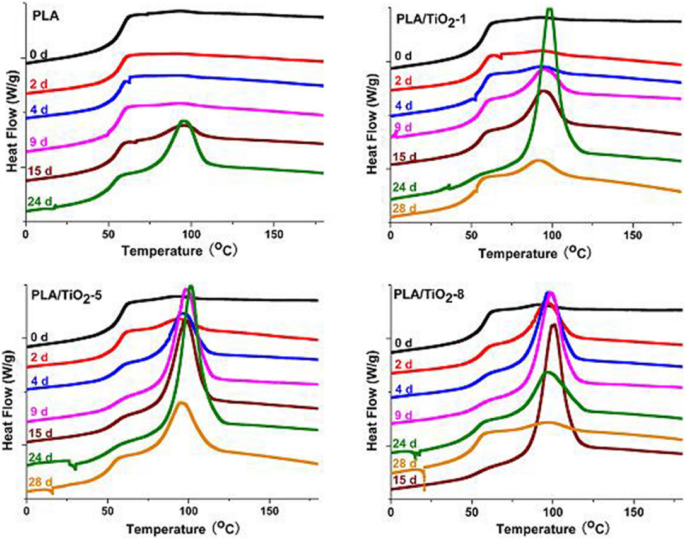
Thermogrammes DSC de PLA pur biodégradé et PLA/TiO2 nanocomposites à différents temps d'incubation, analyse de refroidissement
XRD fournit une méthode idéale pour surveiller les changements dans la cristallisation des polymères pendant la dégradation. Les motifs XRD du PLA et de ses nanocomposites (Fig. 4) montrent que la matrice polymère conserve une structure amorphe avant la biodégradation. Seulement après 2 jours, deux forts pics à 2θ = 16,4, 18,5°, 20,9° et 23,6° apparaissent clairement et leur intensité augmente avec le temps d'incubation. Ce résultat impliquait la formation de structures cristallines de type poly (L-lactide) ou poly (D-lactide) [46, 47]. Le changement de pic cristallin indiquait que les régions amorphes se dégradaient plus rapidement que les régions cristallines, ce qui augmentait la valeur du rapport des régions cristallines aux régions amorphes. Ce résultat était cohérent avec les résultats DSC et le changement de transparence des échantillons.
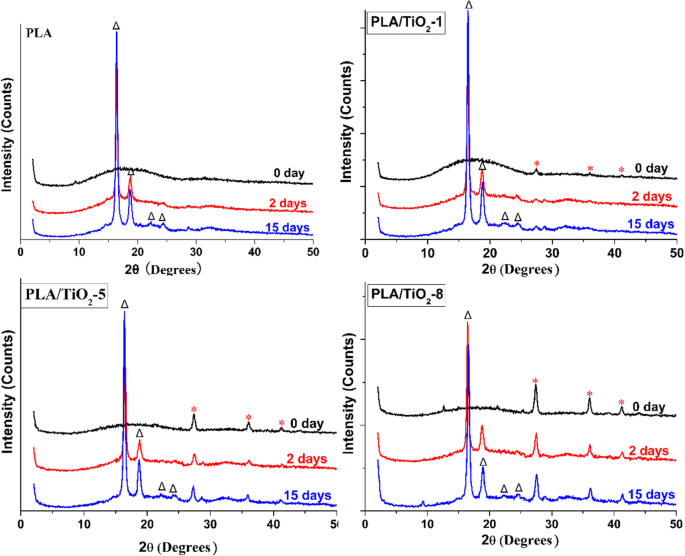
Modèles XRD de PLA pur et PLA/TiO2 nanocomposites à différents temps d'incubation
L'évaluation de la validation de l'inoculum est cruciale lors de la biodégradation en conditions de compostage. L'activité de l'inoculum a été mesurée comme requis par la méthode standard :D t du matériau de référence doit être d'au moins 70 % à la fin des 45 jours d'essai. L'insert de la Fig. 5 montre que le MCE commence à se biodégrader après 5 jours et que le pourcentage de biodégradation atteint jusqu'à 72 % à la fin des 45 jours d'incubation. Ces résultats ont indiqué que le MCE dans l'expérience était efficace comme matériau de référence. Dans l'expérience, les cuves de compostage en double ont montré une bonne reproductibilité (écart type ± 1,3 %). La figure 5 montre D t pour du PLA soigné et du PLA/TiO2 nanocomposites pendant l'incubation. Un comportement similaire a été observé pour le PLA et le PLA/TiO2 nanocomposites, c'est-à-dire qu'une phase de latence a d'abord été observée, qui est ensuite suivie d'une augmentation linéaire abrupte de la biodégradation et ensuite d'une phase de plateau pour tous les échantillons. La raideur de l'augmentation devrait indiquer une dégradation accrue. Cependant, les courbes indiquaient que la phase de latence des nanocomposites était un peu plus courte que celle du PLA pur. Ce résultat indique la présence de TiO2 , dans une certaine mesure, a accéléré la phase initiale de dégradation et augmenté le pourcentage de CO2 produit à la fin de la période d'incubation. Après 80 jours d'incubation dans des conditions de compostage contrôlées, D t pour PLA, PLA/TiO2 –1, PLA/TiO2 –2, PLA/TiO2 –5, PLA/TiO2 –8, et PLA/TiO2 –15 a atteint 78,9, 86,9, 92,0, 97,8, 91,3 et 85,0%, respectivement. Kunioka et al. [48] ont rapporté que la biodégradabilité finale du PLA était de 80 %. Les résultats de notre expérience ont montré que D t du produit PLA commercialement pur était également de près de 80 % au bout de 80 jours. La diminution de D t à partir de PLA/TiO2 –8 est attribué à l'agglomération intense de TiO2 lorsque sa teneur dépassait 8 % en poids [16]. De plus amples détails sont présentés dans la section suivante.
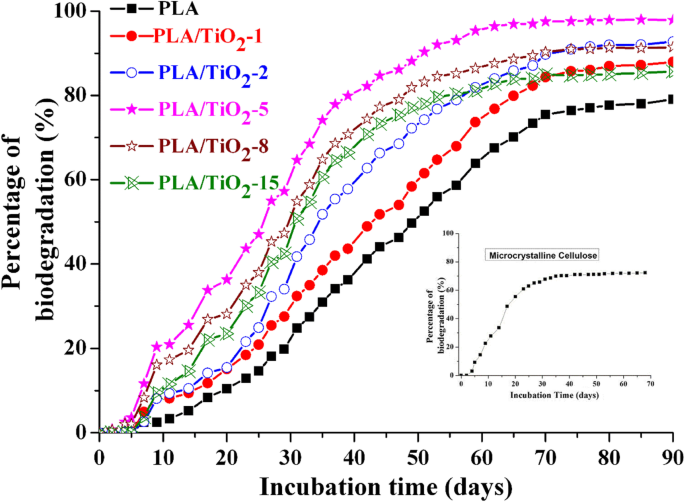
Pourcentage de biodégradation en fonction du temps d'incubation pour le PLA pur et le PLA/TiO2 nanocomposites. L'insert est le pourcentage de biodégradation en fonction du temps pour la cellulose microcristalline
Les différents pourcentages de biodégradation sont liés aux différents changements de poids moléculaire de la matrice polymère. La figure 6 montre le changement de poids moléculaire des échantillons en fonction du temps d'incubation. Les courbes montrent que les changements de Mn dans le PLA/TiO2 les nanocomposites étaient similaires (c'est-à-dire une diminution rapide de Mn suivie d'une phase de plateau de presque un Mn constant) au moins dans le temps d'incubation déterminé. Pour explorer les mécanismes de dégradation causés par l'ajout de nanocharges, un modèle qui tient compte de l'autocatalyse par les groupes terminaux d'acide carboxylique générés a été utilisé pour calculer la constante de vitesse de dégradation catalysée selon la référence [17, 49] :
$$ \ln {M}_{nt}=\ln {M}_{n0}- kt $$ (3)où k est une constante de vitesse de dégradation hydrolytique catalysée, M n0 est le poids moléculaire moyen en nombre avant dégradation, M nt est le poids moléculaire moyen en nombre à tout moment.
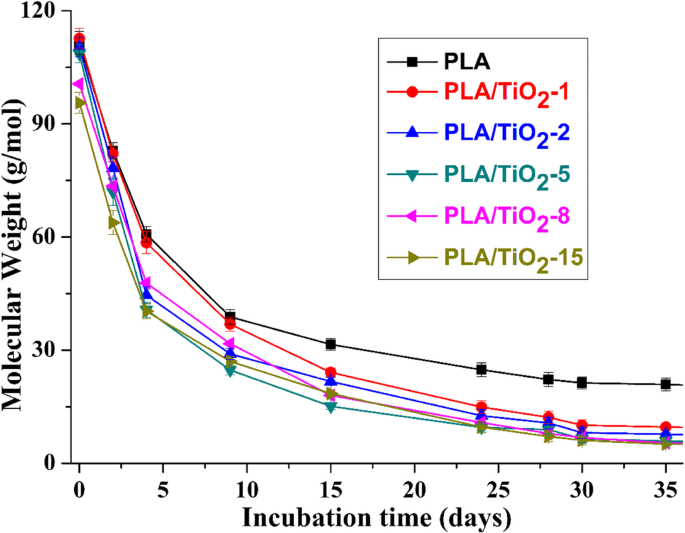
Evolution de Mn en fonction du temps pour PLA pur et PLA/TiO2 nanocomposites
Le k valeurs évaluées par l'Eq. (3) sont tracés sur la figure 7. À partir de la figure 7, le taux de dégradation des nanocomposites PLA et PLA a pu être identifié à deux et trois phases, respectivement. Le Mn a diminué rapidement au cours des 8 premiers jours et suivi d'une phase de plateau par la suite pour le PLA pur. Pour PLA/TiO2 nanocomposites, les valeurs les plus élevées de k signifie que M n diminué rapidement au cours de la première phase (c'est-à-dire de 0 à 4 jours). Les 5 à 24 jours suivants sont attribués à la deuxième phase et aux valeurs de k légèrement diminué par rapport à la première phase. Peu d'études [13, 50] ont montré que la partie cristalline du PLA était plus résistante à la dégradation que la partie amorphe; ainsi, la diminution de k dans cette phase pourrait être causée par l'augmentation de la cristallinité de la matrice PLA. Après 24 jours (c'est-à-dire la dernière phase), la valeur de k diminué à nouveau. A ce stade, le polymère s'est complètement dégradé en fragments d'oligomères ou en acide lactique, et les micro-organismes ont minéralisé les matériaux restants pour générer en continu du CO2 .
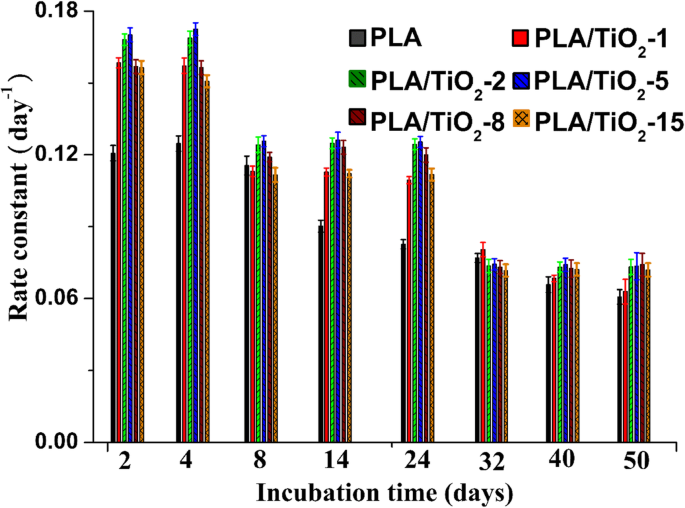
Taux de biodégradation en fonction du temps d'incubation pour le PLA pur et le PLA/TiO2 nanocomposites
Dans des conditions de compostage, les facteurs qui affectent la tendance à la biodégradation du PLA contrôleraient la dégradation du PLA/TiO2 nanocomposites. Lorsqu'une quantité de g-TiO2 était dispersé de manière homogène dans la matrice PLA, les molécules d'eau pénétraient facilement dans les échantillons pour déclencher le processus de dégradation [17]. Par conséquent, Mn a diminué considérablement dans la première phase. L'évolution de la phase de latence du CO2 pour le PLA et ses nanocomposites au cours de cette période a indiqué que les micro-organismes ont besoin de chaînes polymères appropriées pour se minéraliser. Avec l'augmentation du temps d'incubation, les chaînes polymères dans les régions amorphes se sont dégradées et le nombre de régions amorphes a diminué; ainsi, le pourcentage de cristallin à la région amorphe (c'est-à-dire, c ) a augmenté [39], entraînant ainsi la diminution de k dans la deuxième phase. Cependant, les fragments d'oligomères ont commencé à être minéralisés par des micro-organismes à ce stade, indiquant ainsi que la phase productive pour la minéralisation du PLA s'est produite. Avec la diminution des fragments d'oligomères restants et l'augmentation de χc , k et D t diminué et une phase de plateau presque longue a été observée pour k et D t dans la troisième étape. Dans notre étude précédente [16], la morphologie de chaque nanocomposite a été rapportée et déterminée par SEM et MET; les résultats ont montré que la dispersion de g-TiO2 avec moins de 5 % en poids dans le PLA/TiO2 nanocomposites était meilleur que celui obtenu avec une forte concentration de nanocharges. En termes de dispersion et de teneur en TiO2 , PLA/TiO2 -5 avait le plus grand k et D t par rapport aux autres nanocomposites de notre expérience.
Conclusions
PLA/TiO2 des nanocomposites ont été préparés (à base de PLA et de g-TiO2 fonctionnalisé ) et soumis à une biodégradation dans des conditions de compostage contrôlées. En utilisant un tel standard, l'information des motifs à la surface des échantillons et l'augmentation rapide de la cristallinité indiquaient que le PLA et le PLA/TiO2 les nanocomposites avaient des mécanismes de biodégradation hétérogènes. L'étude de dégradation des nanocomposites dans des conditions de compostage a montré que le caractère dégradable inhérent du PLA persistait après l'incorporation de nanoparticules de dioxyde de titane fonctionnalisées (PLA/TiO2 ). L'ajout du TiO2 les nanoparticules ont augmenté le taux de dégradation de la matrice PLA car les molécules d'eau ont facilement pénétré le PLA/TiO2 nanocomposites, activant ainsi le processus de dégradation. Ce phénomène était particulièrement évident pour le PLA/TiO2 –5 à cause de son TiO2 élevé teneur et bonne dispersion de TiO2 nanocharges dans la matrice PLA par rapport à d'autres nanocomposites.
Abréviations
- DSC :
-
Calorimétrie différentielle à balayage
- D t :
-
Pourcentage de biodégradation
- GPC :
-
Chromatographie par perméation de gel
- g-TiO2 :
-
TiO greffé2
- MCE :
-
Cellulose microcristalline
- Mn :
-
Poids moléculaire moyen en nombre
- Mw :
-
Poids moléculaire moyen en poids
- PLA :
-
Poly (acide lactique)
- SEM :
-
Microscopie électronique à balayage
- Tcc :
-
Pic de cristallisation à froid
- Tg :
-
Température de transition vitreuse
- XRD :
-
Diffraction des rayons X
Nanomatériaux
- ADM et LG Chem explorent la production américaine d'acide lactique et de PLA
- Détection photo-électrochimique améliorée de l'acide urique sur une électrode de carbone vitreuse modifiée par nanoparticules d'Au
- Nanofibres polymères électrofilées décorées de nanoparticules de métaux nobles pour la détection chimique
- Synthèse facile de composite CuSCN coloré et conducteur revêtu de nanoparticules CuS
- Nouveaux nanocomposites de polystyrène avec polyaniline dopé à l'acide lauryl sulfurique
- Cibler les cellules endothéliales avec des nanoparticules GaN/Fe multifonctionnelles
- Activités photocatalytiques renforcées par des nanoparticules Au-Plasmonic sur une photoélectrode de nanotube de TiO2 recouverte de MoO3
- Stabilité améliorée des nanoparticules magnétiques d'or avec du poly(acide 4-styrènesulfonique-co-acide maléique) :propriétés optiques adaptées pour la détection des protéines
- Effets synergiques des nanoparticules d'Ag/BiV1-xMoxO4 avec une activité photocatalytique améliorée



